Научные статьи по раку щитовидной железы

Рак щитовидной железы (РЩЖ) занимает 5 место в структуре заболеваемости злокачественными заболеваниями у женщин и 9 место в структуре общей заболеваемости злокачественными новообразованиями в США. Ежегодно от этой патологии умирают менее 2000 человек. На протяжении нескольких десятилетий показатели смертности остаются стабильными. Наиболее часто встречающаяся форма РЩЖ, дифференцированный РЩЖ (ДРЩЖ), возникает из фолликулярных клеток щитовидной железы (ЩЖ). Выделено 2 гистотипа ДРЩЖ – папиллярный и фолликулярный РЩ. Большинство пациентов излечиваются от этой патологии или заболевание имеет индолентное течение. Небольшой процент больных имеют метастазы, не отвечающие на терапию радиоактивным йодом или тироксином [4].
В России за последнее десятилетие отмечается неуклонный рост заболеваемости РЩЖ. В структуре заболеваемости злокачественными заболеваниями женского населения страны в 2014 году рак щитовидной железы составил 2.8 %. К примеру, в 2004 году в России было выявлено 1141 человек с впервые установленных диагнозов РЩЖ. В 2014 эта цифра составила 1655 человек. Динамика стандартизованных показателей заболеваемости РЩЖ в России характеризуется приростом на 13,11 % за 10 лет (2004–2014). Самые высокие показатели заболеваемости РЩЖ приходятся на возрастную группу от 52 до 54 лет [1].
Показатели выживаемости у больных ДРЩЖ высокие. У них, как привило, не бывает отдалённых метастазов и не отмечено локального роста. В 85 % случаев эти больные преодолевают порог 10-летней выживаемости [4].
Большинству пациентов с диагнозом дифференцированного РЩЖ показано оперативное лечение первичной опухоли. Объем операции (гемитиреоидэктомия, тиреоидэктомия или удаление ЩЖ с лимфодиссекцией) определяется согласно предоперационному риску рецидива. Так же назначается и терапия радиоактивным йодом после тиреоидэктомии. Локальные или отдалённые метастазы могут выявляться у 10 % больных дифференцированным РЩЖ. В этих случаях имеются различные варианты лечения. Терапия может включать назначение нескольких сеансов терапии радиоактивным йодом, удаление метастаза хирургически, и /или ДЛТ [5]. Несмотря на лечение, одна – две трети пациентов с метастатическим дифференцированным РЩЖ становятся резистентными к радионуклидной терапии. Радиойодрезистентность случается менее, чем у 5 % пациентов с РЩЖ. Эта группа пациентов имеет плохой прогноз, 10–летняя выживаемость составляет 10 % , а средняя продолжительность жизни от выявления метастазов колеблется в диапазоне от 3 до 5 лет. Пациентам с распрострарнённым, прогрессирующим и радиойодрезистентным ДРЩЖ назначается таргетная терапия мультикиназными ингибиторами (МКИ) [4]. На настоящий момент одобрены 2 МКИ – сорафениб и ленватиниб. Практическое применение МКИ в клинике варьирует в зависимости от локальных рекомендаций и опыта лечащего врача [3]. Существуют некоторые аспекты назначения этих препаратов в клинической практике. Наиболее важными задачами в клинике являются установление факта радиойодрефрактерности и отбор кандидатов для системной терапии [10].
Гистологические особенности ПРЩЖ
Недавно проведённые исследования указывают, что некоторые варианты ПРЩЖ (диффузно-склерозирующий, высококлеточный и инсулярный варианты) проявляют себя либо как высокоагрессивные опухоли, либо как дифференцированный ПРЩЖ или недифференцированная карцинома ЩЖ, с высокой частотой метастазирования, рецидивов, радиойодрезистентностью.
Фолликулярный вариант ПРЩЖ сложно отличить от фолликулярной аденомы. Отличия выявляются на уровне цитологических признаков. По этой причине в сложных случаях необходимо определять иммуногистохимические и молекулярные маркеры для установления диагноза. Прогноз при этом типе опухоли такой же, как и при ПРЩЖ, за исключением случаев диффузного или многоузлового фолликулярного варианта с более агрессивным течением. Прогноз зависит от степени инвазии. Высококлеточный вариант составляет лишь 1 % ПРЩЖ, имея боле агрессивное течение в отличие от типичного ПРЩЖ. Он представлен клетками, которые в 2–3 больше в длину, чем в ширину. Исходя из имеющихся данных, при этом варианте распространение за пределы ЩЖ наблюдается в 33 % случаев. Также поражение лимфоузлов чаще наблюдается у мужчин, чем у женщин. Мутация BRAF обнаружена у 93 % пациентов с высококлеточным типом и в 77 % случаев типичного ПРЩЖ. Диффузно-склерозирующий вариант ПРЩЖ составляет 0.7–6.6 % ПРЩЖ. Зачастую этот вариант встречается в педиатрической практике и у пациентов, подвергшихся воздействию излучения [8]. Наиболее частые мутации – T1799A миссенс – мутация в 15 экзоне гена BRAF и мутация RET/PTC, ведущие к активации сигнального каскада RAS-RAF-MAPK [10]. Этот подтип связан с высокой частотой отдалённых метастазов, плохим прогнозом, женским полом и молодым возрастом [9]. Инсулярный РЩЖ встречается в 0.3 % ПРЩЖ. Зачастую эта опухоль выявляется у пожилых пациентов в возрасте от 48–61 года. Характерна для мужчин [10]. Распространяется за пределы ЩЖ в 47.3 % случаев, лимфоузлы вовлечены в 61.9 % случаев, около 30 % пациентов имеют отдалённые метастазы [6].
Молекулярные особенности ДРЩЖ
За последние тридцать лет наблюдается значимый прорыв в понимании влияния соматических генных нарушений на клинические исходы у больных ДРЩЖ. Большинство этих генетических реаранжировок и мутаций влияют на инициацию опухолевого роста, но не на прогрессирование. Реаранжировки RET/PTC были описаны среди первых молекулярных нарушений при ДРЩЖ. Наиболее распространённые реаранжировки – RET/PTC 1 и RET/PTC3. Перестройка RET/PTC 1 характерна для молодых пациентов и ассоциирована с высокой частотой метастатического поражения лимфоузлов. С другой стороны, реаранжировка RET/PTC 3 встречается в детском возрасте и ассоциирована с предшествующим облучением. Онкогены RAS кодируют 3 белка (H-, K-, and N-RAS). Наиболее часто при ДРЩЖ выявляются точковые мутации в кодонах 12 или 61. Активация этих белков увеличивает пролиферативную активность клеток ЩЖ и снижает экспрессию тиреоглобулина, тиреопероксидазы и NIS протеина. Мутации RAS встречаются с одинаковой частотой в аденомах ЩЖ, ДРЩЖ и анапластических опухолях. Около 15 %–20 % папиллярных опухолей ЩЖ могут иметь мутации онкогена RAS, в основном фолликулярного варианта, которые инкапсулировнаы и имеют низкую частоту метастазирования в лимфоузлы [4]. Высокая частота этой мутации выявлена у больных ДРЩЖ с отдалёнными метастазами, чувствительными к радиойоду. Несмотря на способность к накоплению препарата, радиойодтерапия оказывается неэффективной у большинства пациентов с ДРЩЖ, чувствительным к радиойоду и имеющим мутацию RAS [7]. Тем не менее, наличие мутации RAS может служить предиктором эффективности терапии МКИ селюметинибом у больных радиойодрефрактерным ДРЩЖ. Описаны случаи более агрессивного течения ДРЩЖ при наличии этой мутации.
Мутации в гене B-RAF (V600E) обнаружены у 30 %–70 % больных папиллярным РЩЖ. Установлено, что опухоли с этой мутацией чаще распространяются за пределы ЩЖ, метастазируют в лимфоузлы, чаще рецидивируют и меньше поглощают радиойод. Также описано ,что B-RAF мутация может присутствовать в различных участках опухоли.
Сигнальный каскад фосфоинозитид – 3 – киназы (PI3K) регулирует рост, подвижность и выживаемость клеток. Активирующие мутации гена PI3K в основном присутствуют в клетках фолликулярного и анапластического рака. Тем не менее, амплификация PI3K встречается в 13 % фолликулярных аденом, 16 % папиллярного РЩЖ, 30 % фолликулярного РЩЖ и в 50 % анапластического РЩЖ.
Недавно при ДРЩЖ обнаружена гиперэкспрессия гена обратной транскриптазы теломеразы (TERT), которая играет значимую роль в иммортальности клеток. Также обнаружены соматические точковые мутации, которые повышают активность теломеразы. TERT мутации обнаружены в 11 % случаев при фолликулярном РЩЖ и в 16 %–40 % случаев папиллярного рака ЩЖ (зачастую ассоциированы с B-RAF мутациями). Гиперэкспрессии или мутации гена TERT коррелируют с более агрессивным течением опухолей, чем при наличии мутаций B-RAF. Эти пациенты имеют высокий риск рецидива заболевания.
Фактор роста эндотелия сосудов (VEGF) гиперэкспрессирован как в самой опухоли, так и в кровеносных сосудах опухоли. Его основной рецептор – VEGFR-2– гиперактивирован при ДРЩЖ и вовлечен в неопластический рост, прогрессирование и агрессивность. На сегодняшний день это основная мишень многих МКИ при радиойодрефрактерном ДРЩЖ [4].
Возможности таргетной терапии при ДРЩЖ
Сорафениб – это МКИ одобренный для лечения первичного рака почки, распространённой гепатоцеллюлярной карциномы и распространённого прогрессирующего ДРЩЖ. Мишени Сорафениба – C-RAF, B-RAF, VEGF – рецептор (VEGFR)-1, -2, -3, PDGF receptor (PDGFR)-β, RET, c-kit, and Flt-3. Препарат ингибирует рост опухоли, прогрессию, метастазирование и ангиогенез, а также нарушает механизмы защиты клетки от апоптоза [4].
В июле 2014 года опубликовано первое рандомизированное, двойное слепое, плацебо-конролируемое исследование (DECISION) по анализу эффективности стандартной дозы сорафениба 800 мг у больных радиойдрефрактерным местнораспространённым или метастатическим ДРЩЖ. Популяция включила 417 пациентов (207 в группе сорафенибва и 210 в группе плацебо) с медианой наблюдения 16.2 месяца. Выживаемости без прогрессирования (ВБП) была длиннее на 5 месяцев в группе больных, получавших сорафениб в сравнении с пациентами, получавшими плацебо (10.8 и 5.8 месяцев соответственно, отношение рисков [ОР] 0.587, 95 % ДИ 0.454–0.758; P
Похожие темы научных работ по клинической медицине , автор научной работы — Червякова Г. А., Каменский Д. З., Томилова Е. Н., Коджая А. Н.
Рак щитовидной железы
Рак щитовидной железы
^ Г.А. Червякова, Д.З. Каменский, Е.Н. Томилова, А.Н. Коджая
Кафедра госпитальной терапии № 1 Лечебного факультета РГМУ
Кафедра эндокринологии РГМУ Городская клиническая больница № 15 им. О.М. Филатова, г. Москва
Специализация в медицине повысила точность диагностики и эффективность лечения большинства болезней. Больные, как правило, обращаются сначала к участковому терапевту, который ставит предварительный диагноз и направляет их для детального обследования к специалисту, а нередко и в стационар. Тем не менее своевременность диагностики и лечения в значительной мере зависит от решения, принятого терапевтом.
Увеличение лимфатических узлов может служить одним из признаков различных заболеваний, в пожилом возрасте оно нередко становится одним из проявлений злокачественной опухоли. Перечень этих заболеваний можно найти в терапевтических справочниках, однако не во всех источниках есть указание на то, что причиной увеличения лимфатических узлов может явиться рак щитовидной железы (ЩЖ).
Рак ЩЖ — нечасто встречающаяся опухоль (менее 1% всех случаев злокачественных новообразований). Его дифференцированные формы имеют относительно благоприятное течение с пятилетней выживаемостью около 60—80%. Наиболее часто встречающиеся формы рака ЩЖ (папиллярный и фолликулярный) составляют 60 и 30% всех раков ЩЖ соответственно, более злокачественные варианты (апластический и медуллярный) — около 10%. По данным БгапвБШа К.О., метастазы в лимфатические узлы при папиллярном раке ЩЖ наблюдались у 42% пациентов. Пятилетняя выживаемость при папиллярном раке ЩЖ составила 85%, а при фолликулярном — 54%.
Приводим случай посмертной диагностики злокачественной опухоли ЩЖ, ос-
новным проявлением которой было увеличение шейных лимфатических узлов.
Больной К., 62 лет, был госпитализирован в кардиологическое отделение с жалобами на одышку в покое, усиливающуюся при физической нагрузке, сопровождающуюся затрудненным вдохом и чувством нехватки воздуха, слабость. Имелись также боли за грудиной сжимающего характера (прием нитроглицерина — без эффекта).
Из анамнеза известно, что пациент страдал артериальной гипертензией на протяжении длительного времени, адаптирован к артериальному давлению (АД) 130/100 мм рт. ст. В 2000 г. перенес инфаркт миокарда. Наблюдался по месту жительства с диагнозом: Ишемическая болезнь сердца: постинфарктный кардиосклероз, стенокардия напряжения, II функциональный класс. Артериальная гипертензия III стадии. У эндокринолога не наблюдался. В семейном анамнезе по линии отца имелись случаи рака щитовидной железы.
Состояние постепенно ухудшалось с октября 2004 г., когда появилась слабость, стал отмечать увеличение шейных и подмышечных лимфатических узлов. Поводом для госпитализации стало появление одышки в покое (за неделю до поступления в клинику).
Состояние при поступлении средней тяжести. Температура тела 36,6°С. Сознание ясное. Телосложение правильное, питание пониженное. Кожные покровы бледные, с умеренным диффузным цианозом. Отмечается затрудненный продолжительный вдох с участием вспомогательной дыхательной
Случай из практики
Рентгенограмма грудной клетки в боковой проекции: дополнительная тень спереди от трахеи однородной структуры.
мускулатуры. В легких выслушиваются сухие рассеянные хрипы. Частота дыхания — 26/мин. Сердечные тоны приглушены, ритм правильный, частота сердечных сокращений — 90/мин. АД — 140/90 мм рт. ст. Пальпируются группы лимфатических узлов в над- и подключичной области и единичный узел в подмышечной области справа. Узлы при пальпации плотные, безболезненные, подвижные, не спаяны с кожей и окружающими тканями. Размер их варьирует от 0,5 до 3 см. В надключичной области пальпируется неподвижный конгломерат, плотно спаянный с окружающими тканями. Щитовидная железа при пальпации увели -чена незначительно, плотноватой консистенции, подвижна. Живот мягкий, безболезненный, печень и селезенка не увеличены. Симптом поколачивания по поясничной области отрицательный с обеих сторон.
На электрокардиограмме — перегрузка правых отделов сердца, гипертрофия миокарда левого желудочка.
Клинический анализ крови: гемоглобин — 152 г/л, тромбоциты — 277 х 109/л, лейкоциты — 8,2 х 109/л, нейтрофилы палочкоядерные — 7%, сегментоядерные — 70%, эозинофилы — 3%, лимфоциты — 16%, моноциты — 4%, СОЭ — 29 мм/ч.
Биохимический анализ крови: общий белок — 61,1 г/л (норма 67—87 г/л), холестерин — 6,0 ммоль/л (норма до 5,7 ммоль/л), другие стандартные показатели в пределах нормы.
На обзорной рентгенограмме грудной клетки определяется расширение тени верхнего средостения в обе стороны. В боковой проекции — дополнительная тень спереди от трахеи однородной структуры (рисунок).
При ультразвуковом исследовании органы брюшной полости и почки без грубой патологии, лимфатические узлы брюшной полости не увеличены.
Эзофагогастродуоденоскопия: эзофагит, поверхностный гастрит, грыжа пищеводного отверстия диафрагмы.
Ультразвуковое исследование щитовидной железы: контуры ровные, размеры правой доли 18 х 29 х 54 мм, левой доли — 25 х 20 х х 52 мм. Толщина перешейка — 8 мм (норма до 4 мм). В перешейке определяется ги-поэхогенный, умеренно неоднородный, с неровными контурами узел размером 6,5 х х 4,7 мм. Общий объем ЩЖ — 26,6 см3 (норма до 25 см3).
Для проведения дифференциальной диагностики был удален шейный лимфатический узел из надключичной области. При гистологическом исследовании: большую часть узла занимает опухолевая ткань — аденокарцинома с наличием перстневидных клеток.
За время пребывания в стационаре аппетит у пациента был снижен, он потерял в весе 5 кг, нарастали симптомы сдавления трахеи. Больной умер во сне.
Результаты вскрытия: щитовидная железа размером 6 х 3 х 2,5 см, плотная на ощупь, перешеек несколько увеличен в
Рак щитовидной железы
размерах. Из области перешейка исходит
опухолевое образование, располагающееся по передней поверхности трахеи. Его размеры: высота 7 см, ширина 6 см, толщина
2.5 см, на разрезе плотная серая ткань. Обнаружены увеличенные лимфатические узлы: шейные, над- и подключичные (до 1 см в диаметре), паратрахеальные (2,5 см), бифуркационные и пульмональные (до
1.5 см), а также лимфатический узел диаметром 0,8 см около нижней трети пищевода. В обоих надпочечниках белые плотные узлы диаметром 1 и 1,5 см. Микроскопическое исследование ткани ЩЖ: фолликулярный рак с переходом в недифференцированный рак.
Клинико-анатомический диагноз: злокачественная опухоль щитовидной железы с метастазами в регионарные лимфатические узлы, перикард, эпикард и надпочечники. Осложнением основного заболевания стало сдавление трахеи опухолью щитовидной железы, приведшее к острой дыхательной недостаточности, которая и послужила непосредственной причиной смерти больного.
Больной был госпитализирован с нарастающей одышкой, которая вначале была расценена как кардиальная (с учетом перенесенного инфаркта миокарда). При осмотре было установлено, что имеет место сте-нотическое дыхание, предположительно обусловленное нарушением проходимости верхних дыхательных путей. Были предприняты попытки выяснить причину затруднения дыхания, а также увеличения лимфатических узлов. В первую очередь, дифференциальный диагноз проводился с наиболее часто встречающимися в терапевтической практике заболеваниями, сопровождающимися увеличением лимфатических узлов (лимфогранулематоз, лейкозы, саркоидоз, метастатическое поражение и др.). Не исключалось первичное опухолевое поражение лимфатических узлов. Одновременно проводилась борьба с
явлениями гипоксии и поддержание сердечно-сосудистой системы. Быстро наступивший летальный исход не позволил поставить прижизненный диагноз.
Вопрос о раке ЩЖ должен возникать у врача общей практики или терапевта, когда в соответствии с обязательным алгоритмом физикального обследования (необходима тщательная пальпация ЩЖ!) выявляется:
• узел (узлы) в ЩЖ (узловой эутиреоид-ный зоб);
• увеличение лимфатических узлов шеи;
• сочетание вышеперечисленных признаков;
• метастазы в легких или костях.
Понятие “узловой эутиреоидный зоб” относится к разным по морфологии узлам ЩЖ: узловой коллоидный зоб, фолликулярная аденома, узлоподобные уплотнения при хроническом аутоиммунном тиреои-дите, кисты и, наконец, рак ЩЖ. Пальпа-торно выявляемые узлы (более 1 см в диаметре) имеются примерно у 5% населения. Однако лишь у 1 из 20 таких пациентов узлы имеют признаки злокачественного роста. К наиболее подозрительным в отношении рака ЩЖ относятся узлы:
• вызывающие парез голосовых связок и, тем более, сдавление органов шеи;
• у женщин моложе 30 лет;
• у мужчин старше 50 лет;
• при отягощенном семейном анамнезе. Ультразвуковое исследование ЩЖ позволяет уточнить локализацию и распространенность процесса. Метастазы фолликулярного рака способны захватывать йод (осуществляя синтез тиреоглобулина и, реже, тиреоидных гормонов), что используется при радиоизотопной диагностике и при лечении радиоактивным йодом. Как правило, “функционирующая” злокачественная опухоль ЩЖ является фолликулярным раком. В случае выявления узла позволяет верифицировать диагноз аспирационная тон-
Случай из практики
коигольная биопсия ЩЖ, желательно под контролем ультразвукового исследования. Оснований для диагностических ошибок при данном алгоритме обследования мало.
Более сложные диагностические коллизии возникают при диагностике причин увеличения шейных лимфатических узлов. При раке ЩЖ они обычно плотные, могут быть спаянными между собой или с окружающими тканями, наиболее рано обнаруживаются по ходу сосудистого пучка и грудино-ключично-сосцевидной мышцы. В случае одновременного выявления узла в ЩЖ вероятность рака ЩЖ становится очень высокой. Если же узел в ЩЖ не пальпируется, то диагностический поиск идет, прежде всего, по пути исключения первичного поражения лимфатической системы, а также рака полости рта и гортани. Алгоритм должен включать ультразвуковое исследование ЩЖ для выявления непаль-пируемых узлов (обычно менее 1 см).
В нашем наблюдении возможность запущенного рака ЩЖ была недооценена из-за того, что внимание было акцентировано на других причинах увеличения лимфатических узлов шеи и стеноза трахеи.
Подходы к лечению
Как правило, для лечения больных переводят в специализированное отделение, где решается вопрос о тактике. Прежде всего определяется необходимость и срочность вмешательства (в том числе паллиативного) по поводу нередко возникающего сдавления дыхательных путей увеличенными лимфатическими узлами или самой опухолью ЩЖ. В нашем наблюдении активность в этом направлении оказалась недостаточной.
В настоящее время при раке ЩЖ применяется тиреоидэктомия, лечение радиоактивным йодом и рентгенотерапия.
Во всех случаях оперативного лечения узлового зоба удаленную опухоль направляют на экспресс-диагностику, и операцию заканчивают только после получения результатов гистологического исследования.
При злокачественной опухоли ЩЖ объем вмешательства зависит от стадии процесса: производится тотальная тиреоидэктомия с удалением лимфатических узлов и вовлеченных в процесс окружающих тканей. В тех случаях, когда опухоль локализуется в одной доле ЩЖ, резекции подлежит и вторая доля, так как в большинстве случаев через внутриорганные лимфатические пути опухоль распространяется и на вторую долю железы, кажущуюся интактной.
После удаления злокачественной опухоли ЩЖ назначается терапия тиреоидными гормонами для подавления секреции ти-реотропного гормона и торможения роста единичных клеток опухоли, которые могли остаться после операции.
Балаболкин Н.И. Эндокринология. М., 1998. Виноградов А.В. Дифференциальный диагноз внутренних болезней: Справочное руководство для врачей. М., 2001. С. 491—512.
Майкл Т, Дермотт М. Секреты эндокринологии. М., 1998. С. 257-267.
Ошибки в клинической онкологии: Руководство для врачей / Под ред. Чиссова Н.И. М., 1993. С. 187-200.
Потемкин В.В. Эндокринология. М., 1999. С. 234-242.
Хеглин Р. Дифференциальная диагностика внутренних болезней / Под ред. Тареева Е.М. М., 1997. С. 475-478.
Эндокринология: Пер. с англ. / Под ред. Лавина Н. М., 1999. С. 571-577.

Рак щитовидной железы является наиболее часто встречающейся злокачественной опухолью эндокринной системы и составляет 1–3 % в общей структуре онкологической заболеваемости [3].
В мире ежегодно регистрируется около 150 тысяч новых случаев рака щитовидной железы. И, согласно статистике, в настоящее время отмечается стремительный рост заболеваемости данной патологией [2]. Что в большей степени связано с ростом выявляемости рака щитовидной железы вследствие внедрения в клиническую практику высокоинформативных методов исследования, позволяющих обнаруживать в щитовидной железе непальпируемые образования размером от 4 мм [3].
Также отмечается, что среди абсолютного числа заболевших раком щитовидной железы преобладают женщины. Согласно данным ВОЗ, на их долю приходится 2,7 % всех онкологических заболеваний щитовидной железы, а мужчины составляют всего лишь 0,7 % [5, 7, 9]. За последние 13 лет стандартизированный показатель заболеваемости раком щитовидной железы среди женского населения вырос в 7 раз [1].
Основная доля рака щитовидной железы, порядка 90–95 %, имеет фолликулярно-клеточное происхождение, остальные 5–10 % опухолей – парафолликулярного (С–клеточного) [11].
По степени дифференцировки выделяют дифференцированный, умеренно дифференцированный и недифференцированный рак щитовидной железы. Дифференцированный фолликулярно-клеточный рак, к которому относят папиллярный и фолликулярный рак, составляет 65–85 % всех злокачественных новообразований щитовидной железы и имеет благоприятный прогноз и 95 % пятилетнюю выживаемость. Однако 15 % этого рака рано метастазирует. Папиллярный рак – самая часто встречаемая форма рака щитовидной железы, составляет 80 %, фолликулярный рак встречается в 10–15 %.
Высокоагрессивные малодиффернцированные формы рака, такие как анапластический и плоскоклеточный, встречаются в 1–1,6 % и связаны с высоким риском летального исхода [11, 12].
На сегодняшний день, важнейшими вопросами хирургического лечения больных раком щитовидной железы являются: определение оптимального варианта операции, а также выбор доступа в начале и в ходе операции. Выбор объема хирургического вмешательства определяется главным образом локализацией образования, размерами первичной опухоли и объемом поражения регионарных лимфатических коллекторов, наличием инвазии в те или иные анатомические структуры [8]. Стандартной операцией по удалению рака щитовидной железы является тотальная или субтотальная тиреоидэктомия. Подобный объем операции снижает риск местного рецидива заболевания, сопряжен с минимальным риском осложнений и базируется на доказанном повышении выживаемости среди больных [6].
Наиболее часто встречающиеся осложнения при операциях на щитовидной железе связаны с повреждением щитовидных артерий (0,3–5 %), возвратных гортанных нервов (0,3–13,5 %) и околощитовидных желез (3,5–34,2 %), что обусловлено высокой вариабельностью топографии данных анатомических структур [4, 10].
Исход при раке щитовидной железы зависит от нескольких факторов: размера и типа опухоли, от того, есть ли метастазы в различные части тела (головной мозг, легкие, печень), от возраста пациента на момент выявления заболевания [3].
Цель исследования: изучить частоту заболеваемости раком щитовидной железы, половую приверженность, преобладающую морфологическую структуру, выбор оптимальной тактики лечения пациентов и риск послеоперационных осложнений.
Материалы и методы исследования
- 2589
- 1,8
- 1
- 3
![]()
Аполлинария Боголюбова![]()
Андрей Панов



Спонсором приза зрительских симпатий выступила компания BioVitrum.
Несомненно, XXI век — время развития научно-технического прогресса. Вместе с совершенствованием технологий приходит и их доступность в повсеместном использовании. Медицина не является исключением. Благодаря развитию технологий диагностики и лечения самых разных заболеваний мы стали спасать тех пациентов, которые когда-то входили в число неизлечимых. Однако не на все сферы медицины прогресс повлиял так положительно. Поэтому сегодня мы бы хотели познакомить вас с такими животрепещущими вопросами медицины, как гипердиагностика и гиперлечение. Сейчас мы остановимся лишь на одной, но весьма значимой стороне данной проблемы — гипердиагностика узлов щитовидной железы, а также гиперлечение этих узлов и рака щитовидной железы.
Что мы знаем сегодня про узлы щитовидной железы?
Однако то, что эта проблема была озвучена совсем недавно, не значит, что о ней больше не надо писать. Мы не хотим загружать вас медицинской терминологией, вновь писать о TI-RADS и разбирать по кусочкам, что может написать функциональный диагност в заключении. Мы обращаемся к вам в качестве потенциальных пациентов и хотим донести мысль, что не всегда узел в щитовидной железе опасен, а рак априори смертелен.
База, с которой нам нужно познакомиться: щитовидная железа
Немножко о щитовидной железе (ЩЖ). Это орган эндокринной системы человека, который располагается на передней поверхности шеи в области гортани, прямо перед щитовидным хрящом. Состоит железа из левой и правой долей и перешейка. ЩЖ богато кровоснабжается разными артериями, а иннервируется гортанными нервами.
Главной функцией щитовидной железы (лат. glandula thyroidea) является синтез тиреоидных гормонов, необходимых нашему организму. Под тиреоидными гормонами мы подразумеваем два соединения: тироксин (Т4) и трийодтиронин (Т3). Основной функцией Т4 и Т3 является увеличение потребления клетками кислорода. Иначе говоря, эти гормоны стимулируют все энергетические процессы в клетке и обмен веществ, причем их влияние распространяется на все клетки организма.
Также клетки ЩЖ производят кальцитонин, ответственный за обмен кальция в организме.
Прямо за щитовидной железой располагаются четыре небольшие паращитовидные железы. Последние производят паратиреоидный гормон, который также отвечает за поддержание уровня кальция в организме, причем в большей степени, чем кальцитонин.
Откуда берется столько случаев рака щитовидки?
Рак щитовидной железы (РЩЖ) — наиболее распространенное злокачественное новообразование эндокринной системы [2]. Все чаще мы слышим, что заболеваемость РЩЖ неуклонно растет. И звучит это ужасающе, однако так ли всё просто на самом деле? Возможно, вы будете шокированы, какая правда скрывается за этими, на первый взгляд, однозначными научными фактами. И прежде, чем мы разберемся с истинной причиной роста заболеваемости РЩЖ, необходимо ознакомиться с тем, какие виды рака щитовидки существуют.
Итак, начнем. Сейчас нам понадобится привести немного численных данных, но не пугайтесь их, всё крайне просто. В научном сообществе выделяют пять типов РЩЖ:
- Папиллярный (80–85% случаев).
- Фолликулярный (10–15% случаев).
- Медуллярный (5% случаев).
- Низкодифференцированный (1% случаев).
- Недифференцированный (0,1–0,2% случаев).
Наиболее благоприятными принято считать два первых типа РЩЖ. И как мы можем заметить, они встречаются наиболее часто. Их также называют высокодифференцированными типами рака. Медуллярный, низкодифференцированный и недифференцированный типы считаются агрессивными формами РЩЖ. В нашей статье мы сделаем акцент лишь на первых двух типах РЩЖ, так как они являются наиболее распространенными.
Что касается рака — если клетки, из которых состоит опухоль, являются высокодифференцированными, в большинстве случаев врачи считают исход благоприятным. Однако если опухоль состоит из низкодифференцированных клеток, то с большой вероятностью она склонна к агрессивному течению. Как уже было сказано, наиболее часто выявляемые РЩЖ являются высокодифференцированными.
Папиллярный РЩЖ — наиболее распространенная форма: 80–85%. И с самым хорошим прогнозом. Пятилетняя выживаемость пациентов с РЩЖ — 98,1% [2]. Что это значит для пациента? Что наиболее часто выявляемые случаи РЩЖ имеют благоприятный исход!
Рак, ушедший в себя
Подбираемся к корню проблемы: статистика и диагностика
Вернемся к распространенности РЩЖ. Теперь мы готовы понять, что возросшее число случаев данной патологии не является поводом для беспокойства.
В 1975 году заболеваемость РЩЖ составляла 4,9 на 100 000 человек и оставалась относительно стабильной до начала 1990-х годов [6]. За последние 25 лет заболеваемость РЩЖ выросла более чем в 3 раза, то есть на 300% (рис. 1) [7], [8], причем в большинстве случаев за счет высокодифференцированного папиллярного РЩЖ. При этом очень важно понимать, что, несмотря на такой значительный рост, смертность от РЩЖ остается стабильной, примерно 0,5 случаев на 100 000 человек [6].
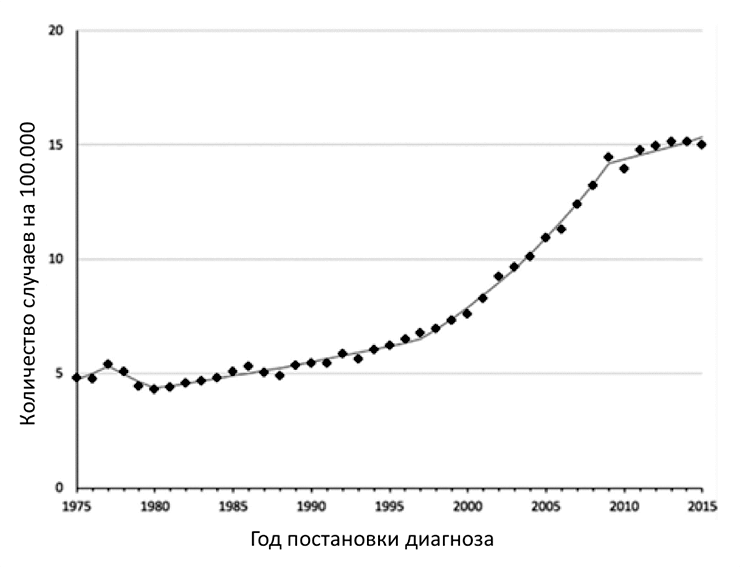
Рисунок 1. Данные заболеваемости раком щитовидной железы в период с 1975 по 2015 годы
Чувствуете, что тут что-то не так? Нет связи между возросшим числом случаев РЩЖ и смертностью от этой патологии! Среди врачей и ученых до сих пор продолжаются дебаты, почему так происходит. Сейчас выделяют несколько теорий. Наиболее вероятная — широкое распространение методов ультразвуковой диагностики (УЗИ). Пусть корни УЗИ уходят к Леонардо да Винчи и XV веку, широкое медицинское распространение данный метод получил с 50-х годов XX века [9], [10]. Сегодня УЗИ является наиболее простым, дешевым, неинвазивным и информативным методом выявления опухолевых образований щитовидной железы. Поэтому, как вы можете догадаться, УЗИ стали делать почти всем, причем независимо от показаний.
Сейчас научное сообщество активно дискутирует на тему, связаны ли такие показатели с истинным увеличением заболеваемости РЩЖ, или же проблема в гипердиагностике тех небольших образований ЩЖ, которые не требуют никакого вмешательства со стороны человека [11], [12].
Для более полного понимания проблемы вернемся на чуть более ранний этап диагностики РЩЖ.
Что такое узлы и как их найти?
Узлы ЩЖ — это радиологически различимые объемные образования в ЩЖ, которые могут быть доброкачественными и злокачественными. Узлы можно найти в 50% случаев всех проводимых УЗИ ЩЖ. При этом только 5% выявляемых образований будут злокачественными [13], [14].
Весомый вклад УЗИ в возросшее количество диагностированных узлов и РЩЖ можно показать на примере одного нашумевшего исследования в Южной Корее [3], [15], [16]. В 1999 году там была утверждена национальная программа, направленная на скрининг злокачественных заболеваний. Под программу попала и щитовидная железы. В результате повсеместного внедрения УЗИ щитовидки частота выявления рака выросла в 15 (!) раз с 1993 по 2011 год. И это мы еще не говорим просто об узлах, которые также могут быть психологической проблемой пациента. Большинство выявляемых случаев — папиллярный РЩЖ. Как вы помните, этот вид рака имеет весьма благоприятный исход. Однако простому населению идея жить с раком настолько чужда и неприятна, что было проведено огромное число полного удаления щитовидных желез, причем часто без видимой на то необходимости! А такая операция имеет серьезные последствия, о которых мы расскажем чуть ниже.
Врачи, осознав свою ошибку, убрали УЗИ щитовидки из списка обязательных скрининговых тестов. И результат не заставил себя ждать. В последней на эту тему публикации 2015 года сказано, что на 30% снизилась заболеваемость РЩЖ, а число операций на щитовидной железе снижалось на 35% ежегодно. Вывод напрашивается сам собой: в основе увеличения числа диагностированных случаев узлов щитовидки (в том числе и РЩЖ) является ставшее таким доступным УЗИ.
Думаем, следует также сказать, что образования ЩЖ выявляются не только при выполнении УЗИ, но и при использовании других методов лучевой диагностики (КТ, МРТ, ПЭТ), что стало возможным благодаря улучшению разрешающей способности оборудования. Следовательно, увеличилось чисто случайно выявляемых образований щитовидной железы (в том числе, рака) — инциденталóм (от англ. incidence — случайность) [17]. Инциденталомы клинически никак себя не проявляют и могут оставаться в организме бессимптомно всю жизнь. И многие из таких инциденталом обнаруживались лишь посмертно, случайно, и не являлись причиной кончины человека. Это позволяет говорить нам о существовании резервуара пациентов с узлами или раком щитовидной железы, который клинически является скрытым и никак себя не проявляет до его случайного обнаружения [18].
Приведенные данные обобщены на рисунке 2.

Рисунок 2. Что даст нам УЗИ щитовидки на самом деле?
рисунок авторов статьи
Напомним, что в нашей статье мы делаем акцент на наиболее распространенных типах РЩЖ (папиллярный, фолликулярный). Агрессивные формы РЩЖ (медуллярный, низкодифференцированный, недифференцированный и редко папиллярный) требуют дальнейшего более детального изучения
Самое главное: почему гипердиагностика и гиперлечение РЩЖ являются проблемой?
В связи с выявленным фактом, что в оперативном лечении таких РЩЖ, вполне возможно, нет необходимости (а ведь удаление ЩЖ сопровождается серьезными последствиями, о чем мы расскажем далее), с 2015 года в США уже принимаются меры по снижению частоты гипердиагностики и гиперлечения [24]. Например, уже настоятельно рекомендовано не проходить скрининг РЩЖ пациентам, у которых нет никаких симптомов, поскольку выявление агрессивных типов рака в этом случае крайне маловероятно.
Что врачи думают о данной проблеме?
Проблема гиперлечения РЩЖ существует не только среди пациентов, но и среди медицинского сообщества.
Конечно, выбор, удалять ли щитовидную железу или нет, стоит больше перед пациентом, нежели перед лечащим врачом. И пациент вполне может выбрать хирургическую тактику лечения. А врач должен определять, сколько ткани щитовидной железы в конкретном случае нужно убирать.
В качестве уменьшения гипердиагностики Американская тиреоидологическая ассоциация рекомендует воздержаться от скрининга и биопсии мелких образований щитовидной железы при отсутствии на то иных клинических симптомов [6].
Как вообще лечат рак щитовидной железы?
Давайте разберемся, какие существуют пути лечения РЩЖ [26].
- Полное удаление ЩЖ, тотальная тиреоидэктомия, вместе с окружающей клетчаткой, а иногда и рядом лежащими лимфатическими узлами.
- Терапия радиоактивным йодом I 131 после тотальной тиреиодэктомии. Не пугайтесь — это не опасно! Такой йод влияет только на клетки щитовидной железы и убивает их.
Почему мы, авторы, так не хотим, чтобы щитовидную железу удаляли без серьезных на то причин? Казалось бы, мы уберем орган, где сидит рак, и будем жить себе спокойно, только лишь принимая препараты гормонов щитовидной железы. Это ведь лучше, чем жить с раком. Или все-таки нет? Так вот, сама сложность вопроса заключается в операции.
Чем чревато полное удаление щитовидки (или, как говорят врачи, тотальная тиреоидэктомия)?
Существует два серьезных осложнения тотальной тиреоидэктомии [27].
- Стойкое снижение функции щитовидной железы (гипопаратиреоз). Наиболее серьезное и жизнеугрожающее осложнение. Итак, прямо за щитовидной железой располагаются четыре паращитовидные железы. Они производят паратиреоидный гормон, который отвечает за обмен кальция в нашем организме (а из него состоит бóльшая часть наших костей!). Паращитовидные железы совсем маленькие: диаметром 5 мм и весом 0,5 г. Их легко не заметить во время операции и удалить вместе с щитовидной железой. К тому же, даже если сохранить эти железы, высока вероятность повреждения питающих их кровеносных сосудов и нервов. А значит, железы просто перестанут работать, и в организм перестанет поступать паратиреиодный гормон. Это чревато возникновением тетанических приступов (подергиваний, которые могут переходит в судороги), нарушением питания волос и ногтей, кожи, эмали зубов, а также отложением кальция вне костей, например, между нервными клетками, что может проявляться в виде паркинсонизма или хореоатетоза — комбинации быстрых порывистых движений с медленными судорожными.
- Повреждение возвратного гортанного нерва и парез гортани. Щитовидная железа располагается прямо перед гортанью. Там же рядом находятся голосовые связки. Все эти структуры иннервируются гортанными нервами. И в случае повреждение некоторых из них — возвратных гортанных нервов — у пациента будет наблюдаться уменьшение активности гортанных мышц, что влечет за собой проблемы работы голосовых связок (в основном, осиплость голоса) и нарушения функций дыхания.
Какой существует выход?
Одним из наиболее перспективных выходов из ситуации является частичное удаление ткани ЩЖ, а именно поврежденной доли. В таком случае пациент, во-первых, избавляется от необходимости принимать пожизненную заместительную терапию гормонами щитовидной железы, а во-вторых, избегает тех серьезных последствий, которые несет за собой операция полного удаления ЩЖ. Однако стоит понимать, что такой вариант не касается опухолей большого размера, а также тех новообразований, которые потенциально могут быть агрессивными (это решает врач!).
Сейчас терапевты и хирурги, которые занимаются патологией щитовидной железы, разделились на два лагеря: те, кто считает, что лучше перестраховаться, и при выявлении даже самой маленькой опухоли удалить всю щитовидную железу, и те, кто считает, что лучшим выходом будет частичное удаление ткани железы, а именно поврежденной ее доли. К сожалению, этот вопрос до сих пор остается открытым. Врачи все еще не могут прийти к единому знаменателю в данном вопросе. Проблема в том, что достоверная объективная доказательная база, на которую врачи могли бы опираться в качестве актуального клинического руководства, вовсе отсутствует. Существуют лишь отдельные исследования, которые обозревают вопрос лишь с одной субъективной стороны [21]. Оптимальным решением данной проблемы, на наш взгляд, стало бы объединение всех существующих статей с объективным и всесторонним взглядом на этот вопрос. Однако подобное исследование лишь ожидает нас в будущем.
Финальный аккорд
С этими и другими мыслями вы можете ознакомится по оставленной нами ссылке [26].
Итак, дорогие наши читатели! Опираясь на всё, о чем мы рассказали выше, мы бы хотели, чтобы вы сделали три главных вывода:
Всем хорошего дня, и берегите свои щитовидки и нервы. :)
Читайте также:



