Научные статьи по гемангиомам
А. В. Буторина
Доктор медицинских наук, В. В. Шафранов, доктор медицинских наук, профессор, РГМУ, Москва
Гемангиомы у детей — наиболее часто встречающиеся доброкачественные сосудистые опухоли, которые составляют более 50% всех опухолей детского возраста [1, 4, 5, 9, 10, 11, 16].
В отношении морфологической принадлежности этих новообразований можно с уверенностью сделать вывод об опухолевой, а не диспластической природе гемангиом [6, 13, 15].
Многими авторами установлена высокая митотическая активность в клетках опухоли, в то же время отмечена возможность спонтанной регрессии гемангиом, что полностью соответствует опухолевой природе заболевания [6, 10, 14, 17].
Несмотря на свою доброкачественность, гемангиомы отличаются быстрым прогрессирующим ростом. Разрастаясь, они разрушают окружающие ткани и наносят ребенку значительный косметический ущерб. В первую очередь это относится к гемангиомам лица и головы. При локализации гемангиом на веках, ушной раковине, носу, а также на слизистой ротовой полости, помимо косметических проблем, могут возникать чисто физиологические в виде нарушений функций некоторых важных органов (зрение, слух, дыхание). Поэтому можно сказать, что гемангиомам присущи некоторые черты клинически злокачественного течения.
Особенностью течения гемангиом является непредсказуемость их “поведения”; порой небольшая, точечная гемангиома щеки в течение 2-3 недель может превратиться в обширную и глубокую ангиому сложной анатомической локализации (например, гемангиома околоушной области, без тенденции к остановке роста). Расчет на спонтанную регрессию в этих случаях оказывается неоправданным, а потеря времени идет явно не на пользу больному.
Помимо этого, сосудистые опухоли могут изъязвляться, вызывать кровотечения и инфицироваться. Характерная особенность изъязвившихся и нагноившихся гемангиом — продолжительное течение заболевания и отсутствие тенденции к быстрому заживлению язвенных поверхностей.
Отдельного разговора заслуживает спонтанная регрессия гемангиом. По нашим данным, спонтанной регрессии подвергаются около 7-8% простых гемангиом, находящихся на “закрытых” участках тела и только у доношенных детей в возрасте старше одного года. Кавернозные и комбинированные гемангиомы практически не регрессируют.
Надеяться на спонтанную регрессию большой и глубокой ангиомы в области лица у маленького недоношенного ребенка в возрасте до шести месяцев было бы ошибкой!
Процесс течения гемангиом достаточно сложный и требует постоянного внимания, причем чем меньше ребенок, тем внимательнее надо следить за состоянием гемангиомы. Особенно быстрый рост ангиом наблюдается в первое полугодие жизни ребенка, после этого рост замедляется, кроме гемангиом сложной анатомической локализации.
Поскольку в ранний возрастной период прогноз довольно сложен, лечение гемангиом, по нашему мнению, следует начинать как можно раньше, и даже недоношенность ребенка не является противопоказанием к раннему лечению.
Вероятно, универсального метода лечения гемангиом у детей нет и быть не может. И хотя морфологические данные явно свидетельствуют в пользу опухолевой природы ангиом, использование простых и эффективных хирургических и парахирургических методов лечения приводит к положительному результату.
Клиника детской хирургии РГМУ за 20 лет накопила опыт лечения 300 тыс. детей с гемангиомами различной локализации и вида.
Но занимаясь проблемой лечения гемангиом, мы столкнулись с группой больных с обширными и глубокими гемангиомами сложной анатомической локализации: лицо, околоушная область и шея.
Эти гемангиомы отличаются определенным своеобразием: бурным ростом опухоли, клинической злокачественностью течения, характеризующейся разным уровнем деструкции окружающих тканей, изъязвлениями, артериальными кровотечениями. Лечение таких гемангиом представляет значительные трудности для хирурга, так как традиционные методы чаще всего оказываются неэффективными.
Поэтому мы решили выделить этих больных в отдельную группу (см. табл.).
| Распределение детей с гемангиомами по виду и количеству последних | ||
| Вид ангиом | Количество больных | % |
| Простые | 215500 | 71,8 |
| Кавернозные | 19 500 | 6,6 |
| Комбинированные | 53000 | 17,7 |
| Смешанные | 10500 | 3,5 |
| Гемангиомы сложной анатомической локализации | 1500 | 0,5 |
| Всего | 300000 | 100 |
При анализе полученных данных подход к лечению детей с гемангиомами становится вполне очевиден. Наименьшую проблему представляют простые гемангиомы, наибольшую — гемангиомы сложной анатомической локализации, хотя в количественном отношении первые явно преобладают над последними.
Из ныне существующих методов наиболее удачным для лечения простых гемангиом является локальная криодеструкция аппаратом, где в качестве хладоагента применяется жидкий азот (с температурой –1960 С) [3, 8].
Криогенное лечение гемангиом проводится амбулаторно. Специальной подготовки ребенка к лечению не требуется. Метод прост, экономичен, не требует анестезии, абсолютно бескровен. Во время процедуры и после нее нарушений общего состояния ребенка, повышения температуры и патологических реакций не наблюдается.
Оптимальное время криовоздействия — 20-30 с для гемангиом, располагающихся на коже, и 7-15 с для гемангиом, локализующихся на слизистых оболочках.
При множественных гемангиомах, особенно если они были малых и средних размеров, мы проводили криодеструкцию одновременно двух или трех ангиом, но так, чтобы общая площадь криоповреждения не превышала 10 см2.
При локализации гемангиом в местах, наиболее подверженных травмированию, особенно в области промежности и ягодиц, площадь однократного криовоздействия не должна превышать 5 см2.
При крупных и обширных гемангиомах лечение должно проводиться в несколько этапов с интервалами между ними 10-14-21 день. За это время местная реакция в области криовоздействия стихает, и лечение может быть повторено.
Для предупреждения распространения опухолевого процесса и с целью ограничения роста гемангиомы рекомендуется начинать лечение с периферии.
Наиболее выраженный перифокальный отек наблюдается после криовоздействия на гемангиомы лица, век, сгибательных поверхностей, а также слизистой оболочки губ и половых органов. Образование сухой корочки отмечается на третий-четвертый день, эпителизации идет под струпом в течение 2-4 недель.
Успеха при криогенном лечении удается достичь в 100% случаев. Очень важной стороной лечения является получение хороших косметических и эстетических результатов (99,7%) благодаря особенностям регенерации кожи после криогенных вмешательств (органотипическая регенерация). Осложнения при криогенном лечении гемангиом наблюдаются крайне редко, в 0,2% случаев.
Среди общепринятых методик лечения наибольшей популярностью пользуется хирургическое иссечение опухоли с пластикой кожи или без нее.
В 95% случаев клиника отказалась от традиционных хирургических методов лечения гемангиом, отдавая предпочтение эффективным консервативным способам. Причем за 20 лет частота оперативных вмешательств снизилась в 50 раз.
Хирургический способ наиболее целесообразен при локализации гемангиом на “закрытых” участках тела, тогда как при расположении опухолей в области лица и шеи иссечение представляет определенную косметическую проблему.
Оперативный метод лечения целесообразно также использовать при зрелых формах гемангиом, которые закончили свою дифференцировку. Операция в качестве корригирующего метода может быть использована при наличии избытка кожи на месте большой туберозной гемангиомы в случае ее полного спонтанного исчезновения.
Для лечения небольших кавернозных гемангиом лица и кончика носа с успехом применяется склерозирующая терапия. Она основана на принципе асептического воспаления или тромбирования сосудов, возникающих в гемангиоме в результате введения склерозирующих веществ.
У всех больных для инъекций использовали 70%-ный спирт, отек на месте инъекции исчезал самостоятельно к 5 – 6 дню.
Недостатком инъекционного метода лечения является болезненность и длительность лечения, 76% больных потребовались дополнительные неоднократные инъекции спирта.
Диатермоэлектрокоагуляция применяется значительно реже, лишь при небольших точечных ангиомах, в тех случаях, когда опухоль располагается в областях, где нельзя воспользоваться другими методами лечения.
Эффективна, особенно в первом полугодии жизни ребенка, гормональная терапия гемангиом по альтернирующей схеме. Данный метод лечения был применен нами у 630 больных.
При подборе больных для кортикостероидной терапии мы руководствовались следующими критериями: сложность, т. е. критичность анатомической локализации; обширность поражения; быстрый рост гемангиом и поражение опухолью различных анатомических областей.
Мы считаем, что гормональной терапии подлежат самые обширные и самые сложные гемангиомы у детей.
Гормональное лечение проводилось преднизолоном по 4-6-8 мг на 1 кг веса ребенка. Суточная доза преднизолона в таблетках делилась на два приема: в 6 часов утра ребенок получал 2/3 дозы, в 9 часов утра 1/3 дозы. Препарат принимался через день без снижения дозировки. Продолжительность курса лечения составляла 28 дней.
Уже после второго или третьего приема преднизолона у большинства больных отмечались признаки регрессии ангиом, побледнение и некоторое уплощение опухоли. А к окончанию курса преднизолонотерапии все гемангиомы уменьшались в объеме, прекращался их рост и на поверхности опухоли появлялись белесоватые островки участков здоровой кожи, которые расчленяли ангиому на все меньшие и меньшие участки. После перерыва в 1-2 месяца, при необходимости, проводили повторные курсы гормонотерапии по той же методике.
Каких-либо осложнений во время лечения преднизолоном и после его отмены мы не наблюдали.
Гормонотерапия является довольно результативным методом лечения ангиом, однако при высокой его эффективности (98%) желаемого косметического результата достичь практически невозможно. Только у 2% детей ангиомы удалось полностью вылечить с помощью гормонотерапии, долечивание гемангиом другими методами позволяет решать лишь косметические проблемы.
Рентгенотерапия гемангиом относится к высокоэффективным методам. Она является весьма результативной, если лечение проводится у детей от 3 до 8 месяцев, так как в этом возрасте чувствительность ангиомной ткани к ионизирующему излучению очень высока, что обеспечивает излечение геманигиом с полным восстановлением нормальной кожи.
Близкофокусная рентгенотерапия применяется для лечения гемангиом таких областей, где другие методы невозможно использовать, например область орбиты, ретробульбарного пространства или простые гемангиомы большой площади.
Разовые очаговые дозы составляли от 0,8 до 1,6 Гр, в зависимости от возраста ребенка. Показанием к прекращению лучевой терапии при ангиомах являлось замедление роста и побледнение гемангиомы, т. е. лечение проводилось до появления симптомов регрессии, аналогичной естественной, после чего облучение прекращалось [7].
При лучевой терапии в дозах, не вызывающих местной реакции, изменения кожи и мягких тканей не развиваются. Надо учитывать, что этот метод лечения все же относительно сложен, и чтобы проявился эффект от лучевой терапии, требуется довольно длительное время.
При лечении кавернозных и комбинированных гемангиом с выраженной подкожной частью, чаще сложной анатомической локализации, следует проводить криоусиление за счет дестабилизации “связанной воды” путем предварительного СВЧ-воздействия на область замораживания. СВЧ-облучение проводится в физиотерапевтическом режиме в течение 3-5 минут, последующая криодеструкция выполняется в упомянутых выше режимах.
На наш взгляд, недоношенность не является противопоказанием к выполнению СВЧ-криодеструкции. В ряде случаев целесообразно проводить СВЧ-криогенное лечение по индивидуальным показаниям, например у новорожденных детей или в случае относительно большого объема опухоли.
Метод СВЧ-криодеструкции позволяет частично или полностью отказаться от хирургического лечения и добиться при этом хорошего результата (98%).
В клинике разработан подход к диагностике обширных и глубоких гемангиом сложной анатомической локализации, заключающийся в обязательной ангиографии. В результате были выявлены определенные закономерности, объясняющие, на наш взгляд, причину неэффективности лечения подобных опухолей. Оказалось, что через гемангиому проходит питающий ее мощный артериальный ствол, чаще аномального характера, который создает условия для активного роста сосудистой опухоли.
После обязательной ангиографии и эмболизации опухоли проводится лечение. Принимая во внимание преимущественную локализацию опухолей в проекции лицевого нерва, наиболее целесообразно было использовать СВЧ-криогенное вмешательство, так как этот способ гарантировал сохранность лицевого нерва, мимической мускулатуры и контуров лица ребенка.
Вмешательство не сопровождалось кровотечением и не было тяжелым для больного. В течение 5-6 месяцев гемангиома исчезала, оставляя после себя участки атрофированной кожи и атрофические рубцы.
К недостаткам этой методики мы отнесли развитие массивных отеков лица, которые держались до 5-7 дней, а затем исчезали самостоятельно, а также хоть и относительную, но все же хирургическую интервенцию.
На рис. 1, 2 представлен ребенок с ангиомой околоушной области до и после лечения (методом СВЧ-криодеструкции).
В последние годы исследуется и не без успеха применяется методика локальной СВЧ-гипертермии обширных и глубоких ангиом околоушной области. Данная методика была реализована у 180 больных. Метод заключается в повышении температуры в опухоли, регистрируемом введением под опухоль датчика в виде иглы. Температура доводится до 43-440С и поддерживается на этом уровне 5-6 минут.
Среди основных преимуществ методики основным является отказ от хирургического вмешательства, отсутствие отеков и возможность быстрой выписки ребенка домой. Косметические вмешательства, если ребенок в таковых будет нуждаться, можно выполнять в более старшем возрасте.
На рис. 3, 4 представлен ребенок с двухсторонней ангиомой сложной локализации до и после лечения (методом локальной гипертермии).
Таким образом, современное лечение гемангиом у детей и использование всего арсенала средств, имеющегося на вооружении в детской хирургии, позволяет добиться полного излечения опухоли с хорошим косметическим результатом. А следовательно, получить не только здорового, но и красивого ребенка!
1. Баиров Г. А. Хирургия пороков развития у детей. Л., 1968, с. 561-577.
2. Исаков Ю. Ф. Хирургические болезни у детей. М., 1993, с. 519-562.
3. Кандель Э. И. Криохирургия. М., 1974, с. 303.
4. Кондрашин Н. И. Клиника и лечение гемангиом у детей. М., 1963, с. 103.
5. Краковский Н. И., Таранович В. А. Гемангиомы. М., 1974, с. 168.
6. Лебкова Н. П., Кодрян А. А. О гистегенезе и механизме регрессии врожденных гемангиом кожи у детей // Архив патол., 1997, вып. 3. с. 44-50.
7. Свистунова Т. М. Низковольтная рентгенотерапия при гемангиомах у детей. Л., 1974, с. 142.
8. Ситковский Н. Б., Гераськин В. И., Шафранов В. В., Новак М. М. Лечение гемангиом у детей жидким азотом. Киев, 1968, с. 120.
9. Терновский С. Д. Хирургия детского возраста. М., 1959, с. 179-200.
10. Федореев Г. А. Гемангиомы. Л., 1974, с. 192.
11. Demuth R. J., Miller S. H., Keller F. Complications of embolization treatment for problem cavernous hemangiomas // Ann. Plast. Surg. 1984. V. 13. № 2. P. 135-144.
12. Edgerton M. T. Steroid therapy of haemangiomas // Symposium on Vascular Malformations and Melonotic Lesions. Ed. By Williams H. G. St. Louis, C. V. Mosby. 1983. P. 74-83.
13. Enjolras O., Herbretean F. Et al., Hemangiomes et Malformations vasculares superficielles: classification // J. Des Maladies Vasculaires. Paris. 1992. V. 17. № 1. P. 2-19.
14. Fingerhut A. Angiomas of the Smallintestine, Diagnostic and therapeutic problems // Gastroenterol. Clin. Biol. 1978. V. 2. № 12. P. 103-104.
15. Pasyk K. Classification and clinical and histopathological features of hemangiomas and other vascular malformations // Vascular Birthmarks. 1987. P. 1-54.
16. Peck J. E. The treatment of hemangiomas // British Med. J. 1974. V. 2. P. 198-200.
17. Traub E. F. Involution of Haemangiomas // Arch. Pediat. 1933. V. 50. P. 272-278.





Универсальным маркером для оценки клеточного цикла является белок Ki-67, по экспрессии которого можно исследовать пролиферативную активность клеток. Антитела к Ki-67 выявляют пролиферирующие клетки, находящиеся в разных фазах цикла. Это наиболее надежный и четкий маркер пролиферации.
CD31 — гликопротеин, который принадлежит к молекулам клеточной адгезии семейства иммуноглобулинов, известный также как молекула адгезии PECAM-I (эндотелиальная молекула адгезии тромбоцитов), представлен на тромбоцитах, гранулоцитах и клетках эндотелия. Ранее считалось, что этот белок менее специфичен для эндотелия, чем фактор VIII. Однако CD31 оказался более чувствительным маркером злокачественных сосудистых опухолей в связи с его способностью иммуноокрашивать низкодифференцированные очаги в ангиосаркомах и веретеноклеточные поля саркомы Капоши. В случаях мезотелиомы и некоторых аденокарцином может выявляться слабое цитоплазматическое окрашивание на белок CD31.
Специалисты ISSVA рекомендуют проводить следующие иммуногистохимические исследования: GLUT1, Lewis Y antigen, FcyRII, CD15, CCR6, IDO [6]. Авторы проводят свои исследования, не подтверждая и не опровергая предложенный набор иммуногистохимических маркеров.



Выходит, что все, что написано в статье, все что сделано, сводилось к изменению тактики лечения?! Но если не брать в расчет эту статью, то принципы и подходы в лечении младенческих гемангиом уже сформулированы (пример протокола лечения младенческих гемангиом пропранололом), даны рекомендации. Единственное, протоколы и принципы международные и нам надо их адаптировать и использовать. Существует международная классификация сосудистой патологии (ISSVA), которая устраивает специалистов из 68 стран Мира. Все необходимое уже есть.

«Сосудистые гиперплазии «- опять придумали?

Рубрика: 6. Клиническая медицина
Дата публикации: 24.11.2014
Статья просмотрена: 1605 раз
Гемангиомы (ГА) и лимфангиомы (ЛА), будучи доброкачественными врождёнными дисонтогенетическими образованиями, возникают в эмбриональном периоде как порок развития эндотелия пролиферирующих сосудов и проявляются, чаще всего, сразу же после рождения ребёнка или в грудном возрасте. Располагаясь в челюстно-лицевой области (ЧЛО), они зачастую приводят к эстетическим недостаткам или нарушению функции [1, 2, 3, 7, 8, 10].
Особенности топографо-анатомической локализации ГА и ЛА на языке и в области дна полости рта обуславливают наибольшие трудности в их диагностике, выборе тактических приёмов и методов лечения, ведь послеоперационный период сопровождается высокой вероятностью развития осложнений. Поэтому целью нашего исследования стало установление частоты встречаемости, изучение клинико-морфологических особенностей и определение принципов лечения гемангиом и лимфангиом языка у детей.
Материал и методы исследования. В ходе работы мы проанализировали данные фундаментальных научных трудов и периодических изданий касательно указанной проблематики, сопоставив их с результатами изучения историй болезни 81 ребёнка с гемангиомами и 7 с лимфангиомами мягких тканей головы и шеи в возрасте от 2 месяцев до 15 лет, находившихся на лечении с 2005 по 2014 годы в клинике кафедры детской хирургической стоматологии, которая расположена в хирургическом отделении детской городской клинической больницы г.Полтавы.
Среди пациентов мальчиков было 39 (44,3 %), а девочек 49 (55,7 %). Общесоматический и местный статус определяли согласно классических принципов обследования детей данной категории [10].
Во всех случаях образцы послеоперационного материала отправлялись на гистологическое исследование, позволившее на препаратах, изготовленных по общепринятым методикам [4], изучить морфологическое строение ГА и ЛА языка у детей.
Результаты исследования и их обсуждение. Согласно данных, опубликованных ранее сотрудниками нашей кафедры [11], среди доброкачественных опухолей мягких тканей ЧЛО второе место после дермоидных кист (32,6 %) занимают гемангиомы (26,0 %), а лимфангиомы такой локализации встречаются достаточно редко, составляя лишь 3,0 % от общего числа новообразований мягких тканей лица и шеи.
Согласно полученных нами статистических результатов исследования в таблице 1 представлена структура гемангиом мягких тканей головы и шеи в зависимости от локализации. Характерно, что опухоли языка встречались среди них в 2,5 % случаев. Следует отметить, что в 3 наблюдениях (3,7 %) клиническое течение ГА осложнялось изъязвлением покрывающих их тканей или возникновением периодических кровотечений.
Локализация гемангиом мягких тканей головы и шеи у детей
Анатомическая область
Количество случаев
Волосистая часть головы
Другие области лица
Слизистая оболочка щек
Несколько анатомических областей
Из 7 наблюдений лимфангиом мягких тканей головы и шеи в наших исследованиях в 2 случаях опухоли (28,57 %) локализовались в околоушно-жевательной, щёчной области и на языке, а 1 (14,29 %) располагалась в области затылка.
Анализ данных литературных источников показал некоторые разногласия в подходах к классификации сосудистых опухолей [8]. Так, клиницисты делят ГА на капиллярные, гроздевидные, кавернозные, комбинированые и смешанные [1, 2, 10], но, по мнению патоморфологов, гроздевидную форму опухоли выделять нецелесообразно [5]. Кроме того, исследователи считают, что гистологическая структура большинства гемангиом в детском возрасте представлена незрелыми капиллярными образованиями, впоследствии дифференцирующимися в другие формы ГА [3].
В свою очередь лимфангиомы большинство специалистов предпочитает делить по гистологическому строению (капиллярные, кавернозные, кистозные, смешанные), степени роста (ограниченные, диффузные, поверхностные, глубокие) и локализации [1, 2, 7, 10], невзирая на утверждения некоторых патоморфологов, что в мягких тканях ЧЛО у детей встречаются лишь капиллярные и кавернозные формы образований, причём настаивая на подавляющем преобладании последних [5].
В нашем исследовании на языке во всех случаях клинически диагностировались кавернозные гемангиомы и лимфангиомы, что вдальнейшем подтверждалось морфологическими данными.
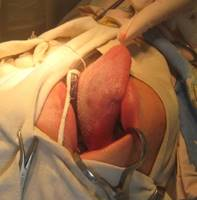
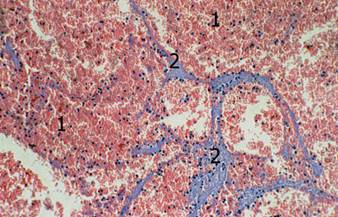
Микроскопически во всех наблюдениях кавернозные гемангиомы языка состояли из тонкостенных полостей, выстланных уплощённым эндотелием, заполненых кровью и анастомозирующих между собой (Рис. 1 в), что соответствует строению кавернозных форм этих опухолей любой локализации [5].
а 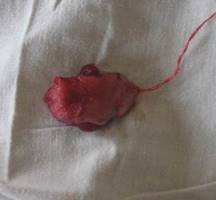
б
в
Рис. 1. Внешний вид перед началом оперативного вмешательства (а), макропрепарат (б) и микроскопическое строение (в) (окраска гематоксилин-эозином, об. 6,3 х , ок. 10 х ) кавернозной гемангиомы языка. 1 — полости, заполненные форменными элементами крови; 2 — соединительнотканные перегородки
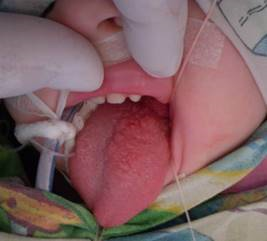
Рис. 2. Общий вид поверхностной кавернозной лимфангиомы языка
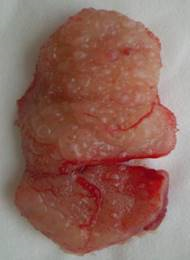
Макроскопически лимфангиомы представляли собой губчатые узлы без выраженной капсулы (Рис. 3 а), состоящие из множества заполненных прозрачной или мутной жидкостью полостей, сообщающихся между собой.
Микроскопически ЛА состояли из сильно расширенных лимфатических сосудов либо пространств, выстланных эндотелием и содержащих различное количество лимфы, лимфоцитов, а иногда и эритроцитов. В отдельных случаях в стенках пространств встречались пучки гладкомышечных волокон со скоплениями лимфоцитов, а в строме обычно определялись фиброз и признаки воспалительной инфильтрации (Рис. 3 б). Следует отметить, что подобная морфологическаая картина также присуща и кавернозным лимфангиомам других локализаций [5].
Общей особенностью лимфангиом у детей исследователи считают предрасположенность к воспалению [1, 2, 10], однако нам такие случаи не встречались.
Выбор метода лечения ГА и ЛА зависит, безусловно, от нозологической формы и распространённости опухолевого процесса. При этом возможны диатермокоагуляция, склерозирующая терапия, хирургическое удаление, лазеротерапия, прошивание опухоли, системное применение гормонов и интерферона, лучевая и компрессионная терапия [1, 2, 6, 8, 9, 10].
а 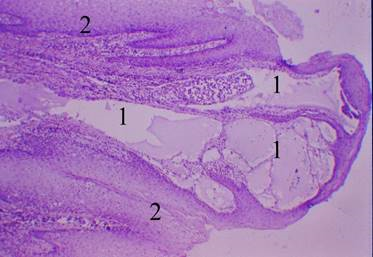
б
Рис. 3. Макропрепарат (а) и микроскопическое строение (б) (окраска гематоксилин-эозином, об. 3,5 х ; ок.10 х ) поверхностной кавернозной лимфангиомы языка. 1 — каверны, заполненные лимфой; 2 — покровный эпителий слизистой оболочки языка
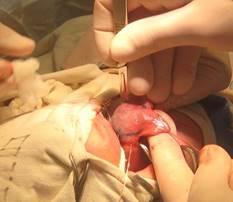
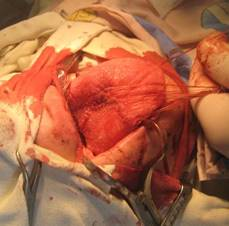
Во всех наших наблюдениях лечение гемангиом и лимфангиом языка сводилось к их хирургическому удалению (Рис. 4, 5). Учитывая склонность кавернозной лимфангиомы к рецидивированию [1, 3, 9, 11], прооперированные дети находятся на диспансерном наблюдении.
а 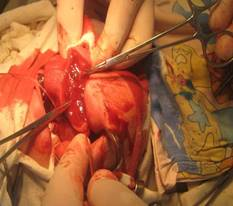
б
в
Рис. 4. Этапы хирургического удаления кавернозной гемангиомы языка
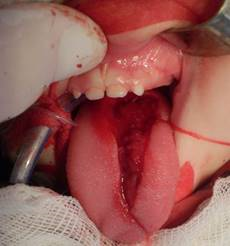
Рис. 5. Вид послеоперационной раны после удаления поверхностной кавернозной лимфангиомы языка
Полученные данные позволяют сделать следующие выводы.
1. В структуре гемангиом и лимфангиом мягких тканей головы и шеи у детей эти опухоли языка составляют, соответственно, 2,5 % и 28,57 %.
2. По клинической симптоматике во всех наблюдениях гемангиомы и лимфангиомы языка у детей являлись кавернозными образованиями, что подтверждено результатами морфологического исследования, выявившего сходство их строения с кавернозными формами опухолей иной анатомической локализации. Это позволяет использовать научные наработки по данному вопросу и применительно к образованиям, располагающимся непосредственно в области лица и шеи.
1. Бернадский Ю. И. Основы челюстно-лицевой хирургии и хирургической стоматологии / Ю. И. Бернадский — М.: Медицинская литература, 2000. — 404 с.
2. Зеленский В. А. Детская хирургическая стоматология и челюстно-лицевая хирургия / В. А. Зеленский, Ф. С. Мухорамов — Москва, 2008. — 206 с.
3. Колесов А. А. Новообразования мягких тканей и костей лица у детей и подростков / А. А. Колесов, Ю. И. Воробьёв, Н. Н. Каспарова — М.: Медицина, 1989. — 302 с.
4. Меркулов А. Б. Курс патогистологической техники / А. Б. Меркулов — Л.: Медицина, 1969. — 237 с.
5. Пальцев М. А. Патологическая анатомия / М. А. Пальцев, Н. М. Аничков — М.: Медицина, 2001. — 525 с.
6. Тетруева Н. А. Тактика лечения гемангиом челюстно-лицевой области у детей. Применение пропранолола в качестве первой линии терапии гемангиом сложных локализаций / Н. А. Тетруева, А. В. Тимошенко, Д. В. Лучинский / Нові технології в хірургічній стоматології і щелепно-лицевій хірургії // Матеріали науково-практичної конференції, присвяченої 100-річчю з дня народження професора Г.І.Семенченка. — Одеса, 2014. — С. 21–27.
7. Ткаченко П. И. Лимфангиомы челюстно-лицевой локализации у детей: статистика и диагностический алгоритм / П. И. Ткаченко, Е. В. Гуржий, С. А. Белоконь // Матеріали ІІІ (Х) з’їзду Асоціації стоматологів України. — Полтава, 2008. — С. 337.
8. Ткаченко П. И. Сосудистые опухоли мягких тканей челюстно-лицевой области у детей / П. И. Ткаченко, И. И. Старченко, С. А. Белоконь, Е. В. Гуржий — СтоматологИнфо. — 2014. — № 7–8. — С. 36–42.
9. Харьков Л. В. Діагностика та лікування гемангіом щелепно-лицевої ділянки у дітей / Л. В. Харьков, Л. М. Яковенко, Кисельова Н. В. / Нові технології в хірургічній стоматології і щелепно-лицевій хірургії // Матеріали науково-практичної конференції, присвяченої 100-річчю з дня народження професора Г.І.Семенченка. — Одеса, 2014. — С. 17–19.
10. Харьков Л. В. Хірургічна стоматологія дитячого віку / Л. В. Харьков, Л. М. Яковенко, І.А.Чехова — К.: Книга-плюс, 2003. — 480 с.
11. Шешукова Я. П. Структура та частота доброякісних новоутворень м’яких тканин обличчя, щелепних кісток у дітей і дорослих / Я. П. Шешукова. — Український стоматологічний альманах. — 2013. — № 3. — С. 46–49.
Похожие статьи
[2] У детей опухоль часто сочетается с различными пороками развития.
В отдельных случаях наблюдаются кавернозные полости с сосочковыми образованиями или участки солидного строения.
При микроскопии использовались окраска гематоксилин-эозин, ШИК-реакция по.
Рис. 2. Микроскопическое строение мягкой фибромы. Окраска гематоксилин-эозином.
Рис. 5. Микроскопическое строение внутрикостной фибромы. Окраска по Ван-Гизону. Об.
Белоконь С. А. Гемангиомы мягких тканей челюстно-лицевой области у детей.
(2012 г.), сосудистые опухоли являются наиболее распространенными доброкачественными опухолями головы и шеи в младенчестве и детстве. Сосудистые аномалии головы и шеи были разделены на 2 категории, включая гемангиомы и сосудистые мальформации.
– множество мелких пигментных пятен (типа веснушек) в подмышечных или паховых областях
Гистологические препараты окрашивались гематоксилин-эозином, пирофуксином по
Фоновое: Нейрофиброматоз, васкулярная форма с образованием гемангиом желудка.
По данным литературы, больные шилоподъязычным синдромом чаще всего жалуются на болезненные ощущения в передней области шеи и иррадиацией боли в глотку, корень языка, ухо.
Важнейшей функцией лимфатических образований твердой оболочки головного мозга
А. В. Демин (1999), М.Johnston, D. Armstrong, L. Koh (2007) находили места резорбции ликвора около кавернозного синуса, в
(окраска гематоксилином-эозином и по методике Ван-Гизона).
Гемангиомы могут располагаться в области спины, шеи и головы, на верхних и нижних конечностях, ягодицах и туловище [4]. Выделяют три типа гемангиом: гипертрофические (доброкачественные гемангиоэндотелиомы), капиллярные, кавернозные.
карциноид. гемангиома. гамартома. Метастаз аденокарцином.
Окраска гематоксилин-эозин. Ок.15Хоб.40.
Капсула утолщена, в области казеозного некроза обнаружены единичные гранулематозные инфильтраты.
Одностороннее увеличение шейных или нижнечелюстных лимфатических узлов предполагает лимфому или опухоль нелимфоидной природы в области головы и шеи, либо метастазы злокачественных опухолей.
- Как издать спецвыпуск?
- Правила оформления статей
- Оплата и скидки
Похожие статьи
[2] У детей опухоль часто сочетается с различными пороками развития.
В отдельных случаях наблюдаются кавернозные полости с сосочковыми образованиями или участки солидного строения.
При микроскопии использовались окраска гематоксилин-эозин, ШИК-реакция по.
Рис. 2. Микроскопическое строение мягкой фибромы. Окраска гематоксилин-эозином.
Рис. 5. Микроскопическое строение внутрикостной фибромы. Окраска по Ван-Гизону. Об.
Белоконь С. А. Гемангиомы мягких тканей челюстно-лицевой области у детей.
(2012 г.), сосудистые опухоли являются наиболее распространенными доброкачественными опухолями головы и шеи в младенчестве и детстве. Сосудистые аномалии головы и шеи были разделены на 2 категории, включая гемангиомы и сосудистые мальформации.
– множество мелких пигментных пятен (типа веснушек) в подмышечных или паховых областях
Гистологические препараты окрашивались гематоксилин-эозином, пирофуксином по
Фоновое: Нейрофиброматоз, васкулярная форма с образованием гемангиом желудка.
По данным литературы, больные шилоподъязычным синдромом чаще всего жалуются на болезненные ощущения в передней области шеи и иррадиацией боли в глотку, корень языка, ухо.
Важнейшей функцией лимфатических образований твердой оболочки головного мозга
А. В. Демин (1999), М.Johnston, D. Armstrong, L. Koh (2007) находили места резорбции ликвора около кавернозного синуса, в
(окраска гематоксилином-эозином и по методике Ван-Гизона).
Гемангиомы могут располагаться в области спины, шеи и головы, на верхних и нижних конечностях, ягодицах и туловище [4]. Выделяют три типа гемангиом: гипертрофические (доброкачественные гемангиоэндотелиомы), капиллярные, кавернозные.
карциноид. гемангиома. гамартома. Метастаз аденокарцином.
Окраска гематоксилин-эозин. Ок.15Хоб.40.
Капсула утолщена, в области казеозного некроза обнаружены единичные гранулематозные инфильтраты.
Одностороннее увеличение шейных или нижнечелюстных лимфатических узлов предполагает лимфому или опухоль нелимфоидной природы в области головы и шеи, либо метастазы злокачественных опухолей.
Читайте также:

