Миелобластный лейкоз терминальная стадия
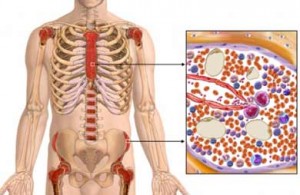
Терминальная стадия хронического миелолейкоза (ХМЛ) может иметь разные клинико-гематологические характеристики. Клиническая картина в этой стадии резко отличается от благополучной картины в хронической стадии и малосимптомных проявлений в стадии акселерации. Появляются резкая слабость, длительные ноющие, а иногда очень сильные боли в костях, суставах или радикулярные, подъемы температуры, нередко до 38—39 °С, часто сопровождающиеся ознобом, проливные поты, снижение массы тела. Как правило, начинает быстро увеличиваться в размерах селезенка.
Нередко в этот период в связи с быстрым нарастанием опухолевой массы в селезенке развиваются инфаркты. Часто увеличивается печень, иногда быстро и значительно, выступая из-под реберного края на 15—20 см, чего мы никогда не наблюдали в хронической стадии болезни. Как правило, присоединяются симптомы геморрагического диатеза. Состояние больного в большинстве случаев тяжелое.
У 80—85 % больных гематологические проявления в терминальной стадии хронического миелолейкоза характеризуются развитием бластного криза с увеличением бластных клеток в крови и/или костном мозге от 30 % и выше.
В большинстве случаев бластные клетки в крови и костном мозге составляют 60—80—95 % от всех ядросодержащих клеток. Не менее чем у 50 % больных в этой стадии обнаруживается выраженный фиброз костного мозга.
Количество лейкоцитов в периоде бластного криза может резко увеличиться, но может быть и небольшим — всего 10—15•10 9 /л.
В крови и костном мозге в момент появления экстрамедуллярных очагов бластной инфильтрации может не быть признаков терминальной стадии. Такое положение иногда сохраняется очень долго (в одном из наших наблюдений более одного года), однако в большинстве случаев бластный криз развивается на протяжении ближайших месяцев или даже недель.

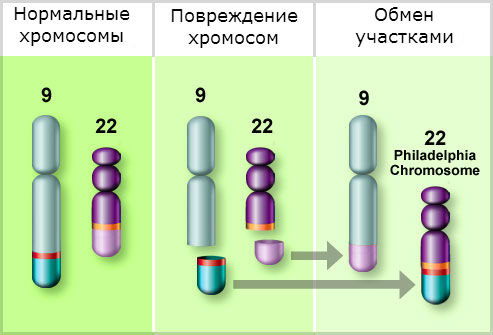
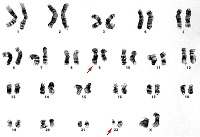
У подавляющего числа больных (70—80 %) в терминальной стадии хронического миелолейкоза (ХМЛ) цитогенетическое исследование позволяет обнаружить, помимо t(9;22)(q34;q11), добавочные хромосомные аберрации. Наиболее частые из них в порядке убывания: трисомия хромосомы 8, вторая Ph-хромосома, перестройка хромосомы 17 с появлением вместо нормальной изохромосомы 17q, трисомия хромосомы 19. Нередко наблюдается сочетание этих изменений, одновременное обнаружение клеток с разными хромосомными аберрациями у одного больного или наличие клеток, в которых одновременно имеются различные аберрации.
Например, нередко сочетание в одной клетке трисомии 8 с изохромосомой 17. В некоторых случаях наблюдаются аберрации с большим числом добавочных хромосом, обычно это вторая Ph-хромосома; одновременно трисомия хромосом 19, 6 и др..
Существует определенный параллелизм между морфоцитохимическим типом бластного криза и характером хромосомных аберраций. Так, при недифференцированном варианте бластного криза нередко нет добавочных хромосомных аберраций, при миелобластном варианте часто обнаруживается изохромосома 17q. При лимфоидном варианте, наоборот, не наблюдается инверсии хромосомы 17 или других ее изменений, однако нередко встречаются множественные аберрации с преобладанием клеток с большим числом хромосом.
В тех случаях, когда терминальная стадия проявляется образованием экстрамедуллярного бластного инфильтрата, нередко удается обнаружить появление именно в этих очагах клеток, имеющих, помимо t(9;22), другие хромосомные аберрации. Мы наблюдали больных, у которых вначале клетки с добавочными хромосомными аберрациями были обнаружены только в лимфатическом узле или другой экстрамедуллярной опухоли, а при развившемся затем бластном кризе эти клетки составили преобладающий клон среди элементов костного мозга.
Показано, что уровень экспрессии гена BCR-ABL начинает увеличиваться за некоторое время до появления морфологических признаков перехода заболевания в фазу акселерации или развития бластного криза. Возможно, это свидетельствует об уже начавшемся увеличении пула незрелых предшественников, поскольку известно, что экспрессия BCR-ABL наиболее высока именно в этих клетках и прогрессивно уменьшается во все более зрелых элементах гемопоэза.
Кроме того, обнаружено, что как в стадии акселерации, так и особенно в терминальной стадии болезни в лейкемических клетках часто определяется мутантный тип гена ТР53, что ведет к нарушению его функции, обеспечивающей апоптоз клеток с измененным геномом (например, с хромосомными аберрациями). В то же время в лейкемических клетках в этих стадиях болезни обнаружено увеличение экспрессии гена BCL-2, функцией которого является уменьшение чувствительности клеток к сигналам апоптоза.
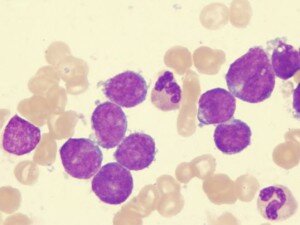
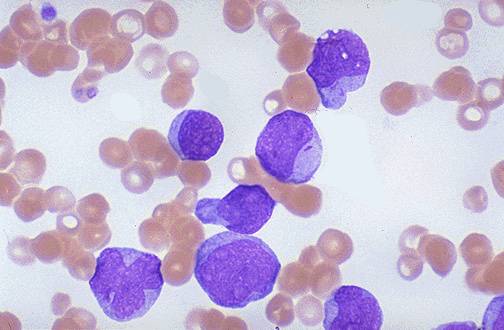
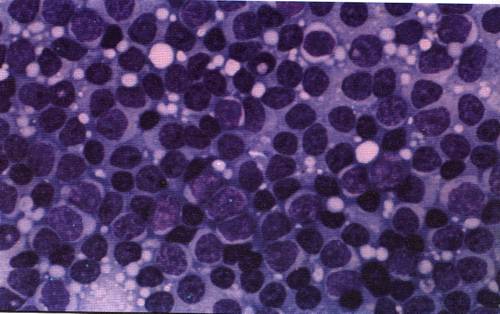
Картина крови при остром лейкозе (бласты)
Острый лейкоз — это группа тяжелых заболеваний крови опухолевой природы, при которых патологический процесс начинается на уровне клеток-предшественниц гемопоэза (стволовых клеток), утрачивающих свою способность созревать до зрелых форм, что приводит к несостоятельности гемопоэза и накоплению в костном мозге и крови незрелых бластных форм.
Основной субстрат опухоли составляют молодые, так называемые бластные клетки.
В зависимости от морфологии и цитохимических показателей клеток в группе острых лейкозов выделяют: острый миелобластный лейкоз, острый монобластный лейкоз, острый миеломонобластный лейкоз, острый промиелоцитарный лейкоз, острый эритромиелоз, острый мегакариобластный лейкоз, острый недифференцируемый лейкоз, острый лимфообластный лейкоз.
Этиология
Причиной возникновения острых лейкозов и хронического миелолейкоза человека могут быть нарушения состава и структуры хромосомного аппарата, наследственно обусловленные или приобретенные под влиянием некоторых мутагенных факторов. Одним из них является ионизирующая радиация.
Причиной развития лейкозов является также действие химических мутагенов. Доказано учащение острых лейкозов среди лиц, подвергавшихся воздействию бензола, а также среди больных, получавших цитостатические иммунодепрессанты (имуран, циклофосфан, лейкаран, сарколизин, мустарген и др. ); частота острых лейкозов среди этого контингента больных повышается в сотни раз. Известны факты возникновения острого миелобластного лейкоза, острого эритромиелоза на фоне длительной химиотерапии хронического лимфолейкоза, макроглобулинемии Вальденстрема, миеломной болезни, лимфогранулематоза и других опухолей.
Показана предрасполагающая клейкозам роль наследственных дефектов в миелоидной и лимфатической ткани. Описаны наблюдения доминантного и рецессивного наследования хронического лимфолейкоза, отмечена низкая заболеваемость этим лейкозом в некоторых этнических группах и повышенная — в других. Чаще в этих случаях наследуется не сам лейкоз, а повышенная изменчивость — нестабильность хромосом, предрасполагающая родоначальные миелоидные или лимфатические клетки к лейкозной трансформации.
Стадии лейкоза
1) начальная;
2) развернутая;
3) ремиссия (полная или неполная);
4) рецидив;
5) терминальная.
Начальная стадия острого лейкоза диагностируется чаще всего тогда, когда у больных с предшествующей анемией в дальнейшем развивается картина острого лейкоза.
Развернутая стадия характеризуется наличием основных клинических и гематологических проявлений заболевания.
Ремиссия может быть полной или неполной. К полной ремиссии относятся состояния, при которых отсутствуют клинические симптомы заболевания, количество бластных клеток в костном мозге не превышает 5 % при отсутствии их в крови. Состав периферической крови близок к норме. При неполной ремиссии имеет место отчетливое клиническое и гематологическое улучшение, однако количество бластных клеток в костном мозге остается повышенным.
Рецидив острого лейкоза может возникать в костном мозге или вне костного мозга (кожа и т. д.). Каждый последующий рецидив прогностически более опасен, чем предыдущий.
Терминальная стадия острого лейкоза характеризуется резистентностью к цитостатической терапии, выраженным угнетением нормального кроветворения, развитием язвенно-некротических процессов.
Клиническая картина
Клиническая симптоматика очень разнообразна и зависит от локализации и массивности лейкемической инфильтрации и от признаков подавления нормального кроветворения (анемия, гранулоцитопения, тромбоцитопения).
Первые проявления заболевания носят общий характер: слабость, снижение аппетита, потливость, недомогание, повышение температуры неправильного типа, боли в суставах, появление небольших синяков после мелких травм. Болезнь может начинаться остро — с катаральных изменений в носоглотке, ангины. Иногда острый лейкоз выявляется при случайном исследовании крови.
В развернутой стадии заболевания в клинической картине можно выделить несколько синдромов: анемический синдром, геморрагический синдром, инфекционные и язвенно-некротические осложнения.
Анемический синдром проявляется слабостью, головокружением, болями в области сердца, одышкой. Объективно отмечается бледность кожных покровов и слизистых оболочек. Выраженность анемии различна и определяется степенью угнетения эритропоэза, наличием гемолиза, кровотечений и прочее.
Геморрагический синдром встречается практически у всех больных. Обычно наблюдаются десневые, носовые, маточные кровотечения, геморрагия на коже и слизистых оболочках. В местах уколов и внутривенных инъекций возникают обширные кровоизлияния. В терминальной стадии на месте кровоизлияний в слизистой оболочке желудка, кишечника появляются язвенно-некротические изменения. Наиболее выраженный геморрагический синдром наблюдается при промиелоцитарном лейкозе.
Инфекционные и язвенно-некротические осложнения являются следствием гранулоцитопении, снижения фагоцитарной активности гранулоцитов и встречаются более чем у половины больных острым лейкозом. Часто возникают пневмонии, ангины, инфекции мочевыводящих путей, абсцессы в местах инъекций. Температура может быть различной — от субфебрильной до постоянно высокой. Значительное увеличение лимфатических узлов у взрослых встречается редко, у детей — довольно часто. Особенно характерны лимфаденопатии для лимфобластного лейкоза. Чаще увеличиваются лимфоузлы в надключичных и подчелюстных областях. При пальпации лимфатические узлы плотные, безболезненные, могут быть слегка болезненны при быстром росте. Увеличение печени и селезенки не всегда наблюдается, преимущественно при лимфобластном лейкозе.
Диагностика
В периферической крови у большинства больных обнаруживается анемия нормохромного, реже гиперхромного типа. Анемия углубляется с прогрессированием заболевания до 20 г/л, а количество эритроцитов отмечается ниже 1,0 г/л. Нередко анемия является первым проявлением лейкоза. Количество ретикулоцитов также уменьшено. Число лейкоцитов обычно повышено, но не достигает таких высоких цифр, как при хронических лейкозах. Количество лейкоцитов колеблется в значительных пределах от 0,5 до 50-300 г/л.
Формы острого лейкоза с высоким лейкоцитозом прогностически менее благоприятны. Наблюдаются формы лейкоза, которые с самого начала характеризуются лейкопенией. Тотальная бластная гиперплазия при этом наступает лишь в терминальной стадии болезни.
Для всех форм острого лейкоза характерно снижение количества тромбоцитов до 15-30 г/л. Особенно выраженная тромбоцитопения наблюдается в терминальной стадии.
В лейкоцитарной формуле — бластные клетки до 90 % всех клеток и незначительное количество зрелых элементов. Выход в периферическую кровь бластных клеток является основным морфологическим признаком острого лейкоза.
Для дифференциации форм лейкоза, кроме морфологических признаков, используют цитохимические исследования (содержание липидов, активность пероксидазы, содержание гликогена, активность кислой фосфатазы, активность неспецифической эстеразы и т. д.), биопсию костного мозга, мазки крови.
Формы лейкоза
Острый промиелоцитарный лейкоз характеризуется чрезвычайной злокачественностью процесса, быстрым нарастанием тяжелой интоксикации, выраженным геморрагическим синдромом, приводящим к кровоизлиянию в мозг и к гибели больного.
Опухолевые клетки с крупной зернистостью в цитоплазме затрудняют определение структур ядра. Положительные цитохимические признаки: активность пероксидазы, много липидов и гликогена, реакция на кислую фосфотазу резко положительна, наличие гликозоаминогликана.
Геморрагический синдром зависит от выраженной гипофибриногенемии и избыточного содержания в лейкозных клетках тромбопластина. Выход тромбопластина провоцирует внутрисосудистое свертывание.
Острый миелобластный лейкоз характеризуется прогрессирующим течением, выраженной интоксикацией и лихорадкой, рано наступающей клинико-гематологической декомпенсацией процесса в виде тяжелой анемии, умеренной интенсивностью геморрагических проявлений, частных язвенно-некротических поражений слизистых и кожи.
В периферической крови и костном мозге преобладают миелобласты. При цитохимическом исследовании выявляется активность пероксидазы, повышение содержания липидов, низкая активность неспецифической эстеразы.
Острый лимфомонобластный лейкоз является субвариантом острого миелобластного лейкоза. По клинической картине они почти идентичны, однако миеломонобластная форма протекает злокачественней, с более выраженной интоксикацией, глубокой анемией, тромбоцитопенией, более выраженным геморрагическим синдромом, частыми некрозами слизистых и кожи, гиперплазией десен и миндалин. В крови выявляются бластные клетки — крупные, неправильной формы, с молодым ядром, напоминающим по форме ядро моноцита. При цитохимическом исследовании в клетках определяется положительная реакция на пероксидазу, гликоген и липиды. Характерным признаком является положительная реакция на неспецифическую эстеразу в клетках и лизоцим в сыворотке и моче.
Средняя продолжительность жизни больных вдвое меньше, чем при миелобластном лейкозе. Причиной смерти обычно являются инфекционные осложнения.
Острый монобластный лейкоз — редкая форма лейкоза. Клиническая картина напоминает острый миелобластный лейкоз и характеризуется анемийной налонностью к геморрагиям, увеличением лимфатических узлов, увеличением печени, язвенно-некротическим стоматитом. В периферической крови — анемия, тромбоцитопения, лимфомоноцитарный профиль, повышенный лейкоцитоз. Появляются молодые бластные клетки. При цитохимическом исследовании в клетках определяется слабоположительная реакция на липиды и высокая активность неспецифической эстеразы. Лечение редко вызывает клинико-гематологические ремиссии. Продолжительность жизни больного составляет около 8-9 месяцев.
Острый лимфобластный лейкоз чаще встречается у детей и у лиц молодого возраста. Характеризуется увеличение какой-либо группы лимфоузлов, селезенки. Самочувствие больных не страдает, интоксикация выражена умеренно, анемия незначительная. Геморрагический синдром часто отсутствует. Больные жалуются на боли в костях. Острый лимфобластный лейкоз отличается частотой неврологических проявлений (нейролейкемия).
В периферической крови и в пунктате-лимфобласта молодые крупные клетки с округлым ядром. При цитохимическом исследовании: реакция на пероксидазу всегда отрицательная, липиды отсутствуют, гликоген в виде крупных гранул.
Отличительной чертой лимфобластного острого лейкоза является положительный ответ на применяемую терапию. Частота ремиссии — от 50 % до 90 %. Ремиссия достигается применением комплекса цитостатических средств. Рецидив болезни может проявляться нейролейкемией, инфильтрацией нервных корешков, костномозговой ткани. Каждый последующий рецидив имеет худший прогноз и течет более злокачественно, чем предыдущий. У взрослых заболевание протекает тяжелее, чем у детей.
Эритромиелоз характеризуется тем, что патологическая трансформация кроветворения касается как белого, так и красного ростков костного мозга. В костном мозге обнаруживаются молодые недифференцированные клетки белого ряда и бластные анаплазированные клетки красного ростка — эритро- и нормобласты в большом количестве. Красные клетки больших размеров имеют уродливый вид.
В периферической крови — стойкая анемия, анизоцитоз эритроцитов (макроциты, мегалоциты), пойкилоцитоз, полихромазия и гиперхромия. Эритро- и нормобласты в периферической крови — до 200-350 на 100 лейкоцитов. Часто отмечается лейкопения, но может быть умеренное увеличение лейкоцитов до 20-30 г/л. По мере развития болезни появляются бластные формы-монобласты. Лимфаденопатии не наблюдается, печень и селезенка могут быть увеличены или оставаться в норме. Заболевание протекает более длительно, чем миелобластная форма, в некоторых случаях отмечается подострое течение эритромиелоза (до двух лет без лечения).
Лечение
Длительность непрерывной поддерживающей терапии должна быть не менее 3-х лет. Для своевременного выявления рецидива необходимо производить контрольные исследования костного мозга не реже 1 раза в месяц в первый год ремиссии и 1 раз в 3 месяца после года ремиссии. В период ремиссии может проводиться так называемая иммунотерапия, направленная на уничтожение оставшихся лейкемических клеток с помощью иммунологических методов. Иммунотерапия заключается во введении больным вакцины БЦЖ или аллогенных лейкемических клеток.
Рецидив лимфобластного лейкоза лечится обычно теми же комбинациями цитостатиков, что и в период индукции.
При нелимфобластных лейкозах основная задача сводится обычно не к достижению ремиссии, а к сдерживанию лейкемического процесса и продлению жизни больного. Это связано с тем, что нелимфобластные лейкозы характеризуются резким угнетением нормальных ростков кроветворения, в связи с чем проведение интенсивной цитостатической терапии часто невозможно.
Для индукции ремиссиии у больных нелимфобластными лейкозами используют комбинации цитостатических препаратов; цитозин-арабинозид, дауномицин: цитозин арабинозид, тиогуанин; цитозин-арабинозид, онковин (винкристин), циклофосфан, преднизолон. Курс лечения длится 5-7 дней с последующим 10-14 дневным перерывом, необходимым для восстановления нормального кроветворения, угнетаемого цитостатиками. Поддерживающая терапия проводится теми же препаратами или их комбинациями, применяющимися в период индукции. Практически у всех больных нелимфобластными лейкозами развивается рецидив, требующий смены комбинации цитостатиков.
Важное место в лечении острого лейкоза занимает терапия внекостномозговых локализаций, среди которых наиболее частым и грозным является нейролейкемия (менинго-энцефалитический синдром: тошнота, рвота, нестерпимая головная боль; синдром локального поражения вещества головного мозга; псевдотуморозная очаговая симптоматика; расстройство функций черепно-мозговых нервов; глазодвигательного, слухового, лицевого и тройничного нервов; лейкозная инфильтрация нервных корешков и стволов: синдром полирадикулоневрита). Методом выбора при нейролейкемии является внутрилюмбальное введение метотрексата и облучение головы в дозе 2400 рад. При наличии внекостномозговых лейкемических очагов (носоглотка, яичко, лимфатические узлы средостения и др.), вызывающих сдавление органов и болевой синдром, показана локальная лучевая терапия в общей дозе 500-2500 рад.
Лечение инфекционных осложнений проводится антибиотиками широкого спектра действия, направленных против наиболее частых возбудителей — синегнойной палочки, кишечной палочки, золотистого стафилококка. Применяют карбенициллин, гентамицин, цепорин. Антибиотикотерапию продолжают не менее 5 дней. Антибиотики следует вводить внутривенно каждые 4 часа.
Для профилактики инфекционных осложнений, особенно у больных с гранулоцитопенией, необходим тщательный уход за кожей и слизистой оболочкой полости рта, помещение больных в специальные асептические палаты, стерилизация кишечника с помощью неадсорбируемых антибиотиков (канамицин, ровамицин, неолепцин). Основным методом лечения геморрагии у больных острым лейкозом является переливание тромбоцитарной массы. Одномоментно больному переливают 200-10000 г/л тромбоцитов 1-2 раза в неделю. При отсутствии тромбоцитарной массы можно переливать с гемостатической целью свежую цельную кровь или пользоваться прямым переливанием. В некоторых случаях для купирования кровоточивости показано применение гепарина (при наличии внутрисосудистой коагуляции), эпсилон-аминокапроновой кислоты (при повышенном фибронолизе).
Современные программы лечения лимфобластного лейкоза позволяют получить полные ремиссии в 80-90 % случаях. Длительность непрерывных ремиссий у 50 % больных составляет 5 лет и выше. У остальных 50 % больных терапия оказывается неэффективной и развиваются рецидивы. При нелимфобластных лейкозах полные ремиссии достигаются у 50-60 % больных, однако рецидивы развиваются у всех больных. Средняя продолжительность жизни больных составляет 6 месяцев. Основными причинами смерти являются инфекционные осложнения, выраженный геморрагический синдром, нейролейкемия.
Хронический миелолейкоз - опухолевое заболевание крови. Характеризуется бесконтрольным ростом и размножением всех ростковых клеток крови, при этом молодые злокачественные клетки способны созревать до зрелых форм.
Во время хронического миелолейкоза в крови повышается содержание особой разновидности лейкоцитов – гранулоцитов. Они образуются в красном костном мозге в огромном количестве и выходят в кровь, не успевая до конца созреть. Одновременно содержание всех остальных видов лейкоцитов снижается.
Причины хронического миелолейкоза
Причины хромосомного нарушения, приводящего к хроническому миелолейкозу, до сих пор изучены недостаточно.
Считается, что имеют значение следующие факторы:
![]()
Слабые дозы радиации. Их роль доказана только у 5% больных.- Электромагнитные излучения, вирусы и некоторые химические вещества – их влияние не доказано окончательно.
- Применение некоторых лекарственных препаратов. Известны случаи возникновения хронического миелолейкоза при лечении цитостатиками (противоопухолевые препараты) в сочетании с лучевой терапией.
- Наследственные причины. Люди с хромосомными нарушениями (синдром Клайнфелтера, синдром Дауна) имеют повышенный риск хронического миелоидного лейкоза.
- Клетки размножаются неконтролируемо, как раковые.
- Для этих клеток перестают работать естественные механизмы гибели.
Фазы хронического миелолейкоза
- Хроническая фаза. В этой фазе находится большинство пациентов, которые обращаются к врачу (около 85%). Средняя продолжительность – 3 – 4 года (зависит от того, насколько своевременно и правильно начато лечение). Это стадия относительной стабильности. Пациента беспокоят минимальные симптомы, на которые он может не обращать внимания. Иногда врачи выявляют хроническую фазу миелолейкоза случайно, при проведении общего анализа крови.
- Фаза акселерации. Во время этой фазы патологический процесс активируется. Количество незрелых белых кровяных телец в крови начинает быстро нарастать. Фаза акселерации является как бы переходной от хронической к последней, третьей.
- Терминальная фаза. Финальная стадия болезни. Возникает при нарастании изменений в хромосомах. Красный костный мозг практически полностью замещается злокачественными клетками. Во время терминальной стадии пациент погибает.
Проявления хронического миелолейкоза
![]()
Вначале симптомы могут полностью отсутствовать, либо они выражены настолько слабо, что больной не придает им особого значения, списывает на постоянное переутомление. Заболевание выявляется случайно, во время очередной сдачи общего анализа крови.- Нарушение общего состояния: слабость и недомогание, постепенная потеря веса, снижение аппетита, повышенная потливость по ночам.
- Признаки, обусловленные увеличением размеров селезенки: во время приема пищи больной быстро наедается, боли в левой части живота, наличие опухолевидного образования, которое можно прощупать.
- Признаки, связанные с нарушением функции тромбоцитов и белых кровяных телец: различные кровотечения либо, напротив, образование тромбов.
- Признаки, связанные с повышением количества тромбоцитов и, как следствие, повышением свертываемости крови: нарушение кровообращения в головном мозге (головные боли, головокружения, снижение памяти, внимания и пр.), инфаркт миокарда, нарушение зрения, одышка.
- Резкая слабость, значительное ухудшение общего самочувствия.
- Длительные ноющие боли в суставах и костях. Иногда они могут быть очень сильными. Это связано с разрастанием злокачественной ткани в красном костном мозге.
- Проливные поты.
- Периодическое беспричинное повышение температуры до 38 - 39⁰C, во время которого возникает сильный озноб.
- Снижение массы тела.
- Повышенная кровоточивость, появление кровоизлияний под кожей. Эти симптомы возникают в результате уменьшения количества тромбоцитов и снижением свертываемости крови.
- Быстрое увеличение размеров селезенки: живот увеличивается в размерах, появляется чувство тяжести, боли. Это происходит за счет роста опухолевой ткани в селезенке.
Диагностика заболевания
| Название исследования | Описание | Что выявляет? |
| Общий анализ крови | Рутинное клиническое исследование, выполняется при подозрении на любые заболевания. Общий анализ крови помогает определить общее содержание лейкоцитов, их отдельных разновидностей, незрелых форм. Кровь для анализа берут из пальца или вены в утренние часы. |
Симптомы
- Приапизм – болезненная, чрезмерно длительная эрекция.
Данные симптомы это предвестники тяжелого состояния (бластного криза), появляются за 6- 12 месяцев до его начала.
- Снижается эффективность лекарств (цитостатиков)
- Развивается анемия
- Увеличивается процент бластных клеток в крови
- Ухудшается общее состояние
- Увеличивается селезенка
- Симптомы соответствую клинической картине при остром лейкозе (см. Острый лимфолейоз).
Как лечат миелолейкоз?
Цель лечения снизить рост опухолевых клеток и уменьшить размеры селезенки.
Лечение заболевания должно быть начато сразу после того, как установлен диагноз. От качества и своевременности терапии во многом зависит прогноз.
Лечение включает различные методы: химиотерапия, лучевая терапия, удаление селезенки, пересадка костного мозга.
Химиотерапия
- Классические препараты: Миелосан (Милеран, Бусульфан), Гидроксиуреа (Гидреа, Литалир), Цитозар, 6-меркаптопурни, альфа-интерферон.
- Новые препараты: Гливек, Спрайсел.
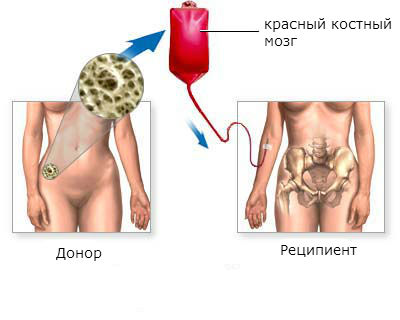
Пересадка костного мозга даёт возможность полностью выздороветь больным хроническим миелолейкозом. Эффективность пересадки выше в хронической фазе заболевания, в остальных фазах гораздо ниже.
Трансплантация красного костного мозга является наиболее эффективным методом лечения хронического миелоидного лейкоза. Более чем у половины пациентов, которым была произведена пересадка, наступает стойкое улучшение в течение 5 лет и дольше.
Чаще всего выздоровление происходит в том случае, когда красный костный мозг пересаживают больному моложе 50 лет в хроническую фазу заболевания.
Этапы трансплантации красного костного мозга:
- Поиск и подготовка донора. Лучшим донором стволовых клеток красного костного мозга является близкий родственник больного: близнец, брат, сестра. Если близких родственников нет, или они не подходят, ищут донора. Проводят ряд тестов для того, чтобы убедиться, что донорский материал приживется в теле пациента. Сегодня в развитых странах созданы большие банки доноров, в которых находятся десятки тысяч донорских образцов. Это дает шанс быстрее найти подходящие стволовые клетки.
- Подготовка пациента. Обычно этот этап продолжается от недели до 10 дней. Проводят лучевую терапию и химиотерапию для уничтожения как можно большего количества опухолевых клеток, предотвращения отторжения донорских клеток.
- Собственно пересадка красного костного мозга. Процедура похожа на переливание крови. В вену пациента заводят катетер, через который в кровь вводят стволовые клетки. Они какое-то время циркулируют в кровотоке, а потом оседают в костном мозге, приживаются там и начинают работать. Для предотвращения отторжения донорского материала врач назначает противовоспалительные и противоаллергические средства.
- Снижение иммунитета. Донорские клетки красного костного мозга не могут прижиться и начать функционировать сиюминутно. Для этого нужно время, обычно 2 – 4 недели. В течение этого срока у больного сильно снижен иммунитет. Его помещают в стационар, полностью ограждают от контакта с инфекциями, назначают антибиотики и противогрибковые средства. Этот период является одним из самых сложных. Сильно повышается температура тела, в организме могут активироваться хронические инфекции.
- Приживление донорских стволовых клеток. Самочувствие пациента начинает улучшаться.
- Восстановление. В течение нескольких месяцев или лет функция красного костного мозга продолжает восстанавливаться. Постепенно пациент выздоравливает, восстанавливается его работоспособность. Но он все еще должен находиться под наблюдением врача. Иногда новый иммунитет не может справиться с некоторыми инфекциями, в этом случае примерно через год после пересадки костного мозга делают прививки.
Проводится в случаи отсутствия эффекта от химиотерапии и при увеличенной селезенке после приема медикаментов (цитостатиков). Метод выбора при развитии локальной опухоли (гранулоцитарная саркома).
В какой фазе заболевания применяется лучевая терапия?
Лучевая терапия используется в развернутой стадии хронического миелолейкоза, которая характеризуется признаками:
- Значительное разрастание опухолевой ткани в красном костном мозге.
- Рост опухолевых клеток в трубчатых костях 2.
- Сильное увеличение печени и селезенки.
Применяется гамма-терапия – облучение области селезенки гамма-лучами. Основная задача – уничтожить или прекратить рост злокачественных опухолевых клеток. Лучевую дозу и режим облучения определяет лечащий врач.
| К длинным трубчатым костям относят кости плеча, предплечья, пальцев, голени, бедра. В детстве эти кости целиком заполнены красным костным мозгом. У взрослого человека красный костный мозг сохраняется только в головках костей, а в теле кости он замещается на желтый костный мозг (жир). При хроническом миелоидном лейкозе желтый костный мозг может быть вытеснен опухолевой тканью. |
Удаление селезенки используется редко по ограниченным показаниям (инфаркт селезенки, тромбоцитопения, выраженный дискомфорт в животе).
Операцию обычно проводят в терминальную фазу заболевания. Вместе с селезенкой из организма удаляют большое количество опухолевых клеток, тем самым облегчая течение заболевания. После операции обычно увеличивается эффективность медикаментозной терапии.
Каковы основные показания к операции?
- Разрыв селезенки.
- Угроза разрыва селезенки.
- Значительное увеличение органа в размерах, что приводит к сильному дискомфорту.
При высоких уровнях лейкоцитов (500,0 · 10 9 /л и выше), могут использовать лейкаферез для предотвращения осложнений (отек сетчатки, приапизм, микротромбозы ).
При развитии бластного криза, лечение будет таким же, как при острых лейкозах (см. острый лимфолейкоз).
Лейкоцитаферез – лечебная процедура, напоминающая плазмаферез (очищение крови). У пациента берут определенное количество крови и пропускают через центрифугу, в которой она очищается от опухолевых клеток.
В какой фазе заболевания проводят лейкоцитаферез?
Так же, как и лучевую терапию, лейкоцитаферез проводят во время развернутой стадии миелолейкоза. Нередко его применяют в тех случаях, когда отсутствует эффект от применения лекарственных средств. Иногда лейкоцитаферез дополняет медикаментозную терапию.
Читайте также: