Маркеры рака шейки матки p16ink4a

Риск рака шейки матки является вторым по частоте онкологическим заболеванием, угрожающим жизни женщины. Несмотря на достижения в диагностике, лечении и исследованиях этого заболевания, смертность в развивающихся странах продолжает оставаться высокой. Так, в 2008 году было зарегистрировано 529000 новых случаев и 275000 смертей от рака шейки матки. Прошло более 40 лет со времени открытия возбудителя этого заболевания. В 1970-х Harold zur Hausen предположил наличие корреляции между инфицированностью ВПЧ и развитием неопластических процессов в шейке матки. Вирус обладает высоким сродством к сквамозным эпителиальным клеткам и легко инфицирует их. Поражение вирусом, тем не менее, зависит от взаимодействия нескольких факторов: онкогенов, генов восстановления ДНК и генов-супрессоров опухоли [5].
Важное значение в профилактике рака шейки матки имеют диагностические программы обследования женщин. Заболеваемость раком шейки матки в мире колеблется в значительных пределах, и зависит во многом от экономической составляющей. Так, в США заболеваемость раком шейки невысока, в 2016 году 12990 женщин заболели и 4120 умерли от этого заболевания. Анализ показывает, что причиной этого является применение современных диагностических технологий, так женщинам в возрасте 21–29 лет раз в 3 года проводится анализ, предусматривающий гистологическую оценку методом жидкостной цитологии [6].
Применение Рар теста в гинекологической практике явилось фактором, поднявшим диагностику рака шейки матки на новый уровень. Вместе с тем, заболеваемость и смертность от рака шейки матки остается высокой, несмотря на контроль с помощью Рар теста, что указывает на ограниченные возможности этого диагностического метода. Частыми причинами ложных результатов анализа являются гиперплазия клеток, воспалительная атипия и сквамозная метаплазия. Наличие этих факторов приводит к необходимости повторных исследований или проведению более травматичных процедур [1]. Рак шейки матки вызывается 14 типами вируса папилломы человека (ВПЧ), а типы 16 и 18 являются причиной заболевания в 70 % случаев. Известно, что ВПЧ инфекция определяет развитие рака шейки матки, однако иммунная система в большинстве случаев обеспечивает элиминацию вируса в течение одного или двух лет [3, 4].
Современные программы скрининга основаны на жидкостной цитологии, включающей забор пробы маленькой пластиковой щеткой в питательную жидкую среду с целью дальнейшего приготовления мазков. Цервикальная цитология зависит от получения хороших образцов и экспертной интерпретации микроскопической картины, что практически не выполнимо без соответствующего оборудования и подготовки.
Весьма перспективным тестом диагностики дисплазии и рака шейки матки может быть иммуноцитохимическое определение повышенной экспрессии гена-супрессора p16INK4a. В норме, кодируемый этим геном, белок p16INK4a блокирует вызываемую фактором роста стимуляцию деления клетки за счет угнетения циклин- зависимой киназы, что приводит к нарушению фосфорилирования белка ретинобластомы (БРБ). В этих условиях БРБ связывается с фактором транскрипции Е2F, блокирует его митотическую активность и останавливает деление клетки. Однако, при ВПЧ инфекции, встроенная в геном хозяина ДНК вируса начинает синтезировать два онкогена, Е6 и Е7. Онкоген Е7 связывается с белком ретинобластомы, препятствуя ингибированию E2F. Это приводит к неконтролируемому делению клетки и повышенному синтезу белка p16INK4a, что может быть зафиксировано с помощью цитоиммунохимическиой реакции [2]. Определение онкобелка p16INK4a позволяет вявить ранние стадии возникновения предрака и рака шейки матки. По эффективности этот тест является более релевантным, чем генотипирование ВПЧ или кольпоскопия.
Материалы и методы исследования
В сети медицинских клиник MedSwiss программой ДМС предусмотрено скрининговое исследование ранних пролиферативных процессов шейки матки. Эта программа включает:
1. Анализ данных жидкостной цитологии с поверхности шейки матки в режиме реального времени с применением компьютеризированной программы BD Focal Point и определение онкопротеина p16INK4a
2. ПЦР-тест на выявление основных 14 типов ВПЧ при первичном обследовании пациентки
3. Расширенное кольпоскопическое исследование на приеме у гинеколога.
В рамках этой программы при первичном осмотре у гинеколога пациенткам проводится Рар-тест в современной модификации, основанной на жидкостной цитологии. С этой целью одновременно из трех зон (поверхность шейки матки, из цервикального канала и зоны трансформации) берется биологический материал и помещается в виалу. Клеточный состав пробы обогащается, окрашивается на 2 стеклах и анализируется (на первом этапе одна проба) с помощью линейки приборов BD PreMate, BD SurePath, BD Focal Point.
Результаты исследования и их обсуждение
Результаты исследования, степень дисплазии клеток, представляются по Цитологической классификации ВОЗ (CIN I, CIN II и CIN III) и Цитологической классификации Бетесда (ASCUS, LSIL и HSIL). В случае обнаружения патологических изменений проводится исследование второй пробы на экспрессию белка p16INK4a. Одновременно всем пациенткам проводится анализ на выявление ВПЧ методом ПЦР диагностики (14 типов вируса). Неотъемлемым компонентом первичного обследования гинеколога является расширенная кольпоскопия.
Важным компонентом алгоритма является интегрированная оценка анализа жидкостной цитологии, наличия ВПЧ в анализе ПЦР и данных кольпоскопии. Действительно, часто интегративный анализ всех трех компонентов- положительная ПЦР, результаты жидкостной цитологии и кольпоскопии является определяющими при дальнейшем обследовании и ведении таких пациенток. Так, при положительном анализе ПЦР диагностики на наличие вируса высокого онкогенного риска (типы 31, 33,35, 39,45,51, 52, 56, 58, 59, 66, 68 и особенно 16 и 18) и характерных изменениях данных жидкостной цитологии возможно отсутствие визуальных изменений при кольпокопии.
В зависимости от инфицированности ВПЧ, результатов цитологического исследования и наличия белка p16INK4a нами разработаны были дорожные карты ведения пациенток, предусматривающие схемы от наблюдения до медикаментозного лечения и хирургической деструкции шейки матки [4].
Заключение
Таким образом, применение теста на белок p16INK4a позволяет повысить и специфичность, и чувствительность диагностики при дисплазии шейки матки, обеспечивая адекватное ведение пациенток с этой патологией [7].
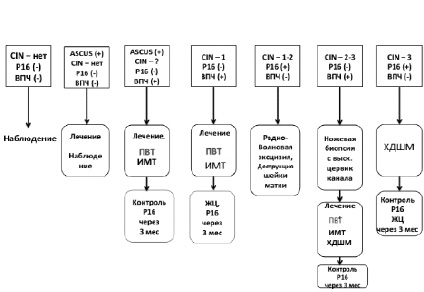
Тактика ведения пациенток с патологией шейки матки. Лечение – медикаментозные методы лечения. Сокращения: ИМТ – иммуномодулирующая терапия; ПВТ – противовирусная терапия; ХДШМ – хирургическая деструкция шейки матки; ЖЦ – жидкостная цитология
Иммуноцитохимическое исследование, позволяющее выявить экспрессию белка р16 (p16INK4a) на поверхности эпителиальных клеток. Белок р16 является биологическим маркером начала канцерогенеза – повышение его экспрессии наблюдается при предраковых изменениях и может рассматриваться как непрямой маркер активной онкогенной экспрессии ВПЧ высокого онкологического риска (выявляется при переходе ВПЧ из эписомальной формы в интегрированную). Определение экспрессии белка р16 позволяет с высокой точностью обнаружить риск развития рака шейки матки, своевременно поставить диагноз и назначить лечение. Определение уровня экспрессии позволяет выявить степень нарушения пролиферации, сопутствующей опухолевому росту, способность опухоли к инвазии и метастазированию.
Белок p16INK4a; иммуноцитохимическое исследование.
Синонимы английские
Оncoprotein p16INK4ain; immunocytochemical study.
Иммуноцитохимический метод + жидкостная цитология.
Какой биоматериал можно использовать для исследования?
Аспират из полости матки.
Общая информация об исследовании
Одной из самых современных методик ранней диагностики предраковых состояний является иммуноцитохимическое исследование - определение онкопротеина р16ink4a для оценки потенциала дисплазии эпителия.
Было доказано, что экспрессия онкопротеина р16ink4a связана с низкой, умеренной и тяжелой дисплазией (по цитологической классификации ВОЗ (CIN I, CIN II и CIN III) и цитологической классификации Бетесда (ASCUS, LSIL и HSIL), причем экспрессия онкопротеина р16ink4a не встречалась в плоском эпителии без признаков дисплазии. В норме кодируемый геном-супрессором белок p16INK4a блокирует вызываемую фактором роста стимуляцию деления клетки за счет угнетения циклин-зависимой киназы, что приводит к нарушению фосфорилирования белка ретинобластомы (БРБ). В этих условиях БРБ связывается с фактором транскрипции Е2F, блокирует его митотическую активность и останавливает деление клетки. Однако при ВПЧ инфекции встроенная в геном хозяина ДНК вируса начинает синтезировать два онкогена, Е6 и Е7. Онкоген Е7 связывается с белком ретинобластомы, препятствуя ингибированию E2F. Это приводит к неконтролируемому делению клетки и повышенному синтезу белка p16INK4a, что может быть зафиксировано с помощью цитоиммунохимической реакции.
В то же время, хотя отмечается четкая корреляция обнаружения ДНК вируса папилломы человека с дисплазиями, имеется также большое количество ПЦР-позитивных по HPV случаев (с эписомальной локализацией HPV), в которых при последующем гистологическом исследовании отсутствует предрак и рак. Это подтверждается негативной иммуноцитохимической реакцией на р16ink4a в диспластических клетках.
В данном исследовании применяется современная технология приготовления цитопрепаратов - жидкостная цитология. Важная особенность метода, повышающая качество исследования: исследуемый материал берется в специальный стабилизирующий раствор, который обеспечивает его сохранность без разрушения и потери клеток. При этом весь клеточный материал сохраняет без изменения свои морфологические и иммуноцитохимические свойства. В последние пять лет в разных странах проводилось много исследований, в которых сравнивалась эффективность традиционной техники и жидкостной цитологии с использованием для подтверждения диагнозов гистологической экспертизы как "золотого стандарта" и оценки цитопрепаратов согласно классификации TBS (The Bethesda System). Метод жидкостной цитологии признан надежным лабораторным тестом, который снижает количество ложноотрицательных результатов, неудовлетворительных для анализа препаратов и время, необходимое цитологу для оценки препарата.
Материал для цитологического исследования получают с поверхности слизистой оболочки. Слизь, присутствующая во взятом материале, мешает перенести на мазок клетки, также материал невозможно равномерно перемешать. При переносе материала на стекло традиционным способом клетки области шейки матки могут не попасть в препарат, подсушивание и потеря прилипших к инструменту клеток значительно снижает диагностическую информативность микропрепаратов. Метод жидкостной цитологии позволяет исключить эти негативные факторы. Преимущество жидкостной цитологии состоит в том, что при взятии материала можно получить до 5-6 "серийных" (то есть одинаковых по клеточному составу) мазков. Это дает возможность применения дополнительных методов исследований.
Данное обследование может быть применено в диагностике поражения шейки матки, где это является наиболее частым и востребованным методом исследования. Оно может позволить:
- достоверно оценивать потенциал дисплазии в отношении развития рака шейки матки и, соответственно, выбирать более консервативную или более агрессивную тактику лечения;
- уточнять заключения цитолога - дополнительному исследованию на онкопротеина р16ink4a подлежат все случаи атипической цитологии (кроме инвазивного рака шейки матки), неопределенные цитологические заключения (атипические клетки плоского эпителия неясного значения-ASCUS) и все изменения железистого эпителия;
- разрешать спорные вопросы при выявлении гинекологом высокоаномальной кольпоскопической картины, не сопровождающейся изменениями в цитологическом мазке;
- во многих случаях обоснованно отказаться от биопсии - у большинства пациенток пожилого возраста с цитологической картиной дисплазии на фоне атрофического цервицита обоснованно избирать выжидательную тактику, отказавшись не только от лечения, но и от биопсий, и увеличить интервалы между диспансерными осмотрами; у небольшого числа р16ink4a-позитивных пациенток этой возрастной группы, напротив, обоснованно избрать более активную тактику;
- определять индивидуальную тактику в отношении пациенток, инфицированных штаммами вируса папилломы человека высокого онкогенного потенциала, если у них нет цитологических и кольпоскопических изменений; у женщин с позитивной ПЦР по HPV выделить группу пациенток, у которых уже инициирован канцерогенез в эпителии шейке матки, и направить на них необходимое лечебное воздействие; соответственно, в более многочисленной группе р16ink4a-негативных женщин необходимо продолжить мониторинг;
- усовершенствовать мониторинг пациенток, прошедших органосохраняющее лечение по поводу "тяжелой дисплазии" или "рака in situ", добавив определение онкопротеина р16ink4a к рутинному цитологическому исследованию, это позволит у пациенток наибольшего риска повысить чувствительность цитологического исследования и тестировать персистирующую папиллома-вирусную инфекцию до появления морфологических изменений.
Для чего используется исследование?
- Обследование женщин независимо от наличия или отсутствия патологии шейки матки;
- обследование женщин и мужчин при подозрении на рак шейки матки, рак толстой кишки, рак молочной железы, рак мочевого пузыря, рак предстательной железы;
- наличие патологии шейки матки;
- контроль эффективности лечения патологии шейки матки
Когда назначается исследование?
- При наличии клинико-анамнестических признаков (эрозия, лабораторно подтвержденное инфицирование ВПЧ), позволяющих заподозрить онкологический процесс в шеечной части матки, мочевого пузыря, прямой кишке;
- все случаи атипической цитологии (кроме инвазивного рака шейки матки), неопределенные цитологические заключения (атипические клетки плоского эпителия неясного значения) и все изменения железистого эпителия;
- при выявлении высокоаномальной кольпоскопической картины, не сопровождающейся изменениями в цитологическом мазке;
- при наблюдении за пациентками, прошедшими органосохраняющее лечение по поводу "тяжелой дисплазии" или "рака in situ" в целях повышения чувствительности цитологического исследования.
Что означают результаты?
Референсные значения: отсутствие экспрессии белка р16 в клетках эпителия (негативная реакция).
Заключение включает в себя два подраздела: цитологическое описание и иммуноцитохимическое исследование на р16ink4a.
Цитологическое заключение интерпретируется в зависимости от выявления онкомаркера р16ink4a. В особенности это относится к дисплазиям шейки матки.
Белок р16(INK4a) осуществляет контроль разобщения комплекса E2F-Rb, препятствуя пролиферации клетки. В норме по механизму обратной связи синтез р16 сдерживается, таким образом, концентрация данного белка в нормальной клетке чрезвычайно мала, что проявляется негативной иммуноцитохимической реакцией.
Достоверно показано, что экспрессия р16 связана с низкой, умеренной и тяжелой дисплазией, причем экспрессия р16 практически не встречается в плоском эпителии без признаков дисплазии (0-2% случаев).
Экспрессия белка р16 нарастает с увеличением степени дисплазии и выявляется:
- в 16% случаев при CIN I – плоскоклеточном интраэпителиальном поражении низкой степени тяжести – воспалительные изменения, характерные для инфекции ВПЧ, слабая дисплазия эпителия;
- в 64% при CIN II - плоскоклеточное интраэпителиальное поражение высокой степени тяжести – умеренная дисплазия эпителия;
- в 90% случаев при CIN III - тяжелая дисплазия эпителия и внутриэпителиальный рак шейки матки;
- в 100% при плоскоклеточном раке шейки матки.
Кто назначает исследование?
120 Определение предиктора изменений эндометрия PTEN, Ki67
56 Human Papillomavirus высокого канцерогенного риска (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типы), ДНК генотипирование [реал-тайм ПЦР]
Где проводится: Тонус
Срок выполнения: 7-10 рабочих дней
- Описание
- Подготовка
- Показания
- Интерпретация результатов
Жидкостная цитология шейки матки является новой стандартизированной технологией приготовления цитологического препарата. На сегодняшний день данный метод является самым информативным в диагностике интраэпителиальных неоплазий. Благодаря новой технологии количество ложных результатов значительно ниже, чем при использовании классических методов цитологического исследования мазка. Это достигается использованием специального стабилизирующего раствора и инструментов для взятия мазка – щеточки cervex-brush.
Жидкостная цитология шейки матки в современной медицине является очень важным исследованием. В настоящее время рак шейки матки занимает вторую позицию по распространенности рака среди женщин и согласно ВОЗ смертность от данной патологии быстро увеличивается.
Для того, чтобы рак шейки матки развился требуется длительное время. От появления интраэпителиальных поражений низкой и высокой степени до возникновения инвазивного рака должно пройти не менее 10 лет. Из этого можно сделать вывод, что у женщины достаточно времени, чтобы диагностировать начальные изменения и начать профилактику. Чаще в клиниках используются классические цитологические исследования мазка – окрашивание биоматериала по Папаниколау и Рар-тест. Эти цитологические методы часто дают ложноотрицательные результаты – до 40 процентов. Это обусловлено неадекватно приготовленным препаратом, нарушениями процедур взятия материала. При использовании жидкостной цитологии шейки матки частота ошибок значительно уменьшается.
Преимущества жидкостной цитологии шейки матки:
- Отличное качество материала для анализа на цитологию
- Длительное хранение биоматериала в специальном растворе, что дает возможность его хранить или транспортировать (без разрушения и потери клеток).
- Приготовление препарата происходит быстро
- Из одного материал можно приготовить несколько препаратов для анализа на цитологию
- Методики окрашивания препарата стандартизированы
Таким образом, жидкостной цитологии шейки матки качество цитологического исследования мазка значительно повышается.
Анализ на цитологическое исследование мазка рекомендуется сдавать в качестве скрининга, даже когда симптомов нет. Сдать анализ на цитологию в первый раз следует через 3 года после начала половой жизни, либо при достижении 21 года. Скрининг необходимо проходить ежегодно. Если после 30 лет у женщины три последовательных отрицательных результата анализа на цитологию, то скрининг можно проходить раз в два-три года, но при наличии факторов риска (иммунодефицит, инфицирование ВПЧ) у женщины, ей необходимо анализ на цитологию ежегодно. Также скрининг следует проводить женщинам, у которых была удалена матка, но сохранена шейка матки. Ранняя диагностика при помощи жидкостной цитологии шейки матки позволяет вовремя выявить патологию и предотвратить развитие злокачественной опухоли, путем своевременного адекватного лечения.
Доказано, что ВПЧ (вирус папилломы человека) является фактором, который индуцирует развитие рака шейки матки. Значительно повышает эффективность скрининга определение клеточного протеин p16INK4a. Его экспрессия увеличивается при репликации онкобелков E6 и E7, которые реплицируются при интеграции вируса папилломы человека в генетический материал клеток эпителия шейки матки. В норме данный белок вырабатывает в очень малых количествах, которые нельзя обнаружить. При развитии канцерогенеза эпителия шейки матки это протеин синтезируются в больших количествах и дает возможность оценить дисплазию. Выявление p16INK4a является отличным дополнением к жидкостной цитологии шейки матки, так как совместное их применение позволяет выявить патологию на ранних стадиях развития (особенно CIN II, CIN III и начальные формы рака). Выявление заболевания на данных стадиях развития позволяет излечить пациентку практически в 100%.
Сдать анализ на цитологию при профилактическом скрининге следует после пятого дня менструального цикла, а также спустя двое суток после полового контакта. Не рекомендуется проводить жидкостную цитологию шейки матки на фоне применение вагинальных лекарственных препаратов, лубрикантов, спермицидов, применения спринцеваний влагалища, а также во время месячных или при наличии генитальной инфекции.
Вышеперечисленные факторы не должны учитывать, если на шейке матки патология обнаруживается визуально.
Сдать анализ на цитологию следует для профилактического скрининга, данное исследование рекомендуется женщинам в возрасте от 21 до 65 лет.
- Оценка адекватности образца:
- Адекватный (при этом описывается клеточный состав)
- Недостаточно адекватный (образец недостаточно адекватный по количественному и качественному составу, указывается причина (при этом описывается клеточный состав)
- Неудовлетворительный образец для оценки (клеточного состава недостаточно для уверенного заключения)
Описывает клеточный состав, клетки эпителия, отдельно описывается зона трансформации (метаплазия эпителия, цилиндрический эпителий). При наличии описываются интраэпителиальные изменения, которые также указываются в пункте №4.
- Доброкачественные изменения:
- Дегенеративные
- Репаративные
- Дискератоз, гиперкератоз, паракератоз
- Бактериальный вагиноз
- Увеличения ядер плоского, метаплазированного эпителия
- Лучевые изменения
При отсутствии доброкачественных изменений отмечается, что они не обнаружены.
- Патологические изменения в цитологическом исследовании мазка, согласно классификации, Bethesda:
- ASC-US атипия плоского эпителия неясного значения;
- ASC-H атипия плоского эпителия, не исключающая HSIL;
- LSIL плоскоклеточное интраэпителиальное поражение низкой степени;
- HSIL плоскоклеточное интраэпителиальное поражение высокой степени;
- CIS карцинома in situ;
- AG-US атипия железистого эпителия неясного значения;
- AIS- эндоцервикальная карцинома in situ.
При отсутствии патологических изменений отмечается, что они не обнаружены.
Данный пункт может содержать информацию об обнаруженных грибках рода Кандида, бактериях, трихомонаде вагиналис и другой флоре.
Тест на p16INK4a оценивается совместно с жидкостной цитологией шейки матки. Положительный результат анализа на белок p16INK4a означает, что без соответствующего лечения данное состояние приведет к раку шейки матки.
Описание
Иммуногистохимическое исследование маркёра ранней диагностики дисплазии с высокой степенью озлокачествления (скрининг рака шейки матки) p-16NK-4a + Ki-67 — исследование биоптата ткани, меченого антителами, под микроскопом для выявления маркёров рака шейки матки в самом начале развития болезни.
ИГХ-исследования проводят после выполнения гистологического исследования.
ИГХ-исследования выполняют для:
- проведения дифференциальной диагностики злокачественных новообразований;
- определения гистогенеза опухоли;
- определения темпа роста и прогноза опухоли;
- определения возможности применения гормональных препаратов в лечении опухоли;
- выявления ответа на таргетную терапию.
Рак шейки матки — группа новообразований, растущих из эпителия экзоцервикса и слизистой шеечного канала. Имеет злокачественную природу.
Причинызлокачественной трансформации эпителия шейки матки:
- ранняя активная половая жизнь;
- частая смена половых партнеров;
- применение гормонсодержащих контрацептивных препаратов;
- инфекции, передающиеся половым путем;
- носительство вирусов папилломы человека (ВПЧ);
- частые роды;
- курение;
- нарушение гормонального фона, провоцирующее структурные перестройки шейки матки (псевдоэрозия).
В большинстве случаев рак шейки матки развивается на фоне дисплазий шейки матки — CIN, которая обусловлена инфицированием вирусом папилломы человека высокоонкогенного типа. Дисплазии никак себя не проявляют или могут маскироваться иными заболеваниями. В большинстве случаев они не сопровождаются симптоматикой и могут быть выявлены случайно.
Прогноз выживаемости и выбор терапии зависит от стадии, на которой болезнь была обнаружена.
Своевременное выявление изменений, предшествующих раковым, позволяет провести радикальное лечение.
Существует закономерность разрастания рака шейки матки и активность белка p-16INK-4a.
p-16INK-4a
В норме протеин p-16ink-4a в клетках эпителия продуцируется в незначительных количествах и при анализе не определяется.
При заражении ВПЧ, вирус встраивается в геном клетки-хозяина и изменяет процессы ее деления и синтеза веществ. В результате клетки эпителия находятся в состоянии постоянной гиперэкспрессии p-16ink-4a. Его обнаружение свидетельствует о неконтролируемой пролиферации эпителиальных клеток и может считаться началом онкологического процесса. Белок p-16INK-4a является достоверным и надежным маркёром оценки риска прогрессирования CIN и развития рака шейки матки. Его определение позволяет выявить и пролечить женщин с предраковой патологией, что снижает заболеваемость.
После проведённого лечения анализ имеет прогностическое значение и определяет вероятность возникновения рецидива.
Ki-67
Ki-67 — это маркёр пролиферативной активности опухоли. Он показывает, насколько агрессивен рост опухоли.
При проведении гистологического исследования в сторонней лаборатории, необходимо обязательно предоставить протокол гистологического исследования.
Интерпретация результатов
Ответ выдаётся в виде описания микропрепарата, применяемых красителей. Он содержит заключение, в котором указано количество белка p16INK4a и индекс белка ki-67. Заключение может интерпретировать только врач, направивший на проведение исследования.
Определение онкомаркера р16ink4a при наличии плоскоклеточных интраэпителиальных поражений и раке шейки матки
Троханова Ольга Валентиновна,
доктор медицинских наук, профессор кафедры акушерства и гинекологии,
Чижова Юлия Анатольевна,
ассистент кафедры акушерства и гинекологии,
Сутугина Ольга Николаевна,
ассистент кафедры акушерства и гинекологии,
Григорьева Мария Алексеевна,
ассистент кафедры акушерства и гинекологии.
Ярославский государственный медицинский университет Министерства здравоохранения Российской Федерации.
Determination of tumor marker р16ink4a the presence of squamous intraepithelian lesions and cervical cancer
O.V. Trokhanova, Y.A. Chijova, O.N. Sutugina, M.A. Grigorieva .
Природа рака шейки матки с его обычно медленным прогрессированием от ранних предраковых заболеваний до инвазивного рака даёт обоснованную возможность проведения скрининга, раннего выявления заболевания и его лечения. Предшественниками плоскоклеточного цервикального рака являются цервикальные интраэпителиальные неоплазии (CIN) [4, 6]. Подтверждение этиологической роли ВПЧ в развитии неоплазий и рака шейки матки привело к тому, что тестирование на ВПЧ стало рассматриваться как важнейший элемент скрининга этих заболеваний. На сегодняшний день генотип ВПЧ остается лучшим предиктором риска прогрессирования заболевания, и наибольший удельный вес прогрессирования наблюдается при инфицировании ВПЧ 16 и 18 типами. Роль измерения вирусной нагрузки для любых генотипов ВПЧ до сих пор не является клинически доказано полезной [4, 6, 8, 12]. Несмотря на огромное разнообразие клинических форм проявления папилломавирусной инфекции, различают два основных варианта, или две стадии, ее развития:
I стадия - репродуктивной инфекции, при которой ДНК ВПЧ находится в инфицированной клетке в свободном (эписомальном) состоянии; II стадия - интегративной инфекции, при которой ДНК вируса встраивается в геном инфицированных клеток. I стадия является обратимой. При ее благополучном исходе у многих ВПЧ-инфицированных наступает ремиссия [4, 6, 9, 11, 13]. В отличие от нее, при второй стадии, в результате включения вирусной ДНК в геном клетки-хозяина происходят глобальные изменения клеточного метаболизма, основным из которых является частичная потеря вирусного генетического материала, но с обязательным сохранением онкогенов Е6 и Е7 и их последующей гиперэкспрессией. Повышенная продукция вирусных онкогенов Е6 и Е7 через модуляцию активности широкого спектра внутриклеточных сигнальных белков приводит к активации патологической пролиферации и, соответственно, снижению апоптоза, усилению клеточного деления, неоангиогенеза и инвазии, т.е. появлению основных биологических событий, опосредующих канцерогенез. Плюс к этому, индуцируются процессы хромосомной нестабильности (нарушения геномной целостности). В ДНК хозяина возникают генетические мутации и эпигенетические модификации, результатом которых является усиленная опухолевая трансформация вирус-инфицированных клеток. С течением времени в результате последовательной селекции клеточных клонов, содержащих интегрированную вирусную ДНК и обладающих повышенной малигнизирующей активностью, формируется злокачественная опухоль. Таким образом, экспрессия онкогенов Е6 и Е7 вирус-инфицированными эпителиальными клетками шейки матки - это фактически инициация их опухолевой трансформации [3, 4, 6]. С момента возникновения интегрированной формы ВПЧ инфекции начинается синтез белка р16ink4a. Нормальный клеточный цикл состоит из G1, S, G2 и M фаз. E2F – киназа обеспечивает прохождение клетки из G1 в S фазу клеточного цикла. В норме она неактивна и находится в связанном состоянии с белком супрессором Rb (продукт гена ретинобластомы). Белок р16 (INK4a) осуществляет контроль разобщения комплекса E2F-Rb, не допуская безудержной пролиферации клетки. Синтез р16ink4a в норме по механизму обратной связи сдерживается и концентрация данного белка в нормальной клетке чрезвычайно мала, что проявляется негативной иммуноцитохимической реакцией. Белок Е7 вируса папилломы человека высокого онкогенного риска при своем взаимодействии с продуктом гена ретинобластомы приводит к разобщению комплекса E2F-Rb. E2F находится постоянно в активном состоянии, стимулируя пролиферацию клетки. р16ink4a пытается сдержать пролиферацию клетки, что приводит к бесконтрольному его синтезу. Уровень р16 в клетке повышается, что иммуноцитохимически проявляется позитивной реакцией и является биомаркером инициации канцерогенеза в эпителии шейки матки [3, 4, 6].
Учитывая появление сигнала р16ink4a при интегрции ВПЧ в клетку хозяина и возможное прогрессирование течения заболевания при этом, было решено выявить возможные взаимосвязи между изменениями показателей электропроводности и появлением данного онкомаркера, а также установить целесообразность его определения при различных степенях цервикальных интраэпителиальных неоплазий, преинвазивном и микроинвазивном раке шейки матки.
II . Материалы и методы исследования
Материалом для исследования послужили результаты комплексного обследования шейки матки у 106 женщин в возрасте от 18 до 60 лет, которые составили 4 клинические группы:
1 группа - 46 пациенток с диагностированной низкой степенью плоскоклеточных интраэпителиальных поражений (LSIL).
2 группа - 33 пациентки с высокой степенью плоскоклеточных интраэпителиальных поражений (HSIL).
3 группа – 11 пациенток с преинвазивным раком (0 ст.).
4 группа – 16 пациенток с микроинвазивным раком (IA ст.).
В каждой группе выделены подгруппы с учетом возраста пациенток (до 30 лет и после 30 лет).
Для четкого формирования групп и выявления патологии шейки матки использовались следующие методы диагностики:
· Осмотр влагалища и шейки матки в зеркалах.
· Бактериоскопическое исследование мазков на флору с окрашиванием по Грамму.
· Бактериологический метод исследования с использованием селективных сред.
· Метод жидкостной онкоцитологии.
· Молекулярно-биологический метод (ПЦР-диагностика).
· Иммуноцитохимическое определение онкомаркера р16ink4a.
· Электроимпедансная томография шейки матки при помощи компактного гинекологического томографа (ГИТ) [1, 2, 5, 7, 10, 14]. Метод позволил проводить визуальную оценку влагалищной части шейки матки, а также оценивать показатели электропроводности шейки на трех уровнях сканирования (2, 5 и 8 мм).
III. Результаты исследования
При проведении комплексного обследования у 28 женщин до 30 лет и 18 женщин после 30 лет (всего 46 человек), составивших первую клиническую группу с цервикальными интраэпителиальными неоплазиями низкой степени выявлено:
· Отсутствие жалоб со стороны женских половых органов.
· Наличие отягощенного гинекологического анамнеза: единичные эпизоды специфических и неспецифических цервицитов и вагинитов, ИППП у 7 пациенток, выявление ВПЧ 16 типа у 23 женщин, ВПЧ 18 типа – у 6 пациенток, ВПЧ 16 и 18 типов – у 4 женщин. ВПЧ негативные тесты – у 6 женщин и 7 женщин ранее не обследовались.
· Отсутствие визуальных изменений во влагалище и шейке матки при осмотре в зеркалах у 24 пациенток, у 12 пациенток визуальные признаки эктопии цилиндрического эпителия.
· Отсутствие патологии при бимануальном исследовании.
· П ри бактериоскопическом исследовании отделяемого из влагалища – лейкоцитов до 10-15 в поле зрения, палочковая флора, единичные кокки .
· Отсутствие этиологически значимой флоры при проведении бактериологического исследования отделяемого из цервикального канала.
· Отсутствие ИППП на момент обследования.
· Положительный ВПЧ тест в 43 случаях наблюдения: ВПЧ 16 типа обнаружен – у 33 женщин, ВПЧ 18 типа – у 6 пациенток, ВПЧ 16 и 18 типов – у 4 женщин. ВПЧ негативные тесты – у 3 женщин (возможно, инфицированы другими онкогенными типами, на которые обследование не проводилось).
· При цитологическом исследовании: во всех случаях низкая степень плоскоклеточного интраэпителиального поражения.
· При проведении расширенной кольпоскопия – признаки плоскоклеточных интраэпителиальных поражений легкой степени во всех случаях наблюдений ( тонкий ацето-белый эпителий, нежная мозаика и пунктуация на пробе с 3% раствором уксусной кислоты, йоднегативные зоны при пробе Шиллера) .
· При выполнении прицельной биопсии методом радиоволновой хирургии - признаки CIN 1 и койлоцитоз у 18 женщин старше 30 лет.
При проведении комплексного обследования у 15 женщин до 30 лет и 18 женщин после 30 лет (всего 33 человека), составивших вторую клиническую группу с цервикальными интраэпителиальными неоплазиями высокой степени выявлено:
· Отсутствие жалоб со стороны женских половых органов.
· Наличие отягощенного гинекологического анамнеза: единичные эпизоды специфических и неспецифических цервицитов и вагинитов, ИППП у 6 пациенток, выявление ВПЧ 16 типа у 24 женщин, ВПЧ 18 типа – у 2 пациенток, ВПЧ 16 и 18 типов – у 2 женщин. ВПЧ негативные тесты – у 2 женщин и 3 женщин ранее не обследовались.
· Отсутствие визуальных изменений во влагалище и шейке матки при осмотре в зеркалах у 22 пациенток, у 11 пациенток визуальные признаки эктопия цилиндрического эпителия.
· Отсутствие патологии при бимануальном исследовании.
· П ри бактериоскопическом исследовании отделяемого из влагалища - лейкоцитов до 10-15 в поле зрения, палочковая флора, единичные кокки .
· Отсутствие этиологически значимой флоры при проведении бактериологического исследования отделяемого из цервикального канала.
· Отсутствие ИППП на момент обследования ( Chlamydia trachomatis, Mycoplasma genitalium, Neisseria gonorrhoeae, Trichomonas vaginalis) .
· Положительный ВПЧ тест: ВПЧ 16 типа обнаружен в 27 случаях, ВПЧ 16 и 18 типов – в 2 случаях, ВПЧ 18 типа – в 2 случаях, в 2 случаях ВПЧ-негативные тесты (возможно, инфицированы другими онкогенными типами на которые обследование не проводилось).
· При цитологическом исследовании: высокая степень плоскоклеточного интраэпителиального поражения (LSIL).
· При выполнении расширенной кольпоскопии – признаки плоскоклеточных интраэпителиальных поражений высокой степени ( плотный ацето-белый эпителий, грубая мозаика и пунктация при пробе с уксусной кислотой; резкие контуры поражения, йоднегативные зоны при пробе Шиллера) .
· При проведении прицельной биопсии у 24 женщин или эксцизии шейки матки у 9 женщин (с неадекватной кольпоскопией) методом радиоволновой хирургии - признаки СIN II и CIN III. Пациентки без СIN и с СIN I в данную группу не включались.
При проведении комплексного обследования у 3 женщин до 30 лет и 24 женщин после 30 лет (всего 27 человек), составивших третью и четвертую клинические группы с перинвазивным и микроинвазивным раком шейки матки выявлено:
· Жалобы на контактные кровянистые выделения из половых путей у 5 пациенток, диспареуния у 3 женщин, болевой синдром у 3 женщин, сочетание нескольких жалоб у 4 пациенток. В большинстве случаев наблюдения пациентки жалоб не предъявляли.
· Отягощенный гинекологический анамнез: ВПЧ 16 типа персистировал в 12 случаях, ВПЧ 16 и 18 типов – в 4 случаях, ВПЧ 18 типа – в 1 случае. 10 женщин не были обследованы на ВПЧ на момент первичного обращения.
· Отсутствие визуальных изменений во влагалище и шейке матки при осмотре в зеркалах у 9 пациенток, у 11 пациенток визуальные признаки эктопии цилиндрического эпителия, у 7 женщин выраженный сосудистый рисунок слизистой экзоцервикса.
· Отсутствие патологии при бимануальном исследовании.
· При проведении бактериоскопического исследования отделяемого из влагалища: лейкоциты до 10-15 в поле зрения, палочковая флора, единичные кокки .
· Отсутствие этиологически значимой флоры при проведении бактериологического исследования отделяемого из цервикального канала.
· Отсутствие ИППП на момент обследования ( Chlamydia trachomatis, Mycoplasma genitalium, Neisseria gonorrhoeae, Trichomonas vaginalis) .
· Положительный ВПЧ тест: ВПЧ 16 типа обнаружен в 19 случаях, ВПЧ 16 и 18 типов в 5 случаях, ВПЧ 18 типа – в 2 случаях, в 1 случае наблюдался ВПЧ-негативный результат (возможно инфицирование другими онкогенными типами, на которые пациентки не обследовались).
· При оценке цитологического исследования: плоскоклеточный рак.
· При проведении расширенной кольпоскопии – признаки плоскоклеточных интраэпителиальных поражений высокой степени ( плотный ацето-белый эпителий, грубая мозаика и пунктация на пробе с уксусной кислотой; резкие контуры поражения, йоднегативные зоны при пробе Шиллера) . В 15 случаях кольпоскопия неадекватная – стык различных типов эпителия не визуализировался.
· При проведении прицельной биопсии или эксцизии (в 15 случаев у пациенток с неадекватной кольпоскопией) методом радиоволновой хирургии - во всех случаях диагностирован плоскоклеточный рак шейки матки. У 11 пациенток старше 30 лет выявлена 0 стадия (интраэпителиальная или преинвазивная карцинома). У 3 пациенток до 30 лет и у 13 женщин после 30 лет диагностирована IА стадия (микроинвазивная карцинома) с глубиной инвазии до 3 мм и шириной не более 7 мм [4, 6].
Всем женщинам была выполнена электроимпедансая томография шейки матки, проведено иммуноцитохимическое определение онкомаркера р16ink4a, изучена частота его встречаемости в этих группах и проведен корреляционный анализ с показателями электропроводности при различных степенях интроэпителиальных неоплазий и раке шейки матки на преинвазивной и микроинвазивной стадии. Полученные результаты представлены в таблицах 1, 2, 3 и 4.
Показатели средней электропроводности при цервикальных интраэпителиальных неоплазиях и раке в первую фазу МЦ у женщин различных возрастных групп. 50 кГц. 1 уровень сканирования (М ± SD).
Читайте также:

