Лимфодиссекция при раке гортани
Использование открытых хирургических доступов в лечении злокачественных новообразований надсвязочного и связочного отделов гортани проверено долгими годами практики, с их помощью возможно добиваться отличных онкологических результатов. Среди открытых методов удаления новообразований выделяют, в порядке возрастания сложности: ларингофиссура с хордэкто-мией и последующей реконструкцией, вертикальная частичная ларингэктомия, надскдалочная горизонтальная ларингэктомия, надперстневидная ларингэктомия, тотальная ларингэктомия.
Все варианты вмешательств, при которых гортань не удаляется полностью, называют органосохраняющими.
Хордэктомия с последующей реконструкцией проводится пациентам с опухолью Т1, которым по каким-то причинам невозможно выполнение эндоскопической операции. У некоторых пациентов (например, с ретрогнатией, тризмом, лучевой терапией в анамнезе) визуализация передней комиссуры затруднена, поэтому удалить опухоль эндоскопически невозможно. Хордкэтомия с реконструкцией не рекомендуются пациентам, у которых опухоль прорастает на противоположную голосовую складку.
Чаще всего необходима трахеотомия. При простой хордкэтомии приемлемым вариантом реконструкции является простое заживление вторичным натяжением, впоследствии, если это требуется, выполняется аугментационная медиализация. Также описаны методы интраоперационной реконструкции, когда новая голосовая складка формируется из подподъязычных мышц.
В большинстве случаев у пациентов, которым была проведена хордэктомия с ларингофиссурой, функции речи и глотания сохраняются, хотя чаще всего голос становится слабым.
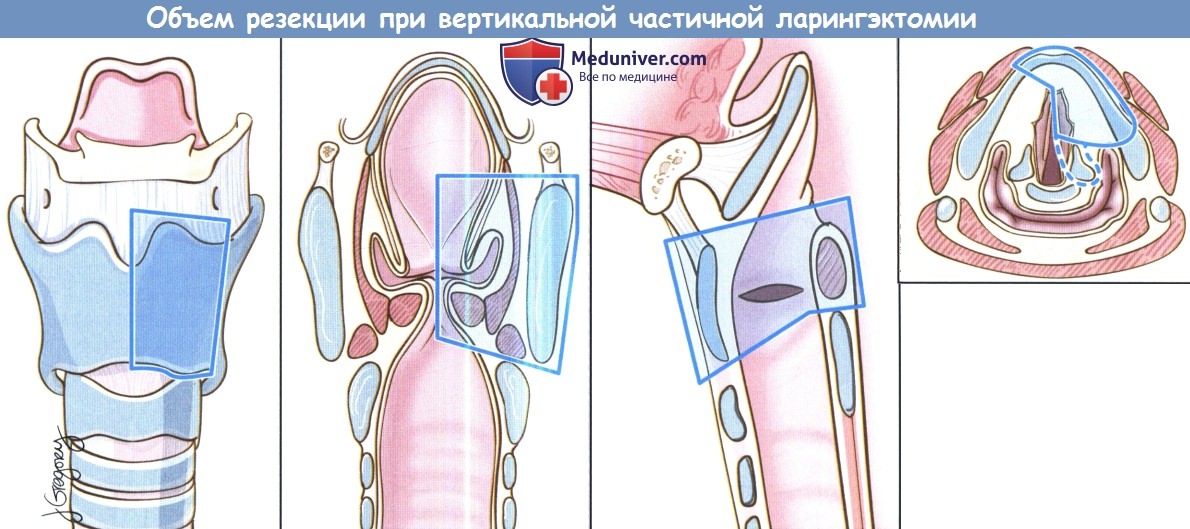
Вертикальная частичная ларингэктомия выполняется при опухолях Т1 и некоторых Т2. Чаще всего требуется трахеотомия. К противопоказаниям относится наличие опухоли Т3 без фиксации перстнечерпаловидного сустава, т.к. в данном случае предпочтительнее надперстневидная ларингэктомия. Выполняется ларингофиссура, локализация разреза для тиреотомии зависит от расположения опухоли, предварительно оцениваемого при помощи эндоскопии.
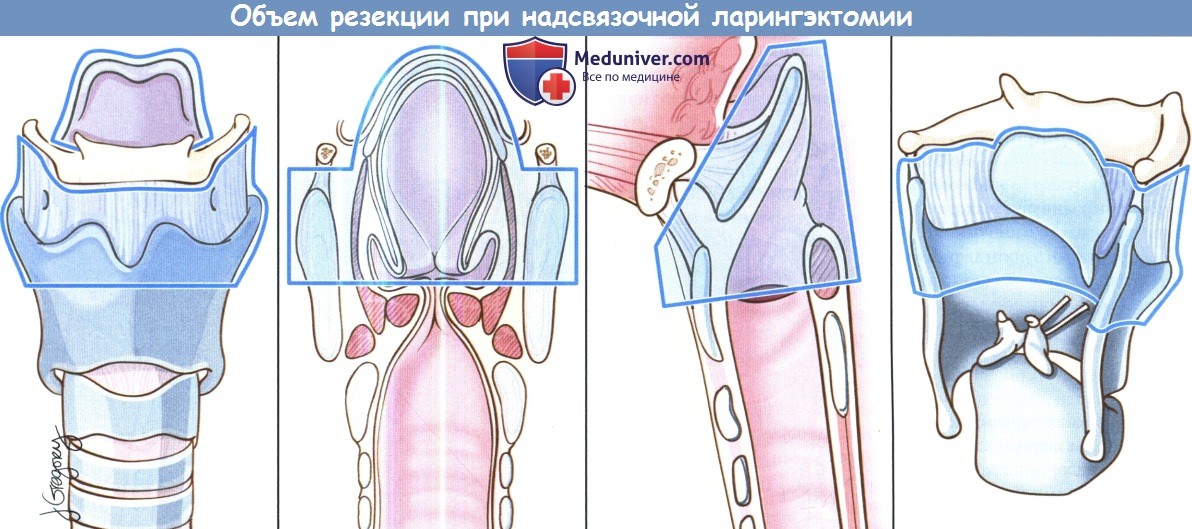
Открытая надскладочная ларингэктомия выполняется при опухолях Т1 и Т2, локализующихся в надсвязочном отделе гортани. Успешность лечения при опухолях Т1 составляет более 90%. Противопоказания включают распространение опухоли до уровня голосовой щели, инвазию в перстневидный или щитовидный хрящи, инвазию в корень языка более, чем на 1 см от желобовидных сосочков, поражение глубоких мышц языка или преднагортанникового пространства. При стандартной надскладочной ларингэктомии сохраняются обе голосовые складки, оба черпаловидных хряща, корень языка и подъязычная кость.
При инвазии опухоли в преднагортанниковое пространство необходимо удаление подъязычной кости, которую в противном случае можно оставить нетронутой. При резекции щитовидной кости особенно важно сохранить верхний гортанный сосудисто-нервный пучок (также об этом необходимо помнить при надперстневидной ларингэктомии). Методы реконструкции те же, что и при надперстневидной ларингэктомии.
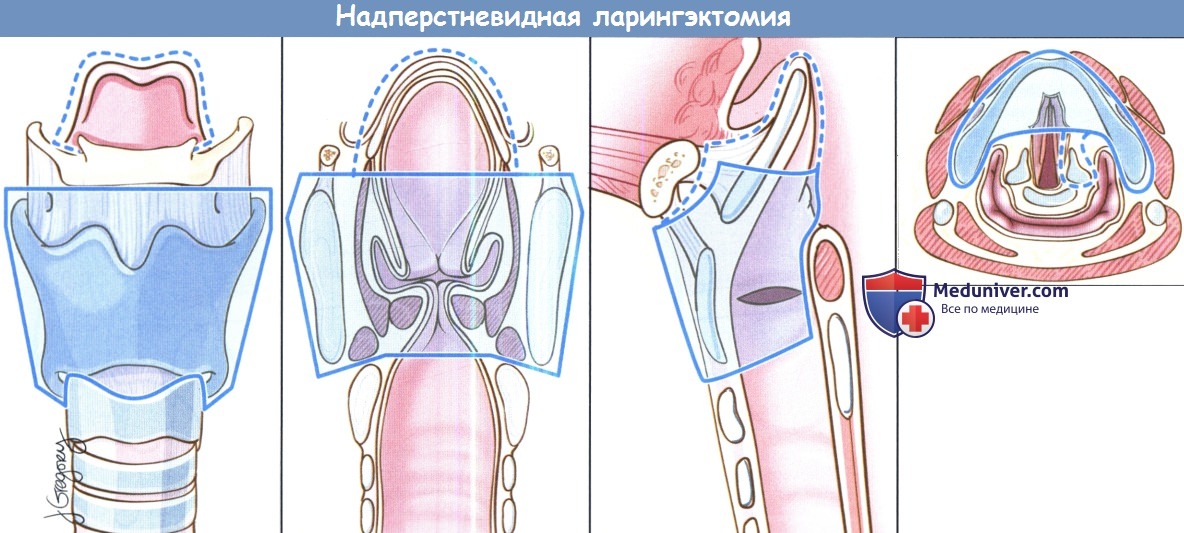
Самый широкий спектр возможностей обеспечивает надперстневидная ларингэктомия, поскольку она может использоваться при опухолях Т1,Т2,Т3 и некоторых Т4 стадий, как при надскладочной, так складочной локализации. Выполнение надперстневидной ларингэктомии возможно и при снижении подвижности или фиксации голосовых складок, поражении гортанных желудочков или передней комиссуры, ограниченной эрозии щитовидного хряща без экстраларингеального распространения.
В большинстве крупных исследований удавалось добиться высоких уровней пятилетней выживаемости и подавления местно-регионарного опухолевого роста. Противопоказаниями к надперстне-видной ларингэктомии являются фиксация перстнечерпаловидного сустава, поражение наружных мышц гортани, поражение возвратного гортанного нерва, распространение в подскладочное пространство более чем на 1 см, инвазия в перстневидный хрящ, заднюю комиссуру, экстраларингеальный рост, поражение надхрящницы наружной поверхности щитовидного хряща. Все ткани удаляются единым блоком.
Резекция включает обе истинные голосовые складки, обе ложные голосовые складки, оба окологолосовых пространства, весь щитовидный хрящ, в некоторых случаях надгортанник, иногда один или оба перстневидных хряща. При разделении перстнечерпаловидных суставов крайне важно сохранить возвратные гортанные нервы. Как уже упоминалось выше, для сохранения в послеоперационном периоде нормального глотания крайне важно оставить нетронутыми верхние гортанные сосуды и нерв. Для реконструкции подъязычную кость, корень языка, в некоторых случаях и надгортанник, подшивают к перстневидному хрящу тремя симметричными подслизистыми швами викрилом 1-0.
Осложнения всех органосохраняющих операций сходны. Аспирация и дисфагия обычно встречаются лишь в раннем послеоперационном периоде, но у некоторых пациентов они сохраняются в течение длительного времени, требуя чрескожной гастростомии. Возможно формирование глоточно-кожных фистул, но риск ниже, чем при полной ларингэктомии. При выполнении органосохраняющих открытых методов, например, надперстневидной ларингэктомии, крайне важно, чтобы заново сформированная гортань была отделена от трахеостомы. Невозможность деканулировать пациента в послеоперационном периоде связана либо с повреждением возвратных гортанных нервов, либо с сужением просвета дыхательных путей из-за некачественно выполненной реконструкции.
Наконец, при тотальной (полной) ларингэктомии удаляется вся гортань, подъязычная кость и несколько колец трахеи (в зависимости от распространения опухоли в подскладочный отдел). При выполнении полной ларингэктомии дыхательный тракт и пищеварительный тракт полностью отделяются друг от друга. Эффективность данной операции проверена временем, с ее помощью можно добиваться превосходных онкологических результатов.
Свободным элеватором вверху отслаивается слизистая оболочка грушевидных карманов, учитывая возможность использования для последующего сшивания глотки. Затем идентифицируют верхние и нижние паращитовидные железы и отводят их вбок на стороне первичного поражения, чтобы сохранить нижнюю щитовидную артерию. Со стороны первичного поражения обычно включается и доля щитовидной железы. Противоположная доля железы отсепаровывается от трахеи электрокоагулятором, при этом необходимо сохранить питающую ножку верхнего полюса и нижнюю щитовидную артерию. После разделения надподъязычных мышц мобилизуется подъязычная кость, большие рога отделяются от окружающих мягких тканей. При мобилизации верхнего рога в латеральном направлении нужно сохранить поъязычный нерв. Если трахеотомия уже выполнена, трахея рассекается на уровне трахеостомы.
Место входа в глотку зависит от результатов предоперационной фиброскопии или непрямой ларингоскопии. Как правило, хирургу следует вскрыть глотку в месте, не затронутом опухолевым ростом, т.к. это позволит выделять гортань под контролем зрения. Этим местом могут быть валлекулы, грушевидные синусы или слизистая позадиперстневидной области. Наиболее быстрым вариантом является доступ через валлекулы. Определить нужное место рассечения глотки можно пропальпировав валлекулы пациента через ротоглотку аспиратором или небольшим крючком.
После рассечения слизистой оболочки глотки, надгортанник берется на зажим. Хирург, стоя у изголовья пациента, изогнутыми ножницами рассекает глоточно-надгортанную складку, осторожно оставляя вокруг опухоли участок здоровых тканей. Разрез продолжается книзу. Размер сохраненной слизистой оболочки грушевидных синусов зависит от степени распространенности опухоли. Затем, после рассечения слизистой оболочки позадиперстневидной области, гортань может быть удалена. Если статус границ резекции неясен, следует отправить ткань с краев резекции на экспресс-исследование (также отправляются границы резекции на уровне трахеи). Для сохранения просвета трахеостомы в послеоперационном периоде выполняется пластика стомы (особенно важно, если в дальнейшем пациенту планируется проводить лучевую терапию).
Одним из возможных вариантов является модифицированная W-пластика. Трахея рассекается вдоль двух колец по средней линии. Кожа вокруг стомы рассекается в форме буквы W. 2-0 полипропиленовыми нитями трахея подшивается к коже полупогружными матрацными швами. Затем, при помощи 2-0 полипропиленовых швов и 2-0 полиглактин 910 формируется нижняя часть стомы. Перед ушиванием глотки рассекается перстнеглоточная мышца. Если в дальнейшем планируется выполнение трахео-эзофагеальной пункции, на заднюю стенку трахеи ниже 1 см будущей стомы накладывается зажим. Затем в пищевод устанавливается резиновый катетер размером 14F. В некоторых центрах для питания в раннем послеоперационном периоде устанавливают назогастральный зонд, но при грамотном уходе питание может осуществляться и через катетер, который легче переносится больными, чем назогастральный зонд.
Методика ушивания глотки зависит от разных факторов (количество слизистой оболочки, предоперационная лучевая терапия, предпочтения хирурга). При наличии достаточного объема слизистой возможно вертикальное ушивание глотки обратным швом по Connel. Первый шов накладывается на уровне корня языка, затем слизистая глотки ушивается книзу по вертикали. По мере продвижения хирурга книзу опытный ассистент должен выворачивать края слизистой грушевидных синусов. Горизонтальное наложение швов обычно представляет большую сложность, особенно ближе к центру, поскольку здесь натяжение тканей максимально, особенно в центре Недостатком Т-образного ушивания глотки является образование трифуркации в центре (самое слабое место шва, где натяжение максимально). Но при правильном исполнении все три данных метода дают хорошие результаты.
Для дополнительного укрепления глоточного шва возможно сшивание над ним волокон нижнего констриктора глотки вворачивающим швом, но данный метод увеличивает вероятность развития послеоперационной дисфагии. Для исключения просачивания слюны при помощи шприца в глотку вводится метиленовый синий. Места, в которых появился краситель, дополнительно ушиваются вворачивающим швом. Вне зависимости от метода ушивания глотки необходим тщательный послеоперационный уход для минимизации риска развития свища. Фибриновый клей, нанесенный на шов, также может снизить риск формирования фарингостомы.
Если пациенту перед операцией проводилась лучевая терапия, реконструкция может выполняться по той же схеме, что была описана выше. Даже при достаточном объеме слизистой оболочки грушевидных синусов можно использовать другие методы реконструкции: пектораль-ный мышечно-кожный лоскут, свободный лучевой лоскут предплечья, свободный антеролатеральный лоскут бедра. Преимуществом этих методик является снижение риска формирования стриктур пищевода и глоточно-кожных фистул.
Традиционно пациентам с рецидивом или сохранением заболевания после курса химиотерапии выполнялась тотальная ларингэктомия. Но в последние годы появляются сообщения о том, что у тщательно отобранных пациентов данной группы можно использовать эндоскопические лазерные или органосохраняющие открытые методики. В качестве операции отчаяния Steiner и соавт. предлагают использовать трансоральную лазерную микрохирургическую резекцию.
Holsinger и соавт. в качестве операции отчаяния прибегают к открытым органосохраняющим методикам, чаще всего к надперстневидной ларингэктомии; но данный подход связан с увеличением риска аспирации, дисфагии и обструкции дыхательных путей вследствие отека оставшейся части гортани. Тем не менее, специалист по хирургии головы и шеи всегда должен помнить о существовании данных подходов в лечении рецидивирующих опухолей гортани.
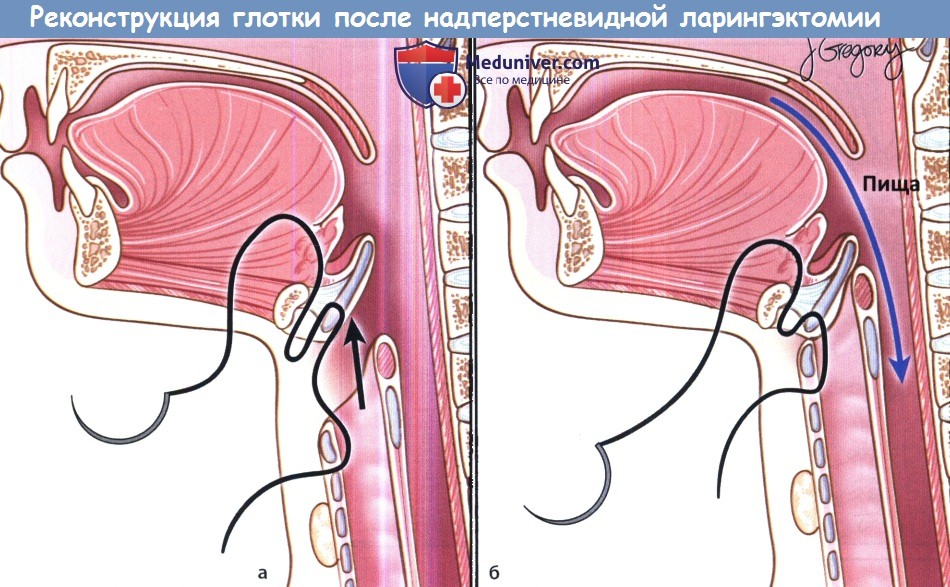
(а, б) Реконструкция глотки после надперстневидной ларингэктомии заключается в проведении крикохиоидо(эпиглотто)пексии, при которой глотка подшивается сверху к корню языка.
Пища проходит сзади от дыхательных путей, аспирация не развивается.
Если для полного удаления опухоли требуется удаление надгортанника, он резецируется. 
Тотальная ларингэктомия.
Подъязычная кость освобождается от надподъязычных мышц и мобилизуется.
Следует избегать возникающего на данном этапе риска повреждения подъязычного нерва. 
(а) Для увеличения размеров трахеостомы выполняется W-пластика, намечены линии разрезов.
(б) Трахея рассекается вдоль средней линии, ее лоскуты подшиваются к коже.
(в) Итоговый результат. 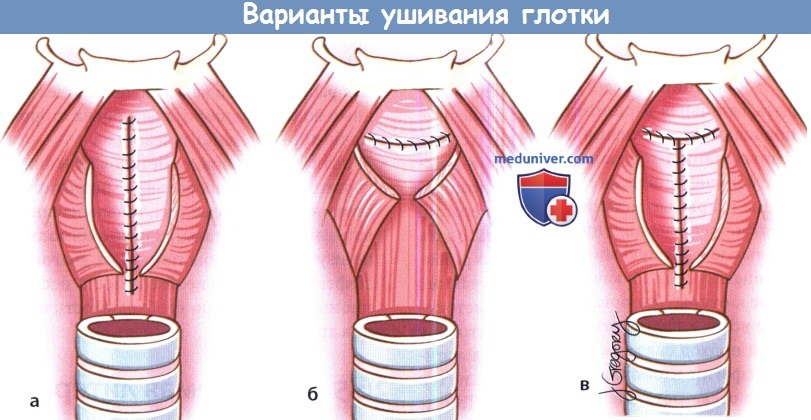
(а, б, в) Ушивание глотки может выполняться вертикально, горизонтально или Т-образно.
Лимфодиссекция при раке гортани. Решение о выборе метода воздействия на лимфоузлы шеи зависит от стадии первичной опухоли по системе TNM, пораженного отдела гортани, метода воздействия на первичную опухоль. На ранних стадиях рака голосового отдела относительно редко развиваются метастазы в регионарные лимфоузлы, поскольку лимфотток от этой области достаточно беден. У пациентов с раком голосового отдела гортани ранней стадии и статусом лимфоузлов N0 разумной стратегией является простое динамическое наблюдение. Надсвязочный отдел, напротив, характеризуется богатым двусторонним лимфоттоком в узлы яремно-двубрюшной цепи.
И хотя в отдельных случаях опухоли Т1 можно прибегнуть к консервативной тактике, большинству пациентов с более распространенными опухолями необходимо селективное воздействие на лимфоузлы шеи (или хирургическое уровней II, III и IV, или лучевое, включающее зоны риска), вне зависимости от данных клинического осмотра. Если в лечении первичного очага использовалась лучевая терапия, центральные и латеральные лимфоузлы шеи также следует включать в поле облучения. При статусе лимфоузлов N+ выполняется соответствующая шейная лимфодиссекция.
Ключевые моменты:
• Предоперационная лучевая или химиолучевая терапия значительно затрудняют заживление послеоперационных ран и снижают вероятность достижения хорошего функционального результата. Тем не менее, они не являются противопоказаниями к проведению органосохраняющих операций.
• При раке передней комиссуры на ранней стадии лучше прибегать к эндоскопическим лазерным или открытым органосохраняющим хирургическим методикам, а не проводить изолированную лучевую терапию.
• При раке надсвязочного отдела или связочного отдела с распространением в надсвязочный отдел необходимо воздействие на лимфоузлы с обеих сторон шеи (либо хирургическое, либо лучевое).
• И хотя исследования новых методов лечения раков гортани, таких как трансоральная микрохирургическая эндоскопическая резекция, только начинают давать свои первые результаты, их необходимо тщательно изучать для того, чтобы понять их долгосрочную эффективность, оценить необходимость послеоперационной лучевой терапии, необходимость выполнения трахеотомии.
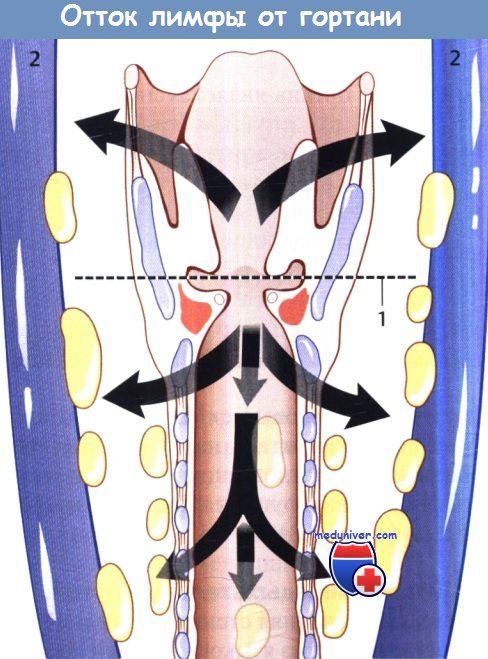
Лимфатический барьер гортани, включающий надскладочные и подскладочные лимфатические узлы.
Первым эшелоном надскладочных лимфатических узлов являются непостоянный предгортанный лимфатический и верхние глубокие шейные лимфатические узлы.
Первым эшелоном подскладочных лимфатических узлов являются пре- и паратрахеальные и нижние глубокие яремные лимфатические узлы.
1 - лимфатический барьер гортани; 2 - внутренняя яремная вена.
СМОТРЕТЬ ДРУГИЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
Год утверждения 2018
Профессиональные ассоциации:
- Ассоциация онкологов России
- Российское общество специалистов по опухолям головы и шеи
- Российское общество клинической онкологии
Оглавление
1. Краткая информация
Рак гортани – злокачественная опухоль из элементов неороговевающего эпителия гортани.
- Длительное курение
- Употребление алкоголя
- Работа при повышенной запылённости (текстильное производство)
- Вдыхание канцерогенов (нефть и продукты перегонки, бензол, фенольные смолы, асбест)
- ВПЧ-ассоциированный папилломатоз
- рецидивирующий папилломатоз
- пахидермия
- дискератоз
- хронические воспалительные процессы (ларингиты).
Стандартизованная заболеваемость в РФ (2015г.):
- 6,69 мужчины
- 0,33 женщины
Смертность на 100 тыс. населения в РФ (2015г.):
- 4,01 мужчины
- 0,18 женщины
С32.0– Злокачественное новообразование собственно голосового аппарата
C32.1 – Злокачественное новообразование над собственно голосовым аппаратом
С32.2 – Злокачественное новообразование под собственно голосовым аппаратом
С32.3 – Злокачественное новообразование хрящей гортани
С32.8 – Злокачественное новообразование, выходящее за пределы одной и более вышеуказанных локализаций
С32.9 – Злокачественное образование гортани неуточненное
Международная гистологическая классификация опухолей гортани. (классификация ВОЗ, 4-е издание, 2010 г)
Злокачественные эпителиальные опухоли
- 8070/3 Плоскоклеточный рак, БДУ
- 8051/3 Бородавчатый рак, БДУ
- 8083/3 Базалоидный плоскоклеточный рак
- 8052/3 Папиллярный плоскоклеточный рак
- 8074/3 Плоскоклеточный рак, веретеноклеточный
- 8075/3 Плоскоклеточный рак, аденоидный
- 8560/3 Железисто-плоскоклеточный рак
- 8082/3 Лимфоэпителиальный рак
Доброкачественные эпителиальные образования
- 8050/0 Папиллома, БДУ
- 8060/0 Плоскоклеточный папилломатоз
Степень распространенности представлена в классификации TNM 2009 г.
Плоскоклеточный рак составляет 98%.
2. Диагностика
- Стойкая осиплость, редко кашель.
- Затруднение дыхания при перекрытии просвета.
- Постоянный кашель, не купируемая антибактериальным и противовоспалительным лечением боль в горле.
- Увеличение шейных лимфоузлов
- Изменение контуров шеи
- Увеличение регионарных лимфоузлов
- Изменение подвижности, ширины остова гортани
- Развернутый клинический анализ крови
- Биохимический анализ крови
- Исследование свёртывающей системы крови
- Анализ мочи
- Титр антител к HPV 16 и 18 подтипов (ПЦР)
Фиброскопическое эндоскопическое исследование верхних дыхательных и пищеварительных путей:
- с биопсией;
- с мазками-отпечатками с эрозий и изъязвлений;
- пункция уплотнений без изъязвлений.
УЗИ лимфоузлов (ЛУ) шеи с пункцией непальпируемых ЛУ.
УЗИ органов брюшной полости и забрюшинного пространства.
Рентгенография грудной клетки.
ПЭТ-КТ при подозрении на диссеминированный процесс.
ЭКГ.
КТ костей лицевого скелета и шеи с внутривенным контрастированием при подозрении распространения опухоли на нижнюю/верхнюю челюсти, основание черепа.
Остеосцинтиграфия при подозрении на метастатическое поражение костей.
Тонкоигольная аспирационная биопсия (ТАБ) под контролем УЗИ при подозрении на метастазы в ЛУ шеи.
Дополнительно при хирургическом лечении:
- ЭХО-КГ,
- холтеровское мониторирование,
- ФВД,
- УЗДГ сосудов шеи и нижних конечностей,
- Консультации кардиолога, эндокринолога, невропатолога.
Обязательное гистологическое исследование удаленной опухоли с указанием:
- Размера опухоли;
- Глубины инвазии;
- Гистологического строения;
- Степени дифференцировки;
- Лимфоваскулярной, периневральной инвазии;
- рТ;
- рN (число исследованных и поражённых ЛУ);
- Поражения опухолью краев резекции.
- Лечение
3. Лечение
Хирургическое вмешательство - основной метод радикального лечения.
Адъювантное/неоадъювантное химиолучевое лечение по показаниям.
Эндоларингеальная резекция или лучевая терапия (ЛТ).
ЛТ или резекция гортани (эндоскопическая или открытая) ±операция на ЛУ шеи.
Конкурентная химиолучевая терапия (ХЛТ) при неблагоприятных гистологических признаках:
- прорастание опухолью капсулы ЛУ;
- наличие периневральной инвазии;
- опухолевые эмболы в сосудах.
Повторное оперативное вмешательство или ЛТ при наличии опухолевых клеток в краях резекции.
Конкурентная ХЛТ с цисплатином или ЛТ или ларингэктомия с резекцией щитовидной железы на стороне поражения +/- одно/двусторонней шейной лимфодиссекцией (N+).
Конкурентная ХЛТ при неблагоприятных гистологических признаках:
- прорастание опухолью капсулы ЛУ,
- положительные края,
- периневральная инвазия,
- сосудистая эмболия.
Хирургическое вмешательство при остаточной опухоли и/или метастатических ЛУ после ХЛТ или консервативного лечения на первом этапе.
При полной регрессии метастатических узлов в результате ХЛТ - динамическое наблюдение
Конкурентная ХЛТ с цисплатином или ларингэктомия с резекцией щитовидной железы на стороне поражения, одно/двусторонней шейной лимфодиссекцией или индукционная ХТ.
При остаточной опухоли и/или метастатических ЛУ после конкурентной ХЛТ рекомендовано хирургическое вмешательство.
При полной регрессии метастатических узлов после конкурентной ХЛТ - динамическое наблюдение.
При стабилизации или прогрессировании на индукционной ПХТ показана ларингэктомия с резекцией щитовидной железы на стороне поражения, одно/двусторонней шейной лимфодиссекцией.
При неблагоприятных гистологических признаках в удалённом блоке опухоли показана конкурентная ХЛТ.
Ларингэктомия с резекцией щитовидной железы на стороне поражения, одно/двусторонней шейной лимфодиссекцией с послеоперационной ХЛТ.
Конкурентная ХЛТ или индукционная полихимиотерапия (ПХТ) с последующей конкурентной ХЛТ.
При остаточной опухоли и/или метастатических ЛУ после ХЛТ рекомендовано хирургическое вмешательство.
При полной регрессии метастатических узлов после ХЛТ показано динамическое наблюдение.
При общем состоянии по шкале Карновского:
0-1 балла - конкурентная ХЛТ или индукционная полихимиотерапия (ПХТ) с последующей ХЛТ;
2 балла - самостоятельная лучевая терапия с последующей химиотерапией;
3 балла - паллиативная лучевая терапия, монохимиотерапия или симптоматическое лечение
При общем состоянии по шкале Карновского:
0-1 балла – поли- или монохимиотерапия с последующей конкурентной ХЛТ;
2 балла - монохимиотерапия или симптоматическое лечение;
3 балла - симптоматическое лечение.
Хирургическое вмешательство или конкурентная химиолучевая терапия или индукционная химиотерапия с последующей конкурентной ХЛТ.
При неблагоприятных гистологических признаках в удалённой опухоли - конкурентная ХЛТ.
При положительных краях резекции – повторное оперативное вмешательстве или ЛТ.
Хирургическое вмешательство с обсуждением повторной ЛТ или повторная ЛТ с последующей ХТ.
При общем состоянии по шкале Карновского:
0-1 балла – поли- или монохимиотерапия;
2 балла - монохимиотерапия или симптоматическое лечение;
3 балла - симптоматическое лечение.
ЛТ или резекция гортани (эндоскопическая или открытая) ±операция на ЛУ шеи.
При неблагоприятных гистологических признаках в удалённой опухоли - конкурентная ХЛТ.
При положительных краях резекции – обсуждение повторного оперативного вмешательства или проведение ЛТ.
Конкурентная ХЛТ или ЛТ (противопоказание к ХЛТ) или ларингэктомия с резекцией щитовидной железы на стороне поражения +/-одно/двусторонней шейной лимфодиссекцией (при N+) или индукционная ХТ.
При остаточной опухоли и/или метастатических ЛУ после ХЛТ рекомендовано хирургическое вмешательство.
При полной регрессии метастатических узлов после ХЛТ - динамическое наблюдение.
При неблагоприятных гистологических признаках в удалённой опухоли показана конкурентная ХЛТ, при отсутствии неблагоприятных гистологических признаков - ЛТ.
При полной или частичной регрессии опухоли после 2-3 курсов индукционной ПХТ показана ЛТ или ХЛТ.
При остаточной опухоли и/или метастатических ЛУ после ХЛТ рекомендовано хирургическое вмешательство.
При полной регрессии метастатических узлов после ХЛТ – динамическое наблюдение.
При стабилизации или прогрессировании на фоне индукционной ПХТ показана ларингэктомия с резекцией щитовидной железы на стороне поражения, одно/двусторонней шейной лимфодиссекцией.
При неблагоприятных гистологических признаках в удалённой опухоли показана конкурентная ХЛТ, при отсутствии неблагоприятных признаках рекомендована ЛТ.
Конкурентная ХЛТ или ЛТ (при противопоказаниях к ХЛТ) или надскладочная резекция гортани и одно/двусторонней шейной лимфодиссекцией (при N+) или индукционная ХТ.
При остаточной опухоли и/или метастатических ЛУ после ХЛТ рекомендовано хирургическое вмешательство.
При полной регрессии метастатических узлов после ХЛТ - динамическое наблюдение.
При неблагоприятных гистологических признаках в удалённой опухоли показана конкурентная ХЛТ, при отсутствии признаков - ЛТ.
При полной или частичной регрессии первичной опухоли после 2-3 курсов ПХТ проводят ЛТ или ХЛТ.
При остаточной опухоли и/или метастатических ЛУ после ХЛТ рекомендовано хирургическое вмешательство.
При полной регрессии метастатических узлов после ХЛТ – динамическое наблюдение.
При стабилизации или прогрессировании на фоне ПХТ показана ларингэктомия с резекцией щитовидной железы на стороне поражения, одно/двусторонней шейной лимфодиссекцией.
При неблагоприятных гистологических признаках в удалённой опухоли рекомендована ХЛТ, при отсутствии признаков - ЛТ.
Конкурентная ХЛТ или ЛТ (при противопоказаниях к ХЛТ) или надскладочная резекция гортани и одно/двусторонней шейной лимфодиссекцией (при N+) или индукционная ХТ.
При наличии остаточной опухоли и/или метастатических ЛУ после ХЛТ - хирургическое вмешательство.
При полной регрессии метастатических узлов после ХЛТ - динамическое наблюдение.
При неблагоприятных гистологических признаках в удаленной опухоли –конкурентная ХЛТ, при отсутствии признаков рекомендована ЛТ.
При полной или частичной регрессии первичной опухоли после 2-3 курсов ПХТ рекомендована ЛТ или ХЛТ.
При остаточной опухоли и/или метастатических ЛУ после ХЛТ - хирургическое вмешательство.
При полной регрессии метастатических узлов после ХЛТ – динамическое наблюдение.
При стабилизации или прогрессировании на фоне индукционной ПХТ показана ларингэктомия с резекцией щитовидной железы на стороне поражения, одно/двусторонней шейной лимфодиссекцией.
При неблагоприятных гистологических признаках в удаленной опухоли показана ХЛТ, при отсутствии признаков - ЛТ.
Ларингэктомия с резекцией щитовидной железы на стороне поражения, одно/двусторонней шейной лимфодиссекцией с послеоперационной конкурентной ХЛТ.
Конкурентная ХЛТ или индукционная ПХТ с последующей ХЛТ.
При остаточной опухоли и/или метастатических ЛУ после ХЛТ - хирургическое вмешательство.
В случае полной регрессии метастатических узлов после ХЛТ показано динамическое наблюдение.
Хирургическое вмешательство или конкурентная ХЛТ или индукционная ХТ с последующей ХЛТ.
При неблагоприятных гистологических признаках в удалённой опухоли показана ХЛТ.
При положительных краях резекции – повторная операция или ЛТ.
Хирургическое вмешательство с обсуждением повторной ЛТ или повторная ЛТ с последующей ПХТ.
При общем состоянии по шкале Карновского:
0-1 балла - поли- или монохимиотерапия;
2 балла - монохимиотерапия или симптоматическое лечение;
3 балла - симптоматическое лечение.
ЛТ в самостоятельном варианте ежедневно с понедельника по пятницу:
- на первичный очаг 70 Гр (2 Гр/фракция) 7 недель;
- на клинически определяемые регионарные метастазы 70 Гр (2 Гр/фракция) 7 недель;
- на клинически не измененные ЛУ 50 Гр (2.0 Гр/фракция).
Конкурентная ХЛТ ежедневно с понедельника по пятницу:
- на первичный очаг – 70Гр (2,0 Гр/фракция) 6-7 недель;
- на клинически определяемые регионарные метастазы – 70Гр (2,0 Гр/фракция) 6-7 недель;
- на клинически неизмененные ЛУ 50 Гр (2.0 Гр/фракция).
Послеоперационная ЛТ ежедневно с понедельника по пятницу:
- интервал между оперативным вмешательством и ЛТ не более 6 недель;
- при высоком риске (неблагоприятные морфологические признаки) 60-66 Гр (2 Гр/фракция) 6-6,5 недель;
- при низком/среднем риске на клинически не измененные ЛУ 50 Гр (2.0 Гр/фракция.)
До лечения специализирующийся на ОГШ хирург-онколог оценивает:
- адекватность биопсийного материала;
- правильность стадирования;
- оптимальность визуализации опухолевого процесса (КТ, МРТ);
- исключает синхронный рак;
- текущий функциональный статус и возможность хирургического лечения;
- разрабатывает проспективный план наблюдения для полной реабилитации.
Не следует модифицировать хирургическое вмешательство на основании клинического ответа на лечение, за исключением случаев прогрессии, вынуждающих к более обширной операции.
Оценка операбельности
Ухудшает прогноз или классифицируется как Т4b:
- значительное поражение крыловидно-небной ямки;
- тяжелые тризмы из-за инфильтрации опухолью крыловидных мышц;
- макроскопическое распространение на основание черепа;
- возможная инвазия (охват) стенки общей или внутренней сонной артерии;
- распространение опухоли из регионарных ЛУ на кожу, структуры средостения, предпозвоночную фасцию или шейные позвонки.
Удаление первичного очага
- Удаление единым блоком.
- Предпочтительны трансоральные резекции CO2-лазером и под оптическим увеличением.
- При прилежании опухоли к двигательному или сенсорному нерву не исключена периневральная инвазия, что требует выделения нерва в проксимальном и дистальном направлениях и его резекции.
- Срочная диагностика проксимального и дистального краев нерва методом замороженных срезов.
Края резекции
Адекватное удаление - расстояние от края резекции до макроскопически видимой опухоли ≥ 2 см или отрицательный край замороженного среза.
Чистый край - расстояние от инвазивного края опухоли ≥ 5 мм от края резекции.
Близкий край - расстояние от инвазивного края опухоли до края резекции равное
Шейную диссекцию ориентируют или выполняют срезы по порядку для определения уровня ЛУ, включенных в зону диссекции.
Реконструкция хирургических дефектов
- Использование конвенциальной техники по усмотрению хирурга.
- По возможности рекомендуется первичное ушивание, без пренебрежения широкими краями резекции, свободными от опухоли.
- По усмотрению хирурга пластическое ушивание местными/регионарными лоскутами, свободным лоскутом, расщепленным кожным лоскутом или другими лоскутами с/без реконструкции нижней челюсти.
Индивидуальный выбор схемы ХТ.
Индукционная ХТ - 2-3 курса с интервалом 3 недели с последующей ХЛТ:
- Доцетаксел 75мг/м2 1 день
- Цисплатин 75мг/м2 1 день
- 5-ФУ 1000мг/м2/сут 1-4 дни.
Конкурентная (одновременная) ХЛТ после индукции
Химиотерапия (один из препаратов):
- Цисплатин 100мг/м2 1, 22, 43 дни;
- Карбоплатин 1,5-2,0 AUC еженедельное (меньшая токсичность);
- Цетуксимаб 400мг/м2 за неделю до начала ЛТ и 250мг/м2 еженедельно во время ЛТ.
Лучевая терапия ежедневно с понедельника по пятницу 6-7 недель на первичный очаг и клинически определяемые регионарные метастазы – 70Гр (2,0 Гр/фракция) или на неизмененные ЛУ 44-60 Гр (2.0 Гр/фракция).
Противорецидивная химиотерапия
Полихимиотерапия 1 линии:
- DC + цетуксимаб
- PtxCarbo + цетуксимаб
Монохимиотерапия 1 линии:
- Цисплатин,
- Карбоплатин,
- Паклитаксел,
- Доцетаксел,
- 5-ФУ,
- Метотрексат,
- Цетуксимаб,
- Гемцитабин.
Химиотерапия 2 линии:
- DC + цетуксимаб,
- PtxCarbo + цетуксимаб,
- ниволумаб (прогрессирование на платиносодержащей схеме),
- пембролизумаб (прогрессирование на платиносодержащей схеме),
- афатиниб (прогрессирование на платиносодержащей схеме).
4. Реабилитация
Ориентир на общие принципы реабилитации пациентов после хирургических вмешательств, лучевой терапии и/или химиотерапии.
- голосовое протезирование;
- электрогортань;
- формирование пищеводной речи.
Для адекватной реабилитации речевой, глотательной функции - консультация логопеда.
5. Профилактика и диспансерное наблюдение
Физикальный осмотр и сбор жалоб:
- 1-2 года - каждые 3-6 месяцев,
- 3-5 лет – 1 раз в 6-12 месяцев,
- после 5 лет - ежегодно или при появлении жалоб.
При высоком риске рецидива перерыв между обследованиями можно сократить.
- Анамнез и физикальное обследование
- Ларингоскопия
- УЗИ ЛУ шеи с 2-х сторон, органов брюшной полости и малого таза каждые 3-6 мес. в зависимости от риска прогрессирования;
- Рентгенография органов грудной клетки каждые 12 мес.
Цель наблюдения - раннее выявление прогрессирования заболевания и метахронных ОГШ
Читайте также:

