Костный мозг клеточный лейкоз
При подозрении на лейкоз врачи назначат анализ крови на бласты. Это исследование помогает своевременно выявить опасное заболевание и приступить к лечению как можно раньше. Как правильно подготовиться к взятию пробы? И как расшифровать результаты анализа? Эти вопросы мы рассмотрим в статье.
Что это такое?
Бласты представляют собой незрелые кровяные клетки, которые продуцируются в костном мозге. В дальнейшем они преобразуются в эритроциты, лейкоциты и тромбоциты. Бластные клетки являются предшественниками зрелых кровяных телец.
У здорового человека бласты в костном мозге составляют не более 5 % клеток. При инфекционных заболеваниях их концентрация может возрастать до 10 %. Однако в норме незрелые клетки не должны попадать в кровоток. Они могут находиться только в пределах костного мозга.
При тяжелых гематологических патологиях у пациента появляются бласты в крови. Что это значит? Такой результат анализа указывает на онкологические болезни системы кроветворения. При этих патологиях в костном мозге образуется чрезмерное количество незрелых элементов. Избыток бластов выбрасывается в кровоток. Их наличие в анализе является тревожным признаком.
В начальной стадии рака крови в костном мозге может находиться около 40 % бластных клеток. В дальнейшем из этих незрелых элементов образуется злокачественная опухоль.
Анализ крови
Как выявить присутствие в кровотоке бластов? Это можно сделать с помощью общего анализа крови. Это исследование показывает количество зрелых и незрелых клеток.
Для пробы берут кровь из пальца или из вены. Биоматериал изучают под световым микроскопом. Это устройство имеет специальную сетку для подсчета кровяных клеток. С ее помощью и определяют концентрацию бластов. В расшифровке анализа количество незрелых клеток указывается в процентах.
Показания к исследованию
В каких случаях врачи назначают анализ на бласты? Это исследование показано, если у пациента отмечаются следующие симптомы:
- увеличение лимфатических узлов;
- беспричинное повышение температуры;
- увеличение печени и селезенки;
- слабость;
- воспаление миндалин в тяжелой форме;
- красные точки на коже;
- повышенная кровоточивость.

Очень часто пациенты принимают эти проявления за признаки ангины и других инфекционных болезней. Однако такие симптомы могут свидетельствовать о наличии тяжелой патологии костного мозга. С целью дифференциальной диагностики врачи назначают анализ на наличие бластов в крови.
Подготовка к анализу
Пробу на бластные клетки обычно берут утром, натощак. Результаты анализа чаще всего бывают готовы уже на следующий день.
Какие правила нужно соблюдать перед взятием биоматериала на бласты? Это исследование не требует сложной подготовки. Нужно придерживаться следующих рекомендаций:
- прекратить прием еды за 8 часов до теста;
- не употреблять алкоголь накануне исследования;
- за 2 часа до взятия крови исключить курение.
Рекомендуется также прекратить прием лекарств за 3 дня до анализа. Если же больной не может прервать курс медикаментозного лечения, то нужно рассказать врачу обо всех принимаемых препаратах.
Расшифровка
В норме бласты должны отсутствовать в анализе. В этом случае в результатах исследования указано, что их показатель равен 0 %. У здорового человека в крови могут находиться только зрелые элементы.
Если в анализе присутствует даже малый процент бластов, то это является опасным признаком. Результаты пробы нужно обязательно показать врачу и немедленно приступить к лечению.

Причина отклонений: лейкоз
Основной причиной появления в пробе бластных клеток является лейкоз. Это заболевание иначе называется лейкемией или раком крови. Патология сопровождается неконтролируемым делением незрелых клеток в костном мозге, которые в дальнейшем образуют опухоль.
Врачи выделяют две формы лейкоза:
- острую;
- хроническую.
При острой лейкемии в крови обнаруживается огромное количество бластных клеток. Их концентрация может быть более 20 %. При хронической форме рака крови показатель незрелых элементов обычно не превышает 5-10 %.
Другие показатели крови
При изучении результатов анализа врач обязательно обращает внимание и на другие показатели клинического исследования. Наличие бластных клеток в биоматериале всегда рассматривается в сочетании с другими параметрами крови. На наличие лейкоза могут указывать следующие данные:
- Лейкоцитоз. Примерно у 15 % больных острой формой лейкемии показатель белых кровяных телец превышает норму в десятки раз.
- Низкий гемоглобин. У пациентов с раком крови отмечается тяжелая анемия и снижение числа эритроцитов.
- Падение уровня тромбоцитов. По этой причине у больных лейкемией отмечается повышенная кровоточивость.
- Снижение ретикулоцитов. Эти клетки являются молодыми формами эритроцитов. Их малое количество приводит к анемии.
- Полное отсутствие эозинофилов и базофилов. Это становится причиной резкого снижения иммунитета.
Вышеперечисленные признаки вместе с появлением бластных клеток в крови позволяют врачу поставить диагноз "лейкоз".
Исследование костного мозга
Если у пациента в крови обнаружены бласты, то врачи обычно назначают пункцию костного мозга. Исследование проводят под местным обезболиванием. Специальной длинной иглой делают прокол в области грудины или позвоночника и берут на исследование кусочек ткани костного мозга.
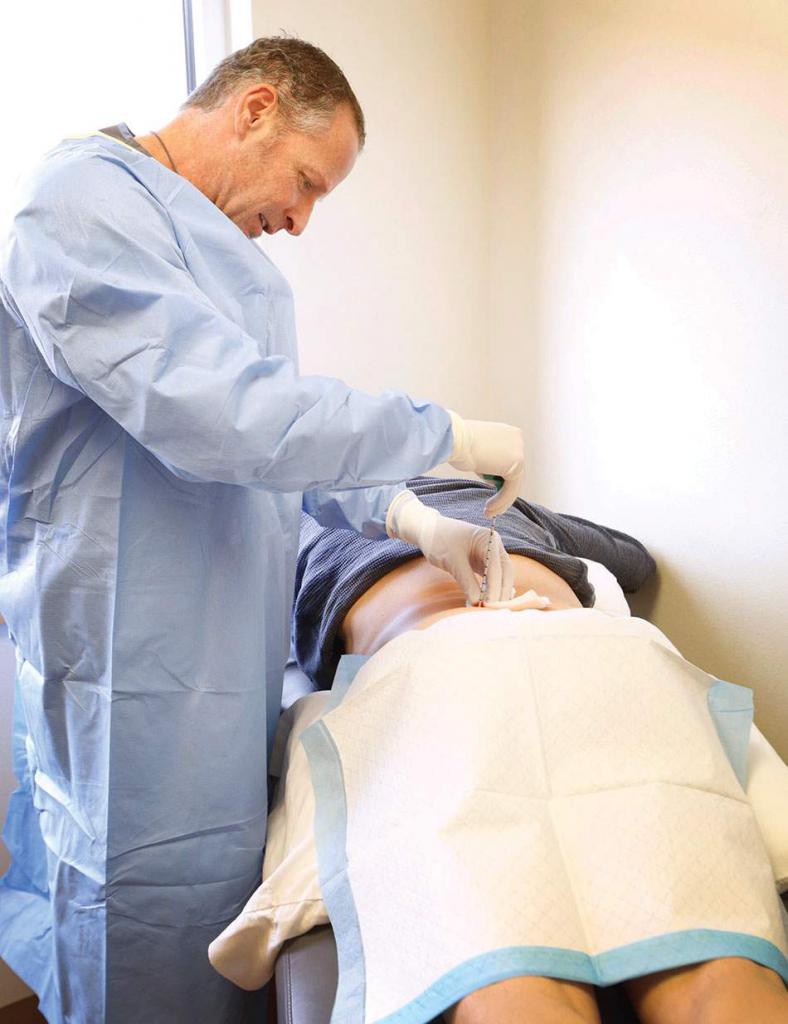
Пунктат исследуют при помощи микроскопа. В биоматериале определяют количество зрелых и незрелых элементов крови. Повышение бластных клеток до 10 % не всегда указывает на лейкемию. Такой результат исследования возможен при сильном стрессе или инфекционном заболевании. Если же концентрация бластов превышает 30 %, то это чаще всего является признаком рака крови. При этом у больного уменьшается количество эритроцитов, тромбоцитов и лейкоцитов в пункционном материале.
При подозрении на лейкоз также проводят цитохимический анализ пунктата. Он позволяет выявить уровень ферментов бластных клеток. Эти вещества вступают в реакцию с некоторыми красителями, что и используется при лабораторном исследовании. Положительные результаты пробы указывают на лейкоз. С помощью измерения уровня каждого бластного фермента можно определить форму рака крови.
Лечение
Что делать, если анализ крови показал наличие бластных клеток? В этих случаях врач обычно назначает ряд дополнительных анализов. Самым информативным из них является пункция костного мозга. Чрезмерно высокое количество бластов в пунктате является признаком лейкемии.
Если диагноз "лейкоз" подтвердился, то необходимо немедленно приступать к лечению. Важно помнить, что на ранних стадиях рака крови вполне возможно достичь полной или частичной ремиссии. В наши дни применяются следующие методы лечения лейкемии:
- Химиотерапия. Пациенту назначают цитостатики, которые подавляют рост новообразования в костном мозге. Такое лечение может занимать довольно длительное время.
- Переливание крови. Пациенту вводят внутривенно эритроциты и тромбоциты, полученные от донора. Это помогает поднять уровень гемоглобина и уменьшить кровоточивость.
- Радиотерапия. Такой вид лечения показан при хроническом лейкозе. Пациенту облучают увеличенные лимфоузлы и область селезенки.
- Антибактериальная терапия. Пациенты с лейкозом очень подвержены инфекционным патологиям. С целью предотвращения таких заболеваний назначают курсы приема антибиотиков.
- Пересадка костного мозга. Такая операция помогает полностью избавиться от лейкоза. Сложность трансплантации заключается в том, что чужой орган кроветворения не всегда приживается.
После комплексной терапии проводят повторную пункцию костного мозга. Если концентрация бластов снизилась до 5 %, то врачи говорят о полной ремиссии. Если же показатель незрелых клеток не превышает 20 %, то ремиссия считается частичной. В любом случае пациенту необходимо пожизненно соблюдать рекомендации врача. Лейкоз относится к опасным и тяжелым заболеваниям. Даже при полной ремиссии нельзя исключать рецидивы патологии.
Отвечаем на самые важные вопросы про лейкоз
" title="Показать лейкоз может исследование периферической крови
" itemprop="contentUrl">
Показать лейкоз может исследование периферической крови
Фото: Сергей Яковлев
В сентябре мы познакомились с архангелогородкой Вероникой Рожновской, жизнь которой изменилась, когда у её дочери Даши диагностировали лейкоз. Девочка в тот момент училась в пятом классе, а на недомогания врачи не обращали должного внимания. Специалисты отмечают, что рак крови действует тем агрессивнее, чем моложе организм, который поражает болезнь. На другие важные вопросы об этом раке отвечают профессор кафедры онкологии и медицинской радиологии Уральского государственного медицинского университета Сергей Берзин и гематолог из Уфы Нэлли Янтурина.
Лейкоз — опухолевое заболевание клеток крови. При лейкозе происходит патологическая трансформация лейкоцитов и их бесконтрольное деление. В итоге они замещают собой нормальные клетки костного мозга, из которых образуются циркулирующие в крови лейкоциты, эритроциты и тромбоциты.
При хронических лейкозах деление клеток идёт медленнее, и клиника тоже развивается с меньшей скоростью. Лейкозный клон током крови разносится по всей кроветворной ткани. Органами-мишенями, где откладываются метастазы, становятся почки и кости. Оседая в костной ткани, эти клетки, по-другому они называются миеломные, нарушают ее структуру. Это может проявляться частыми переломами, болью в позвоночнике, ребрах. Хронические лейкозы могут годами протекать без каких-либо явных отклонений в самочувствии, тогда выявить их можно только при исследовании крови.
Начало заболевания нередко протекает без выраженных симптомов. Больные отмечают общую слабость, утомляемость, неопределенную боль в костях, непостоянную температуру по вечерам в пределах 37,1–38 градусов. Но уже в этот период у некоторых больных можно обнаружить небольшое увеличение лимфатических узлов, селезенки. В анализе крови тоже будут изменения — повышение или снижение количества лейкоцитов, анемия.
Лейкоз может проявляться разнообразными симптомами. При острой форме пациенты могут жаловаться, что стали часто простывать, у них возникли инфекционные осложнения или синяки на теле, а кого-то будет беспокоить резкая потеря веса, появление шишек на теле или увеличение лимфоузлов.
Симптомы лейкоза неспецифичны, они таковы:
- слабость;
- головокружения;
- высокая температура без явных на то причин;
- боли в руках и ногах;
- кровотечения.
При замещении патологически размножающимися лейкоцитами других клеток крови на первое место выходят анемии и кровотечения из-за уменьшения числа других клеток крови — эритроцитов и тромбоцитов. Из-за накопления лейкоцитов в лимфоузлах, печени или селезёнке эти органы могут увеличиться, но обнаружить эти симптомы уже может только врач.
При лейкозе субстратом опухоли является костный мозг, который находится во всех трубчатых и плоских костях. Здесь же развиваются предшественники крови: эритроциты, лейкоциты и тромбоциты. Когда в ткани начинают развиваться опухолевые клетки, места для нормальных здоровых клеток крови просто не остается. Если в случае с раком желудка пораженный участок можно удалить, вовремя провести химиотерапию и добиться длительной ремиссии, то при раке крови такая тактика не приемлема.
Есть формы острого лейкоза, которые могут развиваться с первых дней жизни человека. Хроническим формам лейкоза подвержены люди старшего возраста. Чем моложе возраст, тем агрессивнее протекает болезнь, но при современных методиках лечения больной может жить до 5–7 лет. На течение хронического миелолейкоза (и это научно доказано) большое влияние оказывает состояние нервной системы больного — если есть стрессы, депрессии, люди сгорают буквально на глазах.
Лечение лейкоза — это достаточно длительный процесс. В среднем на достижение ремиссии при острых лейкозах уходит от 3 месяцев до 2–3 лет.
Первый и самый сложный этап в лечении острого лейкоза — это интенсивная химиотерапия, с помощью которой мы должны убить опухолевые клетки. Пациенты должны находиться в специальном асептическом блоке, в котором созданы стерильные условия, чтобы исключить их контакт с любой инфекцией. Больные в этот момент не имеют никаких собственных факторов защиты, потому что кроветворение у них пострадало от самой болезни и применяемых химиопрепаратов. Для закрепления результатов терапии после этапа восстановления (или поддержки ремиссии) принимается решение о необходимости трансплантации костного мозга.
Пересадку можно делать, если пациента ввели в ремиссию. Она бывает двух видов: аутотрансплантация, когда пересаживается костный мозг самого больного, и аллотрансплантация, в этом случае ткани забирают у донора.
В первом случае у пациента из вены берется периферическая кровь, из нее при помощи сепаратора извлекают стволовые клетки, консервируют и передают на хранение в банк. Затем пациенту проводят сильнейшую химиотерапию, а следом проводят пересадку — так же, через вену, вводят стволовые клетки, и они начинают творить новое потомство. Технически это выглядит как переливание крови. Пересадка может быть сделана и при хроническом лейкозе.
Аллотрансплантация дает хорошие результаты, если доноры — родные сестра или брат, у них самый близкий фенотип. Пересадка даже от двоюродных родственников не всегда бывает столь успешна, но все равно это шанс на то, что человек будет жить.
Лучшие доноры костного мозга — это мужчины в возрасте 30–40 лет, семейные, имеющие постоянное место работы. Желательно — на промышленном производстве, на заводах. Практика показывает, что именно такие люди относятся к донорству с наибольшей ответственностью.
Женщина тоже может стать донором костного мозга. Но здесь важно учесть, что после родов и беременностей в крови у женщин циркулируют антитела, и их лейкоциты уже настроены бороться с чужеродными антигенами. Поэтому результат пересадки может оказаться хуже.
Известно, что озлокачествленные клетки при остром лимфобластном лейкозе накапливаются в субарахноидальном пространстве, где они избегают разрушающего действия терапевтических средств (кроме больших доз метотрексата). В ликворе, заполняющем это пространство, эффективные концентрации цитотоксических препаратов не достигаются. Поэтому клетки, там находящиеся, представляют собой потенциальный центр, из которого развивается новый рецидив опухоли. Источником нового рецидива острого лимфобластного лейкоза могут стать и скопления опухолевых клеток в гонадах, особенно в яичках. В то же время вовлечение в процесс мягких мозговых оболочек и яичек при остром нелимфобластном лейкозе наблюдается редко. Диагностика острых лейкозов основывается на клинической симптоматике, картинах крови и пунктата костного мозга. Чтобы правильно выбрать лечение и оценить прогноз, необходимо отличать острый лимфобластный лейкоз от острого нелимфобластного лейкоза (табл. 12.3) и идентифицировать их подтипы. Субклассификация лейкозов базируется на протоколах франко-американобританской (FAB) исследовательской группы, которая рубрифицировала острые лимфобластные лейкозы и острые нелимфобластные лейкозы по строению лейкозных клеток, окрашенных по Романовскому (табл. 12.4 и 12.5). С использованием цитохимических и иммуноцитохимических маркеров, представленных в таблицах, классификационное разделение острых лимфобластных лейкозов и острых нелимфобластных лейкозов стало еще более точным. Лишь около 2 % острых лейкозов у взрослых и примерно 1 % у детей не удается типировать, применяя указанные подходы. Таблица 12.3. Дифференциально-диагностические признаки острого лимфобластного лейкоза (ALL) и острого нелимфобластного лейкоза (ANLL)| Признаки | ALL | ANLL |
| Цитологические Размеры лейкозных клеток | От малых до уме | От умеренных до крупных |
| Ядрышки в ядрах опухолевых | ренных Имеются 1—2 | Часто имеют более 2 яд |
| клеток | ядрышка | рышек |
| Цитоплазма | Скудная или уме | Умеренно развитая или |
| ренно развитая, | обильная, зернистая, ино | |
| однородная | гда с палочками Ауэра | |
| Цитохимические Реакция с пероксидазой и Суданом черным В | Отрицательная | Положительная |
| Реакция с кислой фосфатазой | Положительная | Обычно отрицательная |
| Окраска на терминальную дезоксинуклеотидилтрансферазу | Положительная | Иногда положительная |
| Реакции, выявляющие маркеры\ кластеров дифференцировки (CD, см главу 5) на опухолевых клеткахCD19 (маркер В-лимфоиитов) | Положительная | Отрицательная |
| CD7 (рецептор IgM, маркер Т-клеток) | (общая и нуллерная формы ALL)Положительная | |
| CD13 и CD33 | Отрицательная | Положительная |
Франко-американо-британская (FAB) классификация острых лимфобластных лейкозов
Франко-американо-британская (FAB) морфологическая классификация острых нелимфобластных лейкозов
Анализ иммунофенотипов клеток по их маркерам облегчается с помощью моноклональных антител, давших возможность выделить множество кластеров (скоплений) антигенов дифференцировки (CD).
Казалось бы, о состоянии системы крови можно и нужно судить по общему анализу – с детства известной рутинной медицинской процедуре. Но на самом деле, данные этого анализа — отражение процессов, происходящих в кроветворной системе, и ее главном органе – костном мозге. Поэтому при подозрении на болезнь кроветворной системы анализируют состояние костного мозга. Пункция костного мозга – это вмешательство, которое позволяет получить 0,5-1мл. этой субстанции для дальнейшего исследования.
Что такое костный мозг и зачем его изучают?
Красный костный мозг находится в плоских костях – ребрах, грудине, позвонках, костях черепа и таза – и в эпифизах (концевых частях) трубчатых костей. Он состоит из двух типов клеток – стромы, или, говоря простым языком, основной структуры, и кроветворных ростков из которых, собственно, и формируются форменные элементы: эритроциты, лейкоциты и тромбоциты.

Все элементы крови развиваются из одинаковых стволовых клеток-предшественников. Созревая (в медицине этот процесс называется дифференцировкой), клетки формируют два ростка кроветворения: лимфоидный, из которого потом созревают лимфоциты и миелоидный, создающий остальные форменные элементы. Незрелые клетки крови называются бластами. Обычно 90% всех стволовых клеток находятся в состоянии покоя.
В организме взрослого мужчины в сутки созревает 300г. форменных элементов крови, то есть 9 кг за год и около 7 тонн за 70 лет жизни. Новые клетки формируются взамен состарившихся или погибших по другим причинам (например, в борьбе с инфекциями).
В норме количество вновь созревших клеток строго равно числу погибших. При гемобластозах (лейкозах) клетки кроветворного ростка мутируют, перестают реагировать на регуляторные сигналы организма, и начинают бесконтрольно делиться. Если активность этого процесса настолько велика, что вновь сформированные клетки не успевают созреть, лейкоз называется острым. Если преобладают зрелые формы – хроническим.
Прежде чем выйти в кровоток, измененные лейкозные клетки накапливаются в красном костном мозге. И только инфильтрировав (заполонив) его, поступают сосуды. Изменения в анализе крови далеко не всегда соответствуют происходящему в костном мозге: на некоторых стадиях развития лейкоза количество форменных элементов в крови может не только не увеличиваться, но и уменьшаться.
Именно по этим причинам пункцию костного мозга и миелограммы выполняют при подозрении на любые болезни кроветворной системы.
Как и для чего выполняют пункцию костного мозга?
Чтобы получить материал для исследования, нужно проткнуть (пунктировать) кость там, где она находится близко к коже. В зависимости от возраста (а количество костного мозга в разных анатомических структурах изменяется со временем), это могут быть:
- у детей младше 2 лет – пяточная или большеберцовая кость;
- у детей старшего возраста – гребень подвздошной кости;
- у взрослых – грудина или гребень подвздошной кости.
Прокол делают специальной иглой с ограничителем – иглой Кассирского. 
Она может выглядеть по-разному. Но суть в том, что ограничитель позволяет зафиксировать глубину прокола.
Иногда полученный материал бывает неинформативен. Тогда (и при некоторых других показаниях) делается трепанобиопсия – метод, при котором специальной толстой иглой одним блоком забирают не только красный костный мозг, но и участок костного фрагмента над ним. Такую биопсию обычно делают в области гребня подвздошной кости.

Место прокола закрывается стерильной повязкой или пластырем. Боль может беспокоить и некоторое время после процедуры. Если нет противопоказаний, можно принять обезболивающие. Место прокола нельзя мочить в течение суток, соответственно, не рекомендуют принимать душ или ванну. Какого-то дополнительного ухода после пункции костного мозга не требуется.
Процедура эта безопасна, единственное абсолютное противопоказание – тяжелые нарушения свертывающей системы крови, когда любая травма приводит к обширным гематомам. Относительные противопоказания (когда сравнивают возможную пользу и вред), это:
- острый инфаркт миокарда;
- декомпенсированная сердечнососудистая патология;
- декомпенсированный сахарный диабет;
- гнойные поражения кожи в области предполагаемой пункции.
- кровотечение;
- инфицирование;
- аллергия – при непереносимости обезболивающих средств;
- сквозной прокол грудины, перелом (если пункция выполняется из грудины).
Вероятность осложнений невелика – по данным Британского общества гематологов за время с 1995 по 2001 год на 54890 проведенных пункций пришлось 26 осложнений разной степени тяжести.
Расшифровка и оценка результатов: миелограмма.
В первую очередь, в счетной камере подсчитываются мегакариоциты и миелокариоциты.
Мегакариоциты – это крупные клетки с большими ядрами, предшественники тромбоцитов. Их должно быть более 20, но менее 50 в 1 мкл.
Далее в окрашенных мазках подсчитывают процентные соотношения клеток различных рядов кроветворения. Полученный результат называется миелограммой.

Чтобы оценить по миелограмме качество костного мозга, важно знать не только процентное и количественное содержание гемопоэтических (кроветворных) элементов, но и их соотношение. Вот расшифровка некоторых показателей.
Высчитывается по формуле: (Промиелоциты + миелоциты + метамиелоциты) / (Палочкоядерные + сегментоядерные нейтрофилы). Нормальное значение 0,6 – 0,8.
Формула расчета: (Полихроматофильные + оксифильные нормобласты) / (Все ядросодержащие клетки красного ростка этого пунктата). Норма 0.8 – 0.9 и снижение индекса говорит о чрезмерно медленном наполнении гемоглобином эритроцитов (например, при железодефицитной анемии).
Как и у любого инструментального исследования, референсные значения (нормы) миелограммы могут изменяться в зависимости от лаборатории и используемых аппаратов.
Особенности миелограммы при лейкозах.
Как при остром, так и при хроническом лейкозе усиленный рост патологических клеток сопровождается уменьшением количества эритроцитов и тромбоцитов на всех стадиях созревания.
Если в миелограмме видны признаки лейкоза, пунктат костного мозга дополнительно проходит иммуногистохимическое, цитохимическое и генотипическое исследования – они нужны чтобы определить характерные особенности мутации опухолевого клона. Это важно для выбора схемы лечения конкретного пациента.
Это крайне опасное состояние для здоровья и жизни. Если страдает концентрации лимфоцитов или лейкоцитов — наблюдается снижение иммунитета. Возможна гибель от простой простуды. Таких вариантов десятки и все имеют неблагоприятный исход.
Потому –то так важно своевременно обнаружить патологический процесс и начать его лечение, сначала симптоматическое, поскольку причины зачастую установить невозможно.
Прогнозы во всех случаях довольно туманны. Конечные перспективы зависят от типа патологического процесса, его агрессивности, скорости развития и формы.
Занимается расстройством врач-гематолог. По потребности привлекают онкологов и прочих специалистов.
Разновидности острого лейкоза
В зависимости от того, какие клетки поражаются (миелопоэзного или лимфопоэзного ростка), выделяют два основных вида острого лейкоза:
- ОЛЛ – острый лимфобластный лейкоз.
- ОМЛ – острый миелобластный лейкоз.
ОЛЛ чаще развивается у детей (80% всех острых лейкозов), а ОМЛ – у людей старшего возраста.
Существует и более детальная классификация острых лейкозов, которая учитывает морфологические и цитологические особенности бластов. Точное определение вида и подвида лейкоза необходимо врачам для выбора тактики лечения и составления прогноза для больного.
Стадии заболевания
В отличие от большинства раковых заболеваний органов, лейкозы имеют три основных стадии.
- На первом этапе мутация только начинает развиваться, у человека появляются первые признаки болезни, а состав крови еще не успел слишком сильно измениться. Лечение наиболее простое, а прогнозы благоприятнее, чем на остальных стадиях, но диагностика может быть затруднена.
- Вторая стадия называется развернутой. Происходит нарастание симптоматики, начинает страдать иммунитет, возможно образование метастазов в органах. На этом этапе лейкозы также поддаются лечению: можно добиться временной или стойкой ремиссии.
- Третья стадия – терминальная. Мутации становятся необратимыми, возможна только поддерживающая терапия.
Наиболее хорошие результаты дает вмешательство на ранних этапах, так что знать, что такое лейкемия крови и как она себя проявляет, необходимо не только врачам. Своевременный поход к врачу существенно увеличивает шансы.
Причины острых лейкозов
Изучение проблемы острых лейкозов – это одно из приоритетных направлений современной медицинской науки. Но, не смотря на многочисленные исследования, точные причины возникновения лейкемий до сих пор не установлены. Ясно лишь то, что развитие недуга тесно связано с факторами, способными вызывать мутацию клеток. К таким факторам можно отнести:
- Наследственную склонность. Некоторые варианты ОЛЛ практически в 100% случаев развиваются у обоих близнецов. Кроме того, не редкими являются случаи возникновения острой лейкемии у нескольких членов семьи.
- Воздействие химических веществ (в частности бензола). ОМЛ может развиться после химиотерапии, проведенной по поводу другого заболевания.
- Радиоактивное облучение.
- Гематологические заболевания – апластическую анемию, миелодисплазию и т.п.
- Вирусные инфекции, а вероятнее всего аномальный иммунный ответ на них.
Однако в большинстве случаев острой лейкемии врачам так и не удается выявить факторы, спровоцировавшие мутацию клеток.
Симптомы острого лейкоза
В течение острого лейкоза выделяют пять стадий:
- Предлейкоз, который часто остается незамеченным.
- Первую атаку – острую стадию.
- Ремиссию (полную или неполную).
- Рецидив (первый, повторный).
- Терминальную стадию.
С момента мутации первой стволовой клетки (а именно с одной клетки все и начинается) до появления симптомов острого лейкоза в среднем проходит 2 месяца. За это время в костном мозге накапливаются бластные клетки, не дающие созревать и выходить в кровяное русло нормальным форменным элементам крови, вследствие чего появляются характерные клинические симптомы недуга.
- Лихорадка.
- Ухудшение аппетита.
- Боль в костях и суставах.
- Бледность кожи.
- Повышенная кровоточивость (геморрагии на коже и слизистых, носовые кровотечения).
- Безболезненное увеличение лимфатических узлов.
Эти признаки очень напоминают острую вирусную инфекцию, поэтому не редко больных лечат от нее, а в ходе обследования (включающего общий анализ крови) обнаруживают ряд изменений, характерных для острого лейкоза.
В целом картина болезни при острой лейкемии определяется доминирующим синдромом, их выделяют несколько:
- Анемический (слабость, одышка, бледность).
- Интоксикационный (ухудшение аппетита, лихорадка, снижение массы, потливость, сонливость).
- Геморрагический (гематомы, петехиальная сыпь на коже, кровотечения, кровоточивость десен).
- Костно-суставный (инфильтрация надкостницы и суставной капсулы, остеопороз, асептический некроз).
- Пролиферативный (увеличение лимфатических узлов, селезенки, печени).
Помимо этого, очень часто при острых лейкозах развиваются инфекционные осложнения, причиной которых является иммунодефицит (в крови недостаточно зрелых лимфоцитов и лейкоцитов), реже – нейролейкемия (метастазирование лейкозных клеток в головной мозг, которое протекать по типу менингита или энцефалита).
Описанные выше симптомы нельзя оставлять без внимания, поскольку своевременное выявление острого лейкоза значительно повышает эффективность противоопухолевого лечения и дает шанс больному на полное выздоровление.
Симптоматика
Лейкоз на разных этапах своего развития проявляет себя по-разному. Кстати, именно от стадии рака крови зависит, сколько живут больные. На первоначальном этапе болезнь острого типа проявляет себя таким образом:
Чаще всего на начальных стадиях заболевание редко диагностируется, потому симптомы очень схожи с другими, менее опасными состояниями.
Изменения клеток крови при наличии рака
Когда же болезнь набирает обороты, то появляются более серьезные признаки, например: тошнота, которая время от времени сопровождается головокружениями и рвотными позывами, внезапные случаи укачивания в транспорте, интенсивное выделение пота ночью, ну и то, что нельзя не заметить – стремительное снижение массы тела.
Приведенные ниже признаки свидетельствуют о том, что рак крови острого типа перешел в свою последнюю и самую опасную 4 стадию, в условиях которой сколько живут, зависит от скорости оказанной медицинской помощи. В данном случае показатель выживаемости близится к нулю. Итак, больному требуется срочная госпитализация, если у него:
- синеют губы и ноги;
- модифицируются все уровни сознания;
- ощущается боль в сердце, в виде тесноты и давления в груди;
- температура тела выше 38 градусов;
- ЧСС зашкаливает;
- в брюшной полости ощущаются толчки;
- сильно течет кровь и не останавливается.
Диагностика острого лейкоза
Диагностика острой лейкемии состоит из нескольких этапов:
- На первом этапе проводится общий анализ крови (в динамике). Повторные исследования необходимы для исключения ошибки. В анализе больных острым лейкоза обнаруживается изменение соотношения клеточных элементов и появление бластов.
- Следующий этап диагностики, который проводится в специализированном онкогематологическом отделении, заключается в исследовании костного мозга с обязательным цитохимическим анализом (окрашиванием мазков крови и костного мозга специальными красителями, которые позволяют продифференцировать клетки и установить вид лейкоза). Далее для уточнения диагноза проводится иммунофенотипирование бластов, а также цитогенетический анализ для выявления хромосомных аномалий. По рекомендациям ВОЗ, диагноз острый лейкоз ставится при обнаружении в костном мозге более 20% бластных клеток.
- Третий этап диагностики – определение степени вовлечения в патологический процесс внутренних органов. Для этого проводится рентгенография грудной клетки, УЗИ внутренних органов, диагностическая люмбальная пункция и другие исследования при наличии показаний.
Лечение острого лейкоза
Существует два метода лечения острых лейкозов: многокомпонентная химиотерапия и трансплантация костного мозга. Протоколы лечения (схемы назначения лекарственных препаратов) при ОЛЛ и ОМЛ применяются различные.
Первый этап химиотерапии – это индукция ремиссии, основная цель которой заключается в уменьшении количества бластных клеток до необнаруживаемого доступными методами диагностики уровня. Второй этап – консолидация, направленная на ликвидацию оставшихся лейкозных клеток. За этим этапом следует реиндукция – повторение этапа индукции. Помимо этого, обязательным элементом лечения является поддерживающая терапия оральными цитостатиками.
Выбор протокола в каждом конкретном клиническом случае зависит от того, в какую группу риска входит больной (играет роль возраст человека, генетические особенности заболевания, количество лейкоцитов в крови, реакция на проводимое ранее лечение и т.п.). Общая длительность химиотерапии при острых лейкозах составляет около 2 лет.
Критерии полной ремиссии острой лейкемии (все они должны присутствовать одновременно):
- отсутствие клинических симптомов недуга;
- обнаружение в костном мозге не более 5% бластных клеток и нормальное соотношение клеток других ростков кроветворения;
- отсутствие бластов в периферической крови;
- отсутствие экстрамедуллярных (то есть расположенных за пределами костного мозга) очагов поражения.
Химиотерапия, хотя и направлена на излечение больного, очень негативно действует на организм, поскольку токсична. Поэтому на ее фоне у больных начинают выпадать волосы, появляется тошнота, рвота, нарушения функционирования сердца, почек, печени. Чтобы своевременно выявлять побочные действия лечения и следить за эффективностью терапии, всем больным необходимо регулярно сдавать анализы крови, проходить исследования костного мозга, биохимический анализ крови, ЭКГ, ЭхоКГ и т.д. После завершения лечения больные также должны оставаться под медицинским наблюдением (амбулаторным).
Немаловажное значение в лечении острых лейкозов имеет сопутствующая терапия, которая назначается в зависимости от появившихся у больного симптомов. Пациентам может потребоваться переливание препаратов крови, назначение антибиотиков, дезинтоксикационное лечение для уменьшения интоксикации, обусловленной заболеванием и применяемыми химиопрепаратами. Помимо этого, при наличии показаний проводится профилактическое облучение головного мозга и эндолюмбальное введение цитостатиков для предупреждения неврологических осложнений.
Также очень важен правильный уход за больными. Их необходимо оберегать от инфекций, создавая условия жизни, наиболее приближенные к стерильным, исключая контакты с потенциально заразными людьми и т.д.
Путь к излечению
Лечение включает в себя три этапа. Первый подразумевает интенсивную терапию нарушений костномозгового кровоснабжения. Химиотерапия помогает ликвидировать бластные клетки. Конечно, цитостатики небезопасны, однако альтернативу ещё не разработали.
Затем следует закрепление ремиссии, длящееся около полугода. Пациенту назначаются процедуры и препараты, направленные на предотвращение размножения раковых клеток, от которых не удалось избавиться в процессе химиотерапии. Последний этап подразумевает поддерживающую терапию.
Грамотное лечение действительно способно продлить жизнь. Есть немало людей, которых не сломило даже такое тяжелое заболевание, как острый лейкоз крови. Сколько живут, отзывы врачей и пациентов не помогут установить однозначно, но важно помнить, что с этим недугом стоит бороться, не сдаваясь. И тогда рак отступит.
Когда у взрослого человека диагностируют рак, это потрясение и большое горе, но если онкология обнаруживается у ребёнка — это огромная трагедия. Лейкемия или лейкоз — это рак крови, при котором поражается костный мозг и система кроветворения. Из-за одной мутирующей клетки, превратившейся в злокачественную, которая беспрерывно делится, вытесняя собой здоровые. Различают две формы течения болезни хроническую и острую, вторая в большинстве случаев развивается именно у детей. Ежегодно в Российской Федерации диагностируют лейкемию примерно у пяти тысяч детей и подростков, в возрасте до 18 лет. В среднем, эта цифра составляет 15-17 человек на сто тысяч населения.
Трансплантация костного мозга
Больным острыми лейкозами пересаживают костный мозг, потому что только в нем есть стволовые клетки, которые могут стать родоначальниками форменных элементов крови. Трансплантация, проводимая таким пациентам, должна быть аллогенной, то есть от родственного или неродственного совместимого донора. Показана эта лечебная процедура и при ОЛЛ, и при ОМЛ, причем пересадку желательно осуществлять во время первой ремиссии, особенно если есть высокий риск рецидива – возвращения болезни.
При первом рецидиве ОМЛ трансплантация вообще является единственным спасением, поскольку выбор консервативного лечения в таких случаях весьма ограничен и часто сводится к паллиативной терапии (направленной на улучшение качества жизни и облегчение состояния умирающего человека).
Противопоказания к трансплантации костного мозга:
- Серьезные нарушения функции внутренних органов.
- Острые инфекционные заболевания.
- Рецидив лейкоза, неподдающийся лечению.
- Пожилой возраст.
Лечебная тактика
Лечение проводят в стерильных условиях стационара, потому что пациент особо подвержен бактериям и инфекциям. Необходима обработка ротовой полости, половых органов и пролежней для предотвращения присоединения патогенной микрофлоры.
Клинические рекомендации основываются на соблюдении высококалорийной богатой витаминами диете. Пища не должна вызывать брожения. Исключаются жирные сорта мяса, копчёная и жареная пища. Строго запрещено употребление спиртосодержащих напитков. Разрешено есть растительную пищу после термической обработки, варёную рыбу и птицу, каши и травяные чаи.
Основное лечение заключается в проведении комплексной химиотерапии, продолжительность которой занимает до 6-ти недель. После достижения ремиссии курс приёма препаратов продолжается в домашних условиях. Следующие 3 года пациент принимает противорецидивные лекарства.
При вторичных новообразованиях применяют лучевую терапию. Метод уничтожает аномальные клетки и устраняет болевые ощущения в теле больного.
Действия врачей направлены на достижение ремиссии, закрепление результата и поддержание эффекта.
Масштабное развитие атипичных клеток и полное поражение костного мозга требует трансплантации донорского материала. Метод проводят путём интенсивной химиотерапии, направленной на уничтожение собственного кроветворного органа. В этот период человек лишается иммунитета и организм не в силах бороться с простейшими инфекциями. Поэтому пациента содержат в специализированном стерильном блоке, доступ в который имеет только медперсонал. Помещение обрабатывается дезинфицирующими средствами. Малейший контакт с внешним миром может стать причиной скоропостижной смерти.
Забор донорского материала проводят из кости бедра или ребра. Введение новых клеток происходит как при переливании крови. Катетер вводят в артерию.
Донорами могут стать близкие родственники или посторонние люди, однако подходящий биоматериал тяжело найти. Для этой роли лучше всего подходят однояйцевые близнецы.
Процент выживших после проведения трансплантации – 50%. Организм остальных пациентов не принимает чужой материал, и развиваются осложнения.
Прогноз при лейкозе
На прогноз влияют следующие факторы:
- возраст больного;
- вид и подвид лейкоза;
- цитогенетические особенности заболевания (например, наличие филадельфийской хромосомы);
- реакция организма на химиотерапию.
Прогноз у детей с острой лейкемией намного лучше, чем у взрослых. Связано это, во-первых, с более высокой реактогенностью детского организма на лечение, а во-вторых, с наличием у пожилых пациентов массы сопутствующих заболеваний, не позволяющих проводить полноценную химиотерапию. Кроме того, взрослые пациенты чаще обращаются к врачам, когда заболевание уже запущенно, к здоровью же детей родители относятся обычно более ответственно.
Если же оперировать цифрами, то пятилетняя выживаемость при ОЛЛ у детей, по разным данным, составляет от 65 до 85%, у взрослых – от 20 до 40%. При ОМЛ прогноз несколько отличается: пятилетняя выживаемость отмечается у 40-60% пациентов моложе 55 лет, и всего у 20 % больных старшего возраста.
Подводя итог, хочется отметить, что острый лейкоз – это тяжелая болезнь, но излечимая. Эффективность современных протоколов ее лечения достаточно высокая, а рецидивы недуга после пятилетней ремиссии практически никогда не возникают.
Зубкова Ольга Сергеевна, медицинский обозреватель, врач-эпидемиолог
39, всего, сегодня
(51 голос., средний: 4,45 из 5)
На заметку
Достижения отечественной онкогематологии, прежде всего детской, стали возможны благодаря вниманию государства к этой отрасли медицины.
В России программы неродственного донорства костного мозга только зарождаются — такие пересадки стали делать всего лет 10 назад. В масштабах страны их ничтожно мало — не более 70–80 в год. Всего в стране 13 клиник имеют лицензии на трансплантацию, и есть 70–75 сертифицированных врачей-гематологов, онкологов и трансфузиологов, которые могут проводить эту процедуру. Одно из самых крупных отделений трансплантации — открывшийся в 2011 году в Москве Научно-клинический центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачёва.
Читайте также:

