Клоны клеток злокачественных новообразований
1.1. Характерные признаки опухолевой клетки
Злокачественные новообразования возникают в результате неограниченной пролиферации клеточного клона, выходящего за пределы собственной ткани и способного к росту на территориях других тканей. При этом в силу высокой генетической изменчивости и селекции, происходящей под давлением со стороны организма, в популяции клеток такого клона постоянно возникают и отбираются все более и более автономные и агрессивные субклоны, что описывается термином опухолевая прогрессия. В результате довольно длительной эволюции неопластического клона формируется опухоль, способная убить организм. В последнее десятилетие был достигнут значительный прогресс как в идентификации генов, нарушения функции которых ведут к развитию новообразований, так и в выяснении роли белковых продуктов таких генов в физиологии клетки. Все это позволило выделить ряд важнейших свойств, приобретение которых предопределяет способность клетки образовывать злокачественную опухоль (Рис.1).
Важнейшие свойства неопластической клетки, приобретаемые в ходе опухолевой прогрессии и обеспечивающие злокачественный рост. (Объяснения в тексте).
Во-первых, это пониженная потребность во внешних сигналах для инициации и поддержания клеточной пролиферации - так называемая самодостаточность в пролиферативных сигналах. Данное положение может быть проиллюстрировано двумя примерами (Рис. 2). При культивировании in vitro большинство типов нормальных клеток размножается лишь при условии, если питательная среда содержит 10-20% сыворотки, т.е. при довольно значительном содержании в ней различных ростовых факторов (Рис. 2А). Связывание ростовых факторов со своими рецепторами инициирует передачу сигналов внутри клетки, приводящую к репликации ДНК и делению клетки. Оказалось, что многие типы опухолевых клеток способны размножаться в среде с 1% и даже 0,1% сыворотки, т.е. при содержании ростовых факторов в десятки и сотни раз меньшем, чем необходимо для стимуляции размножения нормальных клеток. Такая пониженная потребность в растворимых ростовых факторах достигается изменениями в системах внутриклеточной сигнализации, которые либо вызывают секрецию необходимых факторов роста самими трансформированными клетками, либо резко увеличивают количество рецепторов для необходимых факторов роста, либо запускают в отсутствии ростового фактора каскад событий, аналогичный тому, который в норме инициируется связыванием ростового фактора со своим рецептором.
Другим примером пониженной потребности неопластических клеток во внешних пролиферативных сигналах является их так называемая независимость от субстрата (anchorage-independence) - Рис. 2Б. Большинство типов нормальных клеток способны размножаться лишь при условии их прикрепления к определенному внеклеточному матриксу. Например, фибробласты начинают делиться при взаимодействии с фибронектином. В ином случае пролиферативный стимул, исходящий от растворимых ростовых факторов, не вызывает полноценного каскада передачи внутриклеточных сигналов, необходимого для стимуляции размножения клеток. Многие типы опухолевых клеток, в отличие от их нормальных предшественников, способны пролиферировать, не прикрепляясь к субстрату, например, в полужидкой среде. Эти два примера показывают, что неопластические клетки приобретают способность генерировать внутри себя пролиферативные сигналы, в норме исходящие от внешних стимулов.
Вторым важнейшим приобретенным свойством неопластических клеток является их пониженная чувствительность к рост-ингибирующим сигналам. Как известно, в организме существует множество антипролиферативных сигналов, поддерживающих определенное число клеток в каждой из тканей. Такие сигналы генерируются как секретируемыми растворимыми факторами (цитокинами), так и взаимодействиями клеток с внеклеточным матриксом и друг с другом. Классическим примером здесь является так называемое контактное торможение размножения клеток в культурах in vitro. (Рис. 2В).
Наряду с этим, опухолевые клетки, как правило, значительно менее чувствительны к действию рост-ингибирующих цитокинов, факторов специфического и неспецифического противоопухолевого иммунитета, а кроме того, не останавливают свою пролиферацию при ДНК-повреждающих воздействиях или неблагоприятных условиях - недостатке пула нуклеотидов, гипоксии и т.д.
Еще одним важнейшим свойством опухолевых клеток является отсутствие репликативного старения, или приобретение бессмертия (иммортализация). Как известно, существует механизм, ограничивающий число делений большинства типов зрелых клеток человека. Так, в культурах человеческих фибробластов in vitro после 60-80 делений (так называемое число Хейфлика) наблюдается необратимая остановка размножения клеток и их постепенная гибель. Между тем, чтобы образовать из одной клетки-родоначальницы сначала опухоль, а затем и метастазы, в условиях жесткого давления со стороны организма, когда многие опухолевые клетки погибают, может потребоваться большее число делений. И, действительно, в опухолевых клетках наблюдается нарушение работы такого "счетно-ограничительного" механизма контроля репликации.
Следующим важным свойством неопластических клеток является ослабление индукции в них апоптоза. Апоптоз представляет собой активный механизм клеточного самоубийства, поддерживающий в организме определенное число клеток и, кроме того, защищающий его от накопления аномальных клеточных вариантов. Он вызывается как физиологическими сигналами (связыванием специфических киллерных цитокинов со своими рецепторами), так и различными внутриклеточными повреждениями или неблагоприятными условиями, в частности нарушениями структуры ДНК, нехваткой ростовых факторов, гипоксией и т.д. Уход от апоптоза резко повышает жизнеспособность неопластической клетки, делает ее менее чувствительной к факторам противоопухолевого иммунитета и терапевтическим воздействиям.
К важнейшим приобретенным свойствам опухолевых клеток принадлежит и их способность стимулировать неоангиогенез, т.е. формировать новые кровеносные и лимфатические сосуды из эндотелиальных клеток предсуществующих окружающих мелких сосудов. Это необходимое условие для дальнейшего роста опухолевого узелка, достигшего в диаметре 2-4 мм. В ином случае клетки в центре опухоли, не получая кислород и питательные вещества, будут погибать.
Важнейшим свойством опухолевых клеток являются и изменения морфологии и движения клеток. В основе морфологических нарушений лежат взаимосвязанные между собой изменения цитоскелета, адгезионных взаимодействий клеток друг с другом и с внеклеточным матриксом. Вкратце, они выражаются в нарушении формирования фокальных контактов и ухудшении прикрепления клеток к внеклеточному матриксу, дезорганизации системы актиновых микрофиламентов. Это приводит к изменениям активности псевдоподий и подвижности. В целом, наблюдаемая картина напоминает изменения, возникающие в нормальных клетках при действии мотогенных цитокинов - факторов, стимулирующих миграцию клеток. Однако так называемый локомоторный фенотип в неопластических клетках, как правило, сильно утрирован, что позволяет различать по морфологии опухолевую клетку от движущейся нормальной клетки. Необходимо подчеркнуть, что именно эти нарушения, вместе с некоторыми другими свойствами, в частности способностью секретировать протеолитические энзимы, предопределяют приобретение неопластическими клетками двух свойств, лежащих в основе злокачественного роста: способность к инвазии, т.е. проникновению в окружающие здоровые ткани, и сопряженную с ней способность к метастазированию - образованию вторичных очагов опухолевого роста. Метастазирование - наиболее опасное проявление опухолевой прогрессии, являющееся основной причиной смерти онкологических больных. Чтобы дать метастаз клетка должна приобрести ряд свойств: умение проникать в глубину окружающих нормальных тканей, в том числе в кровеносные или лимфатические сосуды; способность выживать после попадания в сосуды, а затем - выходить из них и размножаться в несвойственном для данного типа клеток микроокружении, давая новый очаг опухолевого роста. Таким образом, способность к метастазированию складывается из комплекса более простых признаков, таких как приобретение локомоторного фенотипа, способности стимулировать образование новых кровеносных и лимфатических сосудов, создавая тем самым пути эвакуации опухолевых клеток из первичного очага, возникновение независимости от субстрата, подавление апоптоза и т.д. Появление каждого из этих свойств увеличивает метастатический потенциал клетки.
Для многих опухолевых клеток характерны и нарушения клеточной дифференцировки, т.е. образования специализированных типов клеток, синтезирующих специфические белки. Особенно ярко это проявляется в гемобластозах, новообразованиях из кроветворных тканей, при которых их клетки оказываются как бы замороженными на той или иной стадии созревания. Общепринятым является представление, согласно которому меньшая зрелость лейкозных клеток является не следствием дедифференцировки зрелых клеток, претерпевших неопластическую трансформацию, а отражает их происхождение из незрелых клеток, в которых блокированы процессы дальнейшей дифференцировки. Следует заметить, однако, что это свойство не является универсальным: во многих типах опухолей наблюдается сохранение способности к дифференцировке, причем в отличие от лейкозов созревание клеток не препятствует приобретению злокачественного фенотипа. Примерами этого могут служить плоскоклеточный ороговевающий рак кожи и высокодифференцированные аденокарциномы толстой кишки, происходящие из незрелых клеток, которые сначала несколько раз делятся, а затем дифференцируются (Рис. 3).
Происхождение из незрелых клеток не противоречит представлению о том, что опухолевые клетки в ходе прогрессии могут претерпевать определенную дедифференцировку, утрачивая в первую очередь те дифференцировочные белки, отсутствие которых придает клеткам селективные преимущества (например, рецепторы стероидных гормонов в раках молочной железы и т.д.).
Рис.3. Модели, объясняющие происхождение новообразований из незрелых клеток определенной стадии дифференцировки, в которых либо сохранена (внизу слева), либо блокирована (внизу справа) способность к дальнейшему созреванию.
И, наконец, важнейшим признаком неопластических клеток является их генетическая нестабильность. Очевидно, что канцерогенез - многоступенчатый процесс накопления мутаций и других генетических изменений, приводящих к нарушениям регуляции размножения и миграции клеток, понижению их чувствительности к различным рост-супрессирующим сигналам, ослаблению индукции в них апоптоза, блокированию дифференцировки и т.д. Вероятность возникновения в одной клетке нескольких генетических изменений, придающих совокупность вышеуказанных свойств, резко повышается при нарушениях работы систем, поддерживающих целостность генома. Поэтому мутации, ведущие к генетической нестабильности, также являются неотъемлемым этапом опухолевой прогрессии. Генетическая нестабильность неопластических клеток базируется на уменьшении точности воспроизведения генетического аппарата, нарушениях механизмов репарации ДНК и изменениях регуляции клеточного цикла в поврежденных клетках. Это, вместе с уходом от апоптоза, позволяющим генетически измененным клеткам выживать, делает популяции опухолевых клеток высоко изменчивыми, создает основу для постоянного возникновения и отбора все более и более злокачественных вариантов. Таким образом, генетическая нестабильность является двигателем неуклонной опухолевой прогрессии.
- Чем раковые клетки отличаются от нормальных?
- Каковы причины появления раковых клеток?
- Какие бывают типы генов рака?
- Основные характеристики и строение раковых клеток
- Как выглядят раковые клетки под микроскопом?
- Как развиваются раковые клетки, какие этапы проходят в своем развитии?
- Ликвидация раковых клеток: что помогает их уничтожить?

Чем раковые клетки отличаются от нормальных?
Для того чтобы организм человека правильно работал как единое целое, каждая клетка в нем должна подчиняться общим правилам и обладать некоторыми основополагающими свойствами:
Не перестает размножаться. Сколько бы своих копий ни создала опухолевая клетка, она не останавится. Злокачественная опухоль постоянно растет и распространяется в организме.
Не специализируются. Раковая клетка не становится специализированной и не выполняет полезные для организма функции. Процесс клеточной специализации называется дифференцировкой. Чем ниже степень дифференцировки, тем агрессивнее ведет себя рак.
Каковы причины появления раковых клеток?
Почему в теле конкретного человека возникли раковые клетки — вопрос во многом риторический.
Каждая живая клетка функционирует и размножается в соответствии с заложенной в ней генетической информацией. При возникновении определенных мутаций эти тонкие механизмы регуляции сбиваются, и может произойти злокачественное перерождение.
Сложно сказать, что именно привело к таким мутациям в каждом конкретном случае. Современным врачам и ученым известны лишь факторы риска, которые повышают вероятность злокачественного перерождения и развития заболевания. Вот основные из них:
- Неблагоприятная экологическая ситуация.
- Курение.
- Чрезмерное употребление алкоголя.
- Профессиональные вредности, контакт с канцерогенными веществами и различными излучениями на производстве.
- Ожирение, избыточная масса тела.
- Ультрафиолетовое излучение солнца и соляриев.
- Малоподвижный образ жизни.
- Возраст: со временем мутации накапливаются, поэтому вероятность возникновения в организме раковых клеток повышена у пожилых людей.
- Нездоровое питание: преобладание в рационе животных жиров, красного и обработанного мяса.
Ни один из этих факторов не приводит со стопроцентной вероятностью к развитию злокачественной опухоли.
Какие бывают типы генов рака?
Не все мутации одинаково опасны. К раку приводят те, которые возникают в определенных генах:
Онкогены активируют размножение клеток. Злокачественное перерождение происходит, когда они становятся слишком активны. В качестве примера можно привести ген, который кодирует белок HER2. Этот белок-рецептор находится на поверхности клетки и заставляет ее размножаться.
Мутации, которые приводят к раку, могут быть наследственными (возникают в половых клетках) и соматическими (возникают в клетках тела в течение жизни).

Основные характеристики и строение раковых клеток
Раковые клетки обладают тремя основополагающими характеристиками, за счет которых так опасны онкологические заболевания:
- Способность к бесконтрольному размножению.
- Способность к инвазии — прорастанию в окружающие ткани.
- Способность к метастазированию — распространению в организме и образованию новых очагов в различных органах.
Не всякая опухолевая клетка — раковая. Раком или карциномой называют злокачественные опухоли из эпителиальной ткани, которая выстилает кожу, слизистые оболочки внутренних органов, образует железы. Из соединительной ткани (костной, жировой, мышечной, хрящевой, кровеносных сосудов) развиваются саркомы. Злокачественные заболевания органов кроветворения называют лейкозами. Опухоли из клеток иммунной системы — лимфомы и миеломы.
Как выглядят раковые клетки под микроскопом?
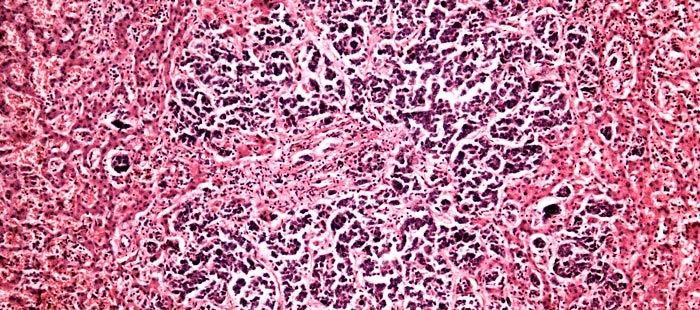
Если коротко, то они сильно отличаются от нормальных, тех, что ожидает увидеть патологоанатом, когда рассматривает под микроскопом фрагмент ткани. Раковые клетки имеют более крупные или мелкие размеры, неправильную форму, аномальное ядро. Если нормальные клетки в одной ткани все примерно одинаковых размеров, то раковые зачастую разные. Ядро содержит очень много ДНК, поэтому оно крупнее (его размеры тоже вариабельны), а при окрашивании специальными веществами выглядит более темным.
Из нормальных клеток образуются определенные структуры, например, железы. Раковые клетки располагаются более хаотично. Например, они образуют железы искаженной, неправильной формы или непонятные массы, которые на железы совсем не похожи.
Как развиваются раковые клетки, какие этапы проходят в своем развитии?
Раковые опухоли растут за счет деления клеток, которые входят в их состав. Во время деления злокачественная клетка образует две своих копии, таким образом, рост происходит в геометрической прогрессии. Например, для того чтобы образовалась опухоль размером 1 см, нужно около 30 удвоений. Через 40 удвоений новообразование достигает веса 1 кг, и этот размер считается критическим, смертельным для пациента.
Согласно современным представлениям, за рост злокачественной опухоли отвечают так называемые стволовые опухолевые клетки. Они активно делятся, в то время как другие опухолевые клетки просто существуют. Современные ученые заняты поиском методов лечения, направленных против этих стволовых клеток.
Время удвоения опухолевых клеток бывает разным. Например, при лейкозе это происходит за 4 дня, а при раковых новообразованиях толстой кишки — за 2 года. Проходит много времени, прежде чем опухоль достигнет настолько больших размеров, что станет проявляться какими-либо симптомами. Например, если у онкологического больного появились некоторые жалобы, и после этого он прожил год, вероятно, опухоль в его организме на момент появления жалоб существовала уже около трех лет, просто он об этом не знал.
Пока раковая опухоль небольшая, ей вполне хватает кислорода. Но по мере роста она все сильнее испытывает кислородное голодание — гипоксию. Чтобы обеспечить свои потребности, опухолевые клетки вырабатывают вещества, которые стимулируют образование кровеносных сосудов — ангиогенез.
По мере роста опухоли происходит инвазия — распространение раковых клеток в окружающие ткани. Они вырабатывают ферменты, которые разрушают нормальные клетки.
Некоторые из них отрываются от материнской опухоли, проникают в кровеносные и лимфатические сосуды, образуют в них вторичные очаги — метастазы. В этом самая главная опасность злокачественных опухолей. Именно метастатические очаги становятся причиной гибели многих онкологических пациентов.
Ликвидация раковых клеток: что помогает их уничтожить?
С раковыми клетками можно бороться разными способами. Например, удалить их из организма хирургическим путем. Но это возможно лишь в случаях, если опухоль не успела сильно распространиться в организме. Даже если можно выполнить радикальную операцию, никогда нет стопроцентной гарантии того, что в организме не остались микроскопические опухолевые очаги, которые в будущем станут причиной рецидива. Поэтому зачастую хирургические вмешательства дополняют адъювантной и неоадьювантной терапией.
Другие методы лечения:
В Европейской клинике применяются наиболее современные оригинальные препараты для борьбы с раком. У нас есть возможность провести молекулярно-генетический анализ опухолевой ткани, разобраться, из-за каких мутаций клетки стали злокачественными, и назначить наиболее эффективную персонализированную терапию. Свяжитесь с нами, мы знаем, как помочь.

Кандидат биологических наук Илья Щеглов.
История онкологии началась с незапамятных времён. Первые систематические попытки лечения опухолей предпринимались ещё в Древнем мире. С тех пор прошло несколько тысячелетий, но и сейчас в подавляющем большинстве случаев полное излечение злокачественных новообразований недостижимо. Однако теперь мы хотя бы знаем, что за преграда не даёт нам достигнуть заветной цели. Раковые стволовые клетки, практически никому не известные ещё каких-нибудь пятнадцать лет назад, сегодня оказались в центре внимания учёных. Выяснилось, что буквально все клинические проблемы, от устойчивости онкологических заболеваний к различным препаратам до фатальных рецидивов спустя десятилетия после кажущегося исцеления, связаны с этими клетками.
Модель раковых стволовых клеток (РСК) подразумевает, что любое злокачественное новообразование (неоплазия) развивается из одной клетки. В результате неких событий генетический аппарат некогда нормальной клетки трансформируется настолько, что происходит её перерождение в инициирующую раковую клетку. В результате последующей пролиферации (деления) этой клетки формируется злокачественная опухоль. Согласно концепции РСК, эта опухоль устроена иерархически, то есть разные типы раковых клеток обладают разной способностью к делению.
Раковые стволовые клетки составляют лишь небольшую популяцию опухолевых клеток. Однако, будучи истинно стволовыми клетками, они (и только они) способны к неограниченному числу делений и постоянному самовоспроизведению. Число делений остальных клеток, если они способны к пролиферации (то есть формально обладают неким стволовым потенциалом), строго ограничено.
В основе процесса самовоспроизведения РСК лежит так называемый асимметричный тип деления стволовых клеток, который заключается в том, что родительская стволовая клетка даёт начало двум клеткам. Одна из них — с такими же стволовыми свойствами, что и материнская, другая же способна к ограниченному числу делений и поэтому называется частично дифференцированной, временно пролиферирующей раковой клеткой. Конечные потомки таких клеток — раковые клетки, не способные к делению. Их называют терминально дифференцированными. Соответственно иерархия опухолевой ткани выглядит так: раковые стволовые клетки → временно пролиферирующие раковые клетки → терминально дифференцированные раковые клетки. Два последних типа клеток образуют при этом основную массу опухоли.
Точно такая же иерархия имеет место и в нормальных тканях, стволовые клетки которых, способные к самовоспроизведению и поддержанию собственной популяции, также дают начало ограниченно пролиферирующим клеткам — предшественникам зрелых клеток. Эти зрелые тканевые клетки не способны к делению вовсе и погибают через какое-то время после выполнения свойственных им функций.
Итак, согласно модели раковых стволовых клеток, не все опухолевые клетки обладают равной способностью к делению и самовоспроизведению. И несмотря на то что основная масса опухоли состоит из злокачественных клеток той или иной степени дифференцировки, её рост и развитие определяются небольшой по численности, но наивысшей в иерархии популяцией раковых стволовых клеток.
Упреждая аргументы критиков РСК-модели, следует отметить, что некоторые злокачественные новообразования не вписываются в эту модель, а, скорее, соответствуют модели клональной эволюции. Есть виды неоплазий, при которых могут встречаться разные популяции раковых стволовых клеток, имеющих разные хромосомные нарушения. Хрестоматийные примеры таких новообразований — хроническая миелоидная лейкемия и колоректальный рак. В этих случаях РСК-модель не может полностью описать развитие опухоли, так как в соответствии с ней все клетки опухоли — потомки одной инициирующей РСК. Здесь же возможна либо инициация опухоли сразу из нескольких злокачественных стволовых клеток, формирующих несколько генетически различающихся клонов, либо эволюция одного клона из другого за счёт последовательного накопления генетических нарушений. Разные клоны могут обладать разной злокачественностью и соответственно могут конкурировать за ресурсы. Иными словами, будет проходить эволюция опухолевых клонов.
Некоторые новообразования, отличающиеся экстремальной злокачественностью, также больше соответствуют модели клональной эволюции, нежели иерархической модели РСК. К ним относятся, например, различные злокачественные меланомы, при которых доля активно делящихся раковых клеток составляет чуть ли не более половины опухолевой массы. При этом в пределах одной опухоли сосуществуют РСК с различными фенотипами, которые при различных воздействиях на опухоль могут легко превращаться один в другой. Очевидно, что и для этих случаев РСК-модель не вполне подходит.
Однако, как можно заметить, в современной интерпретации модели клональной эволюции центральная роль инициирующих раковых стволовых клеток в запуске развития злокачественного новообразования ни в коей мере не оспаривается. Дискуссии продолжаются лишь относительно тех или иных сценариев развития опухоли*. А коли так, мы со спокойной совестью можем говорить о раковых стволовых клетках.
Более полувека спустя, в 1930-х годах, теория зародышевого остатка получила новый импульс. Гистологические наблюдения одной из опухолей мозга — медуллобластомы — показали, что её клетки морфологически очень напоминают клетки эмбрионального мозжечка, на основании чего было выдвинуто предположение, что эта форма опухолей мозга развивается из зародышевого остатка, состоящего из медуллобластов, утративших способность к дифференцировке.
Очередной значительный шаг на пути к концепции раковых стволовых клеток сделан в середине прошлого века. Исследования различных миелопролиферативных заболеваний (особой группы злокачественных новообразований, развившихся из клеток крови**) показали, что в развитие данной группы заболеваний могут быть вовлечены все ветви гемопоэза, за исключением лимфоидных ростков. Это послужило основанием для предположения, что все указанные патологии связаны со злокачественным перерождением клеток — предшественников всех остальных клеток миелоидного ряда, теперь известных как миелоидные cтволовые клетки.
А уже в 1960 году Питер Ноуэл (Peter Nowell) и Дэвид Хангерфорд (David Hungerford) открыли уникальную взаимосвязь так называемой филадельфийской хромосомы с одним из миелопролиферативных заболеваний — хронической миелоидной лейкемией. Филадельфийская хромосома — следствие хромосомной аномалии, которая приводит к образованию мутантного белка BCR-ABL1. К несчастью, этот мутантный белок сохраняет способность одного из своих родительских белков (ABL) к передаче пролиферативного (стимулирующего деление клетки) сигнала внутрь клетки. Более того, он передаёт сигналы гораздо интенсивнее и при этом делится вне зависимости от внешних сигналов. В результате клетки, несущие такую мутацию, начинают быстро и неконтролируемо делиться. В дальнейшем наличие филадельфийской хромосомы при этом заболевании было подтверждено во всех клетках, не относящихся к лимфоидному ряду, на основании чего выдвинули гипотезу о происхождении всех клонов лейкемических клеток от одного предшественника.
Как видно, модель клональной эволюции подразумевает, что одни раковые клоны отличаются большей злокачественностью, другие — меньшей, но в целом все они обладают сопоставимой способностью к делению. И в этом заключается принципиальное отличие стохастической теории канцерогенеза от иерархической теории, которая базируется на модели раковых стволовых клеток.
Тем не менее, как уже было упомянуто выше, модель клональной эволюции до сих пор не потеряла своей актуальности, поскольку в несколько большей степени, нежели модель РСК, объясняет развитие нескольких типов новообразований.
Долгое время концепция РСК находилась на вторых ролях. Однако в 1997 году Доминик Бонне (Dominique Bonnet, London Research Institute) и Джон Дик (John Dick, Toronto General Research Institute) продемонстрировали, что единичные лейкемические стволовые клетки, взятые у пациентов с острой миелоидной лейкемией, при трансплантации мышам дают начало полному спектру клеток с различными злокачественными фенотипами, наблюдаемыми при этом заболевании у человека. После этой работы число исследований, посвящённых РСК, стало лавинообразно нарастать.
В начале 2000-х годов раковые стволовые клетки были идентифицированы и в солидных опухолях (при одной из форм рака молочной железы). На сегодняшний день РСК описаны для абсолютного большинства форм онкологических заболеваний, и с этими клетками связывают все основные клинические проблемы в онкологии.
Поскольку любое новообразование может развиться только из активно делящейся клетки, наиболее подходящие кандидаты для злокачественной трансформации — нормальные тканевые стволовые клетки (дающие начало полностью дифференцированным клеткам, выполняющим свои узкоспецифические задачи в том или ином типе тканей), так как они обладают длительным сроком жизни и высокой скоростью деления. В соответствии с этим концепция РСК подразумевает, что инициирующее событие в канцерогенезе — злокачественное перерождение нормальных тканевых стволовых клеток***, которые становятся инициирующими РСК.
Ещё одна неприятная особенность раковых стволовых клеток — их чрезвычайная устойчивость ко всем известным видам лечения. Какой бы вид противоопухолевой терапии ни применялся (радио-, химио-, иммунотерапия, таргетная), РСК будут погибать последними, когда все дифференцированные раковые клетки уже успешно побеждены.
Известно несколько механизмов терапевтической устойчивости РСК. Во-первых, РСК характеризуются повышенной экспрессией транспортных белков семейства ABC (ATP-binding cassette). Это эволюционно консервативные белки, присутствующие у всех организмов — от бактерий до человека. В норме они локализуются преимущественно в плазматической мембране клеток и отвечают за транспорт полезных веществ (например, витаминов) в клетку и выведение из неё вредных токсинов и ксенобиотиков. В РСК эти белки экспрессируются на особенно высоком уровне и отвечают за выведение из них различных химиотерапевтических препаратов.
Во-вторых, РСК, как никакие другие клетки, отличаются обилием фермента альдегид-дегидрогеназы (ALDH). В норме функция этого белка — окисление токсичных для организма альдегидов до карбоновых кислот. В РСК же он отвечает за инактивацию многих химиотерапевтических препаратов.
Это основные, но далеко не все механизмы устойчивости РСК. В тех же случаях, когда системы резистентности РСК к терапии дают сбой, раковые стволовые клетки впадают в дормантность (состояние покоя), в которой они могут пребывать несколько десятилетий, после чего активируются и обусловливают скоротечный фатальный рецидив. Дормантные РСК отличаются очень низким уровнем метаболизма, экстремальной устойчивостью к повреждающим воздействиям и практически не экспрессируют поверхностные белки, которые могли бы послужить мишенями для создания таргетных препаратов. На сегодняшний день дормантные РСК представляют собой наибольшую трудность для лечения. Однако надежда на успех есть. Во-первых, испытываются и неплохо себя проявляют различные сложные комбинации уже существующих таргетных препаратов. Во-вторых, удалось вплотную приблизиться к получению препаратов, воздействующих на процессы, лежащие в основе образования вторичных метастатических РСК. В-третьих, обнаружены белки, отвечающие за дормантность РСК и обеспечение их жизнеспособности в состоянии покоя. Наконец, разрабатываются препараты, способствующие выходу РСК из дормантности, что делает их более чувствительными к существующим формам терапии.
Cловарик к статье
Клеточная дифференцировка — процесс клеточной дифференцировки заключается в так называемом созревании стволовой клетки-предшественника в клетку со строго определённым фенотипом (например, кардиомиоцит или пирамидный нейрон), называемую дифференцированной.
Пролиферация (от лат. proles — отпрыск, потомство и fero — несу) — разрастание ткани организма путём размножения клеток делением.
Репарация ДНК — внутриклеточная молекулярная система восстановления исходной последовательности ДНК после её повреждений.
Стохастический (от греч. στοχαστικός — умеющий угадывать) означает неопределённость, случайность чего-либо.
Фенотип (от греческого слова phainotip — являю, обнаруживаю) — совокупность характеристик, присущих индивиду на определённой стадии развития (особенности строения и жизнедеятельности).
Комментарии к статье
* Большинство ведущих специалистов сегодня склоняются к мнению, что универсального сценария развития опухоли не существует. Возможна реализация обеих моделей.
*** Само злокачественное перерождение может быть результатом одного или нескольких канцерогенных событий (например, мутаций, но не только их).
Читайте также:

