Клиническими проявлениями анемии при лейкозе являются
Виды лейкозов - острые и хронические
Анатомия и физиология костного мозга
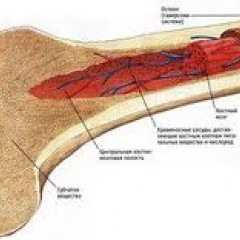
Костный мозг – это ткань находящаяся внутри костей, преимущественно в костях таза. Это самый главный орган, участвующий в процессе кроветворения (рождение новых клеток крови: эритроцитов, лейкоцитов, тромбоцитов). Этот процесс необходим организму, для того чтобы, заменить погибающие клетки крови, новыми. Костный мозг состоит из фиброзной ткани (она образует основу) и кроветворной ткани (клетки крови на разных этапах созревания). Кроветворная ткань включает 3 клеточные линии (эритроцитарный, лейкоцитарный и тромбоцитарный), по которым образуются соответственно 3 группы клеток (эритроциты, лейкоциты и тромбоциты). Общим предком этих клеток, является стволовая клетка, которая запускает процесс кроветворения. Если нарушается процесс образования стволовых клеток или их мутация, то нарушается процесс образования клеток по всем 3 клеточным линиям.
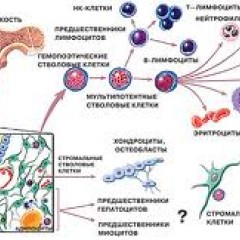
Эритроциты – это красные кровяные клетки, содержат гемоглобин, на нём фиксируется кислород, при помощи которого питаются клетки организма. При недостатке эритроцитов происходит недостаточное насыщение клеток и тканей организма кислородом, в результате чего проявляется различными клиническими симптомами.
Лейкоциты к ним относятся: лимфоциты, моноциты, нейтрофилы, эозинофилы, базофилы. Представляют собой белые клетки крови, они играют роль в защите организма и выработке иммунитета. Их недостаток вызывает снижение иммунитета и развитие различных инфекционных заболеваний.
Тромбоциты – это кровяные пластинки, которые участвуют в образовании тромба. Недостаток тромбоцитов приводит к различным кровотечениям.
Подробнее о видах кровяных клеток читайте в отдельной статье пройдя по ссылке.
Причины лейкоза, факторы риска
Симптомы различных видов лейкозов
- При острых лейкозахотмечаются 4 клинических синдрома:
- Анемический синдром: развивается из-за недостатка выработки эритроцитов, могут присутствовать множество симптомов или некоторые из них. Проявляется в виде усталости, бледности кожи и склер, головокружение, тошнота, быстрое сердцебиение, ломкость ногтей, выпадение волос, патологическое восприятие запаха;
- Геморрагический синдром: развивается в результате недостатка тромбоцитов. Проявляется следующими симптомами: вначале кровотечения из десен, образование синяков, кровоизлияния в слизистые оболочки (язык и другие) или в кожу, в виде мелких точек или пятен. В дальнейшем при прогрессировании лейкоза, развиваются и массивные кровотечения, в результате ДВС синдрома (диссеминированное внутрисосудистое свёртывания крови);
- Синдром инфекционных осложнений с симптомами интоксикации: развивается в результате недостатка лейкоцитов и с последующим снижением иммунитета, повышение температуры тела до 39 0 С, тошнота, рвота, потеря аппетита, резкое снижение веса, головная боль, общая слабость. У больного присоединяются различные инфекции: грипп, пневмония, пиелонефрит, абсцессы, и другие;
- Метастазы - по току крови или лимфы опухолевые клетки попадают в здоровые органы, нарушая их структуру, функции и увеличивая их в размере. В первую очередь метастазы попадают в лимфатические узлы, селезёнку, печень, а потом и в другие органы.
Эритробластный острый лейкоз, поражаются клетки предшественницы, из которых в дальнейшем должны развиться эритроциты. Чаще встречается в пожилом возрасте, характеризуется выраженным анемическим синдромом, не наблюдается увеличение селезёнки, лимфатических узлов. В периферической крови снижено количество эритроцитов, лейкоцитов и тромбоцитов, наличие молодых клеток (эритробластов).
Монобластный острый лейкоз, нарушается выработка лимфоцитов и моноцитов, соответственно они будут снижены в периферической крови. Клинически, проявляется, повышением температуры и присоединением различных инфекций.
Мегакариобластный острый лейкоз, нарушается выработка тромбоцитов. В костном мозге при электронной микроскопии обнаруживают мегакариобласты (молодые клетки, из которых образуются тромбоциты) и увеличенное содержание тромбоцитов. Редкий вариант, но чаще встречается в детском возрасте и обладает неблагоприятным прогнозом.
Хронический миелолейкоз, усиленное образование миелоидных клеток, из которых образуются лейкоциты (нейтрофилы, эозинофилы, базофилы), в результате чего, уровень этих групп клеток будет повышен. Долгое время может протекать бессимптомно. Позже появляются симптомы интоксикации (повышение температуры, общая слабость, головокружение, тошнота), и присоединение симптомов анемии, увеличение селезёнки и печени.
Хронический лимфолейкоз, усиленное образование клеток - предшественниц лимфоцитов, в результате уровень лимфоцитов в крови повышается. Такие лимфоциты не могут выполнять свою функцию (выработка иммунитета), поэтому у больных присоединяются различные виды инфекций, с симптомами интоксикации.
Диагностика лейкоза
- Повышение уровня лактатдегидрогеназы (норма 250 Ед/л);
- Высокий АСАТ (норма до 39 Ед/л);
- Высокая мочевина (норма 7,5 ммоль/л);
- Повышение мочевой кислоты (норма до 400 мкмоль/л);
- Повышение билирубина ˃20мкмоль/л;
- Снижение фибриногена 30%;
- Низкий уровень эритроцитов, лейкоцитов, тромбоцитов.
- Трепанобиопсия (гистологическое исследование биоптата из повздошной кости): не позволяет точно поставить диагноз, а лишь определяет разрастание опухолевых клеток, с вытеснением нормальных клеток.
- Цитохимическое исследование пунктата костного мозга: выявляет специфические ферменты бластов (реакция на пероксидазу, липиды, гликоген, неспецифическую эстеразу), определяет вариант острого лейкоза.
- Иммунологический метод исследования: выявляет специфические поверхностные антигены на клетках, определяет вариант острого лейкоза.
- УЗИ внутренних органов: неспецифический метод, выявляет увеличенные печень, селезёнку и другие внутренние органы с метастазами опухолевых клеток.
- Рентген грудной клетки: является, неспецифическим метом, обнаруживает наличие воспаления в лёгких при присоединении инфекции и увеличенные лимфатические узлы.
Лечение лейкозов
- Полихимиотерапия, применяется с целью противоопухолевого действия:
- Трансфузионная терапия: эритроцитарная масса, тромбоцитарная масса, изотонические растворы, с целью коррекции выраженного анемического синдрома, геморагического синдрома и дезинтоксикации;
- Общеукрепляющая терапия:
- применяется с целью укрепления иммунитета. Дуовит по 1 таблетке 1 раз в день.
- Препараты железа, для коррекции недостатка железа. Сорбифер по 1 таблетке 2 раза в день.
- Иммуномодуляторы повышают реактивность организма. Тималин, внутримышечно по 10-20 мг 1 раз в день, 5 дней, Т-активин, внутримышечно по 100 мкг 1 раз в день, 5 дней;
- Гормонотерапия: Преднизолон в дозе по 50 г в день.
- Антибиотики широкого спектра действия назначаются для лечения присоединяющих инфекций. Имипенем по 1-2 г в сутки.
- Радиотерапия применяется для лечения хронического лейкоза. Облучение увеличенной селезёнки, лимфатических узлов.
Использование солевых повязок с 10% солевым раствором (100 г соли на 1 литр воды). Намочить льняную ткань в горячем растворе, ткань немного сжимать, сложить в четверо, и накладывать на больное место или опухоль, закрепить лейкопластырем.
Настой из измельчённых игл сосны, сухая кожа лука, плоды шиповника, все ингредиенты смешать, залить водой, и довести до кипения. Настоять сутки, процедить и пить вместо воды.
Употреблять соки из красной свеклы, граната, моркови. Кушать тыкву.
Настой из цветков каштана: взять 1 столовую ложку цветков каштана, залить в них 200 г воды, вскипятить и оставить настаиваться на несколько часов. Пить по одному глотку на один приём, необходимо выпить 1 литр в день.
Хорошо помогает в укреплении организма, отвар из листьев и плодов черники. Кипятком примерно 1 литр, залить 5 ложек листьев и плодов черники, настоять несколько часов, выпивать всё за один день, принимать около 3 месяцев.
1.продукция аутоантител к эритроцитам
2.нарушение продукции эритропоэтина
3.нарушение образования эритроцитов в костном мозге *
4.нарушение всасывания железа
5.дефицит витаминов и микроэлементов
Основное различие острых и хронических лейкозов
1. характер начала заболевания
2. продолжительность жизни
3. степень созревания опухолевых клеток*
4. выраженность клинических синдромов
Хронический лимфолейкоз характеризуется
1. относительным лимфоцитозом
2. абсолютным лимфоцитозом в крови более 3х10/л
3. абсолютным лимфоцитозом более 5х10/л
4. абсолютным лимфоцитозом более 10х10/л *
Гемофилии относятся к геморрагическим диатезам, обусловленным
1. нарушением плазменного звена гемостаза *
2. нарушением мегакариоцитарно-тромбоцитарной системы
3. нарушением сосудистой системы
4. сочетанными нарушениями
71) Инфекционный эндокардит это:
1. Аутоиммунное заболевание, поражающее клапанный аппарат сердца
2. Инфекционное заболевание, протекающее по типу сепсиса, поражающее клапанный аппарат сердца*
3. Верны оба положения.
72) Особенность пульса при аортальном стенозе:
1. медленный, малый *
3. высокий, скорый
4. аритмичный, разного наполнения
73) Первая жалоба больного с митральным стенозом:
1. отеки на нижних конечностях
2. отеки на лице
3. увеличение печени
Геморрагический васкулит (болезнь Шенлейн-Геноха) относится к геморрагическим диатезам, обусловленным
1. нарушением плазменного звена гемостаза.
2. нарушением мегакариоцитарно-тромбоцитарной системы
3. нарушением сосудистой системы *
4. сочетанными нарушениями
Клинические признаки тромбоцитопении появляются при уровне тромбоцитов
1. менее 400 х10 9 /л
2. менее 200 х10 9 /л
3. менее 100 х10 9 /л
4. менее 50 х10 9 /л *
76) Механизм (рефлекс) Китаева:
1. спазм легочных артериол*
2. спазм легочных вен
3. дилятация легочных артериол
Повышенное разрушение тромбоцитов при болезни Верльгофа вызвано
1. образованием антитромбоцитарных антител, относящихся к классу IgG. *
2. дефицитом гликопротеинов IIb/IIIa на мембранах тромбоцитов, ведущий к нарушению их взаимодействия с агрегирующими агентами
3. снижением содержания фибриногена в тромбоцитах
4. повышением агрегационных свойств тромбоцитов при нестабильности их мембран
78) Критическим митральный стеноз называется при площади митрального отверстия:
1. при пиелонефрите; *
2. при гломерулонефрите
3. при амилоидозе почек
4. при всех перечисленных заболеваниях
В I триместре беременности для лечения пиелонефрита можно назначить
1. полусинтетические пенициллины; *
4. карбенициллина динатриевую соль.
Для диагностики В12-дефицитной анемии необходимо выявить
1. гиперхромную, гиперрегенераторную, макроцитарную анемию
2. гиперхромную, гипорегенераторную, микроцитарную анемию
3. гипохромную, гипорегенераторную, макроцитарную анемию
4. гиперхромную, гипорегенераторную, макроцитарную анемию*
Наиболее частая причина железодефицитной анемии
Наиболее информативный показатель для подтверждения диагноза железодефицитной анемии
1.общая железосвязывающая способность сыворотки крови
2. уровень гемоглобина в клиническом анализе крови
3. цветной показатель
Если у больного имеется анемия, тромбоцитопения, бластоз в периферической крови, то следует думать о
Анемия
Анемии и лейкозы у детей
Анемия (малокровие) – это полиэтиологическое заболевание, характеризующееся понижением содержанием гемоглобина, часто в сочетании с уменьшением количества эритроцитов.
Клиника.Заболевание проявляется изменением внешних признаков (бледностью кожных покровов, слизистых, склер), слабостью, головокружением, одышкой, тахикардией, нарушением памяти, появлением нарушений со стороны мышечной системы (слабости, снижения тургора тканей), отклонениями в центральной нервной системе (вялостью, апатией, легкой возбудимостью), функциональными нарушениями со стороны сердечно-сосудистой системы (расширением границ, появлением систолического шума), развитием гепатомегалии и спленомегалии, уменьшением в крови общего количества гемоглобина, эритроцитов, их осмотической стойкости.
Классификация анемий.Первичные (наследственные) и вторичные (приобретенные).
1) дефицитные анемии, железодефицитные, витаминодефицитные, протеинодефицитные;
2) гипо– и апластические анемии: врожденная анемия Фанкони, анемия Даймонда – Блекфена, приобретенные анемии;
3) гемолитические анемии: сфероцитарная, серповидно-клеточная, аутоиммунная.
1) легкая анемия – гемоглобин в пределах 90 – 110 г/л, число эритроцитов снижается до 3 млн;
2) анемия средней тяжести – гемоглобин 70 – 80 г/л, число эритроцитов снижается до 2,5 млн;
3) тяжелая анемия – гемоглобин ниже 70 г/л, число эритроцитов ниже 2,5 млн.
По цветовому показателю:
Железодефицитные анемиихарактеризуются снижением содержания гемоглобина из-за дефицита железа, связаны с нарушением синтеза порфиринов, талассемии, содержания эритроцитов в результате его нарушения при поступлении, усвоении или патологических потерь.
Этиология.Антенатальные причины:
1) нарушение маточно-плацентарного кровообращения, плацентарная недостаточность (токсикозы, угроза прерывания и перенашивания беременности, гипоксемический синдром, обострение соматических и острых инфекционных заболеваний);
2) фетоматеринские и фетоплацентарные кровотечения;
3) внутриутробная мелена;
4) недоношенность, многоплодие;
5) глубокий и длительный дефицит железа в организме беременной.
1) фетоплацентарная трансфузия;
2) преждевременная или поздняя перевязка пуповины;
3) интернатальные кровотечения из-за травматических акушерских пособий и (или) аномалий развития плаценты и сосудов пуповины.
1) недостаточное поступление железа с пищей (раннее искусственное вскармливание, использование неадаптированных молочных смесей, вскармливание коровьим или козьим молоком, несбалансированная диета, лишенная достаточного содержания мясных продуктов);
2) повышение потребности в железе у детей с ускоренными темпами роста (недоношенные, дети с большой массой тела при рождении, дети с лимфатическим типом конституции, дети пре– и пубертатного периода);
3) повышенная потеря железа из-за кровотечений различной этиологии, нарушения кишечного всасывания (наследственные и приобретенные синдромы мальабсорбции, хронические заболевания кишечника, гемморагические маточные кровотечения у девочек в период становления менструального цикла в пубертате), нарушение обмена железа в организме из-за гормональных нарушений (пре– и пубертатный гормональный дисбаланс), нарушения транспорта железа из-за снижения активности или содержания трансферрина в организме.
Клиника.В анамнезе – недостаточное, неправильное питание, вялость, повышенная утомляемость, сухость, шероховатость кожных покровов, ломкость ногтей, искривление и поперечная исчерченность ногтей, выпадение волос, извращения вкуса и обоняния, астеновегетативные нарушения, нарушения процессов кишечного всасывания, сердцебиение, одышка при физической нагрузке. По содежанию гемоглобина и эритроцитов анемии делятся на легкие (гемоглобин в пределах 90 – 109 г/л, эритроцитов менее 4 – 3,5 x 10 12 ), анемии средней тяжести (гемоглобин в пределах 89 – 70 г/л, эритроцитов менее 3,5 x 10 12 ), тяжелые анемии (гемоглобин менее 70 г/л, эритроциты менее 2,5 x 10 12 ).
Диагностика– на основании клинических и лабораторных данных. в анализе крови – уменьшение эритроцитов, гемоглобина, концентрации сывороточного железа, уменьшение элементов крови, анизоцитоз, пойкилоцитоз. Цветовой показатель обычно низкий (иногда ниже 0,5); выраженная гипохромия эритроцитов, их анизоцитов, пойкилоцитоз; СОЭ обычно незначительно увеличена. Важнейший показатель болезни – снижение уровня железа в сыворотке (норма – 13 – 28 ммоль/л для мужчин; 11 – 26 ммоль/л для женщин). Низкий уровень сывороточного железа и ферритина, а также повышение уровня общей железосвязывающей способности сыворотки.
Лечениенапрвлено на устранение дефицита железа и восстановление необходимого его запаса в организме. Терапию необходимо начать с устранения причин ее вызывающих и организации правильного, сбалансированного питания (в рацион должны включаться продукты, богатые витаминами и железом, особенно мясные). Лечение парентерально вводимыми препаратами железа менее эффективно, чем прием его в виде таблеток внутрь.
Для внутримышечного введения применяют жектофер, фербитол, Феррум Лек и др. Последний препарат выпускают и для внутривенного введения. Показанием к парентеральному введению железа при железодефицитной анемии служат тяжелые энтериты, состояния после обширных резекций тонкой кишки (но не резекций желудка). Дозы назначают из расчета 1,5 мг железа на 1 кг массы тела в сутки. Жектофер вводят в/м по 2 мл в день больному с массой тела 60 кг. Переливание крови при содержании гемоглобина ниже 60 г/л. Прием препаратов железа усиливает костномозговую продукцию эритроцитов и сопровождается подъемом уровня ретикулоцитов в крови через 8 – 12 дней после начала терапии (факт, имеющий дифференциально-диагностическое значение).
Прогнозблагоприятный. Диспансерное наблюдение в течение 12 месяцев.
Анемии, связанные с дефицитом витамина В12независимо от причин этого дефицита характеризуются появлением в костном мозге мегалобластов, внутрикостномозговым разрушением эритроцитов, тромбоцитопенией и нейтропенией, атрофическими изменениями слизистой оболочки желудочно-кишечного тракта и изменениями нервной системы.
Этиология.Недостаточность витаминов редко бывает экзогенной (чаще эндогенной) природы, связанной с повышенным потреблением (при гельминотозах) и нарушением их всасывания различной природы (при заболеваниях желудка, синдроме мальабсорбции).
Патогенез.Дефицит витамина В12 чаще связан с нарушением выработки гликопротеина, соединяющегося с пищевым витамином В12 и обеспечивающего его всасывание (внутренний фактор). Нередко первые признаки заболевания появляются после перенесенного энтерита, гепатита. В первом случае это связано с нарушением всасывания витамина В12 в тонкой кишке, во втором – с расходованием его запасов в печени, являющейся основным депо витамина В12. Развитие В12-дефицитной анемии после тотальной гастрэктомии (когда полностью ликвидируется секреция внутреннего фактора) происходит через 5 – 8 лет и более после операции. В течение этого срока больные живут запасами витамина в печени при минимальном пополнении его за счет незначительного всасывания в тонкой кишке, не соединенного с внутренним фактором витамина. Редкой формой В12-дефицитной анемии является нарушение ассимиляции витамина при инвазии широким лентецом, когда паразит поглощает большое количество витамина В12. Причинами нарушенного всасывания витамина В12 при поражении кишечника могут быть тяжелый хронический энтерит, дивертикулез тонкой кишки, терминальный илеит, возникновение слепой петли тонкой кишки после операции на ней.
Клиникадефицита витамина В12 характеризуется поражением кроветворной ткани, пищеварительной и нервной систем. Появляются слабость, утомляемость, сердцебиения при физической нагрузке. Желудочная секреция угнетена, возможна стойкая ахлоргидрия. Нередко наблюдаются признаки глоссита – полированный язык, ощущение жжения в нем. Кожные покровы слегка желтушны, в сыворотке крови увеличен уровень непрямого билирубина (за счет повышенной гибели гемоглобинодержащих мегалобластов костного мозга). Определяется небольшое увеличение селезенки, реже печени.
Диагностика– на основании клинических и лабораторных данных. В анализе крови – гиперхромная анемия, лейкопения, тромбоцитопения, резко выраженный анизоцитоз эритроцитов наряду с очень крупными (более 12 мкм в диаметре) клетками – мегапоцитами, резчайший пойкилоцитоз, повышенное насыщение эритроцитов гемоглобином – гиперхромия, появление полисегментированных нейтрофилов, гиперхромный, реже нормохромный характер анемии, тромбоцитопения, лейкопения. Исследование костного мозга обнаруживает резкое увеличение в нем числа элементов эритроидного ряда с преобладанием мегалобластов. Клетки красного ряда, очень напоминающие мегалобласты, могут встречаться при остром эритромиелозе, который, как и В12-дефицитная анемия, сопровождается небольшой желтушностью, часто сочетается с лейко– и тромбоцитопенией. Однако при этом лейкозе нет столь выраженного анизо– и пойкилоцитоза, как при В12-дефицитной анемии, а главное – в костном мозге наряду с мегалобластоподобным и клетками встречаются в большом количестве миелобласты или недифференцируемые бласты. В сомнительных случаях следует после пункции костного мозга начать терапию витамином В12, которая при В12-дефицитной анемии через 8 – 10 дней приведет к резкому возрастанию в крови процента ретикулоцитов (рецикулоцитарный криз), подъему уровня гемоглобина, исчезновению в крови выраженного анизоцитоза, а в костном мозге – мегалобластов.
Лечение.Цианкобаламин (витамин В12) вводят ежедневно п/к в дозе 200 – 500 мгк 1 раз в день в течение 4 – 6 недель. После нормализации кроветворения и состава крови, наступающей через 1,5 – 2 месяца, витамин вводят 1 раз в неделю в течение 2 – 3 месяцев, затем в течение полугода 2 раза в месяц (в тех же дозах, что и в начале курса). В дальнейшем больных следует поставить на диспансерный учет; профилактически им вводят витамин В12 1 – 2 раза в год короткими курсами по 5 – 6 инъекций. Эта рекомендация может быть изменена в зависимости от динамики показателей крови, состояния кишечника, функции печени.
Фолиево-дефицитная анемия– мегалобластная анемия, сходная с проявлениями с В12-дефицитной анемии; развивается при дефиците фолиевой кислоты. Нарушение всасывания фолиевой кислоты наблюдается у беременных, страдающих гемолитической анемией, у недоношенных детей, при вскармливании их козьим молоком, у лиц, перенесших резекцию тонкой кишки, при целиакии, а также при длительном приеме противосудорожных препаратов типа фенобарбитала, дифенина.
Клиникааналогична, как при дефиците витамина В12.
Диагностика– на основании клинических и лабораторных данных. В анализе крови – снижение уровня фолиевой кислоты в эритроцитах и сыворотке крови.
Профилактика.Назначение фолиевой кислоты лицам, перенесшим ее дефицит, беременным, болеющим гемолитической анемией.
Гипо– и апластические анемии.В основе этого заболевания лежит уменьшение продукции клеток костного мозга.
Гемолитические анемииразвиваются вследствие разрушения эритроцитов, характеризуются увеличением в крови содержания продуктов распада эритроцитов – билирубина или свободного гемоглобина или появлением гемосидерина в моче. Важный признак – значительное нарастание в крови ретикулоцитов за счет повышения продукции клеток красной крови. Костный мозг при гемолитических анемиях характеризуется значительным увеличением числа клеток красного ряда.
Анемия постгеморрагическая острая– малокровие вследствие острой кровопотери в течение короткого срока.
Этиология.Причиной кровопотери могут быть травмы, хирургическое вмешательство, кровотечение при язве желудка или двенадцатиперстной кишки, из расширенных вен пищевода, при нарушении гемостаза, внематочной беременности, заболеваниях легких и т. п.
Патогенезскладывается из явлений острой сосудистой недостаточности, обусловленной острым опустошением сосудистого русла, потерей плазмы; при массивной кровопотере наступает и гипоксия из-за потери эритроцитов, когда эта потеря уже не может быть компенсирована ускорением циркуляции за счет учащения сердечных сокращений.
Клиника.Сосудистые нарушения (сердцебиение, одышка, падение артериального и венозного давления, бледность кожных покровов и слизистых оболочек).
Лечениеначинают с остановки кровотечения.
Наследственные анемии, связанные с нарушением синтеза порфиринов (сидероахрестические анемии), характеризуются гипохромией эритроцитов, повышением уровня сывороточного железа, отложением железа с картиной гемосидероза органов.
Патогенезсвязан с нарушением синтеза протопорфирина, что ведет к нарушению связывания железа и накоплению его в организме при резко нарушенном образовании гемоглобина.
Клиника.Жалобы отсутствуют или отмечают небольшую слабость, утомляемость. Чаще страдают мужчины. Болезнь наследуется по рецессивному типу, наследование сцеплено с Х-хромосомой. В начале болезни отмечается небольшое увеличение селезенки, в дальнейшем в связи с повышенным отложением железа в органах развивается гемосидероз печени (печень увеличивается и становится плотной), поджелудочной железы (появляется картина сахарного диабета). Накопление железа в сердечной мышце приводит к тяжелой недостаточности кровообращения, гемосидероз яичек сопровождается развитием евнухоидизма. Иногда кожа приобретает серый оттенок.
Диагностика– на основании клинических и лабораторных данных. В анализе крови – выраженная гипохромия эритроцитов (цветовой показатель 0,4 – 0,6), уровень гемоглобина снижен, в меньшей степени изменено число эритроцитов, повышен уровень сывороточного железа. Морфологически отмечают анизоцитоз, пойкилоцитоз, иногда небольшое количество мишеневидных форм. Содержание ретикулоцитов обычно нормальное.
Лечение.Назначают пиридоксин (витамин В6) по 1 мл 5%-ного раствора в/м 2 раза в день. При эффективной терапии через 1,5 недели резко возрастает содержание ретикулоцитов, а затем повышается и уровень гемоглобина.
Мегалобластные анемии– группа анемий, общим признаком которых служит обнаружение в костном мозге своеобразных эритрокариоцитов со структурными ядрами, сохраняющими эти черты на поздних стадиях дифференцировки (результат нарушения синтеза ДНК и РНК в клетках, называемых мегалобластами), в большинстве случаев мегалобластная анемия характеризуется цветовым показателем выше единицы. Поскольку синтез нуклеиновых кислот касается всех костномозговых клеток, частыми признаками болезни являются уменьшение числа тромбоцитов, лейкоцитов, увеличение числа сегментов в гранулоцитах.
Лейкозы – это общее название злокачественных опухолей возникающих из кроветворных клеток и поражающих костный мозг. Заболеваемость колеблется от 1 до 5 на 1 000 000 детского населения с пиком в возрасте от 2 до 4 лет. Хронический миелолейкоз – это опухоль, возникающая из дифференцирующихся клеток – предшественников миелопоэза.
Этиология.Не установлена, но наиболее распространенная теория – вирусно-генетическая. Роль факторов, ослабляющих реактивность организма: иммунодефицитные состояния, хромосомные аномалии, врожденная и гипопластическая анемия Фанкони, ионизирующее излучение, акселерация с лимфатизмом.
Патогенез.Лейкозные клетки являются потомством одной мутировавшей костномозговой кроветворной клетки, утратившей способность к созреванию, но сохраняющей способность к размножению.
Опухолевая прогрессия при лейкозах: угнетение нормальных ростов кроветворения, изменение морфологии пораженной кроветворной клетки и исходящего из ее клона опухолевых клеток, метастазирующих и растущих вне органов кроветворения; выделение лейкозными клетками веществ, угнетающих нормальное кроветворение; самоподдерживаемость лейкемического клона и динамичность его свойств в процессе лечения с приобретением большой агрессивности и устойчивости к действию цитостатиков.
Классификация:острые лейкозы (могут быть лимфобластными и миелобластными) и хронические лейкозы.
Клиника.Основные синдромы – это анемический, интоксикационный, геморрагический, пролиферативный, костно-суставной, поражение внутренних органов, нервной системы, инфекционные осложнения.
Диагностика– на основании клинических и лабораторных данных, анализа периферической крови, миелограммы, цитохимического исследования бластов крови и костного мозга.
Дифференциальный диагнозпроводят с инфекционным мононуклеозом, инфекционным лимфоцитозом, лейкемоидными реакциями при инфекционных заболеваниях, лекарственной болезни и отравлениях.
Лечениепрепаратами, обладающими иммунодепрессивным и цитостатическим эффектами по периодам индукции, консолидации, реиндукции. Симптоматическая терапия, лечение инфекционных осложнений.
Содержание:
- Отличие лейкоза: острого и хронического
- Классификация лейкозов
- Симптоматика
- Диагностика
- Лечение
← Как происходит пересадка костного мозга при лейкемии?
Сведения об остром промиелоцитарном лейкозе →
Фазы развития заболевания
В развитии патологии медики выделяют три стадии. Первая стадия носит название медленной, или хронической, которая может протекать до трех лет. Ухудшение симптомов заболевания после этого периода говорит о вступлении болезни в новую фазу – фазу акселерации. В этой фазе при мощном и своевременном лечении рак крови можно перевести в предыдущую фазу. Обычно такая фаза длится до полутора лет. После чего либо проходит ухудшение состояния здоровья пациента, либо его здоровье стабилизируется. а опухоль поддается контролю.
Отличие лейкоза: острого и хронического
Ранняя стадия острого лейкоза характерна накапливанием незрелых клеток и отсутствием их роста. Их переизбыток в 80% случаев угнетает нормальное кроветворение ростков. Хронический лейкоз способствует синтезу развитых клеток — гранулоцитов для постепенного замещения в периферической крови здоровых клеток.
Важно знать. Лейкоз хронический НЕ становится острым лейкозом и наоборот.
Симптомы у взрослых в начальной стадии острого лейкоза нередко проходят незамеченными, поскольку в крови больших колебаний биохимических показателей в сторону повышения или понижения не бывает. Позднее:
- появится ощущение ослабленности;
- имеющиеся хронические болезни обострятся;
- возможно активирование вируса герпеса и иного вида вирусных и бактериальных инфекций.
Рекомендуем изучить по данной теме также:
Химиотерапия как способ лечения острого миелобластного лейкоза
В развернутом периоде начинают ярко выражаться клинические и гематологические проявления острого лейкоза. Обострения переходят в ремиссии. Болезнь полностью излечивается или переходит в терминальную стадию.
Важно. В течение 5 лет при отсутствии бластных клеток в периферической крови устанавливается клинико-гематологическое излечивание (полная ремиссия).
В терминальной стадии цитостатики, используемые для лечения острого лейкоза, перестают действовать. Это становится причиной полного угнетения кроветворной системы. Даже при трансплантации костного мозга в этот период крайне высока смертность людей.
Если лейкоз хронический, то в крови присутствуют дозревшие клетки, многие из которых не способны выполнять свою прямую функциональную работу. При исследовании лабораторных анализов в крови выявляют повышенный уровень бесполезных лейкоцитов. Они не защищают организм от инфекций.
Тогда у пациентов возникает вопрос: хронический лейкоз — болезнь проходит или нет? При переизбытке гранулоцитов, мешающих кровотоку, избыток лейкоцитов и онкоклеток удаляют посредством лейкофареза. Процедура обеспечивает быстрый, но временный эффект.
Начальной фазы у хронического заболевания может и не быть, в 50% его выявляют по анализу крови по другому поводу. Даже при подтверждении диагноза хроническая болезнь может протекать на моностадии доброкачественно, поскольку опухоль состоит из одного клона клеток.
На последующей стадии появляются вторичные клоны опухоли. Поликлоновая стадия протекает быстро на фоне увеличения количества бластов. Эту стадию еще называют бластным кризом, поскольку 80% пациентов при этом погибают.
Лейкоз хронический проявляется:
- сплено- и гепатомегалией — увеличиваются в размере печень и селезенка;
- общей анемией с хроническим течением;
- генерализованные поражения лимфоузлов.
Причины заболевания
Хронический лейкоз возникает чаще всего у людей зрелого возраста, заболевание диагностируется в большинстве случаев у пациентов старше сорока лет. Преимущественно страдают хроническим лейкозом мужчины. У детей белокровие диагностируется довольно редко – всего в одном проценте случаев.
Точные причины заболевания установить до сегодняшнего времени не удалось. Сейчас разрабатывается вирусно-генетическая теория гемобластозов, согласно которой пусковым механизмом для заболевания может стать проникновение в организм определенных вирусов, например, Эпштейна-Барра, ретровирусов, способных встраиваться в незрелые клетки крови и провоцировать их бесконтрольное деление.
Врачи утверждают, что определенную роль в заболевании играет и наследственный фактор, ведь по статистике у значительного числа пациентов с лейкозом подобные заболевания диагностировались и у ближайших родственников. Также может возникать хроническая лейкемия и по вине 22 хромосомы, которая может нести в себе аномалию.
Не последнюю роль играет и негативное внешнее воздействие на организм – получение высоких доз радиации, рентгеновское облучение, работа во вредной промышленности (например, производство лакокрасочных изделий, фармацевтических препаратов, работа на золотоприисках). Риск развития увеличивается при табакокурении, чрезмерном употреблении алкогольных напитков, контакте с химикатами, удобрениями.
Классификация лейкозов
Если подтверждены хронические лейкозы — классификация включает две подгруппы:
- миелоидную;
- лимфоидную.
Миелоидная подгруппа состоит из хронических миелопролиферативных лейкозов:
- миелолейкоза;
- миелоза сублейкемического (остеомиелосклероза, миелофиброза);
- эритремии (истинной полицетемии);
- миеломоноцитарного;
- моноцитарного;
- мегакариоцитарного (идиопатической тромбоцитемии).
Важно. При хроническом миелолейкозе происходит пролиферация стволовой клетки в сопровождении повышения уровня предшественников гранулоцитов, эритроцитов и тромбоцитов.
Лимфоидная подгруппа состоит из лимфопролиферативных лейкозов:
- лимфолейкоза хронического;
- плазмоцитомы (миеломной болезни);
- лимфогранулематоза;
- лимфомы неходжкинской.
Ранее мы уже писали о лейкозе у детей и рекомендовали добавить эту статью в закладки.
Важно. При лимфолейкозе хронической стадии происходит пролиферация малых лимфоцитов: мозга костей, ЛУ, печени, селезенки и периферической крови.
Симптоматика
Опасные симптомы у взрослых проявляются признаками лейкемии: соматическими и гематологическими. Первичные соматические проявления белокровия характерны:
- ощущением постоянного утомления, слабости и недомогания;
- постоянным желанием спать или бессонницей;
- нарушением деятельности мозга: больные жалуются на ухудшение памяти, невозможность сосредоточиться;
- изменением цвета кожи (она становится бледной), долгим заживлением ран, синяков и мелких царапинок, проявлением нагноений;
- кровотечениями из десен и носа;
- ломотой и болями в любом суставе или кости;
- увеличением печени, селезенки и лимфоузлов;
- настырными простудами, обострением хронических форм болезней, как герпес, тонзиллит, бронхит, пиелонефрит;
- снижением веса на фоне отсутствия аппетита.
- повышается или понижается СОЭ;
- повышаются лейкоциты и проявляется лейкоцитоз;
- снижается гемоглобин в крови (проявляется анемия).
Диагностика
По анализу крови узнают количество кровяных клеток. При хроническом лейкозе лейкоциты повышаются, эритроциты и тромбоциты — снижаются. По биохимическому анализу крови уточняется функция почек и состав крови.
- красного мозга костей подтверждается диагноз и оценивается лечение хронического лейкоза;
- спинномозгового экссудата (пункции) — выявляются онкоклетки и проводится химиотерапия.
Чтобы уточнить тип лейкоза, исследуют цитохимию, проточную цитометрию, иммуноцитохимию, цитогенетику и молекулярную генетику. По рентгенограмме грудины и костей выявляют пораженные лимфоузлы средостения, костных суставов.
По КТ обнаруживают пораженные ЛУ в грудине и животе. МРТ исследуют мозг головы и спины. УЗИ необходимо для отличия новообразований: опухолевых и кистозных, выявления поражений в почках, печени, селезенке и ЛУ.
Лечение
Тактику лечения выбирают, зависимо от группы риска. Пациентов в группе с низким риском наблюдают, а при появлении явных симптомов назначают лечение. Прогноз выживаемости — 20-25 лет.
В группе с промежуточным и высоким риском больным терапию временно не применяют, если отсутствуют симптомы. Далее основным лечением будет являться химиотерапия с применением мощных лекарств. Препараты уничтожают лейкозные клетки, которые быстро и бесконтрольно делятся, нарушая важные этапы цикла. При этом могут повредиться и нормальные клетки.
Лечение лимфобластного лейкоза проводится рядом агентов: L-аспарагиназой или PEG-L- аспарагиназой, Даунорубицином (Дауномицином), Винкристином, Преднизолоном. Из других препаратов — Доксорубицином, Цитарабином, Этопозидом, Дексаметазоном.
Применяют Хлорамбуцил, или заменяют его Циклофосфамидом с меньшими побочными эффектами Как рассчитывается для взрослых максимальная доза Дексаметазона при лечении хронических лейкозов?
Дозировку внутривенных струйных или капельных вливаний, инъекций внутримышечных назначает врач. За первые сутки вводят 4-20 мг 3-4 приемами. Курс — 3-5 дней. Для капельного введения пользуются раствором натрия хлорида изотонического или 5%-ного декстрозного раствора.
Если лейкоз хронический, лечение Дексаметазоном в таблетках назначают по 0,5 мг или 1,5 мг с едой. За сутки максимальная доза составляет 15 мг (не более), минимальная — 1 мг. При установлении стабильного состояния дозу снижают до 3 мг/сутки. Детям рассчитывают 83,3-333,3 мкг/кг.
Эффективно лечение хронического миелоидного лейкоза Мезилатом иматиниба (Гливеком). Хронического лимфолейкоза — Флударабином с Циклофосфамидом.
Нередко проводят трансплантацию костного мозга в самом начале комплексной терапии для улучшения результатов. При этом проводится химиотерапия и облучение (редко) для уничтожения онкоклеток, а также вливание стволовых клеток для прорастания в костный мозг и вырабатывания нормальных здоровых клеток.
Проводят радиоиммунотерапию, Т клеточную иммунотерапию для облучения онкоклеток с минимальным повреждением здоровых тканей, для минимилизации токсичности для больного и предотвращения рецидива. Лучевой терапией по спирали вокруг опухоли достигают эффекта и уменьшают травматизацию здоровых клеток, что снижает количество осложнений.
Для лечения хронического лейкоза необходимо применять комплексную терапию: химиотерапию, операции, радиоиммунотерапию, Т клеточную иммунотерапию, моноклональные антитела и стволовые клетки для трансплантации.
← Как происходит пересадка костного мозга при лейкемии?
Сведения об остром промиелоцитарном лейкозе →
Прогноз
Дальнейшая жизнь пациента, ее качество и длительность зависит от типа рака и своевременности лечения. В среднем при раннем диагностировании большинство больных живут 10 лет и больше, при средне запущенной болезни – 5-7, при поздней медицинской помощи – 1-3 года. Так же на прогноз влияет возраст. Чем меньше возраст пациента, тем больше шансов на длительную ремиссию или даже полное выздоровление.
Стоит отметить, что повторный криз еще не означает смерть – если прошлое лечение хорошо подействовало и прошло много времени, это же лечение может исцелить пациента снова. В крайнем случае врач может назначить другую химиотерапию, которая, возможно, окажется более эффективной.
Читайте также:

