Истощение и кахексия основные звенья патогенеза
Механизм развития эндогенного истощения и кахексии различен при их первичных и вторичных (симптоматических) формах.
Первичные эндогенные формы истощения и кахексии имеют 3 основные разновидности: гипоталамическую, кахектиновую и анорексическую формы.
Патогенез первичной гипоталамической формы (диэнцефальной, подкорковой) истощения и кахексии заключается в снижении или прекращении синтеза и выделения в кровь нейронами гипоталамуса пептида Y. Это приводит к развитию последовательных процессов, представленных на рисунке 11-8.
Рис. 11-8. Основные звенья первичного гипоталамического механизма истощения и кахексии.
Патогенез первичной кахектиновой (цитокиновой) формы истощения и кахексии включает в себя звенья, приведенные на рисунке 11-9.
Рис. 11-9. Основные звенья первичного кахектинового механизма истощения и кахексии.
Патогенез анорексической формы истощения и кахексии представлен на рисунке 11-10.
Рис. 11-10. Основные звенья первичного анорексического механизма истощения и кахексии.
У лиц, имеющих предрасположенность к развитию анорексии, критическое отношение к своему телу (воспринимаемому как имеющему избыточную массу) вызывает развитие нервно-психических расстройств. Это приводит к длительным эпизодам отказа от приема пищи. Наиболее часто наблюдается у девочек-подростков и девушек до 16–18-летнего возраста.
При повторных и эмоционально негативно окрашенных стресс-реакциях наблюдается избыточное образование серотонина и холецистокинина, подавляющих аппетит. Дальнейшее течение процесса может привести к реализации эффектов нейропептида Y и кахектина. Эти факторы и лежат в основе патогенеза нервной анорексии. При затяжном течении процесса развивается выраженное снижение массы тела, вплоть до кахексии.
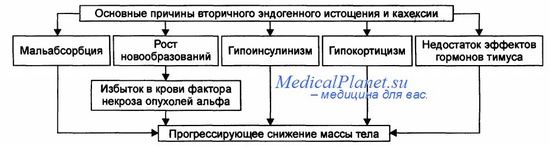
Вторичные эндогенные формы истощения и кахексии являются важными, нередко главными, симптомами других патологических состояний и болезней (рис. 11-11). Формы патологии, приводящие к истощению и кахексии рассмотрены в соответствующих разделах учебника.
Рис. 11-11. Основные причины вторичного эндогенного истощения и кахексии.
Липодистрофии — состояния, характеризующиеся генерализованной или локальной утратой жировой ткани, реже — избыточным ее накоплением в подкожной клетчатке.
Липидозы—типовая форма нарушения липидного обмена, характеризующася расстройствами метаболизма различных форм липидов. К ним относят, например, сфинголипидозы, ганглиозидозы, муколипидозы, адренолейкодистрофии, лейкодистрофии, липофусцинозы, цереброзидозы.
Дислипопротеинемии — состояния, характеризующиеся отклонением от нормы содержания, структуры и соотношения в крови различных ЛП.
Нарушения метаболизма ЛП — главное звено патогенеза атеросклероза, ИБС, панкреатита и других заболеваний.
Характер течения и клинические проявления дислипопротеинемий определяются несколькими факторами:
Ú наследственными свойствами организма (например, составом, соотношением и уровнем различных ЛП; особенностями их метаболизма);
Ú действием агентов внешней среды (например, набором продуктов питания, особенностями рациона и режима приема пищи);
Ú наличием (или отсутствием) сопутствующих заболеваний (например, ожирения, гипотиреоза, СД, поражений почек и печени).
В плазме крови циркулируют различные липиды. Свободные жирные кислоты переносятся альбуминами, а триглицериды, холестерин, эфиры холестерина и фосфолипиды, небольшое количество жирных кислот транспортируются в составе ЛП. Эти сферические частицы состоят из гидрофобной сердцевины (содержит эфиры холестерина и триглицериды) и гидрофильной оболочки (содержит холестерин, фосфолипиды и аполипопротеины). Основные характеристики разных ЛП приведены в таблице 11-2.
Таблица 11-2. Виды и основные свойства липопротеинов
Ú продолжительное профузное потоотделение с выделением большого количества солей;
Ú повторная или неукротимая рвота (например, при отравлениях или беременности), ведущая к потерям Na + и K + ;
Ú мочеизнурение сахарное (при СД) или несахарное (например, при дефиците АДГ), сочетающееся с экскрецией солей K + , Na + , глюкозы, альбуминов;
Ú профузные поносы (например, при холере или синдроме мальабсорбции), сопровождающиеся потерей кишечного сока, содержащего K + , Na + , Ca 2+ и другие катионы;
Ú неправильное или необоснованное проведение процедур диализа (гемодиализа или перитонеального диализа с низкой осмоляльностью диализирующих растворов). Это приводит к диффузии ионов из плазмы крови в жидкость для диализа;
Ú коррекция изоосмоляльной гипогидратации растворами с пониженным содержанием солей.
Истощение и кахексия -- патологическое снижение массы жировой ткани ниже нормы. При истощении дефицит жировой ткани может составлять 20-25% и более (при индексе массы тела ниже 20 кг/м2), а при кахексии -- ниже 50%. При истощении и особенно при кахексии наблюдаются существенные расстройства жизнедеятельности организма, могущие привести к смерти.
Вынужденное или осознанное полное либо частичное голодание (в последнем случае чаще всего с целью похудания).
Полное голодание -- состояние, при котором в организм не поступают продукты питания (например, при их отсутствии, отказе от еды, невозможности приёма пищи).
Неполное голодание -- состояние, характеризующееся значительным дефицитом пластических веществ и калорий в пище (например, при неполноценном в количественном и качественном отношении питании, однородной пище, вегетарианстве).
Низкая калорийность пищи, не восполняющая энергозатрат организма. Основные причины вторичного истощения и кахексии.
Эндогенные причины истощения и кахексии Истощение эндогенного генеза подразделяют на первичное и вторичное.
Причины первичного (гипоталамического, диэнцефального) истощения рассмотрены на рисунке.
Причины вторичного (симптоматического) истощения приведены на рисунке. Основные звенья патогенеза экзогенного истощения и кахексии. Патогенез истощения и кахексии.
Экзогенное истощение и кахексия. Отсутствие или значительный дефицит продуктов питания приводит к развитию цепи последовательных и взаимозависимых процессов, рассмотренных на рисунке. Первичные эндогенные формы истощения и кахексии. Наибольшее клиническое значение имеют гипоталамическая, кахектиновая и анорексическая формы.
Гипоталамическая форма истощения и кахексии.
При гипоталамической (диэнцефальной, подкорковой) форме истощения и кахексии происходит снижение или прекращение синтеза и выделения в кровь нейронами гипоталамуса пептида Y. Это приводит к последовательным процессам, перечисленным на рисунке. Основные звенья кахектинового механизма истощения и кахексии.
Кахектиновая форма истощения и кахексии Патогенез кахектиновой, или цитокиновой, формы истощения и кахексии рассмотрен на рисунке. Основные звенья анорексического механизма истощения и кахексии. - Анорексическая форма истощения и кахексии.
Основные звенья патогенеза анорексической формы истощения и кахексии перечислены на рисунке. Основные причины вторичного эндогенного истощения и кахексии. - У лиц, имеющих предрасположенность к развитию анорексии, критическое отношение к своему телу (воспринимаемому как имеющему избыточную массу) вызывает развитие нервно-психических расстройств. Это приводит к длительным периодам отказа от приёма пищи. Наиболее часто наблюдается у девочек-подростков и девушек до 16--18-летнего возраста.
При повторных и эмоционально негативно окрашенных стресс-реакциях наблюдается избыточное образование серотонина и холецистокинина, подавляющих аппетит.
Дальнейшее течение процесса может привести к реализации эффектов нейропептида Y и кахектина. Эти факторы, скорее всего, лежат в основе патогенеза нервной анорексии. При затяжном течении процесса развивается выраженное снижение массы тела, вплоть до кахексии. Вторичные эндогенные формы истощения и кахексии являются важными, нередко -- главными, симптомами других патологических состояний и болезней.







- · Снижение массы тела. Кахексия наблюдается при понижении массы тела менее, чем на 70% от должной, а также снижение индекса массы тела (ИМТ -- соотношения веса и роста) менее 16-17 кг/м 2 .
- · Слабость, нарушение сна (сонливость днем и бессонница ночью), снижение работоспособности.
- · Мышечная слабость, снижение переносимости физической нагрузки.
- · Склонность к частым (рецидивирующим) инфекциям.
- · Бесплодие, снижение либидо (полового влечения), импотенция (половое бессилие).
- · Гиповитаминоз (снижение содержания и поступления витаминов в организм).
- · Сухость кожи, слизистых оболочек.
- · Выпадение волос и ломкость волос, ногтей.
- · Склонность к гипотонии (снижению артериального давления).
- · Отеки.
- · Депрессивные состояния, плаксивость, плохое настроение.
- · Психические и неврологические нарушения: обмороки, тяжелые нарушения сознания вплоть до коматозного (кома - тяжелое состояние, связанное с угнетением центральной нервной системы, приводящее к потере сознания и нарушению функций жизненно важных органов) состояния, параличи (отсутствие движений) и др.
Формы. анорексический истощенный жировой патологический
Выделяют 2 формы кахексии:
- · первичную (экзогенная) -- при низком поступлении пищи в организм или в том случае, если ее энергетическая и питательная ценность низки;
- · вторичную (эндогенная) -- является осложнением различных заболеваний.
Основные причины кахексии следующие.
Факторы, условно способствующие развитию кахексии, можно разделить на несколько групп:
Чем раньше Вы обратитесь за помощью к специалисту, тем больше шансов сохранить здоровье и снизить риск развития осложнений:
1. Врач терапевт поможет при лечении заболевания
Записаться к врачу терапевту
- · Анализ анамнеза заболевания и жалоб (когда (как давно) стал снижаться вес, за какой период времени, с чем пациент связывает это, произошло ли снижение массы тела из-за голодания, придерживается ли пациент диет, постов и др.).
- · Анализ анамнеза жизни (есть ли у пациента онкологические заболевания, проходил ли лечение по поводу опухолей, были или есть сейчас хронические заболевания, инфекции, были ли операции, травмы и др.).
- · Физикальный осмотр. Отмечается выраженная худоба, обязательно измерение массы тела, индекса массы тела (соотношение веса и роста), толщины подкожной жировой клетчатки, оценивается тургор (упругость) кожных покровов, слизистых оболочек, измеряется мышечная сила, степень нарушения сознания и др.
Кахексия - это серьезное состояние, которое требует обследования и лечения в условиях стационара.
Изменения лабораторных и инструментальных данных разнообразны, поэтому для того чтобы вылечить ее, нужно установить причину, степень развития полиорганной недостаточности (нарушение функции со стороны многих органов и систем организма).
Требуется проведение всех методов обследования, в том числе:
- · общий анализ крови;
- · биохимический анализ крови;
- · посев крови при подозрении на сепсис (заражение крови);
- · общий анализ мочи;
- · ультразвуковое исследование (УЗИ), компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), рентгенологическое исследование, эзофагогастродуоденоскопия и др.
Возможны также консультации гастроэнтеролога, эндокринолога, хирурга, онколога, невролога,психиатра.
Лечение кахексии обычно проводят в стационаре под контролем врача. Прежде всего, необходимо выявить причину и назначить лечение основного заболевания, которое привело к развитию кахексии.
- · Полноценное питание. Лечение начинают обычно с назначения смесей, сбалансированных по содержанию питательных веществ, витаминов, микроэлементов. Введение веществ может быть:
- o энтеральным (при котором пища попадает непосредственно в желудочно-кишечный тракт);
- o парентеральным (питательные вещества минуют желудочно-кишечный тракт, обычно назначают внутривенные инфузии (вливания)). Парентеральное питание рекомендуется при выраженном истощении, онкологических заболеваниях, тяжелых инфекциях, после лечения онкологических заболеваний, при нарушениях глотания (психические заболевания, отказ от пищи, тяжелые коматозные состояния (кома -- тяжелое состояние, связанное с угнетением центральной нервной системы, приводящее к потере сознания и нарушению функций жизненно важных органов)).
- · Поливитаминные препараты для лечения гиповитаминоза (дефицита витаминов в организме).
- · Ферментные препараты (для улучшения пищеварения).
- · Антибактериальная терапия (при лечении инфекционных заболеваний).
К лечению можно добавлять гормоны роста, стимуляторы аппетита, гормональные препараты, однако их эффективность не доказана.
Осложнения и последствия
Чаще всего кахексия является осложнением других заболеваний. Но и сама она может приводить к возникновению болезней.
- · Своевременное и достаточное лечение заболеваний и состояний, на фоне которых развивается кахексия (злокачественных опухолей, цирроза печени (замещения нормальной ткани печени грубой соединительной тканью), инфекций и др.).
- · Лечение алкоголизма, наркомании.
- · Пропаганда здорового питания -- беседы об опасностях нервной анорексии (отказ от еды с целью снижения веса), необходимости правильно и рационально питаться: отказ от слишком жареной, консервированной, слишком горячей и острой пищи, исключение перееданий, употребление в пищу продуктов с высоким содержанием клетчатки (овощи, фрукты, зелень).
Истощение и кахексия — патологическое снижение массы жировой ткани ниже нормы. При истощении дефицит жировой ткани может составлять 20-25% и более (при индексе массы тела ниже 20 кг/м2), а при кахексии — ниже 50%. При истощении и особенно при кахексии наблюдаются существенные расстройства жизнедеятельности организма, могущие привести к смерти.
Различают эндогенные и экзогенные причины истощения.
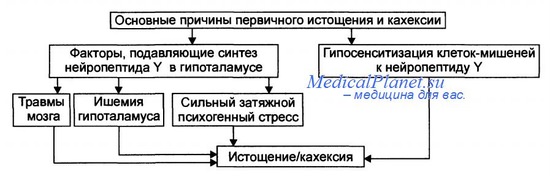
Основные причины первичного истощения и кахексии.
- Вынужденное или осознанное полное либо частичное голодание (в последнем случае чаще всего с целью похудания).
- Полное голодание — состояние, при котором в организм не поступают продукты питания (например, при их отсутствии, отказе от еды, невозможности приёма пищи).
- Неполное голодание — состояние, характеризующееся значительным дефицитом пластических веществ и калорий в пище (например, при неполноценном в количественном и качественном отношении питании, однородной пище, вегетарианстве).
- Низкая калорийность пищи, не восполняющая энергозатрат организма.
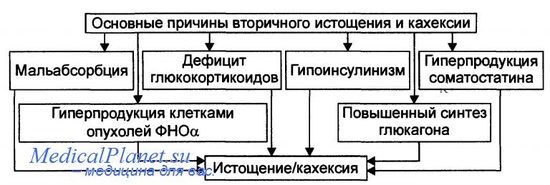
Основные причины вторичного истощения и кахексии.
Истощение эндогенного генеза подразделяют на первичное и вторичное.
- Причины первичного (гипоталамического, диэнцефального) истощения рассмотрены на рисунке.
- Причины вторичного (симптоматического) истощения приведены на рисунке.
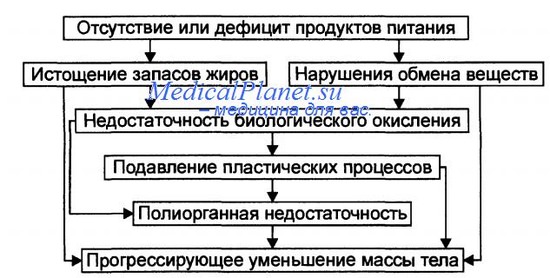
Основные звенья патогенеза экзогенного истощения и кахексии.
• Экзогенное истощение и кахексия. Отсутствие или значительный дефицит продуктов питания приводит к развитию цепи последовательных и взаимозависимых процессов, рассмотренных на рисунке.
Первичные эндогенные формы истощения и кахексии. Наибольшее клиническое значение имеют гипоталамическая, кахектиновая и анорексическая формы.

Основные звенья гипоталамического механизма истощения и кахексии.
- Гипоталамическая форма истощения и кахексии
При гипоталамической (диэнцефальной, подкорковой) форме истощения и кахексии происходит снижение или прекращение синтеза и выделения в кровь нейронами гипоталамуса пептида Y. Это приводит к последовательным процессам, перечисленным на рисунке.

Основные звенья кахектинового механизма истощения и кахексии.
- Кахектиновая форма истощения и кахексии
Патогенез кахектиновой, или цитокиновой, формы истощения и кахексии рассмотрен на рисунке.
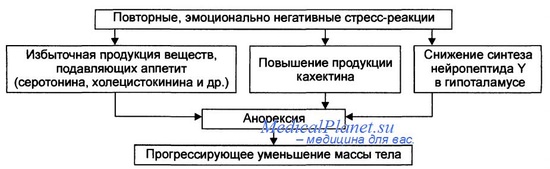
Основные звенья анорексического механизма истощения и кахексии.
- Анорексическая форма истощения и кахексии
Основные звенья патогенеза анорексической формы истощения и кахексии перечислены на рисунке.
Основные причины вторичного эндогенного истощения и кахексии.
- У лиц, имеющих предрасположенность к развитию анорексии, критическое отношение к своему телу (воспринимаемому как имеющему избыточную массу) вызывает развитие нервно-психических расстройств. Это приводит к длительным периодам отказа от приёма пищи. Наиболее часто наблюдается у девочек-подростков и девушек до 16—18-летнего возраста.
- При повторных и эмоционально негативно окрашенных стресс-реакциях наблюдается избыточное образование серотонина и холецистокинина, подавляющих аппетит.
- Дальнейшее течение процесса может привести к реализации эффектов нейропептида Y и кахектина. Эти факторы, скорее всего, лежат в основе патогенеза нервной анорексии. При затяжном течении процесса развивается выраженное снижение массы тела, вплоть до кахексии.
• Вторичные эндогенные формы истощения и кахексии являются важными, нередко — главными, симптомами других патологических состояний и болезней.
Кахексия считается распространенным осложнением многих хронических заболеваний (см. табл. 11.1), и многие исследователи связывают с ней плохой прогноз (кахексия нередко становится причиной смерти, особенно у больных со злокачественными опухолями). Атрофия скелетных мышц — опознавательный знак кахексии. Но так как атрофия мышц может иметь разнообразную этиологию, важно обозначить критерии различия.
Атрофия мышц зачастую наблюдается у больных, длительное время находящихся на постельном режиме, малоподвижных больных. Но, в отличие от кахексии, синтез белка при этом в организме снижен, а масса жировой клетчатки увеличивается. Состояние кахексии характеризуется гиперкатаболизмом и гиперметаболизмом, при которых общий расход энергии достаточно высок, чего не отмечается у малоподвижных больных.
Кахексическую атрофию мышц следует отличать от саркопении (возрастная атрофия и утрата мышечных волокон). При саркопении наблюдается снижение синтеза белка, а при кахексии — повышение его синтеза. При саркопении уровень так называемого разобщающего белка (uncoupling protein — считается, что он может играть важную роль в защите миоцитов от повреждения активными формами кислорода) повышен, а при кахексии — снижен.
Некоторые гены, ответственные за атрофию мышц, активируются при кахексии. Таковым является субсемейство FoxO транскрипционных факторов Fox, играющих роль в большом количестве физиологических процессов, которые, в том числе, способны запускать аутофагию в миоцитах скелетных мышц. Fox03 независимо контролирует две основные протеолитические системы, включающиеся при кахексии: убиквитин-протеосомную и аутофаго-лизосомальную. Лигандом, активирующим данные транскрипционные факторы, является миоста- тин, вещество семейства ростовых факторов, подавляющее мышечный рост за счет ингибирования пролиферации миобластов. В случае кахексии, вызываемой злокачественными опухолями, основную роль играет другой транскрипционный фактор NF-kB, ингибирование которого подавляет развитие кахексии на экспериментальных моделях.
Еще одним транскрипционным фактором является белок MyoD, путем связывания с промотором гена тяжелой цепи миозина обуславливающий экспрессию этого гена.
Остро-фазовая реакция организма опосредована во многом цитокинами, которые вырабатываются клетками, ответственными за реализацию воспалительного ответа, а также клетками злокачественных опухолей. Провоспалительные цитокины вызывают как периферические эффекты (в том числе атрофию мышц), так и центральные, характерные для кахексии. Далее попытаемся рассмотреть действие некоторых цитокинов и их роль в развитии кахексии.
Основными провоспалительными цитокинами, упоминаемыми в литературе в связи с развитием кахексии, являются фактор некроза опухолей TNF-a и интерлейкины IL-1 и IL-6. Данные цитокины оказывают схожее действие на организм, поэтому их действие можно рассмотреть на примере TNF-a. Фактор некроза опухолей TNF-a, продуцируемый моноцитами крови и тканевыми макрофагами, проникает через гематоэнцефалический барьер и воздействует на вентромедиальные ядра гипоталамуса, подавляя аппетит. Блокируя фермент ли- попротеинлипазу, TNF-a препятствует усвоению жирных кислот; цитокин также увеличивает экспрессию гена лептина. Иными словами, TNF-a обладает анорексигенным действием. Данный цитокин стимулирует также экспрессию гена убиквитина (повышает уровень синтеза мРНК), а значит, в некоторой степени может активировать протеолиз миофибрилл; этот же цитокин ингибирует экспрессию гена тяжелых цепей миозина.
Интерлейкин 1 (IL-1) синтезируется лимфоцитами и макрофагами, а также астроцитами и клетками микроглии и, как фактор некроза опухолей, обладает центральным анорексигенным действием, так как подавляет экспрессию нейропептида Y. IL-1 способен запускать протеолиз в миоцитах, по-видимому, по механизму, схожему с TNF-a. Провоспалительные цитокины стимулируют выделение надпочечниками кортизола и катехоламинов, обладающих катаболическим действием. Воздействуя на центральную нервную систему, данные цитокины опосредуют такие проявления кахексии, как апатия, тревога, когнитивный дефицит. Провоспалительные цитокины могут оказывать значимое влияние на функционирование желудочно-кишечного тракта, ухудшая кровоснабжение органов желудочно-кишечного тракта, снижая их моторику, влияя на пролиферацию и обменные процессы в клетках.
Организм, как система, способная к саморегуляции, уравновешивает высвобождение провоспалительных агентов выработкой противовоспалительных веществ. В данном случае имеет смысл упомянуть о противовоспалительных цито- кинах, таких как интерлейкины IL-4, IL-10, IL-13, IL-15, которые подавляют прогрессирование кахексии. IL-15, например, не только обладает анаболическим действием, но и способен блокировать протеолиз в скелетных мышцах.
По-видимому, существует связь между возникновением системного воспалительного ответа и снижением анаболической активности гормонов. Так, резистентность к инсулину, наблюдающаяся у большего числа больных с кахексией, возникает вследствие повышения выработки некоторых провоспалительных цитокинов. Было показано, что в миоцитах TNF-a угнетает фосфорилирование субстрата инсулинового рецептора, а значит, передача сигнала с рецептора ухудшается. Похожее влияние на чувствительность к инсулину оказывает и IL-6. Чувствительность к соматотропину, гормону с преимущественно анаболическим эффектом, у пациентов с кахексией также изменена. Действие соматотропина опосредуется соматомединами и инсулиноподобным фактором роста (IGF-1), синтезирующимся преимущественно в печени. При кахексии синтез IGF-1 угнетается, в результате чего развивается резистентность к соматотропину.
Разнообразные гормоны могут выступать в качестве медиаторов кахексии. Глюкокортикоиды снижают захват глюкозы и аминокислот клетками; ингибируют синтез белков, активируют глюконеогенез, активируют синтез компонентов убиквитин-протеосомной системы миоцитов. Тестостерон, напротив, препятствует развитию кахексии. Этот гормон стимулирует пролиферацию миобла- стов, активирует синтез миофибрилл и способствует репарации поврежденных миоцитов; он также препятствует высвобождению макрофагами провоспалительных цитокинов и повышает выработку противовоспалительных цитокинов.
Недостаток микро- и макронутриентов (то есть истощение) может усугублять состояние кахексии. Было выяснено, что некоторые аминокислоты (лейцин, валин) обладают анаболическим действием и даже способны ингибировать протеолиз.
Как уже говорилось, истощение может сопровождать кахексию, а значит, некоторые проявления кахексии будут усугубляться.
Лечение. Лечение направлено на устранение причины или коррекцию основного заболевания, приведшего к истощению или кахексии. Современная система лечения предполагает применение энтерального и параэнтерального искусственного питания, основанных на сбалансированности смесей нутриентов по белкам, жирам, углеводам и витаминам. При этом в состав смесей включаются липиды (преимущественно в виде высококалорийных жировых эмульсий), углеводы (как источники свободной энергии) и аминокислоты (в виде условно незаменимых аргинина и глютамина). По показаниям применяют анаболические гормоны, переливание крови, ее компонентов и плазмозаменяющие растворы. Энтеральное питание является приоритетным. Оно осуществляется с применением назогастроинтестенального зонда и проводится с целью поддержания естественных процессов всасывания нутриентов из просвета кишечника, восстановления иммунной и барьерной функций эпителия кишечной стенки. При недостаточной эффективности энтерального питания дополнительно применяют параэнтеральное. В состав смесей для параэнтерального питания необходимо вводить концентрированные растворы глюкозы, энергетический поли- ионный раствор, витамины, незаменимые аминокислоты и антиоксиданты. При проведении искусственного лечебного питания необходимо учитывать потребность больных в свободной энергии, которая рассчитывается с учетом энергозатрат с применением непрямой калориметрии или по формуле Харриса и Бенедикта. Неадекватное внутривенное вливание раствора глюкозы может привести к целому ряду осложнений, таких как жировая дистрофия печени, нарушение кислотно-основного состояния, глюкозурии. Энергетический эквивалент дозы глюкозы должен составлять 4 ккал/г массы тела, со скоростью вливания ее 4—5 мг/кг/мин. Альтернативой глюкозе могут служить липиды в виде жировых эмульсий с энергетическим эквивалентом дозы 9 ккал/г массы тела в сутки. В ряде случаев расстройства пищевого поведения требуется лечение у психиатра.
От понимания патогенеза кахексии и истощения будет зависеть, в том числе, и назначаемый курс лечения. Можно сказать, что для терапии истощения нужно обнаружить и далее устранить его причину. Причиной кахексии является некое хроническое заболевание, устранить которое не всегда возможно. По-видимому, можно воздействовать на различные звенья развития кахексии, регулируя, например, цитокиновые или гормональные взаимоотношения. Но, так как биохимический баланс организма очень хрупкий, врачи не могут со стопроцентной вероятностью предсказать ход развития заболевания в каждом конкретном случае. Поэтому на сегодняшний день схемы терапии кахексии только разрабатываются.

Кахексия – это сложный процесс метаболизма, ведущий к истощению организма. Термин „кахексия” происходит из латинского языка (лат. cachexia) или греческого языка (гр. kacheksia), что означает плохое состояние тела.
Симптомы кахексии – это, в том числе, потеря массы тела, липолиз, атрофия мышц и внутренних органов, отсутствие аппетита, хронически возникающая тошнота, слабость, расстройства личности и гиперметаболизм. Возникает, как правило, у пациентов с хроническими заболеваниями, например, рак или СПИД.
Причины кахексии
Кахексия возникает у большинства пациентов с распространенной формой рака и СПИДа, в результате хронического недоедания. Более чем у 80% пациентов, в неизлечимых стадиях рака, перед смертью имеют состояние истощения организма.

Истощение при кахексии.
Примерно в 80% случаев кахексия развивается при опухоли верхней части желудочно-кишечного тракта и в 60% случаев рака легких. Это связано не только с уменьшением жировой ткани, а также распадом мышц и нарушением аппетита.
Также с истощением организма сталкиваются пациенты с крупными опухолями (кроме рака молочной железы). Кахексия чаще встречается у детей и пожилых людей, что делает её прогресс более четким.
Истощения организма также может быть результатом почечной недостаточности, сердечной недостаточности, хронической обструктивной болезни легких или ВИЧ-инфекции.
Последствия истощения организма
Клиническая оценка кахексии требует учета широкого спектра качеств и состояний. К наиболее часто упоминаемым последствиям кахексии относятся:
- общее ослабление организма;
- отсутствие аппетита;
- хроническая тошнота;
- снижение жировой и безжировой массы тела;
- распад мышечной ткани;
- отеки;
- анемия;
- расстройства личности.
В патогенезе кахексии важную роль играет активное производство цитокинов, индуцированных посредников, производимых опухолью или организмом хозяина. Кахексия стимулирует нейрогормональную систему. Увеличивается концентрация гормона стресса – кортизола, усиливается активность ренина, ангиотензина и альдостерона, падает производство инсулина.
Истощения организма приводит к тому, что концентрация альбумина в плазме, как правило, уменьшается. Прямые измерения, например, окружности мышц плеча, могут быть полезны для мониторинга изменений в питании или влияния лечения на пациентов. Более сложные лабораторные исследования обычно не нужны. Иммуноанализы не являются надежными маркерами состояния питания онкологических больных или людей, страдающих от иммунодефицитом.
Терапия кахексии
Лечение истощения направлено на улучшение общего состояния пациента, даже если рак находится на продвинутой стадии, а прогноз плохой. Терапия должна включать в себя комплексные фармакологические, диетические и реабилитационные меры, а команда, занимающаяся лечением, должна состоять из врачей, медсестер и врача-диетолога.
Лечебные процедуры должны быть направлена на контроль основной болезни, избавления от тошноты и рвоты, повышение аппетита и улучшения перистальтики кишечника, сокращения анемии, противодействие боли и повышение настроения.
В некоторых случаях может потребоваться процедурное вмешательство, например, при разрастании клеток. Правильно сбалансированная диета поможет улучшить состояние больного, путем увеличения поступления калорий. Правильное питание улучшает качество жизни больного.
Существенное значение имеет достаточное количество белка – полноценного и хорошо усваиваемого. Питание должно быть малыми порциями, но частое. Полезно использование специальных добавок. Если питание оральным путем невозможно, следует рассмотреть другие способы, например, парентеральное питание (внутривенное питание).
Читайте также:

