Ингибиторы протеинкиназы в онкологии
Препараты подгрупп исключены. Включить
Препараты
| Действующее вещество | Торговые названия |
| Абемациклиб* (Abemaciclibum) | Верзенио ™ |
| Акалабрутиниб (Akalabrutinibum) | Калквенс ® |
| Акситиниб* (Axitinibum) | Инлита ® |
| Алектиниб (Alectinibum) | Алеценза ® |
| Афатиниб* (Afatinibum) | Гиотриф ® |
| Бозутиниб* (Bosutinibum*) | Бозулиф |
| Вандетаниб* (Vandetanibum) | Капрелса ® |
| Вемурафениб* (Vemurafenibum) | Зелбораф ® |
| Гефитиниб* (Gefitinibum) | Гефитиниб Гефитиниб Канон Гефитиниб-натив Гефитиниб-ТЛ Иресса ® ЛАНГОТЕР ® |
| Дабрафениб + Траметиниб [набор] (Dabrafenibum + Trametinibum) | Тафинлар ® Комбо |
| Дабрафениб* (Dabrafenibum) | Рафинлар Тафинлар ® |
| Дазатиниб* (Dasatinibum) | Дазатиниб Дазатиниб-натив Спрайсел ® |
| Ибрутиниб (Ibrutinibum) | Ибрутиниб-натив Имбрувика |
| Иксазомиб (Ixazomibum) | ИКСАЗОМИБА ЦИТРАТ Нинларо ® |
| Иматиниб* (Imatinibum) | Албитиниб Генфатиниб Гистамель Глемихиб ® Гливек ® Иглиб ® Имаглив ® Иматиб Иматиниб Иматиниб Гриндекс Иматиниб Д-р Редди'с Иматиниб медак Иматиниб Форсайт Иматиниб-Актавис Иматиниб-Альвоген Иматиниб-Сигардис Иматиниб-Тева Иматиниб-ТЛ Иматиниба мезилат Иматиниба мезилат α-форма Иматиниба мезилат форма X Иматиниба мезилат форма Альфа Имвек Неопакс ® Филахромин ® Филахромин ® ФС Цитониб |
| Кабозантиниб* (Cabozantinibum) | Кабометикс ® |
| Кобиметиниб* (Cobimetinibum*) | Котеллик ® |
| Кризотиниб* (Crizotinibum*) | Ксалкори ® |
| Лапатиниб* (Lapatinibum) | Тайверб ® |
| Ленватиниб* (Lenvatinib) | Ленвима ® |
| Мидостаурин* (Midostaurini) | Митикайд |
| Нилотиниб* (Nilotinibum) | Нилотиниб-натив Нилотиниба гидрохлорида моногидрат Тасигна ® |
| Нинтеданиб (Nintrdanibum) | Варгатеф ® |
| Осимертиниб (Osimertinibum) | ОСИМЕРТИНИБА МЕЗИЛАТ Тагриссо |
| Пазопаниб* (Pazopanibum) | Вотриент ® Пазопаниб Пазопаниб-ТЛ Пазопаниба гидрохлорид ПОТАРБИН ® |
| Палбоциклиб* (Palbociclibum) | Ибранса Итулси |
| Регорафениб* (Regorafenibum) | Стиварга ® |
| Рибоциклиб* (Ribociklibum) | Кискали Рисарг |
| Руксолитиниб* (Ruxolitinibum) | Джакави ® |
| Сорафениб* (Sorafenibum) | Нексавар Сорафениб Сорафениб геми-тозилат моногидрат Сорафениб-натив Сорафениба тозилат |
| Сунитиниб* (Sunitinibum) | Сунитиниб-нaтив Сунитиниба малат Сутент ® |
| Темсиролимус* (Temsirolimusum) | Торизел |
| Траметиниб* (Trametinibum) | Мекинист ® |
| Церитиниб* (Ceritinibum) | Зикадия ® |
| Эверолимус* (Everolimusum) | Афинитор ® Сертикан ® Эверолимус 2% Эверолимус 9,09% |
| Эрлотиниб* (Erlotinibum) | Тарлениб Тарцева ® Эрлотиниб Эрлотиниб - натив Эрлотиниба гидрохлорид |
Еще много интересного
Все права защищены.
Не разрешается коммерческое использование материалов.
Информация предназначена для медицинских специалистов.
Открытие системы внутриклеточной передачи внешнего сигнала обеспечило возможность разработки нового поколения противораковых препаратов. Эти препараты блокируют белковый синтез в цепочке передачи сигнала и клеточное деление. Оба процесса жизненно важны для нормальной клетки. Для передачи внешнего сигнала в клетке существует много альтернативных путей.
Поэтому действие препарата на опухоль будет зависеть от того, в какой степени в опухолевых клетках реализуется тот или иной путь его передачи.
Ростовые факторы и их рецептор. Рецепторы тирозинкиназ (RTK). Действие RTK схематически представлено на рисунке ниже. К числу лигандов, запускающих систему передачи сигнала, относятся эпителиальный ростовой фактор (EGF), трансформирующий ростовой фактор-а (TGF-а), ростовой фактор эндотелия сосудов (VEGF) и их рецепторы HER 1-4. Существует два подхода к разработке лекарственных средств:
• получение моноклональных антител, которые связываются с ростовыми факторами или с клеточными рецепторами, тем самым блокируя передачу сигнала;
• поиск соединений, способных связываться с киназой, или с критическими компонентами системы реализации сигнала. Один из наиболее удачных примеров использования моноклональных антител — разработка препарата Трастузумаб (Герцептина). Он представляет собой моноклональные антитела человека, которые блокируют HER-2. Показано, что препарат В последнее время в клиническую практику вошло несколько низкомолекулярных ингибиторов тирозинкиназ.
Они проявляют некоторую, хотя и не абсолютную, специфичность к какой-либо определенной киназе. С-abl представляет собой цитоплазматическую тирозинкиназу, которая в результате транслокации 9;22, происходящей при хроническом миелобластном лейкозе, образует ковалентно-связанный комплекс с bcr. Функционирование комплекса bcr/abl является существенным фатором, ответственным за рост лейкозных клеток. Иматиниб представляет собой соединение, которое блокирует функции комплекса.
Препарат оказывает высокий и продолжительный противоопухолевый эффект у больных хроническим миелобластным лейкозом. Кроме того, он подавляет гиперэкспрессию c-KIT тирозинкиназы, которая происходит в клетках опухолей стромы желудочно-кишечного тракта, и используется как основное терапевтическое средство для лечения больных с этими опухолями.
Гефитиниб блокирует EGF-рецептор тирозинкиназы. Препарат проявляет активность у 10% больных с распространенным немелкоклеточным раком легкого и у 50% больных со стабилизировавшимся опухолевым процессом. Рандомизированные испытания препарата, назначаемого совместно с химиотерапевтическими средствами, не показали увеличения выживаемости больных. Гефитиниб оказывает токсическое действие на легкие (что может приводить к снижению выживаемости), вызывает кожную сыпь и диарею.
Эрлотиниб представляет собой ингибитор EGF-рецептора тирозинкиназы, который применяется перорально, и эффективен при распространенном немелкоклеточном раке легкого. В настоящее время исследуется возможность его применения в схемах комбинированой терапии этого и других видов рака. Препарат оказывает токсический эффект на роговицу и сердечную деятельность, а также вызывает появление сыпи и диарею.
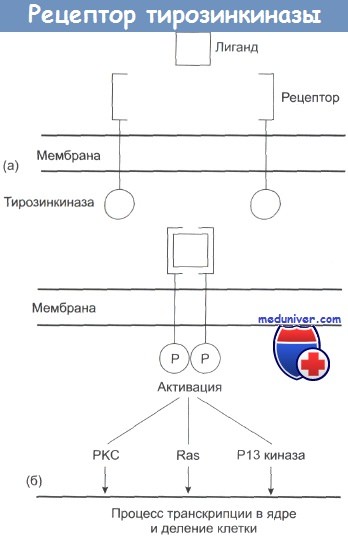
Функционирование рецептора тирозинкиназы.
(а) Рецептор расположен на наружной, а тирозинкиназа — на внутренней стороне клеточной мембраны,
(б) Присоединение лиганда приводит к димеризации и к активации тирозинкиназы за счет ее фосфорилирования (Р).
Этот процесс приводит к активации протеинкиназы С (РКС), Ras и Р13 киназы, которые запускают процесс транскрипции и синтез ДНК.
Активация онкогена ras является существенным фактором злокачественного роста. До активации белки семейства ras должны модифицироваться при участии фермента фарнезилтрансферазы.
В модельных экспериментах ингибиторы этого фермента проявляют противоопухолевое действие.
Известно много изоформ этого фермента. Первым соединением, испытанным в клинике, был бриостатин. Он проявил небольшую эффективность. Основной токсический эффект препарата — развитие миалгии. В настоящее время его испытывают при комбинированном применении. Стауроспорин действует на каталитический центр РСК и на первой фазе клинических испытаний препарат проявил противоопухолевую активность.
В плазме крови это соединение и его производные связываются с кислыми гликопротеинами, что увеличивает срок его выведения из организма. В настоящее время соединения проходят испытания при совместном применении со стандартными противоопухолевыми препаратами.
Циклинзависимые киназы являются важным компонентом механизма регуляции клеточного цикла. В настоящее время различные ингибиторы киназ проходят первую фазу клинических испытаний. Наиболее полно исследован флавопиридол, который оказался эффективным по отношению к различным опухолям. Токсические проявления включают миалгию и диарею. Испытываются также другие средства.
Металлопротеазы клеточного матрикса представляют собой секретируемые ферменты, участвующие в прохождении клеток через соединительную ткань. Они секретируются в неактивной форме и при активации расщепляются. Активность этих ферментов регулируется тканевыми ингибиторами металлопротеаз. Вероятно, эти ферменты играют важную роль в локальном росте опухолей и в их метастазировании. Наиболее полно исследованным соединением этого типа является маримистат.
На 2-й стадии испытаний этот агент предотвращал увеличение уровня опухолевых маркеров, однако при более обширных исследованиях целесообразность его применения в клинике не подтвердилась. Основным токсическим осложнением при применении маримистата является миалгия.

Группа так называемых блокаторов или ингибиторов роста рака. К данному типу биологической терапии относят:
- ингибиторы тирозинкиназы;
- ингибиторы протеасы;
- ингибиторы MTOR;
- ингибиторы PI3K (фосфатидилинозитол-3-киназы).
Достать лекарства от рака с гарантией оригинального происхождения препарата просто, если вы обратились в компанию Tlv.Hospital.
Мы предлагаем сертифицированные фармацевтические группы для традиционных методов коррекции онкологии и реализации авторских программ.
Закажите ингибиторы (блокаторы) роста раковых новообразований для выполнения терапевтического протокола в отечественной клинике или оформитесь на лечение в Израиле через официального представителя Израильской ассоциации компаний медицинского туризма - сервис Tlv.Hospital.
Факторы роста опухоли
Факторы роста – это химические вещества, производимые организмом для контроля роста клеток. Существует много различных типов факторов роста, и все они работают по-разному. Некоторые из них передают информацию, каким видом клетки должна стать данная, конкретная клетка. Другие побуждают клетки расти и делиться; есть те, которые передают информацию, когда клетка должна перестать расти или умереть.
Факторы роста работают, подключаясь к рецепторам на поверхности клеток. Они посылают сигнал внутрь клетки, запуская целую сеть сложных химических реакций.
Существует целый ряд различных факторов роста:
- Эпидермальный фактор роста (EGF) – контролирует рост клеток.
- Фактор роста эндотелия сосудов (VEGF) - координирует развитие кровеносных сосудов.
- Тромбоцитарный фактор роста (PDGF) - контролирует развитие сосудов и рост клеток.
- Фактор роста фибробластов (FGF) – отвечает за рост клеток.
Каждый фактор роста присоединяется к соответствующим рецепторам на поверхности клетки, чтобы оказывать воздействие на нее.
Ингибиторы факторов роста блокируют факторы, которые дают сигнал раковым клеткам делиться и расти. Ученые разрабатывают различные способы, чтобы осуществить это:
- Снизить содержание факторов роста в организме.
- Блокировать рецепторы факторов роста на клетке.
- Противодействовать сигналам внутри клетки.
Большинство этих методов работают, блокируя процессы передачи сигнала, которые используют злокачественные клетки, чтобы начать деление.
Раковые клетки обладают повышенной чувствительностью к факторам роста опухоли. Поэтому если есть возможность заблокировать их, можно остановить рост некоторых видов онкологии. Ученые разрабатывают различные ингибиторы для разных типов факторов роста.
Есть сложности с классификацией различных типов биологической терапии, поскольку они часто пересекаются. Некоторые ингибиторы факторов роста блокируют рост кровеносных сосудов в растущей опухоли. Такое же действие оказывают моноклональные антитела.
Существуют различные типы ингибиторов, их можно сгруппировать в соответствии с химическими веществами, которые они блокируют.
Виды ингибиторов роста рака
Ингибиторы тирозинкиназы также называют ИТК. Они блокируют ферменты под названием тирозинкиназы. Эти ферменты помогают передавать сигналы роста к клеткам. Таким образом, предотвращают рост и деление клетки. Может быть блокирован один тип тирозинкиназы или несколько. ИТК, оказывающие воздействие на несколько видов ферментов, называют мультиингибиторами.
ИТК, которые применяют в лечебной практике, а также в рамках клинических испытаний:
- Afatinib (Giotrif)
- Axitinib (Inlyta)
- Bosutinib (Bosulif)
- Crizotinib (Xalkori)
- Дазатиниб (Sprycel)
- Эрлотиниб (Tarceva)
- Гефитиниб (Иресса)
- Иматиниб (Гливек)
- Лапатиниб (Tyverb)
- Нилотиниб (Tasigna)
- Pazopanib (Votrient)
- Регорафениб (Stivarga)
- Сорафениб (Nexavar)
- Сунитиниб (Сутент)
Данные препараты принимают в таблетках или в капсулах, обычно один или два раза в день.
Противоопухолевые препараты - ингибиторы протеасомы
Протеасомы – крошечные структуры всех клеток, по форме напоминающие бочку. Они помогают расщеплять белки, которые не нужны клетке, на более мелкие части. Эти белки потом используются для создания новых, необходимых белков. Работу протеасом блокируют ингибиторы протеасом. Это вызывает накопление нежелательных белков в клетке, приводя к ее смерти.
Бортезомиб (Velcade) – ингибитор протеасом, который применяют в лечении меланомы. В организм его вводят внутривенно.
MTOR – тип белка под названием протеинкиназа. Он воздействует на клетки, чтобы они синтезировали химические вещества под названием циклины, которые способствуют развитию клеток. Кроме того, они содействуют синтезу белков клетками, провоцирующих развитие новых кровеносных сосудов, которые необходимы опухолям.
Некоторые типы белка mTOR одновременно способствуют росту злокачественных клеток и созданию новых сосудов. Ингибиторы таких белков являются инновационными препаратами, блокирующими рост опухолевого процесса. К ингибиторам данного белка относят:
- Темсиролимус (Torisel)
- Эверолимус (Afinitor)
- Deforolimus
PI3K (фосфатидилинозитол-3-киназы) – группа близкородственных белков киназ. Они выполняют несколько действий в клетках. Например, активируют другие белки – к примеру, mTOR. Активация PI3K приводит к росту и делению клеток, развитию кровеносных сосудов, помогает клеткам передвигаться.
При некоторых видах рака PI3K постоянно активированы, что означает бесконтрольный рост раковых клеток. Исследователи разрабатывают новые методы лечения, которые блокируют PI3K, что останавливает рост злокачественных клеток и приводит к их гибели. Этот тип ингибитора пока доступен только в рамках клинических испытаний. Необходимо некоторое время, прежде чем убедиться, что препарат эффективен в лечении рака.
Ингибиторы гистондеацетилазы также называют ингибиторами HDAC или HDIS, ингибиторами селективного действия. Они блокируют действие группы ферментов, которые удаляют вещества из ацетильной группы конкретных белков. Это останавливает рост и деление злокачественных клеток, а иногда и полностью их уничтожает.
Ингибиторы гистондеацетилазы – новый тип ингибиторов факторов роста. Препараты, которые используются в лечении рака и в рамках клинических испытаний:
- Vorinostat (Zolinza)
- Belinostat
- Panobinostat
- Entinostat
- Mocetinostat
Данные блокаторы нацелены на группу белков под названием Hedgehog pathway. У развивающегося эмбриона эти белки посылают сигналы, которые помогают клеткам расти в правильном направлении и в правильном месте. Данный белок также контролирует рост кровеносных сосудов и нервов. У взрослых Hedgehog pathway обычно не активен. Но у некоторых людей изменения в генах включают его. В настоящее время разработаны блокаторы Hedgehog pathway, которые выключают белок и останавливают рост рака.
Этот вид биологической терапии достаточно новый. Vismodegib (Erivedge) – пример такого ингибитора, участвующего в клинических испытаниях.
Опухоль нуждается в хорошем кровоснабжении, чтобы поступали питательные вещества, кислород и удалялись отходы. Когда она достигает в ширину 1-2 мм, ей необходимо вырастить новые кровеносные сосуды, чтобы увеличить объем необходимых поступающих веществ. Некоторые раковые клетки создают белок под названием фактор роста эндотелия сосудов (VEGF). Этот белок прикрепляется к рецепторам на клетках, выстилающих стенки кровеносных сосудов внутри опухоли. Эти клетки называются эндотелиальными. Они дают импульс к росту кровеносных сосудов, чтобы опухоль могла расти.
Ангиогенез означает рост новых кровеносных сосудов. Если удается остановить создание новых сосудов, снижается рост опухолевого процесса, а иногда и уменьшается. Ингибиторы ангиогенеза как раз направлены на остановку создания новых кровеносных сосудов у опухоли.
Существуют разные препараты, блокирующие рост кровеносных сосудов:
- Ингибиторы, блокирующие фактор роста (VEGF) от присоединения к рецепторам на клетках, выстилающих кровеносные сосуды. Это останавливают развитие сосудов. Таким препаратов является бевацизумаб (Авастин), которые также представляет собой моноклональное антитело.
- Ингибиторы, блокирующие передачу сигналов. Некоторые препараты останавливают передачу сигналов о росте от VEGF рецепторов к клеткам кровеносных сосудов. Такие препараты также называют блокаторами факторов роста или ингибиторами тирозинкиназы. Сунитиниб (Сутент) – один из видов ИТК, блокирующий сигналы роста внутри клеток кровеносных сосудов. Его применяют в лечении рака почек и при редком типе рака желудка – стромальных опухолях.
- Ингибиторы, влияющие на передачу сигналов между клетками. Некоторые препараты оказывают действие на химические вещества, которые клетки используют, чтобы подавать сигналы о росте друг другу. Это может остановить процесс развития кровеносных сосудов. Такими препаратами являются талидомид и леналидомид (Revlimid).
Все препараты способны вызывать побочные эффекты, у всех – разные. Но есть несколько общих потенциальных нежелательных последствий:
- усталость;
- диарея;
- сыпь на коже или потеря цвета;
- стоматит;
- слабость;
- утрата аппетита;
- низкие показатели крови;
- отеки.
Основным преимуществом таргетной терапии перед классическими способами лечения онкологических заболеваний является высокая специфичность, избирательность лекарственного препарата на клетки мишени и минимальное влияние на организм. Назначение таргетной терапии зависит от наличия специфических рецепторов в самих опухолевых клетках. Наличие этих рецепторов определяется иммуногистохимическим анализом либо FISH — исследованием биоптата. Таргетные препараты применяют для стабилизации злокачественного процесса и перевода его из стадии активного развития в хроническую, снижения дозы химиопрепаратов или лучевой нагрузки, для предупреждения рецидива рецидива рака и подавления роста метастазов, а также в случаях, когда химиотерапия противопоказана (пожилые, пациенты в тяжелом состоянии).
Существует несколько основных групп таргетных препаратов, выделяемых по механизму их действия:
Бевацизумаб (Авастин) –моноклональные антитела блокирующие васкулярный эндотелиальный фактор роста (VEGF). Препарат устраняет разрастание сосудов раковой опухоли. Уже на первом курсе терапии дает заметное уменьшение сосудистой сетки раковой опухоли, снижается ее кровенаполнение и, следовательно, рост опухоли замедляется. Затем рак переходит из стадии разрастания в стабильную хроническую стадию. Применение бевацизумаба позволяет существенно повысить эффективность при лечении химиотерапией злокачественных опухолей молочной железы, легкого, почек, толстой кишки, а также глиобластомы головного мозга.
Трастузумаб (Герцептин) – антитела против эпидермального фактора роста (Her2/neu). Применяется в лечении рака молочной железы, рака желудка, рака поджелудочной железы. Выживаемость пациентов увеличивается на 40%, в два раза снизился показатель возникновения рецидива.
Цетуксимаб (Эрбитукс) – моноклональные антитела блокирующие рецептор эпидермального фактора роста (EGFR) , относящихся к семейству Her. Ингибирует пролиферацию и индукцирует апоптоз опухолевых клеток человека, экспрессирующих РЭФР. Применяется при раке толстого кишечника, раке голова и шеи.
Панитумумаб (Вектибикс) – человеческие моноклональные антитела, блокирующие рецептор эпидермального фактора роста (EGFR). Используется при метастатическом колоректальном раке, при этом происходит увеличение выживаемости без прогрессии опухоли.
Ритуксимаб (Ацеллбия, Мабтера) – связывается с трансмембранным антигеном CD20. Этот антиген экспрессируется более чем в 90% В-клеточных неходжкинских лимфом, но отсутствует в нормальных плазматических клетках и здоровых тканях. При связывании ритуксимаба и антигена CD20 индуцируется лизис (разрушение) опухолевых клеток.
Гефитиниб (Иресса) – является низкомолекулярным ингибитором протеинкиназы тирозинкиназного домена EGFR. Тормозит рост опухоли, метастазирование и ангиогенез, а также ускоряет апоптоз опухолевых клеток. Применяется для лечения железистого рака легкого. Показал наивысшую эффективность при лечении химиотерапией рака легкого у некурящих женщин, его применение способствует уменьшению размеров опухоли у большинства пациентов. Также используется для облегчения состояния пациента при отсутствии улучшений от предшествующего лечения.
Эрлотиниб (Тарцева) – является ингибитором домена EGFR. Понижает или блокирует разрастание опухоли, облегчает самочувствие больных, увеличивает выживаемость и способствует устранению симптомов болезни, таких как боль, одышка и кашель. Используется для лечения метастатического рака почки, рака печени, рака поджелудочной железы, плоскоклеточного рака пищевода, а также меланомы и глиобластомы.
Сорафениб (Нексавар) – мультикиназный ингибитор, подавляет многочисленные внутриклеточные киназы (с-CRAF, BRAF и мутантную BRAF) и киназы, расположенные на поверхности клетки (KIT, FLT-3, RET, VEGFR-l, VEGFR-2, VEGFR-3 и PDGFR-β). Используется для лечения метастатического рака почки, первичного рака печени. Уменьшает пролиферацию опухолевых клеток, облегчает самочувствие больных и увеличивает продолжительность жизни пациента.
Лапатиниб (Тайверб) – обратимый, селективный ингибитор внутриклеточной тирозинкиназы, связывающийся с EGFR (erbB1) и HER2/neu (erbB2). Назначается при обширном и метастатическом раке молочной железы.
Иматиниб (Имаглив, Гливек, Неопакс, Филахромин, Гистамель, Генфатиниб) – ингибитор протеинтирозинкиназы (Bcr-Abl тирозинкиназы). Bcr-Abl тирозинкиназа — аномальный фермент, продуцируемый филадельфийской хромосомой при хроническом миелолейкозе. Подавляет пролиферацию и индуцирует апоптоз Bcr-Abl-позитивных клеточных линий, а также молодых лейкозных клеток с положительной филадельфийской хромосомой при хроническом миелолейкозе. Ингибирует пролиферацию и индуцирует апоптоз клеток стромальных опухолей ЖКТ, экспрессирующих c-kit мутации. Используется в лечении хронического миелолейкоза и гастроинтестинальных стромальных опухолей.
Эверолимус (Афинитор, Сертикан) — ингибитор пролиферативного сигнала FRAP (ключевой регуляторный белок, который управляет клеточным метаболизмом, ростом и пролиферацией). Является активным ингибитором роста и пролиферации опухолевых клеток, эндотелиальных клеток, фибробластов и гладкомышечных клеток кровеносных сосудов. Снижает риск прогрессирования заболевания и смерти больных на 67% у пациентов с распространенным или метастатическим почечно-клеточным раком, прогрессирующим после предшествующей терапии ингибиторами тирозиновых киназ.
Темсиролимус (Торизел) – ингибитор пролиферативного сигнала mTOR (ключевой регуляторный белок, который управляет клеточным метаболизмом, ростом и делением клеток). Ингибирование активности фермента mTOR-киназы приводит к прекращению роста в GI фазе опухолевых клеток, в результате чего происходит селективное нарушение трансляции белков, регулирующих клеточный цикл. Приводит к торможению развития кровеносных сосудов, питающих опухоль. Применяется при распространенном почечно-клеточном раке в качестве терапии первой линии.
Ингибитор протеинкиназы представляет собой тип ингибитора фермента , который блокирует действие одного или более протеинкиназ . Протеинкиназы ферментов , которые добавляют фосфат (PO 4 ) группа в белка , и могут модулировать его функцию.
Фосфатные группы обычно добавляют к серин, треонин, тирозин или аминокислот на белок: большинство киназ действуют на обоих серина и треонина, что тирозинкиназы действуют на тирозин, а также ряд ( двойной специфичностью киназы ) действуют на всех трех. Есть также протеинкиназы , которые фосфорилируют другие аминокислоты, в то числе гистидинкиназ , которые фосфорилируют остатки гистидина.
Фосфорилирование регулирует многие биологические процессы, и ингибиторы протеинкиназы может быть использованы для лечения заболеваний, в связи с гиперактивными протеинкиназами (в том числе мутантных или избыточно экспрессируются киназ при раке) или для модулирования функции клеток, чтобы преодолеть другие драйвера заболевания.
содержание
- 1 Клиническое применение
- 2 Примеры
- 3 Сравнение доступных агентов
- 4 Смотрите также
- 5 Ссылки
- 6 Внешние ссылки
Клиническое применение
Ингибиторы киназ , такие как дазатиниб часто используются при лечении рака и воспаления .
Некоторые из ингибиторов киназы , используемых при лечении рака являются ингибиторами тирозинкиназы . Эффективность ингибиторов киназ на различных раковых заболеваниях может варьироваться в зависимости от пациента к пациенту.
Примеры
В настоящее время существует несколько препаратов, запущенных или в процессе развития, которые нацелены на протеинкиназы и рецепторы, которые активируют их:
| название | цель | Компания | Учебный класс | одобрение FDA |
|---|---|---|---|---|
| Adavosertib | Wee1 | AstraZeneca | Малые молекулы | Еще нет |
| Afatinib | EGFR / ErbB2 | Boehringer Ingelheim | Малые молекулы | 2013 рак легких немелкоклеточного |
| Axitinib | VEGFR1 / VEGFR2 / VEGFR3 / PDGFRB / с-KIT | Пфайзер | Малые молекулы | 2012 почечно - клеточный рак |
| Bosutinib | BCR-ABL / SRC | Пфайзер | Малые молекулы | 2012 Хронический миелоидный лейкоз |
| Cetuximab | EGFR | Imclone / BMS | Моноклональные антитела | 2006 Mar (ПРГШ) |
| Cobimetinib | MEK | Exelixis / Genentech - Рош | Малые молекулы | 2015 Ноябрь (Advanced меланомы с мутацией BRAF) в комбинации с Vemurafenib (BRAF) |
| Crizotinib | ALK / Met | Пфайзер | Малые молекулы | 2011 Август (НМРЛ с мутацией Alk) |
| Cabozantinib | RET / MET / VEGFR2 | Exelixis | Малые молекулы | 2012 Ноябрь (метастатического рака медуллярной щитовидной железы ) |
| Dasatinib | несколько целей | BMS | Малые молекулы | 2006 |
| Entrectinib | TrkA / TrkB / TrkC / ROS1 / ALK | Ignyta | Малые молекулы | Orphan Drug обозначения ( нейробластома 12/14, колоректальный рак , НМРЛ, и 2/15) |
| Erdafitinib | FGFR | Janssen | Малые молекулы | 2018 Breakthrough терапия |
| Erlotinib | EGFR | Genentech | Малые молекулы | 2004 |
| фостаматиниб | Syk | Ригель Фармацевтика / AstraZeneca | Малые молекулы | Еще нет |
| Gefitinib | EGFR | AstraZeneca | Малые молекулы | 2003 немелкоклеточного рака легкого (НМРЛ) |
| ибрутиниб | БТК | Pharmacyclics | Малые молекулы | 2013 |
| иматиниба | BCR-ABL | Novartis | Малые молекулы | 2001 (CML), 2002 (GIST) |
| Лапатиниб | EGFR / ErbB2 | GSK | Малые молекулы | 2007 (HER2 + груди) |
| Lenvatinib | VEGFR2 | Eisai Co. | Малые молекулы | 2015 (щитовидная железа), 2016 (почки) |
| Mubritinib | ? | Takeda | Малые молекулы | Пока нет, возможно, отказались |
| Nilotinib | BCR-ABL | Novartis | Малые молекулы | 2007 |
| Pazopanib | VEGFR2 / PDGFR / с-Kit | GlaxoSmithKline | Малые молекулы | 2009 (РСС) |
| Pegaptanib | VEGF | OSI / Пфайзер | РНК Аптамер | 2004 (AMD) |
| Ruxolitinib | JAK | Incyte | Малые молекулы | 2011 (Миелофиброз) |
| Sorafenib | несколько целей | Onyx / Bayer | Малые молекулы | 2005 декабрь (почки) |
| Sunitinib | несколько целей | SUGEN / Пфайзер | Малые молекулы | 2006 Ян (RCC и GIST) |
| SU6656 | Src, другие | SUGEN | Малые молекулы | Не одобрено |
| Vandetanib | RET / VEGFR / EGFR | AstraZeneca | Малые молекулы | 2011 |
| Vemurafenib | BRAF | Roche | Малые молекулы | 2011 Август (Advanced меланомы с мутацией BRAF) |
Сравнение доступных агентов
| лекарственный | спонсор | цель | Показания к применению | Основные токсические | предупреждение (ы) Черный ящик | МИЗ | D | FR | PC (AU) | PC (США) | FDA AD | EMA AD | TGA А.Д. |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Afatinib | Boehringer Ingelheim | ErbB семья (необратимое) | Расширенный немелкоклеточного рака легкого | Гепатотоксичность, почечная недостаточность, электролитные аномалии ( в основном гипокалиемия ) и интерстициальная болезнь легких (редко). | Никто | - | +++ | - | С | D | 12 июля 2013 | 25 сентября 2013 | 7 ноября 2013 |
| Aflibercept | Bayer , Regeneron | VEGF | Расширенный колоректальный рак и влажная дегенерация желтого пятна . | GI перфорация, кровотечение и гепатотоксичность | Никто | +++ / ++ | +++ / ++ | - | D | С | 21 ноября 2011 | 22 ноября 2012 | 2 апреля 2013 |
| Axitinib | Пфайзер | VEGFR , PDGFR , с-KIT | Почечно-клеточный рак | Дисфункция щитовидной железы, сгустки крови, геморрагия, синдром обратимой задней лейкоэнцефалопатии (редко), GI перфорация / свищ (редко) и электролитные нарушения | Никто | ++ | ++ | - | D | D | 27 января 2012 | 3 сентября 2012 | 26 июля 2012 |
| бевацизумаб | Genentech | VEGF | Колоректальный рак , рак молочной железы , немелкоклеточный рак легкого , рак почки , дегенерация желтого пятна и глиобластомы | Гипертензия, Г.И. перфорация, угасание функции яичников, Г.И. кровотечение, сгустки крови, электролиты аномалия, илеус , застойная сердечная недостаточность , остеонекроза челюсти (редко), некротизирующий фасцият (редко), желчный пузырь перфорация (редко) | GI перфорация, кровотечение и заживления ран | ++ | ++ / + | - | D | С | 26 февраля 2004 | 12 января 2005 | 24 февраля 2005 |
| Bosutinib | Пфайзер | BCR-ABL | Вторая линия Хронический миелолейкоз лечение | Инфекции нижних дыхательных путей, анафилактический шок (редко), электролитные аномалии, сердечно-сосудистые эффекты (особенно QT пролонгации интервала), GI кровотечение (редко), гепатотоксичность и почечной недостаточности. | Никто | ++ / + | +++ | + | N / A | D | 4 сентября 2012 | 27 марта 2013 | N / A |
| Cabozantinib | Exelixis | с-Met , VEGFR2 | Метастатический рак щитовидной железы | Электролит аномалия, гипотензия, периферическая сенсорная нейропатия, Г.И. перфорация / свищ, синдром обратимой задней лейкоэнцефалопатии (редко), сгустки крови и остеонекроза . | GI кровотечение, перфорация и свищи | ++ | +++ / ++ | - | N / A | D | 29 ноября 2012 | N / A | N / A |
| Crizotinib | Пфайзер | АЛК , HGFR , с-МЕТ | Анапластический лимфома киназа -положительного рак легкого немелкоклеточного | Периферийная невропатия, электролитные аномалии, сгустки крови, почек киста, печеночная недостаточность, интерстициальная болезнь легких и кардиотоксичность (вероятно , QT пролонгации интервала). | Никто | ++ | ++ | ++ / + | D | D | 26 августа 2011 | 23 октября 2012 | 27 сентября 2013 |
| Dasatinib | Bristol-Myers Squibb | BCR-ABL , Src , с-KIT | Вторая линия Хронический миелолейкоз лечение | Электролит нарушения, кровоизлияния, задержка жидкости, сердечная недостаточность (редко), инфаркт миокарда (редко) и легочная гипертензия | Никто | +/- | ++ | ++ | D | D | 28 июня 2006 | 20 ноября 2006 | 15 января 2007 |
| Erlotinib | Roche | EGFR | Расширенный немелкоклеточного рака легкого и рака поджелудочной железы | GI кровотечения (редко), печеночная недостаточность (редко), печеночно синдром (редко), кожные реакции EGFR и интерстициальной болезни легких (редко). | Никто | - | +++ / ++ | - | С | D | 18 ноября 2004 | 19 сентября 2005 | 30 января 2006 |
| Gefitinib | AstraZeneca , Teva | EGFR | Расширенный немелкоклеточного рака легкого с мутацией EGFR | Кровотечение, кожные реакции EGFR ( в том числе синдром Стивенса-Джонсона [SJS; редкие] и токсический эпидермальный некролиз [TEN; редкие]), печеночная недостаточность (редко), гепатит (редко), панкреатит (редко) и интерстициальная болезнь легких (редко). | N / A | - | +++ / ++ | - | С | D | 5 мая 2003 (выпуск прекращен) | 24 июня 2009 | 7 сентября 2011 |
| иматиниба | Novartis | BCR-ABL | Первая линия хронический миелолейкоз лечение | Кровотечение, электролитные нарушения, кардиотоксичности (редко), почечная недостаточность (редко), GI перфорация, гепатотоксичность (редко) и рабдомиолиз (редко) | N / A | +++ / ++ | + | ++ | D | D | 10 мая 2001 | 7 ноября 2001 | 13 августа 2001 |
| Лапатиниб | GlaxoSmithKline | HER2 | HER2-положительный рак молочной железы, | Гиперчувствительность (редко), гепатотоксичность (редко), интерстициальная болезнь легких (редко) и сердечно-сосудистые проблемы. | Hepatotoxicity | - | ++ | - | С | D | 13 марта 2007 | 10 июня 2008 | 28 июня 2007 |
| Nilotinib | Novartis | BCR-ABL | Вторая линия хронический миелолейкоз лечение | Гипергликемия, электролитные нарушения, задержка жидкости, панкреатит и кардиотоксичности ( в основном интервала QT пролонгации). | QT пролонгации интервала и электролитные аномалии | ++ | + | + | D | D | 29 октября 2007 | 2 июня 2009 | 17 января 2008 |
| Panitumumab | Amgen | EGFR | Колоректальный рак | Электролит аномалии, анафилаксии, сгустки крови, сепсис и фиброз легких. | Дерматологические реакции и инфузионные реакции | - | + | + | С | С | 10 октября 2006 | 3 декабря 2007 | 20 марта 2012 |
| Pazopanib | GlaxoSmithKline | VEGFR , PDGFR , с-KIT | Почечная карцинома и саркома мягких тканей | Кардиотоксичность ( в основном QT пролонгации интервала , но и сердечная недостаточность [редкость]), сгустки крови, кровотечение, тиреоидные аномалии ( в основном гипотиреоз), глюкоза крови аномалии ( гипогликемия и Гипергликемия ), трепетание-мерцание (редко), гепатотоксичность (редко), GI перфорация / свищ (редко) и синдром обратимой задней лейкоэнцефалопатии (редко). | Hepatotoxicity | - | ++ | - | D | D | 19 октября 2009 | 14 июня 2010 | 30 июня 2010 |
| Pegaptanib | OSI , Пфайзер | VEGF | Влажная дегенерация желтого пятна | Гипертония, катаракта, кровоизлияние, стекловидное тело Floater, транзиторная ишемическая атака , отслойка сетчатки, сахарный диабет и инфекции мочевыводящих путей | Никто | - | +/- | ++ | N / A | В | 17 декабря 2004 | 31 января 2006 | N / A |
| Ponatinib | ARIAD Pharmaceuticals | BCR-ABL , BEGFR, PDGFR , FGFR , ОЭП , SRC , с-KIT , RET , TIE - 2 , FLT3 | T315I-положительный Хронический миелоидный лейкоз и T315I-положительно- Острый лимфобластный лейкоз | Гипертония, пневмония, инфекция мочевых путей, сепсис, GI кровотечение, печеночная недостаточность, сердечно-сосудистые проблемы и сгустки крови. | печеночная недостаточность, сгустки крови и гепатотоксичность | ++ | + | + | N / A | D | 14 декабря 2012 | 1 июля 2013 | N / A |
| ранибизумаба | Novartis | VEGF-A | Влажная дегенерация желтого пятна и макулярный отек ( в том числе диабетического макулярного отека) | Кровотечение (конъюнктивы, стекловидное тело и в месте инъекции), повышенное внутриглазное давление, стекловидное отделение и дегенерацию сетчатки. | Никто | - | - | - | D | С | 10 августа 2012 | 22 января 2007 | 27 февраля 2007 |
| регорафениб | Bayer | RET , VEGFR , PDGFR | Расширенный колоректальный рак , желудочно - кишечные стромальные опухоли | Электролит аномалия, гепатотоксичность, гипотензия, кровотечение, GI свищи, проблемы щитовидной железы и сгустки крови. | Hepatotoxicity | +++ / ++ | ++ | - | D | D | 27 сентября 2012 | 26 августа 2013 | 29 ноября 2013 |
| Ruxolitinib | Novartis | JAK | Миелофиброз | Гиперхолестеринемия , инфекция мочевых путей , опоясывающий герпес , туберкулез и гепатотоксичность | Никто | +++ | - | - | С | С | 16 ноября 2011 | 23 августа 2012 | 3 июля 2013 |
| Sorafenib | Bayer | VEGFR , PDGFR , BRAF , с-KIT и т.д. | Advanced карцинома почек и гепатоцеллюлярной карциномы | Гипертония, периферическая нейропатия, нарушение функции щитовидной железы, сердечно - сосудистые заболевания (например , QT пролонгации интервала, сердечный приступ или сердечная недостаточность), электролитные аномалии, GI перфорация (редко), панкреатит (редко), гепатит (редко), нефротический синдром (редко) и обратимой задней синдром лейкоэнцефалопатии (редко) | Никто | ++ | ++ | - | D | D | 20 декабря 2005 | 19 июля 2006 | 27 сентября 2006 |
| Sunitinib | Пфайзер | VEGFR , PDGFR | Почечно - клеточной карциномы , GI стромальные опухоли, рак поджелудочной нейроэндокринные опухоли | Сгустки крови, сердечно - сосудистые проблемы ( в основном сердечная недостаточность или дисфункция левого желудочка , но и QT пролонгация интервала и трепетание-пуанты), дисфункция щитовидной железы, электролитные аномалии, кожные реакции ( в том числе SJS [редкое] и TEN [редкий]), печеночная недостаточность (редко) и панкреатит (редко). | Hepatotoxicity | + | ++ | + | D | D | 26 января 2006 | 19 июля 2006 | 14 сентября 2006 |
| Tofacitinib | Пфайзер | JAK | Ревматоидный артрит | Инфекции и злокачественные опухоли | Серьезные инфекции и злокачественные опухоли | - | - | - | N / A | С | 6 ноября 2012 | N / A; отказалась 26 апреля 2013 | N / A |
| трастузумаб | Genentech | HER2 | Рак молочной железы (или для метастатического заболевания или адъювантной терапии), метастатический рак желудка | Застойная сердечная недостаточность , депрессия, легочная токсичность, инфекция и тахикардия (сердце высокого уровня) | Легочная токсичность, кардиомиопатия и предупреждение путаницы | - | + | + | Би 2 | D | 25 сентября 1998 | 28 августа 2000 | 14 сентября 2000 |
| Vandetanib | AstraZeneca | VEGFR , EGFR , RET , BRK | Расширенный медуллярный рак щитовидной железы | Инфекции мочевыводящих путей , гипертония , QT интервала пролонгация, электролитные аномалии, депрессия, GI перфорация и щитовидная железа аномалия | QT пролонгации интервала | - | ++ | - | D | D | 21 апреля 2011 | 17 февраля 2012 | 31 января 2013 |
| Vemurafenib | Roche | BRAF | Метастатическая злокачественная меланома | Светочувствительность , плоскоклеточный рак и гепатотоксичность | Никто | - | + | + | D | D | 17 августа 2011 | 10 мая 2012 | 17 февраля 2012 |
Примечание:
AD = дата утверждения.
МС = миелосупрессии.
D = Диарея.
FR = Удержание жидкости.
Что касается миелосупрессии, диареи и удержания жидкости идет: +++ средства> 70% пациенты демонстрируют клинический значимую миелосупрессию. ++ означает , что 30-70% пациентов демонстрируют значительный миелосупрессии. + Означает 10-30% пациенты демонстрируют значительные миелосупрессии. - означает , что 0-10% пациентов демонстрируют этот побочный эффект.
Общие ссылки шаблоны приведены, которые отсылаем читателя к соответствующей базе данных лекарств.
Читайте также:

