Химиотерапия при метастатическом раке молочной железы
Здравствуйте, дорогие читатели. Если вы нашли эту страничку, и ищите, какая проводится химиотерапия при раке молочной железы , значит где-то рядом беда. Но помните, что поделившись бедой это разделить ее пополам. Половина ноши — все-таки не целая. Скажите, что можем мы, сделать на расстоянии? Поменьшей мере информировать вас. Ведь самое страшное в серьезных диагнозах это незнание: незнание вообще и методов лечения в частности.
Самые популярные вопросы и немного печальной статистики

Рак молочной железы (РМЖ) насколько это частый недуг? Достаточно частый (с тенденцией к росту и повышению летальности в нашей стране), чтобы о его лечении стоило поговорить! РМЖ на первом месте и по первому пункту (порядка 38% больных раком — это женщины с раком груди) и по второму — погибают 13,2% женщин. Статистика печальна.
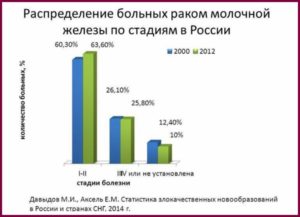
Какими же методами мы боремся с РМЖ? Наши методы в основном сводятся к комбинированному лечению. Но в целом они таковы:
- хирургия;
- лучевая методика ;
- лекарственное лечение;
- комбинация 2 методов;
- комплексная терапия.
И сегодня мы говорим об одном из них лекарственном методе лечения . Итак, х имиотерапия — что это такое и зачем она нужна?
Это метод лечения специальными препаратами. Нужен он чтобы убить клетки рака, и при этом постараться сохранить не раковые клетки работоспособными. Используется в борьбе за жизнь раковых больных как основной или вспомогательный метод.
Это тяжелое для пациента лечение, но часто необходимое. Оно повышает:
- благоприятность прогноза;
- влияет на размер опухоли (в том числе метастазов);
- позволяет контролировать рост опухоли и ее распространение;
- уменьшает размер новообразования и помогает облегчить состояние (опухоль меньше сдавливает окружающие ткани, и это улучшает самочувствие);
- а порой химиотерапия дает шансы на полное выздоровление.

Конкретные препараты, длительность курса лечения, схему подбирает онколог, руководствуясь и состоянием больной, и противопоказаниями к применению определенных лекарств и течением процесса ( стадией болезни, склонностью новообразования выбрасывать метастазы).
Влияет ли на самочувствие человека такое лечение. Да, и, к сожалению, отрицательно. Самые распространенные побочные эффекты такого лечения:
- малокровие (анемия);
- снижение полового влечения;
- отеки;
- неврозы;
- нарушение работы кишечника;
- тошнота, снижение аппетита;
- шум в ушах;
- утомляемость и слабость;
- алопеция (потеря волос).
Субъективно вы будите чувствовать сердцебиение и слабость, одышку и головокружение, шум в ушах (это признаки анемии). Аппетит будет падать из-за интоксикации препаратами и пища с трудом продвигаться по кишечнику (запор) или наоборот пациента беспокоит повышенное газообразование и понос.
И придется надевать на голову уборы, скрывающие потерю волос. Хотя в современных клиниках есть специальные шапочки, уменьшающие алопецию. Правда, в основном в зарубежных.
- меньшую токсичность для здоровых клеток;
- направленное действие токсина (нацеленность на опухолевые клетки);
- временность последствий.
Что важно при лечении рака молочной железы? Самое важное ваше желание победить болезнь. В этом случае уместно выражение вижу цель — не вижу препятствий! А еще придется понимать, что будет сложно и во время лечения и после. И что рецидив тоже возможен, даже если лечение было максимально грамотно подобрано. И это не повод сложить руки.
А еще при лечении рака грудной железы, как и любого другого важна: диета (никаких сладостей, алкоголя, мало жиров до 35%, много овощей и фруктов, питание щадящее и дробное, очень важны витамины А и С, Д и Е). Также же важно избегать попадания под прямые солнечные лучи (загорать противопоказано). Обязателен регулярный осмотр у лечащего врача, если лечение было успешным.
Что такое лечение по протоколу РМЖ? Режим, схема лечения иначе называется протоколом. В каждом мировом центре существует разработанный онкологами проток лечения онкобольных. Лечение может проводится по европейским протоколам. Но если у больного на руках есть протокол другой страны, это может быть учтено лечащим врачом или привлечен независимый консультант для решения проблемы стандартизации схемы. 
Всем ли можно делать химию? Нет. Ее не проводят больным с метастазами в печени и тканях мозга, при истощении и высоких показаниях билирубина в крови.
Лекарственная терапия
Классификаций этого метода прилично. Об одной из них мы говорили в начале статьи — по принципу главенства.
- Либо перед операцией и тогда она будет называться неадьювантной. Такая процедура нужна при РМЖ, как подготовка к вмешательству оперирующего хирурга. Чтобы значительно уменьшить рост новообразования и уменьшить необходимость вмешательства хирурга.
- Или после вмешательства хирурга и это будет уже адьювантный метод. Этот вариант хорош тем, что иногда одну-единственную клеточку рака (которая даст корни новой опухоли) можно не увидеть, а химические препараты, введенные после операции , ее не пропустят. И это значит, снизится риск рецидива.
Кроме этого используют и другие признаки.
Медики делят такое лечение по типу используемых препаратов. Есть 5 основных групп:
- Вещества, влияющие на фактор роста опухолевой ткани (ингибитор фермента роста).
- Средства, разрушающие структуру ДНК атипичных клеток, и препятствующие их делению (например, 5-фторурацил) .
- Алкалоиды фитопрепартов ( травы ), угнетающие опухолевые клетки (болиголов, чистотел и другие), нарушающие дыхательных цикл клетки или иным образом препятствующие ее нормальной жизнедеятельности и делению.
- Препараты , влияющие на метаболизм в клетках опухоли, снижающие его рост (антиметаболитики).
- Специфические антибиотики, направленные на нарушение воспроизводства нуклеиновых кислот и таким образом, губящие клетки рака. Например, Адриамицин. Это средство часто сочетают с применением Циклофосфана.
Есть и другие группы средств. В целом все препараты можно разделить на 2 группы:
В каких случаях назначают те или иные препараты, решает онколог, видящий картину в целом.
Пациенты же предпочитают немного другое деление, связано оно с цветом препарата.
Вот по цвету можно выделить 4 группы терапии химическими препаратами :
Как переносится лечение , зависит и от стадии болезни, и от выносливости организма и от применяемых средств. Самой легкой считается последняя группа препаратов.
Ограничен метод тем, что вводить препарат нужно в определенный момент развития опухоли для достижения максимального эффекта. Если рассматривается эта методика в конкретном случае, больной обязан будет пройти иммуногистохимическое исследование.
Нацелен этот метод не на уничтожение опухолевых клеток как обычно на разрушение микросреды вокруг новообразования (сосудов, стромы), которые поддерживают и питают опухолью. Считается, что переносимость этого метода лечения выше.
Впечатляющие результаты дает комбинация относительно нового препарата авастин и метрономной терапии. Длительность курса определяется врачом. Причем в данном случае она может корректироваться в зависимости от результатов лечения.
Это введение химических препаратов при больших (неоперабельных) размерах опухоли, с целью уменьшить ее до операбельного габарита.
Этот метод применим, если пациент очень стар или ослаблен предыдущим лечением, у больного диагностирована IV ст. рака или формула крови серьезно нарушена. Минус этого лечения в том, что убить все раковые клетки оно не способно. А значит, велика вероятность рецидива. И проводится оно ради улучшения качества жизни пациента и ее продления.
Вы наверняка услышите и о других методах лечения рака (платиновой терапии или горячем лечении, высокодозной химии, но при РМЖ их не используют).
На сегодня разработаны 2 метода процедуры терапии:
- полихимия (в этом случае в организм пациенту вводят несколько препаратов либо одновременно, либо поочередно);
- монохимия (при этом методе вводят пациенту одно лекарство)
Первый способ при правильном выборе медикаментов максимально эффективен. Но не все препараты совместимы и не каждое лекарство может применяться при РМЖ.
Как проходит процедура? Чаще всего средство вливается внутривенно, реже непосредственно в саму опухоль. Некоторые инъекции делают внутримышечно или подкожно, есть и таблетированная химиотерапия (врач выписывает специальные таблетки). Считается, что при лечении РМЖ химическими веществами в большинстве случаев женщина может продолжать обычную жизнь. Но с каждой инъекцией или приемом таблетки самочувствие женщины будет ухудшаться.
Введение химических препаратов имеет свои особенности, связанные с состоянием пациента и особенности патологического процесса. Например, иногда требуется медленное введение лекарства в течение нескольких суток.
Хорошие результаты дает лечение при процедуре раз в 2 недели. Но для больного это тяжелое испытание. И не каждый организм может его выдержать.
Схемы терапии РМХ химическими препаратами
Есть 4 стандартных комбинаций веществ, применяемых при РМЖ (это называется схемой лечения):
- Адриамицин в сочетании с препаратом Таксотер;
- Циклофосфан в сочетании с препаратом Метотрексат, плюс Фторурацил;
- Фторурацил в сочетании с препаратом Адриабластин, плюс Циклофосфан (эта комбинация имеет 2 вариации с использованием одних и тех же химических средств, но в разной дозировке, причем препараты используют с разной частотой);
- Адриамицин в сочетании с препаратом Циклофосфан.
РМЖ склонен к рецидивам, поэтому врачи предпочитают довести курс введения лекарств до конца, даже если пациентке очень плохо и осложнения выражены!
А если лечение не помогает?
Бывает ли, что лечение химиопрепаратами не помогает? Да, бывает и облучение , и резекция помогают не всегда. Если опухоль очень агрессивна, а терапевтического курса было недостаточно. Что делать, если лечение не помогло? Обратиться к врачу. Скорее всего будет назначена вторая химиотерапия.
Есть ли альтернатива при рецидиве ? Некоторые медики утверждают, что да. Но не торопитесь радоваться. Инновационные технологии в лечении рака груди сегодня — это TIL-терапия либо лечение на основе NK-клеток. Это лечение может заменить и опасную химию, помочь в продлении жизни пациентам с раком на IV ст. болезни. Но пока эти инновации общедоступными не стали. И данные утверждения прерогатива американской ассоциации онкологов.
На этом мы заканчиваем обзор темы, и надеемся увидеть вас и ваших друзей на страницах нашего сайта.
Рак молочной железы – наиболее частое злокачественное заболевание у женщин в РФ.
У 3-10 % больных раком молочной железы развитие заболевания связано с наличием мутаций в генах BRCA1, BRCA2, CHECK, NBS1, tP53. У остальных пациентов рак молочной железы имеет спорадический характер, то есть не связан с наличием известных наследственных синдромов.
Общие принципы лечения рака молочной железы:
- рекомендуется составлять план лечения на консилиуме с участием хирурга, химиотерапевта и радиотерапевта
- лечение имеет несколько этапов: операция, лучевая терапия, химиотерапия, причем в разных последовательностях, в зависимости от конкретной клинической картины, стадии, биологического подтипа опухоли.
В ММОЦ химиотерапию проводят высококвалифицированные врачи-онкологи, химиотерапевты, с непосредственным вовлечением в процесс должным образом обученного среднего медицинского персонала, что дает несомненное преимущество в эффективности лечения. Лечение проводится на основании действующих современных клинических рекомендаций (NCCN, RUSSCO, АОР) с использованием оригинальных химиопрепаратов, таргетных препаратов, иммунопрепаратов.
Кому показана химиотерапия при раке молочной железы?
Рещение о необходимости проведения химиотерапии принимается на мультидисциплинарном консилиуме, так как рак молочной железы – это гетерогенная болезнь. Показания к химиотерапии зависит от многих факторов: молекулярно-биологического подтипа опухоли, распространенности процесса (первично-операбельный, местнораспространенный или метастатический рак), общего состояния пациента и характера сопутствующей патологии.
Условно химиотерапию при раке молочной железы можно разделить на два типа, если мы говорим не о метастатическом раке молочной железы: неоадъювантная (предоперационная) и адъювантная послеоперационная).
Адъювантная лекарственная терапия проводится в дополнение к локальным (хирургическому и лучевому) методам лечения и позволяет снизить риск рецидива болезни. При планировании адъювантной лекарственной терапии необходимо оценить прогноз, ожидаемую пользу адъювантного лечения, возможные побочные эффекты и сопутствующую патологию, а также учесть предпочтения пациента. Возраст не является ограничением для лекарственной терапии при отсутствии сопутствующей патологии.
Алгоритм назначения адъювантной системной терапии зависит от молекулярно-биологического подтипа и степени распространенности рака молочной железы.
Биологические подтипы РМЖ:
Люминальный А: В большинстве случаев показана только гормонотерапия. Назначение адъювантной ХТ (в дополнение к адъювантной гормонотерапии) должно быть рассмотрено при наличии одного из следующих факторов: большая степень распространения болезни:
- 4 или более пораженных метастазами регионарных лимфатических узлов;
- ≥Т3
- низкая степень дифференцировки ткани опухоли G3
В качестве химиотерапии рекомендуются режимы АС (доксорубицин+циклофосфамид) 4 курса или DC (доцетаксел + циклофосфамид – при противопоказаниях к антрациклинам) 4 курса.
Люминальный В (HER2 отрицательный):
В большинстве случаев химиотерапии в сочетании с гормонотерапией
T1a (≤5 мм) и N0: только адъювантная гормонотерапия. Для остальных больных в дополнение к гормонотерапии:
T1b-2N0 АС (4 курса), DC (4 курса) или CMF (6 курсов)
T3 или N+ 4 курса АС → 4 курса таксанов.
Люминальный В (HER2 положительный): ХТ + анти-HER2 терапия + ГТ
T1a (≤5 мм) и N0 только адъювантная гормонотерапия; химиотерапия и анти-HER2 терапия не показаны
T1b,с (>5 мм, но ≤20 мм) и N0 возможна химиотерапия паклитакселом** (без антрациклинов) в сочетании с трастузумабом** с последующей гормонотерапией
Т2-Т4 (>20 мм) или N+ антрациклины→таксаны + анти-HER2 терапия с последующей гормонотерапией;
при противопоказаниях к назначению антрациклинов может быть рекомендован режим DСН (6 курсов).
HER2 положительный (не люминальный): химиотерапия + анти-HER2 терапия:
T1a (≤5 мм) и N0 системная терапия не показана
T1b (>5 мм, но ≤10 мм) и N0 возможна химиотерапия паклитакселом (без антрациклинов) в сочетании с трастузумабом с последующей гормонотерапией
При Т1с-Т4 (>10 мм) или N+ антрациклины → таксаны + анти-HER2 терапия с последующей гормонотерапией;
при противопоказаниях к назначению антрациклинов рекомендуется режим DСН (6 курсов).
Тройной негативный (протоковый): химиотерапия с включением антрациклинов и таксанов
При T1a (≤5 мм) и N0: системная терапия не показана. В связи с отсутствием убедительных данных об увеличении выживаемости больных тройным негативным, в т.ч. BRCA-ассоциированным раком молочной железы при добавлении производных платины к антрациклинам и таксанам, в рутинной практике включение этих препаратов (производных платины) в режимы адъювантной химиотерапии не рекомендуется. С учетом данных ряда исследований об увеличении частоты полных патоморфологических регрессий при тройном негативном фенотипе включение производных платины в режимы неоадъювантной химиотерапии может быть рассмотрено в индивидуальном порядке.
Неоадъювантная терапия
Неоадъювантная лекарственная терапия рекомендована при соблюдении следующих условий:
- тройной негативный фенотип или положительный HER2 статус;
- доказанный инвазивный первично операбельный РМЖ (T2N0M0, T2N1M0, T3N0M0, T3N1M0) и наличие всех критериев, за исключением размеров опухолевого узла, свидетельствующих о возможности выполнения органосохраняющей операции;
- согласие больной на выполнение органосохраняющей операции, с пациенткой обсуждается необходимость лучевой терапии в случае выполнения органосохраняющего лечения, а также вероятность повторной операции при обнаружении резидуальной опухоли в краях резекции;
- четкие показания к проведению данного вида лекарственной терапии по результатам дооперационного обследования; при отсутствии достаточной информации (например, о размерах опухолевого узла, состоянии подмышечных лимфоузлов, наличии инвазивного компонента при внутрипротоковом РМЖ) на первом этапе показано оперативное лечение с изучением удаленной опухоли.
Назначение неоадъювантной (предоперационной) терапии также проводится в зависимости от биологического подтипа опухоли, согласно действующим клиническим рекомендациям.
Основные принципы неоадъювантной лекарственной терапии
Химиотерапия рецидивного и метастатического рака молочной железы
Рекомендуется проводить химиотерапию следующим категориям больных:
- РМЖ с отрицательными РЭ и РП
- люминальный РМЖ, резистентный к гормонотерапии
- люминальный РМЖ с признаками висцерального криза
Стандарта химиотерапии первой линии рецидивного и метастатического РМЖ нет. Выбор режима должен быть индивидуальным и учитывать особенности опухоли и больного, а также состав и эффективность предшествующей, в т.ч. адъювантной/неоадъювантной ХТ, если таковая проводилась.
Режимы химиотерапии, рекомендуемые при рецидивном и метастатическом раке молочной железы:
АС: доксорубицин 60 мг/м2 в/в в 1-й день + циклофосфамид 600 мг/м2 в/в в 1-й день каждые 3 недели
ЕС: эпирубицин 75 мг/м2 в/в в 1-й день + циклофосфамид 600 мг/м2 в/в в 1-й день 59 каждые 3 недели
FAC: фторурацил 500 мг/м2 в/в в 1-й день + доксорубицин 50 мг/м2 в/в в 1-й день + циклофосфамид 500 мг/м2 в/в в 1-й день каждые 3 недели
FEC: фторурацил 500 мг/м2 в/в в 1-й день + эпирубицин 50–100 мг/м2 в/в в 1-й день + циклофосфамид 500 мг/м2 в/в в 1-й день каждые 3 недели
CAF: циклофосфамид 100 мг/м2 внутрь в 1-й – 14-й дни + доксорубицин 30 мг/м2 в/в в 1-й и 8-й дни, фторурацил 500 мг/м2 в/в в 1-й и 8-й дни каждые 4 недели
пегилированный липосомальный доксорубицин 50 мг/м2 в/в в 1-й день каждые 4 недели (при противопоказаниях к назначению традиционных антрациклинов);
доксорубицин 60–75 мг/м2 в/в в 1-й день каждые 3 недели или 20 мг/м2 в/в еженедельно;
эпирубицин 60–90 мг/м2 в/в в 1-й день каждые 3 недели
Паклитаксел 80 мг/м2 в/в еженедельно
Доцетаксел 75 мг/м2 в/в в 1-й день каждые 3 недели
паклитаксел 80 мг/м2 в/в + карбоплатин AUC2 в/в еженедельно
альбумин-связанный паклитаксел 100–150 мг/м2 в/в в 1-й, 8-й и 15-й дни или 260 мг/м2 в/в в 1-й день каждые 3 недели
CMF: циклофосфамид 100 мг/м2 внутрь в 1-й – 14-й дни + метотрексат 40 мг/м2 в/в в 1-й и 8-й дни + фторурацил 600 мг/м2 в/в в 1-й и 8-й дни каждые 4 недели
Капецитабин 2000–2500 мг/м2 внутрь в 1-й – 14-й дни каждые 3 недели
Винорелбин 25 мг/м2 в/в в 1-й и 8-й дни в/в каждые 3 недели
Винорелбин 60 мг/м2 внутрь в 1-й, 8-й, 15-й дни; с 22-го дня – 80 мг/м2 1 раз в неделю
Гемцитабин 800–1200 мг/м2 в/в в 1-й, 8-й, 15-й дни каждые 4 недели
Гемцитабин 1000 мг/м2 в/в в 1-й и 8-й дни + цисплатин 75 мг/м2 в/в в 1-й день (или карбоплатин AUC5 в/в в 1-й день) каждые 3 недели
циклофосфамид 50 мг/сут. внутрь ежедневно + метотрексат по 2,5 мг внутрь 2 раза в день в 1-й и 2-й дни каждой недели (метрономный режим)
иксабепилон 40 мг/м2 в/в в 1-й день каждые 3 недели (при резистентности к антрациклинам, таксанам, капецитабину)
эрибулин 1,4 мг/м2 в/в в 1-й и 8-й дни каждые 3 недели
этопозид 100 мг/сут. внутрь в 1-й – 10-й дни каждые 3 недели
Рекомендуется химиотерапию с использованием одной и той же комбинации продолжать до прогрессирования болезни, доказанного клинически и/или с помощью методов инструментальной диагностики, или неприемлемой/дозолимитирующей токсичности.
Длительная стабилизация болезни расценивается как положительный эффект лечения и не должна являться основанием для прекращения или смены терапии в отсутствие неприемлемой/дозолимитирующей токсичности.
Режимы лекарственной терапии HER2-положительного рецидивного и метастатического рака молочной железы:
Трастузумаб 2 мг/кг (нагрузочная доза 4 мг/кг) в/в еженедельно или 6 мг/кг (нагрузочная доза 8 мг/кг) в/в в 1-й день каждые 3 нед. в сочетании с одним из следующих режимов:
паклитаксел 60 мг/м2 в/в в 1-й, 8-й, 15-й дни каждые 4 нед. + карбоплатин AUC2 в/в в 1-й, 8-й, 15-й дни каждые 4 недели
паклитаксел 80 мг/м2 в/в еженедельно
доцетаксел 75 мг/м2 в/в в 1-й день каждые 3 недели
винорелбин 25 мг/м2 в/в в 1-й и 8-й дни в/в каждые 3 недели
винорелбин 60 мг/м2 внутрь в 1-й, 8-й, 15-й дни; с 22-го дня – 80 мг/м2 1 раз в неделю
капецитабин 2000 мг/м2 внутрь в 1-й – 14-й дни каждые 3 недели
циклофосфамид 50 мг/сут. внутрь ежедневно + метотрексат по 2,5 мг внутрь 2 раза в день в 1-й и 2-й дни каждой недели (метрономный режим)
эрибулин 1,4 мг/м2 в/в в 1-й и 8-й дни каждые 3 недели
гемцитабин 800–1200 мг/м2 в/в в 1-й, 8-й, 15-й дни каждые 3 недели
гемцитабин 1000 мг/м2 в/в в 1-й и 8-й дни + цисплатин 75 мг/м2 в/в в 1-й день (или карбоплатин AUC5 в/в в 1-й день) каждые 3 недели
Возможно продолжение терапии трастузумабом без химиотерапевтического препарата в случае возникновении непереносимой токсичности последнего.
Пертузумаб 420 мг (нагрузочная доза 840 мг) в/в в 1-й день 1 раз в 3 нед. + трастузумаб 6 мг/кг (нагрузочная доза 8 мг/кг) в/в в 1-й день 1 раз в 3 нед. + таксаны (доцетаксел 75 мг/м2 в/в в 1-й день 1 раз в 3 нед. или паклитаксел 80 мг/м2 в/в еженедельно)
Трастузумаб-эмтанзин 3,6 мг/кг в/в в 1-й день 1 раз в 3 недели
Лапатиниб 1250 мг/сут. внутрь ежедневно + капецитабин 2000 мг/м2 /сут. внутрь в 1-й – 14-й дни каждые 3 недели
Лапатиниб2 1000 мг/сут. внутрь ежедневно + трастузумаб 2 мг/кг в/в еженедельно (нагрузочная доза 4 мг/кг в/в) или 6 мг/кг (нагрузочная доза 8 мг/кг) в/в 1 раз в 3 недели
Режимы гормонотерапии
Ингибиторы ароматазы (летрозол 2,5 мг/сут. или анастрозол 1 мг/сут. или эксеместан 25 мг/сут.) + трастузумаб 6 мг/кг (нагрузочная доза 8 мг/кг) в/в в 1-й день каждые 3 недели
Ингибиторы ароматазы (летрозол 2,5 мг/сут. или анастрозол 1 мг/сут. или эксеместан 25 мг/сут. внутрь ежедневно) + лапатиниб 1500 мг/сут. внутрь ежедневно
Фулвестрант 500 мг в/м 1 раз в мес. (в первый месяц – по 500 мг в 1-й и 15-й дни) + трастузумаб1 6 мг/кг (нагрузочная доза 8 мг/кг) в/в в 1-й день каждые 3 недели
Тамоксифен 20 мг/сут. внутрь ежедневно + трастузумаб1 6 мг/кг (нагрузочная доза 8 мг/кг) в/в в 1-й день каждые 3 недели
Ингибиторы ароматазы (летрозол 2,5 мг/сут. или анастрозол 1 мг/сут. или эксеместан 25 мг/сут. внутрь ежедневно) + трастузумаб 6 мг/кг (нагрузочная доза 8 мг/кг) в/в в 1-й день каждые 3 нед. + лапатиниб 1500 мг/сут. внутрь ежедневно
Эффективность лекарственной терапии при раке молочной железы оценивается каждые 2-3 курса по данным инструментальных обследований (УЗИ, КТ, МРТ), клинической картины (объективного осмотра).
Подготовка к проведению химиотерапии
Необходимо сдать развернутый общеклинический анализ крови с тромбоцитами и лейкоцитарной формулой, общий анализ мочи, биохимический анализ крови (АЛТ, АСТ, билирубин, креатинин, мочевина, общий белок), коагулограмму (при необходимости), ЭКГ с расшифровкой (ЭХО-КГ по показаниям – при проведении таргетной терапии трастузумабом/пертузумабом или назначении антрациклинов). Перечень анализов пациенту выдается при первичной консультации у врача-онколога.
Сколько длится курс химиотерапии?
В целом при раке молочной железы химиотерапия проводится одним днем без длительных 2-суточных введений. В среднем на введение препаратов уходит от 30 минут до 8 часов в зависимости от применяемого режима и назначенной схемы.
Побочные реакции
У любого режима лекарственной терапии есть возможные побочные реакции, о наиболее распространенных вам расскажет лечащий доктор перед первым курсом терапии, даст памятку по методам борьбы и профилактики этих побочных явлений. При правильном взаимодействии врача и пациента данные реакции возможно легко скорректировать, а в некоторых случаях и избежать их.
Восстановление
Химиотерапия воздействует не только на заболевание, но и на организм полностью. Чтобы восстановиться и облегчить состояние, женщина должна следовать рекомендации по специальной диете. При РМЖ органы истощаются, из-за чего находятся в ослабленном состоянии. Важно наполнить организм энергией, придать человеку дополнительных жизненных сил. Добавить организму больше питательных микроэлементов поможет правильная диета и сбалансированное меню. Необходимо особое питание при химиотерапии.
- Суточная норма белков составляет примерно 25% от общего объёма калорий.
- Дневная норма углеводов достигает 80% от количества калорий.
- В сутки обязательно нужна сумма растительных жиров в 25%.
- В правильное питание в обязательном порядке включаются бобовые, зерновые и злаковые, можно есть блюда из фруктов и овощей.
- Ежедневно необходимо следить за употреблением полезных витаминов.
- Важно ежедневно поддерживать в организме достаточное количество жидкости. Суточная норма воды 1,5-2 литра.
- Рекомендуется отходить от привычного объёма либо уменьшить массу употребляемого сахара и животных продуктов.
- Из рациона питания исключаются копчёные, жирные, жареные продукты и консервы.
- Химиотерапия вызывает обезвоживание организма, поэтому рекомендуется обильное питьё.
После химиотерапии в диете делается упор на восстановление и балансировку питательных микроэлементов – белков, жиров, углеводов. Помочь организму окрепнуть способны белковые продукты. Важно сделать рацион более щадящим. Это уменьшит нагрузку на печень, почки и органы пищеварительного тракта.
Рекомендуется добавить в рацион нежирные вареные мясные блюда, омлет, молочные продукты, сливочное масло и морепродукты. Восполнить недостаток элементов калия, витаминов и белковых веществ помогут продукты семейства бобовых, орехи и сухофрукты. Для укрепления организма и восстановления иммунной системы рекомендуется каждый день есть тушеные овощи, свежие фрукты и ягоды. Полезные микроэлементы усилят защиту организма, устранят авитаминоз и улучшат функционирование кишечника.
Для выведения токсинов и вредоносных бактерий, а также для устранения обезвоживания требуется пить 2 литра жидкости в сутки – обязательна чистая вода, травяной чай, компот, свежевыжатые соки. Из рациона необходимо исключить острые, кислые, пряные и избыточно сладкие блюда. Запрещены кофе, крепкие чаи, какао, алкогольные напитки и сладкие мучные продукты.
В развитых странах в структуре онкологической заболеваемости женщин рак молочной железы (РМЖ) занимает 1-е место (26% всех случаев рака).
По данным ВОЗ, в мире ежегодно умирает от РМЖ 590 000 женщин.
В 2006 г. в России рак молочной железы составил 17,8% всех злокачественных опухолей у женщин.
Показатель заболеваемости в 2006 г. составил 65,5 случая на 100 000 населения, абсолютное число заболевших — 48 821. Смертность в 2006 г. равнялась 29,5 случая на 100 000 женского населения, 1-летняя летальность — 11,5%. Мутация генов BRCA1 и BRCA2 увеличивает риск РМЖ.
Выбор метода лечения больных раком молочной железы зависит от стадии заболевания и от биологической характеристики опухоли (степень злокачественности, рецепторный статус, экспрессия HER2).
Ниже приводится классификация РМЖ по системе TNM и группировка по стадиям (табл. 9.17).
Первичная опухоль (Т)
ТХ — недостаточно данных для оценки первичной опухоли.
Т0 — признаков первичной опухоли нет.
Tis — рак in situ.
Tis (DCIS) — протоковый рак in situ.
Tis (LCIS) — дольковый рак in situ.
Tis (Paget's) — рак Педжета соска при отсутствии опухоли в паренхиме железы. При этом рак Педжета в сочетании с опухолью паренхимы оценивают в соответствии с размерами последней.
Т1 — опухоль не более 2 см в наибольшем измерении.
T1mic — микроинвазивный рак размером 0,1 см и менее в наибольшем измерении.
Т1а — опухоль более 0,1 см, но не более 0,5 см.
T1b — опухоль более 0,5 см, но не более 1 см.
T1c — опухоль более 1 см, но не более 2 см.
Т2 — опухоль более 2 см, но не более 5 см в наибольшем измерении.
Т3 — опухоль более 5 см в наибольшем измерении.
Т4 — опухоль любого размера с непосредственным распространением на а) грудную стенку, б) кожу с учетом описанных ниже принципов:
Т4а — опухоль поражает грудную стенку;
Т4b — отек (включая симптом лимонной корки), изъязвление кожи или метастазы в
коже той же молочной железы;
Т4с — сочетание признаков Т4а и Т4b;
T4d — диффузный рак.
Регионарные лимфоузлы (N)
NX — недостаточно данных для оценки регионарных лимфоузлов (например, они были ранее удалены).
N0 — регионарные лимфоузлы не пальпируются.
N1 — пальпируются подвижные подмышечные лимфоузлы с той же стороны.
N2 — пальпируются подмышечные лимфоузлы с той же стороны, спаянные друг с другом или окружающими тканями, либо имеются клинические признаки метастазов в окологрудинных лимфоузлах той же стороны при отсутствии таких признаков для подмышечных лимфоузлов.
N2a — подмышечные лимфоузлы на стороне опухоли спаяны друг с другом или окружающими тканями.
N2b — клинические признаки метастазов в окологрудинных лимфоузлах той же стороны при отсутствии таких признаков для подмышечных лимфоузлов.
N3 — пальпируются подключичные лимфоузлы (лимфоузел) вне зависимости от состояния подмышечных лимфоузлов, либо имеются клинические признаки метастазов в окологрудинных и подмышечных лимфоузлах, либо имеются метастазы в надключичных лимфоузлах, необязательно в сочетании с метастазами в подмышечных или окологрудинных лимфоузлах.
Отдаленные метастазы (М)
MX — недостаточно данных для оценки отдаленных метастазов.
М0 — отдаленных метастазов нет.
M1 — отдаленные метастазы имеются.
Таблица 9.17. Группировка рака молочной железы по стадиям (6-е издание, 2002)

Своеобразное течение РМЖ и биологические особенности этой опухоли обусловливают использование на определенных этапах заболевания всех существующих методов лечения — хирургического, лучевого, гормонального, химиотерапевтического, включая таргетную терапию; однако оптимальная последовательность их применения до настоящего времени остается предметом активных клинических исследований.
По современным представлениям, для выбора оптимальной терапии больной раком молочной железы необходимо иметь сведения о содержании в опухоли рецепторов стероидных гормонов (рецепторов эстрогена (РЭ), рецепторов прогестерона (РП)), экспрессии HER2 и степени злокачественности опухоли, определяемой по степени ее дифференцировки.
С точки зрения биологических особенностей, определяющих возможности лечения, все больные РМЖ делятся на три группы:
1) больные с гормоночувствительными опухолями, содержащими РЭ, РП; в лечении этих больных, как правило, используется гормонотерапия;
2) больные, опухоль которых характеризуется гиперэкспрессией HER2; этим больным показан трастузумаб (Герцептин);
3) больные РМЖ, у которых опухоль не содержит ни рецепторов стероидных гормонов, ни HER2 (так называемые трижды негативные опухоли); при лечении таких больных наиболее перспективна цитотоксическая химиотерапия (XT).
Эти клинические группы соответствуют молекулярным подтипам рак молочной железы (люминальный А и Б HER2-позитивный, базальный нормоклеточный).
Гормонотерапия — один из важнейших методов лечения РМЖ. Около 60% больных РМЖ (а среди пожилых больных до 80%) имеют гормонозависимые опухоли, т.е. опухоли, содержащие РЭ и РП.
Существует прямая корреляция между наличием и уровнем рецепторов стероидных гормонов и эффективностью гормонотерапии. Эффективность лечения РЭ-положительных опухолей составляет 50-60%, тогда как при РЭ-отрицательных злокачественных опухолях молочной железы положительный эффект гормонотерапии отмечается лишь у 5-10% больных. Около 30% больных с неизвестным рецепторным статусом отвечают на гормональные воздействия.
К методам гормонотерапии относятся: хирургическая, лучевая и химическая (с помощью суперагонистов LH-RH) кастрация у женщин с сохранной менструальной функцией, применение антиэстрогенов, ингибиторов ароматазы, прогестинов, андрогенов и их аналогов, кортикостероидов.
В принципе в основе всех методов гормонотерапии рака молочной железы лежит попытка воспрепятствовать стимулирующему воздействию стероидных гормонов (эстрогенов) на клетки опухоли.
У женщин в пременопаузе это может быть достигнуто путем овариэктомии или облучения яичников либо с помощью применения суперагонистов LH-RH, под влиянием которых функционируют яичники. Такая химическая кастрация носит обратимый характер и достигается применением гозерелина (Золадекс) или лейпрорелина, бусерелина.
У женщин в менопаузе синтез эстрогенов происходит в основном в жировой ткани путем реакции ароматизации андрогенов, продуцируемых корой надпочечников, а следовательно, использование ингибиторов ароматазы снижает содержание эстрогенов.
К селективным ингибиторам ароматазы относятся нестероидные — летрозол (Фемара), анастрозол (Аримидекс) — и стероидный ингибитор экземестан (Аромазин).
Антиэстрогены блокируют РЭ в опухоли. В эту группу входят селективные модуляторы эстрогенных рецепторов (SERM) — тамоксифен и торемифен и селективный супрессор эстрогенных рецепторов (SERD) — фульвестрант (Фазлодекс). Эти препараты активны как в пре-, так и в менопаузе.
Менее ясен механизм противоопухолевого действия прогестинов (мегестрол, медроксипрогестерон), которые также используются в гормонотерапии РМЖ.
РМЖ — опухоль, чувствительная к большинству современных противоопухолевых цитотоксических препаратов, прежде всего к антрациклинам — доксорубицину, который эффективен у 40% больных. Аналогичная эффективность и у эпирубицина, митоксантрона, циклофосфамида (35%), метотрексата (35%), фторурацила и тегафура (25 %). В 1990-е годы в клиническую практику вошли таксаны: паклитаксел (Таксол), эффективность 56-60%, доцетаксел (Таксотер) — 57-75%, винорелбин (Навельбин) — 41-51 %, капецитабин (Кселода) вторая линия — 20-36%, гемцитабин (Гемзар) вторая линия — 25%. У больных с гиперэкспрессией HER2 эффективен таргетный препарат трастузумаб (Герцептин) — гуманизированное МКА к EGFR — и лапатиниб (Тайверб, Тайкерб) — двойной ингибитор тирозинкиназы рецепторов EGF (HER2/HER1).
Лекарственная терапия раннего (операбельного) рака молочной железы
Больные с операбельным раком молочной железы нуждаются в дополнительной (адъювантной) лекарственной терапии, улучшающей отдаленные результаты лечения, снижающей риск рецидива заболевания и увеличивающей выживаемость больных. Исключение составляет лишь небольшая прогностически благоприятная группа больных старше 35 лет с высокодифференцированной (G1) гормоночувствительной (РЭ+, РП+) опухолью размером до 1 см, без метастазов в лимфоузлах (T1aN0M0) и без гиперэкспрессии HER2.
Важнейшими прогностическими факторами являются наличие и число пораженных лимфоузлов, размер первичной опухоли, степень злокачественности, определяемая по дифференцировке опухоли (G), возраст больной и состояние ее менструальной функции, содержание РЭ и/или РП в опухоли, а также гиперэкспрессия HER2 (табл. 9.18).
Таблица 9.18. Распределение больных раком молочной железы на категории риска

Рекомендации по выбору методов лечения в зависимости от чувствительности РМЖ к гормонотерапии приведены в табл. 9.19 и 9.20.
Таблица 9.19. Рекомендации по выбору методов лечения в зависимости от чувствительности к гормонотерапии (ГТ)

Примечание: При необходимости назначения XT и тамоксифена прием последнего должен быть начат после завершения XT (ХТ->ГТ) Вопрос относительно последовательности назначения ингибиторов ароматазы и XT (XT + ГТ или ХТ->ГТ) остается дискутабельным У больных в пременопаузе применение аналогов гонадотропин-рилизинг гормона может быть начато одновременно с XT для максимально быстрого достижения менопаузы.
Таблица 9.20. Рекомендации по лечению больных с гормоночувствительными опухолями

Примечание: В круглых скобках указаны лечебные опции, являющиеся предметом дискуссий и оцениваемые в соответствующих клинических исследованиях. Т — тамоксифен; ИА — ингибиторы ароматазы, ГТ — гормонотерапия; ОС — овариальная супрессия
При высоком риске N0 и отсутствии гормональных рецепторов послеоперационно проводится 4-6 курсов химиотерапии с включением антрациклинов (AC, FAC) или 6 курсов CMF. Больным в пременопаузе с положительными рецепторами и N0 после XT назначается тамоксифен на 5 лет. Альтернативой у этой категории пациенток служит выключение функции яичников с назначением тамоксифена.
У больных с низким риском в пременопаузе с N0 используется выключение функции яичников с помощью агонистов LH-RH в течение 2 лет, изучается целесообразность более длительного применения этих препаратов.
У больных в постменопаузе с N0 и положительными рецепторами используются ингибиторы ароматазы либо тамоксифен в течение 5 лет или прием тамоксифена в течение 2-3 лет с последующим переходом на ингибиторы ароматазы (до 5 лет). У больных в постменопаузе адъювантная гормонотерапия на любом этапе ее проведения может включать ингибиторы ароматазы. В ряде исследований было показано, что лечение тамоксифеном неэффективно у НЕR2-позитивных больных, что служит показателем резистентности к тамоксифену.
При высоком риске и N0 даже в менопаузе считается целесообразным назначение химиотерапии, а затем гормонотерапии ингибиторами ароматазы или тамоксифеном. У больных старше 70 лет основой адъювантной лекарственной терапии является тамоксифен.
При N+ в пременопаузе и при количестве метастазов в подмышечных лимфоузлах менее 4 показано проведение 6 курсов антрациклинсодержащих комбинаций CAF, FAC, АС или 6 курсов классического режима CMF с пероральным приемом циклофосфамида. При наличии 4 метастазов и более считается целесообразным назначение более длительной химиотерапии с дополнительным использованием таксанов. Далее при положительных рецепторах назначается тамоксифен на 5 лет.
У больных с сохранной менструальной функцией при поражении не более 3 лимфоузлов и положительных рецепторах допустимо выключение функции яичников с одновременным приемом тамоксифена.
У больных в постменопаузе с положительными рецепторами основой адъювантного лечения считается гормонотерапия (ингибиторы ароматазы или тамоксифен), но при поражении 4 лимфоузлов и более показано на I этапе проведение XT с последующей гормонотерапией. При отрицательных рецепторах в постменопаузе рекомендуется только XT.
Комитет экспертов конференции (St. Gallen, 2009) предложил упростить вопрос выбора показаний к применению гормонотерапии при операбельном РМЖ: все больные, у которых обнаружены РЭ+ (независимо от их уровня), должны получать гормонотерапию. РЭ-положительными считаются все опухоли, в которых при иммуногистохи-мическом исследовании обнаруживается даже минимальное количество РЭ-положительных клеток. При окрашивании более 50% клеток опухоль рассматривается как высокочувствительная к гормонотерапии.
Стандарт гормонотерапии для больных в пременопаузе — это применение тамоксифена либо тамоксифена + выключение функции яичников; ингибиторы ароматазы пациенткам в пременопаузе противопоказаны и могут применяться лишь в случае противопоказаний к использованию тамоксифена, при условии надежного выключения функции яичников по показателю содержания эстрадиола в сыворотке крови (верификация выключения функции яичников желательна даже при назначении ингибиторов ароматазы пациенткам в менопаузе моложе 60 лет). Для женщин в менопаузе предпочтительна гормонотерапия ингибиторами ароматазы, хотя у отдельных больных возможно использование тамоксифена. У больных с высоким риском предпочтительны ингибиторы ароматазы.
Показано, что у больных в менопаузе при рецептор-положительном раком молочной железы длительное применение летрозола (Фемара) по 2,5 мг/сут после окончания 5-летнего приема тамоксифена улучшает эффективность адъювантной гормонотерапии, снижая к 4 годам наблюдения относительный риск рецидива на 42 %.
Современный выбор оптимальных режимов адъювантной химиотерапии достаточно широк и включает использование антрациклинов и таксанов.
Применение антрациклинсодержащих комбинаций позволяет по сравнению с CMF уменьшить риск рецидива на 12%, риск смерти — на 11 % и увеличить 5-летнюю безрецидивную выживаемость на 3,2%, 5-летнюю общую выживаемость — на 2,7%. В США в адъювантном лечении у больных с плохим прогнозом используется паклитаксел после нескольких курсов антрациклинсодержащих комбинаций, в Европе активно ведутся исследования по использованию доцетаксела в адъювантной терапии, показавшие его высокую активность.
У больных с HER2+ РМЖ в рандомизированных исследованиях показано значение адъювантного применения трастузумаба (Герцептин).
На основании предварительного анализа результатов этих исследований международным консенсусом в 2007 г. рекомендовано использование трастузумаба при ранних стадиях HER2+ РМЖ в течение 1 года. Остается неясным вопрос о длительности его применения, целесообразности назначения при N0 и Т 5 лет);
• пожилой возраст;
• метастазы в костях, локорегионарные метастазы, минимальные метастазы в легких;
• гистологически установленная I-II степень злокачественности (G1-G2);
• большая длительность полученной ранее ремиссии в результате предшествовавшей гормонотерапии.
Ответ на гормонотерапию маловероятен в следующих случаях:
• короткий период без метастазирования (
Читайте также:

