Химиотерапия при инфильтрирующем раке
Инфильтративный рак молочной железы – это распространённая онкология среди женщин планеты. Слабый пол подвергается инфильтративному раку груди в числе имеющихся разновидностей злокачественной болезни. Зачастую данная онкологическая патология приводит к летальному исходу. Заболевание характеризует агрессивность поведения и скорость развития поражённого очага.
На ранней стадии рак протекает бессимптомно, из-за чего возникают сложности с его выявлением на начальном этапе. Болезнь протекает скрытно, и пациентки не подозревают наличие в организме атипичного процесса. Злокачественный опасный нарост молочной железы чаще обнаруживают у пожилых женщин. Они находятся в группе серьёзного риска.
Причины развития рака груди
Причина образования инфильтративного рака G2 не выявлена учёными до конца. Существуют теории, описывающие вероятные факторы, провоцирующие онкологическую патологию. По мнению онкологов, человеческий организм подвергается частому травмированию на клеточном уровне, что приводит к мутированию ДНК клеток. Ситуация связана с деятельностью и функциями иммунитета и эндокринной системы. Излишнее количество эстрадиола ведёт к губительным переменам в тканях, попавших под воздействие канцерогенов. Провоцирующий механизм ещё изучается исследователями. Однако врачи отмечают причины, активизирующие онкологический процесс в клетках:

- Возраст свыше 45-50 лет.
- Поздняя беременность после 30 лет.
- Отсутствие беременности.
- Регулярное абортирование.
- Поздняя менопауза.
- Нарушение гормонального уровня в женском организме.
- Длительное применение гормональных средств.
- Раннее половое созревание.
- Генетическая предрасположенность, плохая наследственность – в семье у женщины по женской линии диагностирован рак яичников или молочной железы.
- Патологическая гиперплазия материалов – по результатам биопсии.
- Излишняя масса тела, нездоровое питание, правильная диета, наполненная избыточным количеством животного жира.
- Мутации генов BRCA – в особенности, наблюдаемые у отдельных народов.
- Повышенная чувствительность рецепторов к эстрогену или прогестерону.
- Опухоль, образовавшаяся при участии в процессе специфичных генов.
- Нарушенные сигнальные пути – развитие воспалительного очага, хемотаксис и адгезионный процесс.
Симптомы
На первых стадиях инфильтрирующая карцинома молочной железы протекает без выражения специфических симптомов. Со временем при инфильтрирующем раке наблюдается обширное распространение раковых клеток в груди. Онкологическое заболевание часто выявляют в ходе профилактической диагностики. Инфильтрирующий рак сопровождают такие признаки:

- опухлость тканей;
- ощутимое уплотнение молочной железы;
- проникновение опухолевого образования в близрасположенную ткань;
- сосок втянутый;
- опухоль увеличивается до 10 сантиметров в диаметре;
- атипичные выделения гнойной жидкости, кровь;
- мраморный подтон эпидермиса;
- шелушение кожного покрова;
- чувство жжения и зуда;
- болезненные ощущения при прикосновении к груди.
Проявление даже единичного либо нескольких симптомов выступают предписанием для незамедлительного обращения к врачу и прохождению досконального обследования.
Виды инфильтративного рака груди
Классификация инфильтрирующей карциномы осуществляется на основе месторасположения поражённого участка, гистологической структуры образования и интенсивности дифференцирования. Онкологический процесс подразделяется на типы:
- отёчно-инфильтративный;
- протоковый;
- дольковый;
- неспецифический.
Каждый вид патологии обладает специфическими особенностями и характеристиками.
Отёчно-инфильтративный рак возникает в 5% диагностируемых случаев. Болезнь характеризуется образованием инфильтрата и отёчностью материалов. Диагностика отёчной опухоли затруднена в связи с отсутствием возможности выявить злокачественный процесс во время пальпации. В результате врач может спутать признаки данной онкологии с воспалительным течением. Различают типы патологической болезни – первичный (диффузный) и вторичный (узловой). Диффузно-инфильтративное новообразование отличается:

Также раковый нарост не удаётся увидеть на снимке после маммографии. Узловой вид рака развивается с постепенным появлением отёчности и инфильтрации. По сравнению с предыдущим типом новообразование выявляется во время прощупывания и через маммографию. Симптомы двух видов схожи. После отёка тканей заболевание прогрессирует с большей скоростью.
Узловая форма опухоли имеет ранние метастазы в 95% случаев. У 30-35% женщин при обнаружении онкологической патологии наблюдается поражение полностью всей железы. Картина заметно уменьшает прогноз на выздоровление.
Инфильтрирующий протоковый рак широко распространён по сравнению с прочими опухолями молочной железы. Инфильтрирующая протоковая карцинома с мультифокальным ростом возникает у пациенток старшей возрастной категории. Болезнь образуется в молочном протоке, затем раковая клетка начинает распространяться по близрасположенным тканям. Диагноз инфильтрирующего рака груди устанавливается на основании персональных характеристик онкологической патологии:
- уплотнённая консистенция новообразования;
- овальная форма;
- нечёткие границы, напоминающие звездообразную форму;
- проникновение поражённых клеток в соседнюю здоровую ткань;
- величина опухолевого очага от 0,5 и до 10 см в диаметре;
- отмирание отдельных участков тканей, вызывающих формирование кисты и возникновение микрокальцинатов.
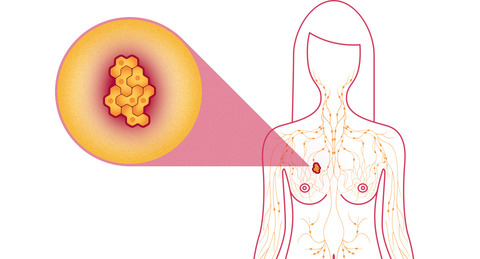
Протоковый вид рака долгое время протекает без признаков специфичности. Пальпация молочных желёз не выдаёт понятных и точных результатов. В ходе развития внутрипротокового новообразования изменяется структура соска, выделяются атипичные жидкости. В отдельных ситуациях кожный покров принимает форму апельсиновой корки. В редких случаях развивается болезнь с преобладающим внутрипротоковым компонентом. Гистология подразделяет раковое образование на виды:
- высокодифференцированный;
- низкодифференцированный;
- усреднённый.
У второго вида высока вероятность метастазирования и рецидива поражённого очага.
Инфильтративный дольковый рак in situ возникает в 10-15% случаев онкологического заболевания женщин. Такая опухоль чаще поражает пациенток старшей возрастной категории. В 50% диагностируемых случаев инфильтрирующий патологический нарост характеризуется двухсторонним симметричным поведением и локализуется на верхнем участке грудной области. Злокачественная раковая клетка формируется в дольке молочных желёз.
Новообразование показывает нечёткую границу и плотную структуру, отличается болезненными ощущениями. Патологические ткани обладают кругообразной формой и локализуются по характеру цепи либо в хаотичном порядке. Первоначальный тип болезни не проявляется. Злокачественный рак диагностируют на поздних этапах. В процессе прогрессирования атипичный процесс доходит до ближайших тканей, располагается на эпителии и рядом с дольковым компонентом.
При запущенной степени развития онкологической болезни возникает сморщивание кожного покрова, втягивается сосок, появляется тяжёлый процесс и последствия в гинекологической области – метастазирование в яичниках и матке. Патология диагностируется по стадии g1 – простой дольковый инвазивный рак. При наличии узлов в долях – g2 и g3 степень – аденокарцинома преобразуется в инфильтративную форму. Прогноз выздоровления позитивный. Определить прогрессирующий рак не составляет труда и удаётся вылечить при помощи консервативной терапии.
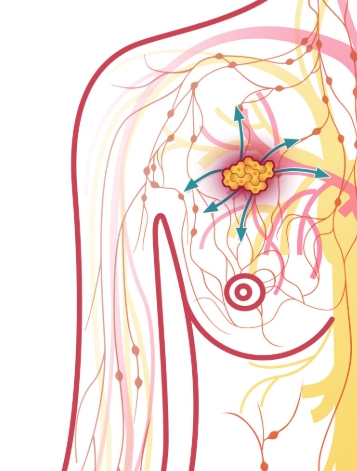
Инфильтративный рак молочной железы неспецифического типа g2 представляет собой группу редких видов онкологических образований инвазивного типа. Группа включает виды:
- коллоидный;
- папиллярный;
- листовидный;
- плоскоклеточная метаплазия;
- тубулярный;
- апокриновый неденокистозный.
Согласно затрагиванию злокачественного течения лимфатических узлов, неспецифическая опухоль подразделяется по прогрессированию на 3 степени:
- 1 степень – поражается лимфоузел в подмышечной части либо возле груди;
- 2 стадия – поражённая клетка проникает в узлы от 4 и до 9;
- 3 этап – более 10 лимфатических узлов подвергаются метастазированию. Раковые клетки распространяются на подключичные лимфоузлы.
Данный тип онкологической болезни встречается редко. Положительной чертой является успешное излечение и благоприятный прогноз на выживаемость среди пациенток.
Диагностика инфильтрирующего рака груди
Первоочередно перед диагностикой врач собирает информацию об истории болезни пациентки. Доктор устанавливает сведения о генетической предрасположенности, наследственной картине, о наличии излечимых ранее болезней гинекологического плана, об ушибах и травмах и патологиях груди. Затем осуществляется внешний осмотр молочных желёз. Центральное место в обследовании занимает плотность структуры опухоли, величина, форма, подвижное состояние и ограниченность железы. Помимо того, врачи проверяют положение близрасположенных надключичных лимфоузлов и в подмышечных впадинах. Полноценная диагностика онкологической патологии состоит из следующих процедур:
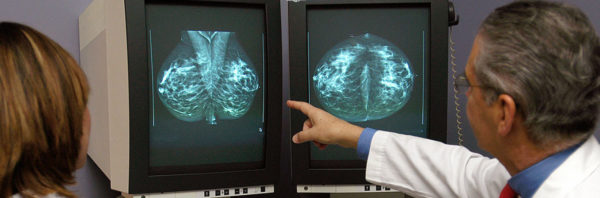
- Инструментальное обследование – проводится обязательно. Применяют единичный либо комплексный метод процедуры:
- Рентгенология (маммография) – выполняется в 2 проекциях (медиолатеральная и кранио-каудальная). Метод помогает обнаружить опухоль величиной от 50 мм и микрокальцинаты, считающиеся достоверными факторами существования в организме онкологического процесса.
- Галактография – применяется в редких случаях. Процедура подразумевает рентген поражённой области. Способ выполняется при выделениях из соска секреции.
- Ультразвуковое исследование – при единичном раковом очаге процедура отражает ухудшение попадания ультразвуковой волны как ток в область с атипичным образованием.
- Магнитно-резонансная томография – предполагает применение контрастного компонента. Осуществляется для выявления рецидива и для оценивания положения материалов железы при установлении имплантата.
- Термография – способ касается гипертермии на злокачественном участке. Проводится изредка.
- Биопсия – подразумевает пункцию или удаление ракового образования с последующим взятием материала для проведения гистологического исследования. Гистология указывает злокачественность опухолевого очага и помогает узнать рецепторное состояние.
- Лабораторные исследования – анализы предполагают выявление онкологических маркеров и проведение оценки гормонального уровня в женском организме. Осуществляется анализ на наличие пролактина, ЛГ, ФСГ и эстрогена.
Дополнительные исследовательские мероприятия назначаются на усмотрение врача и состоят из рентгенографии грудной клетки, компьютерной томографии, сцинтиграфии и УЗИ абдоминальной полости.
Методы лечения инфильтративного рака
Инфильтрирующая карцинома молочной железы лечится сложно. Терапия прописывается после прохождения необходимых диагностических процедур. Лечебные способы проводятся в самостоятельном либо комплексном виде и с применением вспомогательных методик. Длительность стационарной терапии составляет 2-3 недели. Вернуться к привычному образу жизни и ходить на работу женщина сможет спустя 6 месяцев после окончания лечения, при отсутствии вторичных онкообразований и осложнений.

Химиотерапия необходима для лечения инфильтративного рака груди. Способ характеризует высокая эффективность в излечении онкологических патологий. Терапия воздействует на поражённые участки и затрагивает ближайшие здоровые ткани. Процедура протекает затруднительно и сопровождается множественными побочными реакциями – облысение, выпадение волос, резкое уменьшение массы тела, утомляемость и ослабленная иммунная система. Показания к выполнению химиотерапии:
- величина опухоли более 20 мм;
- 2 стадия рака;
- женщина младше 35 лет;
- злокачественный раковый нарост, не связанный с гормональным дисбалансом.
Медикаментозные средства подталкивают организм на борьбу с атипичными тканями. Антиметаболиты воздействуют на генетическую клеточную структуру, разрушая её во время разделения – Гемцитабин. Антрациклины производят свободные радикалы, повреждающие ДНК-клетку – Доксорубицин и Дауномицин. На прогрессирование поражённых тканей действуют Таксаны – Паклитаксел.
Винкаалкалоиды разрушают строение атипичной клетки, провоцируя дальнейшую гибель ткани. Препарат действует смягченно – Винбластин и Винкристин. Таргетное лечение прописывается женщинам при развитии новообразования до специфического гена (трижды негативный рак). В терапии применяют Трастузумаб, блокирующий интенсивность поражённых клеток.
Операция при раке молочной железы выполняется такими способами:
- Радикальная мастэктомия – сохраняет мышечную структуру. Затем врачи восстанавливают грудную форму при помощи операции.
- Мастэктомия с сохранением ареолы – проводится при наличии потокового типа инфильтративного рака. Во время процедуры хирург удаляет новообразование и при необходимости лимфатические узлы. После операции сохраняется визуальный вид груди и работоспособность органа.
- Органосохраняющая терапия – опухоль иссекают без затрагивания здоровых материалов. При мелком размере образования и объёмной молочной железе прогноз улучшается.
- Радикальная резекция – представляет собой полноценное удаление органа. Операция осуществляется при крупной величине нароста.
Гомеопатические средства применяются медицинскими работниками для улучшения действенности реабилитационного периода у женщин после хирургического воздействия. Гомеопатия зарекомендовала себя в целях профилактики развития рецидивов, для повышения и укрепления иммунной системы женского организма. Для лечения прописывают такие препараты, принимаемые внутрь:
- Галиум-Хель;
- Псоринохель;
- Лимфомиозот;
- Фосфор Гомаккорд.
Медикаменты употребляют по 10 капель по 6 подходов в день. После двух месяцев женщина снижает приём до 10 капель в 4 подхода в день. Через новые 60 дней достаточно принимать 3 раза в день. В качестве дополнительных мер врач может назначить введение инъекций средств – Нукс вомика-Гомаккорд, Хепель, Берберис-Гомаккорд и Хелидониум-Гомаккорд. Лекарства способствуют выходу из организма вредных токсинов.
Народная медицина используется в случаях отсутствия результатов традиционного лечения и при необходимости усиления действенности функционирования применяемых лечебных способов. Нетрадиционные методы терапии являются хорошим вспомогательным средством. Рецепты народного лечения подразумевают применение трав и растений, содержащих ядовитые компоненты. Поэтому важно беспрекословно соблюдать предписанную допустимую дозировку во избежание ухудшения состояния организма. Нельзя сосредотачиваться лишь на единственном средстве. Рекомендуется комбинировать разные настойки и отвары.

- Отвар из цветков картофеля. Берут одну столовую ложку сушёных цветов и заливают 0,5 л кипятка. Смесь оставляют настаиваться в термосе на 2-3 часа. Затем настойку пропускают через марлю и выжимают. Полученный отвар рекомендуется хранить в стеклянной таре в холодильнике. Употреблять 3 раза в день за 30 минут до употребления пищи по 160 мл. Продолжительность курса составляет две недели. Приём можно возобновить после 7 дней паузы. Общий курс лечения составляет 6 месяцев.
- Настойка берёзового гриба. Натереть гриб и настаивать в течение 2 дней в тёплой воде в пропорции 1:5 гриб и вода соответственно. Спустя 2 суток отвар профильтровать и употреблять 3 раза в день за 30 минут до еды. Настойку хранить в холодильнике не больше 4 суток.
- Отвар из золотого уса. Смешать 30 мл смеси с 40 мл нефильтрованного подсолнечного масла и выпить залпом. Повторять процедуру 3 раза в день за 20 минут до еды. Курс длится 10 дней через 5, затем 10 через 10 в течение 3 месяцев.
Перед началом использования народной медицины следует проконсультироваться с лечащим врачом. Если в процессе пациентка почувствовала себя хуже, лечение прекращают и отправляются на обследование.
Профилактика и прогноз
Процент выживаемости при инфильтрирующем раке молочной железы не утешителен. В 50% случаев пациентки не живут долго и умирают. Прогноз рассчитывается на основе типа и этапа протекания онкологической болезни. При раннем диагностировании опухоли и начале лечения шанс позитивного результата увеличивается. По статистике пятилетняя выживаемость зависит от стадии:
- 1 стадия – выздоровление в 90% болезней;
- 2 степень – вероятность благоприятного итога составляет 50-70%;
- 3 этап – выздоровления добиваются в 10-50% случаев;
- 4 ступень – шансы понижаются до 10%.
Чтобы избежать развития инфильтрирующей опухоли и рецидивного появления онкоочага, следует соблюдать правила и рекомендации врача. Профилактика атипичного недуга включает в себя следующие рекомендации:
- Следить за собственным весом. Избыточная масса тела благоприятствует появлению опухоли, в особенности после 45 лет.
- Отказаться от употребления алкогольной и табачной продукции из-за ослабления иммунитета.
- Быть активным и энергичным. Проделывать физические упражнения, делая упор на грудных мышцах.
- Правильное питание. Соблюдать диету, наполнить рацион витаминами, полезными микроэлементами и клетчаткой.
- Желательно родить ребёнка до достижения 30-летнего возраста.
- Не отказываться от грудного кормления в течение первых шести месяцев.
- Отказаться от вредной пищи.
- Систематически проходить осмотр и обследование.
- Вовремя начинать лечение возникающих болезней.
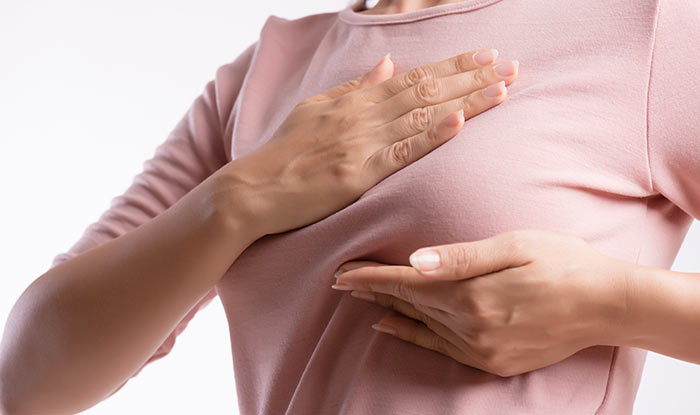
Протоковый рак молочной железы — самая частая клеточная форма, на его долю приходится семь из десяти злокачественных новообразований в груди. Ежегодно протоковую карциному обнаруживают примерно у 40 тысяч россиянок разного возраста.
Одинаковая по клеточной структуре карцинома не обещает однотипного развития заболевания, потому что может относится к любому из четырёх молекулярно-биологических вариаций, различаться злокачественным потенциалом и чувствительностью к лечебному воздействию.
- Общая информация о заболевании
- Классификация
- Факторы риска и причины развития
- Болеют ли мужчины протоковым раком груди?
- Симптомы и диагностика
- Лечение протокового рака груди
- Профилактика
- Прогноз
Общая информация о заболевании
Протоковой карциноме не присущ какой-то один молекулярный тип, она может быть и люминальной — гормонозависимой, и трижды негативной и базальноподобной — любой. В сравнении с другими более редкими морфологическими вариантами, это довольно агрессивный рак молочной железы, но при высокой степени дифференцировки небольшая на момент обнаружения опухоль течет вполне благоприятно и может никогда не откликнуться метастазами.
В каждом клиническом случае протоковый рак молочной железы абсолютно оригинален, но подходы к его лечению стандартизованы и унифицированы до оптимума.
Классификация
Протоковый рак in situ или DCIS начинается с одной или группы злокачественно мутировавших клеток, которые растут в верхних слоях эпителия, не пробивая его базальную мембрану и не внедряясь в глубокие слои. Тем не менее, опухоль может достигать нескольких сантиметров, склонна к развитию локальных рецидивов в зоне операции, в редких случаях даёт метастазы в подмышечные узлы и может привести к смерти от генерализации рака, но в 98% полностью излечивается.
Протоковую неинвазивную карциному разделяют на три типа: чуть более благоприятный по течению некомедо DCIS, несколько более агрессивный комедо DCIS и пограничный. Классификация протокового рака in situ по степени агрессивности — от низкой, через промежуточную до высокой степени злокачественности позволяет рассчитать прогноз и подобрать адекватное лечение.
Излечение протокового рака молочной железы in situ возможно только при использовании хирургии, причём не всегда целесообразна частичная резекция, даже при мизерном протоковом раке клинической необходимостью может стать мастэктомия с последующей профилактической гормонотерапией.
Главная проблема DCIS — высокая частота рецидива после операции, что обусловлено несоответствием размера пальпируемой в железе опухоли реальному раковому поражению тканей, которое максимально точно определяется при рентгенологическом исследовании, а ещё лучше — при МРТ.

Инвазивный протоковый рак имеет все характеристики злокачественного процесса: агрессивность в отношении окружающих тканей, склонность к распространению метастазов и неуклонное стремление к безудержному росту. Инвазивный процесс может быть любой степени злокачественности, с различным набором и концентрацией гормональных рецепторов, индекса пролиферации Ki-67 и гена множественной лекарственной устойчивости HER2.
Стадирование протокового рака стандартно и зависит от размера опухоли в молочной железе, вовлеченности лимфатических лимфоузлов и отдаленного метастазирования.
Факторы риска и причины развития
Причины развития протокового рака молочной железы неизвестны, факторы риска типичны для всех морфологических видов:
- несогласованность гормональной продукции при хронических заболеваниях и аномалиях половой сферы;
- слишком раннее половое созревание, равно как и задержка с завершением менструаций;
- аборты и поздние роды без достаточного по времени грудного вскармливания;
- сахарный диабет, ожирение;
- нездоровый образ жизни с гиподинамией, пристрастием к табаку и алкоголю.
При сочетании нескольких факторов на протяжении десятилетий ко второй половине жизни пятикратно увеличивается риск рака молочной железы.
Болеют ли мужчины протоковым раком груди?
Конечно не все факторы риска рака присутствуют у мужчин, но поведенческие тоже работают во вред. Избыточный вес отражается на продукции тестостерона, что ведет к гиперплазии желез — гинекомастии. Так что неумеренные в еде представители молодых поколений, особенно курящие и выпивающие, со временем могут увеличить популяцию заболевших раком, где точно будет превалировать доля протоковой карциномы.
Симптомы и диагностика
Симптомы протокового рака неотличимы от злокачественного процесса другой морфологической структуры:
- опухолевый узел или инфильтрация молочной железы,
- локальное и специфическое изменение кожи железы,
- увеличение подмышечных лимфоузлов.
- УЗИ при плотной структуре железы, маммография, МРТ для уточнения размеров и в сомнительных случаях.
- Обязательна тонкоигольная биопсия опухоли с ИГХ-исследованием на гормональные рецепторы, ген HER2 и Ki-67.
- При подозрении на отдаленные метастазы проводится дополнительное обследование.
Лечение протокового рака груди
Все протоковые карциномы можно разделить на три группы:
- Операбельные, которым соответствует всё от DCIS до 3 А стадии;
- Сомнительно операбельные — 3 стадия с выходом за границы груди и вколоченными лимфоузлами,
- Неоперабельные — 4 стадия и метастатическая генерализация.
Излечение без хирургии исключается. Хирургическое вмешательство предпочтительно на первом этапе, но может откладываться до завершения курса неоадъювантной химиотерапии. Возможна частичная резекция, во всех случаях дополняемая лучевой терапией, и мастэктомия. Выбор операции зависит от размеров и характера поражения молочной железы и предпочтений пациентки. По результатам выживаемости два оперативных подхода идентичны, но после резекции выше процент рецидивов в рубце. Мастэктомия может быть классической, то есть без реконструкции, современные варианты предполагают одномоментное или отсроченное восстановление молочной железы.
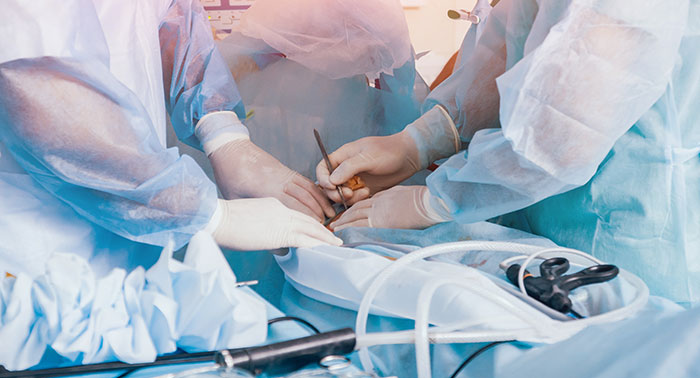
Радиотерапия дополняет операцию или заменяет ее при сомнительной операбельности. Необходима при множественном поражении подмышечных лимфоузлов и неблагоприятных признаках по гистологии: низкая дифференцировка, раковые клетки в сосудистых щелях или около нервных окончаний, высокий индекс пролиферации и обладание геном HER2. После операции облучение возможно только по завершении курса профилактической химиотерапии.
Лекарственная терапия назначается в соответствии с молекулярно-биологическим типом карциномы. Так при люминальном А варианте предпочтительна гормональная терапия, а химиотерапия используется только при наличии факторов неблагоприятного прогноза. Ни одна из схем профилактической химиотерапии не имеет преимуществ по эффективности, поэтому при подборе комбинации цитостатиков ориентировка на ожидаемую токсичность и состояние здоровья женщины. Число циклов химиотерапии зависит от биологического типа и выбранной схемы, лечение начинается при нормализации состояния после операции.
Наличие в клетках рака гена множественной лекарственной резистентности требует регулярных введений таргетного трастузумаба на протяжении года.
Гормональная терапия, а точнее антигормональная, применяется при наличии в опухоли рецепторов эстрогенов. Длительность профилактики от 7 до 10 лет, у менструирующих применяются таблетки тамоксифена или ингибитора ароматазы при подавлении функции яичников. После менопаузы предпочтение отдано ингибитору ароматазы.
Лечение 4 стадии только лекарственное — химиотерапия с антигормонами с учетом молекулярного типа, аналогично проводится лечение генерализации после радикальной операции. Для повышения результативности химиотерапии каждые 3 недели используется таргетная терапия.
Профилактика
Пятилетний прием тамоксифена после удаления протокового рака in situ допускается только при позитивном статусе по рецепторам эстрогена. Антигормон не повышает выживаемости, но снижает частоту рецидивирования при резекции молочной железы и вероятность развития инвазивной карциномы в других участках железы.
Прогноз
Прогноз определяется индивидуальными характеристиками рака на момент его обнаружения: размер опухоли в молочной железы, вовлечение лимфатической системы, клеточные факторы — рецепторный статус и ген устойчивости, а также степень злокачественности.
Естественно, что на дальнейшем течении заболевания отражается выбор лекарственного лечения, который сегодня базируется не только на молекулярно-биологическом типе, но и на персональных генетических характеристиках опухоли.
2. Стенина М.Б., Жукова Л.Г., Королева И.А., и соавт./ Практические рекомендации по лекарственному лечению инвазивного рака молочной железы // Злокач. опухоли: Практические рекомендации RUSSCO #3s2; 2017 (том 7).
3. Goodwin A., Parker S., Ghersi D., Wilcken N. /Post-operative radiotherapy for ductal carcinoma in situ of the breast—a systematic review of the randomised trials// Breast.; 2009 Jun; 18(3).
В развитых странах в структуре онкологической заболеваемости женщин рак молочной железы (РМЖ) занимает 1-е место (26% всех случаев рака).
По данным ВОЗ, в мире ежегодно умирает от РМЖ 590 000 женщин.
В 2006 г. в России рак молочной железы составил 17,8% всех злокачественных опухолей у женщин.
Показатель заболеваемости в 2006 г. составил 65,5 случая на 100 000 населения, абсолютное число заболевших — 48 821. Смертность в 2006 г. равнялась 29,5 случая на 100 000 женского населения, 1-летняя летальность — 11,5%. Мутация генов BRCA1 и BRCA2 увеличивает риск РМЖ.
Выбор метода лечения больных раком молочной железы зависит от стадии заболевания и от биологической характеристики опухоли (степень злокачественности, рецепторный статус, экспрессия HER2).
Ниже приводится классификация РМЖ по системе TNM и группировка по стадиям (табл. 9.17).
Первичная опухоль (Т)
ТХ — недостаточно данных для оценки первичной опухоли.
Т0 — признаков первичной опухоли нет.
Tis — рак in situ.
Tis (DCIS) — протоковый рак in situ.
Tis (LCIS) — дольковый рак in situ.
Tis (Paget's) — рак Педжета соска при отсутствии опухоли в паренхиме железы. При этом рак Педжета в сочетании с опухолью паренхимы оценивают в соответствии с размерами последней.
Т1 — опухоль не более 2 см в наибольшем измерении.
T1mic — микроинвазивный рак размером 0,1 см и менее в наибольшем измерении.
Т1а — опухоль более 0,1 см, но не более 0,5 см.
T1b — опухоль более 0,5 см, но не более 1 см.
T1c — опухоль более 1 см, но не более 2 см.
Т2 — опухоль более 2 см, но не более 5 см в наибольшем измерении.
Т3 — опухоль более 5 см в наибольшем измерении.
Т4 — опухоль любого размера с непосредственным распространением на а) грудную стенку, б) кожу с учетом описанных ниже принципов:
Т4а — опухоль поражает грудную стенку;
Т4b — отек (включая симптом лимонной корки), изъязвление кожи или метастазы в
коже той же молочной железы;
Т4с — сочетание признаков Т4а и Т4b;
T4d — диффузный рак.
Регионарные лимфоузлы (N)
NX — недостаточно данных для оценки регионарных лимфоузлов (например, они были ранее удалены).
N0 — регионарные лимфоузлы не пальпируются.
N1 — пальпируются подвижные подмышечные лимфоузлы с той же стороны.
N2 — пальпируются подмышечные лимфоузлы с той же стороны, спаянные друг с другом или окружающими тканями, либо имеются клинические признаки метастазов в окологрудинных лимфоузлах той же стороны при отсутствии таких признаков для подмышечных лимфоузлов.
N2a — подмышечные лимфоузлы на стороне опухоли спаяны друг с другом или окружающими тканями.
N2b — клинические признаки метастазов в окологрудинных лимфоузлах той же стороны при отсутствии таких признаков для подмышечных лимфоузлов.
N3 — пальпируются подключичные лимфоузлы (лимфоузел) вне зависимости от состояния подмышечных лимфоузлов, либо имеются клинические признаки метастазов в окологрудинных и подмышечных лимфоузлах, либо имеются метастазы в надключичных лимфоузлах, необязательно в сочетании с метастазами в подмышечных или окологрудинных лимфоузлах.
Отдаленные метастазы (М)
MX — недостаточно данных для оценки отдаленных метастазов.
М0 — отдаленных метастазов нет.
M1 — отдаленные метастазы имеются.
Таблица 9.17. Группировка рака молочной железы по стадиям (6-е издание, 2002)

Своеобразное течение РМЖ и биологические особенности этой опухоли обусловливают использование на определенных этапах заболевания всех существующих методов лечения — хирургического, лучевого, гормонального, химиотерапевтического, включая таргетную терапию; однако оптимальная последовательность их применения до настоящего времени остается предметом активных клинических исследований.
По современным представлениям, для выбора оптимальной терапии больной раком молочной железы необходимо иметь сведения о содержании в опухоли рецепторов стероидных гормонов (рецепторов эстрогена (РЭ), рецепторов прогестерона (РП)), экспрессии HER2 и степени злокачественности опухоли, определяемой по степени ее дифференцировки.
С точки зрения биологических особенностей, определяющих возможности лечения, все больные РМЖ делятся на три группы:
1) больные с гормоночувствительными опухолями, содержащими РЭ, РП; в лечении этих больных, как правило, используется гормонотерапия;
2) больные, опухоль которых характеризуется гиперэкспрессией HER2; этим больным показан трастузумаб (Герцептин);
3) больные РМЖ, у которых опухоль не содержит ни рецепторов стероидных гормонов, ни HER2 (так называемые трижды негативные опухоли); при лечении таких больных наиболее перспективна цитотоксическая химиотерапия (XT).
Эти клинические группы соответствуют молекулярным подтипам рак молочной железы (люминальный А и Б HER2-позитивный, базальный нормоклеточный).
Гормонотерапия — один из важнейших методов лечения РМЖ. Около 60% больных РМЖ (а среди пожилых больных до 80%) имеют гормонозависимые опухоли, т.е. опухоли, содержащие РЭ и РП.
Существует прямая корреляция между наличием и уровнем рецепторов стероидных гормонов и эффективностью гормонотерапии. Эффективность лечения РЭ-положительных опухолей составляет 50-60%, тогда как при РЭ-отрицательных злокачественных опухолях молочной железы положительный эффект гормонотерапии отмечается лишь у 5-10% больных. Около 30% больных с неизвестным рецепторным статусом отвечают на гормональные воздействия.
К методам гормонотерапии относятся: хирургическая, лучевая и химическая (с помощью суперагонистов LH-RH) кастрация у женщин с сохранной менструальной функцией, применение антиэстрогенов, ингибиторов ароматазы, прогестинов, андрогенов и их аналогов, кортикостероидов.
В принципе в основе всех методов гормонотерапии рака молочной железы лежит попытка воспрепятствовать стимулирующему воздействию стероидных гормонов (эстрогенов) на клетки опухоли.
У женщин в пременопаузе это может быть достигнуто путем овариэктомии или облучения яичников либо с помощью применения суперагонистов LH-RH, под влиянием которых функционируют яичники. Такая химическая кастрация носит обратимый характер и достигается применением гозерелина (Золадекс) или лейпрорелина, бусерелина.
У женщин в менопаузе синтез эстрогенов происходит в основном в жировой ткани путем реакции ароматизации андрогенов, продуцируемых корой надпочечников, а следовательно, использование ингибиторов ароматазы снижает содержание эстрогенов.
К селективным ингибиторам ароматазы относятся нестероидные — летрозол (Фемара), анастрозол (Аримидекс) — и стероидный ингибитор экземестан (Аромазин).
Антиэстрогены блокируют РЭ в опухоли. В эту группу входят селективные модуляторы эстрогенных рецепторов (SERM) — тамоксифен и торемифен и селективный супрессор эстрогенных рецепторов (SERD) — фульвестрант (Фазлодекс). Эти препараты активны как в пре-, так и в менопаузе.
Менее ясен механизм противоопухолевого действия прогестинов (мегестрол, медроксипрогестерон), которые также используются в гормонотерапии РМЖ.
РМЖ — опухоль, чувствительная к большинству современных противоопухолевых цитотоксических препаратов, прежде всего к антрациклинам — доксорубицину, который эффективен у 40% больных. Аналогичная эффективность и у эпирубицина, митоксантрона, циклофосфамида (35%), метотрексата (35%), фторурацила и тегафура (25 %). В 1990-е годы в клиническую практику вошли таксаны: паклитаксел (Таксол), эффективность 56-60%, доцетаксел (Таксотер) — 57-75%, винорелбин (Навельбин) — 41-51 %, капецитабин (Кселода) вторая линия — 20-36%, гемцитабин (Гемзар) вторая линия — 25%. У больных с гиперэкспрессией HER2 эффективен таргетный препарат трастузумаб (Герцептин) — гуманизированное МКА к EGFR — и лапатиниб (Тайверб, Тайкерб) — двойной ингибитор тирозинкиназы рецепторов EGF (HER2/HER1).
Лекарственная терапия раннего (операбельного) рака молочной железы
Больные с операбельным раком молочной железы нуждаются в дополнительной (адъювантной) лекарственной терапии, улучшающей отдаленные результаты лечения, снижающей риск рецидива заболевания и увеличивающей выживаемость больных. Исключение составляет лишь небольшая прогностически благоприятная группа больных старше 35 лет с высокодифференцированной (G1) гормоночувствительной (РЭ+, РП+) опухолью размером до 1 см, без метастазов в лимфоузлах (T1aN0M0) и без гиперэкспрессии HER2.
Важнейшими прогностическими факторами являются наличие и число пораженных лимфоузлов, размер первичной опухоли, степень злокачественности, определяемая по дифференцировке опухоли (G), возраст больной и состояние ее менструальной функции, содержание РЭ и/или РП в опухоли, а также гиперэкспрессия HER2 (табл. 9.18).
Таблица 9.18. Распределение больных раком молочной железы на категории риска

Рекомендации по выбору методов лечения в зависимости от чувствительности РМЖ к гормонотерапии приведены в табл. 9.19 и 9.20.
Таблица 9.19. Рекомендации по выбору методов лечения в зависимости от чувствительности к гормонотерапии (ГТ)

Примечание: При необходимости назначения XT и тамоксифена прием последнего должен быть начат после завершения XT (ХТ->ГТ) Вопрос относительно последовательности назначения ингибиторов ароматазы и XT (XT + ГТ или ХТ->ГТ) остается дискутабельным У больных в пременопаузе применение аналогов гонадотропин-рилизинг гормона может быть начато одновременно с XT для максимально быстрого достижения менопаузы.
Таблица 9.20. Рекомендации по лечению больных с гормоночувствительными опухолями

Примечание: В круглых скобках указаны лечебные опции, являющиеся предметом дискуссий и оцениваемые в соответствующих клинических исследованиях. Т — тамоксифен; ИА — ингибиторы ароматазы, ГТ — гормонотерапия; ОС — овариальная супрессия
При высоком риске N0 и отсутствии гормональных рецепторов послеоперационно проводится 4-6 курсов химиотерапии с включением антрациклинов (AC, FAC) или 6 курсов CMF. Больным в пременопаузе с положительными рецепторами и N0 после XT назначается тамоксифен на 5 лет. Альтернативой у этой категории пациенток служит выключение функции яичников с назначением тамоксифена.
У больных с низким риском в пременопаузе с N0 используется выключение функции яичников с помощью агонистов LH-RH в течение 2 лет, изучается целесообразность более длительного применения этих препаратов.
У больных в постменопаузе с N0 и положительными рецепторами используются ингибиторы ароматазы либо тамоксифен в течение 5 лет или прием тамоксифена в течение 2-3 лет с последующим переходом на ингибиторы ароматазы (до 5 лет). У больных в постменопаузе адъювантная гормонотерапия на любом этапе ее проведения может включать ингибиторы ароматазы. В ряде исследований было показано, что лечение тамоксифеном неэффективно у НЕR2-позитивных больных, что служит показателем резистентности к тамоксифену.
При высоком риске и N0 даже в менопаузе считается целесообразным назначение химиотерапии, а затем гормонотерапии ингибиторами ароматазы или тамоксифеном. У больных старше 70 лет основой адъювантной лекарственной терапии является тамоксифен.
При N+ в пременопаузе и при количестве метастазов в подмышечных лимфоузлах менее 4 показано проведение 6 курсов антрациклинсодержащих комбинаций CAF, FAC, АС или 6 курсов классического режима CMF с пероральным приемом циклофосфамида. При наличии 4 метастазов и более считается целесообразным назначение более длительной химиотерапии с дополнительным использованием таксанов. Далее при положительных рецепторах назначается тамоксифен на 5 лет.
У больных с сохранной менструальной функцией при поражении не более 3 лимфоузлов и положительных рецепторах допустимо выключение функции яичников с одновременным приемом тамоксифена.
У больных в постменопаузе с положительными рецепторами основой адъювантного лечения считается гормонотерапия (ингибиторы ароматазы или тамоксифен), но при поражении 4 лимфоузлов и более показано на I этапе проведение XT с последующей гормонотерапией. При отрицательных рецепторах в постменопаузе рекомендуется только XT.
Комитет экспертов конференции (St. Gallen, 2009) предложил упростить вопрос выбора показаний к применению гормонотерапии при операбельном РМЖ: все больные, у которых обнаружены РЭ+ (независимо от их уровня), должны получать гормонотерапию. РЭ-положительными считаются все опухоли, в которых при иммуногистохи-мическом исследовании обнаруживается даже минимальное количество РЭ-положительных клеток. При окрашивании более 50% клеток опухоль рассматривается как высокочувствительная к гормонотерапии.
Стандарт гормонотерапии для больных в пременопаузе — это применение тамоксифена либо тамоксифена + выключение функции яичников; ингибиторы ароматазы пациенткам в пременопаузе противопоказаны и могут применяться лишь в случае противопоказаний к использованию тамоксифена, при условии надежного выключения функции яичников по показателю содержания эстрадиола в сыворотке крови (верификация выключения функции яичников желательна даже при назначении ингибиторов ароматазы пациенткам в менопаузе моложе 60 лет). Для женщин в менопаузе предпочтительна гормонотерапия ингибиторами ароматазы, хотя у отдельных больных возможно использование тамоксифена. У больных с высоким риском предпочтительны ингибиторы ароматазы.
Показано, что у больных в менопаузе при рецептор-положительном раком молочной железы длительное применение летрозола (Фемара) по 2,5 мг/сут после окончания 5-летнего приема тамоксифена улучшает эффективность адъювантной гормонотерапии, снижая к 4 годам наблюдения относительный риск рецидива на 42 %.
Современный выбор оптимальных режимов адъювантной химиотерапии достаточно широк и включает использование антрациклинов и таксанов.
Применение антрациклинсодержащих комбинаций позволяет по сравнению с CMF уменьшить риск рецидива на 12%, риск смерти — на 11 % и увеличить 5-летнюю безрецидивную выживаемость на 3,2%, 5-летнюю общую выживаемость — на 2,7%. В США в адъювантном лечении у больных с плохим прогнозом используется паклитаксел после нескольких курсов антрациклинсодержащих комбинаций, в Европе активно ведутся исследования по использованию доцетаксела в адъювантной терапии, показавшие его высокую активность.
У больных с HER2+ РМЖ в рандомизированных исследованиях показано значение адъювантного применения трастузумаба (Герцептин).
На основании предварительного анализа результатов этих исследований международным консенсусом в 2007 г. рекомендовано использование трастузумаба при ранних стадиях HER2+ РМЖ в течение 1 года. Остается неясным вопрос о длительности его применения, целесообразности назначения при N0 и Т 5 лет);
• пожилой возраст;
• метастазы в костях, локорегионарные метастазы, минимальные метастазы в легких;
• гистологически установленная I-II степень злокачественности (G1-G2);
• большая длительность полученной ранее ремиссии в результате предшествовавшей гормонотерапии.
Ответ на гормонотерапию маловероятен в следующих случаях:
• короткий период без метастазирования (
Читайте также:

