Химиотерапия метастатического рака легких
На прошедшем виртуальном конгрессе ASCO 2020 в сессии устных докладов, посвященных лечению метастатического немелкоклеточного рака легкого (НМРЛ), были доложены результаты изучения новых комбинаций иммуноонкологических и таргетных препаратов.
Комбинация иммунотерапевтических препаратов ингибиторов CTLA4 и PD-1 по праву заняла место в арсенале лечебных подходов при проведении системной терапии первой линии диссеминированной меланомы. У больных НМПЛ FDA зарегистрировала комбинацию ипилимумаба и ниволумаба для проведения первой линии при наличии PD-L1 экспрессии по предварительным данным исследования CheckMate 227. Отдаленные результаты данного исследования были доложены на состоявшемся ASCO 2020 [1]. В исследовании были две когорты в зависимости от экспрессии PD-L1. Больных с наличием экспрессии PD-L1 ≥1% рандомизировали в группу ипилимумаба и ниволумаба, ниволумаба или химиотерапии. Больные с отсутствием экспрессии получали ниволумаб+ипилимумаб, химиотерапию или комбинацию химиотерапии и ниволумаба. Основным критерием эффективности было сравнение ипилимумаба+ниволумаба и химиотерапии по показателю PFS и OS у больных с PD-L1 ≥1%.
Результаты исследования представлены в таблице 1. По сравнению с химиотерапией у больных с экспрессией PD-L1 использование комбинации привело к достоверному снижению относительного риска смерти на 21%, увеличению медианы продолжительности жизни (ПЖ) с 14,9 до 17,1 мес. и 3-летней общей выживаемости с 22% до 33%. Использование ниволумаба статистически не улучшило результатов лечения по сравнению с химиотерапией. У больных с отсутствием экспрессии комбинация иммунотерапевтических препаратов увеличила медиану продолжительности жизни (с 12,2 мес. в группе химиотерапии до 17,2 мес.) и 3-летнюю выживаемость (с 15% до 34%), достоверно снизив относительный риск смерти на 36%. Не отмечено достоверной разницы в показателях общей выживаемости для комбинации ниволумаб+xимиотерапия в сравнении с химиотерапией. При длительном наблюдении показано, что у больных с объективным эффектом при использовании комбинации ипилимумаба и ниволумаба 70% и 82% живут 3,5 года и более при наличии или отсутствии экспрессии PD-L1 соответственно. При длительном наблюдении не отмечено возникновения новых серьезных побочных эффектов, обусловленных лечением.
Таблица 1. Отдаленные результаты исследования CheckMate 27.
| PD-L1 ≥1% | Ниволумаб + ипилимумаб | Ниволумаб | Химиотерапия |
| Медиана ПЖ | 17,1 мес. | 15,7 мес. | 14,9 мес. |
| 3-летняя ПЖ | 33% | 29% | 22% |
| PD-L1 ≤1% | Ниволумаб + ипилимумаб | Ниволумаб + химиотерапия | Химиотерапия |
| Медиана ПЖ | 17,2 мес. | 15,2 мес. | 12,2 мес. |
| 3-летняя ПЖ | 34% | 20% | 15% |
* ПЖ – продолжительность жизни или выживаемость.
Авторы делают вывод, что комбинация ипилимумаба и ниволумаба является эффективной первой линией системной терапии НМРЛ с экспрессией PD-L1 ≥1%. Неожиданной представляется равная высокая эффективность комбинации независимо от экспрессии PD-L1. Возможно, эти данные послужат FDA основанием для регистрации комбинации у больных c отсутствием экспрессии.
Еще одно исследование, посвященное изучению комбинации ипилимумаба и ниволумаба, было представлено в исследовании CheckMate 9LA [2]. В этом исследовании сравнивали 4 курса стандартной химиотерапии с включением цисплатина и пеметрекседа с комбинацией ипилимумаба (1 мг/кг каждые 6 недель), ниволумаба (360 мг каждые 3 недели) и 2 курсов подобной химиотерапии. В группе химиотерапии проводилась поддержка пеметрекседом, в группе комбинации иммунотерапия проводилась до 2 лет или непереносимой токсичности. В основе идеи добавления к иммунотерапии химиотерапии короткой продолжительности было желание контроля заболевания до момента индукции и реализации иммунного ответа. В исследование включались больные метастатическим НМРЛ без активирующих мутаций, стратификация проводилась в зависимости от экспрессии PD-L1, пола и гистологии опухоли. Основным критерием эффективности была общая продолжительность жизни.
В исследование было включено 717 больных, в основном мужчин (70%), с аденокарциномой (59%), экспрессией PD-L1 ≥1% (60%). При наблюдении 12,7 мес. и более медиана продолжительности жизни составила 15,6 мес. в группе комбинации и 10,9 мес. в группе химиотерапии, что соответствует достоверному снижению относительного риска смерти на 34% в группе комбинации. Позитивный эффект комбинации не зависел от экспрессии PD-L1 и морфологии опухоли. Ожидаемо побочные эффекты, обусловленные химиотерапией, были более выраженными в группе химиотерапии. В группе комбинации отмечались иммуноопосредованная токсичность, в основном 1-2- степени: кожная (40%), эндокринная (26%), желудочно-кишечная (23%), печеночная (10%). Это послужило причиной досрочной отмены илипимумаба у 5% больных, а двух иммунологических препаратов – у 74%. Медиана продолжительности терапии составила 6,1 мес. в группе комбинации (максимальная продолжительность терапии была 23 мес.) и 2,4 мес. в группе химиотерапии. В каждой группе было зарегистрировано по 2 смерти на фоне проводимой терапии.
Авторы делают вывод, что комбинация ипилимамаба и наволумаба с коротким курсом химиотерапии улучшает результаты лечения больных метастатическим НМРЛ в сравнении со стандартной химиотерапией и может быть рекомендована в качестве одной из опций проведения первой линии.
Результаты этих двух исследований ставят перед нами непростые вопросы. Исходя из результатов двух исследований CheckMate 227 и CheckMate 9LA, выполненных на примерно одинаковой популяции больных НМРЛ, остается неясным, улучшает ли добавление химиотерапии результаты иммунологической комбинации ипилимумаба и ниволумаба. Короткий срок наблюдения в исследовании CheckMate 9LA не позволяет ответить на этот вопрос. Показатели одногодичной PFS и OS двух исследований в цифровых значениях близки, и только дальнейший мониторинг сможет дать ответ.
Таблица 2. Возможные лечебные опции первой линии системной терапии
больных метастатическим НМРЛ без активирующих мутаций.
| PD-L1 негативный | PD-L1 умеренный | PD-L1 высокий |
| Атезо (IMPower 110) | ||
| Пембро (KeyNote 024, KeyNote 042) | ||
| Пембро + химиотерапия (KeyNote 189, KN 407) | ||
| Атезо + химиотерапия неплоскоклеточный (IMPower1 30) | ||
| Атезо + химиотерапияя + бевацизумаб неплоскоклеточный (IMPower 150) | ||
| Ипи + ниво (СheckМate 227) | ||
| Ипи + ниво + короткая химиотерапия (СheckMate М9LA) . | ||
* В скобках приведены номера регистрационных исследований.
Еще одной проблемой является выбор оптимальной опции проведения первой линии системной терапии у больных НМРЛ с отсутствием активирующих мутаций. Появление все новых исследований и регистраций новых препаратов и комбинаций для проведения первой линии без их прямого сравнения в рандомизированных исследованиях и отсутствие биомаркеров, помогающих сделать правильный выбор, затрудняют работу практического врача. Сегодня единственным биомаркером для назначения иммунотерапии отдельно или в комбинации является экспрессия PD-L1. Для больных с высокой экспрессией сегодня потенциально могут быть назначены 6 различных видов системной терапии с включением иммуноонкологических препаратов. Для больных с умеренной экспрессией таких вариантов 5, при отрицательной экспрессии – 4. И сюда возможно добавление ипилимумаба и ниволумаба в сочетании с короткой химиотерапией, которая работает независимо от экспрессии PD-L1 в случае ее одобрения FDA. Если мы предполагаем, что любая из существующих опций имеет равную противоопухолевую эффективность во всех подгруппах больных c различной экспрессией PD-L1, тогда на первый план выходят частота, выраженность и спектр токсичности, оценка качества жизни и экономическая эффективность. Без ответов на эти вопросы выбор первой линии системной терапии НМРЛ будет основываться на субъективных предпочтениях лечащего врача и наличии тех или иных лекарств в учреждении.
Комбинированная таргетная терапия
В рамках сессии были сообщены отдаленные результаты японского исследования NEJ026 по сравнению эрлотиниба и комбинации эрлотиниба150 мг внутрь ежедневно и бевацизумаба 15 мг/кг каждые 3 недели у больных с метастатическим НМРЛ и наличием активирующей мутации в гене EGFR [3]. Ранее были доложены результаты продолжительности времени до прогрессирования, которые убедительно демонстрировали преимущество комбинации. Следует отметить плохую переносимость бевацизумаба (в основном повышение АД), в связи с чем 29% пациентов досрочно прекратили его введение. При дальнейшем наблюдении не отмечено выигрыша в общей выживаемости между двумя группами, хотя сами показатели являются выдающимися и существенно превышают результаты исследования FLAURA c осимертинибом. Больные с прогрессированием после первой линии получали платиновую химиотерапию (38% в группе комбинации и 40% в группе эрлотиниба), 29% больных в группе эрлотиниба затем получали бевацизумаб, осимертиниб был назначен 25% пациентов в каждой группе. Назначение осимертиниба сопровождалось увеличением общей продолжительности жизни по сравнению с больными, его не получавшими. Полученные данные заставили авторов сделать вывод, что, несмотря на выигрыш в медиане времени до прогрессирования, назначение комбинации не приводит к увеличению продолжительности общей выживаемости. Правильное и эффективное лечение современными препаратами (особенно с включением осимертиниба) в последующих линиях терапии нивелирует полученный первоначальный выигрыш и обеспечивает всем больным примерно одинаковый конечный результат. Это повышает интерес к ожидаемым отдаленным результатам исследования RELAY, в котором использовалась комбинация эрлотиниба с другим моноклональным антителом антиангиогенной направленности рамицурумабом.
Таблица 3. Результаты исследования рандомизированных исследований
при метастатическом НМРЛ с наличием мутации в гене EGFR.
| Исследования | Медиана ВДП | Медиана ПЖ |
|---|---|---|
| NEJ026 | ||
| Эрлотиниб + бевацизумаб | 16,9 мес. | 50,7 мес. |
| Эрлотиниб | 13,6 мес. | 46,2 мес. |
| HR | 0,60 | 1,0 |
| RELAY | ||
| Эрлотиниб + рамицирумаб | 19,4 мес. | Нет данных |
| Эрлотиниб | 12,4 мес. | |
| HR | 0,59 | |
| NEJ009 | ||
| Гефитиниб + химиотерапия | 20,9 мес. | 50,9 мес. |
| Гефитиниб | 11,9 мес. | 38,8 мес. |
| HR | 0,49 | 0,72 |
| FLAURA | ||
| Осимертиниб | 18,9 мес. | 38,6 мес. |
| Гефитиниб/эрлотиниб | 10,2 мес. | 31,8 мес. |
| HR | 0,46 | 0,8 |
* ВДП – время до прогрессирования, ПЖ – продолжительность жизни.
Китайские коллеги представили результаты другой комбинации – гефитиниба и лучевой терапии [4]. Больные с олигометастатическим (не более 3 зон поражения и не более чем 5 метастазов всего) НМРЛ с наличием мутации EGFR и отсутствием прогрессирования болезни в течение 4 мес. на фоне терапии гефитинибом рандомизировались в группу продолжения гефитиниба или в группу стереотаксического облучения (25-40 Гр за 5 фракций) имеющихся проявлений болезни на фоне гефитиниба. Наличие метастазов в мозг было исключающим фактором. Основным критерием эффективности была медиана времени до прогрессирования. В исследование было включено 133 больных. При промежуточном анализе медиана времени до прогрессирования составила 20,2 мес. в группе комбинации гефитиниба и лучевой терапии и 12,5 мес. в группе гефитиниба, медиана общей выживаемости 25,5 мес. и 17,4 мес. соответственно. Добавление лучевой терапии не привело к существенному усилению токсичности гефитиниба. Значительный выигрыш в продолжительности времени до прогрессирования в группе комбинированного лечения и при этом короткая общая продолжительность жизни в обеих группах затрудняют трактовку данного исследования. Авторы не дают деталей проведенного лечения после прогрессирования заболевания, которое может быть ответственным за столь невыразительные результаты по общей выживаемости. Следует продолжить изучение комбинированного назначения ингибиторов тирозинкиназы (особенно новых поколений) с локальными методами лечения (стереотаксическая лучевая терапия или хирургическое лечение) при олигометастатической болезни.
Если обобщать исследования, представленные на данном конгрессе ASCO для лечения метастатического НМРЛ, очевидно стремление найти способы повышения эффективности уже существующим иммуноонкологическим и таргетным препаратам. Вот почему так много исследований различного рода комбинаций с существующими лечебными подходами. Иногда это удается, иногда нет, но нельзя скептически относиться к попыткам научиться использовать доступные препараты на 100%. Ибо новые лекарства с лучшей эффективностью и меньшей токсичностью появляются не каждый день.
- Ramalingam SS, Ciuleanu TE, Pluzanski A, et al. Nivolumab + ipilimumab versus platinum-doublet chemotherapy as first-line treatment for advanced non-small cell lung cancer: Three-year update from CheckMate 227 Part 1. ASCO 2020, abstract 9500.
- Reck M, Ciuleanu TE, Cobo Dols M, et al. Nivolumab (NIVO) + ipilimumab (IPI) + 2 cycles of platinum-doublet chemotherapy (chemo) vs 4 cycles chemo as first-line (1L) treatment (tx) for stage IV/recurrent non-small cell lung cancer (NSCLC): CheckMate 9LA. ASCO 2020, abstract 9501.
- Maemondo M, Fukuhara T, Saito H, et al. NEJ026: Final overall survival analysis of bevacizumab plus erlotinib treatment for NSCLC patients harboring activating EGFR-mutations. ASCO 2020, abstract 9506.
- Wang X, Zeng M. First-line tyrosine kinase inhibitor with or without aggressive upfront local radiation therapy in patients with EGFRm oligometastatic non-small cell lung cancer: Interim results of a randomized phase III, open-label clinical trial (SINDAS) (NCT02893332). ASCO 2020, abstract 9508.
- Smit EF, Nakagawa K, Nagasaka M, et al. Trastuzumab deruxtecan (T-DXd; DS-8201) in patients with HER2-mutated metastatic non-small cell lung cancer (NSCLC): Interim results of DESTINY-Lung01. ASCO 2020, abstract 9504.
В современном мире онкологические заболевания очень распространенные. Только от рака легких ежегодно умирают более восьми миллиона человек. Чтобы уберечь себя и своих близких, нужно следить за здоровьем, периодически диагностироваться и при обнаружении болезни незамедлительно обращаться к профессионалам и лечить ее.
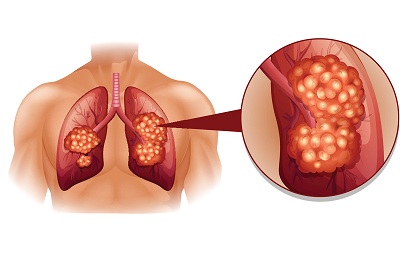
Рак легких – это злокачественная опухоль, которая возникают в легких и бронхах. Чаще всего болезнь прогрессирует в правом легком и в верхних долях. Может быть как рак одного легкого, так и рак двух легких. Клетки быстро разрастаются и могут перейти и охватить другие органы.
Данная болезнь очень опасна, так может привести к летальному исходу. По смертности это заболевание на первом месте среди прочих онкологических. В категорию риска попадают мужчины, перешедшие через шестидесятилетний рубеж. Распространенным видом является плоскоклеточный рак легкого, во время которого опухоль растет через клетки бронхиального эпителия.
Болезнь имеет 4 стадии (степени):
- 1 стадия – небольшая опухоль размером до 2 см, не влияющая на лимфатические узлы,
- 2 стадия – подвижная опухоль более 2см, начинает поражать лимфатическую систему,
- 3 стадия – ограниченная в движении опухоль. Характеризуется метастазирующими лимфоузлами,
- 4 стадия – крайняя. Опухоль растет и локализуется в соседних органах. К сожалению, рак на 4 стадии не лечится.
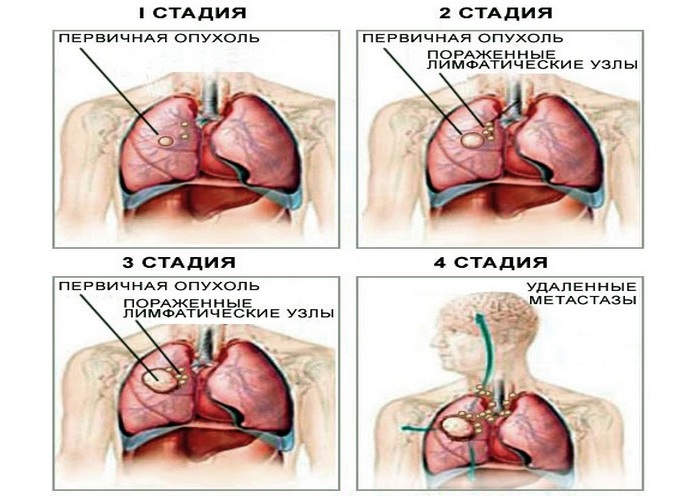
Какая стадия у пациента можно определить после диагностики.
- Показания к проведению химиотерапии рака легких
- Противопоказания и побочные эффекты химиотерапии рака легких
- Как перенести побочные эффекты от химиотерапии?
- Эффект от применения
Понятие химиотерапии и схема ее проведения
Химиотерапевтический способ лечения относится к лечению медицинскими препаратами, которые останавливают деление и размножение онкоклеток. Встречаются и другие виды лечения, но они не являются настолько эффективными.
Химиопрепараты вводят в кровь, где они непосредственно выполняют свою функцию и распространяются по всему телу. Главным плюсом лечения является то, что препараты действуют не на один определенный участок организма, а убивают раковые клетки везде, где они встречаются при этом, практически не влияя на здоровые органы.
Процедура проводится с перерывами в несколько недель. Это нужно для восстановления иммунитета и отдыха организма. Во время курсов доктор наблюдает за состоянием больного, собирает анализы, проводит нужные исследования. Все химические препараты имеют дозировку, которая зависит от веса и возраста человека.
- лекарство вводится в вену с помощью тонкой иглы,
- устанавливается катетер, который не достают до конца курса,
- при возможности задействуют артерию, которая наиболее близка к опухоле,
- также применяются препараты в виде таблеток и мазей.
Химиотерапия плоскоклеточного рака легких включает в себя применение препаратов, которые убивают патологические клетки.
Схема химиотерапии должна быть эффективной и с минимальным уровнем побочных эффектов. Все медицинские лекарства должны быть назначены индивидуально для пациента, а также они должны сочетаться друг с другом.
Процедуру назначают в зависимости от заболевания, его стадии, возраста пациента и других факторов. Количество курсов химиотерапии назначает непосредственно врач. Сначала смотрят на размеры образования, его изменения и деформации.
Обращают внимание на общее состояние организма человека, место образования опухли и ее прогрессирования. Химиотерапия при раке легкого помогает остановить развитие болезни, а порой и избавится от нее.
В идеале данная терапия должна полностью уничтожить раковые клетки. В дальнейшем специалисты назначают химиопрепараты. Все препараты врач назначает индивидуально для каждого пациента. Встречаются разные типы химпрепаратов при раке легкого, которые подбираются и назначаются в клинике.
Данный метод имеет ряд противопоказаний:
![]()
ухудшение состояния,- споры и сомнения докторов в проведении процедуры,
- психические болезни,
- инфекционные заболевания,
- заболевания (хронические) печени и почек,
- неинвазивная раковая болезнь.
Кроме этого, могут отменить процедуры при:
- преклонном возрасте больного,
- иммунодефиците организма,
- приеме антибиотиков,
- ревматоидном артрите.
Точно прогнозировать последствия невозможно. У одних пациентов их вовсе нет, другие – сталкиваются с рядом негативных явлений.
Медицина не стоит на месте и старается усовершенствовать лекарственные препараты. Но знать о негативных последствиях стоит. Они проявляются после проведения процедуры, чаще всего через несколько дней. К основным относятся:
![]()
тошнота, рвота, поносы, запоры и другие расстройства со стороны пищеварительного тракта,- нарушение работы кишечника. В свою очередь, это приводит к понижению веса и снижению иммунной функции организма, что чревато заболеваниями,
- анемия,
- утрата волос,
- кровотечения и синяки,
- язвы в ротовой полости.
Для того, чтобы уменьшить побочные действия химиотерапии, пациент принимает определенные лекарства.
Любая химия влияет на работу организма. До сих пор не создали препарат, который не был бы не токсичным и полностью уничтожал онковые заболевания. Насколько сложно или легко человек перенесет процедуру предугадать невозможно.
Последствия химиотерапии при раке легких различные: начиная от выпадения волос и заканчивая тошной и рвотой.
Для облегчения состояния нужно:
- принимать специальные препараты поддерживающие работу почек, печени и костной ткани,
![]()
стоит следить за правильным рационом питания,- уменьшить количество жирной, соленой и острой еды,
- больше времени находиться на свежем воздухе,
- не забывать про прогулки и физическую активность,
- общаться с доктором, слушать и придерживаться всех его рекомендаций,
- следить за психологическим состоянием, иметь позитивное настроение, верить в полное излечение и знать, что скоро все пройдет и нормальная жизнь восстановится.
Эффективность химиотерапии при раке легких есть. Болезнь сдерживается, уничтожаются раковые клетки, но полное исчезновении онкологии чаще всего невозможно, так как клетки адаптировались к медикаментам.
Лечение рака легких химиотерапией имеет свои положительные результаты: в связи с развитием медицины курсы химиотерапии при раке легких с каждым годом показывают все лучшие результаты и проводятся намного менее болезненно, чем это было раньше. Поэтому делать эту процедуру нужно. Относится к ней нужно с вниманием и понимать, что это необходимая мера. И главное – нужно верить в скорейшее выздоровление и никогда не сдаваться.
Правильное питание во время химиотерапии
В ходе лечения многое зависит от самого пациента. В первую очередь это касается правильного питания.

При побочных эффектах здоровое полноценное питание необходимо. Оно помогает организму нормально функционировать, а человеку быстрее восстановиться. Лекарства негативно влияют на органы пищеварительного тракта. Человек встречается с массой сложностей. Поэтому от качества и регулярности питания также зависит дальнейшее выздоровление.
Следует выпивать много воды, не менее полтора-двух литров в день во время курса химиотерапии. Очень важно обогатить свой рацион всеми группами полезных продуктов: белковых, зерновых, фруктами и овощами и молочными продуктами. К белковым продуктам относятся: фасоль, рыбу, орехи, яйца, соя, мясо. В течение дня лучше всего употреблять такие продукты минимум один раз. К молочным относятся: кефир, йогурт, молочные продукты, сыр и прочие. Они богаты кальцием и магнием.
Диета должна быть обогащена фруктами и овощами, в том числе и сухофруктами и компотами. Не менее четырех раз в день следует употреблять эту группу продуктов. Особенно это касается начала проведения химиотерапии.
Полезным будет употребление свежевыжатого сока. Следует, добавить в рацион свежую зелень. Обязательно кушать морковь и различные фрукты, содержащие витамин С. Также не нужно забывать про крупы и хлеб. Они богаты на углеводы и витамины группы В. По утрам нужно употреблять каши. Во время и после лечения таким способом нужно выпивать витамины. Следует исключить алкогольные напитки.

- Лёгкие - излюбленная мишень для метастазирования опухолей
- Какими бывают метастазы в лёгких
- Диагностика
- Клиническая симптоматика
- Лечение метастазов в лёгкие
- Паллиативная помощь при метастазах рака в легкие
Метастатическим или вторичным раком легких называются опухоли, которым дают начало раковые клетки, попавшие в легочную ткань из других органов.
Лёгкие - излюбленная мишень для метастазирования опухолей
Статистика говорит о том, что у 30-55% онкологических больных обнаруживаются метастазы в легких. Злокачественные опухоли дают отсевы в лёгочную ткань: рак любого органа, саркомы, меланомы, заболевания кроветворной и лимфатической системы. Через лёгкие проходит вся кровь, и условия благоприятны для выживания бактерий, вирусов, грибов и опухолевых клеток.
Собирающий лимфу общий лимфатический проток несёт её в крупные вены, которые впадают в верхнюю полую вену. При посредстве правых отделов сердца венозная кровь, смешанная с лимфой, тоже проходит через лёгкие. Площадь структурных единиц, составляющих то, что мы называем лёгкими - лёгочных альвеол - более 150 квадратных метров. Достаточно места, изумительное полнокровие, прекрасные условия для размножения злокачественных клеток.
Иными словами, присутствуют благоприятные условия для распространения раковых клеток в легкие гематогенным (через кровь) и лимфогенным (через лимфатическую систему) путем.

Какими бывают метастазы в лёгких
Метастатические узлы бывают очень разными, считают, что по плотности они полное отражение первичной опухоли. Если определять плотность на ощупь, то все опухоли тяготеют к каменистости или, по крайней мере, к костной плотности. Но плотность для очагов в лёгких понятие относительное, прощупать их можно только во время операции, которую в метастатической стадии делают чрезвычайно редко. Плотность определяют при рентгенологическом исследовании преимущественно для дифференциальной диагностики, то есть поиска признаков характерных отличий одного заболевания от другого.
Формально метастазы делят на лимфогенные и гематогенные, то есть занесенные в лёгочную ткань с лимфой или кровью, но в каждом конкретном случае разобрать, что принесло раковую клетку в альвеолу вряд ли можно, и практикующему онкологу совсем ненужно, ведь это уже ничего не изменит. Какие бы ни были метастазы по пути распространения, их надо лечить.
Метастазы в лёгких бывают разными по форме, ее определяют по рентгеновским снимкам:
По числу метастазы могут быть:
- солитарными – один очаг;
- единичными – не более десяти;
- множественными.
Метастатические узлы бывают мелкими и крупными, а ещё сливающимися друг с другом, односторонними, когда поражено одно лёгкое и двухсторонними.
Вокруг метастазов тоже могут жить бактерии, всё-таки по бронхиальному дереву проходит нестерильный воздух, а опухоль меняет местный иммунитет, и возникает воспаление. Когда внутренняя часть опухоли не получает достаточного питания - она отмирает, и в центре образуется полость распада. Если такая полость соединится с бронхом, то в неё могут попасть бактерии, и полость заполнится гноем.
Плевра - пленка из соединительной ткани. Она состоит из двух листков: один покрывает снаружи легкие, а другой выстилает изнутри стенки грудной полости. Плевра интимно спаяна с лёгким. В ней тоже могут возникнуть метастазы, но намного реже. Опухоли из легких могут прорастать в плевру и наоборот. Зачастую в легких обнаруживаются метастазы, а плевра не поражена.
Диагностика
При подозрении на метастазы в легких прибегают к следующим методам диагностики:
- Рентгенография. Простой и быстрый, но не самый информативный метод диагностики. Обычно на снимках можно увидеть только опухоли размером более 1 см;
- Компьютерная томография. Позволяет обнаружить очаги менее 5 мм. Это недоступно для рентгенографии и МРТ;
- Биопсия легкого. Обычно проводится при помощи иглы. Получают небольшой фрагмент ткани опухоли для исследования;
- Бронхоскопия. Эндоскопическое исследование, во время которого специальный инструмент с источником света и видеокамерой - бронхоскоп - вводят в бронхиальное дерево. Во время процедуры можно провести биопсию.
Как правило, динамическое наблюдение за онкологическим пациентом после лечения первичной опухоли предполагает регулярную рентгенографию органов грудной клетки. При выявлении теней в лёгких, правильно будет сделать компьютерную томографию с введением контрастного вещества. КТ способна выявить очаги меньше 5 мм, что недоступно магнитно-резонансной томографии. В дальнейшем для контроля динамики процесса после лечения также необходимо будет делать КТ.
Клиническая симптоматика
Клинические признаки метастазов в лёгких зависят от обширности поражения и присоединения воспалительных изменений.
- боль в груди;
- упорный кашель;
- примесь крови в мокроте;
- ослабленное дыхание;
- хрипы;
- слабость;
- снижение веса.
При одиночных очагах округлой формы, небольшого размера никаких признаков поражения может и не быть, их часто случайно обнаруживают при контрольном обследовании. Площадь лёгких огромна, и несколько квадратных сантиметров опухолевого поражения альвеол не отразятся на газообмене и состоянии пациента. Множество теней, когда их уже не пересчитать, ухудшат самочувствие, провоцируя сухой кашель, плохо откликающийся на средства от кашля.
Инфильтративные метастазы раньше меняют самочувствие, поскольку к ним часто присоединяется воспаление окружающей опухоль ткани – пневмонит. Появляется кашель, может быть температура, слабость, почти как пневмония, но чуть-чуть полегче. Закупорка бронха опухолью приведёт к ателектазу – полной безвоздушности части лёгкого, присоединение инфекции существенно ухудшит состояние, повысится температура, появится одышка. Приём антибиотиков помогает снять воспаление и самочувствие улучшается, но ненадолго, потому что опухоль растёт, и безвоздушная часть лёгкого тоже увеличивается. И опять воспаляется, так и идёт по замкнутому кругу.
Лечение метастазов в лёгкие
Сегодня оперировать метастазы в лёгких стали чаще, чем раньше, но всё-таки операции делают довольно редко. Радикальное лечение метастазов в лёгкие – оперативное в принципе возможно при определённых условиях:
- не должно быть первичной опухоли или рецидива;
- не должно быть метастазов в других органах;
- метастаз в лёгком очаговый и единственный или не более 3 очагов;
- скорость прогрессирования опухолевого процесса должна быть невысокой, как правило, после радикального лечения первичной опухоли до появления метастаза должно пройти более года;
- со времени появления метастаза в лёгком в течение полугода не должно появиться других метастазов;
- состояние пациента должно позволять довольно сложное оперативное вмешательство, потому что во время операции реальная ситуация может оказаться значительно хуже, чем описывалась при компьютерной томографии, и придётся удалять больше запланированного.
Основное лечение метастазов в лёгких – химиотерапия, схема которой определяется первичной опухолью, при раке молочной железы ещё и гормональная терапия, естественно, при наличии чувствительности к ней.
Лучевая терапия множественных метастазов в лёгких проводилась в экспериментальных группах, результаты неудовлетворительные. При единственном довольно крупном очаге облучение возможно, но эффективность много хуже, чем при раке лёгкого. Наличие метастаза, где бы то ни было, показатель диссеминации - разброса злокачественных клеток, что не предполагает хорошего прогноза в отношении возможности полного излечения.
Метастазы в любом органе говорят о том, что защитные силы организма исчерпаны, опухолевые клетки успели распространиться по разным органам. Ремиссия в большинстве случаев невозможна. Но это не означает, что врач совсем ничего не может сделать. Паллиативное лечение поможет продлить жизнь, избавит от мучительных симптомов.
Паллиативная помощь при метастазах рака в легкие
Часть легкого, занятая опухолью, выключается из процесса дыхания. Поначалу оставшаяся здоровая ткань успешно справляется и работает за целое легкое. Но постепенно опухоль растет, перестает реагировать на химиотерапию и занимает все больше места.Наступает момент, когда оставшаяся здоровая ткань перестает справляться. Легкие больше не могут обеспечить организм нужным количеством кислорода, развивается дыхательная недостаточность. Кислородное голодание затрагивает все органы, в первую очередь — сердечно-сосудистую систему.
Симптомы дыхательной недостаточности нарастают постепенно:
- Поначалу возникает лишь одышка после ходьбы и физических нагрузок;
- Затем одышка начинает беспокоить при минимальных нагрузках, при любой движении;
- В тяжелых случаях человек задыхается постоянно, даже когда лежит в постели. Больного мучит постоянный кашель, слабость, на ногах появляются отеки, сердцебиение учащается. Стоит совершить небольшое движение, и все симптомы усиливаются на порядок.
Страдания больного может облегчить кислородотерапия. Но проводить ее нужно по 15 часов в день. Существуют специальные дыхательные маски, их можно приобрести, и все же проводить такое лечение в домашних условиях очень сложно.
Государственные онкологические клиники не госпитализируют таких пациентов в экстренном порядке. Помощь можно получить в отделении паллиативной медицины, но таких в Росии пока еще очень мало. В обычном стационаре практически ничем не помогут. Кислородотерапию можно получить в хосписе, но там практически нет симптоматической терапии. При тяжелой дыхательной недостаточности одной кислородотерапии недостаточно. Нужна дыхательная поддержка — искусственная вентиляция легких. В данном случае ИВЛ проводят через маску, интубацию трахеи не проводят.
Такое лечение не избавит от рака и не уничтожит метастазы, но оно способно сильно облегчить состояние больного:
- уменьшится одышка;
- отдохнуть дыхательные мышцы, которым в последнее время пришлось интенсивно работать;
- нормализуется состав крови, уменьшится кислородное голодание;
- уменьшатся даже воспалительные изменения в легких;
- в конце концов, человек перестанет задыхаться, улучшится качество жизни.
Помочь человеку с тяжелым нарушением дыхания в домашних условиях невозможно. Родные постоянно слышат, как он тяжело дышит, хрипит, кашляет, но помочь ничем не могут. Страдают все.
Врачи онкологи и реаниматологи Европейской онкологической клиники знают, как помочь пациенту с метастатическим раком легких в рамках паллиативной помощи. Грамотное лечение избавит от тяжелых симптомов, подарит драгоценное время.
Выберите врача и запишитесь на приём:

Главный врач Европейской клиники, онколог, к.м.н.
Читайте также: