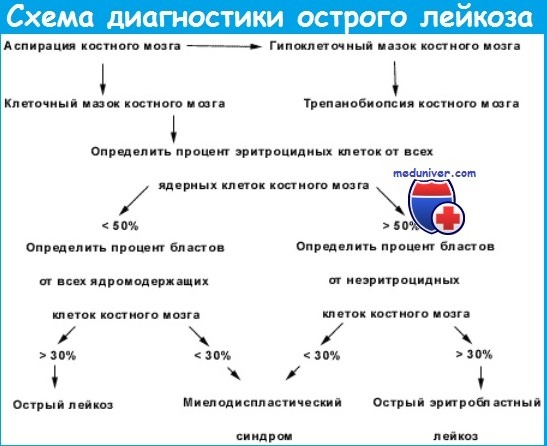
Характерные изменения миелограммы при остром лейкозе

Заболевания системы кроветворения не щадят никого — ни взрослых, ни маленьких детей. Успех лечения, сохранение жизни пациентов прежде всего зависит от своевременной диагностики. Обязательным диагностическим методом контроля состояния костного мозга является костно-мозговая пункция. Получаемая при этом миелограмма покажет все, что происходит с органами кроветворения, поможет выявить злокачественные новообразования на ранних стадиях, назначить правильное лечение.
Что такое миелограмма?

Мазок нормального костного мозга
Миелограмма — это данные гематологического микроскопического исследования, полученные в результате пункции красного костного мозга.
Цель проведения анализа — оценка качественного и количественного состава клеток костного мозга (миелоидная ткань), содержание различных миелокариоцитов в процентах.
Клеточное содержание костного мозга является отражением кроветворной функции организма человека. В нем происходит образование, созревание (дифференцировка) клеток-предшественниц миелоидного ростка кроветворения — форменных элементов крови:
- эритроцитов,
- лейкоцитов,
- тромбоцитов.
Любое изменение со стороны гемопоэза отражается в миелограмме, по данным которой судят о наличии патологии системы крови, оцениваются типы кроветворения, динамика заболевания, назначается, корректируется получаемое лечение.
Для максимально полной оценки состояния системы кроветворения полученные данные миелограммы обязательно необходимо оценивать вместе с общим развернутым клиническим анализом периферической крови.
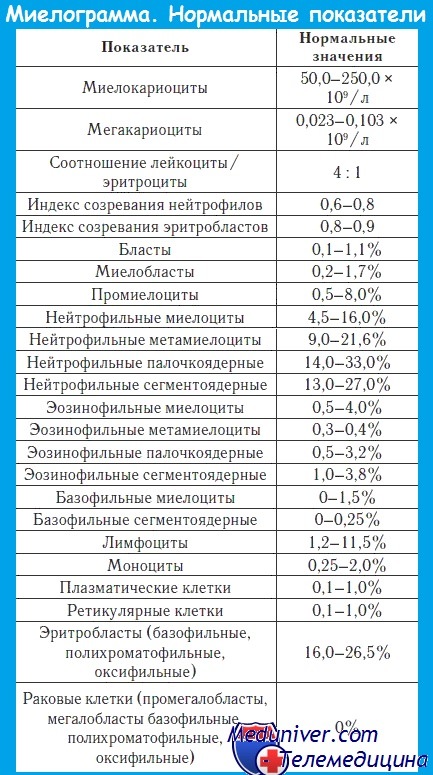
Нормы миелограммы

Миелограмма — картина красного костного мозга в микроскопе
В норме в образцах костного мозга допускается содержание не более 1,7% бластных клеток.
Изменение даже одного показателя миелограммы является показанием для более детального дальнейшего обследования пациентов.
Ниже приведены показатели миелограммы в норме:
| Клеточные элементы | Содержание клеток, % |
|---|---|
| Бласты | 0,1-1,1 |
| Миелобласты | 0,2-1,7 |
| Нейтрофильные клетки: | |
| Промиелоциты | 1,0-4,1 |
| Миелоциты | 7,0-12,2 |
| Метамиелоциты | 8,0-15,0 |
| Палочкоядерные | 12,8-23,7 |
| Сегментоядерные | 13,1-24,1 |
| Все нейтрофильные элементы | 52,7-68,9 |
| Эозинофилы (всех генераций) | 0,5-5,8 |
| Базофилы | 0-0,5 |
| Эритробласты | 0,2-1,1 |
| Пронормоциты | 0,1-1,2 |
| Нормоциты: | |
| Базофильные | 1,4-4,6 |
| Полихроматофильные | 8,9-16,9 |
| Оксифильные | 0,8-5,6 |
| Все эритроидные элементы | 14,5-26,5 |
| Лимфоциты | 4,3-13,7 |
| Моноциты | 0,7-3,1 |
| Плазматические клетки | 0,1-1,8 |
| Кол-во мегакариоцитов (клеток в 1 мкл) | 50-150 |
| Кол-во миелокариоцитов (в тыс. в 1 мкл) | 41,6-195,0 |
| Лейко-эритробластическое соотношение | 4(3):1 |
| Костно-мозговой индекс созревания нейтрофилов | 0,6-0,8 |
Повышенный показатель

Преобладание эритроцитов — признак миелоидного лейкоза
В зависимости от того, какие показатели миелограммы повышены, будет идти речь о каком-либо заболевании крови.
Если в костном мозге отмечается увеличение количества мегакариоцитов, это говорит о наличии метастазов в костях. В случае увеличения бластов на 20% и более речь идет об остром лейкозе. Повышенное соотношение эритроциты/лейкоциты свидетельствует о миелозе, хроническом миелолейкозе, миелозе сублейкемического характера. Индекс созревания нейтрофилов — маркер бластного криза, хронического миелолейкоза.
Рост эритробластов присущ острому эритромиелозу, анемиям. Повышение количества моноцитов наблюдается при хронических миелолейкозах, лейкозах, генерализованных инфекциях. Повышение концентрации плазматических клеток указывает на агранулоцитоз, миеломную болезнь, анемии апластического генеза.
Увеличение эозинофилов в миелограмме говорит о выраженных аллергических реакциях, онкологических заболеваниях различной локализации, лимфогранулематозе, острых лейкозах.
При каждом из обнаруженных изменений необходима дальнейшая диагностика с целью скорейшего начала противоопухолевой терапии и стабилизации состояния пациентов.
Повышение в пунктате костного мозга базофилов может свидетельствовать о миелолейкозе, эритремии, лейкозе базофильного характера. Лимфоцитоз определяется в случае хронических лимфолейкозов, апластической анемии.
Пониженный показатель

Угнетающее влияние на кроветворение могут оказывать цитостатики
Обнаружение снижения синтетической функции костного мозга также свидетельствует о заболеваниях системы кроветворения или является следствием противоопухолевой терапии.
При понижении мегакариоцитов предполагаются аутоиммунные нарушения гипопластического или апластического генеза. Часто такое явление диагностируется на фоне приема цитостатических лекарственных препаратов, радиотерапии.
Снижение данных роста эритроцитарного и лейкоцитарного ростков кроветворения указывает на эритремию, гемолиз, состояния после профузных кровотечений, острый эритромиелоз.
Анемия, вызванная недостатком В12, будет характеризоваться понижением индекса эритробластной дифференцировки. Снижение же количества эритробластов непосредственно характерно для аплазии костного мозга, апластической анемии, статуса после химиотерапевтического и радиологического лечения онкологических больных.
Снижение нейтрофильных миелоцитов, метамиелоцитов, сегментоядерных и палочкоядерных нейтрофилов наблюдается при иммунном агранулоцитозе, анемия апластического генеза, после лечения цитостатическими препаратами.
Показания и противопоказания к проведению

Проведение процедуры имеет показания и противопоказания
Взятие пунктата костного мозга осуществляется по абсолютным или относительным показания.
Обязательно проведение пункции при следующих состояниях:
- любые анемии (кроме анемии, обусловленной недостатком железа);
- понижение клеточного состава любого ростка кроветворения, обнаруживаемые в общем анализе крови;
- лейкозы острые;
- манифестация хронических лейкозов для уточнения диагноза и исключения/подтверждения наличия лейкемоидных реакций;
- одиночное повышение скорости оседания эритроцитов без наличия каких-либо инфекционно-воспалительных заболеваний. В данном случае миелограмма нужна для исключения макроглобулинемии Вальденстрема, множественной миеломы;
- подтверждение/исключение костно-мозговых метастазов;
- лимфогранулематозы;
- неходжкинские лимфомы;
- увеличение селезенки невыясненной этиологии;
- определение тканевой совместимости при операциях по пересадке костного мозга.
К относительным показаниям относят:
- анемии вследствие нехватки железа;
- хронические лейкозы.
Не показано исследование лицам с острой патологией сердечно-сосудистой системы, острой недостаточностью мозгового кровообращения, в периоды обострений патологии сердца, бронхиальной астмы.
Как происходит взятие образца

Проведение стернальной пункции
Процедура занимает 10-15 минут и проводится в стерильных условиях под местной анестезией.
Для этого больного укладывают на кушетку, область прокола обрабатывается антисептическими растворами, а обезболивающее средство вводится подкожно и в надкостницу.
После этого иглой с полым каналом внутри производится прокол по середине грудины на уровне третьей пары ребер. В полость шприца полой иглой набирается приблизительно 0,3 мл пунктата костного мозга, на место прокола накладывается стерильная повязка.
Из полученного образца, ввиду быстрого свертывания крови, сразу же готовится мазок и проводится исследование. Ориентировочное время подсчета миелограммы составляет 4 часа.
Проведение пункции детям младше 2 лет проводится из большеберцовой кости или пяточной кости, детям более старшего возраста — из гребня подвздошной кости, у взрослых образцы берутся не только из грудины, но и из подвздошной кости.
Расшифровка результатов миелограммы

В расшифровке миелограммы помогает следование алгоритму
Для аналитики результатов каждой пункции существует алгоритм, с помощью которого миелограмма полностью отражает картину кроветворения пациентов.
Для этого при описании миелограммы обязательно включаются в описание гемопоэтических характеристик:
- клеточность полученного содержимого;
- состав клеток;
- тип кроветворения;
- очаги атипичных клеток и/или их конгломератов;
- значение индекса соотношения красные/белые кровяные тельца;
- индексы дифференциации нейтрофилов, эритрокариоцитов.
Особую важность составляет отсутствие крови в полученном пунктате. При наличии крови миелограмма будет некорректна, а исследование необходимо будет повторить.
Возможные осложнения

Качественный забор пунктата — минимальный риск осложнений
При неправильной технике забора биологического материала возможны следующие осложнения:
- кровотечение,
- сквозные проколы кости,
- присоединение инфекции в области прокола,
- перелом грудины.
Во избежание развития осложнений необходимо придерживаться рекомендаций врача и тщательно выбирать место проведения пункции костного мозга.
А. анизоцитоз В. причудливая форма ядра
Б. обильная азурофильная зернистость, палочки Ауэра Г. базофильная окраска цитоплазмы
3.75. Для лейкограммы при хроническом миелолейкозе не характерно:
А. увеличение числа лимфоцитов и плазмобластов
3.76. При хроническом моноцитарном лейкозе в картине крови характерен:
Б. абсолютный моноцитоз
3.77. Для лейкограммы обострения хронического миелолейкоза не характерно:
А. уменьшение количества бластных элементов
3.78. Наиболее характерными клинико-лабораторными показателями волосатоклекточного
лейкоза являются: Д. все ответы правильные
А. спленомегалия В. анемия
Б. лейкопения, лимфоцитоз Г. фиброз костного мозга
3.79. При хроническом лимфолейкозе чаще, чем при других лейкозах наблюдается:
А. аутоиммунная гемолитическая анемия
3.80. При остром лейкозе наиболее характерным показателем периферической крови является:
А. анемия, тромбоцитопения, лейкоцитоз с присутствием бластных форм
3.81. Для острого эритромиелоза наиболее характерны:
Г. нормо- или гиперхромная анемия, тромбоцитопения, лейкопения и эритробластоз
3.82. Для развернутой стадии хронического миелолейкоза наиболее характерны:
В. гиперлейкоцитоз, нейтрофилез с левым сдвигом до миелоцитов, промиелоцитов, миелобластов
3.83. Для типичного течения хронического лимфолейкоза наиболее характерны:Г. лейкоцитоз с абсолютным лимфоцитозом
3.84. Выраженная тромбоцитопения с геморрагическим синдромом часто сопровождает:
3.85. По морфологии бластных клеток может быть диагностирован вариант острого лейкоза:Г. промиелоцитарный
3.86. В период полной ремиссии острого лейкоза в миелограмме бластные клетки не должны
превышать:Б. 5%
3.87. При остром лимфобластном лейкозе бластам свойственны положительные реакции: Д. гранулярная ШИК-реакция
При остром Т-лимфобластном лейкозе, бластам свойственны цитохимические реакции: Г. все перечисленные реакции
А. гранулярная ШИК-реакция В. реакция на кислую
Б. реакция на кислую фосфатазу неспецифическую эстеразу
При остром миелобластном лейкозе бласты характеризуются признаками: Д. всем перечисленным
А. реакцией на миелопероксидазу В. реакцией на хлорацетатэстеразу
Б. диффузным типом ШИК-реакции Г. реакцией на липиды
3.90. Маркером острого промнелоцигарного лейкоза является цитохимическая реакция на:В. кислые сульфатированные
Клетки при остром промиелонитарном лейкозе отличаются от нормальных промиелоцитов: Д. все перечисленное верно
А.сетчатым расположением хроматина в В. наличием клеток со складчатыми уродливыми ядрами
ядре Г. наличием в цитоплазме палочек Ауэра
Б. ядерным полиморфизмом
Для острого миеломонобластного лейкоза характерны положительные реакции: Г. все перечисленные
А. на альфа-нафтилацетатэстеразу В. диффузная РА5-реакция Д. ни одна из перечисленных
3.93. При остром монобластном лейкозе бласты характеризуются всеми перечисленными
положительными цитохимическими реакциями,к роме: Б. на альфа-нафтилацетатэстеразу, не подавляемую фторидом натрия м
3.94. Эритрокариоцитам костного мозга при остром эритромиелозе присущи положительные
реакции:Г. на сидеробласты и сидероциты
3.95. Стернальная пункция может не содержать информации при форме миеломной болезни:
А. солитарной миеломе
Цитохимическим маркером острого плазмобластного лейкоза является:Д. все перечисленное неверно
А. гликоген В. неспецифическая эстераза
Б. миелопероксидаза Г. кислая фосфатаза
3.97. Высокий процент плазматических клеток в костном мозге наблюдается при:В. миеломной болезни
3.98. Характерные изменения миелограммы при остром лейкозе:
3.99. Для миелограммы при остром лейкозе свойственны:
А. редукция эритропоэза
При острых лейкозах миелограмме не характерны: Г. все перечисленное
А. нормальная дифференцировка гранулоцитов В. базофильно-эозинофильный комплекс
Б. клетки цитолиза
3.101. Гемограмма при острых лейкозах характеризуется:А. бластозом
3.102. Гемограмме при остром лейкозе не свойственно В. тромбоцитоз
Для гранулоцитов характерна: Д. все перечисленное
А. нейтрофильная специфическая зернистость В. базофильная специфическая зернистость
Б. нейтрофильная и базофильная специфическая Г. эозинофильная специфическая зернистость
3.104. Неэффективный эритропоэз при остром эритромиелозе, миелодиспластическом синдроме
может подтверждаться с помощью цитохимической реакции на:
Клинический анализ крови при остром лейкозе. У большинства больных острым лейкозом (ОЛ) на момент диагностики заболевания имеется нормохромная нормоцитарная анемия, в большей степени выраженная при остром миелобластном лейкозе. При развитии геморрагических осложнений может отмечаться гипохромия вследствие дефицита железа. Количество лейкоцитов периферической крови варьирует в очень широких пределах (от 1 • 10 9 /л до 200 • 10 9 /л), но чаще остается на сублейкемическом уровне и не превышает 20-30 • 10 9 /л.
У 20% пациентов количество бластных клеток превышает 50 • 109/л, а у 10% бласты в периферической крови отсутствуют (при этом обычно отмечаются панцитопения и относительный лимфоцитоз). При уровне лейкоцитов выше 100 • 10 9 /л резко повышается риск развития лейкостатических осложнений (неврологические нарушения, острый респираторный дистресс-синдром, у мужчин, кроме того, приапизм).
Тромбоцитопения выявляется у подавляющего числа больных острым лейкозом и более выражена при остром миелобластном лейкозе (ОМЛ) (у половины больных число тромбоцитов менее 50 • 10 9 /л). В то же время у 1-2% пациентов отмечается тромбоцитоз (более 400 • 10 9 /л).
У части больных может отмечаться увеличение протромбинового и парциального тромбопластинового времени; при остром промиелоцитарном лейкозе часто наблюдается снижение уровня фибриногена и другие признаки синдрома ДВС. Следует отметить, что развитие синдрома ДВС возможно при любом варианте острого лейкоза.
Миелограмма при остром лейкозе. Исследование аспирата костного мозга необходимо для диагностики и установления варианта острого лейкоза. Количество миелокариоцитов обычно повышено, мегакариоциты отсутствуют или их количество снижено. При подсчете миелограммы выявляется не менее 20% бластов, сужение нормальных ростков гемопоэза. Для верификации варианта острого лейкоза необходимо проведение цитохимических, иммунологических и цитогенетических исследований, результаты которых имеют прогностическое значение и позволяют планировать лечебную тактику.
Цитологическое исследование спинномозговой жидкости при остром лейкозе выполняется у всех больных острым лейкозом до начала лечения. При отсутствии патологии при остром лимфобластном лейкозе, миеломонобластных и монобластных острых лейкозов в дальнейшем проводится профилактика нейролейкоза. При развитии нейролейкоза проводят его лечение, результаты которого оцениваются на основании анализа клеточного состава спинномозговой жидкости.
Биохимические исследования при остром лейкозе. В большинстве случаев биохимические показатели находятся в пределах нормальных величин, однако при отдельных вариантах острого лейкоза (ОЛЛ, монобластный лейкоз) может отмечаться нарушение функции почек (повышение уровня креатинина) вследствие их инфильтрации опухолевыми клетками. Специфическая инфильтрация почек и/или их увеличение могут быть документированы с помощью УЗИ или компьютерной томографии. В ряде случаев (при остром лейкозе с гиперлейкоцитозом, острый лимфобластный лейкоз с органомегалией) уже в дебюте заболевания выявляется синдром лизиса опухоли.
Чаще, однако, этот синдром наблюдается при быстром лизисе клеток на фоне химиотерапии и характеризуется гипокальциемией, гиперкалиемией, повышением уровня ЛДГ и гиперурикемией с развитием почечной недостаточности.
Инструментальные исследования при остром лейкозе не имеют решающего значения при остром лейкозе, однако их результаты могут влиять на характер проводимого лечения и прогноз заболевания. Так, рентгенография органов грудной клетки позволяет выявить увеличение лимфатических узлов средостения, пневмонию; электрокардиография — нарушения ритма и/или проводимости, обусловленные специфической инфильтрацией миокарда, антрациклиновой кардиомиопатией и т. д.
Казалось бы, о состоянии системы крови можно и нужно судить по общему анализу – с детства известной рутинной медицинской процедуре. Но на самом деле, данные этого анализа — отражение процессов, происходящих в кроветворной системе, и ее главном органе – костном мозге. Поэтому при подозрении на болезнь кроветворной системы анализируют состояние костного мозга. Пункция костного мозга – это вмешательство, которое позволяет получить 0,5-1мл. этой субстанции для дальнейшего исследования.
Что такое костный мозг и зачем его изучают?
Красный костный мозг находится в плоских костях – ребрах, грудине, позвонках, костях черепа и таза – и в эпифизах (концевых частях) трубчатых костей. Он состоит из двух типов клеток – стромы, или, говоря простым языком, основной структуры, и кроветворных ростков из которых, собственно, и формируются форменные элементы: эритроциты, лейкоциты и тромбоциты.

Все элементы крови развиваются из одинаковых стволовых клеток-предшественников. Созревая (в медицине этот процесс называется дифференцировкой), клетки формируют два ростка кроветворения: лимфоидный, из которого потом созревают лимфоциты и миелоидный, создающий остальные форменные элементы. Незрелые клетки крови называются бластами. Обычно 90% всех стволовых клеток находятся в состоянии покоя.
В организме взрослого мужчины в сутки созревает 300г. форменных элементов крови, то есть 9 кг за год и около 7 тонн за 70 лет жизни. Новые клетки формируются взамен состарившихся или погибших по другим причинам (например, в борьбе с инфекциями).
В норме количество вновь созревших клеток строго равно числу погибших. При гемобластозах (лейкозах) клетки кроветворного ростка мутируют, перестают реагировать на регуляторные сигналы организма, и начинают бесконтрольно делиться. Если активность этого процесса настолько велика, что вновь сформированные клетки не успевают созреть, лейкоз называется острым. Если преобладают зрелые формы – хроническим.
Прежде чем выйти в кровоток, измененные лейкозные клетки накапливаются в красном костном мозге. И только инфильтрировав (заполонив) его, поступают сосуды. Изменения в анализе крови далеко не всегда соответствуют происходящему в костном мозге: на некоторых стадиях развития лейкоза количество форменных элементов в крови может не только не увеличиваться, но и уменьшаться.
Именно по этим причинам пункцию костного мозга и миелограммы выполняют при подозрении на любые болезни кроветворной системы.
Как и для чего выполняют пункцию костного мозга?
Чтобы получить материал для исследования, нужно проткнуть (пунктировать) кость там, где она находится близко к коже. В зависимости от возраста (а количество костного мозга в разных анатомических структурах изменяется со временем), это могут быть:
- у детей младше 2 лет – пяточная или большеберцовая кость;
- у детей старшего возраста – гребень подвздошной кости;
- у взрослых – грудина или гребень подвздошной кости.
Прокол делают специальной иглой с ограничителем – иглой Кассирского. 
Она может выглядеть по-разному. Но суть в том, что ограничитель позволяет зафиксировать глубину прокола.
Иногда полученный материал бывает неинформативен. Тогда (и при некоторых других показаниях) делается трепанобиопсия – метод, при котором специальной толстой иглой одним блоком забирают не только красный костный мозг, но и участок костного фрагмента над ним. Такую биопсию обычно делают в области гребня подвздошной кости.

Место прокола закрывается стерильной повязкой или пластырем. Боль может беспокоить и некоторое время после процедуры. Если нет противопоказаний, можно принять обезболивающие. Место прокола нельзя мочить в течение суток, соответственно, не рекомендуют принимать душ или ванну. Какого-то дополнительного ухода после пункции костного мозга не требуется.
Процедура эта безопасна, единственное абсолютное противопоказание – тяжелые нарушения свертывающей системы крови, когда любая травма приводит к обширным гематомам. Относительные противопоказания (когда сравнивают возможную пользу и вред), это:
- острый инфаркт миокарда;
- декомпенсированная сердечнососудистая патология;
- декомпенсированный сахарный диабет;
- гнойные поражения кожи в области предполагаемой пункции.
- кровотечение;
- инфицирование;
- аллергия – при непереносимости обезболивающих средств;
- сквозной прокол грудины, перелом (если пункция выполняется из грудины).
Вероятность осложнений невелика – по данным Британского общества гематологов за время с 1995 по 2001 год на 54890 проведенных пункций пришлось 26 осложнений разной степени тяжести.
Расшифровка и оценка результатов: миелограмма.
В первую очередь, в счетной камере подсчитываются мегакариоциты и миелокариоциты.
Мегакариоциты – это крупные клетки с большими ядрами, предшественники тромбоцитов. Их должно быть более 20, но менее 50 в 1 мкл.
Далее в окрашенных мазках подсчитывают процентные соотношения клеток различных рядов кроветворения. Полученный результат называется миелограммой.

Чтобы оценить по миелограмме качество костного мозга, важно знать не только процентное и количественное содержание гемопоэтических (кроветворных) элементов, но и их соотношение. Вот расшифровка некоторых показателей.
Высчитывается по формуле: (Промиелоциты + миелоциты + метамиелоциты) / (Палочкоядерные + сегментоядерные нейтрофилы). Нормальное значение 0,6 – 0,8.
Формула расчета: (Полихроматофильные + оксифильные нормобласты) / (Все ядросодержащие клетки красного ростка этого пунктата). Норма 0.8 – 0.9 и снижение индекса говорит о чрезмерно медленном наполнении гемоглобином эритроцитов (например, при железодефицитной анемии).
Как и у любого инструментального исследования, референсные значения (нормы) миелограммы могут изменяться в зависимости от лаборатории и используемых аппаратов.
Особенности миелограммы при лейкозах.
Как при остром, так и при хроническом лейкозе усиленный рост патологических клеток сопровождается уменьшением количества эритроцитов и тромбоцитов на всех стадиях созревания.
Если в миелограмме видны признаки лейкоза, пунктат костного мозга дополнительно проходит иммуногистохимическое, цитохимическое и генотипическое исследования – они нужны чтобы определить характерные особенности мутации опухолевого клона. Это важно для выбора схемы лечения конкретного пациента.
Острые миелоидные лейкозы
Острые миелоидные лейкозы (ОМЛ) представляют гетерогенную группу клональных заболеваний, при которых неопластическая трансформация наблюдается в мультилинейной стволовой клетке или в стволовой клетке с линейной дифференцировкой.
Поскольку мультипотентная стволовая клетка дает начало гранулоцитам, моноцитам, эритроцитам и мегакариоцитам, при ОМЛ возможно поражение всех или отдельных клеточных линий.
В целом неопластический клон прекращает дифференцировку на стадии бласта, что ведет к прогрессирующему накоплению бластов в костном мозге (КМ) с последующим их выходом в периферическую кровь (Рис. 1, 2).

Рис. 1. Схема кроветворения

Рис. 2. Мезенгиогенез. Мезенхимальная стволовая клетка (МСК)
ОМЛ составляют около 20% от всех лейкозов и диагностируются в любом возрасте, однако частота их возникновения увеличивается с возрастом, медиана возраста составляет 60-65 лет.
Заболеваемость составляет 2-3 человека на 100000 населения в год. Этиология острого миелоидного лейкоза неизвестна, однако причинными факторами могут быть: алкилирующие препараты, некоторые химические вещества, пестициды, рентгенконтрастные вещества, красители, миелотоксические агенты, ионизирующее излучение.
Дозы, превышающие 100 рад, оказывают дозо-зависимый эффект в отношении возникновения ОМЛ. Генетическая аномалия - трисомия Хр21 (синдром Дауна) вызывает повышенную частоту развития ОМЛ, хотя в большинстве случаев при этом синдроме развивается острый лимфобластный лейкоз (ОЛЛ).
Повышен риск развития ОМЛ при синдроме Блума, анемии Фанкони, атаксии-телеангиэктазии, нейрофиброматозе Реклингаузена и т.п. Гематологические нарушения - апластическая анемия, хронический миелопролиферативный синдром, миелодиспластические состояния, пароксизмальная ночная гемоглобинурия повышают риск развития острого миелоидного лейкоза.
Клинические проявления неспецифичны. Жалобы на общую слабость, недомогание, головокружение могут задолго предшествовать диагнозу. Нередко отмечается бледность кожных покровов, повышение температуры тела без наличия инфекции, довольно часто отмечается геморрагический синдром по петехиально-пятнистому типу, иногда кровотечения.
Оссалгии отмечаются у 20% больных. Гепатоспленомегалия не является диагностическим признаком ОМЛ, но отмечается у 50% больных. Лейкемиды кожи и инфильтрация десен обычно характерны для миеломоно- и монобластного варианта. Исходное поражение ЦНС встречается редко - при гиперлейкоцитозе и/или монобластном варианте ОМЛ.
Цитохимическими маркерами бластов гранулоцитарного ряда являются липиды, миелопероксидаза (МПО), ASD-хлорацетатэстераза (ASD-ХАЭ). Определение последнего фермента имеет небольшую диагностическую ценность вследствие невысокой ее активности. В диагностике М5а и М5в вариантов ОМЛ главную роль играет исследование неспецифической эстеразы (НЭ), подавляемой фторидом натрия (NaF), антилизоцима.
Применение иммунофенотипирования для диагностики острого миелоидного лейкоза позволяет определить линейность и/или этап дифференцировки бластов, начиная с уровня стволовых клеток-предшественников. Изучение кариотипа бластных клеток позволило выявить закономерные изменения, характерные для отдельных вариантов острых лейкозов.
При цитогенетическом исследовании у 70-80% больных ОМЛ можно выявить неслучайные приобретенные хромосомные аберрации. Некоторые из них, при которых образуется химерный сливной белок, могут служить маркером наличия опухолевого клона. Данные цитогенетического исследования используются для уточнения отдельных вариантов ОМЛ, определения прогноза заболевания, а также для контроля качества и эффективности проводимой терапии.
Таблица 1. Характеристика бластов при ОМЛ (М.А.Френкель, 2001)

Согласно FAB-классификации, выделяют следующие варианты острого миелоидного лейкоза.
Острые миелобластные лейкозы (М0, М1, М2). Этот термин объединяет три подтипа заболевания, которые отличаются друг от друга по степени дифференцировки лейкемических клеток -миелобластов.
М0 составляет около 3-5% ОМЛ. Диагноз может быть установлен только при выполнении иммунофенотипирования. Бласты экспрессируют CD13, CD31. С помощью моноклональных антител (антимиелопероксидазы) - анти-МПО в бластах можно обнаружить фермент миелопероксидазу.
М1 составляет около 15% всех ОМЛ. Морфологически бласты имеют круглое или овальное ядро с рыхлым хроматином, несколько нуклеол и небольшой ободок серо-голубой цитоплазмы без гранул. Тельца Ауэра (первичные лизосомы) выявляются в 10% случаев. При этом варианте определяется минимальная степень миелоидной дифференцировки.
Иммунофенотипическими маркерами является выявление антигенов CD13, 33, 34, HLA-DR. В единичных клетках выявляется транслокация хромосом (Хр) (t 9; 22) и инверсия Хр3. МПО и/или липиды содержатся более чем в 3% бластов.
М2 составляет около 25-32% всех ОМЛ. Более 10% бластов содержит зернистость в цитоплазме в виде нежных темно-красных гранул. Бласты содержат МПО, липиды, гранулоцитарную эстеразу (ГЭ) в большинстве клеток, ШИК-вещество в диффузной форме; бласты экспрессируют антигены CD11, 13, 15, 33, анти-МПО. Примерно в 20-40% случаев выявляется t (8; 21); при этом отмечаются спленомегалия, хлоромы, эозинофилия в периферической крови.
При данной транслокации на длинном плече Хр8 образуется химерный ген AML1-ETO, продуктом деятельности которого является патологический белок CBFa-ETO. При связывании его с ДНК происходит ингибирование транскрипции и, соответственно, нарушаются механизмы дифференцировки миелоидных клеток.
М2 базофильно-клеточный представлен в единичных случаях. Бласты содержат грубую базофильную зернистость, не содержат миелопероксидаза, липиды и ГЭ. Цитогенетически в этих случаях может выявляться t (6; 9). В сыворотке крови повышено содержание гепарина и серотонина. При этой форме острого лейкоза прогноз крайне неблагоприятный.
М3 составляет около 10% случаев острого миелоидного лейкоза. Ядра бластов имеют характерную лопастную форму, цитоплазма содержит обильную азурофильную зернистость и палочки Ауэра. В зависимости от величины гранул выделяют макрогранулярный и микрогранулярный (M3v) варианты данного заболевания. Бласты содержат большое количество МПО, липидов, ГЭ, умеренное количество НЭ, неподавляемой NaF; ШИК-вещество в диффузной форме.
Поскольку в гранулах и тельцах Ауэра содержатся сульфатированные мукополисахариды, обладающие активностью типа тканевого тромбопластина, в большинстве случаев развивается ДВС-синдром (диссеминированное внутрисосудистое свертывание). Бласты экспрессируют антигены CD 11, 13, 15, 33, анти-МПО. В 1977 г. J.D.Rowley и соавторы установили, что в 95% случаев острого промиелоцитарного лейкоза (ОПЛ) обнаруживается t (15; 17).
Вследствие этого PML-ген (ген промиелоцитарного лейкоза), расположенный на Хр15, переносится на длинное плечо Хр17 в область, где находится ген а-рецептора ретиноевой кислоты (RARA). В норме этот ген участвует в регуляции дифференцировки миелоидных клеток. Ген PML является регулятором роста и играет роль в созревании и активации различных клеток.
Продуктом химерного гена PML-RARA является патологический белок, который накапливается в цитоплазме и ядре миелоидных клеток, что приводит к блоку дифференцировки клеток на уровне промиелоцитов. Кроме того, этот белок блокирует механизмы апоптоза, что поддерживает жизнеспособность опухолевых клеток.
В М4 варианте ОМЛ выделяют биклональный (1), бифенотипический (2) и миело-монобластный эозинофильный М4ЕО (3) подварианты. Биклональный вариант составляет около 17% всех случаев, при нем бласты представлены двумя типами клеток -миелобластами и монобластами, и экспрессируют антигены анти-МПО, анти-лизоцим, CD 13, 14, 15, 33. Цитогенетические исследования могут выявить t (8; 21).
Бифенотипический вариант крайне редок. Морфологически бласты характеризуются как миелобласты при М2 варианте, однако во всех бластах одновременно содержится МПО, ГЭ и НЭ, подавляемая NaF.
М5а составляет около 10% острого миелоидного лейкоза. Бласты не имеют специфических морфологических признаков, содержат НЭ, подавляемую фторидом NaF. Отдельные бласты содержат небольшое количество миелопероксидазы и/или липидов. Бласты экспрессируют антигены CD 13, 14, 15, 33, антилизоцим. Иногда (часто после проведенной полихимиотерапии) выявляется аномалия Хр11.
М5в встречается редко. Морфологически бласты имеют моноцитоидную форму ядер, содержат значительное количество НЭ, подавляемой NaF, небольшое количество МПО или липидов. Бласты экспрессируют антигены CD 13, 14, 15, 33, антилизоцим. Как и в предыдущем варианте, может выявляться аномалия Хр11.
Мб (1) - острый эритробластный лейкоз. Характеризуется наличием расширенного патологического красного ростка. Бласты имеют морфологические и цитохимические признаки миелобластов варианта М1. Клетки красного ряда имеют мегалобластоидные изменения с признаками морфологической и цитохимической дисплазии, содержат тельца Жолли, усилена сидерофилия.
Мб (2) - эритромиелоз. В костном мозге преобладает бластная популяция, которая состоит из миелобластов и эритробластов. Бласты не имеют специфических морфоцитохимических признаков, экспрессируют гликофорин А - эритроидный антиген. Цитогенетически можно выявить множественные хромосомные перестройки. Есть мнение, что изменения со стороны клеток красного ряда представляют реакцию на уже имеющийся ОМЛ. Цитогенетические исследования показывают наличие аномалий Хр5,7.
М7 встречается крайне редко. Мегакариобласты в большом количестве в костном мозге с их выходом в периферическую кровь. Цитохимически в бластах находят большое содержание а-нафтил-ацетатэстеразы, не ингибируемой NaF, и некоторое количество а-бутиратэстеразы, выявляется положительная ШИК-реакция. Бласты экспрессируют тромбоцитарные антигены CD 41 и/или CD 61.
Острые лимфобластные лейкозы
Острые лимфобластные лейкозы представляют гетерогенную группу клональных заболеваний лимфопоэтической ткани, характеризующуюся накоплением лимфобластов в КМ. Прогрессирующая инфильтрация опухолевыми лимфобластами костного мозга подавляет продукцию нормальных гемопоэтических клеток. ОЛЛ составляют 10% от всех лейкозов, причем 60% от этого количества наблюдается у детей.
В Европе ОЛЛ является наиболее частым опухолевым заболеванием детского возраста. Пик заболеваемости приходится на возраст 3-7 лет, второй, не очень выраженный пик, отмечается в возрасте 50-60 лет. Заболеваемость острым лимфобластным лейкозом ниже на Среднем Востоке и в Азии. В США частота заболеваемости белого населения в 2 раза выше, чем негроидного.
Подтип В-клеточного ОЛЛ составляет 80% всех случаев ОЛЛ, почти во всех остальных случаях диагностируется Т-ОЛЛ. Крайне редко определяется нуль-клеточный вариант.
Этиология ОЛЛ неизвестна. Не выявлено связи с миелотоксическими агентами, химикатами, ретровирусами, хотя внедрение ретровируса в геном при лечении агаммаглобулинемии Бруттона в некоторых случаях приводило к развитию острого лимфобластного лейкоза.
Умеренное повышение заболеваемости ОЛЛ отмечено под воздействием высоких доз ионизирующего излучения и при некоторых иммунодефицитных состояниях. Хотя вирус Эпштейн-Барра инкорпорируется в геном клеток при африканском варианте лимфомы Беркитта, вирусный геном отсутствует при лимфобластном L3 варианте ОЛЛ. Заболеваемость ОЛЛ в 15-20 раз выше при синдроме Дауна.
В патогенезе ОЛЛ основным является прогрессирующее накопление лимфобластов в КМ, что снижает потенциал дифференцировки и созревания. Для популяции лейкемических лимфобластов характерна остановка дифференцировки трансформированных лимфопоэтических стволовых клеток на специфической стадии, что снижает также уровень апоптоза.
Лейкемические лимфобласты имеют удлиненное время генерации (3 суток) в сравнении с нормальными лимфоидными предшественниками (1 сутки). Поскольку лимфобласты не созревают до более дифференцированной стадии, они накапливаются в костном мозге. Клинически это проявляется анемией, гранулоцитопенией и тромбоцитопенией.
Клиника ОЛЛ обычно представлена неспецифическими симптомами, хотя дебют может быть острым. Наиболее часто отмечаются слабость, сонливость, оссалгии, артралгии, не связанное с инфекцией повышение температуры тела. Иногда единственной жалобой являются оссалгии при отсутствии лимфоаденопатии, органомегалии и изменений в анализах периферической крови.
При вовлечении в процесс ЦНС отмечаются головная боль, тошнота, рвота. Бактериальная инфекция встречается при выраженной нейтропении. При физикальном обследовании может отмечаться бледность кожных покровов, геморрагический синдром по петехиально-пятнистому типу, лимфоаденопатия (чаще в области шеи), гепатоспленомегалия. Крайне редко бывают лейке -миды кожи.
В анализе крови в 60% случаев отмечается сублейкоцитоз, в 10% - гиперлейкоцитоз свыше 100,0х10 9 /л, тромбоцитопения менее 50,0х10 9 /л - у 60% больных в момент диагностики. При гиперлейкоцитозе почти всегда отмечается лимфоаденопатия, гепато- и спленомегалия. Анемия является непостоянным признаком.
В пунктате КМ отмечается гиперклеточность с наличием более 20% бластов. Для установления диагноза необходимо комплексное (морфологическое, цитохимическое, иммунофенотипическое, цитогенетическое) исследование бластных клеток.
Цитогенетическое изучение выявило некоторые аномалии количества хромосом или их структуры в 90% случаев острого лимфобластного лейкоза. Гипердиплоидность (47 или более хромосом) выявлена у 1/3 больных. Обычно существуют хромосомные транслокации, вовлекающие протоонкогены; большинство из них демонстрируют транслокацию c-myc протоонкогена Хр8 в регион гена Хр14, кодирующий иммуноглобулины (Ig). - t (8; 14).
В случаях В-ОЛЛ встречаются t (2; 8) или t (8; 22). Это специфические транслокации, т.к. локус с c-myc дерегулируется промотором Ig. При пре-В-клеточном варианте острого лимфобластного лейкоза специфическая транслокация t (1; 19) наблюдается в 25% случаев. В результате гибридный ген Хр19 кодирует белок, который нарушает регуляцию транскрипции.
Описаны транслокации при Т-клеточном остром лимфобластном лейкозе, вовлекающие Хр11 и локус Т-клеточного рецептора (TCR) на Хр14 и Хр7, а также делеции Хр6, Хр9, Хр12, так что в этих случаях может происходить потеря опухолевых генов-супрессоров. Филадельфийская хромосома (Ph), t (9; 22) выявляется в 20% ОЛЛ у взрослых и менее чем в 5% у детей. Патологический белок, кодируемый гибридным геном при этой транслокации, при ОЛЛ отличается от белка, продуцируемого химерным геном BCR/ABL при хроническом миелолейкозе.
Лимфобласты при ОЛЛ всегда весьма гетерогенны.
Выделяют три подтипа острого лимфобластного лейкоза:
L1 - лимфобласты малой величины, имеют круглое или овальное ядро с тонко организованным хроматином, единичными нуклеолами и ободком голубой цитоплазмы.
L2 - лимфобласты средней и большой величины, имеют ядро неправильной формы с рыхлым хроматином, одну или более нуклеол и ободок умеренно серо-голубой цитоплазмы.
L3 - лимфобласты крупных размеров, с круглым или овальным ядром, содержащим глыбчатый хроматин, 2-5 нуклеол и ободок темно-голубой и частично вакуолизированной цитоплазмы.
С учетом иммунологических маркеров можно выделить четыре подтипа ОЛЛ, три из них В-клеточного и один - Т-клеточного происхождения.
Имеются два подтипа, состоящие из предшественников В-клеток:
- пре-пре-В клеточный ОЛЛ (морфологически - L1 вариант),
- пре-В клеточный ОЛЛ (морфологически - L2 вариант).
Третий подтип В-клеточного ОЛЛ состоит из более зрелых В-клеток (L3 вариант).
Около 20% случаев ОЛЛ происходят из предшественников Т-клеток и относятся морфологически к L2 варианту. Демонстрируется реаранжировка генов в- или гамма-цепей рецептора Т-клеток (TCR).
ОЛЛ из нуль-клеток - это малая пропорция случаев ОЛЛ, отличающаяся по маркерам от В- или Т-линии лимфоцитов и поэтому называемая нуль-ОЛЛ или неклассифицируемым ОЛЛ.
При цитохимическом исследовании характерно наличие терминальной динуклеотидил-трансферазы (Тс1Т) в 95% случаев пре-пре-В-, пре-В клеточного ОЛЛ и Т-клеточном ОЛЛ.
Активность фермента снижена в зрелых В-лимфоцитах и при L3 варианте ОЛЛ. При ОНЛЛ активность фермента выявляется только в 5-10% случаев.
Таблица 2. Характеристика бластов при ОЛЛ (М.А. Френкель, 2001)

Реакции на МПО, специфические и неспецифические эстеразы, ШИК-реакция - отрицательные. Реакция на окрашивание масляным красным - положительная.
Читайте также:

