Гонадотропин секретирующие опухоли гипофиза
Опухоли гипофиза – группа доброкачественных, реже – злокачественных новообразований передней доли (аденогипофиза) или задней доли (нейрогипофиза) железы. Опухоли гипофиза, по статистике, составляют около 15% новообразований внутричерепной локализации. Они одинаково часто диагностируются у лиц обоих полов, обычно в возрасте 30-40 лет. Подавляющее большинство опухолей гипофиза составляют аденомы, которые подразделяются на несколько видов в зависимости от размеров и гормональной активности. Симптомы опухоли гипофиза представляют собой сочетание признаков объемного внутримозгового процесса и гормональных нарушений. Диагностика опухоли гипофиза осуществляется проведением целого ряда клинических и гормональных исследований, ангиографии и МРТ головного мозга.
- Причины опухолей гипофиза
- Классификация опухолей гипофиза
- Симптомы опухолей гипофиза
- Диагностика опухолей гипофиза
- Лечение опухолей гипофиза
- Прогноз при опухолях гипофиза
- Цены на лечение
Общие сведения
Опухоли гипофиза – группа доброкачественных, реже – злокачественных новообразований передней доли (аденогипофиза) или задней доли (нейрогипофиза) железы. Опухоли гипофиза, по статистике, составляют около 15% новообразований внутричерепной локализации. Они одинаково часто диагностируются у лиц обоих полов, обычно в возрасте 30-40 лет.
Гипофиз является железой внутренней секреции, осуществляющей регулятивно-координирующую функцию в отношении некоторых других эндокринных желез. Гипофиз расположен в ямке турецкого седла клиновидной кости черепа, анатомически и функционально связан с отделом головного мозга – гипоталамусом. Вместе с гипоталамусом гипофиз составляет единую нейроэндокринную систему, обеспечивающую постоянство гомеостаза организма.
В гипофизе выделяют две доли: переднюю – аденогипофиз и заднюю – нейрогипофиз. Гормонами передней доли, вырабатываемыми аденогипофизом, являются: пролактин, стимулирующий секрецию молока; соматотропный гормон, влияющий на рост организма через регуляцию белкового обмена; тиреотропный гормон, стимулирующий метаболические процессы в щитовидной железе; АКТГ, регулирующий функцию надпочечников; гонадотропные гормоны, влияющие на развитие и функцию половых желез. В нейрогипофизе образуются окситоцин, стимулирующий сократительную способность матки, и антидиуретический гормон, регулирующий процесс реабсорбции воды в канальцах почек.
Аномальное разрастание клеток железы приводит к образованию опухолей переднего или заднего отдела гипофиза и нарушению гормонального баланса. Иногда в область гипофиза прорастают менингиомы – опухоли мозговых оболочек; реже железа поражается метастатическими отсевами злокачественных новообразований других локализаций.

Причины опухолей гипофиза
Достоверные причины развития опухолей гипофиза до конца не изучены, хотя известно, что некоторые виды новообразований могут быть обусловлены генетически.
В число факторов, предрасполагающих к развитию опухолей гипофиза, входят нейроинфекции, хронические синуситы, черепно-мозговые травмы, гормональные изменения (в том числе вследствие длительного применения гормональных препаратов), неблагоприятное воздействие на плод в период беременности.
Классификация опухолей гипофиза
Опухоли гипофиза классифицируются с учетом их размеров, анатомического расположения, эндокринных функций, особенностей микроскопического окрашивания и т. д. В зависимости от размера новообразования выделяют микроаденомы (менее 10 мм в максимальном диаметре) и макроаденомы (при наибольшем диаметре более 10 мм) гипофиза.
По локализации в железе различают опухоли аденогипофиза и нейрогипофиза. Опухоли гипофиза по топографии относительно турецкого седла и окружающих его структур бывают эндоселлярными (выходящими за границы турецкого седла) и интраселлярными (расположенными в пределах турецкого седла). С учетом гистологической структуры опухоли гипофиза подразделяются на злокачественные и доброкачественные новообразования (аденомы). Аденомы исходят из железистой ткани передней доли гипофиза (аденогипофиза).
- соматотропная аденома
- соматотропинома – опухоль гипофиза, синтезирующая соматотропин - гормон роста;
- пролактиновая аденома
- пролактинома – опухоль гипофиза, синтезирующая гормон пролактин;
- кортикотропная аденома
- кортикотропинома - опухоль гипофиза, секретирующая АКТГ, стимулирующий функцию коры надпочечников;
- тиротропная аденома
- тиротропинома - опухоль гипофиза, секретирующая тиротропный гормон, стимулирующий функцию щитовидной железы;
Фоллтропинпродуцирующие или лютропинпродуцирующие аденомы (гонадотропные). Эти опухоли гипофиза секретируют гонадотропины, стимулирующие функцию половых желез.
Гормонально-неактивные опухоли гипофиза и пролактиномы встречаются наиболее часто (в 35% случаев соответственно), соматотропинпродуцирующие и АКТГ-продуцирующие аденомы – в 10-15% случаев от всех опухолей гипофиза, другие виды опухолей образуются редко. По особенностям микроскопии различают хромофобные опухоли гипофиза (гормонально-неактивные аденомы), ацидофилиные (пролактиномы, тиротропиномы, соматотропиномы) и базофильные (гонадотропиномы, кортикотропиномы).
Развитие гормонально-активных опухолей гипофиза, продуцирующих один или несколько гормонов, может приводить к развитию центрального гипотиреоза, синдрома Кушинга, акромегалии или гигантизма и т. д. Повреждение гормонопродуцирующих клеткок при росте аденомы может вызывать состояние гипопитуаризма (гипофизарной недостаточности). У 20% пациентов отмечается бессимптомное течение опухолей гипофиза, которые обнаруживаются лишь при аутопсии. Клинические проявления опухолей гипофиза зависят от гиперсекреции того или иного гормона, размеров и скорости роста аденомы.
Симптомы опухолей гипофиза
По мере увеличения опухоли гипофиза развиваются симптомы со стороны эндокринной и нервной систем. Соматотропинпродуцирующие аденомы гипофиза приводят к возникновению акромегалии у взрослых пациентов или гигантизма, если они развиваются у детей. Пролактинсекретирующие аденомы характеризуются медленным ростом, проявляются аменореей, гинекомастией и галактореей. Если такие опухоли гипофиза продуцируют неполноценный пролактин, то клинические проявления могут отсутствовать.
АКТГ-продуцирующие аденомы стимулируют секрецию гормонов коры надпочечников и ведут к развитию гиперкортицизма (болезни Кушинга). Обычно такие аденомы растут медленно. Тиротропинпродуцирующие аденомы нередко сопровождают течение гипотиреоза (функциональной недостаточности щитовидной железы). Они могут вызывать упорный тиреотоксикоз, чрезвычайно устойчивый к медикаментозному и хирургическому лечению. Гонадотропные аденомы, синтезирующие половые гормоны, у мужчин приводят к развитию гинекомастии и импотенции, у женщин – к нарушению менструального цикла и маточным кровотечениям.
Увеличение размеров опухоли гипофиза ведет к развитию проявлений со стороны нервной системы. Поскольку гипофиз анатомически соседствует с перекрестом зрительных нервов (хиазмом), то при увеличении размеров аденомы до 2 см в диаметре развиваются зрительные нарушения: сужение полей зрения, отек сосочков зрительного нерва и его атрофия, ведущие к падению зрения, вплоть до слепоты.
Аденомы гипофиза больших размеров вызывают сдавление черепных нервов, сопровождающееся симптомами поражения нервной системы: головные боли; двоение в глазах, птоз, нистагм, ограничение движений глазных яблок; судороги; упорный насморк; деменцию и изменения личности; повышение внутричерепного давления; кровоизлияния в гипофиз с развитием острой сердечно-сосудистой недостаточности. При вовлеченности в процесс гипоталамуса могут наблюдаться эпизоды нарушения сознания. Злокачественные опухоли гипофиза встречаются крайне редко.
Диагностика опухолей гипофиза
Необходимыми исследованиями при подозрении на опухоль гипофиза являются тщательное офтальмологическое и гормональное обследования, нейровизуализация аденомы. Исследование мочи и крови на содержание гормонов позволяет установить вид опухоли гипофиза и степень ее активности. Офтальмологическое обследование включает оценку остроты и полей зрения, позволяющих судить о вовлеченности в процесс зрительных нервов.
Нейровизуализацию опухоли гипофиза позволяет осуществить рентгенография черепа и зоны турецкого седла, МРТ и КТ головного мозга. Рентгенологически могут определяться увеличение размеров турецкого седла и эрозия его дна, а также увеличение нижней челюсти и пазух носа, утолщение костей черепа, и расширение межзубных промежутков. С помощью МРТ головного мозга возможно увидеть опухоли гипофиза диаметром менее 5 мм. Компьютерная томография подтверждает наличие аденомы и ее точные размеры.
При макроаденомах ангиография сосудов головного мозга указывает на смещение сонной артерии и позволяет дифференцировать опухоль гипофиза с внутричерепной аневризмой. В анализе спинномозговой жидкости может определяться повышенный уровень протеинов.
Лечение опухолей гипофиза
На сегодняшний день в лечении опухолей гипофиза эндокринология применяет хирургический, лучевой и лекарственный методы. Для каждого вида опухолей гипофиза существует специфический, наиболее оптимальный вариант лечения, который подбирается эндокринологом и нейрохирургом. Наиболее эффективным считается хирургическое удаление опухоли гипофиза. В зависимости от размеров и локализации аденомы проводится либо ее фронтальное удаление через оптический прибор, либо резекция через клиновидную кость черепа. Оперативное удаление опухолей гипофиза дополняется лучевой терапией.
Гормонально-неактивные микроаденомы лечатся с помощью лучевой терапии. Проведение лучевой терапии показано при наличии противопоказаний к оперативному лечению, а также пожилым пациентам. В послеоперационном периоде проводится гормонозаместительная терапия (кортизоном, тиреоидными или половыми гормонами), при необходимости - коррекция электролитного обмена и инсулинотерапия.
Из лекарственных препаратов используют агонисты дофамина (каберголин, бромокриптин), вызывающие сморщивание пролактин- и АКТГ-секретирующих опухолей гипофиза, а также ципрогептадин, понижающий уровень кортикостероидов у пациентов с синдромом Кушинга. Альтернативным методом лечения опухолей гипофиза является замораживание участка ткани железы при помощи зонда, введенного через клиновидную кость.
Прогноз при опухолях гипофиза
Дальнейший прогноз при опухолях гипофиза во многом определяется размерами аденом, возможностью их радикального удаления и гормональной активностью. У пациентов с пролактиномами и соматотропиномами полное восстановление гормональной функции наблюдается в четверти случаев, при адренокортикотропинпродуцирующих аденомах - в 70-80% случаев.
Макроаденомы гипофиза размером более 2 см полностью удалить невозможно, поэтому возможны их рецидивы в течение 5-летнего срока после операции.
Макроаденома гипофиза
Опухоли гипофиза (аденома гипофиза) составляют 10 – 15% всех внутричерепных опухолей. Если размеры опухоли превышают 10 мм, она называется макроаденомой. Аденома гипофиза размерами до 10 мм, называется микроаденомой.
Аденомы гипофиза – доброкачественные эпителиальные опухоли, состоящие из аденогипофизарных клеток. Первично злокачественные опухоли гипофиза встречаются крайне редко.
Ежегодно выявляется 1-7 случаев аденомы гипофиза в популяции из 100 000 человек.
Эпидемиология
Аденома гипофиза встречается с одинаковой частотой у мужчин и женщин.
Исключением являются кортикотропиномы, встречающиеся чаще у женщин, чем у мужчин (соотношение женщина/мужчина составляет 4/1). В целом у женщин репродуктивного возраста аденомы встречаются чаще, чем у мужчин.
Макроаденомы гипофиза встречаются во всех возрастных группах, с возрастом вероятность возникновения опухолей растет, пик заболеваемости приходит между 3 и 6 десятками жизни.
Клинические проявления:
1. Масс – эффект – сдавление зрительных нервов, зрительного перекреста, зрительных трактов, что приводит к зрительным нарушениям в виде выпадения височных половин полей зрения (битемпоральная гемианопсия), снижению зрения до слепоты.
2. Нарушение гормонального баланса (снижение продукции гормонов из – за компрессии нормальных питуицитов (клеток аденогипофиза) или чрезмерная продукция какого – либо гормона патологическими клетками.
Клиническая картина
- Масс – эффект – повышение внутричерепного давления – головная боль, картина сдавления окружающих нервных структур – при поражении зрительного тракта возникают зрительные нарушения – снижение зрения, сужение полей зрения с височных сторон, битемпоральаня гемианопсия, снижение зрения до слепоты. При росте опухоли в кавернозные синусы возникают глазодвигательные нарушения.
- Пангипопитуитаризм – снижение гормнальной активности нормальных клеток вследствие компрессии патологическими клетками. Клетки аденогипофиза не одинаково чувствительны к компрессии. Более чувствительными к компрессии являются соматотропные и гонадотропные гормоны вырабатывающие клетки, тогда, как вырабатывающие тиреотропные и кортикотропные гормоны клетки, наиболее стойкие к компрессии.
- Описаны случаи внутриопухолевого и внутричерепного кровоизлияния
- Апоплексия гипофиза происходит вследствие инфаркта опухоли или кровоизлияния в ней. В таких ситуациях возникает резкая головная боль, коллапс, шок и наступает летальный исход при отсутствии экстренной медицинской помощи. Кровоизлияния в опухоль происходят как правило в макроаденомах. Назначение стимулирующих препаратов – как тироид – стимулирубщий гормн, гонадотропин – релизинг гормон, инсулин – гипогликемии, приводят к повышению метаболических потребностей опухоли и увеличивают вероятность возникновения некроза. Апоплексия в гонадотропомах может возникать у пожилых людей, получивших агонистную GnRH терапию по поводу рака простаты.
- Синдром Нелсона развивается вследствие лечения болезни Кушинга путем билатеральной адреналэктомии. Отсутствие отрицательной обратной связи приводит к быстрому росту опухоли. Такие опухоли намного более агрессивные и инвазивны, по сравнению с обычными кортикотропными аденомами.
- Часто в гормноальной картине при макроаденомах гипофиза сочетается избыточная выработка некоторых гормонов с недостатком других.
- Гиперпролактинемия – часто сочетается с гипогонадизмом, нефертильностью, аменореей, галактореей. Гиперпролактинемия возникает как вследствие гиперпродукции пролактина опухолевыми клетками, так и вследствие компрессии стебля гипофиза опухолью. Во втором случае уровень пролактина в крови повышается не более чем на 2-3 раза по сравнению с нормой.
- Гиперпродукция кортикотропных гормонов приводит к развитию болезни Кушинга. Кортикотропиномы редко бывают макроаденомами. Выработка патологичного кортикотропина приводит к подавлению нормального кортикотропина, что приводит к глюкокортикоидной недостаточности.
- Избыточная продукция тиротропного гормноа проявляется вторичным гипертироидизмом. Тиротропомы встречаются крайне редко. Они не настолько агрессивны, чем агрессивность и инвазивность обусловлены отсроченной диагностикой. Выработка биологически неадекватного тиротропина приводит к вторичному гипотироидизму.
- Чрезмерная выработка гормона роста приводит к акромегалии. Как правило, соматотропомы бывают микроаденомами.
- Гонадотропиномы чаще асимптоматические и как правило продуцируют неактивный ФСГ- и ЛГ- сходные гликопротеины и/ил альфа – субчастицы. Чаще они макроаденомы и, как правило приводят к гипопитуитаризму. Реже они приводят к тестикулярному увеличению у мужчин и овариальной стимуляции у женщин. Дефицит гонадотропных гормонов проявляется гипогонадизмом и бесплодием.
Гормноально активные опухоли проявляются симптомами стимуляции мишеневых органов.
Лабораторные исследования
- Исследование базального уровня гормонов и динамическое исследование гормонов.
- Исследование базального уровня гормонов – пролактин, тиротропный гормон, АКТГ, кортизол, ЛГ, ФСГ, эстрадиол, тестостерон, гормон роста, ИРФ 1, альфа – субчастица гликопротеина.
Динамическое исследование гормонов позволяет оценить функциональную активность аденомы и имеет дифференциально – диагностическое значение.
- TRH – приводит к повышению уровня пролактина и тиротропина в крови. При пролактиномах, гиперпролактинемических состояниях, при гипертироидизме, пангипопитуитаризме возникает резкий (blunted) ответ. Гонадитропиномы на TRH реагируют парадоксально.
- GHRH – приводит к повышению уровня гормона роста. Данный ответ blunted при дефиците гормона роста, болезни Кушинга, гипопитуитаризме. Другие агенты, которые применяются для данного теста являются инсулин, L- допа, аргинин, клонидин. При акромегалии может быть парадоксальное уменьшение гормона роста.
- Гипергликемия подавляет продукцию гормона роста. Подавление не возникает при питуитарных опухолях, продуцирующих гормн роста, при эктопических гормон роста – вырабатывающих опухолях, при синдроме Кушинга, при нервной анорекии. Парадоксальное повышение уровня гормона роста наблюдается при акромегалии, острых заболеваниях, при ХПН. У многих пациентов с акромегалией возникает парадоксальное повышение уровня гормона роста на TRH и GnRH.
- CRH – приводит к повышению уровня кортикотропина. Данный ответ усиливается при болезни Кушинга, но blunted при других синдромах Кушинга. При сочетании с исследованием уровня гормона в нижнем коменистом синусе можно дифференцировать болезнь Кушинга от доброкачественных эктопических АКТГ вырабатывающих синдромов.
- Инсулином вызванная гипогликемия приводит к повышению уровня кортикотропина, кортизола, гормона роста. Blunted ответ наблюдается при синдроме Кушинга, дефиците гормона роста, гипотироидизме, гипертироидизме.
- Метирапон вызывает повышение утреннего уровня 11-деоксикортизола и 17-гидрокортикостероида. Повышенный ответ наблюдается при болезни Кушинга, но не наблюдается при других синдромах Кушинга.
- Тесты подавления дексаметазона применяются для оценки синдрома Кушинга. Введение 1 мг дексаметазона накануне ночью подавляет утренний уровень кортизола. Супрессия кортизола высокими и низкими дозами дексаметазона применяется для установки диагноза синдрома Кушинга и дифференциации между болезнью Кушинга и эктопической продукцией кортикотропина.
Исследования
- Рентгенография черепа – расширение турецкого седла, разрушение спинки турецкого седла
- КТ головного мозга
- МРТ головного мозга с в/в контрастированием
Консультация окулиста, нейроофтальмолога – исследование полей зрения, остроты зрения, глазодвигательные нарушений
Лечение – целью лечения является полное выздоровление. Если это не возможно, нужно стремиться к уменьшению размеров опухоли, снижению гормональной активности, восстановлению нормального зрения, нормальнизации гормональной функции. Для этой цели применяются лекарства, хирургия, лучевая терапия. Часто требуется нейрохирургические вмешательства. Исключением являются макропролактиномы, которые хорошо лечатся медикаментозно. Фармакотерапия направлена на уменьшение размеров опухоли, нормализацию гормонального уровня, коррекции гормонального дефицита.
Пролактин – секретирующие макроаденомы хорошо отвечают на агонисты допамина. Чаще применяемы лекарства – бромкриптин, каберголин, перголид. Квинаголид является алтернативным лекарстом с меньшими побочными эффектами. Пролактин – сектертирующие макроаденомы настолько чувствительны к лечению, что чаще хирургическое лечение и радиотерапия не применяются. Необходимость в нейрохирургическом лечены при пролактиномах возникает в 25 % случаев.
Соматотропомы как правило лечатся нейрохирургическим путем, часто с последующей лучевой терапией. Лечение акромегалии только хирургически, без лучевой терапии маловероятно. Тем не менее, резекция опухоли имеет большое значение. Лучевая терапия приводит к уменьшению уровня гормона роста на 50 % в течение первых 2 лет, с последующим снижением на 25 % в последующие 2 года. Чем ниже уровень гормона роста, тем больше вероятность ремиссии после лучевой терапии. Для лечения применяются октреотид, соматостатин. Эффективность агонистов допамина ниже эффективности октротида (около 30% при соматотропомах)
Кортикотропин – секретирующие опухоли – хирургия и лучевая терапия (несмотря на то, что они часто нерадиочувствительны). Лкарственные препараты применяются при невозможности выполнить другими способами. Лекарственные препараты делятся на агенты, действубщие центрально, снижающие продукцию кортикотропина и пеиферические агенты, снижающие продукцию и действие кортизола. Центрально действующим агентами ( к сожалению они редко эффективны) являются – бромкриптин, валпроевая кислота, ципрогептадин. Периферическими агентами являются – кетоконазол, митотан, метирапон. Эти лекарства часто комбинируются с лучевой терапией.
Гонадотропин – секретирующие – лечатся хирургически с последующей лучевой терапией. Антагонисты ЛГ – могут снизить уровень гормонов, не без влияния на размеры опухоли. Могут быть применены бромкриптин и октреотид.
Гормонально неактивные – лечатся хирургически. Эффективность лучевой терапии и фармакотерапии при данном виде аденом достаточно низкая. При противопоказаний к хирургии применяются бромкриптин.
Тиротропин – секретирующие – лечатся хирургически, с последующей лучевой терапией. Октреотид достаточно эффективен при данной опухоли и может быть применен как адьювантная терапия.
При отсутствии возможности хирургического лечения применяются радиотерапия и гамма – нож.
Хирургическое лечение – только 1% больных с аденомами гипофиза оперируются транскраниально. Во всех остальных случаях оперативные вмешательства выполняются трансназальным доступом эндоскопически или микронейрохирургически.

Опухоли гипофиза почти всегда доброкачественные и встречаются приблизительно у 10% взрослых.
В большинстве случаев они небольших размеров, их обнаруживают случайно при радиологическом обследовании.
Частота гормон-продуцирующих опухолей:
- пролактин-секретирующие — 25—30%;
- гонадотропин-секретирующие (обычно клинически бессимптомные, т.е. фактически субклинические) — 25—30%;
- АКТГ-секретирующие — 15%;
- СТГ-секретирующие — 15%;
- плюригормональные — 12%;
- ТТГ-секретирующие — 2%.
Симптомы гормонально-активной опухоли гипофиза связаны, с одной стороны, с гиперпродукцией соответствующего гормона. С другой стороны, симптомы могут быть связаны с воздействием на ЦНС массы макроопухоли (диаметром более 1 см) или же опухоли размером менее 1 см, когда происходит экстраселлярный её рост:
- головная боль;
- нарушение зрения (обычно битемпоральная гемианопсия, обусловленная давлением опухоли на перекрест зрительных нервов);
- паралич глазодвигательных нервов;
- гидроцефалия;
- инсульт;
- ринорея цереброспинальной жидкости.
Следует также заметить, что макроопухоль может разрушать гипофиз, вызывая гипопитуитаризм или симптомы НД.
Спонтанное кровоизлияние в опухоль гипофиза (апоплексия гипофиза) регистрируют в 15—20% случаев, причём у 1/3 больных проявляется определёнными симптомами:
- головная боль;
- снижение зрения;
- паралич глазодвигательных нервов;
- другие неврологические симптомы поражения ЦНС.
Лечение при кровоизлиянии в гипофиз может потребовать хирургического удаления гематомы, а также введения глюкокортикоидов и возмещения потери жидкости.
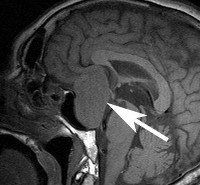
Среди радиологических методов обследования МРТ служит методом выбора в диагностике и оценке степени распространённости опухоли гипофиза. МРТ более чувствительна, чем КТ, в выявлении микроаденом. МРТ можно выполнять как с контрастом, так и без него. Исследование позволяет выявить взаимоотношения опухоли с хиазмой и другими структурами ЦНС. Следует заметить, что нормальная МРТ-картина гипофиза не исключает наличия микроаденом диаметром менее 2—3 мм.
Выбор метода лечения опухоли гипофиза
| Показания | Не показано |
|---|---|
| Хирургический транссфеноидальный доступ | |
| Микроаденома (диаметром менее 1 см). Опухоль распространяется в сфеноидальный синус или происходит ринорея цереброспинальной жидкости. Развилось кровоизлияние в аденому. Макроаденома (диаметром более 1 см) с минимальным или умеренным супраселлярным ростом | Обычно не показано при небольших интраселлярных опухолях без гормональной активности |
| Хирургический трансфронтальный доступ | |
| Большая опухоль с супраселлярным ростом, особенно если распространяется в область диафрагмы турецкого седла или с латеральным супраселлярным ростом. Противопоказание к транссфеноидальному доступу (у больных хроническим синуситом или неполной пневматизацией сфеноидального синуса) | Не проводят при небольших интраселлярных опухолях |
| Лечение допаминергическими агонистами | |
| Главное лечение пролактин-секретирующих опухолей. Быстрое устранение неврологических последствий больших пролактин-секретирующих опухолей. Уменьшение размера опухоли перед её хирургическим удалением. | Нефункционирующие опухоли гипофиза (хотя у некоторых больных возможно уменьшение размера опухоли). Основное лечение акромегалии, за исключением случаев, когда удаление опухоли невозможно |
| Лечение беременных с пролактин-секретирующей опухолью, у которых выявлена склонность к её росту. Дополнительное лечение больных акромегалией или с ТТГ-секретирующей опухолью | |
| Лечение октреотидом | |
| Вспомогателная терапия у больных акромегалией или с ТТГ-секретирующей опухолью. Основное лечение, когда удаление опухоли невозможно | Другие типы опухоли |
| Лечение пегвисомантом | |
| Постоянная гиперсекреция СТГ после удаления опухоли и/или лечение октреотидом | Ведущее лечение акромегалии, за исключением случаев, когда невозможно никакое другое лечение |
| Радиотерапия | |
| Небольшие или среднего размера опухоли с минимальным или умеренным супраселлярным ростом. Хирургическое лечение противопоказано, или больной от него отказывается. Дополнительное лечение после неполного удаления опухоли | Значительный супраселлярный рост опухоли (опасность поражения зрительного нерва облучением). Значительные выпадения полей зрения. Акромегалия, когда уровень СТГ >50 нг/мл перед началом лечения. |
Предоперационная подготовка заключается в исследовании всех гормонов гипофиза, которые затем после операции должны быть исследованы повторно для оценки степени сохранности функции гипофиза. Кроме того, необходимо обязательно исключить дефицит тиреоидной функции (Т3, Т4), так как он существенно влияет на исход операции. Исследование пролактина и ИРФ-1 нужно для исключения так называемых оккультных (субклинических) вариантов течения акромегалии или пролактиномы. Независимо от резервов АКТГ перед операцией в большинстве случаев вводят дополнительно глюкокортикоиды как в предоперационном периоде, так и во время операции, чтобы исключить развитие острого гипокортицизма во время стрессорного хирургического вмешательства.
Послеоперационное наблюдение заключается в оценке необходимости соответствующей заместительной терапии тиреоидными, половыми гормонами и/или глюкокортикоидами, т.е. оценка гипофизарной недостаточности. Регулярный менструальный цикл у женщин после операции указывает на сохранённую в достаточной мере секрецию эстрогенов, поэтому не требуется дополнительного обследования, если не возникает проблема с бесплодием. Аналогично оценивают функцию гипофиза после радиотерапии.
Длительное наблюдение сводится к регулярному осмотру и обследованию больного.
Опухоли гипофиза – группа доброкачественных, реже – злокачественных новообразований передней доли (аденогипофиза) или задней доли (нейрогипофиза) железы.
Опухоли гипофиза, по статистике, составляют около 15% новообразований внутричерепной локализации. Они одинаково часто диагностируются у лиц обоих полов, обычно в возрасте 30-40 лет.
Гипофиз является железой внутренней секреции, осуществляющей регулятивно-координирующую функцию в отношении некоторых других эндокринных желез. Гипофиз расположен в ямке турецкого седла клиновидной кости черепа, анатомически и функционально связан с отделом головного мозга – гипоталамусом. Вместе с гипоталамусом гипофиз составляет единую нейроэндокринную систему, обеспечивающую постоянство гомеостаза организма.
В гипофизе выделяют две доли: переднюю – аденогипофиз и заднюю – нейрогипофиз. Гормонами передней доли, вырабатываемыми аденогипофизом, являются: пролактин, стимулирующий секрецию молока; соматотропный гормон, влияющий на рост организма через регуляцию белкового обмена; тиреотропный гормон, стимулирующий метаболические процессы в щитовидной железе; АКТГ, регулирующий функцию надпочечников; гонадотропные гормоны, влияющие на развитие и функцию половых желез. В нейрогипофизе образуются окситоцин, стимулирующий сократительную способность матки, и антидиуретический гормон, регулирующий процесс реабсорбции воды в канальцах почек.
Аномальное разрастание клеток железы приводит к образованию опухолей переднего или заднего отдела гипофиза и нарушению гормонального баланса. Иногда в область гипофиза прорастают менингиомы – опухоли мозговых оболочек; реже железа поражается метастатическими отсевами злокачественных новообразований других локализаций.
Причины опухолей гипофиза
Достоверные причины развития опухолей гипофиза до конца не изучены, хотя известно, что некоторые виды новообразований могут быть обусловлены генетически.
В число факторов, предрасполагающих к развитию опухолей гипофиза, входят нейроинфекции, хронические синуситы, черепно-мозговые травмы, гормональные изменения (в том числе вследствие длительного применения гормональных препаратов), неблагоприятное воздействие на плод в период беременности.
Классификация опухолей гипофиза
Опухоли гипофиза классифицируются с учетом их размеров, анатомического расположения, эндокринных функций, особенностей микроскопического окрашивания и т. д.
В зависимости от размера новообразования выделяют микроаденомы (менее 10 мм в максимальном диаметре) и макроаденомы (при наибольшем диаметре более 10 мм) гипофиза.
По локализации в железе различают опухоли аденогипофиза и нейрогипофиза. Опухоли гипофиза по топографии относительно турецкого седла и окружающих его структур бывают эндоселлярными (выходящими за границы турецкого седла) и интраселлярными (расположенными в пределах турецкого седла).
С учетом гистологической структуры опухоли гипофиза подразделяются на злокачественные и доброкачественные новообразования (аденомы). Аденомы исходят из железистой ткани передней доли гипофиза (аденогипофиза).
Среди гормонально-активных опухолей гипофиза выделяют:
Соматотропинпродуцирующие аденомы:
- соматотропная аденома
- соматотропинома – опухоль гипофиза, синтезирующая соматотропин - гормон роста;
Пролактинсекретирующие аденомы:
- пролактиновая аденома
- пролактинома – опухоль гипофиза, синтезирующая гормон пролактин;
Адренокортикотропинпродуцирующие аденомы:
- кортикотропная аденома
- кортикотропинома - опухоль гипофиза, секретирующая АКТГ, стимулирующий функцию коры надпочечников;
Тиротропинпродуцирующие аденомы:
- тиротропная аденома
- тиротропинома - опухоль гипофиза, секретирующая тиротропный гормон, стимулирующий функцию щитовидной железы;
Фоллтропинпродуцирующие или лютропинпродуцирующие аденомы (гонадотропные). Эти опухоли гипофиза секретируют гонадотропины, стимулирующие функцию половых желез.
Гормонально-неактивные опухоли гипофиза и пролактиномы встречаются наиболее часто (в 35% случаев соответственно), соматотропинпродуцирующие и АКТГ-продуцирующие аденомы – в10-15% случаев от всех опухолей гипофиза, другие виды опухолей образуются редко.
По особенностям микроскопии различают хромофобные опухоли гипофиза (гормонально-неактивные аденомы), ацидофилиные (пролактиномы, тиротропиномы, соматотропиномы) и базофильные (гонадотропиномы, кортикотропиномы).
Развитие гормонально-активных опухолей гипофиза, продуцирующих один или несколько гормонов, может приводить к развитию центрального гипотиреоза, синдрома Кушинга, акромегалии или гигантизма и т. д. Повреждение гормонопродуцирующих клеткок при росте аденомы может вызывать состояние гипопитуаризма (гипофизарной недостаточности).
У 20% пациентов отмечается бессимптомное течение опухолей гипофиза, которые обнаруживаются лишь при аутопсии. Клинические проявления опухолей гипофиза зависят от гиперсекреции того или иного гормона, размеров и скорости роста аденомы.
Симптомы опухолей гипофиза
По мере увеличения опухоли гипофиза развиваются симптомы со стороны эндокринной и нервной систем.
Соматотропинпродуцирующие аденомы гипофиза приводят к возникновению акромегалии у взрослых пациентов или гигантизма, если они развиваются у детей.
Пролактинсекретирующие аденомы характеризуются медленным ростом, проявляются аменореей, гинекомастией и галактореей. Если такие опухоли гипофиза продуцируют неполноценный пролактин, то клинические проявления могут отсутствовать.
АКТГ-продуцирующие аденомы стимулируют секрецию гормонов коры надпочечников и ведут к развитию гиперкортицизма (болезни Кушинга). Обычно такие аденомы растут медленно.
Тиротропинпродуцирующие аденомы нередко сопровождают течение гипотиреоза (функциональной недостаточности щитовидной железы). Они могут вызывать упорный тиреотоксикоз, чрезвычайно устойчивый к медикаментозному и хирургическому лечению.
Гонадотропные аденомы, синтезирующие половые гормоны, у мужчин приводят к развитию гинекомастии и импотенции, у женщин – к нарушению менструального цикла и маточным кровотечениям.
Увеличение размеров опухоли гипофиза ведет к развитию проявлений со стороны нервной системы. Поскольку гипофиз анатомически соседствует с перекрестом зрительных нервов (хиазмом), то при увеличении размеров аденомы до 2 см в диаметре развиваются зрительные нарушения: сужение полей зрения, отек сосочков зрительного нерва и его атрофия, ведущие к падению зрения, вплоть до слепоты.
Аденомы гипофиза больших размеров вызывают сдавление черепных нервов, сопровождающееся симптомами поражения нервной системы: головные боли; двоение в глазах, птоз, нистагм, ограничение движений глазных яблок; судороги; упорный насморк; деменцию и изменения личности; повышение внутричерепного давления; кровоизлияния в гипофиз с развитием острой сердечно-сосудистой недостаточности. При вовлеченности в процесс гипоталамуса могут наблюдаться эпизоды нарушения сознания.
Злокачественные опухоли гипофиза встречаются крайне редко.
Диагностика опухолей гипофиза
Необходимыми исследованиями при подозрении на опухоль гипофиза являются тщательное офтальмологическое и гормональное обследования, нейровизуализация аденомы.
Исследование мочи и крови на содержание гормонов позволяет установить вид опухоли гипофиза и степень ее активности.
Офтальмологическое обследование включает оценку остроты и полей зрения, позволяющих судить о вовлеченности в процесс зрительных нервов.
Нейровизуализацию опухоли гипофиза позволяет осуществить рентгенография черепа и зоны турецкого седла, компьютерное и магнитно-резонансное исследования головного мозга.
Рентгенологически могут определяться увеличение размеров турецкого седла и эрозия его дна, а также увеличение нижней челюсти и пазух носа, утолщение костей черепа, и расширение межзубных промежутков.
С помощью магнитно-резонансной томографии возможно увидеть опухоли гипофиза диаметром менее 5 мм. Компьютерная томография подтверждает наличие аденомы и ее точные размеры.
Ангиографическое исследование сонной артерии при макроаденомах указывает на ее смещение и позволяет дифференцировать опухоль гипофиза с внутричерепной аневризмой.
В анализе спинномозговой жидкости может определяться повышенный уровень протеинов.
Лечение опухолей гипофиза
Для каждого вида опухолей гипофиза существует специфический, наиболее оптимальный вариант лечения, который подбирается эндокринологом и нейрохирургом. В лечении опухолей гипофиза используются хирургический, лучевой и лекарственный методы.
Наиболее эффективным считается хирургическое удаление опухоли гипофиза. В зависимости от размеров и локализации аденомы проводится либо ее фронтальное удаление через оптический прибор, либо резекция через клиновидную кость черепа. Оперативное удаление опухолей гипофиза дополняется лучевой терапией.
Гормонально-неактивные микроаденомы лечатся с помощью лучевой терапии. Проведение лучевой терапии показано при наличии противопоказаний к оперативному лечению, а также пожилым пациентам.
В послеоперационном периоде проводится гормонозаместительная терапия (кортизоном, тиреоидными или половыми гормонами), при необходимости - коррекция электролитного обмена и инсулинотерапия.
Из лекарственных препаратов используют агонисты дофамина (каберголин, бромокриптин), вызывающие сморщивание пролактин- и АКТГ-секретирующих опухолей гипофиза, а также ципрогептадин, понижающий уровень кортикостероидов у пациентов с синдромом Кушинга.
Альтернативным методом лечения опухолей гипофиза является замораживание участка ткани железы при помощи зонда, введенного через клиновидную кость.
Прогноз при опухолях гипофиза
Дальнейший прогноз при опухолях гипофиза во многом определяется размерами аденом, возможностью их радикального удаления и гормональной активностью.
У пациентов с пролактиномами и соматотропиномами полное восстановление гормональной функции наблюдается в четверти случаев, при адренокортикотропинпродуцирующих аденомах - в 70-80% случаев.
Макроаденомы гипофиза размером более 2 см полностью удалить невозможно, поэтому возможны их рецидивы в течение 5-летнего срока после операции.
Читайте также:

