Генетическая предрасположенность рака предстательной железы
Цена исследования 35 000 руб.
Срок выполнения
35 раб.дн.
Записаться на исследование
+7 (495) 150-66-47
Исследуем: 20 генов
Для кого это исследование
Назначение этой панели исследований показано следующим группам обследуемых:
Здоровым людям с имеющимися случаями онкологических заболеваний в семье (например, при наличии трёх и более случаев рака предстательной железы и/или рака молочной железы, толстой кишки, яичников и поджелудочной железы в семье в одной линии);
Здоровым людям без семейного анамнеза онкологических заболеваний исследование может дать важную информацию о генетической предрасположенности к онкологическим поражениям этого органа. Такая вероятность существует, поскольку человек может быть носителем новых мутаций, которых нет у родителей, и кроме того, наследственный рак может наследоваться от здоровых носителей мутаций. При этом в семье может не быть случаев рака, но у данного конкретного пациента будет присутствовать новая комбинация онкогенных мутаций, унаследованных от обоих родителей-носителей, вызывающая рак.
Пациентам с уже диагностированной опухолью предстательной железы в случае подозрения на наследственную природу заболевания, например, в случае относительно раннего возраста начала развития заболевания, в случае онкологически отягощённого семейного анамнеза, при определённых типах опухолей (по данным исследований, у 8-12% пациентов с метастатическим раком предстательной железы выявляются герминальные мутации в генах, ассоциированных с повышенным риском развития этого рака), при наличии нескольких первичных опухолей разной локализации у одного пациента либо билатерального рака предстательной железы.
У этой группы пациентов выявление мутаций позволяет уточнить диагноз и прогноз, а также выбрать правильную стратегию лечения (имеются, в частности, достаточно успешные клинические испытания и кейс-репорты по эффективности олапариба для лечения пациентов с раком предстательной железы с мутациями в генах BRCA1/2 или TM).
Конечная цель исследования – полная информация о мутациях, связанных с наследственными формами рака предстательной железы, интерпретированная специалистом с точки зрения клинической значимости.
Какие гены мы смотрим
Гены, включенные в панель (на основе рекомендаций Национальной онкологической сети США, NCCN):
ABRAXAS1 (FAM175A), ATM, ATR, BRCA1, BRCA2, BRIP1, CHEK2, EPCAM, GEN1, HOXB13, MLH1, MRE11, MSH2, MSH6, NBN, PALB2, PMS2, RAD51C, RAD51D, TP53
Как сдать тест?
Материал для исследования — венозная кровь, взятая в специальную пробирку.
Кровь можно сдать в лаборатории Genetico либо в других лабораториях по месту жительства. Наша отлаженная логистическая служба доставит биоматериал из любой точки России до места проведения исследования в лаборатории Genetico без дополнительных расходов для пациента.
Метод исследования — высокопроизводительное секвенирование ДНК нового поколения (next generation sequencing, NGS). Секвенирование, то есть определение последовательности нуклеотидов ДНК, относится к современным высокоточным методам молекулярного анализа.
Срок выполнения
Мы проводим полное исследование и формируем заключение в течение 35 рабочих дней.
Сроки могут показаться значительными, но это не так. Это самая высокая скорость на рынке для подобных исследований такого объёма, проводимых с использованием технологии NGS.
Указанное время требуется для выполнения многоступенчатого высокотехнологичного исследования, включающего в себя большое количество лабораторных этапов и промежуточного контроля качества. В результате получается большой массив генетических данных, требующих отдельного анализа и интерпретации с помощью методов биоинформатики, на что тоже необходимо время.
Как выглядит заключение
Формат итогового заключения содержит описание результатов исследования и даёт следующую информацию:
- у пациентов с диагностированным раком — список патогенных, вероятно патогенных мутаций и мутаций с неизвестным клиническим значением, их описание и интерпретация с точки зрения клинической значимости.
- у здорового человека — список патогенных и вероятно патогенных мутаций, их описание и интерпретация с точки зрения клинического потенциала. Мутации с неизвестным клиническим значением в заключение не выносятся в связи с серьёзными сложностями их дальнейшей клинической интерпретации у здорового человека и низкой информативностью для дальнейших диагностических мероприятий.
Заключение отправляется заказчику по электронной почте. Если есть необходимость получить заключение в бумажном варианте, мы отправим его в любой регион почтой России без дополнительных расходов для заказчика.
Что делать, если мутации выявлены?
После выполнения исследования, анализа данных и оформления заключения вы получите информацию о наличии мутаций, ассоциированных с наследственными формами рака предстательной железы и наследственными опухолевыми синдромами, ассоциированными с повышенным риском развития этого типа рака. В случае обнаружения мутаций возможны следующие варианты дальнейших действий:
- обсуждение выявленных мутаций с врачом-генетиком с целью клинической интерпретации полученных результатов;
- обсуждение с врачом-онкологом плана профилактических (например, скрининг на предмет рака предстательной железы начиная с 45 лет) и превентивных мероприятий у здорового человека;
- обследование ближайших кровных родственников на наличие мутаций для выявления носительства методом секвенирования по Сэнгеру;
обсуждение с врачом-генетиком возможностей планирования беременности для рождения здорового потомства (пренатальная диагностика, ПГД) у пациентов детородного возраста;
уточнение диагноза и прогноза у пациентов с диагностированным раком;
выбор стратегии и тактики лечения у пациентов с диагностированным раком, в том числе обсуждение возможности назначения таргетной терапии.
При этом в случае выявления мутаций у здорового человека появится возможность ранней диагностики развития опухолевого процесса, обусловленного наличием единичной мутации или парных мутаций, а у пациента с диагностированным раком в случае выявления мутаций может быть больше возможностей для выработки алгоритма эффективного лечения.
Стоимость исследования
Нам удалось достичь минимальной цены для исследования такого уровня и такого охвата. Стоимость панели составляет 35 000 рублей. При этом все возможные логистические издержки (доставку биоматериала из других городов, отправку заключений) мы берём на себя без дополнительных затрат со стороны обследуемого. Выгрузка сырых данных в указанную стоимость не входит.
Рекомендации
Это максимально полная панель в России, охватывающая наибольшее количество генов (всего – 207), мутации в которых наблюдаются при различных наследуемых злокачественных опухолях.
Рак часто наблюдается у членов одной семьи, объективно подтверждена наследственная природа некоторых злокачественных опухолей. Есть точка зрения, что наследственная предрасположенность — самая вероятная причина всех онкологических заболеваний, и только дело времени, чтобы наука точно установила, мутация какого гена за какой конкретный рак отвечает. Но уже сейчас наследственную передачу рака можно прервать.
Если у человека возникло онкологическое заболевание, очень важно выяснить, есть ли в его роду другие случаи злокачественных новообразований. Семьям, в которых имеется более одного такого случая, нужно пройти консультацию врача-генетика, чтобы понять, есть ли в семейной истории основания для подозрений на наследственный характер патологии. Особенно настораживающим признаком будет онкологическое заболевание в нескольких поколениях семьи. Одним из основных методов работы врача-генетика является составление родословных. Другая важная часть медико-генетической консультации — осмотр и опрос пациента: наследственные заболевания нередко проявляются специфическими признаками.
Принципиальным отличием наследственного рака является возможность его прогнозировать путем выявления патогенных мутаций. На первом этапе семьям, в которых имеется более одного случая развития рака, рекомендуется пройти консультацию врача-генетика, по результатам которого можно будет понять, есть ли в семейной истории основания для подозрения на наследственный характер патологии.
Если в процессе консультации возникают подозрения на наследственную природу заболевания, то следующий этап — целенаправленное генетическое тестирование, поиск мутаций, которые могут вызывать конкретное заболевание. Одни исследования позволяют обнаружить изменения в самом гене, другие — в белке, который кодируется измененным геном. Один ген может претерпеть до 300 мутаций.
В последние годы найдены мутации, ответственные за возникновение и развитие рака молочной железы, яичников, толстой кишки и др. Цель генетического тестирования, или скрининга,— выявить риск возникновения заболевания до появления симптомов. Это дает возможность в одних случаях провести своевременное лечение, в других — рекомендовать меры, позволяющие избежать передачи наследственного заболевания потомству. Мутации генов найдены для нескольких видов рака, тесты на некоторые из них уже используют в клинике — например, тесты на рак груди и кишечника.
От предков или не от предков
Все онкологические заболевания имеют генетическую природу, поскольку при раке гены, отвечающие за правильное деление клетки, повреждены. Но в одних случаях имеют место наследственные мутации, а в других — приобретенные. Результатом повреждения (мутации) гена во всех случаях является бесконтрольное неограниченное деление клеток, что и является сутью ракового процесса.
Несмотря на то что онкологические заболевания имеют генетическую природу, только 10–15% из них передаются по наследству. Почему важно знать, наследственный или ненаследственный рак? Потому что если установлена его наследственная природа, то есть выявлена мутация, вызвавшая его, то известен прогноз и понятна тактика в отношении самого больного и его родственников. Особенно отчетливо наследование мутации прослеживается в случаях так называемого семейного рака молочной железы и яичников, при семейном аденоматозном полипозе и различных опухолевых синдромах (Линча — рак толстой кишки, Ли-Фраумени — разнообразные саркомы и др.). Многие люди, сами будучи здоровыми, являются носителями мутаций, приводящих к наследственным заболеваниям. Если носители одной и той же мутации — оба родителя, заболевание становится неизбежным. Генетическое тестирование позволяет это выявить.
Следует подчеркнуть, что наличие мутации не означает заболевания. Мутация может сидеть в гене много лет до того, как начнет развиваться опухоль. Но, зная про мутацию, врачи могут назначить рациональный режим обследования и профилактического лечения.
Например, у женщин—носительниц гена BRCA1 в 95% случаев в течение жизни разовьется рак груди и в 65% — рак яичников, причем часто рак развивается в молодом возрасте, до 50 лет. Это означает, что носительница должна все время находиться под наблюдением, а в некоторых случаях целесообразно ставить вопрос о профилактическом удалении груди и (или) яичников. У всех на слуху история Анджелины Джоли, которая настояла на удалении обеих молочных желез, поскольку у нее обнаружили мутацию гена BRCA1.
Специалисты знают результаты исследования ткани удаленных молочных желез у 54 шведских женщин—носительниц этого гена в возрасте до 51 года. Ни у одной из них обследование не показывало опухоли груди до операции, но гистологическое изучение удаленной ткани выявило наличие раковых клеток у пяти (10%!) из них.
К профилактической хирургии прибегают и при семейном аденоматозном полипозе, при котором вероятность развития рака толстой кишки после 40 лет достигает 100%, и при других онкологических заболеваниях, если установлена онкогенная мутация.
Понятно, что женщины с отрицательным результатом теста на мутации генов BRCA1 и BRCA2 не застрахованы от спорадического рака груди и яичников. Однако вероятность его возникновения несопоставимо ниже, чем у женщин с положительным тестом.
Женщине следует заподозрить у себя предрасположенность к наследственному раку груди, пройти консультацию врача и генетика и генетическое тестирование, если в семье:
— было более одного случая рака груди или яичников по женской линии (у матери, бабушки, тетки, сестер и т. д.);
— заболевание было диагностировано в молодом возрасте (до наступления климакса);
— были случаи рака груди у мужчины;
— были больные c множественными опухолями (например, у одного человека — рак груди, толстой кишки, матки, рак поджелудочной железы и т. д.);
— были случаи двустороннего рака обеих молочных желез или обоих яичников.
Тестирование и его последствия
Генетическое тестирование имеет несколько преимуществ. Отрицательный результат может принести человеку облегчение, избавить от страха ожидания тяжелой болезни, от которой, возможно, погибли его близкие, а также от регулярных обследований, которые должны быть обязательны в семьях с высоким онкологическим риском. Положительный результат дает человеку возможность принимать обдуманные решения о будущем своем и своего потомства.
Сегодня возможна профилактика наследственного рака, то есть возможность не передать от родителей потомству ген, несущий опасную мутацию. Метод, который позволяет это сделать, называется преимплантационная генетическая диагностика (ПГД). Он заключается в следующем: для пары выполняют ЭКО, проводят генетическую диагностику полученных эмбрионов и переносят в матку женщины только те из них, в которых нет онкогенных мутаций. У родившегося ребенка их не будет, а значит, не будет и наследственного рака.
Открытое письмо Анджелины Джоли, New York Times, 14 мая 2013 года
ПГД проводится не на всем эмбрионе, а на нескольких клетках, которые получают путем его биопсии. Доказано, что биопсия не оказывает влияния на здоровье и состояние ребенка. Другими словами, ПГД не снижает частоту наступления беременности и безопасна для будущего ребенка.
Кроме мутаций, отвечающих за развитие рака груди и яичников, установлены мутации, несущие предрасположенность к меланоме, раку желудка, матки, предстательной, поджелудочной и щитовидной железы, толстой и прямой кишки. Если мутация определена и в семье есть люди, которые хотят иметь ребенка, важно, чтобы они знали о возможности предотвратить передачу следующим поколениям этой мутации и связанного с ней рака с помощью ЭКО и ПГД.

- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
Когда родственник заболевает раком, нам страшно. В какой-то мере страшно и за свое здоровье – передается ли рак по наследству? Прежде чем делать поспешные выводы и впадать в панику, давайте разберемся с этим вопросом.
По своей сути, рак – генетическое заболевание, которое возникает вследствие поломки генома клетки. Раз за разом в клетке происходит последовательное накопление мутаций, и она постепенно приобретает свойства злокачественной – малигнизируется.

Генов, которые участвуют в поломке, несколько, и перестают работать они не одновременно.
- Гены, кодирующие системы роста и деления, называются прото-онкогенами. При их поломке клетка начинает бесконечно делиться и расти.
- Есть гены-супрессоры опухолей, отвечающие за систему восприятия сигналов от других клеток и тормозящие рост и деление. Они могут сдерживать рост клетки, а при их поломке этот механизм выключается.
- И, наконец, есть гены репарации ДНК, кодирующие белки, которые чинят ДНК. Их поломка способствуют очень быстрому накоплению мутаций в геноме клетки.
Генетическая предрасположенность к онкологии
Существует два сценария возникновения мутаций, вызывающих онкологические заболевания: ненаследственный и наследственный. Ненаследственные мутации появляются в изначально здоровых клетках. Они возникают под воздействием внешних канцерогенных факторов, например, курения или ультрафиолетового излучения. В основном рак развивается у людей в зрелом возрасте: процесс возникновения и накопления мутаций может занимать не один десяток лет.
Однако, в 5-10% случаев предопределяющую роль играет наследственность. Происходит это в том случае, когда одна из онкогенных мутаций появилась в половой клетке, которой посчастливилось стать человеком. При этом каждая из примерно 40*1012 клеток организма этого человека также будет содержать начальную мутацию. Следовательно, каждой клетке нужно будет накопить меньше мутаций, чтобы стать раковой.
Повышенный риск развития рака передается из поколения в поколение и называется наследственным опухолевым синдромом. Встречается данный синдром довольно часто – примерно у 2-4% населения.
Несмотря на то, что основную массу онкологических заболеваний вызывают случайные мутации, наследственному фактору также необходимо уделять серьезное внимание. Зная об имеющихся унаследованных мутациях, можно предотвратить развитие конкретного заболевания.
Предрасположенность к раку наследуется как Менделевский доминантный признак, иными словами, как обычный ген с различной частотой возникновения. При этом вероятность возникновения в раннем возрасте у наследственных форм выше, чем у спорадических.
Распространенные генетические исследования
Коротко расскажем вам об основных видах генетических исследований, которые показаны людям из группы риска. Все эти исследования можно провести в нашей клинике.
Определение мутации в гене BRCA
В 2013 году благодаря Анджелине Джоли весь мир активно обсуждал наследственный рак молочной железы и яичников, о мутациях в генах BRCA1 и BRCA2 теперь знают даже неспециалисты. Из-за мутаций теряются функции белков, кодируемых этими генами. В результате основной механизм репарации (восстановления) двунитевых разрывов молекулы ДНК нарушается, и возникает состояние геномной нестабильности – высокой частоты мутаций в геноме клеточной линии. Нестабильность генома является центральным фактором канцерогенеза.
Учеными описано более тысячи различных мутаций в этих генах, многие из которых (но не все) связаны с повышенным риском возникновения онкологического заболевания.
У женщин с нарушениями в BRCA1/2 риск заболеть раком молочной железы составляет 45-87%, в то время как средняя вероятность этого заболевания – всего 5,6%. Растет вероятность развития злокачественных опухолей и в других органах: яичниках (с 1 до 35%), поджелудочной, а у мужчин – и в предстательной железе.
Генетическая предрасположенность к наследственному неполипозному колоректальному раку (синдром Линча)
Колоректальный рак – одно из самых распространенных онкологических заболеваний в мире. Около 10% населения имеет генетическую предрасположенность к нему.
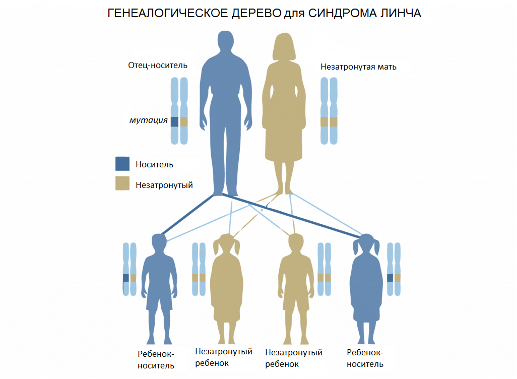
Генетический тест на синдром Линча, также известного как наследственный неполипозный колоректальный рак (НПКР), определяет заболевание с точностью 97%. Синдром Линча – наследственное заболевание, в результате которого злокачественная опухоль поражает стенки толстого кишечника. Считается, что около 5% всех случаев колоректального рака связаны с этим синдромом.
Определение мутации в гене BRaf
При наличии меланомы, опухолей щитовидной или предстательной железы, опухоли яичников или кишечника рекомендуется (а в некоторых случаях обязательно) проведение анализа на BRaf мутацию. Это исследование поможет выбрать необходимую стратегию лечения опухоли.
BRAF – это онкоген, который отвечает за кодировку белка, располагающегося в сигнальном пути Ras-Raf-MEK-MARK. Этот путь, в норме, регулирует деление клеток под контролем фактора роста и различных гормонов. Мутация в онкогене BRaf приводит к избыточному неконтролируемому разрастанию и устойчивости к апоптозу (запрограммированной смерти). Результатом является в несколько раз ускоренное размножение клеток и рост новообразования. По показаниям данного исследования специалист делает заключение о возможности использования ингибиторов BRaf, которые продемонстрировали значительное преимущество по сравнению со стандартной химиотерапией.

Методика проведения анализа
Любой генетический анализ – сложная многоэтапная процедура.
Генетический материал для анализа берут из клеток, как правило, из клеток крови. Но в последнее время лаборатории переходят на неинвазивные методы и иногда выделяют ДНК из слюны. Выделенный материал подвергается секвенции – определению последовательности мономеров при помощи химических анализаторов и реакций. Эта последовательность и является генетическим кодом. Полученный код сравнивают с эталонным и определяют, какие участки относятся к тем или иным генам. На основании их наличия, отсутствия или мутации делают заключение о результатах теста.
Сегодня в лабораториях множество методов генетического анализа, каждый из них хорош в тех или иных ситуациях:
За счет большого количества химических реактивов процедуры генетических исследований достаточно финансово затратные.. Мы стараемся устанавливать оптимальную стоимость всех процедур, поэтому цена на такие исследования у нас начинается от 4 800 рублей.
Группы риска
В группы риска по наследственному раку попадают люди, у которых наблюдается хотя бы один из перечисленных факторов:
- Несколько случаев одного вида рака в семье
(например, рак желудка у деда, отца и сына); - Заболевания в раннем для данного показания возрасте
(например, колоректальный рак у пациента моложе 50 лет); - Единичный случай определенного вида рака
(например, рак яичников, или трижды негативный рак молочной железы); - Рак в каждом из парных органов
(например, рак левой и правой почки); - Больше одного типа рака у родственника
(например, сочетание рака молочной железы и рака яичников); - Рак, нехарактерный для пола пациента
(например, рак молочной железы у мужчины).
Если для человека и его семьи характерен хотя бы один фактор из списка, то следует получить консультацию у врача-генетика. Он определит, есть ли медицинские показания для того, чтобы сдавать генетический тест.
Чтобы обнаружить рак на ранней стадии, носителям наследственного опухолевого синдрома следует проходить тщательный скрининг на онкологические заболевания. В некоторых случаях риск развития рака можно существенно снизить с помощью превентивных операций и лекарственной профилактики.
При проведении теста опухоль анализируется, составляется индивидуальный молекулярный паспорт. В комплексе с анализом крови, в зависимости от требуемого теста, проводится комбинацирование различных анализов на геном и белок. В результате данного теста появляется возможность назначения таргетной терапии, эффективной для каждого типа имеющейся опухоли.
Профилактика
Бытует мнение, что для определения предрасположенности к раку можно сделать простой анализ на наличие онкомаркеров – специфических веществ, которые могут быть продуктами жизнедеятельности опухоли.
Повышение показателя может зависеть от целого ряда причин, совершенно не связанных с онкологическими заболеваниями. В то же время, есть примеры людей с онкологическими заболеваниями, у которых значения онкомаркера оставались в пределах нормы. Специалисты используют онкомаркеры как метод для отслеживания протекания уже обнаруженного заболевания, результаты которого нужно перепроверять.
Для выявления вероятности генетической наследственности в первую очередь, если вы входите в группу риска, нужно обратиться за консультацией к врачу-онкологу. Специалист, исходя из вашего анамнеза, сделает вывод о необходимости проведения тех или иных исследований.
Важно понимать, что решение о проведении какого-либо теста должен принять именно врач. Самолечение в онкологии неприемлемо. Неправильно интерпретированные результаты не только могут вызвать преждевременную панику – вы попросту можете упустить наличие развивающегося онкологического заболевания. Выявление рака на ранней стадии при наличии вовремя поставленного правильного лечения дает шанс на выздоровление.
Стоит ли паниковать?
Рак – неизбежный спутник долгоживущего организма: вероятность накопления соматической клеткой критического числа мутаций прямо пропорциональна времени жизни. То, что рак – генетическое заболевание, не значит, что оно наследственное. Он передается в 2-4% случаев. Если у вашего родственника обнаружили онкологическое заболевание – не впадайте в панику, этим вы навредите и себе, и ему. Обратитесь к врачу-онкологу. Пройдите исследования, которые он вам назначит. Лучше, если это будет специалист, который следит за прогрессом в области диагностики и лечения рака и в курсе всего, что вы сами только что узнали. Следуйте его рекомендациям и не болейте.
Рак предстательной железы, профилактика и ранняя диагостика

Рак предстательной железы, профилактика и ранняя диагостика
Рак предстательной железы – одно из самых распространенных раковых заболеваний у мужчин. Хотя развивается он медленно, тысячи мужчин умирают от этой болезни каждый год. В среднем рак предстательной железы может быть диагностирован у каждого шестого мужчины, причем с возрастом вероятность эта только увеличивается.
Что такое рак предстательной железы и где он возникает
Простата, или предстательная железа, располагается в мужском организме под мочевым пузырем. Она граничит с прямой кишкой (что позволяет врачу при осмотре пальпировать ее заднюю поверхность). Через предстательную железу проходит начальная часть мочеиспускательного канала, куда открываются выводные протоки железы. Кровь к простате и мочевому пузырю подает нижняя мочепузырная артерия, которая отходит от внутренней подвздошной артерии. По обоим сторонам предстательной железы располагается по нейрососудистому пучку, части нижнего подчревного (тазового) сплетения. Предстательное сплетение имеет важное значение для эректильной функции.
Возникает рак простаты, когда клетки предстательной железы начинают делиться с большей скоростью, чем требуется для восполнения числа клеток погибших. Это приводит к неконтролируемому росту опухоли. После перерождения дальнейшие мутации генов могут привести к прогрессированию опухоли и возникновению метастаз. Большинство раков (95%) предстательной железы относятся к аденокарциноме – опухоли, которая возникает из железистого эпителия. В гораздо более редких случаях (всего 4% от общего числа опухолей) рак простаты возникает из уротелия – ткани, которая выстилает мочеиспускательный канал. 1% от диагностированных опухолей составляет плоскоклеточная карционома. Реже всего (насчитывается буквально несколько эпизодов) рак простаты развивается из нейроэндокринных стволовых клеток, которые присутствуют в предстательной железе.
Более всего появлению рака подвержена периферическая зона предстательной железы – там рак возникает 70% случаев. 15-20% относятся к центральной зоне, а 10-15% — к переходной. От предстательной железы рак может распространиться в эякуляторные протоки, семенные пузырьки, перейти на шейку мочевого пузыря и проникать через простатическую капсулу в сосуды.
Время удвоения (когда масса клеток, составляющих раковую опухоль, увеличивается в размере в два раза) у рака простаты превышает четыре года; в редких случаях этот срок сокращается до двух лет. Чем больше опухоль, тем меньше времени требуется ей для удвоения своей массы, тем агрессивнее рак, тем более высокий показатель у него по шкале Глисона.
Причины возникновения рака предстательной железы
В пользу генетической предрасположенности к раку предстательной железы говорит тот факт, что частота его возникновения варьируется в разных местах земного шара, причем верхний показатель выше нижнего более чем в 50 раз! Чаще всего заболевают жители Северной Америки, Австралии и Северной и Центральной Европы, а реже всего – население Юго-Восточной Азии и Северной Африки. Однако те из жителей стран Азии, которые мигрировали в другие страны, болеют чаще, чем их оставшиеся на исторической родине собратья. Это свидетельствует о важности факторов окружающей среды, особенно диеты.
Выходцы из Африки южнее Сахары чаще страдают от рака простаты, чем белые и азиаты, даже при условии одинакового образа жизни. Хотя уровень смертности от рака простаты продолжает снижаться по всему миру, темнокожие мужчины умирают от него в среднем в два раза чаще. Возможно, правда, что свою роль тут играет разница в доступе к квалифицированной медицинской помощи, доходе, образовании и медицинском страховании.
Семейная предрасположенность тоже играет свою роль; недавние исследования показали, что гены, располагающие к возникновению рака предстательной железы, передаются по наследству. Наследственность может отвечать примерно за 5-10% случаев возникновения рака простаты; у мужчин, в семейной истории которых были случаи рака предстательной железы, рак может проявиться лет на 6-7 раньше и с большей вероятностью. Некоторые генные мутации также способны повышать риск развития рака простаты. Также появлению рака предстательной железы способствуют некоторые наследственные болезни, например, синдром Линча.
Интересно, что чаще всего рак предстательной железы обнаруживается у мужчин, умерших по другим причинам; в возрасте 80 лет соотношение диагностированного рака простаты и рака скрытого составляет 20% против 80%. Соотношение это верно для всех стран и всех народов.
Определенную роль в развитии рака предстательной железы могут играть употребляемые в пищу продукты. Хотя сама по себе диета не является панацеей от рака простаты (он вызывается целым комплексом причин, не все из которых изучены до сих пор), однако в некоторых случаях определенный вид питания может снизить вероятность его возникновения. Или, в обратном случае, увеличить этот шанс.
Одна из связей, которая выявлена между возникновением рака простаты и питанием – это количество употребляемого жира. Больше всего жирную еду любят мужчины, живущие в Западной Европе и Северной Америке, соответственно, риск развития рака простаты выше всего именно в этих регионах. Меньше всего едят жирного жители Юго-Восточной Азии, и страдают от рака простаты они тоже меньше. Интересно, что с распространением западной системы питания в Японии (где традиционно употребляли в пищу мало жирного) увеличилось и число заболевших раком простаты, причем в агрессивной его форме.
Также установлена корреляция между употреблением в пищу красного мяса и возникновения рака простаты. Согласно исследованиям, рак простаты у мужчин, предпочитающие есть мясо животных, развивается в 2,64 раза чаще. Риск еще выше, если мужчина любит мясо хорошо прожаренным или регулярно употребляет в пищу мясопродукты вроде сосисок, бекона, грудинки и колбасы. Правда, некоторые ученые считают, что избыток мяса, как и избыток жиров, скорее служат маркером общего нездорового образа жизни, а не их опасности как таковых.
Тем не менее, если мужчина хочет сократить вероятность возникновения у него рака простаты, желательно употреблять в пищу меньше жареного, жирного и красного мяса. Для примера, люди, привыкшие питаться по средиземноморскому типу (обилие фруктов, овощей, злаков, употребление оливкового масла, а в качестве источников животного белка использование мяса птицы и морепродуктов) страдают от рака простаты в меньшей степени.
По результатам множества исследований выявлено, что тучные люди более предрасположены к развитию рака простаты, чем их худые собратья, и рак в таких случаях бывает более агрессивным. Правда, причина тут может быть в том, что у тучных людей сложнее диагностировать рак простаты на ранних стадиях. У больших людей – большая предстательная железа, тем самым врачу труднее определить при помощи биопсии, есть ли в ней раковые клетки. Также увеличенная простата выделяет повышенное количество антигена, ассоциируемого с раком простаты, тем самым затрудняя врачу постановку диагноза.
Считается, что на возникновение рака предстательной железы влияют гормоны. Косвенное доказательство этой теории – что у мужчин, по каким-то причинам перенесших кастрацию, аденокарциномы предстательной железы не бывает. Согласно исследованиям, риск возникновения опухоли увеличивает повышенный уровень лютеинизирующего гомона и соотношение тестостерон/дигидротестостерон.
Во многих случаях причиной возникновения плоскоклеточного рака предстательной железы является лучевая или гормональная терапия.
Чем старше мужчина, тем больше вероятность развития у него рака предстательной железы. Случаи этого заболевания редко диагностируются у мужчин моложе 40 лет. У мужчин старше 55 лет чаще диагностируют метастатические формы рака простаты.
Симптомы рака предстательной железы
Сейчас рак предстательной железы диагностируется на ранних стадиях, когда симптомы рака отсутствуют. Произошло это благодаря открытию диагностического значения простатического специфического антигена (ПСА), способствовавшего существенному сокращению смертности от рака простаты. Диагноз ставится на основании уровня содержания в сыворотке крови ПСА, по результатам рентгенологических исследований или при пальцевом исследовании прямой кишки. Кроме того, рак простаты можно обнаружить путем анализа удаленной ткани при лечении доброкачественной гиперплазии предстательной железы.
До 80-х годов прошлого века, когда о диагностической важности ПСА сведений еще не было, симптомы включали в себя жалобы на затрудненное мочеиспускание, боли в спине, кровь в моче.
При прогрессирующем заболевании симптомы уже другие:
Потеря веса и аппетита.
Боли в костях, с патологическими переломами или без них (рак предстательной железы вообще склонен к образованию метастаз в костной ткани; такие боли – один из симптомов распространения опухоли).
Очаговый неврологический дефицит, возникающий при сдавливании опухолями спинного мозга.
Боли в пояснице, отеки из-за обструкции венозных и лимфатических сосудов (если рак простаты пошел путем узлового метастазирования).
Уремия, вызванная обструкцией мочеточника из-за увеличения простаты.
Постановка диагноза при раке предстательной железы
Первым делом врач проводит пальцевое исследование прямой кишки – когда через задний проход указательный палец врача в перчатке вводится в прямую кишку. Благодаря расположению простаты ее заднюю часть можно легко прощупать через стенку прямой кишки. При обследовании важно обращать внимание на ассиметрию и разницу в плотности ткани. Правда, при пальцевом исследовании сложно отличить доброкачественные образования на предстательной железе от рака – на ощупь кисты или камни не отличаются от раковых опухолей.
Вторая главная компонента постановки диагноза при подозрении на рак предстательной железы — анализ сыворотки крови на содержание простатического специфического антигена (ПСА). Норма его содержания в сыворотке крови зависит от возраста – от 2,5 нг/мл у пациентов от 40 до 49 лет до 6,5 нг/мл у пожилых мужчин старше 70 лет. Если содержание ПСА достигло значения выше 10 нг/мл, значит, требуется провести биопсию.
Биопсия предстательной железы осуществляется при помощи специального устройства – пистолета и игл, а проводят ее под контролем трансректального ультразвукового исследования (ТРУЗИ). Игла проникает в простату через стенку прямой кишки (поэтому перед биопсией пациенту придется подготовиться – принять слабительное и сделать очистительную клизму). Ткань берут не только из подозрительных участков, но и по всей поверхности простаты (вплоть до 24 точек). К сожалению, при биопсии часто возникают ложноотрицательные результаты, поэтому для точного определения рака простаты может потребоваться несколько биопсий. При биопсии также возможно возникновение осложнений: пациент может испытывать боль, у него повышается температура, в крови могут быть обнаружены следы крови и (в редких случаях) дело может дойти до сепсиса. Риск осложнений при повторных биопсиях увеличивается.
При прогрессирующем заболевании полезно исследовать кровь на креатинин и ферменты печени. Также больному потребуется сделать анализ мочи, чтобы определить, есть ли в ней кровь или какая-либо инфекция. Эти данные следует учитывать при планировании лечения рака простаты.
Компьютерная томография применяется, только если у рака простаты высокий риск возникновения метастаз в лимфатических узлах.
Как правило, при проведении всех исследований постановка диагноза не представляет для врача трудности – рак простаты сложно спутать с чем-нибудь другим.
Прогноз при раке простаты
Как правило, чем раньше выявлен рак простаты, тем проще лечение и тем благоприятнее исход. При условии постановки правильного диагноза и квалифицированном лечении трудоспособность мужчины восстанавливается на все 100%. К сожалению, верно и обратное – чем позже выявлен рак простаты, тем вероятнее летальный исход.
Прогноз при раке простаты зависит от следующих факторов:
Уровень простатического специфического антигена.
Уровень по шкале Глисона. Если опухоль определяется по шкале как 4 или 5 уровень (низкодифференцированные формы рака), она более агрессивна, но в то же время лучше поддается лечению химиотерапией и лучевой терапии. Высокодифференцированные опухоли 1 и 2 уровней, хотя и менее склонные к образованию метастаз, реагируют на лечение хуже.
Процент содержания раковых клеток при биопсии и размер опухоли.
Распространение опухоли и наличие метастаз. Несмотря на то что случаи заболевания метастатическим раком простаты сокращаются из года в год (с 20% в 70-х годах до 3,4% в 90-х), риск развития рака в других органах и тканях у мужчин остается высоким.
Возраст пациента. Чем пациент старше, тем сложнее лечение и более неблагоприятен прогноз.
Тип анестезии. Согласно исследованиям, прогноз при раке простаты может зависеть даже от применяемой во время операции анестезии. Результаты исследования показали, что уровень смертности у мужчин, перенесших операцию с общей анестезией, был на 30% выше, чем у мужчин, при обезболивании которых использовались щадящие методики без применения опиодных препаратов.
Лечение рака простаты
При назначении лечения врач учитывает как степень тяжести рака простаты, так возможные риски для пациента, качество его жизни и вероятный прогноз заболевания. Как правило, чем ранее диагностирован рак простаты, тем проще лечение.
Хирургическое удаление простаты (радикальная простатэктомия)
Операционное лечение показано при локализованной форме рака при отсутствии метастаз; как правило, его назначают более молодым пациентам. При простатэктомии удаляется вся железа целиком вместе с семенными пузырьками. Однако даже радикальная простатэктомия не является гарантией долгой жизни. Согласно исследованиям, за 15 лет после операции умерло 7% от пациентов – в основном от плоскоклеточного рака семенных пузырьков.
Облучению может подвергаться как сама простата, так и расположенные поблизости от нее лимфатические узлы. Существует несколько разновидностей лучевой терапии – дистанционная, адъюрвантная, сочетание дистанционной терапии и внутритканевой имплантации радиоактивных препаратов (брахитерапия) и так далее; врач поможет подобрать наиболее подходящий больному способ лечения рака простаты. Осложнения при лучевой терапии могут включать в себя следующее: ректальное кровотечение, диарею, недержание мочи, кровь в моче и эректильную дисфункцию. Также лучевая терапия рака простаты может несколько увеличить вероятность возникновения рака прямой кишки и рака мочевого пузыря.
При этом способе лечения опухоль подвергается воздействию мощного пучка ультразвуковых волн. Часто ультразвуковую абляцию используют при лечении рецидивов, возникших после удаления простаты хирургическим путем или методом лучевой терапии.
Лечение рака простаты гормонами – один из самых редких способов, обычно используется, если рак повторно возник после удаления простаты или если пациент стар и другие способы лечения применить невозможно. Гормональное лечение при раке простаты заключается в введении в организм пациента веществ, вызывающих снижение уровня мужских половых гормонов. Минусы такого рода терапии – снижение либидо и потенции, возможное набухание молочных желез и так далее; правда, возникают они достаточно редко.
К сожалению, все варианты лечения опасны возникновением побочных эффектов. Если рак простаты обнаружен на ранней стадии и мужчину не беспокоят симптомы, врач может предложить ему придерживаться выжидательной тактики – когда вмешательства в организм пациента не происходит до тех пор, пока опухоль не окажется под угрозой распространения. При этом необходимо тщательно следить за состоянием здоровья больного, симтомами и поведением опухоли.
В последнее время появились новые методы лечения рака простаты – например, криотерапия (когда пораженные ткани простаты подвергаются воздействию низких температур и разрушаются) и метод TOOKAD (когда на опухоль, обработанную специальным препаратом, воздействуют лазером). Эти операции по сравнению с традиционными гораздо менее травматичны, риск возникновения осложнений у них меньше, однако насколько они эффективны в долгосрочном периоде, пока неизвестно.
Лечение на поздних стадиях заболевания
В некоторых случаях рак предстательной железы диагностируется на поздних стадиях, когда он уже начал давать метастазы. Вылечить его невозможно, остается только по мере сил купировать симптомы (например, облегчить боль), по мере возможности пытаться замедлить прогрессирование заболевания и тем самым продлить жизнь больного.
Обычно рак простаты прогрессирует очень медленно; порой человек с ним живет десятилетиями, не испытывая неудобств и не нуждаясь в лечении. Тем не менее, сам факт заболевания раком (даже если симптомы его отсутствуют) влияет на качество жизни прежде всего по психологическим причинам. У человека развиваются тревожные состояния, может начаться депрессия. Помочь тут может поддержка семьи, родственников, друзей, общение с другими заболевшими раком простаты.
Профилактика рака простаты
Снизить риск развития рака простаты можно следующим образом:
Здоровое питание. Рекомендуется избегать продуктов и блюд с высоким содержанием жиров; вместо этого предпочтение стоит отдавать фруктам, овощам, цельнозерновому хлебу. Не стоит увлекаться биодобавками – ни одно клиническое исследование не показало, что они способны предотвратить рак. Вместо них следует выбирать продукты, богатые витаминами и минеральными веществами. По некоторым данным, употребление зеленого чая может оказать профилактический эффект; правда, масштабного клинического исследования противораковых свойств зеленого чая еще не проводилось.
Спорт и активный образ жизни. Регулярные физические упражнения способны улучшить состояние здоровья, помогают держать вес в норме и улучшают настроение. Существуют свидетельства, что у мужчин, не занимающихся спортом, уровень ПСА выше. Желательно делать упражнения 3-4 раза в неделю.
Контроль веса. Если текущий вес пациента укладывается в границы нормы, желательно поддерживать его в этом состоянии. В этом могут помочь здоровое питание и регулярная физическая нагрузка. Если же он превышает норму, следует немного увеличить число упражнений и несколько сократить рацион; помочь в этом может консультация у специалиста-диетолога.
Регулярные обследования. Когда мужчина достигает 45-летнего возраста, целесообразно начать каждый год проверяться на уровни ПСА – этот анализ поможет определить рак (если он вообще возникнет) на ранней стадии, когда заболевание проще поддается лечению. Людям, входящим в ту или иную группу риска, рекомендуется проходить осмотр проктолога и проверяться на ПСА каждый год.
Лекарственные препараты и биодобавки при профилактике рака простаты
Рак нельзя предотвратить приемом биодобавок, витаминов или средств народной медицины (или, по крайней мере, пока не существует исследований, доказывающих обратное). Многие вещества, считающиеся полезными – например, витамин Е и витамин Д – не помогают при профилактике заболеваний простаты; исследование их действия не дало положительных результатов. Также не существует данных, подтверждающих эффективность ликопина и гранатового сока.
Согласно некоторым исследованиям, применение ингибиторов 5-альфа редуктазы, включая финастерид и дутастерид, может снизить вероятность возникновения рака почти на четверть.
Читайте также:





