Фторафур при раке поджелудочной железы
Проверенная продукция для здоровья.
- Заказать
- Фотостим
- Радаклин
- Регесол
- Лампа фотостимул
- Радохлорофилл
- Метод лечения онкологических заболеваний
- Область медицины
- Исцеляющий свет (Часть 2)
- Исцеляющий свет (Часть1)
- Фотодинамическая терапия
- Фотодинамическая терапия. Часть 2
- Лечение дистрофических заболеваний сетчатки глаза
- ФОТОСЕНСИБИЛИЗАТОРЫ
- ФДТ и омоложение организма
- Онкология лечение
- Клинические испытания применения ФДТ
- Задать вопрос о примении "Фотостима"
- Профилактика и лечение лучевых повреждений
- Лечение лучевой терапией
- Лучевая терапия восстановление
- Питание при лучевой терапии
- Химиотерапия и лучевая терапия
- Статьи по лучевой терапии
- Введение в химиотерапию
- Если была операция, зачем назначают химиотерапию?
- Когда появились лекарства "от рака"?
- Метастазы рака в печень: возможность хирургического лечения.
- Определение термина "РАК"
- Правда ли, что химиотерапия не на всех действует одинаково?
- Что такое химиотерапия
- Задать вопрос о примении "Фотостима"
- Химиотерапия и питание
- Справочник по химиотерапии
- Рак молочной железы
- Рак легких
- Рак желудка
- Рак головного мозга
- Другие виды рака
- Лечение рака легких
(открыта в США 60 лет назад). Основана на свойстве фотосенсибилизатора накапливаться в онкологических, клетках организма, как в наиболее энергодифицитных зонах. Подробнее.
После фотоактивации онкологические клетки самоуничтожаются (апоптоз)
Российские ученые разработали, доказали десятилетними исследованиями в онкологических центрах и, наконец, предложили для массового применения долгожданный препарат растительного происхождения, обладающий уникальнойспособностью распознавать атипичные (больные) клетки в организме, "метить" их) поднимать иммунную систему на борьбу с ними и из стволовых клеток уничтоженных "уродцев" выращивать молодые, здоровые клетки. Это "чудо XXI века" называется"ФОТОСТИМ".
1) Онкологическая клетка поглощает фотосенсибилизатор, например, "ФОТОСТИМ".
2) Орган освещается светом. Онкологическая клетка погибает.

Применяется в комплексе для лечения онкологических заболеваний.
Повышает иммунитет на 30% в течении 6 месяцев.
Подробнее о кремлевсой таблетке...
Цена: 7200 руб. Доставка по РФ.

Фторафур, легко преодолевая гематоэнцефалический барьер, способен адсорбироваться тканями головного мозга. Примечательно, что препарат в сравнительно высоких концентрациях обнаруживается в опухолевой ткани. Самым существенным отличием фторафура от фторурацила является его невысокая токсичность. Отщепляющийся от фторафура в процессе метаболизма окситетрагидрофуран при дальнейших превращениях может образовывать уоксимасляную кислоту, которая оказывает выраженное депримирующее влияние на центральную нервную систему. Такие вещества, как известно, значительно уменьшают побочные эффекты центрального происхождения.
Фармакологические свойства и терапевтическое действие. Фторафур обладает отчетливой противоопухолевой активностью. По биологическим свойствам он близок к фтор урацилу. В больших дозах фторафур угнетает кроветворение, приводя к развитию лейкопении, тромбоцитопении и анемии. Препарат в 5-7 раз менее токсичен, чем фторурацил, и лучше переносится больными. Показания к применению. Фторафур применяют при раке прямой и толстой кишки, желудка и пищевода, при опухолях мозга и раке молочной железы.
Фторафур эффективность и вредность
Наилучший терапевтический эффект достигнут при раке прямой и толстой кишки. У больных уже в период лечения улучшалось состояние, исчезали тягостные симптомы, опухоль постепенно уменьшалась в размерах; больные прибавляли в весе.
Иногда после химиотерапии фторафуром у больных с неоперабельным раком прямой и толстой кишки удавалось произвести радикальную операцию. Признается, что фторафур является одним из самых активных средств для лечения опухолей этой локализации.
При раке желудка объективный эффект наблюдается в меньшем проценте случаев. Однако следует отметить, что при неоперабельном раке желудка с метастазами в лимфатические узлы и распространением опухолевого процесса на печень и поджелудочную железу после лечения фторафуром наблюдается уменьшение или исчезновение болей улучшение проходимости пищи, уменьшение асцита. У больных с рицидивирующим раком желудка наблюдается уменьшение опухоли.
Есть случаи успешного лечения фторафуром плоскоклеточногс рака пищевода, а также рака молочной железы. У таких больных фторафур может быть рекомендован наряду с другими препаратами. Определенного успеха можно достигнуть при лечении фторафуром больных со злокачественными опухолями мозга.
Фторафур инструкция
Способ применения. Фторафур вводится внутривенно медленно через каждые 12 ч. В случае необходимости интервал может быть удлинен до 24 ч. Разовая доза препарата 1,2-2 г (из расчета 30 мг на 1 кг массы тела). Во время введения препарата возможно головокружение, поэтому его рекомендуется производить в постели. Общая доза препарата на курс-30-40 г, в отдельных случаях она может быть увеличена до 60 г. Во время лечения необходимо регулярно следить за картиной крови и производить анализы не реже 2 раз в неделю, а по окончании курса продолжать их в течение 2-3 недель.
Фторафур – лекарственный препарат противоопухолевого действия, активным веществом которого является тегафур.
Обладающее способностью встраиваться в сложные биохимические процессы, протекающие в тканях злокачественной опухоли, это вещество препятствует ускоренному делению раковых клеток, приостанавливая или вовсе прекращая развитие опухолевого процесса.
Преимуществом данного препарата перед целым рядом аналогов является менее выраженная токсичность и меньшее число вызываемых им побочных эффектов.
Состав, форма выпуска и условия хранения

Разнообразие лекарственных форм фторафура представлено нами в следующем списке.
Препарат выпускают в виде:
- Желатиновых капсул (содержащих 400 мг действующего вещества), предназначенных для внутреннего употребления.
- Ампул, вмещающих 10 мл стерильного 4% раствора для инъекций.
- Мази, упакованной в 35-граммовые тубы и предназначенной для наружного употребления.
- Ректальных (по 1000 мг) свеч.
- Субстанции (порошка натриевой соли), используемой для приготовления инъекционного раствора, вводимого внутривенно.
Фторафур, срок годности которого составляет четыре года, является препаратом списка А. Место его хранения должно быть:
- темным;
- недоступным для детей;
- относительно прохладным (максимальная температура хранения не должна превышать 25 градусов).
Производством препарата, разработанного латвийскими специалистами, занимаются специализированные фармацевтические предприятия:
Экспорт препарата осуществляют латвийские, литовские и японские фирмы-дистрибьюторы.
Показания к применению
Фторафур назначают для лечения:
- Злокачественных новообразований пищеварительного тракта, локализованных в поджелудочной железе, пищеводе, желудке, тканях ободочной и прямой кишки.
- Нейроэктодермальных опухолей, поразивших ткани головного мозга.
- Ретикулоэндотелиоза кожи (заболевания, сопровождающегося прогрессирующим разрастанием ретикулярных кожных структур).
- Рака молочных желез.
- Эндогенных увеитов (воспалительных заболеваний сосудистой оболочки глазных яблок).
- Злокачественных опухолей печени и яичников.
- Диффузных нейродермитов (например, почесухи обыкновенной – болезни, характеризующейся постоянным зудом кожных покровов и симметричной локализацией очагов поражения на гениталиях, лице и сгибательных поверхностях верхних и нижних конечностей).
- Кожных лимфом.
Противопоказания
Применение фторафура противопоказано пациентам, страдающим:
- язвенной болезнью двенадцатиперстной кишки и желудка;
- геморрагией (склонностью к кровотечениям, обусловленным высокой проницаемостью сосудистых стенок или нарушением их целостности);
- тяжелыми инфекционными заболеваниями;
- медикаментозной гиперчувствительностью;
- анемией (недостатком гемоглобина и эритроцитов в крови);
- тромбоцитопенией (дефицитом тромбоцитов в единице объема крови);
- патологическими изменениями в составе крови;
- лейкопенией (снижением содержания лейкоцитов в крови);
- патологиями почек и печени.
Эффективность
![]()
Терапевтический эффект фторафура, используемого при лечении злокачественных опухолей желудка, по результативности аналогичен действию фторурацила; что же касается эффективности его применения в терапии рака прямой и толстой кишок – здесь он значительно превосходит вышеуказанный препарат. В лечении пациентов, страдающих этими видами рака, одинаково высокую результативность показывают все способы введения фторафура: и внутривенное, и пероральное, и ректальное.- Максимально выраженный эффект действия фторафура был замечен при лечении больных, у которых злокачественная опухоль пищеварительного тракта метастазировала в печень. Этот результат обусловлен спецификой фармакокинетики препарата.
- Как показали наблюдения, применение фторафура может привести к объективному и субъективному улучшению состояния пациентов, у которых нейроэктодермальные опухоли головного мозга были выявлены на самых начальных стадиях развития. Такую же картину можно наблюдать и при использовании препарата для терапии послеоперационных рецидивов. Длительность достигнутых ремиссий может составлять при этом не менее полутора лет.
- Фторафур показал некоторую эффективность и как препарат, способный участвовать в определенных схемах полихимиотерапии.
Инструкция по применению Фторафура
Принимать фторафур рекомендуется за полчаса до еды или после нее.
Допустимая суточная доза препарата во время монотерапии составляет не более двух граммов (концентрация лекарственного средства в организме больного должна составлять до тридцати миллиграммов на каждый килограмм массы тела).
Для выполнения инъекций используют готовый ампулированный препарат или стерильный 4% раствор, приготовленный из порошкообразной субстанции натриевой соли.
Внутривенное введение препарата осуществляют капельно или струйно. Больной при этом принимает лежачее положение.
Инъекции фторафура могут осуществляться по следующим схемам:
- В организм пациента внутривенно вводят до пятнадцати миллиграммов препарата на каждый килограмм веса. Продолжительность курса составляет от трех до четырех недель (с месячными интервалами между курсами).
- Фторафур в такой же дозировке вводят один раз в неделю. Полный курс лечения составляет не более десяти инъекций.
- Препарат вводят инфузионным путем (через капельницу), непрерывно делая это на протяжении четырех-пяти суток.
- Если фторафур применяется в комплексной терапии, шестьсот миллиграммов препарата вводят во время первого и восьмого дня лечения. При комбинировании фторафура с фолинатом кальция дозировку первого препарата уменьшают на 30%.
Одна картонная пачка содержит десять ампул с 4% раствором фторафура.
Внутри твердых желатиновых капсул, имеющих корпус желтого цвета и ярко-оранжевый колпачок, находится белый мелкодисперсный порошок, не имеющий запаха, состоящий из действующего вещества (тегафура) и вспомогательной субстанции (стеариновой кислоты).
Корпус каждой капсулы изготавливается из желатина, диоксида титана и хинолинового желтого красителя (пищевой добавки E104); в состав крышечки добавляют пунцовый краситель Понсо 4R (E 124). Капсулы (по 100 штук) расфасовывают в полиэтиленовый флакон, который помещают в картонную пачку.
Если терапия является комбинированной, фторафур назначают в сниженной дозировке. Повторный курс лечения фторафуром возможен через шесть-восемь недель.
5% мазь Фторафур выпускается в тубах, содержащих 35 г препарата и применяется для лечения кожных лимфом, изъязвленных базалиом и диффузных нейродермитов.
Для лечения изъязвленных базалиом рекомендуется курсовое (продолжительностью в три-четыре месяца) применение.
Тонкий слой мази должен наноситься на пораженные участки кожных покровов не менее двух раз в сутки.
Перед каждым применением препарата поверхность изъязвленного участка очищают при помощи антисептических лекарственных средств. Количество мази, используемой для разового применения, не должно превышать четырех граммов.
Повторный курс возможен лишь четыре-шесть недель спустя.
Побочные действия

Применение фторафура может:
- Привести к развитию анемии, тромбоцитопении и лейкопении.
- Спровоцировать приступы тошноты, рвоты, боль в животе, жидкий стул.
- В редких случаях стать виновником развития эзофагита (болезни пищевода, сопровождающейся воспалением слизистых оболочек), стоматита, фарингита, острого панкреатита и гепатита, изъязвлений слизистых оболочек желудочно-кишечного тракта и кровотечений из него.
- Нарушить процесс регенерации ногтевых пластин и кожных структур.
- Вызвать алопецию (выпадение волос).
- Привести к сонливости, спутанности сознания, сильным головокружениям, расстройству координации движений (атаксии).
- Спровоцировать ишемию или инфаркт миокарда, стенокардию или кардиалгию (болевые ощущения в сердечной мышце, не связанные с поражением сердечных артерий).
- Привести к выраженному слезотечению, двоению зрения (диплопии), фиброзу слезных протоков.
- Стать причиной аллергической реакции (вплоть до анафилактического шока), утраты обоняния, нарушения работы почек, обезвоживания организма.
Применение мази может стать причиной местных реакций, проявляющихся в гиперпигментации, сухости, шелушении, покраснении и зуде кожных покровов.
Передозировка
Передозировка препарата может привести к нарушению процесса кроветворения (гемопоэза), состоящего в образовании клеток крови – эритроцитов, лейкоцитов и тромбоцитов. Могут также развиться токсические реакции со стороны органов центральной нервной системы и желудочно-кишечного тракта.
Чтобы устранить последствия передозировки, применяется симптоматическое лечение с обязательным контролем функции кроветворения на протяжении одного месяца.
Особые указания
Назначая фторафур, лечащий врач должен быть особенно внимательным по отношению к больным:
- страдающим язвой ДПК и желудка, инфекционными болезнями, предрасположенностью к кровотечениям;
- имеющим нарушения в работе почек и печени и в функционировании системы кроветворения;
- отличающимся недостаточной выработкой глюкозы.
Такие пациенты нуждаются в постоянном контроле характеристик периферической крови, а также функционального состояния печени и почек. Делать это следует не только во время курсового лечения, но и на протяжении десяти дней после его завершения.
Чтобы предотвратить угнетение функции кроветворения, в организм пациента вливают по 100 мл донорской крови, делая это не менее двух-трех раз.
Стоит отметить, что прием препарата неизбежно заканчивается угнетением репродуктивных функций больного.
Появление серьезных побочных эффектов (стоматита, тромбоцитопении, кровотечений, выраженной лейкопении, фарингита и т. п.) является основанием для немедленного прекращения приема препарата.
Пациент, принимающий фторафур, должен тщательно следить за гигиеной ротовой полости. Во время лечения фторафуром необходимо назначение витаминов.
Лекарственное взаимодействие
![]()
Фторафур усиливает лечебное воздействие фенитоина и метотрексата, принимаемых совместно с ним.- Прием фторафура способствует усилению действия других химиотерапевтических препаратов и сеансов лучевой терапии. Его повторное применение возможно лишь через месяц после завершения предыдущего курса лучевой или химиотерапии.
- Лекарственные препараты диазепам, цитарабин, а также антрациклиновые антибиотики несовместимы с фторафуром.
Отзывы пациентов
Анастасия:
Я прошла несколько курсов лечения фторафуром. В результате организм избавился от множественных метастазов во внутренних органах (за исключением единичных, локализованных в печени). Чувствую себя значительно лучше.
Екатерина:
Химиотерапия с использованием фторафура дала очень хороший результат, но начались побочные эффекты со стороны органов пищеварения. Мое состояние ухудшилось настолько, что в течение семи дней я с трудом пила только воду. Фторафур пришлось отменить, меня перевели на кселоду.
Виктория:
Хочу поделиться простым средством, помогающим защитить органы пищеварения от токсического воздействия фторафура. Во время курса химиотерапии необходимо употреблять обычный овсяный кисель. Благодаря его обволакивающим свойствам слизистые оболочки кишечника и желудка оказываются защищенными от повреждений.
Анжела:
Была удивлена, получив врачебное предписание принимать фторафур во время сеансов лучевой терапии, поскольку в инструкции к препарату сказано, что он несовместим с этой процедурой. Однако специалисты уверяют, что таким образом можно добиться более острой реакции опухоли на радиотерапию.
Цена на Фторафур
Стоимость одной упаковки, содержащей 100 капсул фторафура, в аптеках Москвы колеблется в рамках ценового диапазона от 10 000 до 13 500 рублей.
Аналоги лекарства
Аналогичным действием обладают препараты:
Препарат фторафур имеет множество синонимичных названий. В разных медицинских источниках он именуется как:
- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
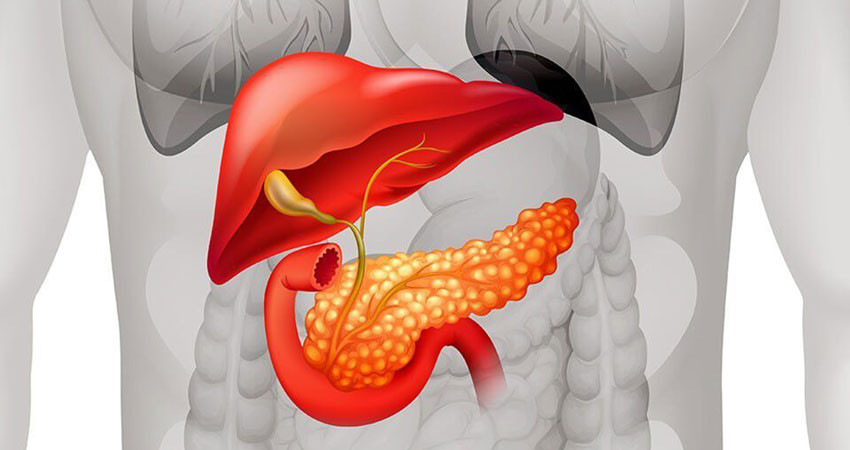
Рак поджелудочной железы относится к онкологическим заболеваниям, с которыми сложно бороться, и которые характеризуются относительно низкой выживаемостью. В течение 5 лет с момента установления диагноза в живых остаются лишь 9% больных. Рак поджелудочной железы нередко диагностируют в запущенной стадии, потому что не существует эффективного рекомендованного скрининга, злокачественная опухоль может долго не вызывать симптомов.
Тем не менее, пациенту можно помочь, даже если заболевание диагностировано на поздней стадии. В случаях, когда невозможно добиться ремиссии, врачи могут продлить жизнь пациента и избавить его от мучительных симптомов. Эффективное лечение можно получить в клинике Медицина 24/7.
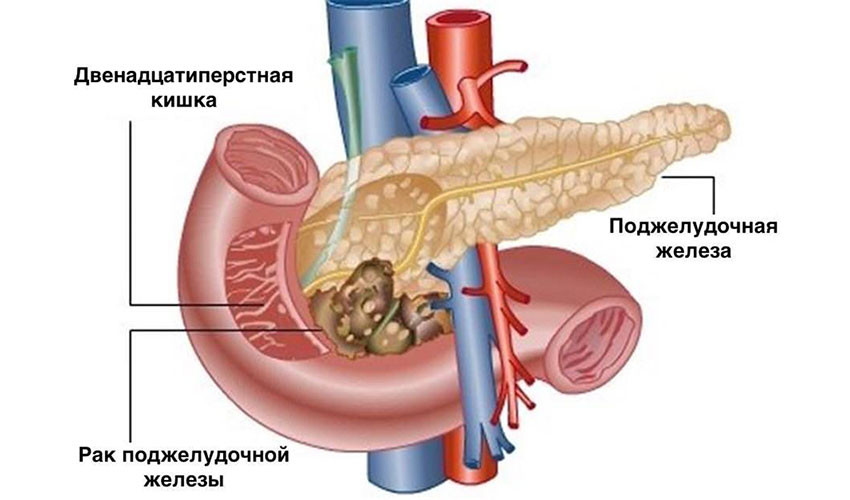
Хирургическое лечение
Хирургическое удаление опухоли — самый эффективный метод лечения рака поджелудочной железы. Это единственная реальная возможность достичь ремиссии. К сожалению, на момент постановки диагноза только у одного из пяти пациентов опухоль не успела распространиться за пределы поджелудочной железы, и лишь у некоторых из них рак можно полностью удалить. Обычно это узлы в головке органа: через неё проходит желчный проток, при его сдавлении развивается механическая желтуха, и эта симптоматика помогает рано диагностировать опухоль.
Операцию проводят, если хирург уверен, что он сможет удалить рак полностью. Циторедуктивные вмешательства, направленные на частичное удаление как можно большего количества опухолевой ткани, не проводятся, так как нет доказательств того, что они помогают продлевать жизнь пациентов.
При раке головки поджелудочной железы чаще всего выполняют операцию Уиппла. Во время нее удаляют головку органа, иногда вместе с телом, и часть окружающих органов: тонкой кишки, желчного протока, ближайшие лимфатические узлы, желчный пузырь, иногда часть желудка.
При резектабельном раке хвоста поджелудочной железы проводят дистальную панкреатэктомию: удаляют хвост поджелудочной железы, иногда вместе с телом, и селезенку.
В редких случаях встречаются ситуации, когда злокачественная опухоль распространилась по всей поджелудочной железе, но все еще является операбельной. При этом может быть выполнена тотальная панкреатэктомия: поджелудочную железу удаляют полностью, вместе с ней — желчный пузырь, часть желудка и тонкой кишки.

Паллиативные операции
Во время паллиативных операций не удаляют рак, их цель — избавить больного от симптомов, вызванных злокачественной опухолью. При раке головки поджелудочной железы нередко развивается механическая желтуха — состояние, вызванное сдавлением желчного протока и нарушением оттока желчи. У больного окрашиваются в желтый цвет кожа, слизистые оболочки и белки глаз, беспокоит кожный зуд, ухудшается общее состояние, прогноз.
С этим осложнением можно справиться тремя способами:
- Дренирование. Во время эндоскопической ретроградной холангиопанкреатографии (РХПГ) или чрескожной чреспеченочной холангиографии в желчные протоки устанавливают дренажную трубку. По ней желчь может оттекать наружу, в просвет двенадцатиперстной кишки или сразу в обоих направлениях. Это достаточно эффективно, но не очень удобно: дренажная трубка постоянно мешается, может случайно сместиться, выпасть.
- Стентирование — более современное решение. Эндоскопически, с помощью катетера, заведенного в желчные протоки из двенадцатиперстной кишки, в заблокированном участке устанавливают стент — трубку с сетчатой стенкой из полимера или металла. Он расширяет просвет протока и обеспечивает свободный отток желчи. Стентирование — быстрая и относительно безопасная процедура, ее выполняют без разрезов.
- Шунтирование — операция, во время которой хирург создает обходной путь для оттока желчи. По сравнению со стентированием, хирургическое вмешательство несет более высокий риск осложнений, его могут перенести не все больные. Но иногда оно позволяет более эффективно, надолго восстановить отток желчи. Во время операции можно перерезать нервы, которых беспокоят мучительные боли.
Насколько эффективна химиотерапия при раке поджелудочной железы?
Химиопрепараты довольно часто применяют при злокачественных опухолях поджелудочной железы. Они могут быть назначены с разными целями:
- Адъювантная химиотерапия проводится до операции, чтобы уменьшить объем опухоли.
- Неоадъювантная химиотерапия проводится после операции, чтобы снизить риск рецидива.
- Химиотерапия как основной метод лечения применяется при неоперабельных опухолях. Цель лечения в таком случае — не достичь ремиссии, а как можно дольше держать болезнь под контролем.
Чаще всего применяют такие химиопрепараты, как гемцитабин (Гемзар), оксалиплатин (Элоксатин), иринотекан (Камптозар), , цисплатин, капецитабин (Кселода). Обычно назначают комбинации из двух препаратов с разными механизмами действия, это помогает повысить эффективность лечения. Ослабленным пациентам назначают только один препарат риска серьезных побочных эффектов.
Эффективность лучевой терапии
Лучевую терапию при раке поджелудочной железы зачастую применяют вместе с химиопрепаратами. Такое лечение называется химиолучевой терапией. Ее назначают после операции, при неоперабельном раке.
Если опухоль находится в пограничном состоянии между резектабельной и нерезектабельной, после курса неоадъювантной лучевой терапии ее размеры могут уменьшиться так, что ее получится удалить хирургическим путем.
Также лучевую терапию при раке поджелудочной железы применяют в качестве симптоматического лечения, например, если беспокоят мучительные боли, и пациенту противопоказано хирургическое вмешательство.
Таргетная терапия
На поверхности раковых клеток в поджелудочной железе нередко увеличено количество молекул EGFR. Активируясь, он заставляет клетки быстро размножаться. Его можно заблокировать с помощью таргетного препарата эрлотиниб (Тарцева). Его часто назначают в сочетании с химиопрепаратом гемцитабином. Эффективность этой комбинации различается у разных онкологических больных.
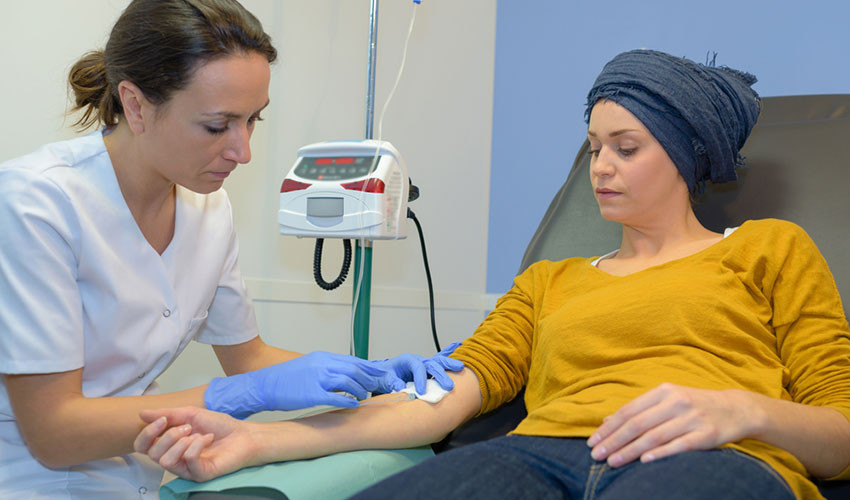
Помогает ли иммунотерапия при раке поджелудочной железы?
Иммунная система человека должна не только атаковать чужеродные агенты, но и знать, когда пора остановиться, чтобы не навредить собственным тканям организма. Для этого в ней есть специальные сигнальные молекулы, подавляющие активность иммунных клеток. При раке эти молекулы начинают мешать. Они не дают иммунитету эффективно распознавать и уничтожать опухолевые клетки. Существуют препараты, которые могут заблокировать эти молекулы, они называются ингибиторами контрольных точек.
При раке поджелудочной железы ингибиторы контрольных точек могут быть полезны для пациентов, у которых выявлены определенные генетические отклонения: высокий уровень микросателлитной нестабильности, мутации в генах восстановления несоответствия (MMR).
В клинике Медицина 24/7 при многих типах рака можно пройти исследование, которое помогает выявить мишени для лекарственных препаратов, имеющиеся в раковых клетках пациента, и назначить оптимальную, персонализированную терапию.
Купирование боли
Боли низкой интенсивности можно купировать с помощью ацетилсалициловой кислоты (аспирина) или парацетамола, при болях средней интенсивности назначают опиаты внутрь (сульфат морфина по 20 мг 2 раза в сут), к которым можно добавить блокаторы Н1-рецепторов гистамина. При более интенсивных болях наркотические анальгетики вводят подкожно, внутривенно, эпидурально или интратекально. Бензодиазепины (диазепам по 2 мг 3 раза в сут) или хлорпромазин (по 25мг 3 раза в сут) усиливают эффект морфина у тревожных больных.
Наиболее эффективно купируют боли наркотические анальгетики, однако их применение ограничено развитием широкого спектра побочных реакций, включающих сухость во рту, запоры, тошноту, рвоту, сонливость, возможность развития галлюцинаций и бреда, что в целом может значительно уменьшать качество жизни. Кроме того, длительное применение наркотических анальгетиков закономерно вызывает развитие физической и психической зависимости.
Непереносимые боли можно уменьшить с помощью лучевой терапии. Для симптоматического лечения используют антацидные препараты, блокаторы Н2-рецепторов гистамина, препараты ферментов ПЖ, иногда — небольшие дозы глюкокортикоидов. Для купирования зуда, связанного с желтухой, назначают колестирамин (холестирамин) или фенобарбитал.
Закономерно к купированию болевого абдоминального синдрома приводит химиотерапия.
Химиотерапия
Оценка эффективности консервативных методов лечения рака ПЖ затруднительна. Это обусловлено тем, что растущая протоковая опухоль ПЖ вызывает десмопластические реакции окружающих тканей, опухоль состоит не только из злокачественных клеток, но и из воспалительных элементов и фиброзной ткани. Кроме того, забрюшинное расположение ПЖ и отсутствие реакции фиброзной ткани на успешную химиотерапию не позволяет уточнить расположение очагов и динамику заболевания при использовании современных диагностических методов, таких, как КТ, МРТ и УЗИ. Таким образом, традиционные современные методы оценки эффективности консервативной противоопухолевой терапии при раке ПЖ не всегда объективно отражают степень регрессии первичной опухоли и метастазов в отдалённых органах и тканях.
До сих пор рак ПЖ считают резистентной к химиолучевой терапии опухолью, поэтому основное внимание исследователи уделяют не столько получению объективного эффекта в виде регрессии опухоли, сколько достижению улучшения качества жизни и продления её.
Поскольку возможности инструментальной регистрации уменьшения опухоли ограничены, были предложены дополнительные показатели оценки эффективности противоопухолевого лечения, основные из которых — качество жизни и её продолжительность. Большое внимание уделяют купированию болевого синдрома и снижению суточной потребности в обезболивающих средствах. Клинические наблюдения показывают, что даже незначительное уменьшение размеров опухоли ПЖ, которое соответствует стабилизации болезни, может сопровождаться исчезновением болевого синдрома и улучшением общего физического статуса пациента.
Таким образом, лучевая терапия, химиотерапия и иммунотерапия — только паллиативное и, в целом, малоэффективное лечение.
В течение многих десятилетий в качестве стандартного препарата для паллиативного лечения рака ПЖ применяли фторурацилиею комбинации с другими цитостатиками. Фторурацил — синтетический аналог естественного пиримидинового основания урацила. В процессе распада фторурацила несколько его метаболитов оказывают повреждающее воздействие на синтез и функционирование ДИК и рибонуклеиновых кислот опухолевых клеток.
Основная мишень — фермент тимидилат синтетаза, контролирующий синтез нормальных тимидиновых нуклеотидов — угнетается метаболитом фторурацила 5-фтордезокси-уридин монофосфатом. Другой фармакологически активный метаболит 5-фтордезоксиуридин трифосфат встраивается в ДНК опухолевых клеток вместо трифосфата тимидина, что ведёт к её разрывам. Ещё один метаболит — 5-фторуридинтрифосфат встраивается в рибонуклеиновую кислоту и серьёзно повреждает её стабильность.
Эффективность монотерапии фторурацилом и различных комбинаций с ним при раке ПЖ крайне низка (0-20%), а средняя выживаемость составляет всего 5—6 мес. Из других цитостатиков, которые проявили противоопухолевую активность при клинических испытаниях, следует отметить цисплатин, эпирубицин, митомицин, стрептозоцин, тегафур (фторафур), эффект которых колеблется в пределах 0-10%.
У ряда врачей сложилось мнение, что химиотерапевтическое лечение существенно не повышает качество жизни у больных с перезектабельным раком ПЖ. Однако, клинические исследования по изучению различных схем химиотерапии при раке ПЖ показали, что химиотерапия — лучше, чем любая симптоматическая терапия, и уж тем более её отсутствие.
Рандомизированные исследования по применению фторурацила в комбинации с доксорубицином (адриамицином), митомицином и этопозидом по сравнению с симптоматической терапией показали достоверное увеличение выживаемости в группе больных, которым проводили химиотерапию.
Внедрение в клиническую онкологию новых оригинальных противоопухолевых препаратов с различным механизмом действия на опухолевую клетку привело к увеличению эффектавности химиотерапии. При изучении препаратов из группытаксановбыли изучены паклитакселидоцетаксел, эффективность которых оказалась 20%. Ралтитрексид (томудекс) оказался активным в 12%, а иринотекан (кампто) — в 11,4% случаев. Наибольшую противоопухолевую активность при раке ПЖ проявил гемцитабин — фторзамещённый аналог дезоксицитидина, близкий по структуре к цитарабину (цитозару). Однако, в отличие от последнего, гемцитабин более липофильный, вследствие чего он быстрее проходит через мембраны опухолевых клеток. У гемцитабина больший аффинитет к мишени — дезоксицидин киназе, его активный метаболит гемцитабин трифосфат дольше, чем цитозар, находится в опухолевой клетке.
При монотерапии гемцитабином частичное уменьшение опухоли происходит в 10,6—12,8%, а симптоматический эффект — в 23,8—43% случаев. Гемцитабин эффективен у больных, рефрактерных к фторурацилу. Таким образом, гемцитабин — наиболее перспективное средство для лечения генерализованного рака ПЖ и, несомненно, препарат первой линии. В последние годы предприняты попытки разработать новые, более эффективные комбинации противоопухолевых препаратов, каждый из которых в той или иной степени эффективен при раке ПЖ. Следует отметить, что большинство применённых схем включали гемцитабин (табл. 5-8).
Учитывая синергизм действия гемцитабина и препаратов платины, были проведены клинические исследования по изучению данной комбинации. Результаты таковы: общий лечебный эффект составляет 50—57%, частичное уменьшение опухоли отмечено в 17% случаев.
При применении цисплатина, эпирубицина, фторурацила и гемцитабина у больных диссеминированным раком ПЖ объективный эффект значительно выше — 58% случаев. Средняя длительность эффекта составляет 8,5 мес, а средняя выживаемость — 11 мес. Симптоматический эффект отмечен у 78% больных.
Предприняты попытки улучшить результаты лечения путём использования комбинации таксанов и гемцитабина — клиническое улучшение происходит у 23—44,4% больных.
Комбинация митомицина и гемцитабина показывает лечебный эффект у 28,5% больных, стабилизацию — у 50%, а симптоматический эффект — у 46,6% больных.
Учитывая экспериментальные данные о радиосенсибилизирующем эффекте гемдитабина, проводят химиолучевое лечение. Средняя выживаемость при этом составляет 17.3 мес.
Таким образом, несмотря на кажущиеся скромные результаты применения гемцитабина при распространённом раке ПЖ, исследования показывают, что средняя продолжительность жизни увеличивается с 4 до 8 мес, а клиническое улучшение общего состояния наступает более чем у половины больных.
Адъювантное и неоадъювантное лечение
Одно из направлений улучшения результатов при неоперабельном раке ПЖ — сочетание лучевой терапии и перспективных противоопухолевых лекарств — позволяет достичь объективного улучшения у 27% больных и средней выживаемости 8—15 мес при хорошей переносимости режима комбинированной терапии. Низкая эффективность методов хирургического и лучевого лечения рака ПЖ создала предпосылки для активного изучения адъювантного и неоадьювантного подхода к лечению рака ПЖ (табл. 5-9). Сводные данные по результатам адъювантного химиолучевого лечения представлены в табл. 5-10.
Попытка адъювантного лечения с помощью химиотерапии без сопутствующею облучения ложа удалённой опухоли не даёт хороших результатов.
Таким образом, адъювантная терапия стала значительной ступенькой в лечении рака ПЖ. Однако полноценное её использование ограничено, потому что только 20% больных операбельны на момент первичной диагностики. Максимальный эффект адъювантного лечения можно получить лишь у 4% всех больных.
Интерес к неоадьювантной терапии рака ПЖ основан на том, что лишь небольшой процент больных обращается в клинику на ранней стадии болезни. Значительно чаще на момент первичной диагностики опухоль распространяется на окружающие ПЖ ткани, вовлекая пара-панкреатическую клетчатку и соседние органы. Другое теоретическое обоснование применения предоперационного лечения — возможность предотвращения имплантационного метастазирования во время хирургического вмешательства. Глобальной задачей неоадъювантного подхода служит попытка увеличить возможность удаления опухоли до 40% (20% за счёт потенциально излечимых больных и 20% за счёт неизлечимых пациентов на момент первичной диагностики путём рестадирования).
Средняя выживаемость при неоадъювантной терапии составляет 12—14 мес. Использование в качестве неоадъювантного лечения только химиотерапии не приводит к достоверному увеличению выживаемости. Необходимо дальнейшее развитие этого метода для лечения рака ПЖ, что позволит увеличить процент резектабельности опухоли и увеличить сроки жизни больных.
Гормонотерапия и перспективы лечения
Считают, что рак ПЖ — опухоль гормонозависимая, в пользу чего свидетельствуют указанные нами ранее половые различия в частоте рака ПЖ (у мужчин чаще), а также обнаружение рецепторов стероидных гормонов. Однако была отмечена низкая способность связывания рецепторов гормонами в культуре клеток рака ПЖ у человека. В эксперименте было показано, что тестостерон может стимулировать рост опухолевых ктеток, а эстрогены — замедлять. Возникла идея применения антагонистов андрогенов и аналогов релизипг-гормонов, но эти попытки не увенчались успехом. У пожилых женщин в ряде исследований выявлено положительное влияние тамоксифена, однако механизм полученного эффекта не совсем ясен. Весьма интересны результаты исследований с применением октреотида (300—600 мг/сут), способствующего стабилизации опухолевого процесса в 27% случаев.
Разработан препарат маримастат — ингибитор опухолевых металлопротсиназ, принимающих участие в росте и метастазировании карциномы. Идут клинические испытания ингибитора фермента фарнезил трансферазы, необходимого для встраивания в клеточную мембрану белка K-ras. На этот протеин, уже встроенный в мембрану, способны действовать монотерпены. Реальные перспективы открылись с развитием генетических аспектов лечения рака ПЖ:
• клонирование участков ДНК, комплементарных мутантным;
• создание на их основе системы переносчиков, эффекторных векторов — рекомбннантного аденовирусного вектора, аденоассоциированных вирусных векторов (из ларвовирусов), катионного липидного комплекса (излилосом) и др.;
• комплементарное внедрение этой системы в культуру поражённых клеток, устранение дефекта.
Одно из перспективных направлений в лечении рака ПЖ — вакцинация. Она основана на развитии цитолитического Т-клеточного ответа при сенсибилизации Т-лимфоцитов опухолевыми антигенами. Сенсибилизацию проводят in vitiv, а затем сенсибилизированные лимфоциты вводят больному.
Ретинодды способны тормозить рост и метастазирование опухоли, повышать дифференцированность её клеток. Это действие усиливается при сочетании ретиноидов с интерфероном-а. Последний и сам обладает антипролиферативным эффектом.
В целом молекулярно-биологические разработки генной терапии, несомненно, радикальным образом изменят лечение рака ПЖ, но это пока ешё впереди. Изменить сложившуюся ситуацию способны только профилактические диагностические подходы, особенно у лиц с отягощенным анамнезом и наличием факторов риска.
Читайте также:







