Фототерапия при раке мочевого пузыря у мужчин
Цель исследования: Целью исследования явилась оценка эффективности применения фотодинамической терапии вместе с трансуретральной резекцией при лечении 36 больных поверхностным раком мочевого пузыря. В качестве фотосенсибилизатора использовали фотодитазин в средней дозе 0,8 мг/кг массы тела. Время экспозиции составляло от 12 до 48 минут. Рецидивирование опухолевого процесса в первые 12 месяцев после проведенного лечения отмечено только у 4 (11,1 %) больных, что расценено как положительный результат.
Ключевые слова: поверхностный рак мочевого пузыря, фотодинамическая терапия, фотодитазин.
Введение
Рак мочевого пузыря (РМП) является актуальной проблемой онкоурологии. Это связано, прежде всего, с высокими показателями заболеваемости и смертности от данной патологии. Ежегодно в мире регистрируют до 200 тыс. новых случаев РМП. В России в 2009 году выявлено 13 260 новых случаев РМП у мужчин, стандартизованный показатель заболеваемости составил 12,18 на 100 тыс. мужского населения. У женщин в 2009 году отмечено 2828 случаев РМП, стандартизованный показатель заболеваемости составил 1,82 на 100 тыс. женского населения [3].
РМП характеризуют прогрессирующее течение и склонность к рецидивированию. В качестве стандартного опера тивного вмешательства при лечении поверхностного РМП в настоящее время рассматривают транс уретральную резекцию стенки мочевого пузыря (ТУР). Однако вероятность возникновения рецидива опухоли после ТУР достаточно высока и в среднем составляет 50 %, при этом примерно половина рецидивов развиваются в течение первого года после операции [1, 11]. Рецидивы после трансуретральной резекции поверхностного РМП выявляют у 30 % больных при наличии одиночной опухоли и у 90 % пациентов при мультифокальном поражении мочевого пузыря [10]. Прогрессирование заболевания и развитие мышечно-инвазивного РМП отмечено у 15 % больных с опухолями стадии Та и у 33 % больных с опухолями стадии Т1. В зависимости от размера опухоли прогрессирование регистрируют в 10 % случаев при опухолях менее 3 см и в 35 % — при размерах опухоли более 3 см [4, 5]. В связи с высокой частотой возникновения рецидивов и прогрессирования поверхностного РМП полное излечение пациентов представляется весьма трудной задачей. В связи с этим важное значение приобретают мероприятия, направленные на профилактику рецидивов опухолевого процесса после ТУР. Основными направлениями адъювантного лечения являются внутрипузырная химиотерапия, иммунотерапия, фотодинамическая терапия (ФДТ), позволяющие уменьшить вероятность рецидивирования РМП в среднем на 20 % [2, 6].
В настоящее время ФДТ применяют в качестве первичного, противорецидивного, паллиативного лечения, а также в комбинации с традиционными методами лечения. При поверхностных формах опухолей мочевого пузыря ФДТ применяют в качестве основной или адъювантной терапии. Для проведения ФДТ предпочтение отдают фотосенсибилизаторам второго поколения. Последние являются производными хлорина Е6 и обладают мощной полосой поглощения в длинноволновой красной области спектра. К препаратам данной группы относится фотодитазин. Исходным сырьем для производства фотодитазина является микроводоросль Spirulina platensis. Препарат создан на основе производных хлорофилла А и характеризуется свойствами, существенно отличающимися от наиболее известных зарубежных и отечественных аналогов. Фотодитазин хорошо растворяется в воде и не образует агрегированных форм, характерных для производных гематопорфирина. Способность фотодитазина связываться с клеточными мембранами опухолевых клеток обусловливает его высокую фотодинамическую активность. Фотосенсибилизатор более интенсивно накапливается в активно делящихся клетках. Максимум накопления в опухоли наступает через 1,5–2 часа после введения препарата в организм человека. Индекс контрастности по отношению к окружающей нормальной ткани при этом составляет более 10.
Для проведения ФДТ при опухолях мочевого пузыря необходимо следующее оборудование: стандартный цистоскоп с прямым рабочим каналом 6Ch или катетеризационный цистоскоп, фиброоптичес кое волокно, эндоскопическая стойка, источник света. Важными характеристиками лазерных установок являются выходная мощность, время выхода на рабочий режим, гарантированное количество часов работы. В этом отношении не оспоримыми преимуществами обладают диодные лазеры. Они портативны, экономичны, не требуют водяного охлаждения, питаются от обычной электрической сети с напряжением 220 вольт и имеют гарантированный длительный период работы. Для проведения света от лазерной установки к опухоли используют кварцевые моноволоконные световоды длиной от 1,5 до 3 метров и диаметром 6Ch. В зависимости от характера отражения выделяют световоды с прямым и боковым отражением света. В качестве диффузора используют цилиндрический и сферический диффузоры.
Длительность светового воздействия при ФДТ рассчитывается, исходя из заданной, эмпирически подобранной эффективной дозы световой энергии (Е). Для фотодинамической терапии опухолей мочевого пузыря эта величина находится в диапазоне 300–600 Дж/см 2. Выходная мощность на конце световода во время ФДТ составляет 1–2 Вт.
Целью настоящего исследования явилась оценка эффективности применения ФДТ вместе с ТУР при лечении больных с поверхностным РМП.
Пациенты и методы исследования
Под наблюдением в урологической клинике СПбГМУ имени акад. И. П. Павлова находились 36 больных с поверхностным РМП. Среди наблюдаемых больных были 21 мужчина и 15 женщин. Возраст пациентов составил в среднем 60,5 ± 8,5 лет и находился в диапазоне от 42 до 80 лет. Всем больным проводили стандартное урологическое обследование, включавшее в себя сбор анамнеза, физикальное обследование, лабораторные исследования, в том числе цитологический анализ мочи, цистоскопию, УЗИ, КТ или МРТ. Диагноз РМП верифицировали гистологически при исследовании образцов ткани из измененных участков стенки мочевого пузыря. При цистоскопии определяли размеры опухоли, характер роста (экзофитный или стелящийся) и количество опухолевых очагов. При УЗИ КТ или МТР оценивали размер и глубину инвазии опухоли.
За 1,5 часа до начала трансуретральной резекции внутривенно капельно пациентам в условиях полутемного помещения вводили препарат фотодитазин из расчета 0,5–1,5 мг/кг массы тела. Доза фотосенсибилизатора рассчитывалась для каждого больного индивидуально и зависела не только от его массы тела, но и от размера и характера опухоли мочевого пузыря. В среднем доза фотодитазина составляла 0,8 мг/кг массы тела. Непосредственно перед введением раствор фотодитазина разводили в 0,9 % растворе NaCl в соотношении 1 : 4. Инфузию препарата осуществлял врач или медицинская сестра в его присутствии. Под спинальной анестезией проводилась ТУР опухоли мочевого пузыря до глубокого мышечного слоя, а затем под визуальным контролем проводили локальное облучение зоны резекции и окружающих тканей лазером. Доза световой энергии составляла от 300 до 600 Дж/см 2, а мощность излучения — от 1 до 2 Вт. После завершения вмешательства мочевой пузырь дренировали уретральным катетером. Продолжительность сеанса ФДТ находилась в интервале от 12 до 48 минут и находилась в прямой зависимости от площади облучаемой поверхности, что, в свою очередь, определялось размером опухоли.
Время лазерного воздействия на опухолевую ткань рассчитывали по формуле:
t = Е × S/P;
где t — время экспозиции, с; E — эффективная доза световой энергии, Дж/см 2; S — площадь поверхности опухоли, см 2; Р — мощность на конце световода Вт, с.
Поскольку фотодитазин выводится из организма в течение 28 часов после введения, больные после проведения ФДТ из-за возможной реакции кожи на свет в течение этого времени находились в специально оборудованной затемненной палате.
С целью оценки эффективности комбинированного лечения и выявления рецидивов РМП после операции больным каждые 3 месяца выполняли цистоскопию и цитологическое исследование мочи и каждые 6 месяцев — ультразвуковое исследование мочевого пузыря.
Результаты и обсуждение
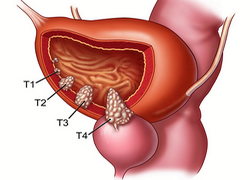
Результаты дооперационного обследования позволили оценить особенности клинических проявлений РМП у наблюдаемых нами больных. Один опухолевый очаг был выявлен у 23 (63,9 %) больных, от 2 до 4 опухолевых очагов — у 11 (30,5 %) больных, 5 и более опухолевых очагов — у 2 (5,6 %) пациентов. Опухоль размерами 3 см и менее обнаружена у 24 (66,7 %), а более 3 см — у 12 (33,3 %) больных. У всех обследованных больных диагнос тирован поверхностный РМП. При этом папиллярная опухоль, не прорастающая в собственную пластинку (стадия Та), выявлена у 9 (25 %), а наличие опухолевой инвазии в субэпителиальную основу (стадия Т1) — у 27 (75 %) пациентов. Степень дифференцировки опухоли была высокой (G-1) у 23 (63,9 %) больных, умеренной (G-2) — у 10 (27,8 %) больных, низкой (G-3) — у 5 (8,3 %) больных. Чаще всего у наблюдаемых нами пациентов мы выявляли высокодифференцированные одиночные опухоли стадии Т1 и размером до 3 см.
В раннем послеоперационном периоде после удаления уретрального катетера у всех больных отмечено учащенное, болезненное мочеиспускание в течение 1–3 суток. Макрогематурия зафиксирована у 3 больных (8,3 %) в первые сутки после операции. В дальнейшем ни у одного из пациентов макрогематурию не наблюдали. Проявлений системной токсичности фотодитазина в виде гиперемии или фотодерматита также отмечено не было.
Все пациенты находились под наблюдением по крайней мере 12 месяцев после операции, поэтому этот срок взят для анализа частоты рецидивирования РМП. Наибольший срок наблюдения на сегодняшний день составляет 18 месяцев после комбинированного лечения.
Рецидивы РМП отмечены у 4 (11,1 %) из 36 находившихся под наблюдением больных. Рецидивы РМП были выявлены при контрольных обследованиях на сроках 9 и 12 месяцев после операции. Отмечено, что рецидивирование опухолевого процесса после комбинированного лечения РМП происходило у больных с изначально множественными очагами опухоли, умеренной или низкой дифференцировкой опухолевой ткани и при опухолях большого объема. В настоящем исследовании мы не смогли выявить связь между временем экспозиции и дозой фотосенсибилизатора, с одной стороны, и вероятностью рецидива опухоли мочевого пузыря с другой. Это связано, по-видимому, с недостаточно большим количеством наблюдаемых пациентов.
Заключение
Результаты проведенного исследования показали целесообразность применения ФДТ вместе с трансуретральной резекцией при комбинированном лечении поверхностного РМП. В течение 1-го года после операции у 88,9 % пациентов не выявлено рецидивирования опухолевого процесса. Продолжение исследований в данном направлении представляется весьма перспективным.
Список литературы
1. Мартов А. Г., Сысоев П. А., Гущин Б. Я. Сравнительные резуль таты ТУР и электровапоризации при поверхностном раке мо чевого пузыря / Материалы 4й Всероссийской науч.практич. конф. 2001. С. 68–69.
2. Русаков И. Г., Быстров A. A. Хирургическое лечение, химио и иммунотерапия больных поверхностным раком мочевого пузыря // Практическая онкология. 2003. № 4. С. 214–224.
3. Чиссов В. И., Старинский В. В., Петрова Г. В. Состояние он кологической помощи населению России в 2009. М., 2010. 196 c.
4. Botteman M. F., Pashos C. L., Hauser R. S. et al. Quality of life as pects of bladder cancer: a review of the literature // Qual Life Res. 2003. Vol. 12, N 6. P. 675–688.
5. Dalbagni G. The management of superficial bladder cancer // Nat. Clin. Pract. Urol. 2007. Vol. 4, N 5. P. 254–260.
6. Dougherty T. J. Gomer C., Henderson B. et al. Photodynamic therapy [Review] // J. Natl. Cancer Inst. 1998. Vol. 90, N 12. P. 889–905.
7. Henderson B. W., Dougherty T. J. How does photodynam ic therapy work? // Photochem. Photobiol. 1992. N 55. P. 145–157.
8. Kelly J. F., Snell M. E., Berenbaum M. C. Photodynamic de struction of human bladder carcinoma // Br. J. Cancer. 1975. N 31. P. 237.
9. Kelly J. F., Snell M.E. Hematoporphyrin derivative: A possible aid in the diagnosis and therapy of carcinoma of the bladder // J. Urol. 1976. Vol. 115. P. 150–151.
10. Lindemann-Docter K., Knuchel-Clarke R. Histopathology of uro thelial carcinomas: crucial for patient management // Urologe A. 2008. Vol. 47, N 5. P. 627–638.
11. Parekh D. J., Bochner B. H., Dalbagni G. Superficial and mus cleinvasive bladder cancer: principles of management for outcomes assessments // J. Clin. Oncol. 2006. Vol. 24, N 35. P. 5519–5527.
Experience of application of photodynamic therapy in the combined treatment of superficial bladder cancer
Slesarevskaya M. N., Sokolov A. V.
Summary. The aim of the study was to evaluate the efficacy of photodynamic therapy and transurethral resection in the combined treatment of 36 patients with superficial bladder cancer. As a photosensitizer was used Photoditazine in average dose of 0.8 mg/kg body weight. Exposure time was from 12 to 48 minutes. Tumor recurrence in the first 12 months after treatment was observed in 4 (11.1%) patients, which is regarded by us as a perfectly acceptable.
Key words: superficial bladder cancer; photodynamic therapy; Photoditazine.
Опухоли мочевого пузыря бывают доброкачественными и злокачественными. По данным Всемирной организации здравоохранения, на рак мочевого пузыря приходится около 3% всех злокачественных новообразований. Среди всех онкоурологических заболеваний рак мочевого пузыря у мужчин занимает второе место по заболеваемости после злокачественных опухолей предстательной железы. Диагностику с помощью новейшей аппаратуры и лечение опухолей мочевого пузыря инновационными методами проводят в Юсуповской больнице.
Палаты оснащены притяжно-вытяжной вентиляцией и кондиционерами, что позволяет в любое время года обеспечить комфортный температурный режим. Пациенты обеспечены индивидуальными средствами личной гигиены и диетическим питанием. Все сложные случаи заболевания обсуждают на заседании Экспертного Совета. Медицинский персонал внимательно относится к пожеланиям пациентов. Повара обеспечивают диету питание при раке мочевого пузыря у мужчин. Качество пищи не отличается от домашней кухни.

Причины развития рака мочевого пузыря
Причины формирования опухолей в стенке мочевого пузыря активно изучаются врачами-онкологами. Однако современное высокоточное оборудование не позволяет в полной мере выявить патологические процессы, способствующие зарождению и прогрессированию опухоли.
Рак мочевого пузыря наиболее распространен среди мужчин, относящихся к возрастной группе от 50 до 80 лет. Многочисленные международные исследования позволили установить факторы риска развития данного заболевания:
- хронические воспалительные заболевания органов мочеполовой системы, к числу которых специалисты относят мочекаменную болезнь и цистит;
- продолжительное взаимодействие с канцерогенными веществами. Наиболее повержены развитию рака мочевого пузыря мужчины, трудовая деятельность которых связана с производством резины, текстиля, красителей и обработкой кожи, контактом с нефтепродуктами и мышьяком;
- возрастные изменения, при которых отмечается утолщение стенок мочевого пузыря, ухудшение их эластичности, вследствие чего уменьшается его емкость;
- наследственная предрасположенность;
- нарушения процессов мочеиспускания, при которых опорожнение мочевого пузыря происходит несвоевременно;
- курение, при котором канцерогенные вещества через сосуды легких проникают в кровь, которая затем распространяется и отфильтровывается почками. Результатом взаимодействия токсичных веществ со слизистой оболочкой мочевого пузыря являются изменения, которые могут перейти в злокачественный процесс.
Симптомы рака мочевого пузыря у мужчин
В самом начале заболевания клинические проявления рака мочевого пузыря скудные. Симптомы опухоли мочевого пузыря у мужчин во многом зависят от стадии болезни, наличия осложнений, сопутствующих заболеваний. Рак мочевого пузыря у мужчин характеризуется гематурией (наличием крови в моче) и расстройствами мочеиспускания.
Гематурия является наиболее ранним и самым частым и признаком рака мочевого пузыря у мужчин. В качестве первого признака болезни макрогематурия (появление крови в моче, которое можно определить визуально) отмечается примерно у 70% больных раком мочевого пузыря. Гематурия при злокачественной опухоли мочевого пузыря может быть терминальной и тотальной. Длительность и частота кровотечений из мочевого пузыря колеблются в широких пределах. Иногда гематурия бывает кратковременной, повторяется с многомесячными и даже многолетними интервалами. В ряде случаев она длится несколько дней подряд и повторяется часто. При запущенных распадающихся злокачественных новообразованиях мочевого пузыря гематурия постоянная.
Дизурия наблюдается в 15—37% случаях рака мочевого пузыря у мужчин. Она обусловлена раздражением слизистой мочевого пузыря и характеризуется следующими симптомами:
- Жжением при мочеиспускании;
- Частыми позывами на мочеиспускание;
- Поллакиурией.
В основном дизурия характерна для опухолей, которые локализуются в области шейки и инфильтративного рака. Мочеиспускание становится учащённым, и затруднённым, и болезненным. При прогрессировании опухолевого процесса у мужчин появляются постоянные боли в надлобковой области, которые усиливаются в конце мочеиспускания. Интенсивность боли зависит от расположения и характера роста опухоли. При локализации злокачественного новообразования в области шейки мочевого пузыря боль появляется рано. Экзофитные новообразования могут достигать больших размеров, не вызывая болей. Эндофитный рост опухолей сопровождается постоянной тупой болью над лоном и в полости малого таза.
Если опухоль прорастает стенки мочевого пузыря, переходит на паравезикальную клетчатку и соседние органы, у мужчин возникают симптомы тазовой компрессии:
- Отёк мошонки, нижних конечностей;
- Флебит;
- Боль в половых органах промежности, крестце, ягодицах, поясничной области.
При прогрессировании заболевания опухоль сдавливает устья мочеточников, что и определяет клинические проявления.
Диагностика рака мочевого пузыря
Цистоскопия в настоящее время проводится на завершающем этапе диагностики, когда пациенту назначается лечение. Как отдельная процедура цистоскопия выполняется только при мониторинге больных раком мочевого пузыря. Преимущественно цистоскопию совмещают с лечебно-диагностической трансуретральной резекцией мочевого пузыря.
Ультразвуковая диагностика является высокоинформативным безболезненным и абсолютно безвредный методом, который позволяет оценить состояние внутренних органов. При плановом обследовании пациентов, страдающих раком мочевого пузыря, онкологи Юсуповской больницы используют ультрасонографию. Ультразвуковое исследование позволяет оценивать опухоль по стадиям, выявлять изменения в забрюшинной и тазовой клетчатке, а также поражённые метастазами лимфоузлы. УЗИ мочевого пузыря у мужчин выполняют с помощью трансабдоминального и трансректального датчика. Проведение ультразвукового исследования только с каким-то одним из датчиков нецелесообразно.
Ошибки в оценке местного распространения рака мочевого пузыря возможны при всех видах ультрасонографии. Они могут быть вызваны наличием цистита, рубцовыми изменениями стенок мочевого пузыря вокруг опухоли, их трабекулярностью. УЗИ не позволяет с высокой степенью точности выявлять опухоли небольшого размера (менее 10 мм) и опухоли в трабекулярном мочевом пузыре. Врачи Юсуповской больницы имеют большой опыт диагностики заболеваний мочевого пузыря, проводят исследования с помощью аппаратов, имеющих высокие разрешающие способности. Это позволяет свести к минимуму количество диагностических ошибок.
С внедрением в практику внутриполостных датчиков значительно повысились диагностические возможности выявления ранних стадий рака мочевого пузыря. Трансуретральная ультрасонография (цистоэндосонография) достаточно достоверно позволяет выявлять поражение мышечного слоя. В отличие от трансабдоминальной и трансректальной ультрасонографии, цистоэндосонография делает возможным детальное изучение местного распространения опухолевого процесса даже при очень небольших размерах (меньше 5 мм) новообразования.
Онкологи Юсуповской больницы в клинической практике активно применяют такие методы диагностики, как рентгеновская компьютерная томография (КТ) и магнитно-резонансная томография (МРТ). Эти исследования проводят только после клинических, ультразвуковых, обычных рентгенологических и эндоскопических процедур, на основании данных которых формируется предварительный диагноз. КТ позволяет определить прорастание злокачественной опухоли за пределы стенки мочевого пузыря с точностью от 60 до 96%. На компьютерных томограммах нельзя отличить участки утолщения мышечной стенки мочевого пузыря от инфильтративных новообразований небольшого размера. Компьютерную томографию в основном применяют не для диагностики рака мочевого пузыря или определения степени инвазии стенки, а для выявления распространения опухолевого процесса за пределы органа и вовлеченности в опухолевый процесс лимфатических узлов.
МРТ сочетает в себе лучшие свойства ультрасонографии и компьютерной томографии. Чувствительность МРТ при распространении опухоли в клетчатку составляет 98%. МРТ, по сравнению с КТ, имеет преимущества в плане определения степени прорастания опухоли в клетчатку таза и окружающие органы. К достоинствам МРТ также относятся:
- Высокое контрастное разрешение (в 70 раз выше, чем при КТ);
- Возможность получения информационных данных по нескольким параметрам;
- Отсутствие ионизирующего излучения.
В Юсуповской больнице применяют методы ранней диагностики рака мочевого пузыря, которые основаны на тумор-ассоциированных антигенах. Имеются моноклональные антитела, специфичные для переходно-клеточного рака мочевого пузыря. Они взаимодействуют с антигенными структурами, которые присутствуют только на клетках переходно-клеточного рака мочевого пузыря и отсутствуют на клетках нормального уротелия. К ним относятся тест ВТА-Stat, ВТА-Stat и NMP22.
Тест ВТА-Stat представляет собой иммунохроматографический метод исследования. Он позволяет производить с использованием моноклональных антител быстрый специфический анализ антигена опухоли мочевого пузыря в моче. Метод прост и доступен для выполнения в амбулаторных условиях. Техника исследования проста: мочу обследуемого пациента вносят в тест-лунку, спустя 5 минут оценивают результат. Положительной проба считается в том случае, когда в окошечке появится красно-коричневая полоска.
В последние годы онкологи всё более широко используют ещё один метод раннего выявления рака мочевого пузыря – фотодинамическую диагностику. Метод основан на возможности стимуляции выработки внутриклеточного флюоресцирующего протопорфирина 9 из 5-аминолевулиновой кислоты выборочно, преимущественно в опухолевой клетке. Этот метод особенно актуальный в онкоурологии по двум причинам: в плоские опухоли мочевого пузыря практически неразличимы при эндоскопии в белом свете, определятся высокий процент резидуальных опухолей после трансуретральной резекции. Особое преимущество метода заключается в том, что все приборы, которые разработаны для флуоресцентной цистоскопии, без ограничения могут использоваться и для цистоскопии в белом свете. Их можно как угодно комбинировать с подходящими стандартными инструментами. Побочные явления в результате внутрипузырной инстилляции 5-аминолевулиновой кислоты возникают редко, и они не выраженные. Врачи Юсуповской больницы не наблюдали проявлении кожной сенсибилизации, фототоксических реакций кожи, как это случается при системно применяемых синтетических порфиринах. После процедуры 7% пациентов предъявляют жалобы на учащённое мочеиспускание.
Лечение рака мочевого пузыря у мужчин
Основным методом лечения злокачественных новообразований мочевого пузыря у мужчин является операция удаления мочевого пузыря. В большинстве случаев хирургические вмешательства дополняются иммунотерапией, химиотерапией или лучевой терапией. Все виды хирургических вмешательств у пациентов, страдающих раком мочевого пузыря, разделяют на 4 группы:
При инвазивном раке мочевого пузыря ТУР используют в качестве диагностической процедуры, позволяющей выявить степень инвазии. С паллиативной целью ТУР выполняется у больных, которые отказываются от цистэктомии или из-за наличия сопутствующих заболеваний не в состоянии перенести операцию. Целью резекции является удаление всего новообразования с участком нормальной мышечной ткани чтобы определить степень инвазии. ТУР может выполняться также под фотодинамическим контролем.
Хирургическое лечение поверхностного рака мочевого пузыря дополняется внутрипузырной иммунохимиотерапией для профилактики рецидивов и предупреждения прогрессирования опухоли. Для этой цели онкологи используют целый ряд препаратов. Все они обладают приблизительно одинаковой эффективностью. Препарат митомицин показывает более высокие результаты. Химиотерапия при раке мочевого пузыря у мужчин проводится паклитакселом, доцетакселом и гемзаром. После химиотерапии по поводу рака мочевого пузыря у мужчин выживаемость не превышает 13 месяцев.
Для иммуномодуляции при раке мочевого пузыря у мужчин используют вакцину БЦЖ. Механизм её противоопухолевого действия вакцины до конца не изучен. Многочисленные исследования показали, что в его основе лежит стимуляция клеточных механизмов иммунитета. БЦЖ вводят внутрипузырно. По эффективности она превосходит все другие препараты.
Радикальная цистэктомия является методом выбора в лечении инвазивного рака мочевого пузыря при благоприятном прогнозе, который касается продолжительности жизни пациента. Большинство урологов выполняют это вмешательство на второй и третьей стадии заболевания, при мультифокальном или быстро рецидивирующем поражении в первой стадии с гистологическими признаками низкодифференцированного роста, раке in situ (на месте), резистентном к БЦЖ терапии. В зависимости от степени прорастания околопузырной клетчатки, предстательной железы у мужчин и вовлечения в опухолевый процесс регионарных лимфатических узлов, выполняют удаление одного только мочевого пузыря или расширенную цистэктомию. По ходу операции наряду с удалением мочевого пузыря у мужчин удаляют предстательную железу с семенными пузырьками. При расширенной цистэктомии подлежат удалению тазовые лимфоузлы, прилегающая брюшина и околопузырная клетчатка.
Хирурги применяют много методик деривации (создание условий оттока) мочи после цистэктомии. Выбор способа лечения связан с возрастом пациента, соматическим статусом, тяжестью основного заболевания и наличием осложнений. Урологи применяют следующие методики деривации мочи:
- Создание артифициального мочевого пузыря;
- Пересадка мочеточников в непрерывную кишку;
- Пересадка мочеточников в изолированный сегмент кишки;
- Непосредственное дренирование почек (нефростомия или пиелостомия);
- Пересадка мочеточников на кожу;
- Трансуретероанастомоз с односторонней нефростомией.
При онкологии мочевого пузыря у мужчин продолжительность жизни зависит от вида опухоли, стадии заболевания и наличия соматической патологии, которая не позволяет применить весь спектр имеющихся в арсенале врачей методов лечения.
Лучевая терапия при раке мочевого пузыря применяется как самостоятельно, так и в сочетании с хирургическим или химиотерапевтическим лечением. Облучение осуществляется на аппаратах для дистанционной и контактной лучевой терапии. Оптимальная методика лучевой терапии выбирается в зависимости от локализации опухолевого процесса в мочевом пузыре и степени его внепузырного распространения. При онкологии мочевого пузыря у мужчин продолжительность жизни после комплексного лечения увеличивается. Прогноз выживаемости улучшается при ранней диагностике заболевания. При наличии подозрения на рак мочевого пузыря немедленно звоните по телефону.
Опухоль мочевого пузыря – новообразование, которое возникает в полости или на стенке органа. Болезнь может протекать как с яркими симптомами, так и без особых признаков, что часто приводит к поздней диагностике. По основной классификации опухоли бывают доброкачественными и злокачественными. Именно тип образования, его размеры и место определяют схему лечения опухоли мочевого пузыря и прогноз выздоровления.
Причины появления опухоли
Механизм развития опухолей заключается в активном делении клеток. Такие процессы могут быть запущены разными факторами, которые провоцируют мутацию генетического клеточного материала. В случае с мочевым пузырем особенно опасны курение, неблагоприятная экология и работа, связанная с химическими веществами. Эти факторы могут вызывать разные виды опухолей мочевого пузыря:
- Доброкачественные: полипы, папилломы, миомы, гемангиомы, фибромы.
- Злокачественные: солидный, переходноклеточный, папиллярный и плоскоклеточный рак, аденокарцинома, а также поверхностный (неинвазивный) и инвазивный рак.
Доброкачественные опухоли часто диагностируются у рабочих, занятых в лакокрасочной, бумажной, химической и резиновой промышленности. Провоцировать заболевание может застой мочи. Чем выше ее концентрация и чем дольше она задерживается в пузыре, тем более сильным оказывается опухолегенное действие веществ в ее составе. У мужчин причинами опухолей выступают заболевания мочеполового тракта:
- аденома простаты;
- простатит;
- камни в органах мочевыделительной системы;
- стриктуры и дивертикулы мочеиспускательного канала.
Ввиду особенностей анатомического строения мужчины больше подвержены риску возникновения новообразований. Злокачественные опухоли мочевого пузыря могут развиваться по тем же причинам:
- из-за работы на вредном производстве;
- паразитарных инфекций;
- длительной задержки мочи;
- инфекций и воспаления урогенитального тракта.
Симптомы опухолевых заболеваний
Рассматривая симптомы опухоли мочевого пузыря, стоит отметить, что на раннем этапе она никак себя не проявляет. Признаки возникают, когда новообразование достигает таких размеров, при которых оно может раздражать стенки органа. В такой ситуации у человека могут быть следующие жалобы:
- изменение цвета мочи;
- спазмы и боль внизу живота;
- ощущение не полностью опорожненного мочевого пузыря;
- выделение мочи небольшими порциями;
- частые позывы к мочеиспусканию;
- нарушение менструального цикла и выделения из половых путей (у женщин);
- отечность в ногах, области промежности;
- нарушения работы органов пищеварения.
Методы диагностики опухоли мочевого пузыря
Поскольку опухоль может носить доброкачественный или злокачественный характер, особое значение приобретает дифференциальная диагностика. Она направлена на то, чтобы определить тип новообразования, поскольку от этого зависит схема лечения. Исходя из этого, в инструментальную и лабораторную диагностику опухоли мочевого пузыря включают:
- Ультразвуковое исследование (УЗИ) органов малого таза.
- Магнитно-резонансную или компьютерную томографию (МРТ или КТ) малого таза.
- Цистоскопию с биопсией новообразования для определения его типа.
- Экскреторную урографию и цистографию.
- Цитологическое тестирование мочи.
Читайте также:

