Гіперпластичний синдром при гострому лейкозі не проявляється
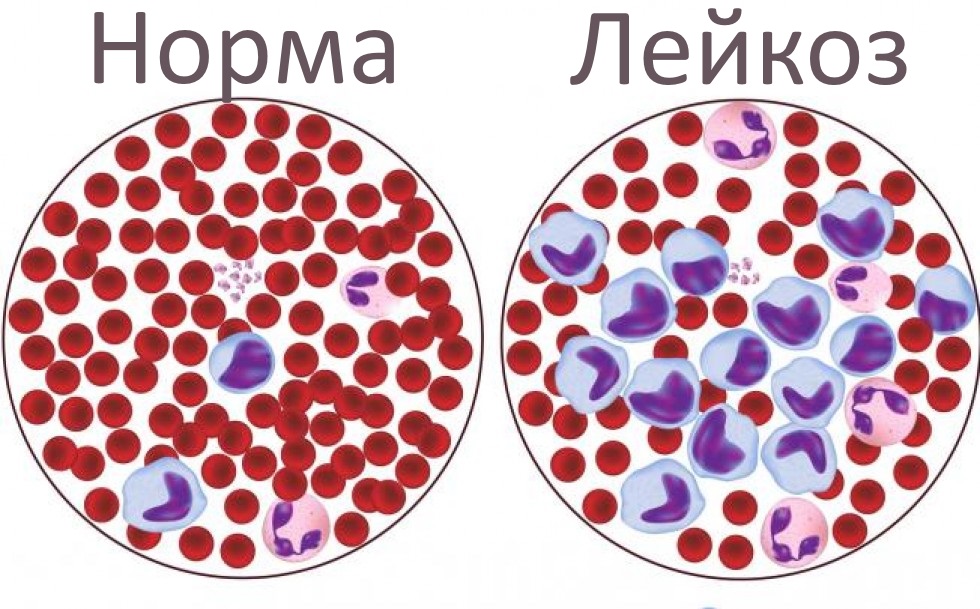
Острый лейкоз – это злокачественное заболевание с поражением костного мозга, органа кроветворения. Аномалия проявляется в мутации стволовых клеток костного мозга и появлением незрелых лимфоидных клеток, называемых лимфобластами. В крови происходит снижение тромбоцитов, лейкоцитов и эритроцитов. С прогрессированием болезни недозревшие клетки попадают в другие органы и ткани. Происходит лейкозная инфильтрация лимфоузлов, слизистых оболочек, селезенки, печени, головного мозга и др. Лейкемией, при которой чаще всего возникает гиперпластический синдром, в основном болеют дети от двух до пяти лет. Согласно статистическим данным, заболеваемость у мальчиков выше, чем у девочек. Взрослых недуг поражает в большей степени после 60 лет.
Клинические синдромы
Различные аномалии системы кроветворения в организме индивида проявляются различными симптомами и синдромами. В некоторых случаях невозможно разделить основные и второстепенные жалобы пациента, поэтому у гематологических больных разумно вместо симптомов говорить о группе признаков общего происхождения или синдромах:
- гиперпластический;
- анемический;
- геморрагический;
- инфекционно-токсический.
Причины развития лейкоза
Одним из приоритетных направлений медицинской науки является изучение проблем, связанных с лейкозами. Однако несмотря на проводимые исследования, ученые до сих пор не выявили точные причины возникновения лейкемии. Определены лишь факторы, способствующие ее развитию. К ним относится:
- Наследственная предрасположенность. Статистические данные свидетельствуют, что лейкозом болеют близкие родственники в нескольких поколениях.
- Воздействие канцерогенов. Токсичные вещества: инсектициды, удобрения, нефтепродукты, а также некоторые медикаментозные препараты (антибиотики пенициллиновой группы и цефалоспорины) негативно влияют на организм индивида.
- Инфекционные и вирусные заболевания иногда вызывают мутацию здоровых клеток, и неожиданно могут возникнуть симптомы острого лейкоза у взрослого человека.
- Наличие хромосомных патологий.
- Радиоактивное облучение, которое вызывает аномальное перерождение здоровых клеток.
- Тяжелые врожденные патологии: синдром Вискотта-Олдрича, Дауна.
- Химиотерапия. Проведение ее для лечения других заболеваний в некоторых случаях провоцирует развитие лейкемии.
- Систематическое курение.
Эти факторы только способствуют возникновению болезни, но недуг развивается и при их отсутствии.
Клинические признаки лейкемии
Общие симптомы острого лейкоза у взрослых:
- Синдром интоксикации. Характеризуется общим недомоганием, слабостью, потерей веса, лихорадкой. Последняя может возникать с присутствием в организме вирусной, бактериальной или грибковой инфекции.
- Геморрагический синдром. Появляются кровоизлияния на дерме и слизистых, рвота с кровью и дегтеобразный стул.
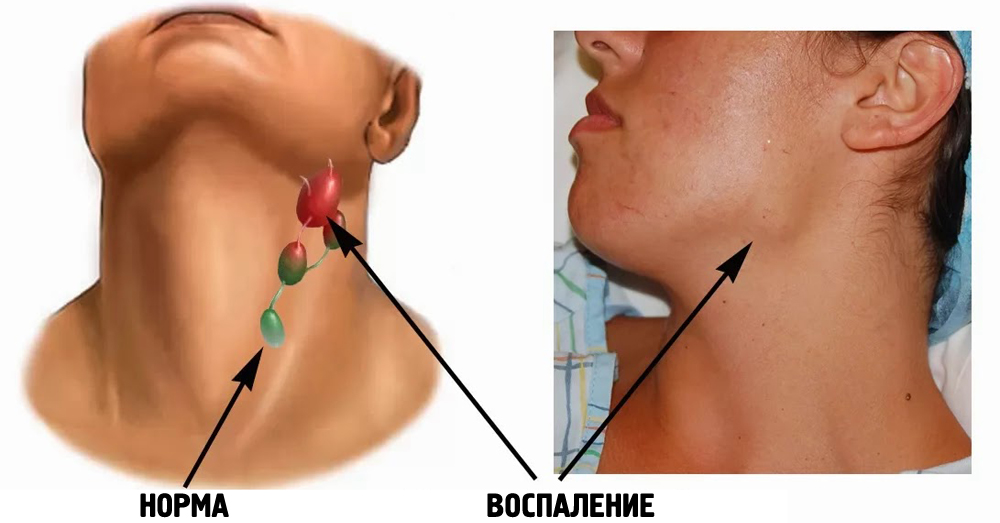
- Гиперпластический синдром. Увеличиваются все лимфоузлы, которые доступны осмотру и пальпации. Они становятся плотными, подвижными, но безболезненными даже при большом увеличении. Селезенка и печень воспаляются и увеличиваются в размерах, возникают болезненные ощущения в животе. В результате инфильтрации суставной капсулы и надкостницы, а также опухоли костного мозга, появляется боли и ломота в костях.
- Анемический синдром. В результате интоксикации кожные покровы становятся бледными, возникают синевато-красные бляшки, при легком повреждении дермы возникают панариции и паронихии, появляются язвенно-некротические изменения в ротовой полости, мучает тахикардия.
- Дыхательные нарушения. Увеличение лимфоузлов средостения приводит к сдавлению бронхов и дыхательной недостаточности.
- Изменения в органах зрения. Происходит отек зрительного нерва, появляется кровоизлияние в сетчатке глаза, возможны лейкемические бляшки на глазном дне.
Диагностика лейкемии
Для выставления диагноза необходимо:
- собрать полный анамнез заболевания;
- осмотреть больного, сделать пальпацию лимфоузлов, печени и селезенки;
- общий анализ крови – определяется количество тромбоцитов, эритроцитов и лейкоцитов, выявляются аномально измененные клетки крови;
- рентген грудной клетки – определяют увеличение периферических лимфоузлов в грудной полости, изменения вилочковой железы и состояние легких;
- аспирация и биопсия костного мозга;
- микроскопическое исследование на определение злокачественных клеток;
- спинномозговая пункция – определяется наличие раковых клеток;
- КТ – на экране компьютера просматривают состояние внутренних органов;
- МРТ – позволяет получить снимки органов и тканей;
- УЗИ – ультразвуковое исследование проводится для подтверждения увеличения печени и селезенки.
На основании комплексного обследования выставляется диагноз и назначается лечение больного.
Стадии течения заболевания
Существует три стадии течения лейкемии:
- Начальная – признаки лейкоза выражены слабо. Они проявляются в легкой усталости и сонливости. Заболевание обнаруживают случайно при профилактических обследованиях или диагностировании других заболеваний, которые в этот период начинают обостряться. Основные показатели крови при лабораторном исследовании могут быть немного изменены, размеры печени нормальные.
- Развернутая – происходит поражение различных органов, поэтому симптомы ярко выражены. В этот период происходит чередование обострений и ремиссии. Лейкоз заканчивается выздоровлением или значительным ухудшением всех показателей.
- Терминальная – лечение оказалось неэффективным, система кроветворения сильно угнетена, происходят язвенные и некротические изменения. Стадия завершается смертью больного.
Лейкемия у малышей
Острый лейкоз у детей возникает и развивается очень быстро. Количество лимфобласт ов быстро растет, что сказывается на самочувствии ребенка. Он становится вялым, жалуется на тошноту и головные боли. В вечернее время повышается температура до 38 градусов и выше, хотя симптомов простудного характера не наблюдается. При купании родители могут заметить появление на теле гематом и синяков. Этот симптом должен насторожить, если малыш не падал во время игры. Признаки недуга выражаются обострениями хронических болезней или длительном течении таких заболеваний, как пневмония, бронхит, фарингит, ангина. Они сложно поддаются лечению, ребенок вынужден продолжительный период принимать медикаменты, подрывая силы и так ослабленного организма. Кроме этого, проявляется гиперпластический синдром при остром лейкозе, выраженный стремительным увеличением лимфоузлов.

В начале заболевания чаще воспаляются шейные, далее вовлекаются подчелюстные, надключичные и подмышечные. Лимфоузлы все время увеличиваются, но не обладают болезненностью, и со временем могут вызвать сдавление бронхов, верхней полой вены, желчного протока. А также быстро происходит увеличение в размерах таких органов, как селезенка и печень, которые легко прощупываются при пальпации и выступают из-под ребер. Иногда у детей возникают желудочные, ректальные и носовые продолжительные и объемные кровотечения. Чаще всего встречается острый лейкоз у детей, поэтому родителям надо быть очень внимательными к состоянию здоровья ребенка и обращать внимание на все его недомогания и жалобы.
Лечение заболевания у детей
При подтверждении лейкемии ребенка госпитализируют в гематологическое или онкологическое отделение специализированной клиники. В результате лечения необходимо:
- уничтожить поврежденные клетки;
- проводить поддерживающую терапию;
- не допустить возникновения инфекционных болезней;
- восполнить недостаток тромбоцитов и эритроцитов крови.

Продолжительность лечения в стационаре для каждого ребенка определяется индивидуально и состоит из:
- химиотерапии – используются различные комбинации препаратов цитостатиков;
- лучевой терапии – подбирается под конкретного пациента;
- трансплантации костного мозга – возможна после проведения терапии лекарственными средствами с высокой дозировкой.
Тактика лечения определяется:
- количеством бластных клеток;
- возможностью возникновения рецидива;
- стадией болезни.
Существуют международные рекомендации (протоколы) по лечению лейкемии. Для терапии ребенка составляется длительная программа по протоколу с четким прогнозом выживаемости, интенсивность курса находится в прямой зависимости от риска рецидива заболевания. Без проведения трансплантации костного мозга, лечение лейкемии продолжается примерно два года. В этот период стационарное лечение несколько раз сменяется амбулаторным.
Этапы терапии
По международным рекомендациям, лечение лейкемии в детском возрасте состоит из следующих этапов:
- Предварительный – в этот период больного готовят для проведения основного курса. Для этого делается краткий курс химиотерапии для уменьшения количества лейкозных клеток и предупреждения сбоев в работе почек.
- Индуктивный – проводится для наступления ремиссии. Используется терапия, усиленная несколькими препаратами и продолжающаяся от полутора до двух месяцев.
- Время консолидации с интенсивной терапией – происходит закрепление достигнутой ремиссии, когда установились нормальные размеры печени и уменьшились лимфоузлы. Предотвращается развитие опухоли на головном и спинном мозге. В этот период при необходимости применяют облучение и вводят в канал спинного мозга цитостатики.
- Повторная комбинация – вводят различные комбинации сильнодействующих препаратов, проводя отдельные курсы. Период может продолжаться до нескольких месяцев. Цель – уничтожить бластные клетки.
- Поддерживающая терапия – проводится амбулаторно. Ребенок может посещать садик или школу. Дозировка препаратов сведена к минимуму.
Применение протоколов способствует повышению результативности лечения, накапливается опыт по предупреждению осложнений и выявлению побочных действий препаратов.
Дифференциальная диагностика гиперпластического синдрома
Проявления этого синдрома следует дифференцировать от:
- язвенно-некротического стоматита Венсана;
- гипертрофического гингивита другой этиологии;
- реакций при тяжелых инфекциях бактериального характера;
- инфекционного мононуклеоза;
- отравлений организма тяжелыми металлами;
- гиповитаминоза C.

Во всех этих случаях в анализе крови и миелограмме отсутствуют маркеры лейкоза. В сомнительных ситуациях проводят исследование костного мозга, в некоторых случаях мультизональное, когда на анализ берут вещество из трех точек.
Методы лечения лейкемии у взрослых
После проведенной диагностики сразу же начинается лечение, которое проводится в центрах онкологической гематологии по установленным схемам назначения лекарств. Основной задачей является восстановление здорового кроветворения, длительная ремиссия, предупреждение рецидива. Для подбора схемы лечения учитывают возраст больного, его индивидуальные особенности и количество белых телец в крови. Основные методы лечения состоят из:
Прогноз при лейкозе
На прогноз оказывают влияние следующие факторы:
- вид лейкемии;
- возраст пациента;
- особенности заболевания;
- индивидуальная реакция на химиотерапию.
У детей с лейкемией прогноз значительно лучше, чем у взрослых. Это связано с тем, что препараты, применяемые для лечения, у детей вызывают меньше побочных реакций. Кроме того, у пожилых людей имеется множество сопутствующих заболеваний, которые не позволяют проводить полноценную химиотерапию. И еще взрослые в большинстве случаев обращаются к врачу с запущенной формой болезни, когда лейкозная гиперплазия ярко выражена. По медицинской статистике, пятилетняя выживаемость при острой лейкемии у детей составляет до 85%, а у взрослых - всего до 40%. Это тяжелая, но излечимая болезнь. Современные протоколы лечения дают высокую эффективность. Надо отметить, что после пятилетней ремиссии рецидивы заболевания никогда не происходят.
Заключение
Острый лейкоз – это быстропрогрессирующая форма рака кроветворной ткани костного мозга. Происходит мутация стволовых клеток, которые разносятся по всему организму, вызывая симптомы болезни. Здоровые клетки начинают вытесняться измененными, а это сопровождается тяжелыми последствиями.
В то же время уменьшается и выработка здоровых клеток, так как наличие опухоли способствует синтезу веществ, подавляющих их рост. Протекает эта патология с поражением костного мозга, селезенки, печени, вилочковой железы и периферических лимфоузлов.
Дальнейшие исследования позволили выявили у больных с резистентной к терапии анемией, как с увеличением количества бластных клеток в костном мозге, так и без, ряд особенностей. Эти особенности касались в первую очередь морфологии костного мозга (нарушение архитектоники ростков гемопоэза, изменения стромальной ткани, признаки дисплазии кроветворных клеток). Кроме того, при выполнении цитогенетического исследования у таких больных часто выявлялись изменение кариотипа гемопоэтических клеток.
Цитогенетическими и ферментными методами была доказана клональная (опухолевая) природа заболевания. Характерной особеностью клеток, происходящих из опухолевого клона, при миелодиспластическом синдроме является их морфологическая и функциональная неполноценность.
Дальнейшие наблюдения позволили установить, что миелодиспластический синдром является неоднородной группой. У больных миелодиспластическим синдромом отмечались существенные различия в тяжести клинических проявлений, длительности течения заболевания (сроках выживаемости больных), в частоте и скорости озлокачествления заболевания — трансформации в острый лейкоз. Различия в течение заболевания требовали и различной тактики ведения больных, то есть возникла необходимость выделения самостоятельных нозологических форм.
Миелодиспластический синдром (МДС) — это группа заболеваний костного мозга, носящих клональный характер и возникающих в результате мутации стволовой клетки крови. При этом потомки мутировавшей стволовой клетки сохраняют способность к дифференцировке до зрелых клеток. Однако процесс дифференцировки носит неэффективный характер, в результате чего зрелые клетки крови изменены морфологически, уменьшены в количестве и ослаблены в функции.
Сегодня общепринятой является классификация МДС разработанная Франко-Америко-Британской исследовательской группой (FAB) и опубликованная в 1982 году. В основе классификации лежат четыре признака:
— количество бластов в костном мозге;
— количество бластов в периферической крови;
— количество атипичных (кольцевидных) сидеробластов в костном мозге;
— количество моноцитов в периферической крови.
Такой набор признаков позволяет разделить группу схожих заболеваний на самостоятельные нозологические формы (таблица 1), которые отличаются по частоте встречаемости, длительности течения, вероятности озлокачествления (трансформации в острый лейкоз) и требуют различной тактики лечения больных. Частота встречаемости различных заболеваний, выделяемых в группе МДС, длительность выживания больных и вероятность трансформации в острый лейкоз представлены в таблице 2.
Таблица 1. FAB-классификация миелодиспластического синдрома (по Bennett et al., 1982).
а) количество бластов в костном мозге менее 5%
б) количество кольцевых сидеробластов в костном мозге менее 15%
в) количество бластов в периферической крови менее 1%
г) количество моноцитов в периферической крови менее 1х10^9/л
2.Рефрактерная анемия с кольцевыми сидеробластами:
а) количество бластов в костном мозге менее 5%
б) количество кольцевых сидеробластов в костном мозге не менее 15%
в) количество бластов в периферической крови менее 1%
г) количество моноцитов в периферической крови менее 1х10^9/л
3.Рефрактерная анемия с избытком бластов:
а) количество бластов в костном мозге более 5%, но менее 20%
б) количество кольцевых сидеробластов в костном мозге менее 15%
в) количество бластов в периферической крови менее 5%
г) количество моноцитов в периферической крови менее 1х10^9/л
4.Рефрактерная анемия с избытком бластов на стадии трансформации:
а) количество бластов в костном мозге более 20%, но менее 30%
б) количество кольцевых сидеробластов в костном мозге менее 15%
в) количество бластов в периферической крови менее 1%
г) количество моноцитов в периферической крови менее 1х10^9/л
5.Хронический миеломоноцитарный лейкоз:
а) количество бластов в костном мозге менее 20%
б) количество кольцевых сидеробластов в костном мозге любое
в) количество бластов в периферической крови менее 5%
г) количество моноцитов в периферической крови не менее 1х10^9/л
Таблица 2. Частота встречаемости каждого из нозологических вариантов МДС, длительность выживания и вероятность трансформации в острый лейкоз.
частота (%) выживаемость (мес) вероятность(%)
1.Рефрактерная анемия: 25 37 11
2.Рефрактерная анемия с кольцевыми сидеробластами: 18 49 5
3.Рефрактерная анемия с избытком бластов: 28 9 23
4.Рефрактерная анемия с избытком бластов
на стадии трансформации: 12 6 48
5.Хронический миеломоноцитарный лейкоз: 17 22 20
Эпидемиология. МДС — патология старшей возрастной группы. 80% случаев МДС приходится на лиц старше 60 лет. В европейских странах среди лиц 50 — 69 лет регистрируется 40 новых случаев МДС на 1 млн населения, а среди лиц 70 лет и старше — 150 новых случаев на 1 млн населения.
Этиология. Несмотря на многочисленные исследования, причины вызывающие развитие МДС остаются во многом неясными. В группе этиологических факторов рассматривают факторы, способные вызывать мутации клеток и тем самым приводить к развитию опухоли: вирусы, ионизирующее излучение, химические агенты. На сегодняшний день каких-либо этиологических факторов, специфичных для МДС не установлено. В ряде случаев развитию МДС предшествует химиотерапия солидных опухолей.
Патогенез. Отправной точкой в развитии МДС является мутация стволовой клетки крови. Потомки мутировавшей клетки получают биологическое преимущество перед нормальными гемопоэтическими клетками, что позволяет им полностью колонизировать костный мозг, вытесняя нормальные гемопоэтические клетки. Особенностью мутации стволовой клетки крови при МДС является частичное сохранение ее потомками способности к созреванию до зрелых клеток крови. Однако, процесс созревания носит неэффективный характер, что приводит к уменьшению количества зрелых клеток в периферической крови. Кроме количественных изменений в составе клеток периферической крови имеет место и снижение их функциональной активности.
Немаловажную роль в развитии патологического клона гемопоэтических клеток играет стромальное микроокружение, однако конкретные механизмы вовлечение стромальной ткани в патологический процесс при МДС изучены еще недостаточно.
Неэффективный характер гемопоэза (дисплазия кроветворения) имеет хорошо выраженный морфологический эквивалент — изменение как морфологических признаков гемопоэтических клеток, так и их расположения внутри костномозговой полости (изменение архитектоники). Третью составляющую морфологических признаков дисплазии кроветворения образуют изменения стромальной ткани. Основные морфологические признаки дисплазии дисплазии кроветворения представлены в таблице 4 и таблице 5.
Таблица 4. Морфологические признаки дисплазии кроветворения при исследовании аспирата костного мозга (по Bartl R, Frisch B и Baumgart R, 1992).
— большие мегакариоциты с одним или несколькими мелкими круглыми ядрами
— увеличение бластных клеток
— гипо- и гипергранулярность
— базофилия цитоплазмы зрелых клеток
— эозинофилы с кольцевыми ядрами
— моноциты с множественными вытянутыми лопастями цитоплазмы
— афзурофильные гранулы в цитоплазме
Ниже представлены несколько фотографий, иллюстрирующих морфологические признаки дисплазии кроветворения.

Рисунок 1. Дисплазия эритроидного ростка в костном мозге: мегалобластоидность, асинхронность ядер, тельца Жоли.

Рисунок 2. Дисплазия мегакариоцитарного ростка в костном мозге: микромегакариоцит.

Рисунок 3. Дисплазия гранулоцитарного ростка в костном мозге: значительная редукция числа гранул.

Рисунок 4. Костный мозг больного рефрактерной сидеробластной анемией: кольцевые сидеробласты.
Таблица 5. Гистологические признаки дисплазии кроветворения при исследовании биоптата костного мозга (по Bartl R, Frisch B и Baumgart R, 1992).
Клеточность костного мозга:
— гиперклеточный (свыше 50% случаев)
— нормоклеточный (30-40% случаев)
— гипоклеточный (менее 20% случаев)
— атипичная локализация незрелых предшественников
— атипичная локализация эритроцитарных предшественников
— атипичная локализация мегакариоцитов
— интраваскулярное расположение гемопоэтических клеток
— расширение синусоидов со склерозом стенок
— интростициальный и парамегакариоцитарный фиброз
— увеличение тучных клеток
— увеличение костного преобразования
В неопластическом клоне могут происходить вторичные мутации клеток. В ряде случаев это приводит к развитию в костном мозге клона гемопоэтических клеток, потерявших способность к созреванию в большей степени, чем гемопоэтические клетки из предшествующего клона. Морфологическим эквивалентом этого события является увеличение в костном мозге количества незрелых клеток — бластов. Если количество бластов в цитологическом препарате костного мозга превышает 30%, то говорят о трансформации в острый лейкоз. При этом следует понимать, что данная ситуация не означает развитие нового (второго) заболевания, а является закономерным продолжением течения данной нозологической фомы миелодиспластического синдрома, подчиняющегося закону опухолевой прогрессии. Трансформация в острый лейкоз при МДС эквивалентна развитию бластного криза при хроническом миелолейкозе.
Клиническая картина. Клиническая картина при различных формах МДС схожа и во многом определяется показателями периферической крови. Изменения периферической крови прямо зависят от степени нарушения созревания гемопоэтических клеток. Анемия постоянный и обязательный признак. Для нее характерны гиперхромия (высокий цветовой показатель) и макроцитоз. Уровень снижения гемоглобина может варьировать от умеренного до значительного. От степени и скорости нарастания анемии будет зависеть самочувствие больного. При медленном снижении гемоглобина организм успевает адаптироваться к гипоксии и количество жалоб у больных может быть минимальным. Если анемия развивается быстро, больные предъявляют жалобы на общую слабость, утомляемость, сердцебиение, одышку. Может утяжеляться течение ишемической болезни сердца, появляются признаки сердечной недостаточности.
Снижение количества зрелых гранулоцитов (нейтропения), а также их функциональная несостоятельность влекут за собой инфекционные осложнения. У 10 % больных развиваются стоматиты, гингивиты, пневмонии, инфекция мочевыводящих путей, абсцессы различной локализации, сепсис. У 20 % больных данной группы инфекционные осложнения становятся причиной смерти. Наиболее многочислены осложнения бактериальной природы, возбудителями которых являются Escherichia coli, Pseudomonas pyocyanea, Klebsiella pneumoniae, Staphylococcus aureus и Streptococcus fecalis. Также достаточно часто тяжелые инфекционные осложнения вызываются Pneumocystic carinii, Cryptococcus neoformous, Candida albicaus, Aspergillus fumigatus и цитомегаловирусом, что связано с функциональной неполноценностью Т-лимфоцитов при МДС.
Клинически значимая тромбоцитопения (приводящая к развитию геморрагического диатеза с петехиально-пятнистым типом кровоточивости) встречается у 15 % больных МДС. У половины из них кровотечение или кровоизлияния становятся причиной смерти. В некоторых случаях МДС, как правило у больных рефрактерной анемией, может отмечаться тромбоцитоз. Проявления гиперпластического синдрома в виде спленомегалии, гепатомегалии, лимфоаденопатии и специфического поражения кожи (лейкемиды) имеют место в основном у больных ХММЛ.
Спленомегалия встречается у 17 % таких больных, гепатомегалия у 13 %, а лейкемиды у 10 %.
Диагностика.Отправной точкой диагностического поиска являются, как правило, жалобы связанные со снижением уровня гемоглобина, подкрепляемые выявлением гиперхромной, макроцитарной анемии при исследовании периферической крови. Выявление при первичном осмотре, наряду с анемическими жалобами, явлений геморрагического диатеза и/или гиперпластического синдрома позволяют сформировать представление о
В качестве вспомогательного метода диагностики может быть использовано цитогенетическое исследование кариотипа гемопоэтических клеток. Различные хромосомные поломки выявляются у 48 % больных МДС. Частота аномалий кариотипа варьирует в зависимости от нозологического варианта МДС. Так у больных РА хромосомные поломки обнаруживаются в 30 % случаев, а у больных РАИБтранс в 60 %. Выявление хромосомных аномалий имеет большое значение для определения прогноза течения заболевания.
Наиболее часто встречающимся изменением кариотипа у больных РА является делеция (утрата) части длинного плеча пятой хромосомы (5q-). Данная аномалия чаще выявляется у женщин (соотношение мужчин и женщин среди заболевших составляет 1:5). Для больных с такой хромосомной поломкой характерны ярко выраженые морфологические аномалии мегакариоцитов (микромегакариоциты), тромбоцитоз периферической крови и достаточно благоприятное течение заболевания с низкой частотой трансформации в острый лейкоз.
Диагноз складывается из морфологически подтвержденного представления о наличии у больного миелодиспластического синдрома и окончательно формулируется (нозологическая форма) на основании количественных критериев миелограммы и гемограммы (FAB-классификация):
РА — бласты костного мозга 5%, моноциты периферической крови
Виды лейкозов - острые и хронические
Анатомия и физиология костного мозга
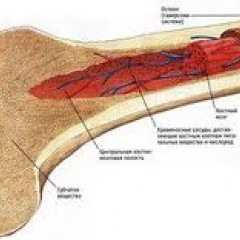
Костный мозг – это ткань находящаяся внутри костей, преимущественно в костях таза. Это самый главный орган, участвующий в процессе кроветворения (рождение новых клеток крови: эритроцитов, лейкоцитов, тромбоцитов). Этот процесс необходим организму, для того чтобы, заменить погибающие клетки крови, новыми. Костный мозг состоит из фиброзной ткани (она образует основу) и кроветворной ткани (клетки крови на разных этапах созревания). Кроветворная ткань включает 3 клеточные линии (эритроцитарный, лейкоцитарный и тромбоцитарный), по которым образуются соответственно 3 группы клеток (эритроциты, лейкоциты и тромбоциты). Общим предком этих клеток, является стволовая клетка, которая запускает процесс кроветворения. Если нарушается процесс образования стволовых клеток или их мутация, то нарушается процесс образования клеток по всем 3 клеточным линиям.
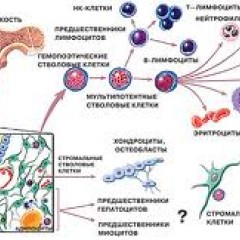
Эритроциты – это красные кровяные клетки, содержат гемоглобин, на нём фиксируется кислород, при помощи которого питаются клетки организма. При недостатке эритроцитов происходит недостаточное насыщение клеток и тканей организма кислородом, в результате чего проявляется различными клиническими симптомами.
Лейкоциты к ним относятся: лимфоциты, моноциты, нейтрофилы, эозинофилы, базофилы. Представляют собой белые клетки крови, они играют роль в защите организма и выработке иммунитета. Их недостаток вызывает снижение иммунитета и развитие различных инфекционных заболеваний.
Тромбоциты – это кровяные пластинки, которые участвуют в образовании тромба. Недостаток тромбоцитов приводит к различным кровотечениям.
Подробнее о видах кровяных клеток читайте в отдельной статье пройдя по ссылке.
Причины лейкоза, факторы риска
Симптомы различных видов лейкозов
- При острых лейкозахотмечаются 4 клинических синдрома:
- Анемический синдром: развивается из-за недостатка выработки эритроцитов, могут присутствовать множество симптомов или некоторые из них. Проявляется в виде усталости, бледности кожи и склер, головокружение, тошнота, быстрое сердцебиение, ломкость ногтей, выпадение волос, патологическое восприятие запаха;
- Геморрагический синдром: развивается в результате недостатка тромбоцитов. Проявляется следующими симптомами: вначале кровотечения из десен, образование синяков, кровоизлияния в слизистые оболочки (язык и другие) или в кожу, в виде мелких точек или пятен. В дальнейшем при прогрессировании лейкоза, развиваются и массивные кровотечения, в результате ДВС синдрома (диссеминированное внутрисосудистое свёртывания крови);
- Синдром инфекционных осложнений с симптомами интоксикации: развивается в результате недостатка лейкоцитов и с последующим снижением иммунитета, повышение температуры тела до 39 0 С, тошнота, рвота, потеря аппетита, резкое снижение веса, головная боль, общая слабость. У больного присоединяются различные инфекции: грипп, пневмония, пиелонефрит, абсцессы, и другие;
- Метастазы - по току крови или лимфы опухолевые клетки попадают в здоровые органы, нарушая их структуру, функции и увеличивая их в размере. В первую очередь метастазы попадают в лимфатические узлы, селезёнку, печень, а потом и в другие органы.
Эритробластный острый лейкоз, поражаются клетки предшественницы, из которых в дальнейшем должны развиться эритроциты. Чаще встречается в пожилом возрасте, характеризуется выраженным анемическим синдромом, не наблюдается увеличение селезёнки, лимфатических узлов. В периферической крови снижено количество эритроцитов, лейкоцитов и тромбоцитов, наличие молодых клеток (эритробластов).
Монобластный острый лейкоз, нарушается выработка лимфоцитов и моноцитов, соответственно они будут снижены в периферической крови. Клинически, проявляется, повышением температуры и присоединением различных инфекций.
Мегакариобластный острый лейкоз, нарушается выработка тромбоцитов. В костном мозге при электронной микроскопии обнаруживают мегакариобласты (молодые клетки, из которых образуются тромбоциты) и увеличенное содержание тромбоцитов. Редкий вариант, но чаще встречается в детском возрасте и обладает неблагоприятным прогнозом.
Хронический миелолейкоз, усиленное образование миелоидных клеток, из которых образуются лейкоциты (нейтрофилы, эозинофилы, базофилы), в результате чего, уровень этих групп клеток будет повышен. Долгое время может протекать бессимптомно. Позже появляются симптомы интоксикации (повышение температуры, общая слабость, головокружение, тошнота), и присоединение симптомов анемии, увеличение селезёнки и печени.
Хронический лимфолейкоз, усиленное образование клеток - предшественниц лимфоцитов, в результате уровень лимфоцитов в крови повышается. Такие лимфоциты не могут выполнять свою функцию (выработка иммунитета), поэтому у больных присоединяются различные виды инфекций, с симптомами интоксикации.
Диагностика лейкоза
- Повышение уровня лактатдегидрогеназы (норма 250 Ед/л);
- Высокий АСАТ (норма до 39 Ед/л);
- Высокая мочевина (норма 7,5 ммоль/л);
- Повышение мочевой кислоты (норма до 400 мкмоль/л);
- Повышение билирубина ˃20мкмоль/л;
- Снижение фибриногена 30%;
- Низкий уровень эритроцитов, лейкоцитов, тромбоцитов.
- Трепанобиопсия (гистологическое исследование биоптата из повздошной кости): не позволяет точно поставить диагноз, а лишь определяет разрастание опухолевых клеток, с вытеснением нормальных клеток.
- Цитохимическое исследование пунктата костного мозга: выявляет специфические ферменты бластов (реакция на пероксидазу, липиды, гликоген, неспецифическую эстеразу), определяет вариант острого лейкоза.
- Иммунологический метод исследования: выявляет специфические поверхностные антигены на клетках, определяет вариант острого лейкоза.
- УЗИ внутренних органов: неспецифический метод, выявляет увеличенные печень, селезёнку и другие внутренние органы с метастазами опухолевых клеток.
- Рентген грудной клетки: является, неспецифическим метом, обнаруживает наличие воспаления в лёгких при присоединении инфекции и увеличенные лимфатические узлы.
Лечение лейкозов
- Полихимиотерапия, применяется с целью противоопухолевого действия:
- Трансфузионная терапия: эритроцитарная масса, тромбоцитарная масса, изотонические растворы, с целью коррекции выраженного анемического синдрома, геморагического синдрома и дезинтоксикации;
- Общеукрепляющая терапия:
- применяется с целью укрепления иммунитета. Дуовит по 1 таблетке 1 раз в день.
- Препараты железа, для коррекции недостатка железа. Сорбифер по 1 таблетке 2 раза в день.
- Иммуномодуляторы повышают реактивность организма. Тималин, внутримышечно по 10-20 мг 1 раз в день, 5 дней, Т-активин, внутримышечно по 100 мкг 1 раз в день, 5 дней;
- Гормонотерапия: Преднизолон в дозе по 50 г в день.
- Антибиотики широкого спектра действия назначаются для лечения присоединяющих инфекций. Имипенем по 1-2 г в сутки.
- Радиотерапия применяется для лечения хронического лейкоза. Облучение увеличенной селезёнки, лимфатических узлов.
Использование солевых повязок с 10% солевым раствором (100 г соли на 1 литр воды). Намочить льняную ткань в горячем растворе, ткань немного сжимать, сложить в четверо, и накладывать на больное место или опухоль, закрепить лейкопластырем.
Настой из измельчённых игл сосны, сухая кожа лука, плоды шиповника, все ингредиенты смешать, залить водой, и довести до кипения. Настоять сутки, процедить и пить вместо воды.
Употреблять соки из красной свеклы, граната, моркови. Кушать тыкву.
Настой из цветков каштана: взять 1 столовую ложку цветков каштана, залить в них 200 г воды, вскипятить и оставить настаиваться на несколько часов. Пить по одному глотку на один приём, необходимо выпить 1 литр в день.
Хорошо помогает в укреплении организма, отвар из листьев и плодов черники. Кипятком примерно 1 литр, залить 5 ложек листьев и плодов черники, настоять несколько часов, выпивать всё за один день, принимать около 3 месяцев.
Читайте также:

