Этан с хлором при
Для того чтобы понять, как получить из этана хлорэтан, для начала проанализируем особенности предельного углеводорода этана.
Краткая характеристика этана
Данный углеводород имеет формулу С2Н6. Углероды в его молекуле находятся в sp3 гибридном состоянии. Это отражается на физических и химических свойствах данного вещества. При обычных условиях этан является газообразным веществом малорастворимым в воде. Как и все остальные представители класса алканов, этан имеет насыщенные простые связи. Это отражается на химических свойствах данного углеводорода. Он не способен вступать в реакции присоединения, для него допустимо только радикальное замещение.
Особенность протекания
Выясним, как получить из этана хлорэтан. Для этого необходимо провести реакцию между этаном и хлором при наличии кванта света (повышенной температуре). Благодаря гомолитическому разрыву связи образуются радикалы хлора. Для образования свободных радикалов необходима определенная затрата энергии.
Ее можно приобретать разными способами. В качестве одного из вариантов образования радикалов можно рассмотреть термический пиролиз. Чтобы из этана получить хлорэтан, уравнение записывается при температуре около 500 0 С. Той энергии, которая при этом будет выделяться, достаточно для разрыва связей. Вторым способом формирования активных радикалов является использование ультрафиолетового излучения.

Механизм реакции радикального замещения
Рассмотрим, как из этана получить хлорэтан. Уравнение реакции протекает по механизму SR-действия галогенов с алканами. В газовой фазе при реакции этана с хлором сначала происходят диссоциация хлора под действием УФ. Данную стадию называют инициированием, именно она характеризуется возникновением активных частиц-радикалов хлора. Образующиеся частицы атакуют молекулу этана, образуя хлороводород, а также радикал этил С2Н5.
Продолжим разговор о том, как получить из этана хлорэтан. На следующем этапе этильный радикал вступает во взаимодействие с молекулой хлора, образуя этанхлорид и еще один радикал хлора. Именно он способен заново вступать в реакцию, продолжая цикл цепной реакции. Данная стадия именуется ростом цепи. Количество активных радикалов на этом этапе взаимодействия не меняется, а сохраняется в полном объеме. В качестве завершения цикла выступает третий этап реакции, который называется обрывом цепи. Он подразумевает столкновения свободных частиц, в результате чего образуются продукты реакции.

Применение
Ответ на вопрос, как получить из этана хлорэтан. Остановимся на применении. Получаемый хлорэтил является серьезным наркотическим веществом. Его применяют в качестве наркоза при хирургических операциях. Достаточно двух-трех секунд для того, чтобы свести к минимуму двигательную активность.
В качестве основного недостатка данного вещества отметим возможность передозировки. Даже незначительное увеличение допустимой нормы вызывает серьезные проблемы для организма человека. В наши дни хлорэтан лишь в некоторых случаях применяют в качестве наркотического вещества.
В большей степени он востребован в качестве местного средства для кратковременного поверхностного обезболивания кожного покрова. Попадая на кожу, вещество испаряется, происходит переохлаждение кожи, понижается ее чувствительность, в результате чего возникает возможность проводить разрезы, то есть, осуществлять незначительные поверхностные операции.
Также данное вещество применяют для снижения кожного зуда, лечения термических ожогов, нейромиозитов, криотерапии воспаления. Ампулу сначала нагревают в ладони, затем направляют струю на кожу. Для лечебных целей процедура проводится один раз в день 7-10 дней.
Мы приступаем к новому разделу - органической химии. Совершенно необязательно (и даже преступно по отношению к собственному времени!) знать наизусть, зубрить свойства органических веществ.
По мере изучения вы поймете, что свойства вещества определяются его строением, и научитесь легко предсказывать ход реакций ;)
В этой связи особый интерес представляет теория химического строения, которая была создана А.М. Бутлеровым в 1861 году. Она включает в себя несколько основных положений:
- Атомы в молекуле соединены в определенной последовательности, в соответствии с их валентностью. Порядок связи атомов отражает химическое строение.
- Зная свойства веществ, можно установить их химическое строение, и наоборот, зная строение вещества можно сделать вывод о его свойствах.
- Атомы или группы атомов оказывают взаимное влияние друг на друга непосредственно или через другие атомы
- Свойства вещества зависят от количественного и качественного состава, а также от химического строения молекулы

Алканы (парафины) - насыщенные углеводороды, имеющие линейное или разветвленное строение, содержащие только простые связи. Относятся к алифатическим углеводородам, так как не содержат ароматических связей.
Алканы являются насыщенными соединениями - содержат максимально возможное число атомов водорода. Общая формула их гомологического ряда - CnH2n+2.
Номенклатура (от лат. nomen - имя + calare - созывать) - совокупность названий индивидуальных химических веществ, а также правила составления этих названий. Названия у алканов формируются путем добавления суффикса "ан": метан, этан, пропан, бутан и т.д.

Гомологами называют вещества, сходные по строению и свойствам, отличающиеся на одну или более групп CH2
Перечисленные выше алканы, являются по отношению друг к другу гомологами, то есть составляют один гомологический ряд (греч. homólogos - соответственный).
Названия алканов формируются по нескольким правилам. Если вы знаете их, можете пропустить этот пункт, однако я должен познакомить читателя с ними. Итак, алгоритм составления названий следующий:
- В структурной формуле вещества необходимо выбрать самую длинную (пусть и изогнутую на рисунке!) цепь атомов углерода
- Атомы выбранной цепи нумеруют, начиная с того конца, к которому ближе разветвление (радикал)
- В начале название перечисляют радикалы и другие заместители с указанием номеров атомов углерода, с которыми они связаны. Если в молекуле имеется несколько одинаковых радикалов, то цифрой указывают нахождение каждого из них в главной цепи и перед их названием соответственно ставят частицы ди-, три-, тетра- и т.д.
- Основой названия служит наименование предельного углеводорода с тем же количеством атомов углерода, что и в главной цепи
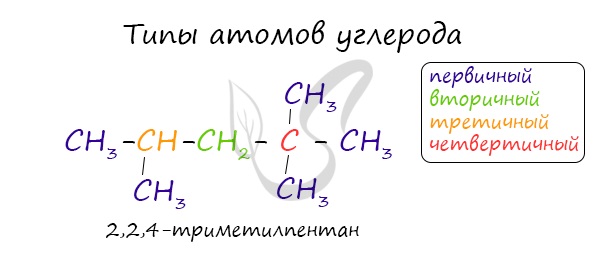
Внимательно изучите составленные для различных веществ названия ниже.

В углеводородной цепочке различают несколько типов атомов углерода, в зависимости от того, с каким числом других атомов углерода соединен данный атом. Различают первичные, вторичные, третичные и четвертичные атомы углерода.
Изомерами (греч. isomeros - составленный из равных частей) называют вещества, имеющие одну молекулярную формулу, но отличающиеся по строению (структурная изомерия) или расположению атомов в пространстве (пространственная изомерия).
Изомерия бывает структурной (межклассовая, углеродного скелета, положения функциональной группы или связи) и пространственной (геометрической, оптической). По мере изучения классов органических веществ вы узнаете о всех этих видах.

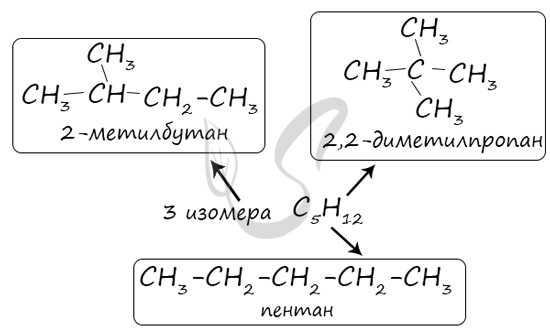
В молекулах алканов отсутствуют функциональные группы, кратные связи. Для алканов возможна изомерия только углеродного скелета. Так у пентана C5H12 существует 3 структурных изомера.
Некоторые данные, касающиеся алканов, надо выучить:
- В молекулах алканов присутствуют одиночные сигма-связи (σ-связи), длина которых составляет 0,154 нм
- Тип гибридизации атомов углерода - sp 3
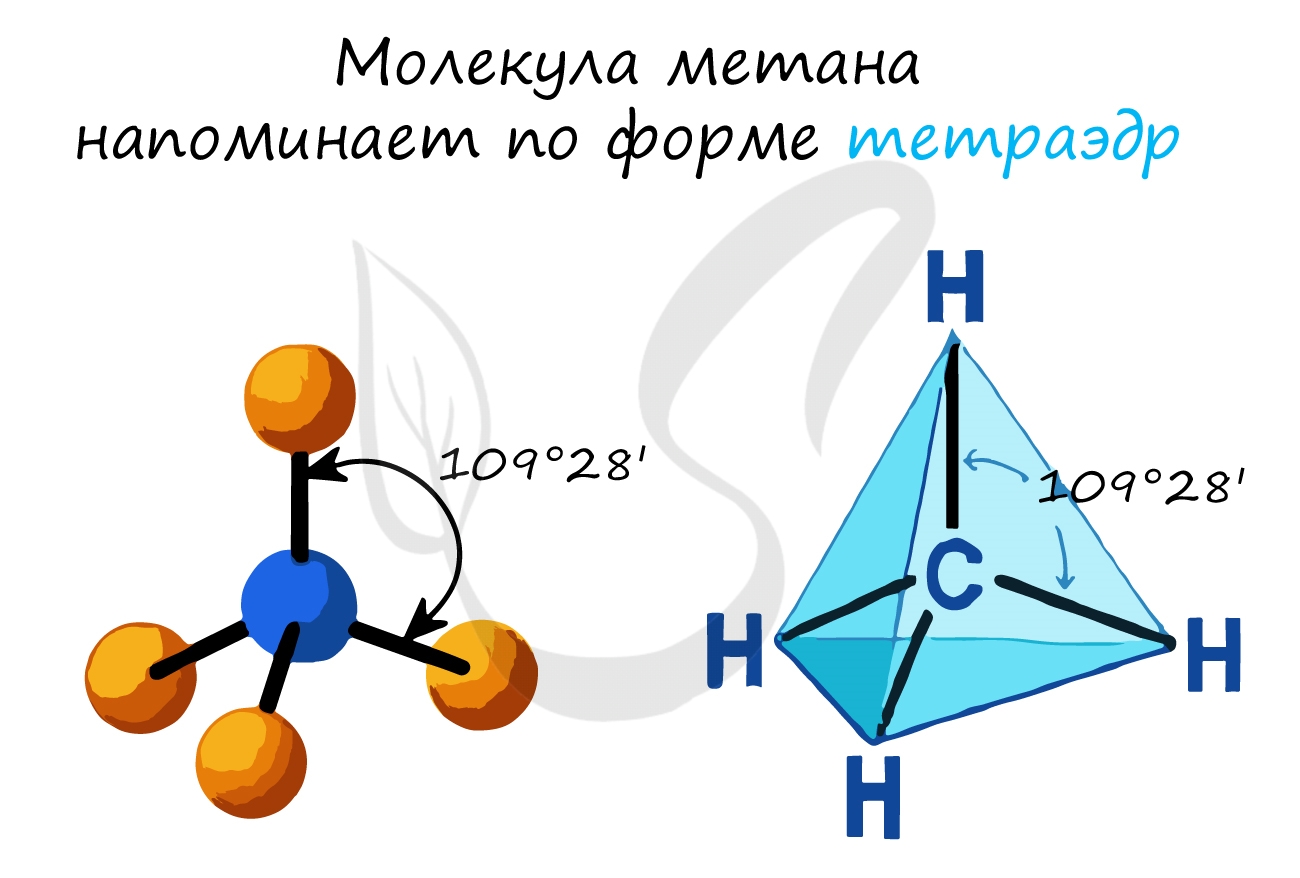
- Валентный угол (между химическими связями) составляет 109°28'
Алканы входят в состав природного газа: метан 80-97%, этан 0.5-4%, пропан 0.2-1.5% , бутан 0.1-1%, пентан 0-1%. Состав нефти нельзя выразить одной формулой, он непостоянен и зависит от месторождения.
В состав нефти входят алканы с длинными углеродными цепочками, например: C8H18, C12H26. Путем крекинга из нефти получают алканы.

В промышленности алканы получают путем:
-
Крекинга нефти
В ходе крекинга нефти получается один алкан и один алкен.
Гидрогенизацией угля (торфа, сланца)
Гидрированием оксида углерода II
В лабораторных условиях алканы получают следующими способами:
-
Синтез Дюма
Данный синтез заключается в сплавлении соли карбоновой кислоты с щелочью, в результате образуется алкан.

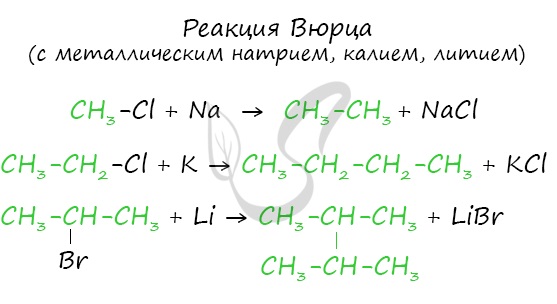
Эта реакция заключается во взаимодействии галогеналкана с металлическим натрием, калием или литием. В результате происходит удвоение углеводородного радикала, рост цепи осуществляется зеркально: в том месте, где находился атом галогена.
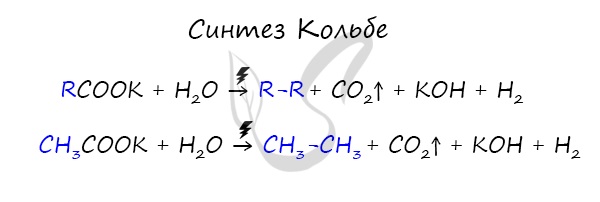
В результате электролиза солей карбоновых кислот может происходить образование алканов.
В результате разложения карбида алюминия образуется метан и гидроксид алюминия.
Гидрированием ненасыщенных углеводородов
Алканы - насыщенные углеводороды, не вступают в реакции гидрирования (присоединения водорода), гидратации (присоединения воды). Для алканов характерны реакции замещения, а не присоединения.
-
Галогенирование
Атом галогена замещает атом водорода в молекуле алкана. Запомните, что легче всего идет замещение у третичного атома углерода, чуть труднее - у вторичного и значительно труднее - у первичного.

Реакции с хлором на свету происходят по свободнорадикальному механизму. На свету молекула хлора распадается на свободные радикалы, которые и осуществляют атаку на молекулу углеводорода.

Реакция Коновалова заключается в нитровании алифатических (а также ароматических) соединений разбавленной азотной кислотой. Реакция идет при повышенном давлении, по свободнорадикальному механизму.
Для удобства и более глубокого понимания, азотную кислоту - HNO3 - можно представить как HO-NO2.

Все органические вещества, в их числе алканы, сгорают с образованием углекислого газа и воды.
В ходе каталитического, управляемого окисления, возможна остановка на стадии спирта, альдегида, кислоты.
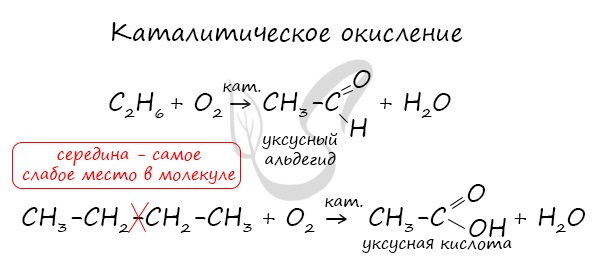
Пиролиз (греч. πῦρ - огонь + λύσις - разложение) - термическое разложение неорганических и органических соединений. Принципиальное отличие пиролиза от горения - в отсутствии кислорода.
В реакциях, по итогам которых образуются изомеры, используется характерный катализатор AlCl3.
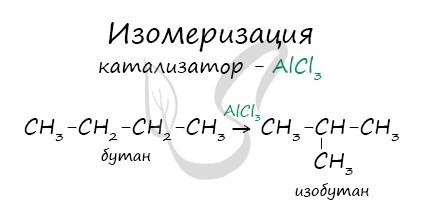
Вам уже известно, что в результате крекинга образуется один алкан и один алкен. Это не только способ получения алканов, но и их химическое свойство.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.

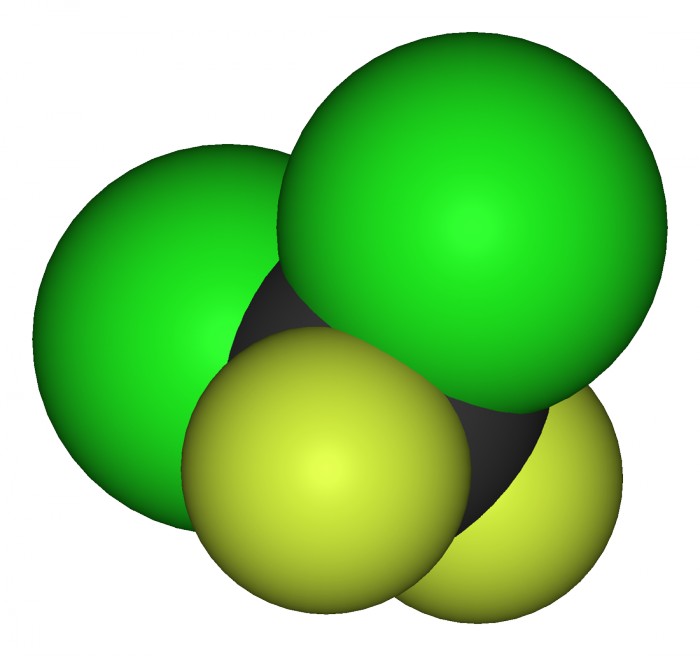
Осталась ещё одна группа соединений - те. которые имеют связь галоген-углерод. Некоторые из них довольно инертны и используются как растворители (хлороформ и дихлорметан), а некоторые - реакционноспособны, токсичны и даже опасны.
Я начну с монозамещённых соединений. Они получаются (в довольно жётских условиях) при реакции алканов с галогеном. При использовании фтора условия становятся жёсткими сами по себе: из-за зашкаливающей активности фтора реакция проходит со взрывом. Хлор - классический пример, но реакция редко бывает селективной - в той или иной степени будут образовываться продукты многократного замещения
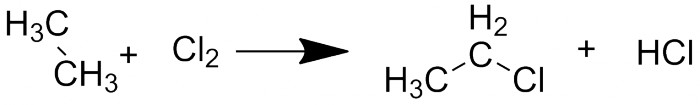
Реакция алканов с галогенами на примере этана и хлора.
Другой, более щадящий способ - реакция спиртов с соответствующими кислотами (вернее, с самим хлороводородом или бромоводородом). Реакция обратима, но происходит с отщеплением воды, поэтому при использовании водоотнимающих реакгентов (например, серной кислоты) удаётся получить нужное соединение с хорошим выходом. Это тоже классическая реакция, которую пишет во всех учебниках и проводят во всех практикумах. Я уже писал о ней в статье про спирты.
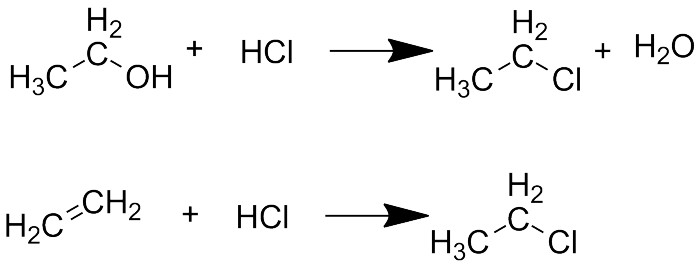
Реакция этанола с хлороводородом и присоединение хлороводорода к этилену
Третий способ - присоединение к алкенам (гидрогалогенирование) - похож на предыдущий. При этом образуется галогеналкан, но присоединение может идти двумя путями с образованием разных соединений. При этом в обычных условиях галоген присоединяется к наиболее замещённому атому углерода, а водород идёт к менее замещённому (то есть тому, у кого больше водородов - как говорилось в школе: "деньги - к деньгам"). Это называется правилом Марковникова. Есть, однако, способы провести присоединение и строго против правила Марковникова.
Надо сказать, что и здесь, и в дальнейшем теория, рассказываемая в учебниках, заметно расходится с практикой, поэтому рекомендую за примерами обращаться к практикумам. Многие реакции (используемые в промышленности) проходят в жёстких условиях и требуют высокого давления, температуры и/или специальных катализаторов - всё это особая наука, на которую тратят свои усилия тысячи не самых глупых людей.
Монозамещённые галогеналканы (или алкилгалогениды, что то же самое) являются выраженными электрофилами: они присоединяются к нуклеофилам (аминам, спиртам, тиолам) с отщеплением галогенводорода. Это можно назвать основным их применением: с их помощью можно конструировать или модифицировать молекулы. Важно знать, что активность растёт в ряду I>Br>Cl>>F, то есть иодпроизводные активно вступают в реакции, а фторопроизводные практически нереакционноспособны.
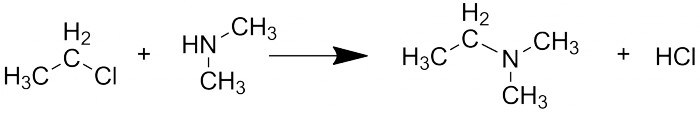
Реакция с нуклеофилами на примере диметиламина.
Нуклеофилы существуют не только в колбах, но и в живых организмах, поэтому активные алкилгалогениды токсичны. Особенно этим славится метилиодид, который вдобавок ещё и крайне летуч.
При реакции метана с хлором получаются все четыре возможных соединения: метилхлорид, дихлорметан, хлороформ и тетрахлорметан (четырёххлористый углерод). В промышленности каждое из веществ затем выделяют перегонкой - чем больше галогенов в молекуле, тем выше температура кипения (а метилхлорид - газ при н.у.). Дихлорметан, хлороформ и ЧХУ используют в основном как растворители, реже - как реагенты. Гомолог дихлорметана - дихлорэтан - также является широко распространённым растворителем. Аналогичные производные более тяжёлых галогенидов (дибромметан, дииодметан, бромоформ и пр.) слишком реакционноспособны и используются гораздо реже.
Галогеналканы легко испаряются и практически негорючи, поэтому их используют в качестве хладагента в холодильниках, ("фреон" - торговая марка для всего семейства хладагентов). Некоторые из таких соединений приведены на рисунке.
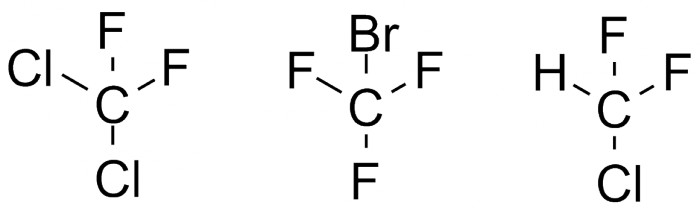
Известная проблема фреонов - их разрушающее действие на озоновый слой, но у новых фреонов оно гораздо слабее. Также все они в той или иной степени токсичны, но это не идёт ни в какое сравнение с применявшимся раньше в этих целях аммиаком.
Большинство галогеналканов не только негорючи, но и активно подавляют горение. В частности, в огнетушителях раньше можно было встретить бромэтан или четырёххлористый углерод. Сейчас на замену им пришли фторированные соединения, в частности Novec 1230 (называемый кое-где "сухой водой").
Хлороформ когда-то использовался как средство для наркоза, но сейчас он вытеснен более безопасными альтернативами - при длительном воздействии хлороформ токсичен для печени.

На нашем сайте собрано более 100 бесплатных онлайн калькуляторов по математике, геометрии и физике.

Основные формулы, таблицы и теоремы для учащихся. Все что нужно, чтобы сделать домашнее задание!

Не можете решить контрольную?!
Мы поможем! Более 20 000 авторов выполнят вашу работу от 100 руб!
Характеристики и физические свойства этана
Не имеет вкуса. Не растворим в воде. Проявляет слабое наркотическое действие.
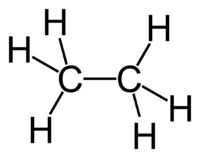
Рис. 1. Строение молекулы этана.
Таблица 1. Физические свойства этан.
Плотность (20 o С), кг/м 3
Температура плавления, o С
Температура кипения, o С
Получение этана
В больших объемах этан получают из попутного нефтяного газа и газов нефтекрекинга.
В лабораторных условиях этан получают следующими способами:
— гидрированием непредельных углеводородов
— по реакции щелочного плавления солей одноосновных органических кислот
— взаимодействием галогеналканов с металлическим натрием (реакция Вюрца)
Химические свойства этана
В обычных условиях этан не реагирует с концентрированными кислотами, расплавленными и концентрированными щелочами, щелочными металлами, галогенами (кроме фтора), перманганатом калия и дихроматом калия в кислой среде.
Для этана наиболее характерны реакции, протекающие по радикальному механизму. Энергетически более выгоден гомолитический разрыв связей C-H и C-C, чем их гетеролитический разрыв.
Все химические превращения этана протекают с расщеплением:
- cвязей C-H
- галогенирование (SR)
- дегидрирование
- связей C-H и C-C
- окисление
Применение этана
Этан используется как сырье в химической промышленности в основном для получения этилена.
Примеры решения задач
| Задание | Определите массу хлора, необходимого для хлорирования по первой стадии 4,5 л этана. |
| Решение | Запишем уравнение реакции хлорирования этана: |
Найдем количество вещества этана:
Согласно уравнению реакции n(C2H6) : n(Cl2) = 1:1, значит,количество моль хлора равно:
Тогда, масса хлора будет равна (молярная масса – 71 г/моль):
| Задание | Рассчитайте объемы хлора и этана, приведенные к нормальным условиям, которые потребуются для получения дихлорэтана массой 10,5 г. |
| Решение | Запишем уравнение реакции хлорирования этана до дихлорэтана (реакция происходит под действием УФ-излучения): |
Рассчитаем количество вещества дихлорэтана (молярная масса равна – 99 г/моль):
По уравнению реакции найдем количество вещества хлора. n(C2H4Cl2) : n(Cl2) = 1:2, т.е. n(Cl2) = 2 × n(C2H4Cl2) = 2 × 0,12 = 0,24 моль. Тогда объем хлора будет равен:
Алканы – это предельные углеводороды, содержащие только одинарные связи между атомами С–С в молекуле, т.е. содержащие максимальное количество водорода.
Алканы – предельные углеводороды, поэтому они не могут вступать в реакции присоединения.
Для предельных углеводородов характерны реакции:
- разложения,
- замещения,
- окисления.
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для алканов характерны только радикальные реакции.
Алканы устойчивы к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагируют с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения.
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование.
Алканы реагируют с хлором и бромом на свету или при нагревании.
При хлорировании метана сначала образуется хлорметан:

Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:

| Химическая активность хлора выше, чем активность брома, поэтому хлорирование протекает быстро и неизбирательно. |
При хлорировании алканов с углеродным скелетом, содержащим более 3 атомов углерода, образуется смесь хлорпроизводных.
Например, при хлорировании пропана образуются 1-хлорпропан и 2-хлопропан: |
Бромирование протекает более медленно и избирательно.
Реакции замещения в алканах протекают по свободнорадикальному механизму.
Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат неспаренный электрон.
Первая стадия. Инициирование цепи.
Под действием кванта света или при нагревании молекула галогена разрывается на два радикала:

Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом.
Вторая стадия. Развитие цепи.
Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород.
При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с новой нераспавшейся молекулой хлора:

Третья стадия. Обрыв цепи.
При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами, образуя молекулы, радикальный процесс обрывается.
Могут столкнуться как одинаковые, так и разные радикалы, в том числе два метильных радикала:

1.2. Нитрование алканов.
Алканы взаимодействуют с разбавленной азотной кислотой по радикальному механизму, при нагревании до 140 о С и под давлением. Атом водорода в алкане замещается на нитрогруппу NO2.
При этом процесс протекает также избирательно.
С третичный–Н > С вторичный–Н > С первичный–Н
2. Реакции разложения.
2.1. Дегидрирование и дегидроциклизация.
Дегидрирование – это реакция отщепления атомов водорода.
В качестве катализаторов дегидрирования используют никель Ni, платину Pt, палладий Pd, оксиды хрома (III), железа (III), цинка и др.
Уравнение дегидрирования алканов в общем виде:
При дегидрировании алканов, содержащих от 2 до 4 атомов углерода в молекуле, разрываются связи С–Н у соседних атомов углерода и образуются двойные и тройные связи.
Например, п ри дегидрировании этана образуются этилен или ацетилен:  |
При дегидрировании бутана под действием металлических катализаторов образуется смесь продуктов. Преимущественно образуется бутен-2:

Если бутан нагревать в присутствии оксида хрома (III), преимущественно образуется бутадиен-1,3:

Алканы с более длинным углеродным скелетом, содержащие 5 и более атомов углерода в главной цепи, при дегидрировании образуют циклические соединения.
При этом протекает дегидроциклизация – процесс отщепления водорода с образованием замкнутого цикла.
Пентан и его гомологи, содержащие пять атомов углерода в главной цепи, при нагревании над платиновым катализатором образуют циклопентан и его гомологи:

Алканы с углеродной цепью, содержащей 6 и более атомов углерода в главной цепи, при дегидрировании образуют устойчивые шестиатомные циклы, т. е. циклогексан и его гомологи, которые далее превращаются в ароматические углеводороды.
Гексан при нагревании в присутствии оксида хрома (III) в зависимости от условий может образовать циклогексан и потом бензол:


Гептан при дегидрировании в присутствии катализатора образует метилциклогексан и далее толуол:

2.2. Пиролиз (дегидрирование) метана .
При медленном и длительном нагревании до 1500 о С метан разлагается до простых веществ:

Если процесс нагревания метана проводить очень быстро (примерно 0,01 с), то происходит межмолекулярное дегидрирование и образуется ацетилен:
Пиролиз метана – промышленный способ получения ацетилена.
2.3. Крекинг.
Крекинг – это реакция разложения алкана с длинной углеродной цепью на алканы и алкены с более короткой углеродной цепью.
Крекинг бывает термический и каталитический.
Термический крекинг протекает при сильном нагревании без доступа воздуха.
При этом получается смесь алканов и алкенов с различной длиной углеродной цепи и различной молекулярной массой.
Каталитический крекинг проводят при более низкой температуре в присутствии катализаторов. Процесс сопровождается реакциями изомеризации и дегидрирования. Катализаторы каталитического крекинга – цеолиты (алюмосиликаты кальция, натрия).
3. Реакции окисления алканов.
Алканы – малополярные соединения, поэтому при обычных условиях они не окисляются даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.).
3.1. Полное окисление – горение.
Алканы горят с образованием углекислого газа и воды. Реакция горения алканов сопровождается выделением большого количества теплоты.
Уравнение сгорания алканов в общем виде:
При горении алканов в недостатке кислорода может образоваться угарный газ СО или сажа С.
Например, горение пропана в недостатке кислорода:
Промышленное значение имеет реакция окисления метана кислородом до простого вещества – углерода:
Эта реакция используется для получения сажи.
3.2. Каталитическое окисление.
- Каталитическое окисление бутана – промышленный способ получения уксусной кислоты:

- При каталитическом окислении метана кислородом возможно образование различных продуктов в зависимости от условий проведения процесса и катализатора. Возможно образование метанола, муравьиного альдегида или муравьиной кислоты:

- Важное значение в промышленности имеет паровая конверсия метана: окисление метана водяным паром при высокой температуре.

4. Изомеризация алканов.
Под действием катализатора и при нагревании неразветвленные алканы, содержащие не менее четырех атомов углерода в основной цепи, могут превращаться в более разветвленные алканы.
Читайте также:

