Эффективность адриамицина при раке щитовидной железы
Синонимы: Adriablasfin, Doxorubicin.

Адриамицин получен в Италии из культуры лучистого грибка Streptomyces peucetius var. cuesius, по химическому строению он отличается от рубомицина тем, что вместо водорода у 14-го углеродного атома имеется гидроксильная группа. Следовательно, он является 14гидроксирубомицином. Так же как и рубомицин, при слабом кислотном гидролизе адриамицин распадается на аминосахар и агликон.
Несмотря на такое малое различие в структуре, оказалось, что адриамицин отличается от рубомицина по спектру противоопухолевого действия, в связи с чем была высказана гипотеза о связи между структурой и активностью этой группы антибиотиков.
Предполагается, что кардиотоксичность адриамицина и рубомицина связана с эффектом аминосахара даунозамина, а противоопухолевый эффект обусловлен хромофорной частью молекулы.
ингибируя профазу в малых дозах и блокируя митоз в больших. Препарат более значительно угнетает синтез ДНК, чем синтез РНК. Синхронизированные клетки чувствительнее к действию адриамицина в фазах S и G2 митотического цикла. В экспериментах на животных показано усиление противоопухолевого эффекта адриамицина в комбинации с метотрексатом или имидазол-карбоксамидом (DTIC).
Наибольшую опасность при длительном введении адриамицина животным представляет развитие "лекарственного миокардита". Оказалось, что нет существенных различий в морфологии повреждения сердца при введении адриамицина и рубомицина: диффузный отек, расширение сосудов, диссоциация волокон, потеря эозинофилии в миофибриллах и т. д. В механизме этого эффекта установлена роль агликоновых метаболитов этих препаратов. Предполагается аутоиммунный характер этих повреждений. В последнее время появились сообщения о положительном эффекте ЭДТА (этилендиаминотетраацетат) и ICRF-159 [1,2-ди(3,5-диоксопиперазин-1) пропан] для предупреждения кардиотоксичности у экспериментальных животных (Bachur, 1973) .
После однократного внутривенного введения меченого адриамицина в дозе 8 мг/кг он быстро переходит из крови в паренхиматозные органы, а затем медленно выводится. Его концентрация в печени, почках, селезенке в 70 раз, а в сердце и легких в 10 раз превышает концентрацию в крови, мозге и опухоли (солидная саркома-180). Адриамицин подвергается превращениям в организме, в частности имеет место образование агликона адриамицинона, наибольшее накопление которого происходит в сердце и легких. Кинетика распределения и выведения адриамицина и рубомицина во многом подобна (Arena е. а., 1972).
У человека отмечено быстрое уменьшение содержания адриамицина в крови с появлением метаболитов; период полураспада в плазме для адриамицина составляет 16,7 ч, а для смеси его метаболитов - 31,7 ч. Выведение адриамицина и его метаболитов с мочой составляет 5% (Di Fronzo, 1973; Bachur, 1973).
Рубомицин с мочой выводится за тот же срок в значительно большем количестве (25% от введенной дозы). Эти результаты дают основание считать, что при недостаточной функции почек адриамицин в отличие от рубомицина может быть введен в полной дозе. Основное количество адриамицина выделяется с желчью, в связи с чем у больных с нарушением функции печени отмечается значительное увеличение содержания антибиотика и его метаболитов в плазме и возрастает при этом токсичность лекарства (Benjamin, 1974).
При всех гистологических типах лимфом адриамицин эффективен у 40% больных; его применение в комбинациях с другими препаратами увеличивает процент успешного лечения до 70-90.
Используются комбинации: адриамицин+блеомицин+преднизолон; адриамицин 4- циклофосфан + винкристин + преднизолон; адриамицин + эмбихин + блеомицин 4- винкристин 4- преднизолон.
При лимфогранулематозе объективный эффект получен у 37-44% больных. В рандомизированном исследовании комбинация адриамицин + блеомицин + винбластин + имидазол-карбоксамид дала такой же процент полных ремиссий, как и комбинация МОПП (эмбихин, винкристин, натулан, преднизолон) без перекрестной резистентности при рецидивах.
При применении комбинации адриамицин + винкристин +натулан + преднизолон по схеме двухнедельного лечения (3-6 циклов) у 16 больных II- IV стадии лимфогранулематоза полные ремиссии получены в 44%, частичные - в 56% случаев (Maiolini, 1972).
полные ремиссии могут быть достигнуты у 11-38% больных (Tan е. а., 1973), при остром миелобластном лейкозе - у 7-33%. Mathe е. а. (1972) получили ремиссии у 38% больных (из 63) при лимфобластном лейкозе и у 30% (из 27) при остром миелолейкозе. Эти данные сходны с результатами применения рубомицина. Включение адриамицина в различные комбинации повышает число успешно леченых больных. Bonadonna е. а. (1972) отмечают 64% полных ремиссий при остром лимфолейкозе при применении комбинации адриамицин + винкристин + преднизолон. Добавление цитозин-арабинозида увеличивает число полных ремиссий до 85%.

можно применять как один адриамицин, так и комбинации его с другими препаратами. Адриамицин вызывает уменьшение метастазов в кожу и мягкие ткани, легкие, печень, кости; объективный эффект наблюдается у 26-37% больных. Следует отметить, что эти результаты получены в основном при применении антибиотика у больных, ранее леченных другими препаратами; при использовании адриамицина у больных, прежде не получавших химиотерапию, объективный эффект был получен в 70% случаев (из 23 больных) (Gottlieb е. а., 1973). Комбинированная химиотерапия адриамицином и винкристином с преднизолоном или без него вызывала объективный эффект у 80 и 76% больных соответственно (Brambilla е. а., 1974).
- 17% из 314 больных (Gottlieb, 1973). Эти данные послужили основанием для дополнительного изучения возможности применения адриамицина в комбинированной химиотерапии мелкоклеточного рака легкого.
Выраженный объективный эффект при применении антибиотика может быть получен у больных с метастазами злокачественных опухолей яичка различного гистологического строения (Monfardini е. а., 1972).
было успешным у 65% больных (Gottlieb е. а., 1973); при нейробластоме - у 50% больных как при использовании одного адриамицина, так и при комбинации адриамицин-|-винкристин4-ЦИклофосфан (Gasparini е. а., 1974).
Имеются сообщения о чувствительности к адриамицину рака щитовидной железы и мочевого пузыря (Bonadonna, 1974), однако они нуждаются в дополнительной проверке.
составляет 22%, при множественной миеломе - 30-40%, при раках желудочно-кишечного тракта-22%, при саркомах мягких тканей и костей -от 10 до 40%. У больных саркомой Юинга полная или частичная регрессия опухоли может быть получена в 42% случаев. Cortes и соавт. (1972) описали объективную регрессию у 41% больных с метастазами остеогенной саркомы в легкие.
(в 46% случаев), при этом наибольший успех (53%) отмечен у больных с метастазами синовиальной саркомы (Н. И. Переводчикова, В. А. Горбунова, 1976). При остеогенной саркоме положительный результат получен у 41,5% больных. Достигнутый эффект усиливается и сохраняется проведением повторных курсов лечения. У некоторых больных повторные курсы необходимы для получения ремиссии (В. А. Горбунова и др., 1973).
Применение адриамицина в комбинации с имидазолкарбоксамидом дает регрессию опухолей у больных с диссеминированными саркомами мягких тканей в 42,5 /0 случаев, при добавлении в схему винкристина - у 48,5% больных (Gottlieb, 1974).
Антибиотик изучают как средство для предупреждения метастазов после ампутаций при остеогенноп саркоме, после операции и лучевой терапии - при саркоме Юинга.
При первоначальном изучении препарат вводили внутривенно по 0,4-0,8 мг/кг ежедневно или через день 3-4 раза с повторением курсов через 4-7 дней. В дальнейшем предпочтение было отдано коротким режимам с использованием высоких разовых доз: по 30 мг/м2 ежедневно
3 дня подряд с перерывом между курсами 3 нед или по 60-75 мг/м2 однократно с повторением введений 1 раз в
4 нед. Эти режимы, а также продолжительный режим применения препарата (по 30 мг внутривенно 2 раза в неделю в течение 2,5-3 нед) могут быть рекомендованы для практического применения.

проявляется как в виде непосредственных, так и отсроченных реакций: тошнота и рвота, стоматит, диарея, анорексня, алопеция, угнетение кроветворения, боли в области сердца, временное ухудшение ЭКГ, флебиты, дерматиты, аллергические реакции и кумулятивная кардиотоксичность. При введении антибиотика в подкожную клетчатку появляются воспаление, некроз и последующий фиброз. (профилактика побочных действий при помощи фотостима. )
Частота побочных явлений зависит от разовых и суммарных доз препарата и режима лечения; при возникновении непосредственных побочных реакций значение имеет интенсивность курса химиотерапии. Тошнота и рвота при коротких курсах отмечаются у 59% больных, при продолжительных - у 21 % больных, анорексия - у 32 и 9% соответственно.
Угнетение гемопоэза проявляется в виде лейкопении, тромбоцитопения и анемии, которые бывают значительными у больных, прежде получавших лучевое лечение или химиотерапию. При коротких режимах лечения это осложнение встречается у 60% больных, при продолжительных курсах -у 32% больных.
Изменения на ЭКГ, наблюдающиеся у 17-20% больных, во время химиотерапии (снижение зубца Т и интервала S-7\ преимущественно в грудных отведениях, тахикардия) не являются опасными и ликвидируются после окончания курса или при отмене лекарства.
Серьезным осложнением, представляющим опасность для жизни больных, является кумулятивная кардиальная токсичность, зависящая от суммарной дозы адриамицина. Симптомами поражения сердца при этом являются: одышка, боли в области сердца, снижение артериального давления, быстрое развитие сердечно-сосудистой недостаточности с рефрактерностью к сердечным гликозидам. Для того чтобы избежать появление этого осложнения, необходимо ограничивать общую дозу адриамицина за несколько курсов 500 мг/м2.
Рост волос возобновляется через VI2-2 мес после окончания химиотерапии. Аллергическая сыпь, появляющаяся в некоторых случаях сразу же посте применения препарата, не нарастает при повторных введениях и чаще всего исчезает самостоятельно.
являются тяжелые заболевания сердца и печени, а также значительные лейко- и тромбоцитопении (лейкоциты ниже 3-Ю3 в 1 мкл и тромбоциты ниже 10-104 в 1 мкл крови). Ослабленным и больным со сниженными резервами кроветворения и с сопутствующими болезнями печени при незначительном нарушении ее функции может быть рекомендован режим продолжительных курсов химиотерапии адрнамнцином (в сниженных дозах).
во время курсов и в течение 3 нед после коротких и 2 нед посте продолжительных курсов.
в отдельном флаконе прилагается растворитель (вода для инъекций). Адриамицин растворяют в растворителе или изотоническом растворе хлорида натрия.
БАД "Фотостим" предназначен для:
- онкологических больных, имеющих злокачественные опухоли разных стадий;
- лиц с риском перерождения доброкачественных дерматозов (родинок, бородавок, папиллом) и предраковых состояний (лейкоплакий, дисплазивных очагов) в онкологические заболевания;
- лиц пожилого возраста для повышения сопротивляемости организма онкологическим заболеваниям;
- лиц, перенесших тяжелые хирургические, лучевые, химиотерапевтические* воздействия, в реабилитационный период для скорейшего восстановления организма;
- кроме того, "фотостим" рекомендуется к применению лицами с ослабленным иммунитетом.
Показания к применению фотостима.Существует несколько показаний для применения "Фотостима" : Механизм действия фотостима."Фотостим" усиливает гуморальный иммунитет в 60-70% случаев за счет роста популяции лимфоцитов, а в 30-40% случаев - популяции нейтрофилов в крови. Стимуляция клеточного иммунитета при употреблении "Фотостима" достигается за счет роста абсолютного количества фагоцитов а у 35% лиц также и за счет роста активности фагоцитов и NK-клеток. NK-клетки активируются под влиянием дисплазивных (аномальных) клеток, бактерий, их токсинов или продуктов метаболизма. В целом, " Фотостим" специфически стимулирует пролиферацию клонов В-клеток костного мозга и продукцию вилочковой железы. "Фотостим" стимулирует формирование антител к опухолевым клеткам, активирует регенерацию пораженных тканей и, таким образом, увеличивает продолжительность жизни (или предотвращает ее сокращение) и значительно улучшает качество жизни онкологических больных. Кроме того, во многих случаях тормозится рост первичного очага опухоли и предотвращается появление метастазов. "Фотостим" способен не только тормозить рост опухолей но и уничтожать предшественников раковых клеток - дисплазивные (аномальные) клетки. Образно выражаясь, фотостим является "разведывательно-диверсионной группой", задачей которой является обнаружение врага - клеток, отличающихся от нормальных, передача информации в центр (в мозг) и осуществление скоординированных мероприятий по их уничтожению. Клинические исследования фотостима.Клинические исследования показали, что "Фотостим" :
"ФОТОСТИМ" Его уникальность заключается в том, что 1) Онкологическая клетка поглощает фотосенсибилизатор, например, "ФОТОСТИМ".
2) Орган освещается светом. Онкологическая клетка погибает.
Заключение института Геронтологии. Анализ полученных результатов свидетельствует о том, ВЫВОДЫ (фрагмент из заключения института геронтологии): "Фотостим" оказывает положительное влияние Заболеваемость раком щитовидной железы в мире: Факторами риска возникновения рака щитовидной железы являются: А). Повышение продукции тиреотропного гормона гипофиза Б). Ионизирующая радиация В). Снижение продукции ТТГ Д). Правильны все ответы Е). Правильны ответы А) и Б) К экзогенным модифицирующим факторам возникновения рака щитовидной железы относят: 1). Ультрафиолетовое излучение 2). Ионизирующее излучение 3). Недостаток поступления в организм йода 4). Избыток поступления в организм йода 5). Применение антитиреоидных препаратов 6). Применение адреноблокаторов К наиболее часто встречающимся морфологическим формам рака щитовидной железы относятся: А). Папиллярная аденокарцинома Б). Фолликулярная аденокарцинома В). Медуллярный рак Г). Плоскоклеточный и недифференцированный рак Медуллярный рак щитовидной железы развивается из: Г). Любой вышеуказанной Частота высокодифференцированных аденокарцином щитовидной железы составляет: Частота медуллярного рака щитовидной железы составляет: 1). Рак щитовидной железы, выявленный только на аутопсии 2). Опухоль малых размеров, выявленная только при УЗИ, без клинических проявлений 3). Наличие метастазов опухоли в лимфоузлы шеи без клинических признаков первичной опухоли 4). Наличие метастаза опухоли в легкое без клинических признаков первичной опухоли Г). Верно все, кроме 4 При медуллярном раке щитовидной железы в крови отмечается: А). Повышение уровня ТТГ Б). Повышение уровня кальцитонина В). Повышение уровня раково-эмбрионального антигена Г). Повышение уровня тиреоидных гормонов Наиболее часто метастазами рака щитовидной железы поражаются: А). Лимфоузлы вдоль внутренней яремной вены А). Появление узлового образования в щитовидной железе, особенно с бугристой поверхностью и плотной консистенцией у человека старше 35 лет Б). Ускоренный рост, уплотнение и появление бугристости ранее существовавшего узлового или диффузного зуба В). Появление без болезненных лимфатических узлов на боковой и передне-боковой поверхности шеи Г). Появление затруднения питания и осиплости голоса у здорового ранее человека Д). Правильно а) и в) Е). Все ответы верные Для медуллярного рака щитовидной железы характерно: В). Синдром Сиппла Г). Все вышеперечисленное Функция щитовидной железы при раке: Г). Все ответы возможны Для диагностики рака щитовидной железы применяются: А). Пункция узлового образования щитовидной железы Б). Пункция увеличенных лимфоузлов шеи В). Изучение уровня Т3,Т4, ТТГ Г). Открытая биопсия узлового образования щитовидной железы Д). Правильно все, кроме Г) В). Метод не информативен При оперативном лечении рака левой доли щитовидной железы у женщины 25 лет в нижнем полюсе правой доли обнаружено узловое образование 7-8 мм. Показано: А). Срочное цитологическое исследование пунктата узла правой доли Б). Левосторонняя гемиструмэктомия с удалением перешейка и резекцией правой доли В). Срочная биопсия узла правой доли Г). Тотальная тиреоидэктомия Самостоятельными методами радикального лечения рака щитовидной железы являются: Г). Все перечисленные Минимально допустимой операцией при высокодифференцированном раке щитовидной железы в I и II стадиях является: А). Внекапсулярное удаление пораженной доли щитовидной железы с перешейком Б). Тотально-субтотальная тиреоидэктомия В). Резекция пораженной доли Г). Энуклеация опухолевого узла При дифференцированном раке щитовидной железы III стадии и недифференцированном раке показано: А). Тотальная тиреоидэктомия Б). Лучевая терапия В). Лучевая терапия затем тиреоидэктомия Г). Химиотерапия затем тиреоидэктомия Десятилетнее выздоровление при дифференцированном раке щитовидной железы достигается у: У больного 55 лет медуллярный рак щитовидной железы T3N1M0. Ему наиболее целесообразно: А). Выполнить тиреоидэктомию с фасциально-футлярным иссечением клетчатки шеи Б). Провести комбинированное лечение с предоперационной дистанционной лучевой терапией на I этапе с последующей тиреоидэктомией и фасциально-футлярным иссечением клетчатки шеи В). Провести комбинированное лечение с предоперационной дистанционной лучевой терапией с последующим лечением радиоактивным йодом Г). Провести самостоятельный курс лучевой терапии по радикальной программе Больному 55 лет произведена гемитиреоидэктомия с резекцией перешейка по поводу аденоматоза щитовидной железы. В двух узлах – фолликулярная аденома. В одном (размером в 1см) – папиллярный рак. Ему следует назначить: А). Повторную операцию – в объеме тиреоидэктомии Б). Профилатическую лучевую терапию В). Профилактическую химиотерапию Г). Лечение радиоактивным йодом Химиотерапия наиболее эффективна: А). При папиллярном раке щитовидной железы Б). При фолликулярном раке щитовидной железы В). При низкодифференцированном раке щитовидной железы Г). Эффективность не зависит от морфологической структуры Эффективность адриамицина при раке щитовидной железы составляет: 1. Заболеваемость раком щитовидной железы в мире: 2. Факторами риска возникновения рака щитовидной железы являются: А). Повышение продукции тиреотропного гормона гипофиза Б). Ионизирующая радиация В). Снижение продукции ТТГ Д). Правильны все ответы Е). Правильны ответы А) и Б) 3. К экзогенным модифицирующим факторам возникновения рака щитовидной железы относят: 1). Ультрафиолетовое излучение 2). Ионизирующее излучение 3). Недостаток поступления в организм йода 4). Избыток поступления в организм йода 5). Применение антитиреоидных препаратов 6). Применение адреноблокаторов 4. К наиболее часто встречающимся морфологическим формам рака щитовидной железы относятся: А). Папиллярная аденокарцинома Б). Фолликулярная аденокарцинома В). Медуллярный рак Г). Плоскоклеточный и недифференцированный рак 5. Медуллярный рак щитовидной железы развивается из: Г). Любой вышеуказанной 6. Частота высокодифференцированных аденокарцином щитовидной железы составляет: 7. Частота медуллярного рака щитовидной железы составляет: 1). Рак щитовидной железы, выявленный только на аутопсии 2). Опухоль малых размеров, выявленная только при УЗИ, без клинических проявлений 3). Наличие метастазов опухоли в лимфоузлы шеи без клинических признаков первичной опухоли 4). Наличие метастаза опухоли в легкое без клинических признаков первичной опухоли Г). Верно все, кроме 4 9. При медуллярном раке щитовидной железы в крови отмечается: А). Повышение уровня ТТГ Б). Повышение уровня кальцитонина В). Повышение уровня раково-эмбрионального антигена Г). Повышение уровня тиреоидных гормонов 10. Наиболее часто метастазами рака щитовидной железы поражаются: А). Лимфоузлы вдоль внутренней яремной вены А). Появление узлового образования в щитовидной железе, особенно с бугристой поверхностью и плотной консистенцией у человека старше 35 лет Б). Ускоренный рост, уплотнение и появление бугристости ранее существовавшего узлового или диффузного зуба В). Появление без болезненных лимфатических узлов на боковой и передне-боковой поверхности шеи Г). Появление затруднения питания и осиплости голоса у здорового ранее человека Д). Правильно а) и в) Е). Все ответы верные 12. Для медуллярного рака щитовидной железы характерно: В). Синдром Сиппла Г). Все вышеперечисленное 13. Функция щитовидной железы при раке: Г). Все ответы возможны 14. Для диагностики рака щитовидной железы применяются: А). Пункция узлового образования щитовидной железы Б). Пункция увеличенных лимфоузлов шеи В). Изучение уровня Т3,Т4, ТТГ Г). Открытая биопсия узлового образования щитовидной железы Д). Правильно все, кроме Г) В). Метод не информативен 16. При оперативном лечении рака левой доли щитовидной железы у женщины 25 лет в нижнем полюсе правой доли обнаружено узловое образование 7-8 мм. Показано: А). Срочное цитологическое исследование пунктата узла правой доли Б). Левосторонняя гемиструмэктомия с удалением перешейка и резекцией правой доли В). Срочная биопсия узла правой доли Г). Тотальная тиреоидэктомия 17. Самостоятельными методами радикального лечения рака щитовидной железы являются: Г). Все перечисленные 18. Минимально допустимой операцией при высокодифференцированном раке щитовидной железы в I и II стадиях является: А). Внекапсулярное удаление пораженной доли щитовидной железы с перешейком Б). Тотально-субтотальная тиреоидэктомия В). Резекция пораженной доли Г). Энуклеация опухолевого узла 19. При дифференцированном раке щитовидной железы III стадии и недифференцированном раке показано: А). Тотальная тиреоидэктомия Б). Лучевая терапия В). Лучевая терапия затем тиреоидэктомия Г). Химиотерапия затем тиреоидэктомия 20. Десятилетнее выздоровление при дифференцированном раке щитовидной железы достигается у: 21. У больного 55 лет медуллярный рак щитовидной железы T3N1M0. Ему наиболее целесообразно: А). Выполнить тиреоидэктомию с фасциально-футлярным иссечением клетчатки шеи Б). Провести комбинированное лечение с предоперационной дистанционной лучевой терапией на I этапе с последующей тиреоидэктомией и фасциально-футлярным иссечением клетчатки шеи В). Провести комбинированное лечение с предоперационной дистанционной лучевой терапией с последующим лечением радиоактивным йодом Г). Провести самостоятельный курс лучевой терапии по радикальной программе 22. Больному 55 лет произведена гемитиреоидэктомия с резекцией перешейка по поводу аденоматоза щитовидной железы. В двух узлах – фолликулярная аденома. В одном (размером в 1см) – папиллярный рак. Ему следует назначить: А). Повторную операцию – в объеме тиреоидэктомии Б). Профилатическую лучевую терапию В). Профилактическую химиотерапию Г). Лечение радиоактивным йодом 23. Химиотерапия наиболее эффективна: А). При папиллярном раке щитовидной железы Б). При фолликулярном раке щитовидной железы В). При низкодифференцированном раке щитовидной железы Г). Эффективность не зависит от морфологической структуры 24. Эффективность адриамицина при раке щитовидной железы составляет:
Спонсором приза зрительских симпатий выступила компания BioVitrum. Несомненно, XXI век — время развития научно-технического прогресса. Вместе с совершенствованием технологий приходит и их доступность в повсеместном использовании. Медицина не является исключением. Благодаря развитию технологий диагностики и лечения самых разных заболеваний мы стали спасать тех пациентов, которые когда-то входили в число неизлечимых. Однако не на все сферы медицины прогресс повлиял так положительно. Поэтому сегодня мы бы хотели познакомить вас с такими животрепещущими вопросами медицины, как гипердиагностика и гиперлечение. Сейчас мы остановимся лишь на одной, но весьма значимой стороне данной проблемы — гипердиагностика узлов щитовидной железы, а также гиперлечение этих узлов и рака щитовидной железы. Что мы знаем сегодня про узлы щитовидной железы?Однако то, что эта проблема была озвучена совсем недавно, не значит, что о ней больше не надо писать. Мы не хотим загружать вас медицинской терминологией, вновь писать о TI-RADS и разбирать по кусочкам, что может написать функциональный диагност в заключении. Мы обращаемся к вам в качестве потенциальных пациентов и хотим донести мысль, что не всегда узел в щитовидной железе опасен, а рак априори смертелен. База, с которой нам нужно познакомиться: щитовидная железаНемножко о щитовидной железе (ЩЖ). Это орган эндокринной системы человека, который располагается на передней поверхности шеи в области гортани, прямо перед щитовидным хрящом. Состоит железа из левой и правой долей и перешейка. ЩЖ богато кровоснабжается разными артериями, а иннервируется гортанными нервами. Главной функцией щитовидной железы (лат. glandula thyroidea) является синтез тиреоидных гормонов, необходимых нашему организму. Под тиреоидными гормонами мы подразумеваем два соединения: тироксин (Т4) и трийодтиронин (Т3). Основной функцией Т4 и Т3 является увеличение потребления клетками кислорода. Иначе говоря, эти гормоны стимулируют все энергетические процессы в клетке и обмен веществ, причем их влияние распространяется на все клетки организма. Также клетки ЩЖ производят кальцитонин, ответственный за обмен кальция в организме. Прямо за щитовидной железой располагаются четыре небольшие паращитовидные железы. Последние производят паратиреоидный гормон, который также отвечает за поддержание уровня кальция в организме, причем в большей степени, чем кальцитонин. Откуда берется столько случаев рака щитовидки?Рак щитовидной железы (РЩЖ) — наиболее распространенное злокачественное новообразование эндокринной системы [2]. Все чаще мы слышим, что заболеваемость РЩЖ неуклонно растет. И звучит это ужасающе, однако так ли всё просто на самом деле? Возможно, вы будете шокированы, какая правда скрывается за этими, на первый взгляд, однозначными научными фактами. И прежде, чем мы разберемся с истинной причиной роста заболеваемости РЩЖ, необходимо ознакомиться с тем, какие виды рака щитовидки существуют. Итак, начнем. Сейчас нам понадобится привести немного численных данных, но не пугайтесь их, всё крайне просто. В научном сообществе выделяют пять типов РЩЖ:
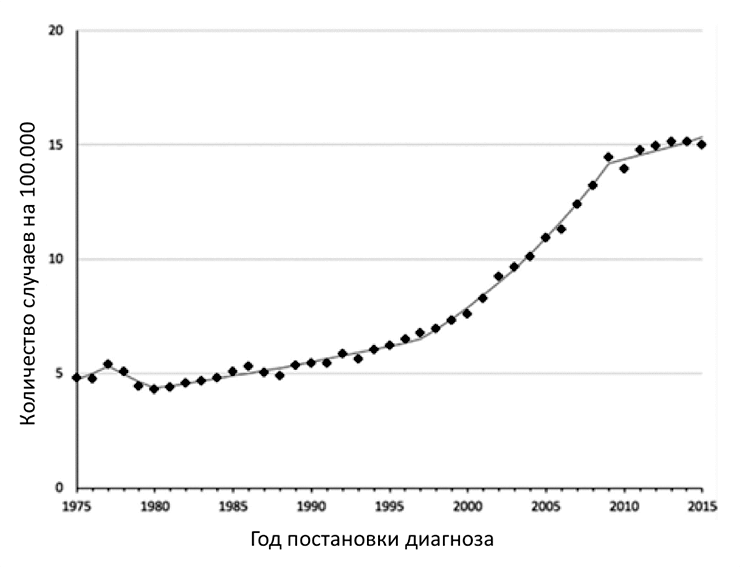
Наиболее благоприятными принято считать два первых типа РЩЖ. И как мы можем заметить, они встречаются наиболее часто. Их также называют высокодифференцированными типами рака. Медуллярный, низкодифференцированный и недифференцированный типы считаются агрессивными формами РЩЖ. В нашей статье мы сделаем акцент лишь на первых двух типах РЩЖ, так как они являются наиболее распространенными. Что касается рака — если клетки, из которых состоит опухоль, являются высокодифференцированными, в большинстве случаев врачи считают исход благоприятным. Однако если опухоль состоит из низкодифференцированных клеток, то с большой вероятностью она склонна к агрессивному течению. Как уже было сказано, наиболее часто выявляемые РЩЖ являются высокодифференцированными. Папиллярный РЩЖ — наиболее распространенная форма: 80–85%. И с самым хорошим прогнозом. Пятилетняя выживаемость пациентов с РЩЖ — 98,1% [2]. Что это значит для пациента? Что наиболее часто выявляемые случаи РЩЖ имеют благоприятный исход! Рак, ушедший в себяПодбираемся к корню проблемы: статистика и диагностикаВернемся к распространенности РЩЖ. Теперь мы готовы понять, что возросшее число случаев данной патологии не является поводом для беспокойства. В 1975 году заболеваемость РЩЖ составляла 4,9 на 100 000 человек и оставалась относительно стабильной до начала 1990-х годов [6]. За последние 25 лет заболеваемость РЩЖ выросла более чем в 3 раза, то есть на 300% (рис. 1) [7], [8], причем в большинстве случаев за счет высокодифференцированного папиллярного РЩЖ. При этом очень важно понимать, что, несмотря на такой значительный рост, смертность от РЩЖ остается стабильной, примерно 0,5 случаев на 100 000 человек [6].
Рисунок 1. Данные заболеваемости раком щитовидной железы в период с 1975 по 2015 годы Чувствуете, что тут что-то не так? Нет связи между возросшим числом случаев РЩЖ и смертностью от этой патологии! Среди врачей и ученых до сих пор продолжаются дебаты, почему так происходит. Сейчас выделяют несколько теорий. Наиболее вероятная — широкое распространение методов ультразвуковой диагностики (УЗИ). Пусть корни УЗИ уходят к Леонардо да Винчи и XV веку, широкое медицинское распространение данный метод получил с 50-х годов XX века [9], [10]. Сегодня УЗИ является наиболее простым, дешевым, неинвазивным и информативным методом выявления опухолевых образований щитовидной железы. Поэтому, как вы можете догадаться, УЗИ стали делать почти всем, причем независимо от показаний. Сейчас научное сообщество активно дискутирует на тему, связаны ли такие показатели с истинным увеличением заболеваемости РЩЖ, или же проблема в гипердиагностике тех небольших образований ЩЖ, которые не требуют никакого вмешательства со стороны человека [11], [12]. Для более полного понимания проблемы вернемся на чуть более ранний этап диагностики РЩЖ. Что такое узлы и как их найти?Узлы ЩЖ — это радиологически различимые объемные образования в ЩЖ, которые могут быть доброкачественными и злокачественными. Узлы можно найти в 50% случаев всех проводимых УЗИ ЩЖ. При этом только 5% выявляемых образований будут злокачественными [13], [14]. Весомый вклад УЗИ в возросшее количество диагностированных узлов и РЩЖ можно показать на примере одного нашумевшего исследования в Южной Корее [3], [15], [16]. В 1999 году там была утверждена национальная программа, направленная на скрининг злокачественных заболеваний. Под программу попала и щитовидная железы. В результате повсеместного внедрения УЗИ щитовидки частота выявления рака выросла в 15 (!) раз с 1993 по 2011 год. И это мы еще не говорим просто об узлах, которые также могут быть психологической проблемой пациента. Большинство выявляемых случаев — папиллярный РЩЖ. Как вы помните, этот вид рака имеет весьма благоприятный исход. Однако простому населению идея жить с раком настолько чужда и неприятна, что было проведено огромное число полного удаления щитовидных желез, причем часто без видимой на то необходимости! А такая операция имеет серьезные последствия, о которых мы расскажем чуть ниже. Врачи, осознав свою ошибку, убрали УЗИ щитовидки из списка обязательных скрининговых тестов. И результат не заставил себя ждать. В последней на эту тему публикации 2015 года сказано, что на 30% снизилась заболеваемость РЩЖ, а число операций на щитовидной железе снижалось на 35% ежегодно. Вывод напрашивается сам собой: в основе увеличения числа диагностированных случаев узлов щитовидки (в том числе и РЩЖ) является ставшее таким доступным УЗИ. Думаем, следует также сказать, что образования ЩЖ выявляются не только при выполнении УЗИ, но и при использовании других методов лучевой диагностики (КТ, МРТ, ПЭТ), что стало возможным благодаря улучшению разрешающей способности оборудования. Следовательно, увеличилось чисто случайно выявляемых образований щитовидной железы (в том числе, рака) — инциденталóм (от англ. incidence — случайность) [17]. Инциденталомы клинически никак себя не проявляют и могут оставаться в организме бессимптомно всю жизнь. И многие из таких инциденталом обнаруживались лишь посмертно, случайно, и не являлись причиной кончины человека. Это позволяет говорить нам о существовании резервуара пациентов с узлами или раком щитовидной железы, который клинически является скрытым и никак себя не проявляет до его случайного обнаружения [18]. Приведенные данные обобщены на рисунке 2.
Рисунок 2. Что даст нам УЗИ щитовидки на самом деле? рисунок авторов статьи Напомним, что в нашей статье мы делаем акцент на наиболее распространенных типах РЩЖ (папиллярный, фолликулярный). Агрессивные формы РЩЖ (медуллярный, низкодифференцированный, недифференцированный и редко папиллярный) требуют дальнейшего более детального изучения Самое главное: почему гипердиагностика и гиперлечение РЩЖ являются проблемой?В связи с выявленным фактом, что в оперативном лечении таких РЩЖ, вполне возможно, нет необходимости (а ведь удаление ЩЖ сопровождается серьезными последствиями, о чем мы расскажем далее), с 2015 года в США уже принимаются меры по снижению частоты гипердиагностики и гиперлечения [24]. Например, уже настоятельно рекомендовано не проходить скрининг РЩЖ пациентам, у которых нет никаких симптомов, поскольку выявление агрессивных типов рака в этом случае крайне маловероятно. Что врачи думают о данной проблеме?Проблема гиперлечения РЩЖ существует не только среди пациентов, но и среди медицинского сообщества. Конечно, выбор, удалять ли щитовидную железу или нет, стоит больше перед пациентом, нежели перед лечащим врачом. И пациент вполне может выбрать хирургическую тактику лечения. А врач должен определять, сколько ткани щитовидной железы в конкретном случае нужно убирать. В качестве уменьшения гипердиагностики Американская тиреоидологическая ассоциация рекомендует воздержаться от скрининга и биопсии мелких образований щитовидной железы при отсутствии на то иных клинических симптомов [6]. Как вообще лечат рак щитовидной железы?Давайте разберемся, какие существуют пути лечения РЩЖ [26].
Почему мы, авторы, так не хотим, чтобы щитовидную железу удаляли без серьезных на то причин? Казалось бы, мы уберем орган, где сидит рак, и будем жить себе спокойно, только лишь принимая препараты гормонов щитовидной железы. Это ведь лучше, чем жить с раком. Или все-таки нет? Так вот, сама сложность вопроса заключается в операции. Чем чревато полное удаление щитовидки (или, как говорят врачи, тотальная тиреоидэктомия)?Существует два серьезных осложнения тотальной тиреоидэктомии [27].
Какой существует выход?Одним из наиболее перспективных выходов из ситуации является частичное удаление ткани ЩЖ, а именно поврежденной доли. В таком случае пациент, во-первых, избавляется от необходимости принимать пожизненную заместительную терапию гормонами щитовидной железы, а во-вторых, избегает тех серьезных последствий, которые несет за собой операция полного удаления ЩЖ. Однако стоит понимать, что такой вариант не касается опухолей большого размера, а также тех новообразований, которые потенциально могут быть агрессивными (это решает врач!). Сейчас терапевты и хирурги, которые занимаются патологией щитовидной железы, разделились на два лагеря: те, кто считает, что лучше перестраховаться, и при выявлении даже самой маленькой опухоли удалить всю щитовидную железу, и те, кто считает, что лучшим выходом будет частичное удаление ткани железы, а именно поврежденной ее доли. К сожалению, этот вопрос до сих пор остается открытым. Врачи все еще не могут прийти к единому знаменателю в данном вопросе. Проблема в том, что достоверная объективная доказательная база, на которую врачи могли бы опираться в качестве актуального клинического руководства, вовсе отсутствует. Существуют лишь отдельные исследования, которые обозревают вопрос лишь с одной субъективной стороны [21]. Оптимальным решением данной проблемы, на наш взгляд, стало бы объединение всех существующих статей с объективным и всесторонним взглядом на этот вопрос. Однако подобное исследование лишь ожидает нас в будущем. Финальный аккордС этими и другими мыслями вы можете ознакомится по оставленной нами ссылке [26]. Итак, дорогие наши читатели! Опираясь на всё, о чем мы рассказали выше, мы бы хотели, чтобы вы сделали три главных вывода: Всем хорошего дня, и берегите свои щитовидки и нервы. :) Читайте также:
|