Доступ при опухолях почки

- Опухоли почки
- Метастазы рака почки
- Как часто и у кого встречается рак почки?
- Диагностика опухолей почек
- Лечение рака почки на разных стадиях
- Цены в Европейской онкологической клинике на лечение рака почки
Опухоли почки
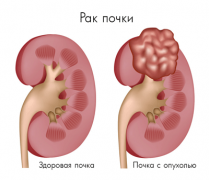
Второй характеристикой опухоли почки, как впрочем и большинства других опухолей, является потеря спецификации клетки – так как клетка быстро делится, она просто не успевает специализироваться. Таким образом, опухоль почки в первом приближении можно характеризовать, как массу клеток, бесконтрольно делящихся и потерявших способность к специализации. Чем меньше специализирована клетка опухоли для выполнения своей функции, чем быстрее она делится и чем больше его способность к распространению по кровеносным и лимфатическим сосудам, тем опухоль злокачественнее.
Почти 90 % опухолей почки злокачественны. Оставшиеся 10 процентов приходятся на ангиомиолипомы и другие, гораздо более редкие доброкачественные опухоли почки. Между тем, даже доброкачественные опухоли почки вполне могут быть опасны для здоровья. Например – ангиомиолипома может повредить сосуды почки, вызывая кровотечение. Что же касается злокачественных опухолей или рака почки, то тут мы сталкиваемся с повреждением функционирующей почечной ткани, ее сосудов и кровотечением, с метастазированием в кости, легкие, головной мозг и, соответственно, нестерпимыми болями.
Метастазы рака почки
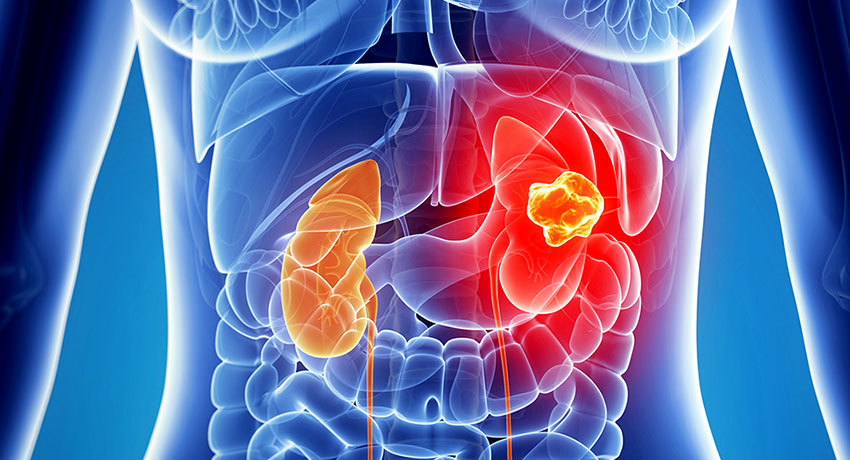
Метастазирование — это распространение опухоли по кровеносным или лимфатическим сосудам. Опухоли, как и всему живому в организме, требуется питание, обеспечиваемое сосудами. Вот в эти сосуды и попадают 1-2 клетки из основной опухоли, которые распространяются на различные органы. Для рака почки характерно метастазирование в кости и легкие, а также в печень, надпочечники и головной мозг.
рака почки, как и основная опухоль, нарушает функцию органа, где развивается. Например, метастаз рака почки в легкие вызывает упорный кашель, метастаз в кости — страшные, изнуряющие боли, от которых помогают только сильнодействующие наркотические препараты. К сожалению, часть пациентов, обративших к врачу, уже имеют отдаленные метастазы в тех или иных органах. Это резко ухудшает прогноз течения заболевания, так как приходится бороться не с одной опухолью, а, по сути, с опухолями множеством опухолей в нескольких органах.
Как часто и у кого встречается рак почки?
Диагностика опухолей почек
При подозрении на рак почки пациенту назначают общий анализ мочи, общий и биохимический анализы крови.
Один из наиболее информативных методов диагностики рака почки – компьютерная томография. Она помогает оценить размер, форму и локализацию злокачественного новообразования, обнаружить очаги в лимфатических узлах и других анатомических структурах за пределами почек. Исследование нередко дополняют внутривенным контрастированием. Введение контраста противопоказано при нарушении функции почек.
Магнитно-резонансную томографию применяют реже, чем КТ. Она показана, когда пациенту нельзя проводить компьютерную томографию с контрастом, если имеется подозрение на прорастание опухоли в нижнюю полую вену или другие крупные сосуды, для обнаружения метастатических очагов в головном и спинном мозге.

Ангиография – рентгенография с контрастирование сосудов, почки. Она помогает в диагностике заболевания и планировании хирургического лечения.
Позитронно-эмиссионная томография помогает обнаружить вторичные очаги рака в различных частях тела. Суть метода в том, что в организм пациента вводят вещество, которое обладает слабой радиоактивностью и накапливается в опухолевых клетках. Затем выполняют снимки с помощью специального аппарата, и на них опухолевые очаги хорошо видны.
В отличие от других онкологических заболеваний, биопсия при раке почки проводится редко. Обычно результатов других исследований хватает для того, чтобы принять решение о необходимости хирургического вмешательства. Уже после операции удаленную опухоль направляют в лабораторию, чтобы подтвердить диагноз. Биопсию проводят, если другие исследования не позволяют разобраться, показана ли операция. В случаях, когда хирургическое вмешательство противопоказано, исследование опухолевой ткани помогает определиться с тактикой лечения.
В медицине нет категоричных, стопроцентных ответов. Какова цель операции по удалению рака почки? Удалить опухоль? Удалить почку с подлежащими структурами? Удалить только первичный очаг опухоли, а потом бороться с метастазами теми или иными способами? Перенесет ли пациент операцию, каково его общее состояние? Какую именно операцию выбрать для конкретного больного? На эти вопросы должен ответить онкоуролог, перед тем, как предложить хирургическое, консервативное или комбинированное лечение. В основном, это зависит от стадии рака почки, расположения опухоли, наличия метастазов в лимфатические узлы и общего состояния здоровья пациента.

Это зависит главным образом от стадии, на которой была диагностирована опухоль, и начато лечение. Пятилетняя выживаемость (процент пациентов, оставшихся в живых спустя 5 лет) наиболее высока для I стадии и составляет 81%. На II и III стадиях она, соответственно, составляет 74 и 53%. При IV стадии — 8%.
Стадия рака почки зависит от размеров и расположения опухоли. Так, рак почки первой стадии — это опухоль меньше 7 см, не выходящая за пределы почки. Рак почки второй стадии — это опухоль меньше 10 см, также не выходящая за пределы почки. А вот рак почки третьей стадии — это уже опухоль любых размеров, ограниченная почкой, либо повреждающая надпочечник, почечную вену, но имеющую метастаз в ближайших лимфатических узлах. Рак почки четвертой стадии может быть любых размеров, однако при этой стадии опухоль либо выходит за пределы почечной фасции, либо имеются больше одного метастаза в ближайших лимфатических узлах, либо имеются метастазы в легкие, кости, печень или головной мозг.
Стадию рака почки определяют в соответствии с международной классификацией TNM. Рядом с каждой из трех букв аббревиатуры указывают индекс, описывающий характеристики первичной опухоли (T), поражение регионарных лимфатических узлов (N), наличие отдаленных метастазов (M):
T1 – опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр не более 4 см (T1a) или 4–7 см (T1b).
T2 - опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр 7–10 см (T2a) или более 10 см (T1b).
T3 – злокачественное новообразование распространяется на почечную вену и ее ветви, на надпочечник на одноименной стороне, паранефральную клетчатку, не прорастая фасцию Героты (T3a), на нижнюю полую вену ниже (T3b) или выше (T3c) диафрагмы или врастает в стенку вены.
T4 – опухоль распространяется за пределы фасции Героты.
N0 – опухолевые очаги в регионарных лимфоузлах отсутствуют.
N1 – обнаруживается опухолевый очаг в одном лимфоузле.
N2 – обнаруживаются опухолевые очаги в двух и более регионарных лимфоузлах.
M0 – отдаленных метастазов нет.
M1 – отдаленные метастазы присутствуют.
В зависимости от значений T, N и M, выделяют четыре стадии рака почки:
- Стадия I: опухоль в почке не более 7 см (T1), лимфоузлы не поражены, отдаленных метастазов нет.
- Стадия II: первичная опухоль более 7 см (T2), отсутствуют очаги поражения в лимфатических узлах и отдаленные метастазы.
- Стадия III: злокачественная опухоль распространяется на соседние структуры (T3) и/или поражен один регионарный лимфатический узел (N1).
Стадия IV: опухоль распространяется на соседние структуры (T4), либо поражено 2 и более регионарных лимфоузла (N2), либо обнаружены отдаленные метастазы (M1).
Опухоль почки размером 2 см может быть расположена вблизи почечных сосудов и ее удаление технически может быть невозможным. Однако данные литературы указывают, что если нет метастазов в лимфатические узлы и отдаленные органы, то опухоль почки до 7 см можно удалять с сохранением почки, что, безусловно, лучше полного удаления почки и инвалидизации пациента.
Лечение рака почки на разных стадиях
Выбор тактики лечения при раке почки в первую очередь определяется стадией опухоли и состоянием здоровья пациента.
При стадиях I и II возможно хирургическое лечение. Стандартным вариантом считается нефрэктомия. К органосохраняющим операциям прибегают реже, в частности, при опухолях в единственной почке. Кроме того, на выбор объема операции влияет размер опухоли. Также удаляют близлежащие лимфатические сосуды, особенно если они увеличены, окружающую жировую клетчатку.
При III стадии рака почки основным методом лечения также является нефрэктомия, при этом должны быть удалены все регионарные метастазы. Если опухоль прорастает в почечную или нижнюю полую вену или мигрирует в их просвете в виде опухолевого тромба, пораженные ткани также нужно удалить, при этом может потребоваться подключение пациента к аппарату искусственного кровообращения.
При высоком риске рецидива после операции применяют адъювантную терапию таргетным препаратом сунитинибом. Пациенты получают его в течение года.
Если хирургическое вмешательство противопоказано, прибегают к радиочастотной аблации, эмболизации.
На IV стадии подходы к лечению могут быть разными, в зависимости от степени распространения рака в организме. В некоторых случаях возможно хирургическое лечение, в том числе циторедуктивные операции, во время которых хирурги не могут убрать опухоль полностью, но стараются удалить как можно больший ее объем. В редких случаев возможно удаление основной опухоли в почке и единичных вторичных очагов в других органах. После операции назначают курс таргетной терапии, иммунотерапии.
При неоперабельном раке почки основными методами лечения становятся иммунотерапия и таргетная терапия.

В некоторых случаях рак почки удается выявить на ранних стадиях, когда опухолевые клетки не распространяются за пределы органа. Но зачастую заболевание диагностируют на более поздних стадиях. Во-первых, это связано с тем, что рак почки может очень долго протекать бессимптомно. Во-вторых, для этого типа рака на данный момент не существует рекомендованных скрининговых исследований.
Все симптомы можно разделить на ренальные (связанные с поражением почек) и экстраренальные.
Среди ренальных проявлений рака почки наиболее характерны три:
- Гематурия (примесь крови в моче) – самый распространенный и зачастую первый симптом. Он возникает более чем у половины пациентов с раком почки. Моча приобретает красный цвет, при этом боль не беспокоит либо носит острый характер и возникает после гематурии. Этим злокачественная опухоль отличается от неопухолевых заболеваний почки, например, мочекаменной болезни, при которой обычно сначала возникает боль, а потом появляется примесь крови в моче. Гематурия периодически исчезает, но через некоторое время снова появляется, причем, промежутки между кровотечениями сокращаются. Количество крови в моче не зависит от размеров опухоли.
- Боли беспокоят около половины пациентов. Острая боль после гематурии возникает из-за того, что сгустки крови перекрывают просвет мочеточника. Тупые сильные боли зачастую говорят о плохом прогнозе.
- Пальпируемая опухоль – симптом, который выявляет врач во время осмотра примерно у трети пациентов.
Все три симптома одновременно встречаются у одного из десяти пациентов с раком почкеи. Обычно при этом выявляют запущенные опухоли.
Среди экстраренальных симптомов в первую очередь стоит отметить повышение температуры тела. У 5% больных лихорадка – единственное проявление заболевания. У некоторых пациентов повышается артериальное давление, отмечается покраснение лица из-за увеличения количества эритроцитов в крови, у мужчин – расширение вен мошонки (варикоцеле). На поздних стадиях снижается аппетит, пациент теряет вес без видимой причины, постоянно ощущает утомление, недомогание.

Опухоль почки — лапароскопия или полостная операция?
Злокачественные новообразования почки на ранних стадиях легко поддаются оперативному лечению. Удалить опухоль можно двумя методами: открытым путем или лапароскопической операцией.

Лапароскопия или полостная операция?
Полостная операция – высокотравматичное хирургическое вмешательство. Она проводится в тех случаях, когда малоинвазивные методики недоступны. Операционный доступ к опухоли осуществляется через разрез на поясничной области. Длина разреза может составлять до 10-15 см. Затем хирург послойно разрезает мышцы и фасции и достигает почки.
Объем кровопотери во время полостной операции больше, чем после лапароскопии. Реабилитация происходит долго, а на теле остается большой косметический дефект в виде рубца. Чтобы избежать таких последствий, на замену открытому способу лечения пришла лапароскопическая резекция.
Применение лапароскопической резекции более предпочтительно для удаления злокачественных новообразований на ранних стадиях. Эффективности метода ничем не уступает традиционной резекции, более того, использование лапароскопа имеет ряд дополнительных преимуществ:
- малоинвазивность;
- низкая травматичность окружающих здоровых тканей — вмешательство осуществляется через маленькие точечные проколы на теле пациента;
- высокая косметичность;
- небольшой объем кровопотери;
- вероятность развития грыж минимальна;
- меньше шанс присоединения вторичной инфекции;
- короче период реабилитации.
Реабилитация после лапароскопической резекции проходит менее болезненно, а к привычному режиму пациент может вернуться уже через неделю после операции.
Реабилитационный период после резекции
Во время восстановительного периода следует придерживаться всех рекомендаций лечащего доктора. Основной принцип послеоперационного периода – как можно раньше восстановить двигательную активность и вернуть пациента к привычной жизни. Болезненность после лапароскопической резекции выражена незначительно, поэтому пациенты могут не придерживаться постельного режима.
Во время всего периода реабилитации следует придерживаться принципов ЗОЖ – так восстановление пройдет быстрее. В первый месяц не рекомендуется заниматься тяжелыми видами спорта, поднимать большие веса. Хоть риск появления грыжи и кровотечения и минимален, но перенапрягаться в первое время не стоит.
Образ жизни после удаления новообразования
После злокачественного новообразования почки следует придерживаться ряда правил:
- отказ от табачных изделий и спиртных напитков;
- нормализация массы тела;
- частое дробное питание и исключение из рациона вредных продуктов;
- лечение сопутствующих болезней – ИБС, артериальная гипертензия, сахарный диабет и т.д.;
- контроль за состоянием почек и мочевыводящей системы.
При выписке врач назначит дату контрольного осмотра. В этот день необходимо обязательно посетить клинику и пройти необходимый перечень обследований. Как правило, список анализов включает в себя клинические анализы крови и мочи, УЗИ-почек и органов брюшной полости.
Онкологический прогноз
Прогноз после удаления опухоли благоприятный, вероятность рецидива составляет менее 7%. Однако, тактика врача предполагает онкологическую настороженность, чтобы в случае рецидива немедленно выявить новый злокачественный очаг. Для этого раз в полгода следует посещать своего врача и проходить необходимые обследования.
Опухоли почки оперируют, одновременно решая две задачи — диагностическую и лечебную. При доброкачественных опухолях главная задача операции — диагностика, поскольку образования бессимптомны и принципиально не требуют удаления, но внешне мало отличаются от рака.
Именно внешняя похожесть большинства доброкачественных процессов на злокачественную опухоль, при большей частоте встречаемости рака, вынуждает прибегать не только к биопсии, но и к удалению доброкачественных образований почки для морфологического исследования. Только операция позволяет поставить правильный диагноз.

Способы удаления опухолей почки
Самый оптимальный способ лечения узлового образования — операция, а объем удаляемой части зависит от размеров опухоли и её характера.
Стандартные оперативные вмешательства при опухолях почки:
- резекция предполагает удаление части почки,
- радикальная нефрэктомия — удаление всего органа,
- циторедуктивная нефрэктомия — максимальное удаление очагов опухоли.
При карциномах операция — это лечение, для выбора оптимального объема хирургии важен размер опухоли, но не только. Резекцию при карциномах относят к органосохраняющим вмешательствам, она имеет неоспоримые функциональные преимущества перед полным удалением органа. Цель резекции — максимальное удаление опухолевого поражения при максимальном сохранении ткани почки и её функции, но без вероятности рецидива в будущем. При невозможности резекции прибегают к нефрэктомии.
Какие доброкачественные опухоли почки оперируют?
Доброкачественные новообразования почки разнообразны по клеточной — морфологической структуре, главное, что объединяет большинство — отсутствие отрицательного влияния на судьбу больного. Эти процессы, как правило, обнаруживают случайно — при профосмотре или обследовании по поводу другого заболевания. С доброкачественной опухолью можно жить всю жизнь, если она не растёт, не давит на соседние органы или не маскируется под злокачественное новообразование. Проблема в том, что внешне они мало отличаются от рака, а биопсия не всегда даёт уверенность в доброкачественном характере процесса.
Третья по частоте опухоль — папиллярная аденома редко бывает единственной, чаще имеется несколько мелких узелков. Одна проблема — по строению аденома похожа на неагрессивный рак, биопсия не поможет их различить, и в этой клинической ситуации нет сомнений в необходимости диагностической резекции.
Резекция почки при раке
Самые частые новообразования органа — карциномы, то есть рак. Очень редко встречаются саркомы и нейроэндокринные опухоли — карциноид.
Всем больным до начала терапии определяется выделительная функция почек, и только после изотопного исследования — динамической урографии вырабатывается тактика ведения пациента и определяется объём хирургического вмешательства — резекция или нефрэктомия.
Резекция выполняется при небольших карциномах 1–2 стадии, а также при больших образованиях и даже при метастатической стадии. При небольшом узле нет сомнений в выборе — резекция, при распространенной опухоли резекция становится способом выбора:
Резекция может выполняться классическим — открытым способом с большим разрезом в поясничной области и с помощью эндоскопического оборудования — лапароскопически, отдалённые результаты одинаковы. Течение послеоперационного периода при лапароскопической резекции почки легче и время пребывания в клинике короче.
Оставьте свой номер телефона
Нефрэктомия
Радикальная нефрэктомия выполняется при больших новообразованиях, занимающих большую часть почки, и при 1–2 стадии рака, когда технически не удаётся резекция. Главное — остающаяся противоположная почка должна быть здоровой и без изъянов.
Нефрэктомию выполняют в двух вариантах:
- радикальная — классическое удаление почки с окружающей клетчаткой, надпочечником и лимфатическими узлами;
- циторедуктивная — удаление части опухоли с паллиативной целью.
Радикальная нефрэктомия — стандарт лечения рака почки, ещё недавно считавшийся самым оптимальным подходом. Сегодня оптимально именно сохранение органа, поэтому пересмотрено не только отношение к назначению нефрэктомии, но также изменился и объём удаляемого:
- надпочечник удаляется только при вовлечении в опухолевый конгломерат или при метастазах, здоровый надпочечник оставляют;
- дополняется тромбэктомией при наличии в сосудах тромба, а образование тромбов — один из специфических симптомов карциномы;
- объем лимфодиссекция определяется хирургом, стандартов не существует.
Циторедуктивная нефрэктомия применяется в метастатической стадии вместе с удалением — резекцией метастазов в легких. Это паллиативное вмешательство, избавляющее от перспективы распадающейся опухоли с кровотечением из разрушенного сосуда, всасывания токсичных продуктов жизнедеятельности карциномы и для снижения рассеивания злокачественных клеток в организме.
Доступ к больной почке определяется хирургом, он должен быть удобным для выполнения поставленной задачи, но преимущество на стороне лапароскопической технологии.
В клинике Медицина 24/7 всё подчинено качественному выполнению любой процедуры, каждого исследования, всех манипуляций, поэтому частота осложнений после операции ниже минимальной. Мы умеем лечить и выхаживать.
Введение
Нефронсберегающее лечение при почечно-клеточном раке (ПКР), обеспечивая хорошие долгосрочные онкологические результаты, претендует на приоритет не только при опухолях до 4 см 3. До сих пор одним из основных противопоказаний к проведению нефронсберегающего лечения является невозможность обеспечения гемостаза при опухолях среднего сегмента, особенно при их интраренальном расположении [1, 3]. Общепризнанными критическими моментами в резекции почки являются время ишемии и адекватность гемостаза 7. Другим камнем преткновения является методика удаления опухоли, а именно, энуклеация или резекция с отступом от края опухоли. Данные литературы разноречивы: много ретроспективных исследований, указывающих на преимущества энуклеации 10. Однако их дизайн не безупречен, а большую часть (60-80%) составляют опухоли до 2 см. В некоторых исследованиях показано, что энуклеация почечной опухоли может увеличить частоту положительного хирургического края, особенно при больших опухолях [12, 13]. Несомненно, большую роль играет вариант доступа: эндоскопия или открытая хирургия.
Цель исследования – оценить эффективность открытой резекции почки.
Материалы и методы
За период 2005-2018 года нами выполнено 152 открытые резекции почки (РП) по поводу ПКР. Средний возраст пациентов составил 55,4±16,2 года; соотношение мужчины/женщины - 52,6/47,4%; правосторонняя/левосторонняя локализация опухоли 42,1/57,9% соответственно. В план предоперационного обследования, помимо рентгенографии или СКТ органов грудной клетки, ультразвукового исследования почек, печени, регионарных лимфатических узлов и почечных вен, стандартно включали СКТ в ангиографическом режиме с регистрацией нативной, артериальной, паренхиматозной, венозной и выделительной фаз.
Результаты и их обсуждение
По абсолютным показаниям оперированы 10,5% пациентов, а именно, 9 пациентов с единственной почкой и 7 с билатеральным раком (в 5 случаях двухсторонняя резекция, в 2 – резекция и нефрэктомия). Относительные показания были выставлены у 29,6% больных, а элективные более чем в половине случаев – 51,6% (рис. 1), что соответствует статистике ведущих российских клиник 4.
Внеполюсное расположение опухоли отмечено в 62,5% наблюдений. В 69,1% наблюдений размеры опухолевого узла превысили Т1а , а 23,7% были стадированы как Т2а . При этом 23% пациентов имели высокий риск осложнений нефрон сберегающего лечения по шкале R.E.N.A.L., средний риск отмечен в 65,1%, а низкий в 11,9% (рис. 2).
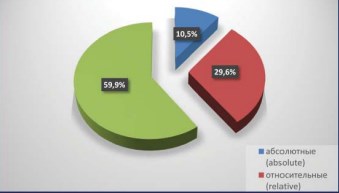
Рисунок 1. Показания к выполнению резекции почки
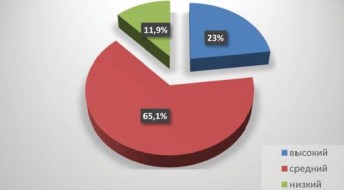
Рисунок 2. Риск интраоперационных осложнений согласно морфометрической шкале R.E.N.A.L.
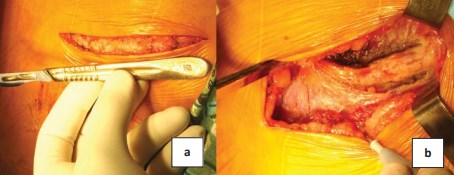
Рисунок 3. Этапы выполнения хирургического доступа: а – кожный разрез в Х межреберье; b – резекция Х ребра
Экстраперитонеальный люмботомический доступ в Х межреберье с резекцией Х ребра обеспечивал прямой выход на почечные сосуды и возможность манипуляций на верхнем полюсе при длине разреза 7-16 см (11,7±4,2 см), (рис. 3). Ранение плеврального синуса отмечено в 15 (9,7%) случаях, диагностировано интраоперационно, ушито без дренажа с аспирацией воздуха, рецидивов пневмо- и гидроторакса не было.
Использование СКТ ангиографии позволило на дооперационном этапе иметь четкое представление о ангиоархитектонике и лоханочно-сосудистых взаимоотношениях в почечном синусе (рис. 4). В 39 (25,7%) наблюдениях имелись аберрантные сосуды, кровоснабжающие опухоль. У 148 (97,4%) пациентов деление почечной артерии на сегментарные отмечалось на уровне или проксимальнее почечной лоханки, и только в 4 (2,6%) наблюдениях зарегистрировано интраренальное деление почечной артерии.
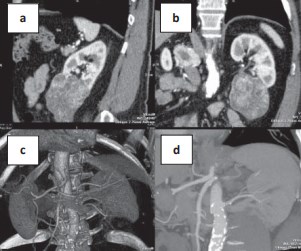
Рисунок 4. СКТ-ангиография пациента с опухолью нижнего полюса левой почки: a – сагитальная плоскость; b – фронтальная плоскость; c – 3D-реконструкция; d – 13 месяцев после операции, фронтальная плоскость
Выделяли сегментарную, субсегментарную или аберрантную артерию, кровоснабжающую опухоль, брали последнюю на держалку (рис. 5а). Опухоль мобилизировали без удаления паРисунок 3. Этапы выполнения хирургического доступа: а – кожный разрез в Х межреберье; b – резекция Х ребра. Figure 3. The steps of the surgical access: a – skin incision in the X intercostal space; b – resection of the X rib. ранефрия. Выключали опухоль из кровотока наложением сосудистого зажима (бульдог) на питающую артерию, вену не клипировали (рис. 5b). Зона ишемии не превышала ¼ органа. Энуклеаций и энуклеорезекций мы не выполняли. Резекцию выполняли с отступом от опухоли 0,5-1 см в пределах визуально неизмененной почечной перенхимы скальпелем или электроножом, принципиальных преимуществ в плане гемостаза при использовании электрохирургии отмечено не было, и инцизия электроножом была несколько затруднена на ишемизированной ткани. Визуально оценивали хирургически край удаленной опухоли (рис. 6а), при необходимости рассекали опухоль (рис. 6б). Экспресс-патогистологии не производили, по данным стандартного морфологического исследования положительный хирургический край не зарегистрирован ни в одном случае. Средний размер отступа от края опухоли при резекции составил 0,7±0,4 см (рис. 6б). Морфологическое исследование в стандартной проводке не выявило положительного хирургического края ни у одного больного. Отдаленные результаты прослежены у 104 пациентов, у которых на сроках наблюдения 87,4±62,5 месяцев не выявлено локального рецидива либо прогрессии заболевания.
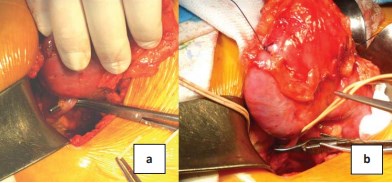
Рисунок 5. Этапы сосудистой изоляции опухоли: а – выделение сегментарной почечной артерии; b – наложение сосудистого зажима на сегментарную почечную артерию
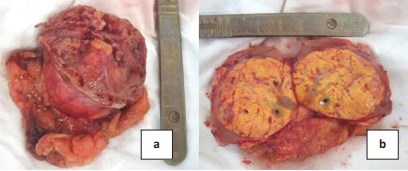
Рисунок 6. Методика оценки хирургического края: а – визуальная оценка края резекции; b – оценка хирургического отступа
Гемостаз осуществляли наложением П-образных швов (Polysorb-0), линию шва укрепляли заплатой из сосудистого протеза (рис. 7). Дренирование полостной системы выполнено в 2 (1,3%), внутренний стент и нефростома. Показанием к дренированию явился риск резидуального нефролитиаза при коралловидном и множественном нефролитиазе. Нефростома установлена вследствие непреодолимого препятствия в интрамуральном отделе мочеточника, удалена на 10 сутки после контроля проходимости мочеточника. Еще один стент (0,7%) установлен в послеоперационном периоде по поводу мочевого свища. Последний отмечен у пациента после резекции почки по поводу опухоли передней поверхности среднего сегмента максимальным размером 5,5 см. Причиной образования свища, на наш взгляд, явилась стриктура лоханочно-мочеточникового сегмента и невозможность двухсторонней компрессии линии шва (риск деформации и нарушения кровоснабжения почки). Свищ закрылся самостоятельно на сроке 2 недель.
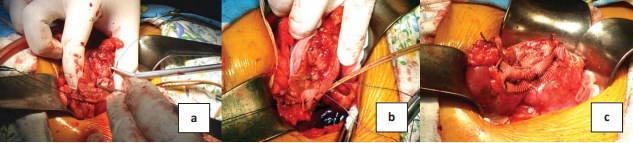
Рисунок 7. Закрытие почечной раны однорядным П-образным швом: а и b – последовательность наложения П-образных горизонтальных швов; c – окончательный вид почечной раны после пуска кровотока
Продолжительность операции составила 109,6±56,7 мин, время частичной ишемии 15,1±8,3 мин, объем кровопотери – 258±93 мл. Отделяемое по дренажам продолжалось в течение 4-12 часов после операции (за исключением выше описанного случая) и составило в среднем 35,7±22,1 мл, дренажи обрезались под повязку на 1 сутки, удалялись на 2-4 сутки послеоперационного периода. Пациенты активизировались через 24 часа, когда удалялся уретральный катетер, в 59 (38,8%) случаях дренирование мочевого пузыря не выполняли. Средний послеоперационный койко-день составил 10,1±4,2. Длительность значимой тепловой ишемии почки по данным различных авторов колеблется от 20 до 40 минут [6, 11]. В литературе освещается возможность использования таких нефропротективных приёмов, как локальная гипотермия за счет обкладывания почки ледяной крошкой во время резекции, локальная гипотермия за счет выключения почки из кровотока и перфузии охлажденным консервирующим раствором, экстракорпоральная резекция почки, компрессия сегментарных сосудов, выполнение резекции без компрессии сосудов почки, в том числе радиочастотная аблация [6 ,7, 11, 14].
Хотелось бы отметить, что у каждого из методов есть как преимущества, так и недостатки. К недостаткам локальных методик защиты нужно отнести необходимость наличия ледяной крошки в ране, перфузионных канюль, что ограничивает возможность манипуляций. Кроме того, необходимость закрытия канюляционных доступов подразумевает выключение кровотока, т.е. тепловую ишемию. Последняя актуальна и при аутотрансплантации после экстракорпоральной резекции. Нулевая ишемия, особенно при сложных опухолях, подразумевает значимую кровопотерю [7, 11, 14, 15]. Это позволяет считать использованную нами сегментарную артериальную ишемию одним из выгодных решений.
Естественно, многие пациенты с низким риском осложнений, согласно морфометрической шкалы, не попали в исследуемую группу ввиду того, что им выполнены лапароскопические операции. Учитывая, что в нашей клинике хирурги выполняют как открытые, так и эндоскопические вмешательства при ПКР, хотелось бы отметить тот факт, что пациенты охотнее соглашаются на открытую резекцию, чем на лапароскопическую нефрэктомию. Это позволяет увеличить пул нефрон сберегающих вмешательств в группах со средним и высоким риском осложнений без ущерба со стороны радикальности.
Парциальная лимфодиссекция выполнена в 83 (54,6%) наблюдениях. Морфологическое исследование удаленных лимфатических узлов в этих наблюдениях было отрицательным.
Выводы
Литература
- Zhang M, Zhao Z, Duan X, Deng T, Cai C, Wu W, Zeng G. Partial versus radical nephrectomy for T1b-2N0M0 renal tumors: A propensity score matching study based on the SEER database. PLoS One. 2018;28;13(2):e0193530. DOI:10.1371/journal.pone.0193530
- Marchioni M, Preisser F, Bandini M, Nazzani S, Tian Z, Kapoor A, Cindolo L, Abdollah F, Tilki D, BrigantiA, Montorsi F, Shariat SF, Schips L, Karakiewicz PI. Comparison of Partial Versus Radical Nephrectomy Eff ect on Othercause Mortality, Cancer-specifi c Mortality, and 30-day Mortality in Patients Older Than 75 Years. Eur Urol Focus. 2018;2.pii:S2405-4569(18)30008-7. DOI:10.1016/j. euf.2018.01.007
- Мосоян М.С., Аль-Шукри С.Х., Есаян А.М., Каюков И.Г. Ранние клинико-функциональные показатели у больных раком почки, перенесших резекцию почки или радикальную нефрэктомию. Нефрология. 2012;16:4:100-104.
- Пучков К.В., Филимонов В.Б., Крапивин А.А., Васин Р.В., Васин И.В. Хирургическое лечение рака почки сегодня: лапароскопическая радикальная нефрэктомия и резекция почки. Урология. 2008;1:47-53.
- Павлов А.Ю., Кравцов И.Б. Функциональное состояние почек и течение послеоперационного периода при резекции почки по поводу рака. Справочник врача общей практики. 2013;7:64-69.
- Bertolo R, Garisto J, Dagenais J, Agudelo J, Armanyous S, Lioudis M, Kaouk J. Cold versus warm ischemia robotassisted partial nephrectomy: Comparison of functional outcomes in propensity-score matched “at risk” patients. J Endourol. 2018;21. DOI:10.1089/end.2018.0383
- Arora S, Rogers C. Partial Nephrectomy in Central Renal Tumors. J Endourol. 2018;32(S1):63-S67. DOI:10.1089/ end.2018.0046
- Serni S, Vittori G, Frizzi J, Mari A, Siena G, Lapini A, Carini M, Minervini A. Simple enucleation for the treatment of highly complex renal tumors: Perioperative, functional and oncological results. Eur J Surg Oncol. 2015;41(7):934- 40. DOI:10.1016/j.ejso.2015.02.019
- Calaway AC, Gondim DD, Flack CK, Jacob JM, Idrees MT, Boris RS. Anatomic comparison of traditional and enucleation partial nephrectomy specimens. Urol Oncol. 2017;35(5):221-226. DOI:10.1016/j.urolonc.2016.12.005
- Mari A, Morselli S, Sessa F, Campi R, Di Maida F, Greco I, Siena G, Tuccio A, Vittori G, Serni S, Carini M, Minervini A. Impact of the off -clamp endoscopic robot-assisted simple enucleation (ERASE) of clinical T1 renal tumors on the postoperative renal function: Results from a matchedpair comparison. Eur J Surg Oncol. 2018;44(6):853-858. DOI:10.1016/j.ejso.2018.01.093
- Huang J, Zhang J, Wang Y, Kong W, Xue W, Liu D, Chen Y, Huang Y. Comparing Zero Ischemia Laparoscopic Radio Frequency Ablation Assisted Tumor Enucleationand Laparoscopic Partial Nephrectomy for Clinical T1a Renal Tumor: A Randomized Clinical Trial. J Urol. 2016;195(6):1677-83. DOI:10.1016/j.juro.2015.12.115
- Minervini A, Campi R, Sessa F, Derweesh I, Kaouk JH, Mari A, Rha KH, Sessa M, Volpe A, Carini M, Uzzo RG. Positive surgical margins and local recurrence after simple enucleation and standard partialnephrectomy for malignant renal tumors: systematic review of the literature and meta-analysis of prevalence. Minerva Urol Nefrol. 2017;69(6):523-538. DOI:10.23736/S0393- 2249.17.02864-8
- Wang L, Hughes I, Snarskis C, Alvarez H, Feng J, Gupta GN, Picken MM. Tumor enucleation specimens of small renal tumors more frequently have a positive surgical margin than partial nephrectomy specimens, but this is not associated with local tumor recurrence. Virchows Arch. 2017;470(1):55-61. DOI: 10.1007/s00428-016-2031-9
- Huang J, Zhang J, Wang Y, Kong W, Xue W, Liu D, Chen Y, Huang Y. Comparing Zero Ischemia Laparoscopic Radio Frequency Ablation Assisted Tumor Enucleationand Laparoscopic Partial Nephrectomy for Clinical T1a Renal Tumor: A Randomized Clinical Trial. J Urol. 2016;195(6):1677-83. DOI:10.1016/j.juro.2015.12.115
- Шкодкин С.В., Татаринцев А.М., Идашкин Ю.Б., Любушкин А.В., Фиронов С.А. Экстракорпоральная резекция почки: а стоит ли? Урология. 2016;3:62-69.
Статья опубликована в журнале "Вестник урологии" №2 2018, стр. 54-61
Читайте также:





