Детские лейкозы и лимфомы
Обращают на себя внимание различия возрастных кривых для частных форм лейкозов: пик частоты острого миелолейкоза (ОМЛ) приходится на первый год жизни (немногим более 1/100 000), а острый лимфолейкоз (ОЛЛ) в 6—7 раз более высокий [(7—9): 100 000] между 3-м и 4-м годами жизни. Распределение ОЛЛ асимметрично: после пика наступает пологий спад до возраста адолесценции, в котором некоторые исследователи регистрируют слабовыраженный второй пик.
В экономически развитых странах общая частота острых лейкозов у детей до 15 лет составляет 3,5—4,5 на 100 тыс. в год; показатель варьирует незначительно. ОЛЛ составляет более 80 % от всех лейкозов и 30— 35 % всех новообразований у детей.
Последние 40—50 лет в развитых странах частота детских лейкозов, а также положение и уровень младенческого ее пика стабильны. У неевропейских народов пик не так высок, а в Африке практически не выражен. В младенчестве заболеваемость выше среди девочек, а затем среди мальчиков с соотношением частоты 1:1,3. Более редкая форма — Т-клеточный ОЛЛ в основном встречается у мальчиков.
В детском возрасте острый миелолейкоз (ОМЛ) составляет 20 % от всех лейкозов и занимает 7-е место среди новообразований у детей. Частота ОМЛ у детей наиболее высока в Азии (1,1 на 100 тыс.) и относительно велика на Ближнем Востоке, в Индии и Новой Зеландии. В Западной Европе и США заболеваемость ОМЛ в среднем 0,5—0,6 на 100 тыс. детей до 15 лет. После пика на первом году жизни заболеваемость стабильна до позднего подросткового возраста (0,4 на 100 тыс.), затем наблюдается постепенный подъем до уровня 5,0 на 100 тыс. на восьмом десятке жизни.
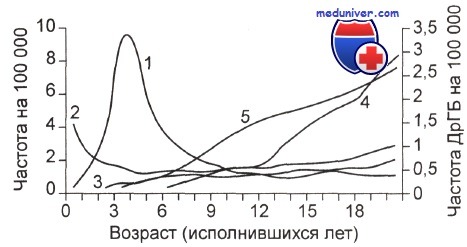
Стандартное возрастное распределение частоты заболеваний гемобластозами у детей.
1 - ОЛЛ; 2 - ОНЛЛ; 3 - ХМЛ; 4 - ЛГ; 5 - НХЛ. Показатели заболеваемости ОЛЛ даны в логарифмической шкале ввиду значительного преобладания этой формы в раннем детском возрасте.
Редко обнаруживается в детском и юном возрасте хронический миелолейкоз (ХМЛ). В России его доля у детей составляет 6,5 %. В африканских странах зарегистрирована несколько большая доля ХМЛ в молодом возрасте по отношению к общему числу лейкозов: от 10 % в Нигерии, до 19 % в Судане. ХМЛ не формирует детского пика заболеваемости и демонстрирует постепенный подъем вплоть до максимума в старшем возрасте.
Второе место среди гемобластозов по заболеваемости детей в западных странах занимают злокачественные лимфомы, включающие НХЛ и ЛХ. Частота НХЛ около 0,7 на 100 тыс.; как и при других гемобластозах, преобладают лица мужского пола в соотношении 2,5:1 — 3,0:1. У детей до 2 лет НХЛ не встречаются.
Детские неходжкинские лимфомы (НХЛ) всегда относятся к группе злокачественных, практически все они диффузного типа и генерализованы к моменту обнаружения. Три основных гистологических типа, по классификации REAL: 22—24 % — лимфобластная лимфома, 18—22 % —крупноклеточная лимфома (В-клеточный и Т-клеточный анапластические типы), 40— 50 % — лимфома Беркитта (ЛБ) (в основном в Африке) и беркиттоподобные лимфомы. Только 1 % лимфом детского возраста относятся к неагрессивным формам, более типичным для взрослых.
Лимфома Ходжкина в тех же гистологических вариантах, что и у взрослых, встречается у детей немоложе 5-лет. До 15 лет частота ее очень медленно нарастает, после чего наблюдается подъем, с которым связано начало первого максимума в возрасте 20—30 лет. В странах экваториальной Африки ЛХ по частоте занимает 2-е место после ЛБ.
До возраста 7—9 лет среди заболеваний гемобластозами в западных странах доминируют лейкозы, причем на первом году жизни ОМЛ. У детей старше 10 лет постепенно все чаще диагностируются лимфомы, а к возрасту 20 лет они составляют очевидное большинство.

Что такое острый лимфобластный лейкоз

Острый лейкоз бывает лимфобластного и нелимфобластного типа, частота их у детей составляет 72-80% и 16-19% соответственно. Оставшиеся 1-3% приходятся на хронический миелолейкоз.
Острый лимфобластный лейкоз (ОЛЛ) — это злокачественное новообразование, возникающее из клеток кроветворной системы, являющихся клетками-предшественницами лимфоцитов в красном костном мозге (ККМ).
Родоначальником лейкозного клона является полипотентная стволовая клетка ККМ, подвергающаяся генетическим мутациям, в результате чего она приобретает черты атипии, не созревает до нужной клеточной генерации и множественно делится, вытесняя из костного мозга клетки остальных ветвей гемопоэза. В результате костный мозг остаётся заполненным лимфобластами, которые также наводняют собой кровоток и некоторые органы (лимфоузлы, селезёнку, печень, головной мозг). Опухолевый процесс поддерживается и мутациями генов, регулирующих апоптоз клеток — их запрограммированную гибель в случае дефектов.
Причины возникновения ОЛЛ у детей

Острый лейкоз является полиэтиологическим заболеванием, то есть, в появлении его могут играть роль несколько факторов.
- Генетический фактор: врождённые генетические дефекты, генные и хромосомные мутации различного типа, наследственные заболевания.
- Повреждающие ДНК клеток внешние факторы:
- ионизирующая радиация;
- тяжёлые металлы, пестициды, гербициды, бензол, индол, нитрокраски;
- лекарственные средства (необоснованное и массивное применение цитостатиков, иммуносупрессоров, антибиотиков, НПВС);
- некоторые долго живущие вирусы, персистирующие в органах человека (вирус простого герпеса, вирус Эпштейн-Барр, ВПЧ).
Симптомы и признаки ОЛЛ у детей

Не специфические симптомы лейкоза — недомогание и слабость
Симптомы общей интоксикации: недомогание, вялость, сонливость, повышение температуры тела, потливость.
Симптомы анемии: одышка, тахикардия, бледность кожи, слизистой рта, конъюнктив, сердечные и сосудистые шумы.
Симптомы иммунных нарушений: некротические и гнойные процессы различной локализации (гнойнички кожи, некротическая ангина, некроз кожи, слизистой рта, кишечника, пневмония).
Симптомы ухудшения свёртываемости крови: кровотечения из носа, рта (дёсневые), мест инъекций, кожные гематомы в местах лёгкой травматизации, кровь в моче.
Симптомы гиперплазии лимфоидных органов:
- увеличение лимфоузлов, печени, селезёнки;
- боли в плоских костях (кости таза, рёбра, грудина, кости черепа), диафизах трубчатых костей и суставах за счёт давления увеличенного в объёме костного мозга на надкостницу;
- гиперплазия кожи — редко;
- уплотнение яичек, семенных канатиков, яичников при их инфильтрации;
- инфильтрация лёгких, сердца — появление клиники бронхита, пневмонии, миокардита.

Ребенка может беспокоить тошнота и рвота
- головные боли, усиление их может провоцироваться ярким светом, громкими звуками, прикосновением к коже;
- тошнота, рвота, ригидность мышц шеи;
- нарушение зрения, слуха, речи, двигательной активности;
- повышенный аппетит, жажда, нарушения психики, коматозное состояние.
Стадии заболевания ОЛЛ

Начальная стадия напоминает ОРВИ
1) Начальный период ОЛЛ зачастую не диагностируется, так как симптомы болезни напоминают клинику ОРВИ, ангины. Больной ребёнок становится вялым, может чувствовать головные боли, головокружение, боли в животе, мышцах, суставах. Часто возникает одышка, ускоренное сердцебиение, температура тела повышается до субфебрильных цифр (в среднем, до 37,5 о С). На коже могут появляться гнойничковые высыпания, появляются или учащаются носовые кровотечения, на нёбных миндалинах могут возникнуть обильные гнойные наложения или некротические массы. Важным симптомом, который должен заставить родителя отвести ребёнка к врачу, является преходящее увеличение разных групп лимфатических узлов.
2) Первично-активная стадия или развёрнутая стадия ОЛЛ.
Разгар болезни протекает с бурным началом. Выражена общая интоксикация: усиливается слабость, головные боли, температура тела волнообразно меняется в течение суток, к вечеру наблюдается субфебрилитет. Усиливаются суставные и костные боли, одышка, тахикардия, бледность кожи и слизистых. Значительно увеличены лимфоузлы (особенно шейные, подмышечные и паховые), слюнные и слёзные железы, печень и селезёнка, которые могут занимать около половины брюшной полости. Повышается кровоточивость, на коже возникают полиморфные высыпания, усиливаются носовые кровотечения, которые трудно купировать.

Лейкоз может уходить в ремиссию
3) Стадия ремиссии:
- полная ремиссия — нет жалоб и объективных симптомов болезни, нет бластных клеток в периферической крови и не более 5% в ККМ;
- неполная ремиссия — те же особенности, но бластов к ККМ может быть 5-20%.
- костномозговой рецидив — часто увеличены лимфоузлы, печень и селезёнка, наблюдаются симптомы анемии, либо клинических проявлений болезни нет, но анализы крови и ККМ изменены;
- экстрамедуллярный рецидив — выраженная клиника без изменения миелограммы (в ККМ до 0% бластов).
5) Терминальная стадия: выраженное угнетение кроветворения с угрожающими жизни ребёнка вторичными инфекционными осложнениями и спонтанными кровотечениями.
6) Стадия выздоровления: полное купирование клиники и лабораторных изменений без остаточных последствий лейкемии. Бывает крайне редко.
Диагностика

Лабораторные тесты указывают на патологию кроветворения
- В общем анализе крови: уменьшение гемоглобина, эритроцитов, тромбоцитов, гранулоцитов, увеличение количества бластных атипичных клеток, ускорение СОЭ.
- В биохимическом анализе крови: увеличение ЛДГ, билирубина, АСТ, щелочной фосфатазы, уменьшение общего белка, альбумина, глюкозы, железа, электролитов.
- В общем анализе мочи: белок, лейкоциты, цилиндры, бактерии.
- В миелограмме (анализ, отражающий клеточный состав ККМ):
- в начальную стадию — до 25% бластов;
- в развёрнутую стадию — более 25% бластов, феномен лейкемического зияния, уменьшение предшественников эритроцитов и тромбоцитов;
- в стадию полной ремиссии — менее 5% бластов, при неполной ремиссии — менее 20% бластов, ростки других клеток в ККМ не угнетены;
- в стадию рецидива — более 5% бластов, либо без изменений.
- Цитохимическое (на ферменты) и иммуногистохимическое (на клеточные маркеры) исследование.
- Генетическое исследование: транслокация генов на 4, 11, 9, 22 хромосоме.
- Спинномозговая пункция: бластоз, увеличение белка в ликворе.
Виды лечения:

Химиопрепараты — терапия выбора при лейкозе
- Полихимиотерапия — лечение сочетанием цитостатических и стероидных препаратов, действие которых направлено на уничтожение клона атипичных клеток.
Фазы лечения: Лекарства: индукция ремиссии преднизолон, винкристин, аспарагиназа, метотраксат, 6-меркаптопурин, циклофосфамид консолидация ремиссии 6-меркаптопурин, аспарагиназа, метотрексат реиндукция ремиссии лекарства первой фазы поддерживающая терапия 6-меркаптопурин и метотрексат
Химиотерапия проводится по специальным протоколам лечения:
- ALL-BFM 95m — утверждён в 1990 году, рассчитан на 6 месяцев интенсивной терапии и до 2 лет поддерживающей терапии;
- ALL-MB — утверждён в 2002 году, рассчитан на 8 месяцев интенсивной терапии с поддержкой лекарствами до 2 лет.
Профилактика ОЛЛ:

Здоровый образ жизни- неотъемлемая часть профилактики
- Исключить воздействие радиации, химикатов, необоснованно назначенных лекарств.
- Использовать доброкачественные продукты питания, безопасные средства ухода за ребёнком.
- Исключить самолечение. Вовремя обратиться к врачу при возникновении у ребёнка: внезапного увеличения лимфоузлов, клиники анемии, некротической ангины, кровотечений, повышенной температуры.
- Женщинам рекомендуется планировать беременность, исследоваться на носительство вирусов, избегать вредные воздействия на организм при беременности (радиация, антибиотики, цитостатики, алкоголь, никотин, наркотики).
Прогноз

Прогноз благоприятный в возрасте 1-9 лет
Прогноз благоприятен при возникновении ОЛЛ у детей 1-9 лет, сравнительно невысоких цифрах бластов в ККМ и периферической крови, хорошем отклике организма на химиотерапию (снижение бластов ККМ до 5% за 1 месяц лечения), при отсутствии повреждения ЦНС.
Неблагоприятным прогнозом считается ОЛЛ у новорождённых и детей старше 9-10 лет, с вовлечением головного мозга, высоким бластозом ликвора, крови, костного мозга, при плохом ответе на терапию (5-25% бластов в ККМ через 1 месяц лечения), при выявлении Т-клеточного иммунофенотипа и транслокаций генов между 9 и 22, 4 и 11 хромосомами.
Как развивается острый лимфобластный лейкоз у детей
Клетки крови (лейкоциты, эритроциты, тромбоциты) производятся костным мозгом и затем разносятся по кровеносной системе.
Двумя основными типами лейкоцитов являются миелоидные и лимфоидные клетки. Они главным образом сконцентрированы в лимфатических узлах, селезенке, вилочковой железе (тимусе) и желудочно-кишечном тракте, обеспечивая наш иммунитет для борьбы с инфекциями.
В норме костный мозг продуцирует три типа лимфоцитов, борющихся с инфекциями:
B-лимфоциты – они формируют антитела против болезнетворных микробов;
T-лимфоциты – уничтожают инфицированные вирусом или инородные клетки, раковые клетки. Они также помогают вырабатывать антитела;
Натуральные киллеры (NK-клетки) – их задача уничтожать вирусы и раковые клетки.
При ОЛЛ костный мозг начинает вырабатывать слишком много дефектных лимфоцитов. Эти клетки, называемые бластами, несут в себе аномальный генетический материал и не могут бороться с инфекциями так же эффективно, как обычные клетки. Кроме того, бласты довольно быстро делятся и вскоре начинают вытеснять здоровые лейкоциты, эритроциты и тромбоциты из крови и костного мозга. Как результат, развивается анемия, инфекции, или даже легкое кровотечение.
Аномальные лимфоциты, характерные для острого лимфобластного лейкоза, довольно быстро разносятся кровотоком и могут затронуть жизненно-важные органы: лимфоузлы, печень, селезенку, центральную нервную систему, половые органы (яички у мужчин или яичники у женщин).
В Международном классификаторе болезней 10-го пересмотра выделяют три разновидности ОЛЛ:
C91.0 Острый лимфобластный лейкоз
C92 Миелоидный лейкоз [миелолейкоз]
C93.0 Острый моноцитарный лейкоз
Всемирная организация здравоохранения (ВОЗ) выделяет несколько разновидностей этого заболевания. Основывается оно на типе лейкоцитов, которые являются источниками бластных клеток:
Острый лимфобластный лейкоз у детей: причины
Онкологи выделяют несколько факторов, которые значительно повышают риск развития ОЛЛ у детей:
родной брат (сестра), перенесший лейкемию;
воздействие радиации или рентгеновских лучей до рождения;
лечение химиотерапией или другими препаратами, ослабляющими иммунную систему;
наличие некоторых наследственных заболеваний, таких как синдром Дауна;
определенные генетические мутации в организме.
У острого лимфобластного лейкоза есть несколько подтипов. Они зависят от трех факторов:
из каких лимфоцитов (группы B или T) начали образовываться бластные клетки;
наличие генетических изменений внутри клеток.
Симптомы острого лимфобластного лейкоза у детей
появление синяков и кровоподтеков;
темно-красные пятна под кожей;
узелки под мышками, на шее или в паху;
трудности с дыханием;
жалобы на боль в суставах;
общая слабость и быстрая утомляемость;
потеря аппетита и необъяснимая потеря веса.
Наличие этих симптомов может и не означать ОЛЛ и указывать на иное заболевание. Однако в любом случае что-либо из этого перечня уже повод обратиться к врачу.
Первым шагом в постановке диагноза ОЛЛ является осмотр и сбор семейного анамнеза. В первую очередь онколог проверит наличие характерных опухолей в районе шеи, проведет опрос о прошлых заболеваниях и лечении.
Однако, чтобы убедиться в наличии болезни, врачу потребуется анализ крови и костного мозга, а также, вероятно, образцы других тканей.
Наиболее распространенные методики:
Подсчет количества эритроцитов и тромбоцитов в крови, а также проверка количества и типа лейкоцитов и их внешний вид.
Биопсия и аспирация костного мозга – небольшой образец спинномозговой ткани и жидкости берется из бедренной кости или грудины. Затем он проверяется под микроскопом на наличие аномальных клеток.
Молекулярно-цитогенетический анализ. Он необходим, чтобы отследить аномалии в генетическом материале лимфоцитов.
Проточная цитометрия (иммунофенотипирование). Исследуются определенные характеристики клеток пациента. При ОЛЛ помогает определить, с чего началось появление бластов – T-лимфоцитов или B-лимфоцитов.
Помимо этих анализов могут быть и дополнительные лабораторные тесты. Онколог также может назначить другие процедуры, чтобы определить, распространился ли рак за пределы крови и костного мозга. Эти результаты будут важны, чтобы спланировать курс лечения.
Дополнительные тесты могут включать в себя:
рентген грудной клетки, компьютерную томографию или УЗИ;
поясничную пункцию (забор спинномозговой жидкости из позвоночника).
Основные риски для детей с острым лимфобластным лейкозом
Лечение ОЛЛ может иметь долгосрочные последствия для памяти, способности к обучению и других аспектов здоровья. Помимо прочего это также может увеличить шансы развития иных онкологических заболеваний, особенно опухоли мозга.
ОЛЛ, как правило, очень быстро прогрессирует, если не приступить к лечению немедленно.
Как избежать острого лимфобластного лейкоза у детей
Медицине не известны способы профилактики ОЛЛ. Болезнь может развиваться и абсолютно здоровых малышей, которые до этого ничем не болели. О факторах рисках мы написали выше.
Лечение острого лимфобластного лейкоза у детей
Лечение ОЛЛ обычно проходит в несколько этапов:
Первый этап - индукционная терапия (лечение при помощи электромагнитных волн). Цель этой фазы - убить как можно больше бластных клеток в крови и костном мозге;
Второй этап – консолидирующая химиотерапия. Во время этой фазы необходимо уничтожить бласты, оставшиеся после первого этапа. Они могут быть неактивными, однако, обязательно начнут размножаться и вызовут рецидив;
Третий этап – поддерживающая терапия. Цель здесь та же самая, что и на втором этапе, но дозы лекарств значительно ниже. При этом поддерживающая терапия крайне важна, чтобы избавиться от негативных последствий химиотерапии.
На протяжении всего курса лечения у ребенка будут регулярно брать новые анализы крови и костного мозга. Это необходимо, чтобы выяснить насколько хорошо организм реагирует на лечение.
Стратегия борьбы с ОЛЛ будет варьироваться в зависимости от возраста ребенка, подтипа заболевания и степени риска для здоровья. В общих чертах для лечения острого лимфобластного лейкоза у детей используют пять видов лечения:
Лучевая терапия. Представляет собой метод лечения ионизирующей радиацией, которая убивает раковые клетки и останавливает их рост. Источником излучения может быть специальный аппарат (внешняя лучевая терапия) или радиоактивные вещества, доставляемые в организм или непосредственно к источнику раковых клеток (внутренняя лучевая терапия). При лечении ОЛЛ онкологи назначают лучевую терапию только в самых крайних случаях с высоким риском, поскольку радиация крайне негативно сказывается на развитии мозга, особенно у детей младшего возраста.
Таргетная (молекулярно-таргетная) терапия. Используется для целевого выявления и уничтожения раковых клеток без ущерба для всего организма. Препараты, называемые ингибиторами тирозинкиназы, блокируют фермент, который стимулирует рост бластных клеток, вызванный специфическими генетическими мутациями.
Кортикостероиды. Детям с ОЛЛ часто назначают курс кортикостероидных препаратов, таких как преднизон или дексаметазон. Однако у этих препаратов могут быть различные побочные эффекты, включая набор веса, повышение сахара в крови, опухание лица.
Новым подходом при лечении острого лимфобластного лейкоза у детей является так называемая CAR-T терапия, или адаптивная клеточная терапия. Препарат изготавливается из крови самого пациента. Клетки модифицируются таким образом, чтобы позволить им идентифицировать аномальные бластные клетки и устранить их.
Нужно понимать, что лечение острого лимфобластного лейкоза всегда рискованно и сопровождается множеством побочных эффектов. Они могут включать:
Информация для родителей
Что такое лимфомы?
Лимфомы относятся к группе гемобластозов, то есть опухолевых заболеваний, которые развиваются из клеток крови. Условно к гемобластозам причисляют:
- лейкозы — с первичной локализацией в костном мозге
- нелейкемические гемобластозы — характеризующиеся опухолевой локализацией вне костного мозга. Это неходжкинские лимфомы и лимфома Ходжкина.
Распространенность НХЛ у детей:
- В детском возрасте НХЛ занимают 3 место среди всей онкологической патологии, составляя 5-7%.
- Частота заболевания у детей до 15 лет составляет 1:700-750 человек. Мальчики болеют чаще, чем девочки. Пик заболеваемости приходится на возраст от 3 до 9 лет.
- Крайне редко НХЛ встречаются у детей до 3-х лет.
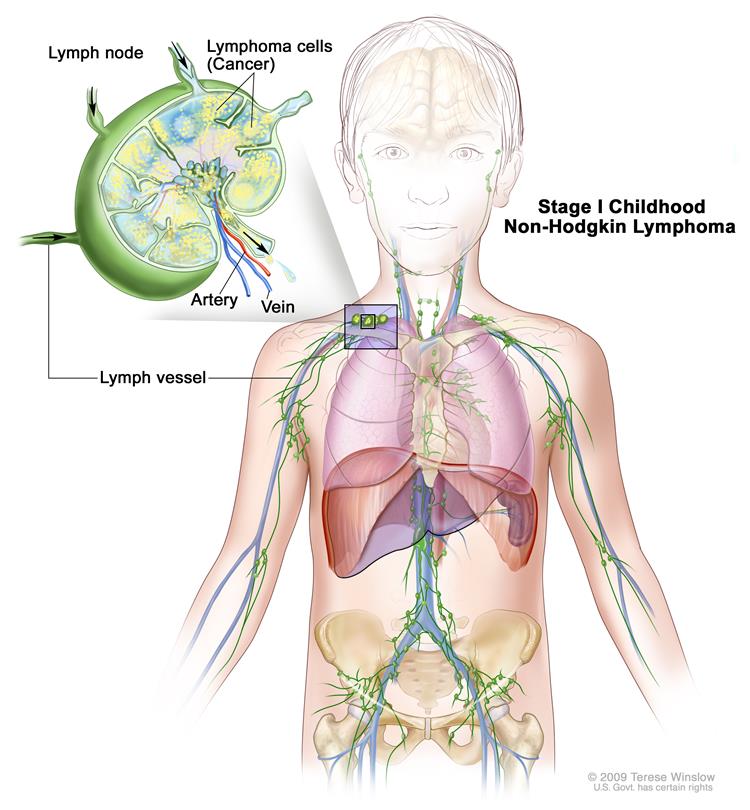
Причины развития лимфом
Болезнь начинает развиваться, когда лимфоциты мутируют, то есть злокачественно изменяются. Почему это происходит, неизвестно. Лимфоциты — это группа белых клеток крови, которые находятся, в основном, в лимфатической ткани. Поэтому неходжкинские лимфомы могут появляться везде, где есть лимфатическая ткань. Чаще всего болезнь развивается в лимфатических узлах. Но она также может развиваться в других лимфоидных тканях и лимфоидных органах, например, селезёнке, тимусе (вилочковой железе), миндалинах и лимфатических бляшках тонкого кишечника.
Некоторые вирусы могут провоцировать возникновение НХЛ. В ряде исследований была установлена возможная связь вирусов и некоторых форм НХЛ.
Клинические стадии НХЛ
- I стадия — поражение опухолью отдельных лимфоузлов одной анатомической группы или поражение одной лимфоидной ткани. За исключением поражения лимфоидной ткани внутри груди и в брюшном пространстве.
- II стадия — поражение опухолью лимфоузлов нескольких анатомических групп или поражение других лимфоидных тканей с локальным распространением и без локального распространения. Но все пораженные опухолью регионы находятся по одну сторону диафрагмы.
- III стадия — поражение опухолью лимфоузлов или лимфоидной ткани с обеих сторон диафрагмы. Или опухоль поразила лимфоидную ткань или другие органы внутри груди — средостение, плевра, вилочковая железа, легкие. Также обширные неоперабельные опухоли в брюшной полости.
- IV стадия — поражение опухолью центральной нервной системы (ЦНС) и (или) костного мозга.
Неходжкинские лимфомы у детей и подростков характеризуются быстрым прогрессированием онкологического процесса. Опухоль растет так быстро, что большинство детей поступают в клинику уже в III-IV стадии заболевания.
Однако, вне зависимости от стадии процесса, лимфомы в детском возрасте имеют хорошую чувствительность к химиотерапевтическому лечению, что позволяет излечить до 80% пациентов.
Группы неходжкинских лимфом
В зависимости от вида раковых клеток под микроскопом и от их молекулярно-генетических особенностей выделяют разные виды лимфом.
Согласно классификации ВОЗ лимфомы делятся на две крупные группы: В-клеточные лимфомы и Т/NK-клеточные лимфомы. Среди них, в свою очередь, выделяют лимфомы из клеток-предшественников (В- и Т-лимфобластные лимфомы) и опухоли из зрелых клеток.
Клинические симптомы лимфом
Нередко первым проявлением заболевания становится увеличение лимфатических узлов, которые, как правило, не болят, приобретают каменистую плотность, сливаются в конгломераты. Лимфатические узлы могут определяться в области головы, на шее, руках, ногах, в подмышечных впадинах, паховых областях, в грудной или брюшной полостях. Часто болезнь переходит на другие органы — селезенку, печень, мозговые оболочки, кости, костный мозг.
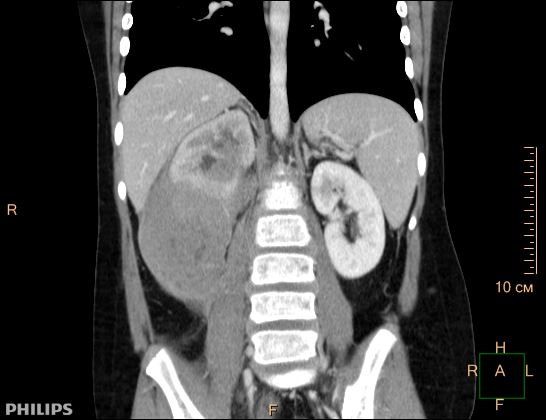
Рис. 1. Узловое образование правой почки, сливающееся с конгломератом увеличенных забрюшинных лимфатических узлов – специфическое поражение при лимфоме
Нередко увеличиваются печень и селезенка.
При локализации опухолевого процесса в грудной клетке типичными жалобами становятся кашель, затрудненное дыхание и глотание, иногда – потеря голоса.
Очень грозным осложнением, развивающимся при резком и значительном увеличении лимфатических узлов средостения является синдром сдавления верхней полой вены. Он проявляется нарушением дыхания, отеком и синюшностью лица и шеи. Появление этих симптомов угрожает жизни больного и требует незамедлительного обращения за медицинской помощью.
Кроме того, может развиваться скопление жидкости в плевральной полости и околосердечной сумке, что также быстро приводит к возникновению дыхательных расстройств.
Заболевание может манифестировать с появления жалоб на заложенность носа, нарушение дыхания, ощущение инородного тела при глотании, что встречается при поражении лимфоглоточного (Вальдейерова) кольца. При осмотре отмечается увеличение миндалин, свисание опухоли из носоглотки, которая нередко закрывает вход в ротоглотку. При этой локализации наиболее часто обнаруживаются увеличенные шейные и подчелюстные лимфатические узлы.
При купании и переодевании ребенка родители могут заметить появление узловатых образований величиной от горошины до размера грецкого ореха, плотной консистенции телесного или синюшно-красноватого цвета с возможным изъязвлением на поверхности. Так проявляет себя поражение мягких тканей при лимфоме. Излюбленной локализацией мягкотканных образований является волосистая часть головы, передняя грудная и брюшная стенка, спина.
У мальчиков заболевание нередко может проявляться увеличением размеров мошонки.
При поражении центральной нервной системы характерны такие симптомы, как головная боль, нарушение зрения, слуха, речи, парезы и параличи.
Первичное поражение костей у детей и подростков встречается редко (2-4%). При этом поражаются кости таза, лопатки, трубчатые кости с наличием различных размеров участков разрушения костной структуры.
Методы диагностики лимфом у детей и подростков
При появлении у ребенка жалоб, описанных выше, необходимо незамедлительно обратиться к педиатру. Если история болезни ребёнка, тщательный осмотр, результат клинического анализа крови, а также ультразвуковое и/или рентгенологическое обследование позволяют заподозрить неходжкинскую лимфому, ребенка направляют в специализированную клинику детской онкологии и гематологии.
В специализированном стационаре проводится комплексное обследование:
- Анализ опухолевой ткани: исследование пораженного лимфатического узла или другой пораженной ткани. Образцы материала получают хирургическим путем. Опухолевую ткань отправляют на цитологический, иммунологический и генетический анализы. По результатам этих исследований можно точно сказать, заболел ли ребёнок неходжкинской лимфомой, и если да, то какой именно её формой.
- Определение распространенности болезни в организме: ультразвуковое исследование органов брюшной полости, забрюшинного пространства и малого таза, компьютерная томография грудной клетки, брюшной полости и малого таза, магнитно-резонансная томография головного и спинного мозга (если есть показания). Чтобы проверить, попали ли опухолевые клетки в центральную нервную систему, проводят люмбальную пункцию – берут спинномозговую жидкость и исследуют, есть ли в ней опухолевые клетки или нет. Также всем детям выполняют пункцию костного мозга, чтобы узнать, успели ли в него попасть злокачественные клетки или нет.
- Для оценки работы сердца проводят электрокардиографию и Эхо-кардиографию.
- Комплексные лабораторные исследования: клинические анализы крови, мочи, биохимический анализ крови с оценкой функции почек и печени, определением мочевой кислоты, электролитов, лактатдегидрогеназы (ЛДГ), исследование свертывающей системы крови (коагулограмма), определение группы крови и резус-фактора.
Современные программы лечения неходжкинских лимфом у детей основаны на индивидуальном подходе с учетом различных морфологических и клинических вариантов заболевания.
Общие принципы лечения неходжкинских лимфом
- При I и II стадиях заболевания применяется менее интенсивная химиотерапия.
- При всех вариантах НХЛ у детей обязательно проводится профилактика поражения центральной нервной системы.
- При интенсивной программной полихимиотерапии лимфом из зрелых клеток у детей лучевая терапия не показана.
- Полихимиотерапия проводится на фоне комплекса адекватной сопроводительной терапии.
Лечение зрелых Т- и В-клеточных лимфом
Для терапии зрелоклеточных лимфом применяется жесткое, но непродолжительное лечение (до полугода) с использованием высокодозной полихимиотерапии и иммунотерапии (рис. 2).
Лечение проводится короткими интенсивными курсами — от 2 до 6. Их количество зависит от стадии болезни и группы риска ребенка. Для определения группы риска учитываются такие параметры, как радикальность операции (если она была), размеры и локализация опухоли, уровень ЛДГ в крови и поражение костного мозга и центральной нервной системы.
Для терапии зрелых В-клеточных лимфом, клетки которых экспрессируют CD20-антиген, используется таргетный препарат ритуксимаб (мабтера, ацеллбия).
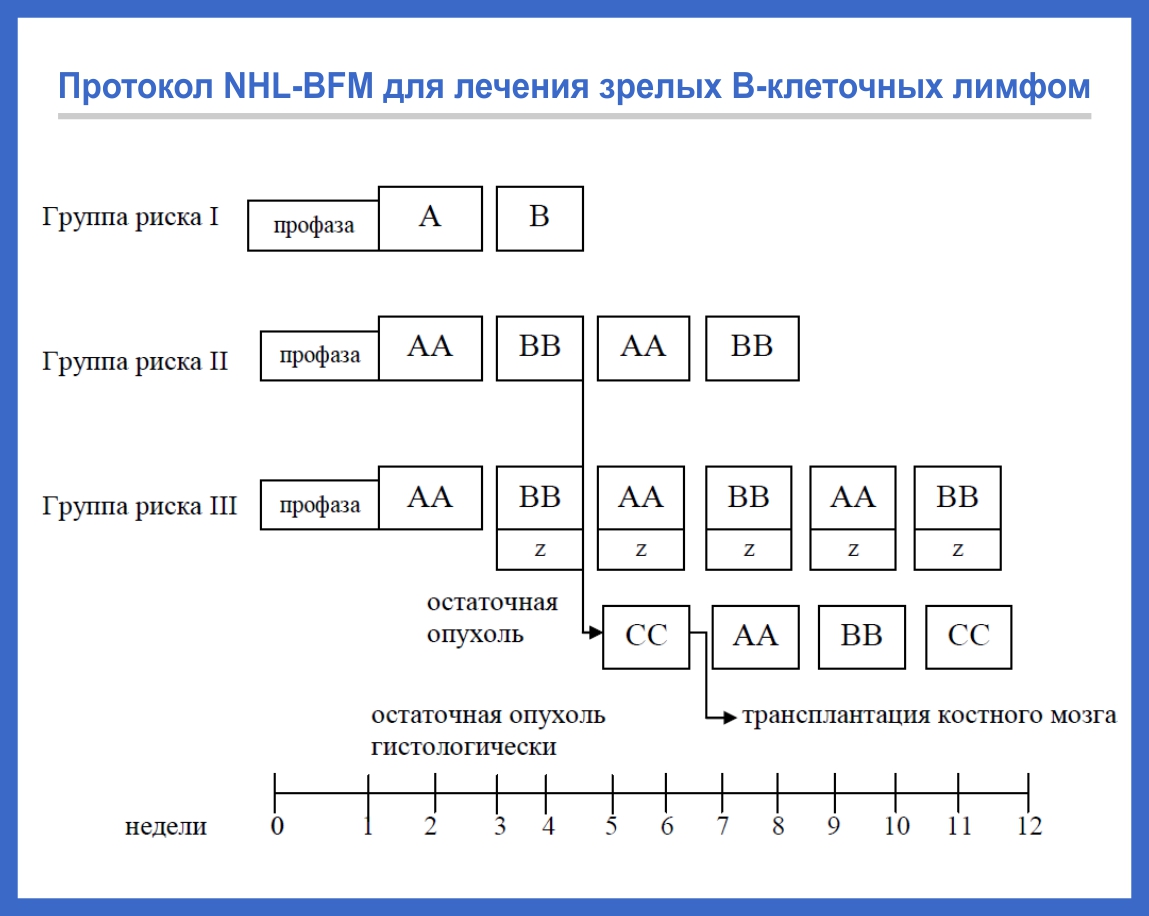
Рис. 2. Протокол NHL-BFM для лечения зрелых В-клеточных лимфом
Лечение лимфобластных лимфом из Т- и В-предшественников
Лечение детей с лимфобластной лимфомой — длительное, непрерывное в течение 2 лет. Оно состоит из нескольких следующих друг за другом фаз: профаза, индукция – протокол I, консолидация – протокол М, реиндукция – протокол II, профилактика поражения центральной нервной системы. Рис. 3.
Для профилактики поражения ЦНС используются введение химиопрепаратов в спинномозговой канал и лучевая терапия. Поддерживающая терапия проводится в течение 1,5 лет.
Интенсивность программы лечения зависит от стадии заболевания.
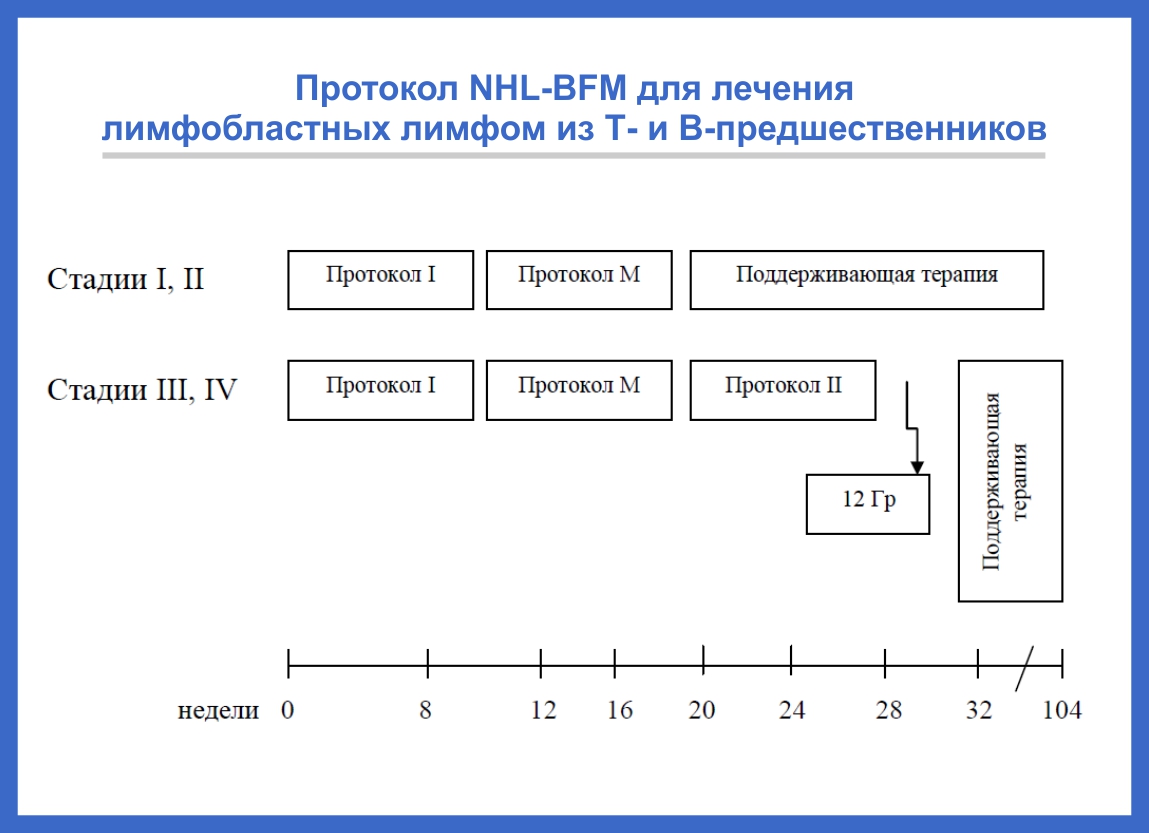
Рис. 3. Протокол NHL-BFM для лечения лимфобластных лимфом из Т- и В-предшественников
Диспансерное наблюдение при НХЛ
Динамическое наблюдение за детьми и подростками проводится в течение не менее 3-х лет после завершения лечебной программы.
В первые 3 месяца пациент обследуется каждый мес, в последующие 9 месяцев – каждый квартал, затем раз в полгода.
Обследование включает осмотр пациента с оценкой жалоб, клинический и биохимический анализы крови с определением ЛДГ, УЗИ очагов первичного поражения, рентгенограмм грудной клетки, по показаниям используются КТ/МРТ.
В последние годы для динамического наблюдения за излеченными больными с целью ранней диагностики рецидива широкое распространение получил метод ПЭТ/КТ всего тела с глюкозой.


Авторская публикация:
КУЛЕВА СВЕТЛАНА АЛЕКСАНДРОВНА
заведующая отделением химиотерапии и комбинированного лечения злокачественных опухолей у детей, доктор медицинских наук
Читайте также:

