Десмоидная опухоль в молочной железе
Zorka Inic 1 , Gordana Pupic 1 , Marko Buta 1 , Merima Oruci 1 , Radan Dzodic 1,2
1) Институт Онкологии и Радиологии Сербии, Белград
2) Университет Медицинской Школы Белграда
В статье представлен клинический случай десмоидной опухоли молочной железы у 38-летней пациентки.
Материалы и методы. У 38-летней пациентки диагностирована опухоль в нижнемедиальном квадранте, в складке под левой молочной железой, с инфильтрацией мягких тканей и увеличенными подмышечными лимфатическими узлами. Клинически и радиографически опухоль была крайне подозрительна на рак.
Результаты. Приведены данные осмотра, ультрасонографии, маммографии и цитологического исследования опухоли, напоминающей рак молочной железы. Объем операции включал широкую резекцию нижнемедиального квадранта левой молочной железы с большой порцией большой грудной мышцы. Исследование замороженных срезов было неинформативно.
В этом клиническом примере гистологическое исследование не выявило рак молочной железы и возможное вовлечение кожи и большой грудной мышцы и подтвердило наличие фиброматоза без инфильтрации кожи и мышечной ткани. Это обусловило широкую резекцию молочной железы с чистыми краями резекции. В связи с подозрением на злокачественное поражение, клинически увеличенные лимфатические узлы I и II порядка в левой подмышечной области, подмышечная лимфаденэктомия была выполнена вместе с биопсией сторожевого лимфатического узла. Плановое гистологическое исследование показало фолликулярную дисплазию подмышечных лимфатических узлов.
Выводы. Фиброматоз молочной железы является крайне редкой патологией. Стандартное первичное лечение – хирургическое, когда оно возможно. Цель операции – получить чистые края резекции с сохранением функции и хорошим косметическим результатом. Принципы оперативного вмешательства включают резекцию единым блоком. Объем хирургического лечения различен, от широкой туморэктомии до радикальной мастэктомии с удалением грудной фасции и грудных мышц. Мы не рекомендуем выполнять подмышечную лимфаденэктомию до получения гистологического анализа биопсии сторожевого лимфатического узла, несмотря на наличие клинически суспициозной опухоли в молочной железе и увеличенных подмышечных лимфатических узлов.
Ключевые слова: десмоидная опухоль молочной железы, фиброматоз, сторожевой лимфатический узел.
Распространенность десмоидных опухолей молочной железы (агрессивного фиброматоза) составляет менее 0,2% первичных новообразований молочной железы [1, 2].
Фиброматоз – это инфильтративная пролиферация фибробластов и клеток мышечных волокон, не обладающая метастатическим потенциалом, но со склонностью к местному рецидивированию [3].
Десмоидная опухоль молочной железы является клинической дилеммой, поскольку клинически, по данным ультрасонографии, маммографии и цитологически ее трудно отличить от рака, и только гистологическое исследование может подтвердить диагноз. Лечение выбора – широкое иссечение с чистыми краями резекции 5.
В этой статье мы описываем 38-летнюю пациентку с опухолью в нижнемедиальном квадранте, в складке под левой молочной железой, с инфильтрацией мягких тканей и увеличенными подмышечными лимфатическими узлами. Клинически и радиографически опухоль была крайне подозрительна на рак. Новообразование было полностью иссечено с резекцией окружающей железистой тканью и клетчаткой с чистыми краями резекции. Мы, безусловно, превысили необходимый объем оперативного вмешательства в связи с клиническими и диагностическими подозрениями, но состояние пациента хорошее с отличными косметическими результатами, лечение прошло без каких-либо осложнений, без рецидива заболевания.
Пациентка 38 лет при самостоятельном осмотре обнаружила опухоль в левой молочной железе. У пациентки не было никаких оперативных вмешательств или травм в области груди. Семейный анамнез по злокачественным новообразованиям не отягощен.
При физикальном осмотре имелись признаки фиброзной дисплазии обеих молочных желез, выявлена опухоль около 1,5 см в диаметре, плотная, неподвижная, вовлекающая кожу и расположенная в складке под левой молочной железой, в нижнемедиальном квадранте, ближе к грудине. У пациентки имелись пальпируемые увеличенные лимфатические узлы I и II порядка в левой подмышечной области.
При ультрасонографии выявлена гетерогенная гипоэхогенная опухоль в складке под левой молочной железой, с неоднородным внутренним эхо и относительно нечеткими границами с затуханием кзади. Опухоль была диаметром 1,5 см, располагалась близко к грудной фасции, которая в других участках была гиперэхогенна и интактна (BI RADS 4-5).
При маммографии в нижнемедиальном квадранте левой молочной железы выявлено дольковое затемнение 16×8 мм.
Перед операцией выполнена лимфосцинтиграфия, коллоид с 99mTc вводили периареолярно. При лимфосцинтиграфии выявлен сторожевой узел в левой подмышечной области. В проекции внутренней грудной артерии фиксации радиоколлоида не было.
Пациентке выполнена широкая резекция нижнемедиального квадранта левой молочной железы с большой порцией большой грудной мышцы. Исследование замороженных срезов было неинформативно.
С помощью гамма-датчика верифицирован горячий лимфатический узел II уровня, который был удален через отдельный разрез и направлен на плановое гистологическое исследование. В связи с клинически увеличенными и суспициозными лимфатическими узлами в левой подмышечной области выполнена лимфодиссекция I и II уровней.
По данным гистологического исследования: фиброматоз молочной железы, опухоль 8×18×12 мм, хорошие края резекции и отсутствие элементов фиброматоза в краях резекции.
При иммуногистохимическом исследовании обнаружена положительная реакция на актин (рис.1), виментин (рис.2) и десмин, CD34 и CD 68, фолликулярная гиперплазия в лимфатических узлах (0/13) и сторожевом лимфатическом узле расценена как гистиоцитоз синусов и липоматоз лимфатических узлов.
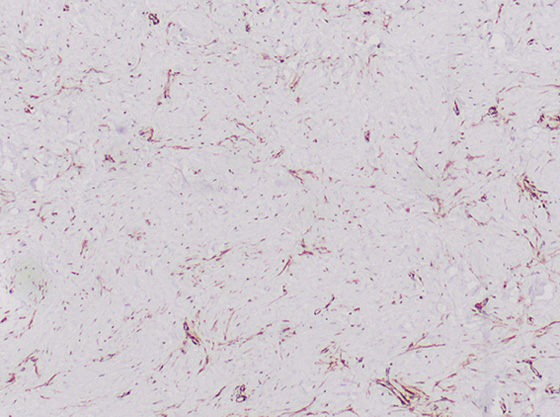
Рис. 1. Гистологическая картина: положительная реакция на актин (гематоксилин и эозин, x4).
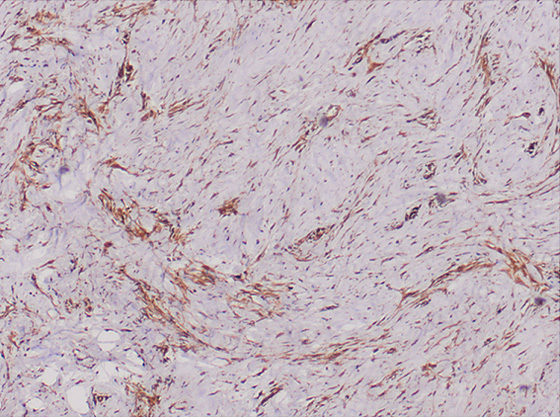
Рис. 2. Гистологическая картина: положительная реакция на виментин (гематоксилин и эозин, x4).
Десмоидная опухоль впервые была обнаружена MacFarlane в 1832 г. [7].
Десмоидные опухоли составляют примерно 0,03% всех новообразований и менее 3% всех опухолей мягких тканей.
Предположительная ежегодная заболеваемость в общей популяции составляет 2-4 на 1 млн. населения [8].
Причина развития десмоидных опухолей полностью не объяснена, но выявлена связь с семейным аденоматозным полипозом (синдром Гарднера), протезированием молочной железы и хирургической травмой. Десмоидные опухоли встречаются у 10-15% пациентов с семейным аденоматозным полипозом, заболеванием, наследуемым по аутосомному типу, обусловленным мутацией в гене APC [9].
Отсутствие мутаций генов H-ras, K-ras и N-ras и генов p53 в этих опухолях свидетельствует о том, что инактивация генов APC играет роль в индукции агрессивного роста десмоидных опухолях с наивысшей частотой рецидивирования. Это составляет важную часть молекулярного механизма образования десмоидных опухолей [10].
Несмотря на повышенную встречаемость у молодых женщин детородного возраста, десмоидные опухоли также обнаруживают у мужчин, но редко [11].
Избыток эстрогенов, например, во время беременности, считают значимым предрасполагающим фактором развития десмоидных опухолей [3, 11].
В десмоидных опухолях обнаруживают хромосомные аномалии, включая делецию хромосомы 5q [12, 13], потерю хромосомы Y [13], трисомию 8 [14] и трисомию 20 [15]. Считают, что трисомия 8, в частности, служит прогностическим фактором рецидива.
Фиброматоз молочной железы проявляется клинически как крайне серьезное солитарное поражение, которое в некоторых случаях вовлекает грудную фасцию за счет локальной инфильтрации [16]. Он может также вызывать втяжение соска и имитировать рак молочной железы [11].
Эти доброкачественные мезенхимальные опухоли, исходящие из мышечной фасции или апоневроза, хотя и не обладают метастатическим потенциалом, но могут быть местно-агрессивными с частотой рецидивирования 23-40% [17].
Радикальное первичное хирургическое лечение играет важную роль для длительного контроля заболевания, при этом обязательны точная предоперационная диагностика и хорошо спланированная операция [18].
Наиболее эффективный метод лечения десмоидных опухолей – полное иссечение. Повторное иссечение рецидивных опухолей оправдано.
Высокодозная лучевая терапия также эффективна для контроля рецидива заболевания и также может подходить для первичного лечения, когда это служит единственной альтернативой калечащей операции [19].
В 1928 г. Ewing был первым, кто в качестве контроля десмоидных опухолей применил лучевую терапию [20].
Помимо лучевой терапии, к другим возможным методам лечения нерезектабельных опухолей или при необходимости удаления прилежащих структур относят гормональную терапию, лечение цитостатиками и противовоспалительными препаратами [11].
Ясно, что многие авторы высказываются в пользу ранней диагностики и широкого иссечения фиброматоза, ограниченного молочной железой и не вовлекающего соседние структуры грудной полости. Эта местная хирургическая стратегия приведет к излечению огромного числа пациентов с фиброматозом только молочной железы и может помочь избежать необходимости дальнейшей радикальной резекции для получения чистого края [21].
В этом клиническом примере гистологическое исследование не выявило рак молочной железы и возможное вовлечение кожи и большой грудной мышцы и подтвердило наличие фиброматоза без инфильтрации кожи и мышечной ткани. Это обусловило широкую резекцию молочной железы с чистыми краями резекции. В связи с подозрением на злокачественное поражение, клинически увеличенные лимфатические узлы I и II порядка в левой подмышечной области, подмышечная лимфаденэктомия была выполнена вместе с биопсией сторожевого лимфатического узла. Плановое гистологическое исследование показало фолликулярную дисплазию подмышечных лимфатических узлов.
Мы, безусловно, превысили необходимый объем лечения нашей пациентки, но у нее нет каких-либо осложнений после подмышечной лимфаденэктомии, получен отличный косметический результат (рис. 3).
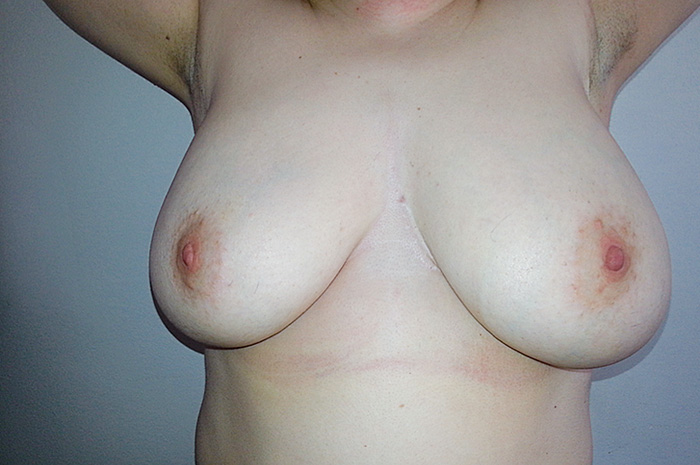
Рис. 3. Отличный косметический результат после операции.
Фиброматоз молочной железы является крайне редкой патологией. Стандартное первичное лечение – хирургическое, когда оно возможно. Цель операции – получить чистые края резекции с сохранением функции и хорошим косметическим результатом. Принципы оперативного вмешательства включают резекцию единым блоком. Объем хирургического лечения различен, от широкой туморэктомии до радикальной мастэктомии с удалением грудной фасции и грудных мышц. Мы не рекомендуем выполнять подмышечную лимфаденэктомию до получения гистологического анализа биопсии сторожевого лимфатического узла, несмотря на наличие клинически суспициозной опухоли в молочной железе и увеличенных подмышечных лимфатических узлов.
Нашей пациентке выполнена широкая (en bloc) резекция с удалением части грудной фасции и порции большой грудной мышцы. Пациентка находилась под динамическим наблюдением в течение 3 лет, у нее отсутствуют признаки рецидива, получен отличный косметический результат.
- Neuman HB, Brogi E, Ebrahim A. Desmoid tumors (fibromatoses) of the breast: a 25-year experience. Ann Surg Oncol 2008; 15: 274-80.
- Devouassoux-Shisheboran M, Schammel MD, Man YG, Tavassoli FA. Fibromatosis of the breast: age-correlated morphofunctional features of 33 cases. Arch Pathol Lab Med 2000; 124: 276-80.
- Basak Erguvan-Dogan, Peter J Dempsey, Geetha Ayyar, Michael Z. Gilcrease. Primary desmoid tumor (extraabdominal fibromatosis) of the breast. AJR 2005; 185(2): 488-9.
- Stephen P Povoski, Rafael E Jimenez. Fibromatosis (desmoid tumor) of the breast mimicking a case of ipsilateral metachronous breast cancer. World J Surg Oncol 2006; 4: 57 doi:10.1186/1477-7819-4-57.
- Ng WH, Lee JS, Poh WT, Wong CY. Desmoid tumor (fibromatosis) of the breast. A clinician's dilemma – a case report and review. Arch Surg 1997; 132(4): 444-6.
- Winnie Yeo, Peter Teo, Wing Kwan, Michael Suen. Desmoid tumor mimicking local recurrence of carcinoma of the breast. Int J Clin Oncol 1998; 3(1): 49-51.
- McFarlane J. Clinical report of the surgical practices of Glasgow Royal Infirmary. Glasgow: Roberson, 1832; 63-6.
- Reitamo JJ, Häyry P, Nykyri E, Saxén E. The desmoid tumor. I. Incidence, sex-, age- and anatomical distribution in the Finnish population. Am J Clin Pathol 1982; 77: 665.
- Brueckl WM, Ballhausen WG, Förtsch T, Günther K, Fiedler W, Gentner B, Croner R, Boxberger F, Kirchner T, Hahn EG, Hohenberger W, Wein A. Genetic testing for germline mutations of the APC gene in patients with apparently sporadic desmoid tumors but a family history of colorectal carcinoma. Dis Colon Rectum 2005; 48(6): 1275-81.
- Michiko Miyaki, Motoko Konishi, Rei Kikuchi-Yanoshita, Masayuki Enomoto, Kiyoko Tanaka, Hiromi Takahashi. Coexistence of somatic and germ-line mutations of apc gene in desmoid tumorsfrom patients with familial adenomatous polyposis. Cancer Res 1993; 53, 5079-82. Advances in Brief.
- Torres Sousa MY, Arias Ortega M, Rozas Rodríguez ML, Murillo Lázaro CM. Fibromatosis of the breast in a 52-year-old man. Eur Radiol 2011; 21(7): 1575.
- Wara WM, Phillips TL, Hill DR, Bovill EG, Luk KH, Lichter AS, Liebel SA. Desmoid tumors. Treatment andprognosis. Radiology 1977; 124: 225-6.
- Dangel A, Meloni AM, Lynch HT, Sandberg AA. Deletion(5q) in a desmoid tumor of a patient with Gardner_syndrome. Cancer Genet Cytogenet 1994; 74: 94-8.
- Bridge JA, Sreekantaiah C, Mouron B, Neff JR, SandbergAA, Wolman SR. Clonal chromosomal abnormalities indesmoid tumors. Cancer 1992; 69: 430-6.
- Fletcher JA, Naeem R, Xiao S, Corson JM. Chromosome aberrations in desmoid tumors. Cancer Genet Cytogenet 1995; 79: 139-43.
- Appelbaum AH, et al. Mammographic appearances of male breast disease. Raiographics 1999; 19: 559-68.
- Pajares B, Torres E, Jiménez B, Sevilla I, Rodríguez A, Rico JM, Trigo JM, Alba E. Multimodal treatment of desmoid tumours: the significance of local control. Clin Transl Oncol 2011; 13(3):189-93.
- Mátrai Z, Tóth L, Szentirmay Z, Vámos FR, Klepetko W, Vadász P, Kenessey I, Kásler M. Sporadic desmoid tumors of the chest: long-term follow-up of 28 multimodally treated patients. Eur J Cardiothorac Surg 2011; 40(5): 1170-6. Epub 2011 Mar 23.
- Easter DW, Halasz NA. Recent trends in the management of desmoid tumors. Summary of 19 cases and review of the literature. Ann Surg 1989; 210(6): 765-9.
- Ewing J. Neoplastic Diseases. 3rd ed. Philadelphia: W.B. Saunders, 1928.
- Stephen P Povoski, William L Marsh, Dimitrios G Spigos, Abbas E Abbas, Brentley A Buchele. Management of a patient with multiple recurrences of fibromatosis (desmoid tumor) of the breast involving the chest wall musculature. World J Surg Oncol 2006; 4: 32 doi:10.1186/1477-7819-4-32.
Сайт использует файлы cookies для более комфортной работы пользователя. Продолжая просмотр страниц сайта, вы соглашаетесь с использованием файлов cookies, а также с обработкой ваших персональных данных в соответствии с Политикой конфиденциальности.

Общие сведения
Фиброма — это доброкачественное опухолевидное образование, имеющее фиброзно-соединительнотканную структуру и не обладающее метастатическим потенциалом. В целом, фиброматоз представляет собой патологический процесс, характеризующийся замещением фибропластов и коллагеновых волокон на соединительную ткань. Визуально фиброма представляет собой плотной консистенции эластичное инкапсулированное образование сероватого цвета, для которого характерен медленный экспансивный рост. Благодаря экспансивному росту фиброма легко вылущивается. На разрезе опухоли: поверхность блестящая без кровоизлияний и некрозов, содержит неравномерно распределенные сосуды. Признаки анаплазии отсутствуют, могут встречаться единичные митозы. Микроскопически состоит из полностью дифференцированных беспорядочно расположенных в разнообразных направлениях соединительнотканных клеток, между которыми определяется множество коллагеновых волокон.
Фиброма может развиваться на самых разнообразных тканях: на слизистых оболочках, коже, сухожилиях и локализоваться в самых различных участках тела: молочной железе, яичниках, матке, стенке желудка. Влияние фибромы на организм и значение этой опухоли определяется ее локализацией. Так, фиброма кожи опасности для организма не представляет, а ее локализация в глазнице, на основании черепа, спинномозговом канале может быть причиной неблагоприятного исхода.
Значительно реже встречается десмоидная фиброма (син. десмоид и агрессивный фиброматоз) представляющая собой мезенхимальную опухоль, которая развивается из дифференцированных фибропластов и коллагеновых волокон. Ее отличительной особенностью является высокая склонность к инфильтрирующему (местнодеструирующему) росту и быстрому рецидивированию (в 15–42% случаев), однако метастазы наблюдаются крайне редко. Десмоиды, как правило, локализуются в мягких тканях, чаще в забрюшинном пространстве/передней брюшной стенке и крайне редко десмоидные опухоли встречаются в молочной железе (0,2% от всей патологии).
Десмоидные фибромы относятся к некапсулированным опухолям, для которых характерна тенденция распространения по фасциальной поверхности в виде узких тяжей на значительное расстояние (10-30 см) от основной опухоли, а также способность разрушать прилегающие костные структуры, окружающие нервы и кровеносные сосуды.
Десмоидные фибромы относится к крайне редко встречающей форме (2-4 случая/1 млн человек/ од). При этом в России на сегодняшний день среди страдающих десмоидными фибромами преобладают лица женского пола удельный вес которых составляет порядка 80%. Ускоряет рост опухоли беременность. Десмоидная опухоль возникает преимущественно у женщин в возрасте 20-40 лет, преимущественно у рожавших пациенток (в 94% случаев). У лиц мужского пола десмоид выявляется чаще в детском/подростковом возрасте.
То есть, десмоидная опухоль в той или иной степени является гормонозависимой, поскольку в ее ткани обнаружены эстрогеновые рецепторы. Соответственно к значимым признакам ее диагностики относятся: нарушение соотношения между андрогенами и эстрогенами. На сегодняшний день локальный контроль за десмоидными фибромами осуществляется операционным путем, однако, при каждом последующем рецидиве опухоли десмоид протекает все более агрессивнее (возрастает численность опухолевых зачатков), а безрецидивный интервал укорачивается. При этом, нарастает риск прорастания десмоида в магистральные сосуды, что может приводить к инвалидизации пациента.
По соотношению паренхимы и стромы выделяют два вида фибром:
- Плотную, для которой характерно преобладание коллагеновых волокон. Твердые фибромы располагаются на широком основании, ножки не имеет. Размер может достигать 1,5 см в диаметре с локализацией по всему телу. Встречается в любом возрасте, гендерные отличия отсутствуют.
- Мягкую с преобладанием клеток и немногочисленными волокнами, волокнистая ткань рыхлая, отечная.
- Фибромы мягкого типа — образования мягкой консистенции на тонкой ножке размером до 1 см светло-коричневого цвета. Мягкие фибромы более характерны для зоны под грудью, подмышечных зон, области спины. Одновременно может формироваться несколько фибром. Чаще диагностируются у женщин после 35 лет.
Патогенез
Патогенез обусловлен нарушением процесса дифференциации клеток и до конца не изучен. На развитие фибромы десмоидного типа влияет мутация в гене CTNNB1 (бетакатенина), вследствие чего нарушается процессы метаболизма в ядре фибробластов, что приводит к нарушению дифференцировки клеток, вызывая их избыточную пролиферацию и неконтролируемый рост.
Классификация
По форме выделяют мягкую, твердую фибромы и фибромы десмоидного типа.
В зависимости от локализации: фиброма кожи, фиброма матки, фиброма молочной железы.
Десмоидные фибромы по локализации делятся на:
- Интраабдоминальные (фибромы забрюшинного пространства).
- Абдоминальные (фибромы передней брюшной стенки).
- Экстраабдоминальные (фибромы конечностей, туловища).
- Мультифокальные фибромы (множественные опухоли различной локализации).
Причины
К основным причинам, способствующим развитию фибром, относятся:
- Генетическая предрасположенность.
- Нарушения функций эндокринной системы/гормональный сбой.
- Негативные репродуктивные факторы (ранее начало и нарушение менструального цикла, прерывание беременности/отсутствие беременности и родов, позднее наступление климакса, злоупотребление гормональными средствами контрацепции/препаратами и др.).
- Нарушение метаболизма — ожирение, сахарный диабет, патологии щитовидной железы.
- Частые травмы/повреждения кожного покрова, травмы груди, конечностей.
- Воспалительные заболевания кожи.
- Избыточное потоотделение.
- Длительное/частое воздействие ультрафиолетового излучения.
- Несбалансированное питание.
Симптомы
Клиническая симптоматика определяется локализацией и размерами фибром. Рассмотрим лишь некоторые локализации фибром.
Фиброматоз молочной железы, как уже указывалось, достаточно редкое явление. Симптоматически фиброма грудной железы у женщин появляется при пальпации как округлая легкоподвижная безболезненная опухоль плотной консистенции с гладкой поверхностью. Фиброма молочной железы небольших размеров в большинстве случаев субъективно дискомфорта не доставляет. Десмоидные фибромы грудной железы растут с многократно рецидивирующей инвазией в окружающие ткани, прилегающие лимфоузлы в большинстве случаев не увеличены. Реже за счет локальной инфильтрации в процесс вовлекается грудная фасция. Иногда патологический процесс может вызывать втяжение соска, имитируя рак молочной железы.
Клиническим проявлением фиброматоза кожи является возникновение на любом из участков тела мягких/твердых образований в виде бугорков. При пальпации пациент может ощущать незначительную боль. При локализации в некоторых местах могут нарушаться функции конечностей. Так, например, подошвенный фасциальный фиброматоз проявляется болями во время ходьбы, сгибательной контрактурой пальцев ноги с ограничением подвижности стопы.
Чаще встречается мягкая фиброма кожи. Фибромы кожи могут появляться на любом участке тела: на лице, голове, руках и ногах, пальцах (мизинце). Ниже приведены фото фибромы кожи на разных участках тела: на руке под кожей на ладони (ладонный/ладонно-пальцевый фиброматоз), на ноге, на голове, на пальце.
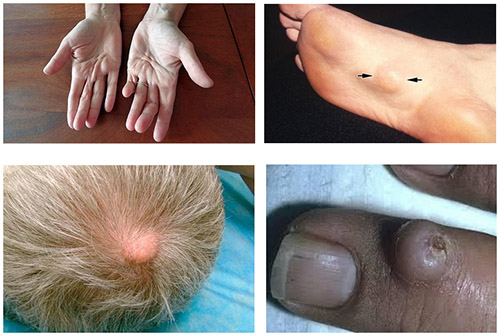
Твердые фибромы жесткие и упругие при пальпации, цвет кожи в пределах новообразования не изменен. Наиболее распространенной их локализацией являются верхние/нижние конечности, встречаются у мужчин.
Мягкая фиброма может располагаться по всему телу, но чаще встречаются на шее, веках, туловище, в подмышечных впадинах, в паху, у женщин в зоне декольте. При расположении в местах трения (на шее, под мышками) они могут воспалиться, что проявляется болезненностью и покраснением.
Экстраабдоминальный десмоидный фиброматоз под кожей при локализации на конечности в поздней стадии проявляется не только болями, но и нарушением чувствительности, что обусловлено сдавлением/вовлечением в процесс нервных окончаний, а также прогрессирующими ограничениями подвижности суставов, разрушением костного вещества.
Анализы и диагностика
Для установления диагноза используются следующие инструментальные процедуры: УЗИ молочных желез, маммография, ренгеногарфия, КТ/МРТ, радиовизиография. При необходимости производят биопсию опухоли и цитологическое исследование биоптата.
Лечение фибром
Лечение фибром сводится преимущественно к их удалению. В настоящее время удаление фибромы может проводится различными методами:
Операция малоинвазивная, проводится в условиях амбулатории под местным обезболиванием. Вначале производится разрез кожи и удаление фибромы лазером, который выпаривает опухолевидную ткань c одновременной коагуляцией сосудов, питающих фиброзную опухоль, что позволяет минимизировать кровотечение в момент деструкции. Воздействие лазерного луча до корня образования (на заданную глубину) исключает риск рецидива. Благодаря минимальной травматизации окружающих тканей послеоперационный восстановительный период очень короткий.
Основан на бесконтактном испарении фиброзных клеток высокочастотными радиоволнами с одновременной коагуляцией сосудов при практическом отсутствии риска инфицирования.
Проводится иссечение фибромы скальпелем новообразований значительных размеров и с глубокой локализацией, когда другие методы слабо эффективны. Проводится хирургическая резекция под местной анестезией, после чего накладываются швы.
Способ применим для небольших/неглубоких образований. В основе воздействие электрического тока на ткани фибромы, что вызывает термическое поражение тканей и отторжение опухоли.
Лечение фибром десмоидного типа проводится с использованием гормонотерапии, методов лучевой и химиотерапии. Такая комбинированная терапия позволяет снизить частоту развития рецидивов. Согласно литературным данным, низкодозная химиотерапия с цитостатиками Метотрексатом/Винбластином в течение 3-4 месяцев в целом по эффективности не уступает другим комбинациям химиотерапии, но при этом нежелательные побочные действия наблюдаются значительно реже. В случаях больших десмоидных опухолей с наличием инфильтрации для достижения быстрого эффекта используется схема VAC (Винбластин, Цисплатин, Ондансетрон, Доксорубицин).
В случаях нарушения гормонального статуса женщинам назначают антиэкстроген Тамоксифен или Золадекс. При лечении гормонозависимых фибром следует ориентироваться на пол пациента, динамику концентрации половых гормонов, объём и локализацию опухоли.
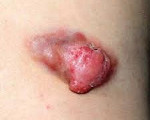
Десмоидная опухоль – опухоль, развивающаяся из мышечно-апоневротических структур и занимающая промежуточное положение между доброкачественными и злокачественными новообразованиями. Склонна к прорастанию окружающих тканей, но не дает отдаленных метастазов. Может возникать на любом участке тела, чаще локализуется в области передней брюшной стенки, спины и плечевого пояса. Представляет собой плотное опухолевидное образование, расположенное в толще мышц или связанное с мышцами. При прогрессировании может прорастать сосуды, кости, суставы и внутренние органы. Диагноз выставляется на основании осмотра и данных дополнительных исследований. Лечение – оперативные вмешательства, лучевая терапия, химиотерапия.
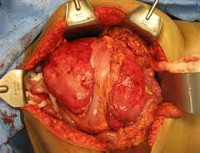
- Причины и патанатомия десмоидной опухоли
- Симптомы десмоидной опухоли
- Диагностика и лечение десмоидной опухоли
- Цены на лечение
Общие сведения
Десмоидная опухоль (десмоид, десмоидная фиброма, мышечно-апоневротический фиброматоз) – редкая соединительнотканная опухоль, развивающаяся из фасций, мышц, сухожилий и апоневрозов. Микроскопически лишена признаков злокачественности и никогда не дает отдаленных метастазов, при этом склонна к местному агрессивному росту и частому рецидивированию (нередко многократному), поэтому онкологи рассматривают десмоид как условно-доброкачественное новообразование. Составляет 0,03-0,16% от общего количества новообразований. В 64-84% случаев страдают женщины.
У представительниц слабого пола десмоидная опухоль обычно возникает на втором или третьем десятилетии жизни, в 94% случаев выявляется у рожавших пациенток, в 6% случаев – у нерожавших. У больных мужского пола десмоид чаще диагностируется в детском или подростковом возрасте. В постпубертатном периоде количество случаев заболевания у мужчин резко уменьшается. Обычно наблюдается медленное прогрессирование. Диагностику и лечение десмоидных опухолей осуществляют специалисты в области онкологии, дерматологии, хирургии, травматологии и ортопедии.

Причины и патанатомия десмоидной опухоли
Причины развития десмоидной опухоли пока остаются невыясненными. В качестве одного из самых вероятных факторов специалисты рассматривают травматические повреждения мышц, связок и апоневрозов (в том числе – в процессе родов у женщин). Кроме того, исследователи указывают на возможную связь десмоидной опухоли с уровнем половых гормонов и некоторыми генетическими нарушениями. По статистике, десмоид диагностируется у 20% пациентов, страдающих семейным аденоматозом – наследственным заболеванием, обусловленным генетической мутацией.
Десмоидная опухоль представляет собой плотный, как правило, одиночный узел, имеющий волокнистое строение. Цвет новообразования на разрезе серовато-желтый. При микроскопическом исследовании десмоидной опухоли видны пучки коллагеновых волокон, расположенные в разных направлениях и переплетающиеся между собой. Выявляются зрелые фиброциты и фибробласты. Митозы возникают очень редко. При исследовании визуально неизмененных окружающих тканей, иссеченных вместе с новообразованием, могут обнаруживаться микроскопические элементы опухоли.
Симптомы десмоидной опухоли
Десмоидная опухоль может развиваться в любой части тела, однако чаще всего располагается на передней поверхности брюшной стенки. К числу достаточно распространенных локализаций также относятся спина и область плечевого пояса. На грудной клетке, верхних и нижних конечностях десмоидные опухоли появляются редко, однако, такие новообразования имеют особое значение, поскольку часто располагаются близко к костям и суставам, интимно спаиваются с близлежащими образованиями или прорастают их, нарушая подвижность суставов, прочность и опорность костей.
Десмоидные опухоли на руках и ногах всегда локализуются на сгибательной поверхности конечности. В зависимости от особенностей поражения тканей различают четыре клинических типа экстраабдоминальных десмоидных опухолей: одиночный узел с поражением окружающей фасции, одиночный узел с поражением фасциальных влагалищ на протяжении, множественные узлы на различных участках тела и злокачественное перерождение десмоида – превращение новообразования в десмоид-саркому.
Наряду с экстраабдоминальными выделяют интраабдоминальные и экстрабрюшные десмоидные опухоли, которые могут располагаться в брыжейке тонкой кишки, в забрюшинном пространстве, области мошонки и мочевого пузыря. Подобные новообразования выявляются реже периферических десмоидов и десмоидов передней брюшной стенки. Десмоидные опухоли в области брыжейки нередко сочетаются с семейным аденоматозом. Симптомы заболевания зависят от локализации и размера новообразования, наличия или отсутствия прорастания близлежащих органов и тканей.
Для десмоидной опухоли характерен медленный рост и малосимптомное течение. При десмоидных опухолях большого размера может наблюдаться болезненность. При прорастании суставов возможны контрактуры, при прорастании костей – патологические переломы, при прорастании внутренних органов – нарушения функции этих органов. В ходе внешнего осмотра обнаруживается плотное малоподвижное новообразование округлой или овальной формы с гладкой поверхностью, располагающееся в толще мышц либо связанное с мышцами и связками.
Диагностика и лечение десмоидной опухоли
Диагноз выставляют на основании осмотра, данных инструментальных исследований и результатов биопсии. Пациентов с десмоидной опухолью направляют на УЗИ, КТ и МРТ. Наиболее информативным методом исследования, позволяющим установить границы опухоли и степень ее инвазии в окружающие ткани, является магнитно-резонансная томография. При необходимости назначают ангиографию сосудов и другие исследования. При прорастании сосудов, нервов, внутренних органов и костных структур может потребоваться консультация сосудистого хирурга, невролога, абдоминального хирурга, торакального хирурга, травматолога, ортопеда и других специалистов.
Из-за высокой вероятности рецидивирования десмоидных опухолей предпочтительным является комбинированное лечение, включающее в себя хирургические операции и лучевую терапию. В ряде случаев применяют химиотерапию и гормональную терапию. По различным данным, десмоидные опухоли рецидивируют в 70-90% случаев после оперативного лечения, использованного в качестве монометодики. Проведение комбинированной терапии позволяет существенно уменьшить частоту рецидивов.
Операция по возможности должна быть радикальной. При наличии одиночного узла его удаляют вместе с пораженной фасцией и окружающими мышцами. При распространении десмоидной опухоли по фасциальному влагалищу иссекают фасцию на протяжении. При прорастании костных структур осуществляют удаление кортикальной пластинки или резецируют костную ткань. При поражении внутренних органов, близком расположении сосудов и нервов тактику операции определяют индивидуально.
Иссечение большого массива тканей при крупных десмоидных опухолях ведет к образованию дефектов. При возможности такие дефекты устраняют сразу после удаления опухоли, осуществляя местную пластику, используя костные ауто- и гомотрансплантаты и т. д. В ряде случаев в отдаленном периоде проводят пластические операции. При поражении близлежащего сустава конечности может потребоваться эндопротезирование. При множественных десмоидных опухолях показано поэтапное хирургическое лечение с особо радикальным удалением окружающих тканей, поскольку такие новообразования проявляют повышенную склонность к рецидивированию.
Взрослым пациентам с десмоидной опухолью назначают предоперационную и послеоперационную лучевую терапию. Недостатком метода являются выраженные постлучевые изменения тканей. Трофические нарушения и крупные рубцы, возникающие после проведения лучевой терапии, могут усложнять повторное хирургическое лечение в случае рецидивирования. В процессе лечения больных детского возраста лучевую терапию не применяют из-за возможного преждевременного закрытия ростковых зон кости в области облучения. При десмоидных опухолях у детей осуществляют оперативные вмешательства на фоне предоперационной и послеоперационной медикаментозной терапии. Пациентам назначают низкие дозы цитостатиков и антиэстрогеновые препараты. Продолжительность медикаментозного лечения десмоидной опухоли может составлять до 2 и более лет.
Прогноз при комбинированном лечении, включающем в себя хирургическое вмешательство и лучевую терапию или хирургическое вмешательство и химио-гормональную терапию, относительно благоприятный. Рецидивы выявляются у 10-15% больных, обычно – в течение 3 лет после удаления десмоидной опухоли. Чаще всего рецидивируют десмоиды, расположенные в области стопы и голени. Отдаленные метастазы не образуются. Летальный исход возможен при прорастании жизненно важных органов, обычно – при расположении десмоидной опухоли в области головы, шеи, живота и грудной клетки.
Читайте также:

