Б я алексеев рак почки
Полный текст:
- Аннотация
- Об авторе
- Список литературы
- Cited By
Современная практика назначения таргетных агентов у пациентов с метастатическим раком почки (РП) основана на результатах нескольких крупных многоцентровых рандомизированных исследований, в которых изучалась эффективность различных препаратов в различных клинических ситуациях. Большинство международных и национальных онкологических и урологических ассоциаций рекомендуют в качестве терапии первой линии у больных метастатическим РП с хорошим и промежуточным прогнозом 3 стандартных варианта лечения: бевацизумаб в комбинации с интерфероном, сунитиниб и пазопаниб.
Одним из актуальных вопросов реальной клинической практики является обоснованный выбор препарата для проведения терапии первой линии. Критериями выбора препарата являются в первую очередь его эффективность и профиль токсичности. Кроме того, особенности статуса здоровья пациента, наличие различных интеркуррентных заболеваний, образ жизни и профессиональные особенности также влияют на выбор схемы лечения. В статье приводится сравнительный обзор эффективности и токсичности бевацизумаба в комбинации с интерфероном в различных дозах, сунитиниба и пазопаниба, на основании которого можно планировать в конкретной клинической ситуации выбор препарата для терапии больных метастатическим РП с хорошим и промежуточным прогнозом.
3. Escudier B., Eisen T., Porta C. et al. Renal cell carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and followup. Ann Oncol 2012;23(Suppl 7): vii65-vii71.
4. Motzer R.J., Hutson T., Tomczak P. et al. Overall survival and updated results for sunitinib compared with interferon alfa in patients with metastatic renal cell carcinoma. J Clin Oncol 2009;27(22):3584–90.
5. Escudier B., Pluzanska A., Koralewski P. et al. AVOREN Trial investigators. Bevacizumab plus interferon alfa-2a for treatment of metastatic renal cell carcinoma: A randomised, double-blind phase III trial. Lancet 2007;370:2103–11.
6. Sternberg C.N., Davis I.D., Mardiak J. et al. Pazopanib in locally advanced or metastatic renal cell carcinoma: results of a randomized phase III trial. J Clin Oncol 2010;28(6):1061–8.
7. Motzer R.J., Hutson T.E., Cella D. et al. Pazopanib versus sunitinib in metastatic renal-cell carcinoma. N Engl J Med 2013;369(8):722–31.
8. Negrier S., Gwenaelle G., Peroll D. et al. Temsirolimus and bevacizumab, or sunitinib, or interferon alfa and bevacizumab for patients with advanced renal cell carcinoma (TORAVA): a randomised phase 2 trial. Lancet Oncol 2011;12:673–80.
9. Motzer R.J., Barrios C.H., Kim T.M. et al. Record-3: Phase II randomized trial comparing sequential first-line everolimus (EVE) and second-line sunitinib (SUN) versus first-line SUN and second-line EVE in patients with metastatic renal cell carcinoma (mRCC). J Clin Oncol 2013;31(suppl);abstr 4504.
10. Melichar B., Bracarda S., Matveev V. et al. A multinational phase II trial of bevacizumab with low-dose interferon-α2a as first-line treatment of metastatic renal cell carcinoma: BEVLiN. Ann Oncol 2013;24(9):2396–402.
11. Patard J.-J., Rioux-Leclercq N., Fergelot P. Understanding the importance of smart drugs in renal cell carcinoma. Eur Urol 2006;49:633–43.
12. Hurwitz H.I., Saltz L.B., Van Cutsem E. et al. Venous thromboembolic events with chemotherapy plus bevacizumab: a pooled analysis of patients in randomized phase II and III studies. J Clin Oncol 2011;29(13):1757–64.
13. Melichar B., Koralewski P., Ravaud A. et al. First-line bevacizumab combined with reduced dose interferon-a2a is active in patients with metastatic renal cell carcinoma. Ann Oncol 2008;19:1470–6.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
- КЛЮЧЕВЫЕ СЛОВА: онкология, урология, онкоурология, онкологические заболевания
В последние годы имеется стойкая и уверенная тенденция к увеличению доли больных раком предстательной железы и раком почки, у которых эти заболевания выявляются на ранних стадиях. В определенном смысле можно сказать, что диагностировать мы научились лучше, чем лечить: к сожалению, своевременное выявление новообразования и вовремя проведенное радикальное лечение еще не являются гарантией того, что болезнь не будет прогрессировать.
Означает ли это, что внедрение онкоурологических скрининговых программ в повседневную практику нецелесообразно?
Разумеется, нет. По данным наших европейских коллег, смертность от рака предстательной железы у мужчин, принимавших участие в скрининговых программах, была на 27% ниже, чем у тех, кто не попал в эти программы.
Сейчас в некоторых регионах нашей страны, например в Воронежской и Пензенской областях, стартуют пилотные проекты по скринингу онкозаболеваний предстательной железы. Пока в качестве основного анализа в данных программах используется тест на PSA, но в научных институтах уже ведется поиск других маркеров злокачественных новообразований простаты, возможно, в скором времени в распоряжении врачей появится принципиально новая панель урологических онкомаркеров.
Вы имеете в виду маркеры рака предстательной железы или различных онкоурологических заболеваний?
Говоря о скрининговых программах в онкоурологии, мы в первую очередь говорим о раннем обнаружении злокачественных новообразований предстательной железы. Дело в том, что любая скрининговая программа должна решать две задачи: способствовать снижению смертности от данного заболевания и уменьшать затраты государства на лечение больных, последующую реабилитацию, инвалидизацию и т.д. Именно поэтому скрининговые программы, если мы говорим о скрининге онкологических заболеваний, в первую очередь ориентированы на раннее выявление таких социально значимых заболеваний, как рак предстательной железы, рак молочной железы и рак легкого.
Впрочем, онкоурологами предпринимались попытки внедрения программ ранней диагностики рака мочевого пузыря. Мне эти программы представляются достаточно актуальными. А вот, скажем, рак почки и в отсутствие скрининговых программ в 70% случаев выявляется на ранних стадиях, поэтому на первый план выходит другая задача: определение биологической агрессивности опухоли и прогнозирование течения заболевания. Сегодня специалисты-онкоурологи уделяют много внимания вопросам предсказания поведения опухоли.
В октябре ожидается VI конгресс Российского общества онкоурологов. Будут ли на нем обсуждаться вопросы диагностики онкоурологических заболеваний и прогнозирования течения этих болезней?
Конечно, полностью обойти вопросы диагностики стороной невозможно, однако в первую очередь предстоящий конгресс будет посвящен проблемам лечения онкоурологических больных. Как я уже сказал, своевременное выявление новообразований онкоурологического профиля на сегодняшний день налажено достаточно хорошо, а вот лечение порой оказывается недостаточно эффективным. Именно поэтому в ходе предстоящего конгресса мы будем рассматривать судьбу онкоурологического больного от момента обнаружения у него новообразования до появления метастазов.
VI конгресс будет уже вторым мероприятием нашего общества, проводимым в не совсем привычной форме: вместо традиционных докладов мы планируем ряд дискуссий и круглых столов, в ходе которых участники конгресса будут обсуждать наиболее актуальные для современной онкоурологии темы. Это и радикальное хирургическое лечение, и радикальная лучевая терапия, применяемая на ранних стадиях, и вопросы наблюдения за больным, перенесшим лечение. Не останутся без внимания и методики так называемой спасительной терапии, проводимой в случаях, когда опухоль продолжает прогрессировать уже после проведения радикального лечения.
Большое внимание будет уделено и проблемам лечения больных с метастазами. Порой врачи просто не знают, что даже таким пациентам можно помочь, благодаря новым методикам и новым препаратам не просто продлив жизнь, но и улучшив ее качество.
Какие методики лечения будут обсуждаться на конгрессе в первую очередь?
В последние годы в онкоурологии наблюдался настоящий прорыв в области лапароскопической хирургии и малоинвазивных методик лечения, таких как радиочастотная термоабляция, фотодинамическая терапия, криоабляция и ультразвуковая абляция. Многие центры в России уже применяют эти методики лечения, однако для большинства клиник они пока недоступны. Хотелось бы, чтобы данные методы лечения получили более широкое распространение, так же как роботизированная хирургия, которая пока применяется лишь в шести отечественных центрах.
А что Вы можете сказать о фармакотерапии онкоурологических заболеваний? Будет ли в программе конгресса уделено внимание консервативным методикам лечения?
Что, по Вашему мнению, можно сделать, чтобы изменить эту ситуацию и сделать информацию о современных препаратах более доступной для практикующих врачей?
Российское общество онкоурологов сотрудничает с фармацевтическими компаниями, в частности, на предстоящем конгрессе пройдут 5 сателлитных симпозиумов. В ходе этих мероприятий участники конгресса смогут больше узнать о новых средствах для фармакотерапии онкоурологических заболеваний.
Однако мне бы хотелось, чтобы фармацевтические компании уделяли больше внимания проведению клинических исследований в региональных ЛПУ. Если врачи, работающие в научно-исследовательских центрах, могут принять участие в международных исследованиях, то у медиков, работающих в обычных онкодиспансерах, такой возможности нет.

- Опухоли почки
- Метастазы рака почки
- Как часто и у кого встречается рак почки?
- Диагностика опухолей почек
- Лечение рака почки на разных стадиях
- Цены в Европейской онкологической клинике на лечение рака почки
Опухоли почки
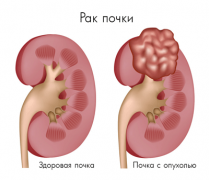
Второй характеристикой опухоли почки, как впрочем и большинства других опухолей, является потеря спецификации клетки – так как клетка быстро делится, она просто не успевает специализироваться. Таким образом, опухоль почки в первом приближении можно характеризовать, как массу клеток, бесконтрольно делящихся и потерявших способность к специализации. Чем меньше специализирована клетка опухоли для выполнения своей функции, чем быстрее она делится и чем больше его способность к распространению по кровеносным и лимфатическим сосудам, тем опухоль злокачественнее.
Почти 90 % опухолей почки злокачественны. Оставшиеся 10 процентов приходятся на ангиомиолипомы и другие, гораздо более редкие доброкачественные опухоли почки. Между тем, даже доброкачественные опухоли почки вполне могут быть опасны для здоровья. Например – ангиомиолипома может повредить сосуды почки, вызывая кровотечение. Что же касается злокачественных опухолей или рака почки, то тут мы сталкиваемся с повреждением функционирующей почечной ткани, ее сосудов и кровотечением, с метастазированием в кости, легкие, головной мозг и, соответственно, нестерпимыми болями.
Метастазы рака почки
Метастазирование — это распространение опухоли по кровеносным или лимфатическим сосудам. Опухоли, как и всему живому в организме, требуется питание, обеспечиваемое сосудами. Вот в эти сосуды и попадают 1-2 клетки из основной опухоли, которые распространяются на различные органы. Для рака почки характерно метастазирование в кости и легкие, а также в печень, надпочечники и головной мозг.
рака почки, как и основная опухоль, нарушает функцию органа, где развивается. Например, метастаз рака почки в легкие вызывает упорный кашель, метастаз в кости — страшные, изнуряющие боли, от которых помогают только сильнодействующие наркотические препараты. К сожалению, часть пациентов, обративших к врачу, уже имеют отдаленные метастазы в тех или иных органах. Это резко ухудшает прогноз течения заболевания, так как приходится бороться не с одной опухолью, а, по сути, с опухолями множеством опухолей в нескольких органах.
Как часто и у кого встречается рак почки?
Диагностика опухолей почек
При подозрении на рак почки пациенту назначают общий анализ мочи, общий и биохимический анализы крови.
Один из наиболее информативных методов диагностики рака почки – компьютерная томография. Она помогает оценить размер, форму и локализацию злокачественного новообразования, обнаружить очаги в лимфатических узлах и других анатомических структурах за пределами почек. Исследование нередко дополняют внутривенным контрастированием. Введение контраста противопоказано при нарушении функции почек.
Магнитно-резонансную томографию применяют реже, чем КТ. Она показана, когда пациенту нельзя проводить компьютерную томографию с контрастом, если имеется подозрение на прорастание опухоли в нижнюю полую вену или другие крупные сосуды, для обнаружения метастатических очагов в головном и спинном мозге.

Ангиография – рентгенография с контрастирование сосудов, почки. Она помогает в диагностике заболевания и планировании хирургического лечения.
Позитронно-эмиссионная томография помогает обнаружить вторичные очаги рака в различных частях тела. Суть метода в том, что в организм пациента вводят вещество, которое обладает слабой радиоактивностью и накапливается в опухолевых клетках. Затем выполняют снимки с помощью специального аппарата, и на них опухолевые очаги хорошо видны.
В отличие от других онкологических заболеваний, биопсия при раке почки проводится редко. Обычно результатов других исследований хватает для того, чтобы принять решение о необходимости хирургического вмешательства. Уже после операции удаленную опухоль направляют в лабораторию, чтобы подтвердить диагноз. Биопсию проводят, если другие исследования не позволяют разобраться, показана ли операция. В случаях, когда хирургическое вмешательство противопоказано, исследование опухолевой ткани помогает определиться с тактикой лечения.
В медицине нет категоричных, стопроцентных ответов. Какова цель операции по удалению рака почки? Удалить опухоль? Удалить почку с подлежащими структурами? Удалить только первичный очаг опухоли, а потом бороться с метастазами теми или иными способами? Перенесет ли пациент операцию, каково его общее состояние? Какую именно операцию выбрать для конкретного больного? На эти вопросы должен ответить онкоуролог, перед тем, как предложить хирургическое, консервативное или комбинированное лечение. В основном, это зависит от стадии рака почки, расположения опухоли, наличия метастазов в лимфатические узлы и общего состояния здоровья пациента.

Это зависит главным образом от стадии, на которой была диагностирована опухоль, и начато лечение. Пятилетняя выживаемость (процент пациентов, оставшихся в живых спустя 5 лет) наиболее высока для I стадии и составляет 81%. На II и III стадиях она, соответственно, составляет 74 и 53%. При IV стадии — 8%.
Стадия рака почки зависит от размеров и расположения опухоли. Так, рак почки первой стадии — это опухоль меньше 7 см, не выходящая за пределы почки. Рак почки второй стадии — это опухоль меньше 10 см, также не выходящая за пределы почки. А вот рак почки третьей стадии — это уже опухоль любых размеров, ограниченная почкой, либо повреждающая надпочечник, почечную вену, но имеющую метастаз в ближайших лимфатических узлах. Рак почки четвертой стадии может быть любых размеров, однако при этой стадии опухоль либо выходит за пределы почечной фасции, либо имеются больше одного метастаза в ближайших лимфатических узлах, либо имеются метастазы в легкие, кости, печень или головной мозг.
Стадию рака почки определяют в соответствии с международной классификацией TNM. Рядом с каждой из трех букв аббревиатуры указывают индекс, описывающий характеристики первичной опухоли (T), поражение регионарных лимфатических узлов (N), наличие отдаленных метастазов (M):
T1 – опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр не более 4 см (T1a) или 4–7 см (T1b).
T2 - опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр 7–10 см (T2a) или более 10 см (T1b).
T3 – злокачественное новообразование распространяется на почечную вену и ее ветви, на надпочечник на одноименной стороне, паранефральную клетчатку, не прорастая фасцию Героты (T3a), на нижнюю полую вену ниже (T3b) или выше (T3c) диафрагмы или врастает в стенку вены.
T4 – опухоль распространяется за пределы фасции Героты.
N0 – опухолевые очаги в регионарных лимфоузлах отсутствуют.
N1 – обнаруживается опухолевый очаг в одном лимфоузле.
N2 – обнаруживаются опухолевые очаги в двух и более регионарных лимфоузлах.
M0 – отдаленных метастазов нет.
M1 – отдаленные метастазы присутствуют.
В зависимости от значений T, N и M, выделяют четыре стадии рака почки:
- Стадия I: опухоль в почке не более 7 см (T1), лимфоузлы не поражены, отдаленных метастазов нет.
- Стадия II: первичная опухоль более 7 см (T2), отсутствуют очаги поражения в лимфатических узлах и отдаленные метастазы.
- Стадия III: злокачественная опухоль распространяется на соседние структуры (T3) и/или поражен один регионарный лимфатический узел (N1).
Стадия IV: опухоль распространяется на соседние структуры (T4), либо поражено 2 и более регионарных лимфоузла (N2), либо обнаружены отдаленные метастазы (M1).
Опухоль почки размером 2 см может быть расположена вблизи почечных сосудов и ее удаление технически может быть невозможным. Однако данные литературы указывают, что если нет метастазов в лимфатические узлы и отдаленные органы, то опухоль почки до 7 см можно удалять с сохранением почки, что, безусловно, лучше полного удаления почки и инвалидизации пациента.
Лечение рака почки на разных стадиях
Выбор тактики лечения при раке почки в первую очередь определяется стадией опухоли и состоянием здоровья пациента.
При стадиях I и II возможно хирургическое лечение. Стандартным вариантом считается нефрэктомия. К органосохраняющим операциям прибегают реже, в частности, при опухолях в единственной почке. Кроме того, на выбор объема операции влияет размер опухоли. Также удаляют близлежащие лимфатические сосуды, особенно если они увеличены, окружающую жировую клетчатку.
При III стадии рака почки основным методом лечения также является нефрэктомия, при этом должны быть удалены все регионарные метастазы. Если опухоль прорастает в почечную или нижнюю полую вену или мигрирует в их просвете в виде опухолевого тромба, пораженные ткани также нужно удалить, при этом может потребоваться подключение пациента к аппарату искусственного кровообращения.
При высоком риске рецидива после операции применяют адъювантную терапию таргетным препаратом сунитинибом. Пациенты получают его в течение года.
Если хирургическое вмешательство противопоказано, прибегают к радиочастотной аблации, эмболизации.
На IV стадии подходы к лечению могут быть разными, в зависимости от степени распространения рака в организме. В некоторых случаях возможно хирургическое лечение, в том числе циторедуктивные операции, во время которых хирурги не могут убрать опухоль полностью, но стараются удалить как можно больший ее объем. В редких случаев возможно удаление основной опухоли в почке и единичных вторичных очагов в других органах. После операции назначают курс таргетной терапии, иммунотерапии.
При неоперабельном раке почки основными методами лечения становятся иммунотерапия и таргетная терапия.

В некоторых случаях рак почки удается выявить на ранних стадиях, когда опухолевые клетки не распространяются за пределы органа. Но зачастую заболевание диагностируют на более поздних стадиях. Во-первых, это связано с тем, что рак почки может очень долго протекать бессимптомно. Во-вторых, для этого типа рака на данный момент не существует рекомендованных скрининговых исследований.
Все симптомы можно разделить на ренальные (связанные с поражением почек) и экстраренальные.
Среди ренальных проявлений рака почки наиболее характерны три:
- Гематурия (примесь крови в моче) – самый распространенный и зачастую первый симптом. Он возникает более чем у половины пациентов с раком почки. Моча приобретает красный цвет, при этом боль не беспокоит либо носит острый характер и возникает после гематурии. Этим злокачественная опухоль отличается от неопухолевых заболеваний почки, например, мочекаменной болезни, при которой обычно сначала возникает боль, а потом появляется примесь крови в моче. Гематурия периодически исчезает, но через некоторое время снова появляется, причем, промежутки между кровотечениями сокращаются. Количество крови в моче не зависит от размеров опухоли.
- Боли беспокоят около половины пациентов. Острая боль после гематурии возникает из-за того, что сгустки крови перекрывают просвет мочеточника. Тупые сильные боли зачастую говорят о плохом прогнозе.
- Пальпируемая опухоль – симптом, который выявляет врач во время осмотра примерно у трети пациентов.
Все три симптома одновременно встречаются у одного из десяти пациентов с раком почкеи. Обычно при этом выявляют запущенные опухоли.
Среди экстраренальных симптомов в первую очередь стоит отметить повышение температуры тела. У 5% больных лихорадка – единственное проявление заболевания. У некоторых пациентов повышается артериальное давление, отмечается покраснение лица из-за увеличения количества эритроцитов в крови, у мужчин – расширение вен мошонки (варикоцеле). На поздних стадиях снижается аппетит, пациент теряет вес без видимой причины, постоянно ощущает утомление, недомогание.
Для покупки документа sms доступом необходимо ознакомиться с условиями обслуживания
 | ВНИМАНИЕ! Услуга для абонентов NEO, Tele2 временно недоступна |
 | ВНИМАНИЕ! Услуга для абонентов Beeline, NEO, Tele2 временно недоступна |
Стоимость услуги - тенге с учетом комиссии.
Таргетная терапия распространенного рака почки сунитинибом
Алексеев Б.Я., Калпинский А.С.
Рак почки (РП) - одно из наиболее распространенных онкоурологических заболеваний. Около 210 тыс. новых случаев РП диагностируется в мире ежегодно, что в структуре онкологической заболеваемости составляет примерно 2% [1].
В 2007 году в России выявлено 16770 больных со злокачественными новообразованиями почки, что составило 4,13% у мужчин и 2,87% у женщин среди всех злокачественных новообразований. По темпам прироста онкологической заболеваемости в России РП устойчиво занимает третье место после рака предстательной и щитовидной железы (35,83 %). Ежегодно в России от РП умирает более 8 тыс. человек. Стандарти зо ванный показатель заболеваемости населения России злокачественными опухолями почки - 8,09 на 100 тыс. населения [2].
Рост заболеваемости РП частично обусловлен как улучшением диагностики на основе современных инструментальных исследований, таких как трансабдоминальное ультразвуковое исследование (УЗИ) и компьютерная томография (КТ), магнитно-резонансная томография (МРТ), так и ростом истинной заболеваемости РП. В настоящее время в 25-40% случаев заболевание выявляют случайно при профилактическом обследовании.
РП относится к агрессивным и непредсказуемым в своем течении злокачественным опухолям. При первичном обращении у 25-30% больных имеются отдаленные метастазы, а после хирургического лечения больных с локализованной и местнораспространенной стадиями заболевания вероятность возникновения рецидива и метастазов составляет 20-30% [1, 3]. Наиболее часто метастатические очаги обнаруживают в легких (55%), лимфатических узлах (34%), костях (32%), печени (32%), надпочечниках (19%), контралатеральной почке (11%) и головном мозге (5,7%) [4].
Показатели общей выживаемости больных диссеминированным РП также разочаровывают: медиана общей выживаемости не превышает 13 месяцев, 5-летняя выживаемость - не более 5%, поэтому проблема лечения данной группы больных крайне актуальна [1, 3].
Хирургическое вмешательство - единственный эффективный метод лечения РП, позволяющий излечить большинство больных на ранних стадиях заболевания [5].
Злокачественные опухоли почки нечувствительны к химиотерапии и гормонотерапии, что обусловлено наличием гена множественной лекарственной устойчивости РП. Несмотря на наличие эстрогеновых рецепторов в почечно-клеточных опухолях, использование гормональных препаратов не приводило к улучшению результатов лечения. Общий ответ на гормональную и химиотерапию составляет менее 5% [5, 6].
Лучевая терапия используется только у больных РП с нерезектабельными метастазами в головной мозг или костными метастазами, не отвечающими на другие консервативные методы лечения. Лучевая терапия костных метастазов позволяет значительно снизить болевой синдром и улучшить качество жизни больных [5].
Организаторами являлись общество онкоурологов Украины и Российское общество онкоурологов под эгидой Национального института рака при поддержке Министерства здравоохранения Украины. В работе конференции приняли участие более 450 онкоурологов, урологов, онкологов, химиотерапевтов и лучевых терапевтов стран СНГ, США и Европы.
В рамках конференции проводились дискуссии, круглые столы, тематические семинары, презентации новых изданий, выставки продукции ведущих фармацевтических компаний и медицинского оборудования Украины и России.

Участников конференции приветствовали директор института рака г. Киева И.Б. Щепотин - д.м.н., профессор и Матвеев В.Б. – д.м.н., профессор, президент РООУ, заведующий отделением урологии НИИ КО РОНЦ им. Н.Н. Блохина РАМН, г. Москва.
На 1-м заседании рассматривались новые методы в диагностике и лечении злокачественных новообразований почки, мочевого пузыря, простаты.
Братславский Геннадий (Нью-Йорк, США) отметил широкое использование ренальной биопсии под УЗ и КТ-контролем при раке почки. Упоминалась разработка молекулярных технологий в диагностике рака почки без инвазивного вмешательства с использованием радиологических методов. Докладчиком было отмечено, что по данным мультицентрового исследования за последние 5 лет результаты криоаблации и радиочастотной аблации уступают результатам резекции почки при наблюдении до 3х лет. Также было отмечено, что резекция почки по онкологическому прогнозу не уступает радикальной нефрэктомии и широко применяется и при Т2 , и при Т3. При этом было отмечено, что частота первичного мультифокального рака почки достигает от 4 до 25%. Несвоевременное выявление множественных очагов может быть расценено как рецидив после выполненной резекции.
Докладчиком также рассматривались вопросы о преимуществах роботассистированной резекции почки. Были представлены вниманию схемы лечения высокодозным интерлейкином-2. В последней части своего обширного доклада д-р Г. Браславский рассмотрел актуальность циторедуктивной нефрэктомии на основании результатов мультицентровых исследований. Он обратил внимание на увеличение продолжительности жизни при сочетании нефрэктомии с химиотерапией по сравнению с только химиотерапией. Также рассматривались вопросы о последовательности хирургического и химиотерапевтического лечения.
Профессор М. Бабюк (Прага, Чехия) осветил исследования по разработке биомаркеров рака мочевого пузыря и их клиническому применению.
Профессор Джован Б.(Нью-Йорк, США) вновь вернулся к значению уровня ПСА. Отмечено, что к группе риска относятся, скорее, не пациенты с субнормальными, но стабильными значениями, а больные с высокой скоростью повышения ПСА. В выступлении были упомянуты новые маркеры – интрамакрофагальный ПСА и маркеры мочи - uPM3(PSA3). Последний, однако, может оцениваться только в сочетании с сывороточным ПСА, что несколько снижает его ценность.
При ответе на вопросы из зала был отдельно отмечен ультрасенситивный ПСА, применяемый при диагностике биохимических рецидивов, в математическом обозначении которого имеется четыре цифры после запятой.
Второе заседание было посвящено почечно-клеточному раку.
В.Б. Матвеевым была освещена важнейшая хирургическая проблема - оперативное лечение рака почки с тромбозом нижней полой вены. Рассмотрены позиции, влияющие на принятие решения о необходимости протезирования НПВ:
- уровень резекции,
- степень и длительность окклюзии НПВ(более для частичной, чем для полной),
- симптомы (отёк нижних конечностей).
Представлены меры профилактики осложнений при протезировании НПВ:
- использование антикоагулянтов,
- создание артериовенозной фистулы,
- интерпозиция сальника между протезом и резецированным органом.
Указан основной ограничивающий фактор при тромбэктомии – блок печёночных вен с печёночной недостаточностью.
Профессором дан обзор периоперационных осложнений:
- высокая частота осложнений (до 70%) и смертности (3-16%);
- большая частота осложнений при левосторонних опухолях и протяжённых тромбах;
- у больных с протяжёнными тромбами более часто имеются явления недостаточности функции печени, почек, сердца и требуется более сложное хирургическое вмешательство.
Развёрнутый обзор таргетной терапии был дан В.Б. Матвеевым. О.А. Войленко представил доклад о циторедуктивной нефрэктомии, в котором было отмечено, что выживаемость больных, подвергшихся хирургическому лечению выше, чем только химиотерапии. Также им была отмечена необходимость удаления лёгочных метастазов, что иногда возможно посредством торакоскопиии.
На 3-м заседании рассматривались методы диагностики и лечения рака мочевого пузыря.
Э.А. Стаховским представлен доклад о методах деривации мочи после цистэктомии. Отмечено, что перевод в кондуит часто имеет меньше осложнений, чем в случае ортотопического мочевого пузыря.
В.А. Шахсуварян (Ереван, Армения) представил доклад, в котором сообщил об опыте применяемой после цистэктомии илеоцистопластике.
7 апреля на 4-м заседании рассматривались вопросы, посвящённые раку предстательной железы.

Проф. Лораном О.Б. был представлен фундаментальный доклад, посвящённый радикальной простатэктомии у больных с местно-распространённым РПЖ. В докладе д.м.н. Лысенко В.В была преставлена целесообразность хирургического лечения при местно-распространённом РПЖ. Оба докладчика предъявили веские аргументы за хирургическое лечение у данной категории больных. Алексеевым Б.Я. была подчёркнута актуальность тазовой лимфаденэктомии у больных РПЖ.
А.В. Говоровым (Москва) был представлен опыт проведения криоаблации простаты у больных РПЖ с Т3. Рассмотрены прогноз и возможные осложнения этого метода лечения.
Матвеевым В.Б. был представлен фундаментальный доклад о гормонотерпии при РПЖ. Было отмечено, что интермиттирующая ГТ не уступает по эффективности постоянной андрогенной блокаде. Однако отмечено, что этот вид ГТ не показан больным с метастатическим РПЖ, с высокими показателями ПСА, и временем удвоения ПСА менее 6 мес. Им было обращено внимание на относительно недавно появившиеся антагонисты релизинг-гормонов. Несомненные преимущества – нет начальной стимуляции и синдрома вспышки. Однако по уровню андрогенного подавления к 28 дню разницы с аналогами релизинг-гормонов не определяется.
Д-ром Б. Джаваном (Нью-Йорк, США), напротив, было высказано сомнение в целесообразности интермиттирующей антиадрогенной терапии и указано на необходимость контроля уровня тестостерона при оценке эффективности лечения.
В заключающем заседание докладе проф. О.Б. Карякин обратил внимание собравшихся на значительную группу больных с кастрационно-рефрактерным РПЖ. В числе прочих подходов к лечению упомянул препарат доцетаксел, применяемый у больных с костными метастазами.
Подводя итоги конференции, Э.А. Стаховский и В.Б. Матвеев поблагодарили участников конференции за активное участие и выразили надежду на дальнейшее совместное сотрудничество.
Отчет подготовила:
Аристова Т.Н., Зеленский М.М.
Читайте также:

