Ампутация ноги при меланоме
Хирургия — основной вид лечения меланомы. Большинству пациентов, после того как диагноз подтвержден при помощи биопсии, показано хирургическое лечение. Во время операции врач стремится удалить из организма пациента всю опухолевую ткань, чтобы не допустить рецидива в будущем.
Прибегают к разным видам хирургического вмешательства, в зависимости от стадии, размеров и расположения меланомы.
Какие виды операций выполняют при меланоме?
Чаще всего выполняют широкое иссечение меланомы. Хирург удаляет опухоль и некоторое количество здоровой ткани вокруг неё. Здоровая ткань вокруг опухоли называется краем резекции. После иссечения врач должен обязательно отправить то, что удалил, в лабораторию. Край резекции изучают под микроскопом на предмет наличия опухолевых клеток:
- негативный результат означает, что раковых клеток в крае резекции нет, меланома удалена полностью;
- позитивный результат говорит о том, что раковые клетки присутствуют в образце, опухоль не удалена, нужна повторная операция.
Размеры края резекции измеряются в сантиметрах и зависят от стадии меланомы:
Также ширина края резекции зависит от того, на какой части тела находится меланома. Если опухоль расположена на лице, важен косметический эффект. Врач может захватить меньше здоровой кожи, но это повышает риск рецидива. Данный вопрос нужно заранее обсудить с хирургом.

Другие виды операций, которые выполняются при меланоме:
- Биопсия сторожевого лимфоузла (сентинель-биопсия). Сторожевым называют ближайший к опухоли лимфатический узел. Он представляет собой первый рубеж, который предстоит преодолеть раковым клеткам, распространяющимся лимфогенным путем. Если опухоль проникла в него, есть вероятность, что она распространилась и в другие близлежащие лимфоузлы. Для того чтобы обнаружить сторожевой лимфатический узел, хирург вводит в ткани, окружающие меланому, специальный краситель. Лимфоузел, который первым прокрашивается, и является сторожевым. Его нужно удалить и отправить на исследование в лабораторию. Существует и более современный метод обнаружить сторожевой лимфоузел: вместо красителя в ткань вводят специальный слабый радиофармпрепарат и следят за его распространением при помощи гамма-камеры.
- Лимфодиссекция. Во время этой операции вместе с меланомой удаляют все регионарные лимфоузлы. Например, если опухоль находится на ноге, врач может удалить лимфоузлы в области паха. Лимфодиссекция может приводить к такому тяжелому осложнению как лимфедема — отек, вызванный нарушением оттока лимфы.
- Ампутация. Иногда, если опухолью поражена целая часть тела, например, палец, её приходится ампутировать.
Существует еще операция Мооса, но в настоящее время она критикуется многими врачами и применяется редко. Суть метода в том, что врач удаляет меланому тонкими слоями. Каждый слой осматривают под микроскопом. Как только раковые клетки перестают обнаруживаться, считается, что злокачественная ткань полностью удалена.
Хирургическая тактика в зависимости от стадии меланомы
Если меланома имеет толщину менее 0,75 мм, можно ограничиться широким иссечением без удаления лимфатических узлов. Такую операцию выполняют под местной анестезией.
При толщине меланомы 0,76 см и более нужно проводить сентинель-биопсию. Если раковые клетки в сторожевом лимфатическом узле не обнаружены, операцию заканчивают. Если же сторожевой лимфоузел поражен опухолевым процессом, диагностируют меланому III стадии и выполняют лимфодиссекцию. Регионарные лимфатические узлы удаляют под наркозом.
При метастатической меланоме (IV стадия) об излечении от рака речи не идет, но пациенту можно помочь. Активное паллиативное лечение помогает продлить жизнь и избавить от мучительных симптомов. Можно удалить хирургическим путем первичную опухоль, регионарные лимфатические узлы, метастазы в других органах. Однако даже если обнаружено всего 1–2 метастаза, скорее всего, есть и другие, просто они настолько малы, что пока незаметны.
Врачи Европейской клиники проводят комплексное лечение меланомы на любой стадии по современным стандартам. Помимо хирургических методов, мы используем современные химиопрепараты, таргетные препараты. На I и II стадиях от опухоли можно избавиться в 99% случаях. При некурабельной меланоме можно улучшить состояние и продлить жизнь. Для того чтобы получить наиболее эффективное и современное лечение, не обязательно ехать за границу. Звоните, мы знаем, как помочь.
Меланома – злокачественное новообразование, которое развивается вследствие повышенной продукции меланина. Это один из наиболее агрессивных видов злокачественной опухоли. Меланома на ноге может располагаться в области пальцев, стопы, голени или бёдер. Онкологи Юсуповской больницы при своевременном обращении пациентка диагностируют опухоль с помощью новейших диагностических методов.
Опасна ли меланома на ноге? Меланома занимает особое место среди злокачественных новообразований кожи, являясь социально значимой проблемой в связи с высоким уровнем летальности. Это обусловлено значительным метастатическим потенциалом опухоли и низкой эффективностью терапии поздних форм заболевания. Пятилетняя выживаемость больных меланомой на поздних стадиях не превышает 18,0%. Диагностика на ранней стадии заболевания значительно улучшает прогноз выживаемости.
Основным методом лечения меланомы является иссечение опухоли. Для лечения меланомы на ноге врачи клиники онкологии применяют современные противоопухолевые и иммуномодулирующие препараты, проводят облучение зоны локализации новообразования и путей оттока лимфы. Для спасения жизни пациента при наличии распространённой меланомы ноги иногда приходится ампутировать нижнюю конечность.
Причины развития
Меланома на ноге образуется под воздействием высокой дозы солнечной радиации. Причиной заболевания может быть мутация генов. Группу крайне высокого риска возникновения меланомы составляют лица со следующими признаками:
- Первый фототип кожи и возраст старше 45 лет;
- Второй фототип кожи и возраст старше 65 лет;
- Рыжий цвет волос;
- Меланома у ближайших родственников;
- Более десяти диспластических невусов и более ста меланоцитарных невусов;
- Перенесенный ранее рак кожи;
- Больше двадцати солнечных кератозов.
Группа высокого риска объединяет лиц, имеющих следующие признаки:
- Голубые глаза;
- Первый фототип кожи и возраст от 25 до 45 лет;
- Второй фототип кожи и возраст от 45 до 65 лет;
- Третий фототип кожи и возраст старше 65 лет;
- Рак кожи в семейном анамнезе;
- Множественные эпизоды солнечных ожогов в прошлом.
В группу умеренного риска включают лиц с I–V фототипом кожи в возрасте старше 45 лет, которые ранее перенесли много солнечных ожогов. Провоцирующим фактором развития меланомы на стопе и околоногтевом валике пальцев ног является хроническая механическая травма.
Симптомы
Часто видна меланома на ноге на фото. Опухоль представляет собой пигментные пятна, которые быстро растут, или родинку, размеры и структура которой быстро изменяется. Несомненным признаком злокачественного новообразования считается потемнение опухоли и образование в ней чёрных вкраплений. По краю пигментного пятна на ноге может появиться покраснение. Пациентов беспокоит сильный зуд. Меланома часто кровоточит. Поверхностные формы меланомы хорошо поддаются терапии.
Узловатые опухоли, слегка приподнятые над кожей ноги, протекают агрессивно. Они встречаются у 15% пациентов. Нередко встречается подногтевая меланома на пальцах стопы. Чаще она локализуется на больших пальцах ног. Для того чтобы установить точный диагноз, дерматологи определяют толщину меланомы. Этот показатель вычисляют при гистологическом исследовании взятых во время операции образцов тканей. Если показатель меньше 1мм, опухоль считается не злокачественной. При толщине меланомы больше 1мм онкологи проводят срочное иссечение пигментного пятна
Одним из методов неинвазивной диагностики меланомы кожи является дерматоскопия. В Исследование проводится с помощью современного цифрового аппарата. Метод дерматоскопии позволяет заподозрить меланому ног на ранних стадиях на основании визуализации эпидермиса, дермоэпидермального соединения и сосочкового слоя дермы при увеличении в 10 раз. Одним из простых и доступных алгоритмов при дерматоскопическом исследовании является трёхбалльная система оценки. Согласно данному алгоритму оценивают асимметрию новообразования, наличие бело-голубой вуали и атипичной пигментной сети.
К обязательным методам обследования пациентов, у которых подозревают наличие меланомы ног, относят физикальный осмотр, тщательное исследование кожных покровов, видимых слизистых и периферических лимфатических узлов. Обязательно выполняют рентгенографию органов грудной клетки в прямой и боковой проекции, ультразвуковое исследование периферических лимфатических узлов, органов брюшной полости, малого таза и забрюшинного пространства. При наличии показаний выполняют компьютерную томографию органов брюшной полости, компьютерную или магнитно-резонансную томографию органов брюшной полости, головного мозга с внутривенным контрастированием, радиоизотопное исследование (сцинтиграфию) костей скелета. Начиная с тетей стадии опухолевого процесса с целью выявления отдалённых метастазов выполняют ПЭТ (позитронно-эмиссионную томографию) или ПЭТ-КТ.
Лечение
Хирургическое лечение первичной меланомы кожи ноги выполняют, соблюдая следующие принципы:
После иссечения первичной меланомы кожи ноги широко используют свободную кожную пластику. В настоящее время при местнораспространенных первичных меланомах ног применяют изолированную регионарную перфузионную терапию мелфаланом и фактором некроза опухоли. Как и другие локальные методы, она не влияет на частоту появления отдалённых метастазов, но предотвращает возникновение местных рецидивов меланомы кожи, увеличивает длительность ремиссии, помогает сохранить конечность более чем у 80 % пациентов. Данный метод имеет положительные стороны. Он позволяет применять цитотоксические дозы химиопрепаратов и цитокинов, воздействовать на зону регионарного метастазирования, позволяет регионарно воздействовать на ногу цитостатическими агентами и гипертермией. Этот метод имеет следующие недостатки:
- Необходимость расширенного хирургического вмешательства;
- Неполная изоляция региона, подверженного перфузии, что обусловливает системную токсичность;
- Повреждающее действие цитостатических препаратов на здоровые ткани.
Онкологи Юсуповской больницы индивидуально подходят к операции иссечения регионарных лимфатических узлов. Проведение превентивной лимфаденэктомии в сроки до четырёх недель после иссечения первичной меланомы кожи ноги не оказывает статистически значимого влияния на показатели пятилетней общей и безрецидивной выживаемости по сравнению с пациентами, которым проводилось широкое иссечение злокачественного новообразования. Подобная операция, выполненная в сроки более четырёх недель после иссечения первичной опухоли, достоверно увеличивает пятилетнюю общую выживаемость.
Фотодинамическую терапию комбинируют с последующей лазериндуцированной гипертермией. При адъювантной терапии, при меланоме кожи ноги, используют как биологически активные вещества, которые обладают иммуногенными свойствами (интерфероны, левамизол, БЦЖ), так и химиотерапевтические средства (производные нитрозомочевины, имидазол-карбоксамида, платины).
Специфической профилактики меланомы ног не существует. Пациентам, которые входят в группы риска, рекомендуют значительно ограничить пребывание на солнце, а при работе в солнечные дни на открытых участках использовать светлую одежду из натуральных тканей. Следует носить удобную обувь, избегать постоянных повреждений кожи стоп и околоногтевого валика. Необходимо регулярно осматривать поверхность ног. При выявлении изменений родинок и пигментных пятен немедленно звоните в контакт центр Юсуповской больницы и записывайтесь на приём к онкологу.
Рассказ о применении перфузии конечности при меланоме кожи.
Итак , наша история. Моя мама (1954 г.р.) больна меланомой. В октябре 2014 года при осмотре у онколога был поставлен диагноз Меланома правой голени и дано направление в местный онкодиспансер на удаление родинки методом широкого иссечения. В ноябре 2014 года была проведена операция по удалению родинки и сразу во время нее БСЛУ. В лимфоузлах все чисто.
По гистологическим исследованиям уровень инвазии составил 3 мм. После выписки из стационара обратились за консультацией к химиотерапевту. Химиотерапия, как и любое другое лечение, назначены не были, врачи сказали, что в этом нет необходимости, требуются только контрольные осмотры, УЗИ, рентген и кровь на окномаркер меланомы S 100 каждый три месяца.
В июле 2015 года при контрольном УЗИ был обнаружен мтс в паховые лимфоузлы. Проведена операция по удалению паховых лимфоузлов. Далее, после выписки из хирургического отделения мама сразу была переведена в отделение химиотерапии, где прошла курс высоких доз интерферонов препаратом Лайфферон 18 млн.ед., и далее был назначен этот препарат в течении года в дозе 3млн.ед. (5 дней /2 дня).
Переносился он тяжело, с высокой температурой, ознобом, тахикардией. Как только маме стало не много легче, в ноябре повезла ее в Казань на ПЭТ (сами мы из Ижевска), в результате обследования были выявлены множественные мтс (8 шт) в толще правой конечности (6 в голени и 2 в бедре). Визуально их видно не было, так как на конечности появился умеренный лимфостаз.
В декабре 2015 с результатами ПЭТ обратились в РОНЦ им.Блохина на консультацию по поводу дальнейшего лечения. Терапия интерферонами была признана бесполезной и отменена, рекомендована операция химиоперфузия с гипертермией локально на ногу, т.к. мтс только в конечности, B-Raf мутация отсутствует. Мы согласились на операцию, т.к. нам объяснили, что для нее есть все показания.
28.01.2016 по квоте была проведена химиоперфузия. На момент проведения операции появились видимые метастазы на лобке, но доктора не предложили отказаться от перфузии, не смотря на то, что эта сложнейшая и тяжелая операция по факту уже была не актуальна, т.к. зона воздействия была меньше чем зона поражения. Операцию маме все же провели, обработав ногу до середины бедра мелфаланом и гипертермией до 42 градусов, а все мтс, которые были выше зоны воздействия были просто удалены хирургически. На операцию мы получили квоту от Минздрава РФ, но тем не менее доктора РОНЦ ******** (тут были имена , фамилии и еще кой чего нехорошее, но это я печатать не буду. прим Дядя Вадик). Они могли нас предупредить, что эффекта от нее не будет и порекомендовать другое лечение, направить к другим специалистам, но не сделали этого.
Во-вторых, опять (регулярно) возникает вопрос: стоит ли рассказывать пациенту о препаратах/методах лечения, которых в данный момент нет в нашей стране?
На самой операции хочу остановится еще более подробно.
Операция сложнейшая, когда конечность подключают на аппарат искусственного кровообращения и через сосуды ноги пропускаю химию, превышающую в 20 раз смертельную дозу для человека, потом отмывают физраствором и сосуды подшивают обратно в общий кровоток. Дополняет это все локальная гипертермия. При презентации этого лечения нам рассказали только одну сторону медали, то что это локальное воздействие на очаг поражения, что нет нагрузки на весь организм, что дозы высоки, поэтому опухоли сгорают без следа и можно надеяться на полное излечение. Но не сказали о возможных последствиях, таких как увеличение лимфостаза (сосуды то практически все сожгли), токсическая нейропатия (обострение чувствительности кожи и мышц ноги) и банальные ожоги.
В результате воздействия высоких доз малфалана и гипертермиии наступил ожег мягких тканей ноги, на третий день после операции нога покраснела, через неделю почернела, появились ожеговые пузыри в диаметре до 5 см, что мама пережила за этот послеоперационный месяц одному Богу известно. Мама не могла встать с постели 2 недели. Пузыри вскрывали, бесконечно перевязывали, обрабатывали регенерирующими мазями, но боли не уменьшались. Кожа со стопы и голени от ожегов сходила толстыми пластами. В выписке указали, что операция осложнилась 3 степенью токсичности. По чей это вине произошло? Это организм так отреагировал или это ошибка врачей — мы до сих пор не знаем.
В результате на данной конечности возникла токсическая нейропатия (нарушение чувствительности конечности). Через месяц после операции маму выписали домой. Дополнительное лечение никакое назначено не было, мотивируя тем, что введенный в таких больших дозах мелфолан будет действовать еще 2-3 месяца. Нас пригласили на повторную консультацию в РОНЦ в мае 2016. Восстановительный период после операции продолжался три месяца. Нейропатия не прошла до сих пор. Когда мы приехали на повторную консультацию, то по результатам диагностики было выявлено прогрессирование заболевания. Мтс появились на лобке, в паху, на ноге выше зоны обработки и в подвздошных лимфоузлах. Мтс в толще ноги тоже никуда не пропали. При этом лимфостаз усилился и практически не поддавался лечению.
Мама начала ходить с затруднениями. Хирурги, видя несостоятельность своего лечения быстро перенаправили нас на 18 этаж к химиотерапевту ******., который назначил маме два курса химии. На тот момент я уже самостоятельно узнала о возможности участвовать в КИ (об этом вообще ни кто не рассказывает), мы начали задавать эти вопросы и *******, и ******, и онкологу на приеме в поликлинике ******. Но как оказалось они ничего не знают ни о сроках, ни о наборах, ни об ответственных за набор докторах (взаимодействия между этажами и сотрудниками РОНЦ нет никакого, как будто это разные государства).
Начали самостоятельно разыскивать по РОНЦ ответственных за КИ, вышли на 21 этаж, зав.Демидов Л.В., нашли сотрудников отделения, кто занимается набором в КИ, и на нашу привеликую радость узнали о предстоящем наборе на КИ Пембролизумаб+эпакадостат, планируемое на июль 2016.
Два месяца провели в ожидании, обследовании, сборе анализов и пр. Конечно же ни о какой химии речи быть не могло, т.к. это является исключением для отбора на КИ. Были пройдены все необходимые обследования, подписаны все документы, выдан на руки договор, страховой полис…и в последний момент от спонсоров из Америки (компания Мерк) при последнем согласовании кандидатов пришел отказ. Доктор *****. прокомментировала его следующим образом, что маму исключили из КИ т.к. ранее присутствовало иммунологическое лечение и оно не дало результатов. Поэтому смысла брать ее в КИ спонсор не видит.
Возможности поехать заграницу на лечение у нас нет, да и мама отказывалась и не рассматривала зарубежные поездки. Денег на полный курс Пембролизумаба (2 года) у нас тоже нет, меньше года доктора сказали ставить его бесполезно, да и покупать его в России пока нет возможности, т.к. препарат не зарегистрирован (сейчас уже зарегистрирован, но толку пока что нет прим. Дядя Вадик). И лечить этим препаратом (контролировать ход лечения в России) мало кто берется.
Итог нашей истории очень грустный. Мама в плохом состоянии, на симптоматическом лечении дома. Виню себя, что повезла маму на химиоперфузию и принесла ей много страданий, а не искала медикаментозные пути лечения болезни (мутации не было и таргетная терапия была не актуальной, про пембролизумаб узнала позже). А потом, когда получили отказ в КИ не попыталась любыми путями купить Пембролизумаб и проставить хотя бы столько, сколько бы мы смогли себе позволить по деньгам. Не повторяйте наших ошибок.
P.S. общаемся с двумя коллегами по несчастью, с которыми познакомились в РОНЦ Блохина когда делали химиоперфузию. Они перенесли тоже эту операцию. Положительного эффекта нет ни у одного пациента, а вот последствия в виде нарушения чувствительности ноги и увеличении лимфостаза есть у всех. Считаю данный вид лечения очень слабо эффективным и небезопасным. Жаль, что нельзя повернуть время назад…
Ну вот, собственно, что тут комментировать? 🙁 Могу только выразить огромную благодарность автору за такой подробный рассказ.
Можно с высокой долей вероятности, а посмотрев нижеприсобаченное видео вы со мной согласитесь, скорее всего, что процедура была назначена не с целью лечения, а с целью проведения самой процедуры, ибо пациентов таких мало (цитата из киношки) и врачи цепляются за любую возможность поэкспериметировать, ведь действительно, какой смысл все это проводить, если уже есть отдаленные метастазы
У меня есть фото результатов проведенного лечения (вам я его не покажу). Никаких положительных результатов я не увидел и вообще, как неспециалисту, мне сложно понять смысл таких жутких манипуляций.
НО
В первом видео вы увидите такую карту:
т.е. данный метод достаточно широко представлен в мире (по крайней мере был представлен до появления последних препаратов), только вот в Штатах видимо нет. И Израиль, кстати, имеется, хотя я вот даже не слышал про такие манипуляции в этой стране.
А теперь обратимся к комментариям специалистов. Первое видео очень познавательное и в т.ч. интересна концовка с 12.45 , когда был задан вопрос (звук громче делайте, т.к. без микрофона вопрошающий глаголит).
Основной метод лечения меланомы на 0, I и II стадиях — хирургический. Прибегают к широкому иссечению — опухоль удаляют, захватывая здоровые ткани вокруг нее и под ней. Количество здоровых тканей, которые следует удалить, определяется размерами новообразования и его локализацией. Например, если меланома находится на лице, важен косметический эффект, поэтому здесь обычно удаляют меньше тканей.

На стадии 0 и IA (если опухоль прорастает в кожу менее чем на 0,8 мм и на ней нет изъязвления) широкое иссечение — единственный метод лечения, в дальнейшем пациент должен находиться под наблюдением.

На стадиях IB и II во время операции проводят сентинель-биопсию. В опухоль вводят радиофармпрепарат или флуоресцентный краситель. Он проникает в лимфатические сосуды и распространяется по ним в лимфатические узлы. Смотрят, в какие узлы препарат попал в первую очередь. Это — дозорные, или сигнальные лимфоузлы. Их удаляют и проводят биопсию. Если в них найдены опухолевые клетки, необходимо удаление регионарных лимфатических узлов. Врач может назначить адъювантную терапию в высоких дозах в течение года.
При III стадии удаляют первичную опухоль и лимфатические узлы. После операции назначают разные варианты адъювантной терапии:
- Иммунопрепараты
- Таргетные препараты
- Лучевая терапия бассейна пораженных лимфатических узлов — для пациентов из группы повышенного риска.
- Биохимиотерапия: сочетание иммунопрепаратов с химиопрепаратами.
Иногда вторичные опухоли находятся рядом с основной, и/или раковые клетки обнаруживаются в лимфатических сосудах, но не в лимфатических узлах. В таких случаях лечебная тактика может быть разной. Если опухоль нерезектабельна (не может быть полностью удалена хирургически), назначают терапию, как при меланоме 4 стадии с метастазами. В других случаях удается полностью удалить опухолевую ткань и добиться негативного края резекции. Есть и другие варианты лечения:
- Лучевая терапия.
- Изолированная гипертермическая перфузия (LIMB) — процедура, во время которой подогретый химиопрепарат вводят в артерию руки или ноги. Лекарство попадает только в определенную часть тела и не проникает в общий кровоток, а за счет более высокой температуры оно эффективнее уничтожает раковые клетки. Иногда такая процедура помогает избежать ампутации конечности.
При меланоме IV стадии проводят паллиативные хирургические вмешательства. Они не избавляют от меланомы, но помогают уменьшить размеры опухоли, справиться с болью и другими симптомами, продлить жизнь пациента.
В паллиативных целях назначают иммунопрепараты, таргетные препараты, химиопрепараты.
Отзывы наших пациентов
8 ноября 2019 г.
Иммунотерапия при меланоме
В норме иммунная система использует некоторые молекулярные механизмы, чтобы удержать себя от атаки на здоровые ткани, это помогает предотвратить тяжелые аутоиммунные заболевания. Те же молекулярные механизмы могут использовать злокачественные опухоли. Особые молекулы — контрольные точки — подавляют активность иммунных клеток. Снова активировать иммунитет и заставить его атаковать клетки меланомы помогают специальные препараты — ингибиторы контрольных точек. Они были разработаны относительно недавно. Для борьбы с меланомой используют три ингибитора контрольных точек:
- Блокаторы PD-1 — белка, который находится на поверхности T-клеток и подавляет их способность атаковать опухоль.
- Блокатор CTLA-4. CTLA-4 — это еще один белок на поверхности T-клеток, который подавляет их активность.
Доказано, что ингибиторы контрольных точек помогают продлить жизнь пациентов, страдающих меланомой, но нет доказательств того, что лечение ими способно привести к ремиссии.
Другие препараты для иммунотерапии меланомы:
- Цитокины — вещества, которые стимулируют иммунную систему. Они помогают уменьшить размеры меланомы у 10–20% пациентов. Иногда эти препараты назначают в сочетании с химиопрепаратами. Для того чтобы препарат эффективно работал, его нужно вводить в больших дозах. Не все пациенты могут получать такое лечение из-за серьезных побочных эффектов.
- Онколитические вирусы заражают и уничтожают злокачественные клетки, а также помогают усилить противоопухолевые иммунные реакции.
- Вакцина БЦЖ стимулирует противоопухолевый иммунитет. Ее, как и онколитический вирус, нужно вводить непосредственно в опухоль. Вакцину БЦЖ обычно применяют при III стадии меланомы.
- Иммуномодулирующее средство — Применяется в форме крема. Его наносят на пораженный опухолью участок кожи 2–5 раз в неделю в течение трех месяцев. Иногда применяют при меланоме III стадии, но не все врачи и исследователи считают, что стоит практиковать такой метод лечения.
Оставьте свой номер телефона
Таргетная терапия меланомы

Мутация гена BRAF имеется примерно в половине меланом. При этом образуется одноименный неправильный белок, который активирует размножение опухолевых клеток. У таких пациентов применяют две группы таргетных препаратов:
- Ингибиторы BRAF: Эти препараты применяют при IV стадии меланомы с метастазами, они помогают продлить жизнь больного. Таргетные препараты могут быть назначены в качестве адъювантной терапии после операции при III стадии меланомы. Ингибиторы BRAF принимают в виде таблеток или капсул 1–2 раза в день.
- Ингибиторы MEK — белка, который работает вместе с белком BRAF. Вместе с ингибиторами BRAF они обеспечивают более выраженный эффект, и есть данные о том, что комбинированная терапия несет меньший риск серьезных побочных эффектов. Ингибиторы MEK принимают в таблетках 1–2 раза в день.
В небольшом количестве меланом выявляется мутация в гене C-KIT. Обычно это меланомы, расположенные на ладонях и подошвах, слизистых оболочках, на областях тела, которые хронически подвергаются воздействию солнечных лучей (шея, лицо). Пациентам с такими опухолями назначают ингибиторы C-KIT.
Химиотерапия меланомы
Химиопрепараты при меланоме применяют нечасто, так как они зачастую оказываются не очень эффективны, опухоль быстро вырабатывает к ним резистентность и начинает снова прогрессировать на фоне лечения.
Насколько эффективно лечение против меланомы? Каков прогноз выживаемости?
В настоящее время удалось добиться следующих показателей пятилетней выживаемости при меланоме:
- I стадия: 92–97%.
- II стадия: 53–81%.
- III стадия: 40–78%.
- IV стадия: 15–20%.
В настоящее время проводятся клинические исследования, ученые ищут новые эффективные методы борьбы с меланомой.
Удаление опухоли кожи. Для локализованных меланом, ограниченных первичным очагом (стадия I), основным методом лечения остается хирургическое вмешательство. Из-за большой вероятности поражения локальных лимфатических узлов большинство хирургов предпочитают выполнять широкое иссечение первичной опухоли, хотя в последнее время проводят более консервативные операции.
В одной из последних публикаций показано, что если граница иссечения отстоит от края первичной опухоли на расстоянии в 1 см, то риск возникновения местного рецидива оказывается выше, чем в случаях, когда это расстояние составляет 3 см. Однако через три года после проведения операции общая выживаемость больных в двух группах была одинаковой. При широком иссечении опухоли нередко необходимо проводить пересадку кожного лоскута, и прогноз операции обычно оказывается благоприятным (уровень 1 или 2 по Кларку и lentigo maligna).
Иногда бывает достаточно провести менее радикальную резекцию и избежать последующей пластической операции. Исследования, проведенные в рамках ВОЗ Группой по изучению меланомы, показали, что в случае опухолей, инвазирующих кожу в глубину до 1 мм, консервативная операция оказывается более безопасной. В настоящее время распространена точка зрения, согласно которой на каждый мм глубины инвазии опухоли достаточно операционного поля в 1 см.
При этом отпадает необходимость в пересадке кожи. Узелковые опухоли инвазируют глубже, обычно до границы между сосочковым слоем и ретикулярными клетками (уровень 3 по Кларку), и в этом случае выполняют более широкое иссечение, чем при первичной меланоме lentigo maligna. В случаях меланом, развившихся на некоторых участках верхних и нижних конечностей (например, под ногтями), лучше проводить частичную ампутацию пальцев.
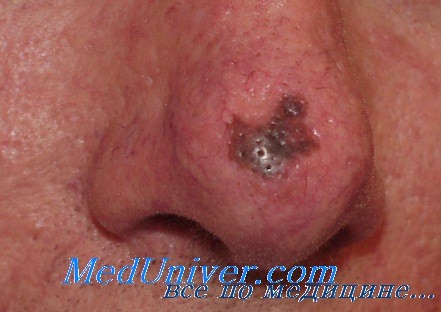
Злокачественная меланома - внешний вид
Необходима ли регионарная лимфаденэктомия во всех случаях злокачественной меланомы? Несомненно, она дает ценную прогностическую информацию для больных с I стадией развития опухоли. При наличии микроскопических признаков заболевания 5-летняя выживаемость снижается с 70% (стадия I, без поражения лимфатических узлов) до 50%, при скрытых поражениях лимфатических узлов, которые обнаруживаются на операции.
Широко обсуждается вопрос о возможном терапевтическом эффекте регионарной лимфаденэктомии и ее роли в улучшении прогноза заболевания. В общем, больные с неплохим прогнозом (небольшие, не носящие узелкового характера опухоли на конечностях, уровень 1 по Кларку) не получают дополнительного лечебного эффекта от проведения лимфаденэктомии. Эта операция обычно показана больным с более глубокими поражениями кожных покровов, например при распространенных узелковых меланомах, уровень 3, 4 или 5 по Кларку.
Лимфаденэктомию обычно проводят в случаях клинического проявления поражения ближайших к опухоли лимфатических узлов. Впрочем, сомнительно, что эта операция увеличивает выживаемость больных. Лишь 10% больных с диагнозом метастатической лимфоаденопатии, подтвержденным при операции, живут не менее 5 лет. Столь печальное положение дел напоминает ситуацию при заболевании раком молочной железы: поражение регионарных лимфатических узлов обычно является следствием скрытого диссеминированного опухолевого процесса.

В обоих случаях прогностически ценная информация получается за счет процедуры, которая сама по себе обладает сомнительной пользой. Однако, несмотря на столь пессимистичный взгляд, единственным средством лечения больных с меланомой в стадии II или III, которое обладает серьезным шансом на успех, является радикальное удаление лимфатических узлов. Для особых групп больных с опухолями на конечностях в клинической стадии II, с крайне неблагоприятным прогнозом, максимальную надежду на излечение дает ампутация.
Некоторые хирурги в Великобритании положительно относятся к профилактическому удалению лимфатических узлов, даже у больных с неблагоприятным прогнозом, хотя бы потому, что при этом получают дополнительную полезную прогностическую информацию. Такая точка зрения сформировалась в результате анализа результатов, полученных на большом контингенте больных в Австралии. Крупные австралийские клиники обладают большим опытом лечения меланомы, которая широко распространена в Австралии и Новой Зеландии.
Так, 5-летняя выживаемость среди больных меланомой в Квинсленде превышает выживаемость больных с этой опухолью в остальных странах мира (Квинсленд 81%, Великобритания 61%, США 37%). Утверждается также, что у большинства австралийцев первичное меланомоподобное повреждение кожи ограничивается эпидермисом и характеризуется сравнительно благоприятным прогнозом. Однако этот вопрос нуждается в тщательной проверке. На основании полученных результатов высказывается предположение о том, что профилактическое удаление лимфатических узлов в случаях неглубоко инвазирующих меланом оказывает благоприятное действие, хотя у большинства больных отмечаются побочные эффекты без видимых улучшений состояния.
Впрочем, в одном из недавних исследований, проведенных с участием нескольких клинических центров, не удалось продемонстрировать положительный эффект профилактического удаления регионарных лимфатических узлов, по крайней мере по показателю выживаемости больных. В этих исследованиях наблюдались больные, у которых инвазивность меланом составляла 1-4 мм. Вызывает удивление, что 5-летняя выживаемость больных с пораженными, но не непальпируемыми лимфатическими узлами была лишь на 20% выше, чем больных с клиническими признаками их поражения (50% и 28% соответственно). Таким образом, вероятно, существует некий предел возможностей хирургического метода.
Читайте также:





