Аллогенная трансплантация при миелофиброзе
Хронический идиопатический миелофиброз (ХИМФ, миелофиброз с миелоидной метаплазией) является клональным заболеванием. Его основу составляет первичное поражение гемопоэтических стволовых клеток с наличием мегакариоцитов и моноцитов, секретирующих PDGF (platelet-derived growth factor) и различные цитокины, что приводит к неклональной пролиферации фибробластов в костном мозге с продукцией белков экстрацеллюлярного матрикса. Заболевание характеризуется развитием фиброза костного мозга, экстрамедуллярным кроветворением, спленомегалий, повышенным содержанием гемопоэтических стволовых клеток в крови.
Назначение химиотерапии для редукции злокачественного клона клеток вызывает обратное развитие этих изменений.
В связи с этим ауто-трансплантации гемопоэтических стволовых клеток и особенно алло-трансплантации гемопоэтических стволовых клеток, по всей вероятности, являются единственными методами терапии, позволяющими рассчитывать на излечение больных с хроническим идиопатическим миелофиброзом (ХИМФ). До настоящего времени трансплантация гемопоэтических стволовых клеток не получила широкого распространения при ХИМФ ввиду ряда причин: возраст больных (большинство старше 40 лет), сложность получения аутологичных ГСК, большая вероятность длительного периода восстановления кроветворения после трансплантации гемопоэтических стволовых клеток из-за наличия выраженных фиброзных изменений костного мозга, спленомегалий и развития тяжелых осложнений. В настоящее время рассматривается возможность лечения больных ХИМФ с помощью ингибитора тирозинкиназы (гливек).
В последние годы получены данные об успешном выполнении ауто-трансплантации периферических стволовых клеток крови (ауто-ТПСКК) и алло-трансплантации гемопоэтических стволовых клеток у больных хроническим идиопатическим миелофиброзом (ХИМФ). Следует отметить, что скорость приживления ГСК после трансплантации гемопоэтических стволовых клеток у части больных хроническим идиопатическим миелофиброзом (ХИМФ) не отличается от восстановления гемопоэза при других вариантах гемобластозов.
Риск развития тяжелых осложнений после алло-трансплантации гемопоэтических стволовых клеток затрудняет принятие решения о выполнении алло-трансплантации гемопоэтических стволовых клеток больным старше 40 лет, а у лиц молодого возраста (до 40 лет) в связи с вероятностью доброкачественного течения хронического идиопатического миелофиброза (ХИМФ) в течение нескольких лет (медиана выживаемости 128 мес). Таким образом, при определении показаний к алло-ТГСК необходимо комплексно оценивать клиническое течение хронического идиопатического миелофиброза (ХИМФ) у конкретного больного по степени фиброзных изменении костного мозга, индексу Dupriez, уровню тромбоцитов и бластов в крови, цитогенетическим изменениям.
Критериями для оценки неблагоприятного прогноза при ХИМФ, по В. Dupriez, являются содержание гемоглобина менее 100 г/л и количество лейкоцитов менее 4*10 9 /л и более 30*10 9 /л.
После ауто-трансплантации периферических стволовых клеток крови (ауто-ТПСКК) 2-летняя общая выживаемость у больных хроническим идиопатическим миелофиброзом (ХИМФ) составила 61 %. При выполнении алло-трансплантации гемопоэтических стволовых клеток 4—5-летняя общая и безрецидивная выживаемость были 47—71 и 59 % соответственно. Эффективность алло-трансплантации гемопоэтических стволовых клеток при хроническом идиопатическом миелофиброзе (ХИМФ) зависит от риска течения заболевания, степени выраженности фиброзных изменений в костном мозге, уровня гемоглобина (благоприятно более 100 г/л), количества гемотрансфузий до алло-трансплантации гемопоэтических стволовых клеток, а также источника гемопоэтических стволовых клеток (родственный, неродственный донор). Наличие в костном мозге фиброзных изменений III степени вызывает необходимость снижения доз в режимах кондиционирования при хроническом идиопатическом миелофиброзе (ХИМФ).
Одним из вариантов может быть назначение режима кондиционирования: бусульфана 10 мг/кг 4- флюдарабина 180 мг/м2 + АТГ 60—90 мг/кг. В других случаях возможно применение стандартных режимов кондиционирования. При сравнении влияния спленэктомии на отдаленные результаты после алло-ТГСК у больных ХИМФ рядом авторов существенного различия не установлено: 4-летняя безрецидивная выживаемость составила 73 % после спленэктомии и 64 % без нее. Следует отметить, что большинство исследователей указывают на отрицательное влияние этого фактора.
Для снижения токсичности и риска развития летальных осложнений у больных хроническим идиопатическим миелофиброзом (ХИМФ) возможно применение алло-трансплантации гемопоэтических стволовых клеток с режимом кондиционирования с уменьшенной интенсивностью дозы. Единичные данные позволяют рассматривать этот метод как наиболее перспективный в будущем.
- Почему не каждый получает пересадку?
- Посттрансплантационный прогноз
- Кто не имеет права?
- Что если вы не имеете права?
- Будущее трансплантатов как лечение
ТРАНСПЛАНТАЦИЯ КОСТНОГО МОЗГА | КЕМЕРОВО | VLOG (Июль 2020).
Выбор оптимального лечения первичного миелофиброза может быть сложной задачей. Часто не существует однозначного выбора. Существует несколько способов лечения первичного миелофиброза, но только трансплантация гемопоэтических стволовых клеток (также называемая трансплантация костного мозга) излечивает.
Почему не каждый получает пересадку?
Лекарство звучит замечательно, поэтому вы можете удивиться, почему каждый человек с первичным миелофиброзом не получает трансплантат. Это все о балансе риска и выгоды.
Лечение первичного миелофиброза определяется категорией риска, основанной на признаках и симптомах, которые вы испытываете. Если у вас нет симптомов или симптомы болезни низкого риска, средняя выживаемость после постановки диагноза составляет 15,4 года. В этом случае потенциальные осложнения (острая или хроническая реакция "трансплантат против хозяина" и смерть), связанные с трансплантацией, перевешивают пользу от излечения. Исследования показали, что пятилетняя выживаемость у людей с низким или средним уровнем риска была ниже, если они перенесли трансплантацию гемопоэтических стволовых клеток. Тем не менее, при промежуточном заболевании и заболевании высокого риска пятилетняя выживаемость была улучшена у людей, которые получили трансплантат, по сравнению с теми, кто этого не сделал.
Посттрансплантационный прогноз
В настоящее время от 40 до 60 процентов людей с первичным миелофиброзом, перенесших трансплантацию, живут не менее трех-четырех лет. Есть некоторые свидетельства того, что проведение спленэктомии (хирургическое удаление селезенки) до трансплантации связано с улучшением показателей выживаемости, особенно у мужчин, но причина этого до конца не выяснена. Кроме того, люди, у которых развивается миелофиброз после полицитемии вера или эссенциальной тромбоцитемии, имеют лучшую выживаемость после трансплантации, чем люди с первичным миелофиброзом.
Кто не имеет права?
Некоторые люди с высоким риском заболевания не являются кандидатами на HSCT. Это в первую очередь определяется вероятностью выживания после ТГСК.
Такие вещи, как чрезмерная большая селезенка (более восьми дюймов ниже грудной клетки) и более 20 переливаний крови до трансплантации (особенно если у вас обоих) были связаны с более низкой пятилетней выживаемостью после трансплантации.
Что если вы не имеете права?
Так что рекомендуется, если у вас первичный миелофиброз высокого риска, но вы не имеете права на HSCT или у вас нет донора? Если у вас есть такие симптомы, как болезненное увеличение селезенки, утомляемость, боль в костях, ночные поты и т. Д., Руксолитиниб может быть разумной терапией.
Руксолитиниб, как было показано, уменьшает симптомы, уменьшает размер селезенки и улучшает анемию у людей с первичным миелофиброзом. Другой альтернативой HSCT может быть участие в клинических испытаниях. Это даст вам доступ к лекарствам, которые изучаются в качестве потенциальной терапии для первичного миелофибоза на ранней стадии.
Нелегко узнать, что вы не подходите для лечения, но не забудьте изучить все ваши варианты.
Будущее трансплантатов как лечение
С улучшением методов лечения вокруг трансплантации, таких как режим, используемый для подготовки костного мозга до трансплантации, и лекарственные средства, используемые для предотвращения трансплантата по сравнению с болезнью хозяина, больше трансплантаций проводится людям старше 60 лет и с альтернативными донорами (родственники не идеально подобранные или подобранные неродственные доноры). Некоторые центры будут пересаживать людей с миелофиброзом до 75 лет.
Надеемся, что с дальнейшими улучшениями HSCT будет доступен большему количеству людей с миелофиброзом. Поскольку первичный миелофиброз является редким заболеванием, потребуются годы, прежде чем мы сможем четко понять роль альтернативных доноров в ТГСК для этого заболевания.
Слабость, недомогание, бессоница
Увеличение в размерах живота, снижение масса тела, ночная потливость
Кожный зуд, лихорадка
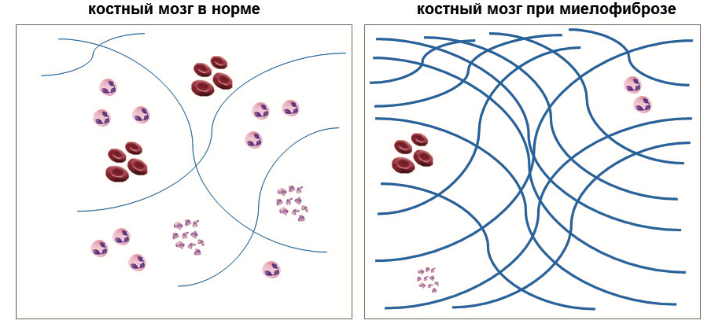
Фиброз вытесняет очаги образования клеток крови в костном мозге
Миелофиброз (ГФФ, в международной литературе – HPP) , – опухолевое заболевание, в результате которого происходит поражение главного элемента кроветворной системы — стволовой клетки. Происходит это потому, что в стволовой клетке нарушается программа, согласно которой клетка осуществляет свои функции. Программа хранится внутри каждой клетки и записана в хромосомах, которые состоят из генов. Известно, что поломки (мутации) внутри хромосом и генов, являются причиной развития многих форм опухолей, в том числе и миелофиброза. При этом измененные клетки крови значительно отличаются по форме и свойствам от нормы. Их количество увеличивается, они способствуют развитию фиброза в костном мозге.
Избыток клеток перемещается в печень и селезенку, в связи с чем эти органы увеличиваются в размерах. Кроме того, опухолевые клетки выделяют большое количество биологически активных веществ. Они способствуют появлению слабости, быстрой утомляемости, кожного зуда, потливости, повышению температуры и многих других симптомов.
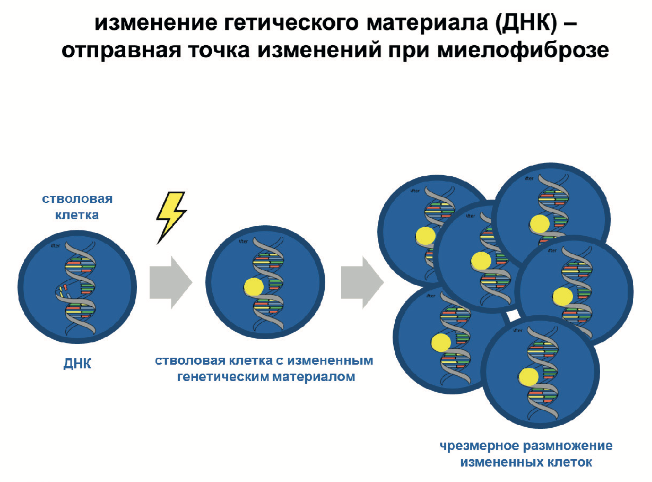
Мутации в генах являются причиной развития миелофиброза. Исследование крови или костного мозга на наличие этих мутаций проводится при первом обращении больного и подтверждает диагноз миелофиброза. Какие факторы приводят к этим поломкам, например, курение, употребление алкоголя, наследственные факторы или может быть облучение, остается не известным. В 7-8% могут наблюдаться семейные случаи миелопролиферативных заболеваний (2 более случая в семье). В некоторых случаях может наблюдаться генетическая предрасположенность к миелопролиферативным заболеваниям.
У многих пациентов незначительные симптомы заболевания наблюдаются задолго до установления диагноза. Вначале пациентов беспокоят симптомы общего характера, такие как слабость, быстрая утомляемость. По мере прогрессирования заболевания состояние больного может существенно ухудшаться; поэтому в любом случае необходимо обратиться к врачу.
Общие симптомы заболевания — слабость, быстрая утомляемость, кожный зуд, повышение температуры, потливость, похудание.
Увеличение селезенки (Спленомегалия) и печени (гепатомегалия) — может проявляться болью, дискомфортом в левом и правом подреберье, может быть причиной чувства быстрого насыщения съеденной пищей. Селезенка – это один из органов иммунной системы. Когда в костном мозге развивается фиброз и формируется “рубец”, опухолевые клетки крови начинают вырабатываться в селезенке и печени, из-за чего они увеличиваются в размерах.
Тромбоцитопения — состояние, при котором наблюдается снижение уровня тромбоцитов в крови. Больные, страдающие тромбоцитопенией, обладают повышенной склонностью к образованию синяков и кровотечениям, возникающим даже при незначительных ударах или царапинах, нередко появляются носовые кровотечения и кровоточивость десен.
Лейкопения — низкое количество лейкоцитов в крови снижает сопротивляемость организма к бактериальной инфекции, поэтому больные с нейтропенией часто болеют инфекциями дыхательных путей (кашель, затруднение дыхания, боль в горле, насморк, повышение температуры тела), мочевыводящих путей (болезненное, учащенное мочеиспускание), у них нередко возникают кожные инфекции.
Тромбоцитоз — увеличение количества тромбоцитов выше нормы. У пациентов с миелофиброзом может наблюдаться как снижение уровня тромбоцитов, так и увеличение. Это может быть одной из причин увеличения вязкости крови и приводить к развитию тромбозов. При повреждении кровеносного сосуда клетки крови (тромбоциты, лейкоциты) формируют сгусток и препятствуют кровотечению. Так происходит в норме. Но при миелофиброзе из-за нарушения свойств клеток крови может происходить спонтанное образование сгустков в сосудах без нарушения их целостности.
Советы пациентам с миелофиброзом
Миелофиброз — это не приговор, течение этого заболевания может быть многолетним. Врач оценивает каждый случай и рекомендует наилучшее лечение, но при этом существенная роль при принятии решения о выборе лечения принадлежит Вам. В зависимости от стадии и формы заболевания врач может назначить Вам наблюдение, наилучшую лекарственную терапию или трансплантацию костного мозга. Трансплантация костного мозга от совместимого донора – единственный метод полного излечения от миелофиброза. Если Ваш возраст меньше 65 лет и у Вас нет тяжелых сопутствующих заболеваний, обсудите с врачом вопрос о возможности пересадки костного мозга. Попросите направить Вас или Ваших братьев или сестер на HLA (тканевое) типирование.
Этот анализ (кровь из вены ) позволит определить, подходит ли Вам в качестве донора костного мозга член Вашей семьи. Совместимый донор может быть найден не только среди родственников, но и в Международном регистре доноров костного мозга. В случае, если Вам не подходит этот метод лечения, то врач назначит наилучшую доступную терапию. Это позволит улучшить качество жизни и контролировать заболевание.
Клинические формы заболевания и факторы риска
Первичный миелофиброз возникает без предшествующего другого миело-пролиферативного заболевания. При развернутой (фибротической) форме наблюдается 2 или 3 степень фиброза в костном мозге, спленомегалия, бласты в крови, лейкоцитоз, анемия или тромбоцитопения. Другие формы миелофиброза возникают как результат заболеваний из группы миелопролиферативных – истинной полицитемии и эссенциальной тромбоцитемии. Диагностика и лечение этих форм заболевания не отличаются от первичного миелофиброза.
Миелофиброз может протекать по-разному. У некоторых пациентов болезнь длительно существует в хронической форме и не требует терапии, у других – прогрессирует в течение 1-2 лет. Существует ряд неблагоприятных признаков заболевания, которые говорят о том, что опухоль будет вести себя более агрессивно и риск осложнений значительно выше. К таким признакам относятся:
- Общие симптомы (повышение температуры, снижение массы тела, потливость)
- Уровень лейкоцитов 25х 109/л и более;
- Анемия, гемоглобин менее 100 г/л;
- Бласты в периферической крови;
- Возраст 65 лет и старше;
- Уровень тромбоцитов менее 100 х 109/л;
- Необходимость в переливаниях крови;
- Неблагоприятные цитогенетические поломки;
На основании суммы этих неблагоприятных факторов определяется группа риска прогрессирования заболевания. Выделяют 4 группы: низкого, промежуточного-1, промежуточного-2 и высокого риска. Определение группы риска помогает доктору выбрать правильное лечение.
Выполнение нескольких медицинских тестов является обязательными, если у пациента предполагается диагноз миелофиброз. Если не сделать самые важные из них, диагноз может быть поставлен неправильно, а последующее лечение — даже навредить больному. При первом осмотре доктор спросит вас о перенесенных ранее заболеваниях. Особенно важными является информация о наличии артериальной гипертензии, ишемической болезни сердца, нарушении обмена липидов, диабете, курении, ранее происходивших тромбозов, кровотечений, потребности в переливаниях крови, наличии опухолевых заболеваний у ваших родственников. Важно сообщить вашему доктору снижался ли у Вас вес, есть ли у Вас потливость, повышение температуры. При осмотре важным является обнаружение увеличенной селезенки и определение её размеров в сантиметрах ниже ребра и печени.
Клинический анализ крови — исследование, которое позволяет определить количество тромбоцитов, лейкоцитов, гемоглобина. Необходимо изучить, есть ли в анализе молодые формы лейкоцитов (миелоциты, метамиелоциты)и бласты, что характерно для миелофиброза. Вашим врачом может быть назначен биохимический анализ крови. Показатели этого анализа позволят оценить функцию внутренних органов (печень, почки), дефицит важных веществ для кроветворения и обмен железа. У пациентов, получающих много переливаний крови, в организме есть избыток железа, которое может быть токсичным для печени и сердца. В некоторых случаях такие состояния требуют назначения препаратов, связывающих и выводящих избыток железа.
Биопсия костного мозга — позволяет определить уровень бластов в костном мозге. Уровень бластов 20% и более означает, что произошло прогрессирование в последнюю стадию миелофиброза – острый миелобластный лейкоз.
Трепанобиопсия костного мозга является одним из основных методов, подтверждающих диагноз миелофиброз. Врач-гистолог исследует под микроскопом полученный в результате трепанобиопсии костный мозг. Он изучает количество, форму и расположение кроветворных клеток костного мозга и определяет степень разрастания фиброза. При наличии характерной картины костного мозга диагноз миелофиброза подтверждается. Сама по себе процедура получения костного мозга для исследования называется трепанобиопсией. Процедура неприятна, но занимает всего несколько минут, для ее проведения не требуется госпитализация. Во время процедуры врач также сначала производит тонкой иглой обезболивание, а затем вводит иглу большего размера, с просветом, для получения узкого (несколько миллиметров в диаметре) столбика костного материала для биопсии. При введении этой иглы в кость пациент обычно испытывает только притупленное давление. Когда врач отсоединяет костный материал и вынимает его, пациент испытывает ощущение подергивания. Процедура может быть болезненной в момент забора костного мозга, но подавляющее число пациентов переносит это без каких-либо проблем. Если Вас беспокоит это исследование, по назначению доктора Вы можете предварительно принять обезболивающий или успокаивающий препарат. После того как взятие пробы костного мозга завершено, пациента обычно отпускают домой. В целях безопасности при возвращении домой пациента должен кто-либо сопровождать, при этом пациенту при возвращении с исследования запрещается самостоятельно вести машину.
Исследование на наличие гена BCR-ABL1 позволяет исключить другое заболевание крови (хронический миелолейкоз) с очень похоже картиной крови и костного мозга. Для пациентов с хроническим миелолейкозом применяется принципиально другое лечение, поэтому данное исследование является важным.
Цитогенетическое исследование костного мозга помогает выявить неблагоприятные хромосомные поломки.
Где в России занимаются диагностикой и лечением можно прочитать в разделе КОНТАКТЫ
Общие сведения
Миелофиброз является заболеванием костного мозга. Особенно пораженными являются гемопоэтические стволовые клетки, используемые для производства эритроцитов, лейкоцитов и тромбоцитов.
Изменение гемопоэтической функции костного мозга приводит к снижению количества зрелых клеток в крови, особенно эритроцитов. Они определяют типичные признаки заболевания, среди которых основными являются анемия и спленомегалия (увеличение селезенки). Могут возникнуть и другие многочисленные симптомы, а иногда и серьезные осложнения. Часто люди, пораженные миелофиброзом, имеют измененный костный мозг не только по функции, но и по структуре; в частности, костный мозг богат волокнами коллагена, фактически фиброзными.
Сегодня существует множество вариантов лечения миелофиброза. Хотя возможно заменить дефектный костный мозг благодаря пересадке от донора, обычно предпочтительнее выбрать менее инвазивное терапевтическое вмешательство, направленное на облегчение всей симптоматики.
Что такое миелофиброз?
Термин миелофиброз относится к серьезному и сложному заболеванию костного мозга, которое изменяет процесс кроветворения. На самом деле, в крови людей с этим заболеванием количество клеток крови отличается от нормального.
Все это приводит к образованию, вредной, волокнистой ткани вместо той, которая обычно составляет костный мозг. С этой заменой тканей, производительная способность костного мозга еще больше снижается, следовательно, эритроцитов, лейкоцитов и тромбоцитов.
Миелофиброз — это редкая опухоль крови, относящаяся к так называемым хроническим миелопролиферативным новообразованиям (когда-то называвшимся хроническими миелопролиферативными заболеваниями); полицитемия вера (в основном характеризуется аномальным увеличением эритроцитов) и эссенциальная тромбоцитемия (в основном характеризуется патологическим увеличением числа тромбоцитов) также относятся к этой группе.
Миелофиброз является довольно редкой патологией, однако его точная частота неизвестна. Он может повлиять на людей любого возраста, хотя есть больше шансов заболеть в возрасте 50-60 лет.
Он чаще встречается среди белых и ашкеназских евреев.
Причины и факторы риска
Точная причина, ответственная за миелофиброз, еще полностью не выяснена. Участие гена, известного как JAK2, в ДНК гемопоэтических стволовых клеток в настоящее время не вызывает сомнений. Как только эта мутация появляется, она передается всем дочерним клеткам, в частности, эритроцитам, изменяя их функции.
Отсутствие в костном мозге здоровых и эффективных гемопоэтических клеток вызывает образование волокнистой ткани, лишенной какой-либо продуктивной активности.
Ген JAK2 играет фундаментальную роль в росте и делении клеток, особенно стволовых клеток крови. Это объясняет, почему его неисправность оказывает драматическое влияние на кроветворение.
Обнаружение связи между геном JAK2 и миелофиброзом является относительно недавним и все еще имеет некоторые нерешенные вопросы. Согласно данным, собранными исследователями, около половины пациентов имеют мутацию JAK2; эта мутация делает ген JAK2 постоянно активным и изменяет отношения между мутированными и соседними клетками.
Существует две формы миелофиброза: первичная и вторичная.
- Первичный миелофиброз — это форма, которая возникает из-за вышеупомянутой генетической мутации JAK2.
- Вторичный миелофиброз, с другой стороны, является осложнением, которое возникает после других патологических состояний, таких как эссенциальная тромбоцитемия и полицитемия вера.
Хотя точные причины миелофиброза до сих пор не определены, с другой стороны, факторы риска были определены с уверенностью.
- Пожилой возраст. Это правда, что миелофиброз может возникнуть в любом возрасте, но в равной степени верно и то, что наиболее пораженными являются люди в возрасте 50-60 лет и старше.
- Некоторые заболевания крови. Такие заболевания, как тромбоцитемия и полицитемия, могут вызывать различные осложнения, включая миелофиброз.
- Воздействие определенных препаратов и химикатов. Длительный контакт с промышленными продуктами, такими как толуол и бензол, в течение длительного времени может вызвать миелофиброз.
- Воздействие радиации. У тех, кто выжил в результате бомб и атомных (ядерных) катастроф, может развиться рак, включая миелофиброз. Кроме того, между 1920 и 1950 годами использование в диагностической медицине радиоактивного контрастного вещества, известного как торотрасто, привело к заболеванию нескольких человек.
Симптомы и осложнения
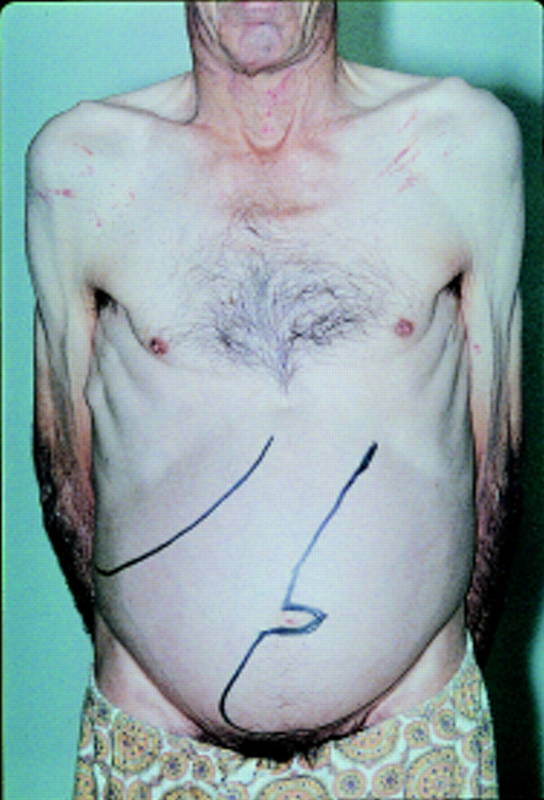
Миелофиброз протекает очень медленно, с симптомами, которые — от почти незаметных в начале — становятся очевидными и очень изнурительными на поздней стадии.
Прогрессивная продуктивная неспособность костного мозга вызывает анемию (недостаток эритроцитов), иногда лейкопению (недостаток лейкоцитов) и тромбоцитопению (недостаток тромбоцитов), а также ряд признаков, непосредственно связанных с этими патологическими состояниями, а именно:
- чувство усталости и слабости;
- одышка;
- увеличенная селезенка (спленомегалия);
- увеличенная печень (гепатомегалия);
- бледность кожи;
- легкое начало гематом и кровотечений;
- ночная потливость;
- лихорадка;
- рецидивирующие инфекции;
- боль в костях.
Лейкопения и тромбоцитопения встречаются реже, чем анемия (которая всегда присутствует) и появляются на более поздней стадии заболевания.
Спленомегалия (или увеличенная селезенка) является одним из основных признаков миелофиброза (поражает около 90% пациентов), поэтому появление этого симптома заслуживает особого внимания.
Из-за процесса фиброза, вовлекающего костный мозг, гемопоэтические стволовые клетки мигрируют в поисках альтернативного участка, где могут быть произведены клетки крови (экстрамедуллярный гемопоэз). Первыми участками, достигаемыми этими клетками, являются селезенка и печень. Здесь, клетки крови, однажды произведенные, накапливаются неуклонно, так как они не входят в кровообращение (даже если бы они это сделали, они все равно были бы дефектными клетками). Это патологическое накопление увеличивает вышеупомянутые органы. Это может вызвать различные осложнения, так как это предрасполагает пациента к инфекциям, кровотечениям, легким травматическим разрывам и т. д.
Характерными выражениями спленомегалии являются боль и ощущение полноты ребер в левой части тела. Эти ощущения особенно выражены, когда желудок, кишечник и мочевой пузырь переполнены.
Осложнения, которые могут возникнуть у пациентов с миелофиброзом, различны; они в значительной степени зависят от сниженных производственных возможностей костного мозга и только в меньшей степени от спленомегалии.
Диагностика
Для точного установления диагноза миелофиброза необходимо физическое обследование, полный анализ крови и биопсия костного мозга. Кроме того, чтобы понять причины и идентифицировать любые осложнения, также необходимо выполнить генетический тест и некоторые радиологические тесты.
— Физическая экспертиза.
Во время физического осмотра врач просит пациента описать их симптомы. Затем он сначала посещает его, измеряя уровень артериального давления и объем лимфатических узлов и живота. Если селезенка и печень опухшие, их также можно определить при пальпации.
— Анализ крови.
На образце крови, взятом у пациента, выполняется так называемый подсчет клеток крови. Человек с миелофиброзом имеет низкое количество эритроцитов (таким образом, анемия) и аномальный уровень лейкоцитов и тромбоцитов.
— Биопсия костного мозга.
Она состоит из сбора костного мозга и его анализа в лаборатории. Она представляет собой исследование объекта, если вы хотите подтвердить подозрения на миелофиброз, возникшие в результате предыдущих исследований.
Образец извлекается из подвздошной кости (из бедра) с помощью шприца и после местной анестезии.
Процедура длится всего 15-20 минут, и пациент может чувствовать небольшую боль в течение нескольких дней после удаления.
— Генетические испытания и радиология.
Генетические тесты полезны, если врач подозревает первичный миелофиброз, поддерживаемый генетической мутацией JAK2.
Рентгенологические исследования, такие как ядерный магнитный резонанс и рентген, дают дополнительную информацию о патологическом состоянии пациента.
Лечение
Для лечения миелофиброза нужно действовать на корень и заменять неэффективный костный мозг трансплантацией.
Тем не менее, эта терапия имеет высокий риск для пациента, поэтому очень часто используются альтернативные, достаточно эффективные методы лечения, которые направлены на смягчение и облегчение основных симптомов миелофиброза. Терапевтическое предложение, имеющее вышеупомянутые цели, является обширным, и выбор одного лечения, а не другого, зависит от типа миелофиброза и тяжести состояний, в которых находится пациент.
Первоначальный миелофиброз является асиноматическим, поэтому диагноз является случайным и обычно ставится после обычного анализа крови. В этих ситуациях пациент не должен проходить какое-либо лечение; единственная забота — проводить периодические проверки для отслеживания развития заболевания.
Недостаток эритроцитов является одним из основных и наиболее изнурительных симптомов. Чтобы облегчить анемию, используйте:
- Периодические переливания крови.
- Андрогенная терапия. Мужские гормоны способствуют выработке эритроцитов. Однако ее применение зависит от причин миелофиброза и не лишено побочных эффектов (повреждение печени и маскулинизация у женщин).
- Стимуляторы эритропоэза: стимулируют выработку эритроцитов. Эритропоэтин, например, представляет собой гормон, обычно вырабатываемый почкой, который стимулирует выработку эритроцитов в костном мозге.
- Талидомид. Связанный с другими лекарственными средствами, такими как леналидомид, он повышает количество эритроцитов и уменьшает спленомегалию.
Спленомегалию можно лечить по-разному, в зависимости от тяжести ситуации.
- Если она присутствует в легкой стадии, пациент может пройти химиотерапию. Это противоопухолевая терапия, которая уничтожает неэффективные клетки крови, присутствующие в селезенке.
- Если спленомегалия тяжелая и химиотерапия не дала результата, решение — хирургическое удаление селезенки.
- Наконец, если вмешательство по удалению было невозможно (из-за проблем со здоровьем у пациента), используется другое противораковое лечение — лучевая терапия. Как и химиотерапия, она также действует за счет уменьшения количества неэффективных клеток крови.
- Химиотерапия:
- уничтожение лейкоцитов;
- токсическое воздействие на сердце.
- Хирургическая операция:
- легкие инфекции;
- венозный тромбоз.
- Радиотерапия:
- воздействие высокоэнергетического излучения;
- усталость;
- раздражение кожи.
Ингибитор вредного гена JAK2 — это недавно открытый и одобренный препарат, известный как руксолитиниб. Этот тип лечения применяется в случаях первичного миелофиброза, для которого была обнаружена генетическая мутация JAK2.
Под трансплантацией костного мозга мы подразумеваем аллогенную трансплантацию (т. е. от совместимого донора) гемопоэтических стволовых клеток.
Это довольно инвазивная и опасная терапевтическая процедура, настолько, что она применяется только в случае крайней необходимости.
Прогноз
Прогноз, связанный с миелофиброзом, варьируется от пациента к пациенту.
Он положителен для тех, кто осторожно реагирует на заботу. Вместо этого он негативен для тех, кто, к сожалению, не получает заметных терапевтических преимуществ.
В обоих случаях, однако, качество жизни ухудшается, учитывая, что человек с миелофиброзом должен постоянно принимать лекарства и следить за состоянием своего здоровья с помощью периодических обследований.
Читайте также:

