Лучевая терапия после операции рака слюнной железы
Лечение доброкачественных и злокачественных опухолей слюнных желез обычно проводят хирургическим методом. При доброкачественных опухолях околоушной железы (чаще всего локализованных в ее поверхностной части) проводят частичную паротидэктомию с сохранением лицевого нерва. При полном удалении опухоли операция дает отличный результат.
Если нет уверенности в радикальном удалении опухоли, обязательно назначают лучевую терапию, которая снижает вероятность рецидивирования. Хотя при подозрении на неполное удаление опухоли некоторые хирурги предпочитают тактику выжидательного наблюдения, такой подход может привести к необходимости проведения повторной операции с сопутствующим риском повреждения лицевого нерва.
Поэтому в таких случаях более безопасно назначить больному курс лучевой терапии. При опухолях подчелюстной и подъязычной желез допустима более радикальная резекция, поскольку в данном случае не существует опасности затронуть лицевой нерв.
К числу показаний к проведению лучевой терапии относятся следующие: недостаточное соблюдение принципов абластики при проведении операции и случаи высокозлокачественных опухолей (особенно сквамозные, анапластические и смешанные опухоли). Лучевая терапия целесообразна, если хирургический метод уже использовался при возникновении рецидива опухоли, и для удаления злокачественной лимфомы околоушной железы.
Также необходимо использовать облучение при наличии противопоказаний к проведению полостной операции. Имеются подтверждения необходимости использования лучевой терапии после проведения операции по поводу любых злокачественных опухолей слюнных желез. К наиболее радиочувствительным опухолям относятся лимфомы и аденокарциномы. В отдельных случаях имеются противопоказания к проведению хирургической операции, например возраст или плохое общее состояние больного.
Также не стоит проводить операцию, если опухоль локализована в малых слюнных железах, в носоглотке или на небе. В этих случаях, после проведения курса лучевой терапии, иногда удается контролировать ее рост в течение длительного промежутка времени.

Проведение лучевой терапии может оказаться технически сложным, поскольку необходимо равномерно облучить большой объем ткани и не допустить переоблучения чувствительных областей, таких как мозговой ствол, глаз и слизистая оболочка. Обычно облучают в двух полях с клиновидными фильтрами. Следует принимать специальные меры к тому, чтобы не допустить облучения контралатерального глаза выходным пучком радиации. Для доброкачественных опухолей обычно назначают дозу 50-55 Гр, которая дается во фракциях на протяжении 5-5,5 недель.
Злокачественные опухоли околоушной железы облучают в большей дозе. При подозрении на неполное удаление опухоли после операции рекомендуется назначать суммарную дозу 60-70 Гр в течение 6-8 недель. Поскольку вначале облучается большой объем опухоли, в дальнейшем поле можно сузить. Околоушную железу следует облучать от скуловой дуги и с нижней стороны до подъязычного уровня, с тем чтобы захватить яремно-двубрюшные и верхние шейные лимфатические узлы. В случаях опухолей подчелюстной и подъязычной желез также необходимо облучать большой объем ткани, поскольку при этом должна быть облучена железа, целиком.
Цистаденоидные опухоли необходимо облучать в радикальной дозе, так как они имеют тенденцию распространяться в периневральное пространство. При цилиндроме всегда необходимо облучать область сосцевидного отростка височной кости.
Следует ли облучать всю цепочку лимфатических узлов у больных со злокачественной опухолью слюнной железы? Степень поражения лимфатических узлов зависит от гистологической характеристики опухоли, поэтому облучать их следует только у больных с опухолями сквамозного или анапластического типа. Облучение лимфатических узлов также необходимо при аденокарциноме или мукоэпидермоидной опухоли и в случаях высокозлокачественных опухолей смешанного типа. В ряде клиник США таким больным проводят удаление лимфатических узлов.
Прогноз рака слюнных желез
Результат лечения зависит от гистологического типа опухоли и от ее операбельности. Назначение после операции курса лучевой терапии улучшает контроль над ростом всех основных опухолей, однако сквамозная, анапластическая и высокозлокачественная мукоэпидермоидная карциномы характеризуются крайне неблагоприятным прогнозом, поскольку часто дают рецидивы и склонны к метастазированию. Более эффективный результат достигается для низкозлокачественных мукоэпидермоидных опухолей и опухолей ацинарных клеток, а также для цистаденоидных карцином и злокачественных опухолей смешанного типа, которые характеризуются промежуточным прогнозом.
В целом, у женщин прогноз более благоприятный, чем у мужчин (10-летняя выживаемость 75% и 60% соответственно).
В случаях локальных рецидивов иногда возможно проведение повторной операции, хотя при наличии отдаленных метастазов назначение курса паллиативной лучевой терапии оказывается для больного более полезным. Особенно это справедливо для случаев менее агрессивных медленнорастущих опухолей. Нередко отмечаются отдаленные метастазы в легкое и в другие органы, особенно при цистаденоидной карциноме. Пока не выяснено, насколько эффективна в данном случае химиотерапия.
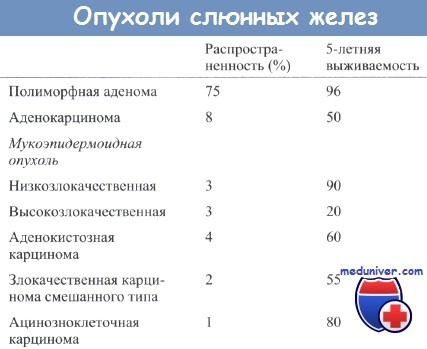
Гистологические характеристики опухолей слюнных желез и выживаемость больных
- Причины рака слюнной железы и группы риска
- Симптомы заболевания
- Методы диагностики
- Классификация: типы рака слюнной железы
- Стадии заболевания
- Лечение
- Осложнения и рецидивы
- Прогноз жизни при разных стадиях рака и профилактика
Слюнные железы вырабатывают слюну — жидкость, находящуюся в ротовой полости и выполняющую некоторые важные функции: смачивание слизистой оболочки, пищи, облегчение артикуляции, глотания, защиту от болезнетворных бактерий и пр. Выделяют две группы слюнных желез:
- Большие: подъязычные, околоушные, подчелюстные.
- Малые имеют микроскопическое строение, разбросаны по всей ротовой полости — всего их насчитывается несколько сотен.
Рак может развиваться во всех этих железах. Чаще всего (в 7 из 10 случаев) доброкачественные и злокачественные опухоли возникают в околоушных слюнных железах. Примерно 1–2 опухоли из десяти приходятся на подчелюстные слюнные железы, в 50% случаев они имеют злокачественный характер. В редких случаев рак развивается в подъязычной или мелких слюнных железах.
Причины рака слюнной железы и группы риска
Выделяют некоторые факторы риска, повышающие вероятность развития злокачественной опухоли:
- Чем старше человек, тем больше накапливается изменений в его генах, тем выше вероятность развития различных типов рака.
- У мужчин рак слюнной железы бывает чаще, чем у женщин.
- Облучение головы. Например, это может быть ранее перенесенный курс лучевой терапии, воздействие ионизирующих излучений на рабочем месте.
- Есть данные о том, что риск рака слюнных желез повышен у людей, которые имеют определенные профессиональные вредности: контакт с асбестом, пылью сплавов никеля, работа на предприятиях, которые занимаются производством резины, деревообработкой.
Роль наследственности на данный момент считается незначительной. Большинство больных не имеют отягощенного семейного анамнеза (близких родственников, у которых был диагностирован тот же тип рака). Не доказана роль алкоголя и табака. Известно, что эти вредные привычки в целом повышают риск развития рака головы и шеи, но связь со злокачественными опухолями слюнных желез не обнаружена.
Опасен ли мобильный телефон? Во время одного исследования ученые обнаружили, что у активных пользователей сотовых телефонов чаще встречаются опухоли околоушной слюнной железы (как правило, доброкачественные). Но другие исследования такой взаимосвязи не выявили.
Симптомы заболевания
Доброкачественные и злокачественные опухоли слюнных желез проявляются сходными симптомами. Одно из главных отличий в том, что рак растет намного быстрее и чаще приводит к ряду симптомов, связанных с прорастанием в окружающие ткани, сдавлением нервов.

Нужно посетить врача, если вас стали беспокоить следующие симптомы:
Методы диагностики
Во время первичного приема врач-онколог беседует с пациентом, расспрашивает его, пытаясь выяснить факторы риска, проводит осмотр. Доктор ощупывает опухоль на лице и шейные лимфатические узлы, оценивает чувствительность лица и работу мимических мышц. После этого больной может быть направлен на дополнительную консультацию к ЛОР-врачу.
Компьютерная томография и магнитно-резонансная томография помогают оценить размеры, форму и расположение опухоли, обнаружить очаги в лимфатических узлах и других органах. В настоящее время золотым стандартом в поиске отдаленных метастазов является ПЭТ-сканирование. Если опухоль находится рядом с челюстью, проводят рентгенографию. Рентгенографическое исследование грудной клетки помогает обнаружить метастазы в легких, оценить состояние легких и сердца перед хирургическим лечением.
Самый точный метод диагностики рака слюнных желез — биопсия. Во время этой процедуры врач получает фрагмент патологически измененной ткани и отправляет в лабораторию для цитологического, гистологического исследования.
Чаще всего проводят тонкоигольную аспирационую биопсию. Опухолевую ткань получают с помощью полой иглы, напоминающей ту, что используют для инъекций. Если не удается получить нужное количество ткани, врач проводит инцизионную биопсию: делает разрез и удаляет часть опухоли.
Если в образце обнаружены опухолевые клетки, диагноз рака практически не вызывает сомнений.
Классификация: типы рака слюнной железы
Слюнные железы состоят из разных типов клеток, любые из них могут дать начало злокачественной опухоли. Поэтому тут встречаются разные типы рака:
- Мукоэпидермоидный рак слюнной железы — наиболее распространенная разновидность. Чаще всего он встречается в околоушных слюнных железах, реже — в подчелюстных и мелких. Эти опухоли редко бывают агрессивными.
- Аденоидная кистозная карцинома характеризуется очень медленным ростом и редким метастазированием. Однако, от этой злокачественной опухоли бывает очень сложно избавиться: она может рецидивировать спустя длительное время после лечения.
- Аденокарциномой называют злокачественную опухоль, которая развивается из железистых клеток. В слюнных железах могут возникать разные виды аденокарцином: ациноклеточный рак, полиморфная аденокарцинома низкой степени злокачественности, базальноклеточная аденокарцинома, светлоклеточный рак, цистаденокарцинома и др.
- К редким типам злокачественных раковых опухолей слюнных желез относят: плоскоклеточный рак, эпителиально-миоэпителиальную карциному, анапластическую мелкоклеточную карциному, недифференцированные карциномы.
Стадии заболевания
Рак слюнных желез, как и другие злокачественные опухоли, классифицируют по стадиям в соответствии с общепринятой системой TNM. Буква T в аббревиатуре обозначает характеристики первичной опухоли: размеры и степень ее прорастания в окружающие ткани, N — распространение в лимфатические узлы, M — наличие отдаленных метастазов. В зависимости от этих показателей, в течении рака слюнной железы выделяют следующие стадии:
Помимо стадий, выделяют три степени злокачественности рака слюнных желез:
- I степень — низкая степень злокачественности. Такие опухоли называют высокодифференцированными. Опухолевая ткань максимально похожа на нормальную ткань слюнных желез. Она медленно растет, и прогноз для таких пациентов наиболее благоприятен.
- II степень — это умеренно дифференцированные опухоли. Опухолевая ткань более существенно отличается от нормальной. Такой рак более агрессивен и отличается более плохим прогнозом.
- III степень — низкодифференцированные опухоли. Раковые клетки практически полностью утрачивают черты нормальных. Такие опухоли ведут себя наиболее агрессивно.
Определение степени злокачественности помогает врачу спрогнозировать, как будет вести себя рак, и правильно спланировать лечение.
Лечение
Лечением пациента занимается команда врачей, в которую могут входить: клинический онколог, ЛОР-врач, онколог-хирург, челюстно-лицевой хирург, химиотерапевт, радиотерапевт и др. Программа лечения определяется стадией рака, гистологическим типом опухоли, ее локализацией (какая железа поражена), возрастом, общим состоянием и сопутствующими заболеваниями пациента.
Если опухоль не сильно проросла в окружающие ткани, то она является резектабельной, то есть ее можно удалить хирургическим путем. Задача хирурга — иссечь опухоль с захватом окружающих тканей так, чтобы на линии разреза не осталось раковых клеток, то есть обеспечить негативный край резекции. Если опухолевые клетки распространились в лимфатические узлы, или по данным биопсии диагностирован агрессивный рак, лимфоузлы также удаляют.
При раке околоушной слюнной железы хирургическое вмешательство представляет определенные сложности, потому что через железу проходит лицевой нерв, который контролирует работу мимических мышц. Если опухоль затрагивает только поверхностную долю железы, можно удалить ее отдельно — выполнить поверхностную паротидэктомию. При этом нет риска повредить лицевой нерв. В некоторых случаях приходится удалять всю железу, а если опухоль проросла в лицевой нерв — то и его.
При раке подъязычной и поднижнечелюстной железы хирург удаляет саму железу и часть тканей, расположенных вокруг нее, в том числе, возможно, костную ткань. В некоторых случаях приходится иссекать нервы, которые контролируют чувствительность, движения в нижней части лица, в языке, чувство вкуса.
При раке мелких желез удаляют пораженную железу и часть окружающих тканей. Объем операции зависит от размеров и расположения опухоли.
Показания к применению лучевой терапии при злокачественных опухолях слюнных желез:
- Для борьбы со злокачественными опухолями, которые не могут быть удалены хирургическим путем в силу своего расположения или размеров. Иногда облучение дополняют курсами химиотерапии.
- После хирургического лечения. Такую лучевую терапию называют адъювантной, иногда ее сочетают с химиотерапией. Облучение после операции помогает уничтожить оставшиеся раковые клетки и предотвратить рецидив.
- При запущенном раке. В данном случае лучевая терапия направлена на борьбу с болью, нарушением глотания, кровотечением и другими симптомами.
Обычно облучение проводят пять дней в неделю в течение 6–7 недель. Если лучевую терапию применяют в паллиативных целях, курс будет короче.
Химиотерапию применяют при злокачественных новообразованиях слюнных желез довольно редко. Противоопухолевые препараты могут уменьшить размеры опухоли, но не способны полностью ее уничтожить. Чаще всего их назначают при запущенном раке в качестве паллиативного лечения или в дополнение к лучевой терапии.
После лечения могут сохраняться некоторые проблемы, связанные с повреждением нервов: нарушение функции мимической мускулатуры лица, расстройства речи, глотания, косметические дефекты. Некоторые побочные эффекты химиопрепаратов и лучевой терапии проходят после завершения терапии, а другие сохраняются в течение длительного времени. В таких случаях показаны курсы реабилитации. Врач составляет программу восстановительного лечения индивидуально, в зависимости от тяжести и характера расстройств.
Осложнения и рецидивы
Даже если лечение завершилось успешно, и по результатам обследования в организме пациента не обнаруживаются признаки присутствия раковых клеток, в будущем может произойти рецидив. Поэтому нужно регулярно наблюдаться у врача-онколога, приходить на осмотры, проходить различные исследования и сдавать анализы.
Обычно доктор назначает осмотры раз в несколько месяцев в течение нескольких лет, затем — реже.
- Если произошел рецидив рака, варианты лечения могут быть разными:
- Если опухоль может быть удалена, выполняют хирургическое вмешательство с последующим курсом лучевой терапии.
- Если опухоль не получается удалить хирургически, врач назначает лучевую терапию в сочетании с химиотерапией.
- Если имеются отдаленные метастазы, основным методов лечения становится химиотерапия. Лучевую терапию и хирургическое лечение можно использовать для борьбы с некоторыми симптомами.
При запущенном раке с метастазами достижение ремиссии становится крайне маловероятным. В таком случае лечение будет направлено на замедление прогрессирования рака, борьбу с симптомами, продление жизни больного.
Врачи Европейской клиники берутся за лечение рака на любой стадии. Для нас не существует безнадежных пациентов. Всегда можно помочь, и мы знаем, как это правильно сделать, у нас есть все необходимые технологии, препараты последних поколений.
Прогноз жизни при разных стадиях рака и профилактика
Прогноз для онкологических больных принято измерять показателем пятилетней выживаемости. Это процент пациентов, которые остались живы в течение пяти лет после того, как у них была диагностирована злокачественная опухоль.
Пятилетняя выживаемость на разных стадиях при злокачественных опухолях слюнных желез составляет:
- Локализованный рак (не распространился за пределы слюнной железы — 0, I и II стадии) — 93%.
- Рак, распространившийся в окружающие ткани и лимфатические узлы (стадии III, IVA и IVB) — 67%.
- Рак с метастазами (стадия IVC) — 34%.
Злокачественные опухоли в слюнных железах бывают разными, поэтому важно понимать, что это средние цифры, они зависят от типа рака и степени его агрессивности. Кроме того, эти цифры рассчитаны на основании данных о пациентах, у которых заболевание было диагностировано 5 лет назад и раньше. Но онкология развивается, возможности врачей постоянно растут. Поэтому больные, которые проходят лечение сейчас, могут иметь лучший прогноз.
Специальных методов профилактики не существует. Нужно в целом вести здоровый образ жизни, своевременно обращать внимание на подозрительные симптомы и обращаться к врачу.
Лучевая терапия в лечении опухолей слюнных желез (СЖ) стала использоваться с момента внедрения этого метода в клинику. До разработки и широкого внедрения в онкологическую практику хирургических вмешательств лучевая терапия оставалась единственно возможным способом лечения. Уже в 30-е годы прошлого века клиницисты имели представление о различной чувствительности опухолей больших и малых СЖ к лучевому воздействию. Так, Н.Н. Петров пишет о высокой чувствительности малодифференцированных карцином и радиорезистентности большинства других карцином и сарком СЖ.
За период существования радиологии в клинике использовались различные источники излучения: от препаратов 226Ra, 60Со до мегавольтных установок, генерирующих излучение различных видов энергий (от 4-6 до 20-50 MB).
Лучевая терапия проводится с радикальной и паллиативной целью. Показанием к проведению радикальной лучевой терапии являются малодифференцированные карциномы слюнной железы с распространенностью T1-T3. Паллиативная лучевая терапия применяется при установлении факта неизлечимости больного с распространенностью процесса Т4 или неоперабельных регионарных метастазов в лимфатических узлах и отдаленных метастазов, при отказе пациента от хирургического вмешательства при любой морфологической форме карциномы, при невозможности выполнения радикальной операции по общему состоянию, из-за преклонного возраста, наличия тяжелой соматической патологии.
Лучевая терапия проводится на первичный очаг, регионарные зоны. Лечению могут также подвергаться пациенты с отдаленными метастазами (преимущественно в легкие и кости скелета). Режим лучевого воздействия выбирается в соответствии с патологией и ожидаемой продолжительностью жизни. Паллиативное лечение может проводиться по радикальной программе и в укороченном режиме.
На радиочувствительность оказывает влияние объем опухоли, наличие большого количества клеток в состоянии гипоксии и в состоянии покоя (фаза GO). На излечимость опухоли влияние оказывает величина толерантной дозы для окружающих нормальных тканей в зоне лучевого воздействия. Известно, что кожа имеет умеренную чувствительность, а соединительная ткань, мышцы, кости относительно рентгенорезистентны. Последствия лучевого воздействия на кожу проявляются развитием эритемы, сухого и влажного эпидермита, нарушением функции сальных и потовых желез, пигментацией или депигментацией, фиброзом, атрофией подкожной клетчатки, телеангиоэктазиями.
Нервная ткань является высокочувствительной к лучевому воздействию, особенно гипоталамус, ствол мозга, хиазма зрительных нервов, поясничный и шейный отделы спинного мозга. Повышение дозы лучевого воздействия больше 50 Гр влечет за собой осложнение в виде миелита с развитием геми- или параплегии, нарушением функции черепных нервов. Чтобы получить положительный эффект, распределение дозы в облучаемом объеме ткани должно точно соответствовать условиям ее гомогенности для всех участков опухоли. В то же время превышение дозы лучевого воздействия на здоровую ткань влечет за собой радиационные осложнения. Таким образом, задача лучевой терапии — излечение опухоли без значительного риска серьезных осложнений.
Большую роль в лучевом лечении играет объем облучаемых тканей. Известно, что с увеличением облучаемого объема уменьшается толерантность к облучению. Для разрушения опухоли необходимо воздействие достаточно большой дозы, величина которой ограничена толерантностью нормальных тканей. Современная радиобиология позволяет определить дозу, необходимую для разрушения клеток различных типов опухоли. Так, для аденокарциномы она составляет от 50 до 75 Гр в зависимости от распространенности процесса при обычном фракционировании.
Принципы лучевого лечения
В основу принципов лучевого лечения положена концепция анатомического поля, предложенная Coutard еще в 1934 г. По этой концепции лучевое лечение первичной опухоли необходимо проводить вместе с путями лимфатического оттока и обязательным включением первого регионарного барьера.
Лучевой метод лечения прошел достаточно большой путь развития с появлением новых источников излучения и совершенствованием технических средств лучевого воздействия. Кроме методов наружного воздействия на опухоль были разработаны способы непосредственного воздействия: аппликационная, внутритканевая, внутриполостная радиевая терапия, близкофокусная рентгенотерапия. Неудовлетворительные результаты лечения инфильтративных и распространенных процессов привели к разработке сочетанных способов лучевого воздействия. Эта методика нашла применение в лечении новообразований слизистых оболочек полости рта и ротоглотки, включая опухоли, исходящие из малых СЖ.
Радикальное лучевое лечение проводится на гамма-терапевтических установках ГУТ-Со-400 или линейном ускорителе. В качестве источников излучения используется Со-60 или мегавольтное излучение. Для обеспечения лучевого лечения проводится рентгенотопометрическая подготовка. Производится дозиметрический расчет плана лучевого лечения. Осуществляется технологическое, дозиметрическое, метрологическое обеспечение лучевой терапии.
Для лечения рака околоушной СЖ используются два противолежащих поля размерами 6x8 см. При низкодифференцированном раке околоушной слюнной железы Т1-3N0M0 режим облучения включает разовую очаговую дозу (РОД) 2 Гр, 5 фракций в неделю до СОД 60-70 Гр.
Лечение проводится по расщепленному плану в два этапа:
1-й этап — СОД 40-50 Гр, 2-й этап — СОД 20-30 Гр. Лучевая терапия при более распространенном опухолевом процессе T4a-bN0-3 или при любом распространении первичной опухоли и отдаленных метастазах может быть рекомендована с паллиативной целью при отказе от других методов лечения или противопоказаниях к операции по сопутствующей патологии, возрасту и функциональным особенностям организма.
Целью данного лечения является максимально возможное подавление опухолевого процесса и продление жизни больного не менее чем на 4-6 мес. Основную роль выполняет наружное облучение методом дистанционной гамма-терапии. При лечении опухолей малых СЖ возможно применение сочетанного лучевого лечения с использованием внутриполостной близкофокусной рентгенотерапии.
Лучевое лечение рецидивов рака околоушной СЖ рекомендуется в случае невозможности использования хирургического или комбинированного методов. Режим лучевого воздействия определяется предшествующим лечением. Если больной ранее подвергался лучевому воздействию, то дистанционная гамма-терапия рекомендуется РОД 1,5-2 Гр до СОД 30-50 Гр с учетом сроков, прошедших после ранее проведенного лечения до СОД 60-70 Гр. Если ранее больной не получал лучевую терапию, то она может быть проведена по радикальной программе.
Методика лучевого лечения
Методика лучевого лечения опухолей малых слюнных желез зависит от локализации и распространенности опухоли. Лечение проводится по принципам, сформированным для плоскоклеточного рака слизистых оболочек. Лучевая терапия карцином малых СЖ в плане самостоятельного лечения проводится методами наружного облучения, внутритканевой терапии и сочетанием наружного облучения и внутритканевой и внутриполостной терапии. Степень распространенности опухолевого процесса соответствует символам Tis, Т1-2N0M0. Методика лечения заключается в воздействии на опухоль дистанционной гамма-терапии чаще способом классического фракционирования или нетрадиционного фракционирования расщепленным курсом СОД 60 Гр с перерывом между курсами 2 недели.
Внутритканевая лучевая терапия проводится путем введения в опухоль радиоактивных игл. В качестве источника излучения представлен СО 60. Лечение осуществляется в течение 3-5-7 дней.
Сочетанное лучевое лечение представляет воздействие наружного облучения до СОД 36-40 Гр и внутриполостной или внутритканевой лучевой терапии в СОД 30-40 Гр. Перед вторым этапом лечения оценивается эффект первого и определяется степень целесообразности выработанного плана. При условии обнаружения радиорезистентности во втором этапе рекомендуется хирургическое лечение.
Лучевое лечение используется также при лечении поражений Т3 как самостоятельный метод и как метод паллиативной терапии в стадии Т4 при невозможности выполнения или отказе от других методов лечения. При паллиативном лечении изъязвленных карцином в полости рта внутритканевая терапия не используется.
Лечение рецидивных карцином зависит от дозы и сроков предшествовавшего рецидиву лучевого лечения. Если ранее применялось только наружное облучение, то возможно использование сочетанного лучевого воздействия.
В качестве подготовки к лучевому лечению необходимо произвести санацию полоти рта: удалить разрушенные и кариозные зубы, корни зубов, кроме зубов, расположенных в зоне опухоли или близко от нее. Также подлежат удалению металлические зубы и коронки, пластины, являющиеся источниками вторичного излучения. Экстракция зубов во время и по окончанию лучевого лечения может привести к перелому челюсти. Необходимо сделать посев флоры из опухолевого очага или полости рта, если опухоль не изъязвлена, для определения чувствительности к антибиотикам. Не рекомендуется употребление спиртных напитков, курение, употребление острой, раздражающей пищи.
В клинике лучевое лечение в качестве самостоятельного метода получали немногие пациенты, которые отказывались от хирургического этапа лечения, или пациенты, которым хирургическое лечение не было показано по распространенности процесса, по сопутствующим заболеваниям и противопоказанию к общей анестезии. Среди пациентов с карциномами больших СЖ лучевое лечение получили 4,6% (32 из 696), а в группе карцином малых слюнных желез — 6,5% (20 из 309).
Применялось наружное облучение расщепленным курсом способом классического фракционирования, РОД 2 Гр, 5 раз в неделю до СОД 60-70 Гр. У части пациентов полная регрессия опухоли отмечена на СОД 48-50 Гр. При дальнейшем наблюдении рецидивы возникли в сроки от 5 мес. до 7 лету пациентов с МК околоушной СЖ, в среднем через 2,4 года. Среди пациентов, которым удалось выполнить хирургическое вмешательство в связи с рецидивом после лучевого лечения, большинство больных умерли в сроки от 1 года до 8 лет, в среднем через 3,8 года, от прогрессирования опухолевого процесса. Паллиативное лучевое лечение, проведенное порадикальной программе пациентам с распространением опухоли Т4, оказалось без эффекта. Через 4 мес. отмечена генерализация опухоли с обширным регионарным, внутрикожным метастазированием.
Лучевая терапия аденоидно-кистозной карциномы (АКК) подъязычной СЖ солидного типа T4aN0M1 проводилась самостоятельно в связи с наличием отдаленных метастазов в легких. Лечение проводилось с трех полей расщепленным курсом в СОД 70 Гр. Через 1 месяц отмечено прогрессирование опухоли, а через 1 год констатирован летальный исход
Лучевая терапия проведена 25% пациентам с АКК твердого и мягкого нёба. Распространенность процесса среди первичных больных соответствовала Т1-3 N0M0, рецидивы после иссечения опухоли носили ограниченный характер. Методика лучевого лечения заключалась в проведении дистанционной гамма-терапии в СОД 60 Гр с полной регрессией опухоли. Наблюдение в течение 10-15 лет не выявило признаков заболевания. Сочетанная лучевая терапия включала наружное облучение в СОД 55 Гр и близкофокусную рентгенотерапию в СОД 35 Гр у пациентов с распространенностью T4N0-1М0. Регрессия опухоли у этих пациентов была более 75%. В связи с отказом от хирургического лечения через 4 мес. отмечен продолженный рост опухоли и метастазов.
Лучевое лечение в качестве самостоятельного метода получили больные с локализацией опухоли в области корня языка и альвеолярного отростка нижней челюсти. Пациент с низкодифференцированным типом рака корня языка наблюдается более 7 лет без признаков заболевания. Пациент с локализацией опухоли в области альвеолярного отростка нижней челюсти (T4N0M0) умер от прогрессирования опухоли через 3 года после лечения.
Весьма эффективным является лучевое лечение АКК трахеи, особенно низкодифференцированного ее варианта. Используется наружное и внутриполостное облучение одновременно или последовательно. Режим фракционирования классический, 5 раз в неделю, РОД — 2 Гр, СОД — 40-70 Гр дистанционной гамма-терапии и 30-80 Гр внутриполостной гамма-терапии (РОД-5-10 Гр) 2-3 раза в неделю.
Режим фракционирования может быть изменен в зависимости от размеров поражения. Пятилетняя выживаемость составляет 70%, 10-летняя — 50%. Лучевая терапия проводится также в случае нерезектабельности опухоли. Отдаленные метастазы в легкие, которые мы наблюдали, не являются противопоказанием к лучевому лечению. Таким образом, лучевое лечение получили 21 (10,5%) из 199 пациентов с АКК малых слюнных желез с выраженным положительным результатом.
Лучевое лечение первичной АК мы не применяли. Но лучевому лечению подвергался пациент с рецидивом АК после хирургического лечения. Лечение проводилось методом дистанционной гамма-терапии в СОД 62,5 Гр. Пациент наблюдается без рецидива и метастазов в течение 5 лет. Чувствительность этой формы опухоли к лучевому воздействию должна быть использована клиницистами при рецидивах карциномы.
Общеизвестно, что аденокарциномы характеризуются низкой радиочувствительностью, и в самостоятельном варианте лучевая терапия применяется только как паллиативное лечение. Положительный ответ в виде 50% регрессии опухоли мы наблюдали у пациентки А., 24 лет, с полиморфноклеточной низкодифференцированной карциномой слезной железы T4N1 МО, которая отказалась от комбинированного лечения. Больная получила 65 Гр телегамма-терапии. В связи с прогрессированием процесса в виде активного продолженного роста и регионарного метастазирования наблюдался летальный исход через 6 мес. после завершения лечения.
Лучевая терапия карциномы слюнного протока околоушной СЖ была произведена 2 (5,4%) из 37 пациентов с распространенностью процесса T4N1М0 и T3N2M0 с паллиативной целью. Проводилась дистанционная гамма-терапия на первичную опухоль и регионарные метастазы расщепленным курсом в СОД 65-70 Гр с субъективным эффектом (уменьшение болей в опухоли, улучшение самочувствия). Через 10 мес. и 1,8 года больные умерли от прогрессирования опухолевого процесса.
Лучевая терапия в самостоятельном варианте была применена при распространенной карциноме из плеоморфной аденомы T4N0M0 и рецидивном инфильтрате. Лечение носило паллиативный характер, размеры опухоли превышали 12x9 см. Больные умерли через 2,5-4 года после окончания лечения.
Дистанционная телегамма-терапия, предпринятая для лечения с паллиативной целью карциномы без определенной морфологической формы с распространенностью T3N1M0, в СОД 64 Гр, вызвала регрессию более 50% объема опухоли. Однако через 5 мес. рост опухоли возобновился с летальным исходом через 8 мес. Таким образом, лучевое лечение как самостоятельный метод перспективно для АК, АКК твердого и мягкого нёба, корня языка, трахеи, особенно низкодифференцированного варианта, недифференцированной карциномы.
Лучевое лечение множественных метастазов в легких проводится по методике крупнопольного облучения легких в два этапа по расщепленной программе. Лечение проводится через день разовой дозой 3,3 Гр по 13,2 Гр на каждое легкое. Через неделю проводится второй этап крупнопольного облучения по прежней методике. СОД на каждое легкое составляет 26,4 Гр. В результате лучевого лечения регрессия легочных метастазов составляла 50-75%, в отдельных случаях регрессия метастазов была полной. Положительные результаты лечения отдаленных метастазов в легких увеличивают продолжительность жизни больного.
В ответ на лучевое воздействие в тканях развиваются лучевые реакции различной степени выраженности. Обычно к концу лечения на коже развивается сухой десквамативный, а иногда и влажный эпидермит. Признаки реактивного радиоэпителиита на слизистой оболочке проявляются гиперемией и отечностью тканей с последующим развитием островкового, затем и пленчатого эпителиита соответственно размерам полей наружного облучения. Степень выраженности лучевых реакций зависит от способа и методики лучевого воздействия.
На протяжении последующих лет после окончания лучевого лечения наблюдаются тканевые реакции, переходящие в стойкие трофические изменения. Кожа полей облучения остается пигментированной, появляется дисхромия кожи (участки пигментации перемежаются с участками кожи, лишенными пигмента). Расширенные капилляры образуют телеангиоэктазии. Кожа полей облучения с течением времени истончается, становится ломкой и сухой, снижается до полного прекращения секреции сальных и потовых желез. Развивается атрофия подкожной жировой клетчатки и подлежащих мышц.
Атрофические и рубцовые процессы ведут к западению и деформации области облучения. Однако все эти изменения сугубо индивидуальны и колеблются от незначительных реакций до выраженных. В полости рта снижается саливация, наступает резкая сухость слизистой оболочки полости рта и глотки, потеря вкусовых ощущений. Слизистая оболочка становится бледной и атрофичной, в тканях на месте опухоли образуются рубцы. Вкусовые ощущения и скудная саливация возвращаются в течение нескольких месяцев или лет. Среди серьезных лучевых осложнений развиваются остеонекрозы челюстей, трофические язвы. Эти процессы бывает достаточно трудно дифференцировать от бластоматозных изменений тканей.
Читайте также:

