Таргетная терапия рака почки как получить бесплатно
Понятие
Таргетная терапия относится к современному методу борьбы с онкологическими заболеваниями. За последние годы борьба с раком значительно изменилась. Если в самом начале при обнаружении опухоли использовалась лишь простые поддерживающие методы лечения, то сейчас применяется комплексный подход, состоящий из разных методов, дополняющих друг друга. Таргетная методика, или молекулярно-прицельная терапия, была разработана с целью результативной борьбы с атипичными клетками.

Ее главной особенностью является направленное воздействие на опухоль без затрагивания соседних здоровых тканей, что позволяет хорошо переносить саму процедуру, снизить риск побочных явлений и предотвратить развитие сопутствующих патологий.
При каких заболеваниях актуальна
Применение таргетной терапии показано для лечения в первую очередь онкологии внутренних органов, поэтому она успешно применяется для борьбы с раковыми заболеваниями:
- почек;
- легких;
- молочных желез;
- желудка;
- поджелудочной железы;
- толстого и прямого кишечника.
Также положительные результаты отмечены при применении данной терапии для лечения онкологических заболеваний кожи. Результаты лабораторных анализов и инструментальные исследования при диагностике рака позволяют принять решение о наиболее действенном методе лечения.
Показания к назначению
Таргетная терапия зачастую применяется при последней стадии рака, когда другие методы и препараты оказались неэффективны, поэтому показания к применению этой терапии следующие:
- тяжелое состояние здоровья пациента, при котором проведение хирургического вмешательства и химиотерапии невозможно из-за угрозы ухудшения самочувствия;
- повышенный риск развития и распространения метастазов;
- снижение отрицательного влияния опасных медицинских препаратов, которые оказывают пагубное воздействие на здоровые ткани организма;
- быстрый темп роста опухоли и распространение ее в соседние ткани и органы.
Виды терапии и препаратов
В медицинской практике используется три основных варианта таргетного воздействия:
- Повреждение внутриклеточных структур, которые обеспечивают нормальную жизнедеятельность опухоли (например, кровеносных сосудов).
- Точечное воздействие на клеточные мишени (ферменты, гены, рецепторы половых гормонов).
- Выключение биохимических сигналов, которые позволяют жить и размножаться пораженным клеткам.
Таргетное лечение основано на применении специальных препаратов, которые уничтожают раковые образования. Существуют разные виды таких средств, предназначенных для выполнения определенных функций:
- Препараты на основе гормонов останавливают выработку секрета и тем самым замедляют рост опухоли.
- Индукторы апоптоза способствуют удалению раковых клеток из организма.
- Модуляторы экспрессии генов изменяют поведение белков, а при меланоме воздействуют непосредственно на мутированные гены.
- Ингибиторы ангиогенеза останавливают развитие сосудов внутри новообразования, что прекращает кровоснабжение опухоли.
- Моноклональные антитела направляют токсичные вещества в раковые клетки и уничтожают их.
Преимущества
Любой метод лечения имеет как положительные, так и отрицательные стороны, и таргетная терапия не исключение. При ее применении отмечаются следующие положительные моменты:
- отсутствие влияния на здоровые клетки, а это означает снижение негативных побочных эффектов;
- дополнительное усиление действия химиотерапевтических препаратов;
- результативный метод лечения при наличии метастазов, позволяет продлить жизнь пациентов на месяцы и даже на годы;
- удобная форма препаратов в виде таблеток позволяет проводить лечение в домашних условиях или корректировать дозу;
- высокая чувствительность к данным препаратам со стороны раковых клеток позволяет продолжить лечение и добиться положительного результата, если перестают помогать средства, относящиеся к классической химиотерапии.
Недостатки
К недостаткам таргетной терапии можно отнести следующие аспекты:
- высокая цена лекарственных средств (получить лечение бесплатно можно только с помощью предусмотренной в России квоты);
- положительный эффект дает только правильно подобранный препарат (определить его можно, основываясь на результатах генетического и молекулярного анализов);
- наличие определенных видов побочных эффектов (нарушение работы ЦНС, повышение артериального давления, появление сыпи на кожных покровах, развитие сердечной недостаточности, неправильная работа эндокринной системы, заболевания почек, гепатит, развитие пневмонии, нарушение свертываемости крови).
Препараты
Препараты таргетной терапии участвуют не только в лечении от раковых заболеваний, но и в диагностировании опухолей. На сегодняшний день разработано большое количество лекарственных средств, применяемых для узконаправленного действия при проведении таргетной терапии.
В чем сложность. При наличии в организме пациента гена HER2 (ген множественной лекарственной резистентности) раковая опухоль может не реагировать на вводимые лекарственные препараты, поэтому при его обнаружении можно заранее сказать о результативности химиотерапии. Атипичные клетки избегают гибели с помощью включения определенных механизмов защиты:
- быстрое восстановление повреждений;
- выведение препаратов в межклеточное пространство;
- изменение роли генов, которые контролируют гибель клеток, они перестают обладать такой способностью и не могут запустить фатальные изменения;
- обезвреживание цитостатика специальными белками;
- смена мишени для воздействия препарата (предлагается похожий белок, который не несет большого значения для дальнейшего процесса жизнедеятельности).
Таргетная терапия в лечении онкологических заболеваний
Данная терапия назначается курсами, общее количество которых колеблется от трех до шести, таким образом, общее время лечения составляет от 70 до 140 дней. Эта методика может быть использована как самостоятельная процедура или же в комплексе с другими действенными методами лечения. Вводимые при проведении таргетной терапии лекарства приводят к прекращению функционирования раковых клеток, их контролируемому распаду и выводу остатков поврежденных тканей из организма. Однако разработанные препараты имеют узкую направленность, специальное средство воздействует на конкретный орган и не может применяться для лечения другого. Из-за постоянной мутации раковых клеток даже при одинаковой форме опухоли у разных пациентов могут применяться для лечения разные препараты.
Рак молочной железы. Таргетная терапия при онкологии груди назначается начиная со второй стадии. Она может применяться в качестве основного или вспомогательного метода. В процессе терапии происходит нарушение белковых соединений опухоли, прекращение процесса деления зараженных клеток и, как следствие, разрушение новообразования. Вид препарата и схема лечения подбираются индивидуально для каждой пациентки на основании результатов анализов и исследований. При данной терапии рака молочной железы побочных эффектов мало, так как влияние на здоровые ткани снижается до минимума. Процесс восстановления и реабилитации пациента проходит достаточно быстро.

Колоректальный рак. При онкологическом заболевании прямой и толстой кишки применяются три группы таргетных препаратов-ингибиторов:
- рецепторов эпидермального фактора роста;
- киназы – фермента, стимулирующего клеточное размножение и деление;
- фактора роста эндотелия сосудов и белка, вырабатываемого раковыми клетками.
Рак легкого. Из-за отсутствия ярких симптомов заболевания зачастую при обращении к врачу рак легкого у пациентов достигает тяжелой неоперабельной стадии. В таком случае есть вариант лечения с помощью таргетной терапии. Для лечения рака легкого используются следующие медицинские препараты:
- блокирующие ферменты роста;
- останавливающие сосудистое разрастание;
- специфические иммуноглобулины.

В настоящее время таргетная терапия бурно развивается. Многие новые препараты проходят клинические испытания, многие уже применяются для лечения пациентов. Некоторые можно использовать при раке почки.

В каких случаях при раке почек назначают таргетную терапию?
Основное показание к назначению таргетных препаратов при злокачественных опухолях почек — неэффективность химиотерапии. Таргетная терапия часто применяется при запущенных злокачественных опухолях на поздних стадиях. Она не предназначена для того, чтобы вылечить рак, но может уменьшить размеры опухоли, замедлить ее рост — это помогает увеличить продолжительность жизни пациента.
Другая сфера применения таргетных препаратов при раке почки — в качестве адъювантной терапии после хирургического лечения. Препарат под названием сунитиниб помогает предотвратить рецидив.
Таргетные препараты при раке почки назначают, как правило, в режиме монотерапии. Одни из них нужно принимать в таблетках, другие вводят внутривенно. Если препарат не работает, его отменяют и назначают другой.
Таргетная терапия при злокачественных опухолях почек пока изучена недостаточно, нельзя сказать, какое лекарство будет работать лучше всего в данном случае, стоит ли их комбинировать, чтобы усилить эффект, и если стоит, то как это правильно делать. Эти нюансы еще предстоит выяснить в ходе исследований.
Какие препараты применяют?
При раке почки применяют таргетные препараты, которые обладают разными механизмами действия, могут блокировать разные вещества.
- Жидкий стул.
- Тошнота.
- Изменение цвета кожи и волос.
- Снижение уровня лейкоцитов и эритроцитов в крови (как следствие, анемия, снижение иммунитета и повышенный риск инфекции).
- Повышение артериального давления.
- Повышенная утомляемость.
- Снижение уровня гормонов щитовидной железы.
- Повышенная кровоточивость.
- Сердечная недостаточность.
Механизм действия. Так же, как и сунитиниб, блокирует тирозинкиназы и рост новых сосудов. Препарат выпускается в таблетках, принимать при раке почки его нужно два раза в день.
Механизм действия. Эверолимус блокирует белок mTOR, который активирует размножение раковых клеток. Обычно его используют в качестве препарата второй линии при запущенном раке почек, если пациенту не помог сорафениб и сунитиниб. Эверолимус принимают в виде таблеток один раз в день.
- Снижение иммунитета и повышенный риск инфекций.
- Язвы во рту.
- Сыпь на коже.
- Жидкий стул.
- Снижение аппетита.
- Тошнота.
- Отеки на ногах.
- Повышенная утомляемость.
- Повышение уровня холестерина и сахара в крови.
- Редкий серьезный побочный эффект — поражение легких, которое проявляется в виде одышки и других симптомов.
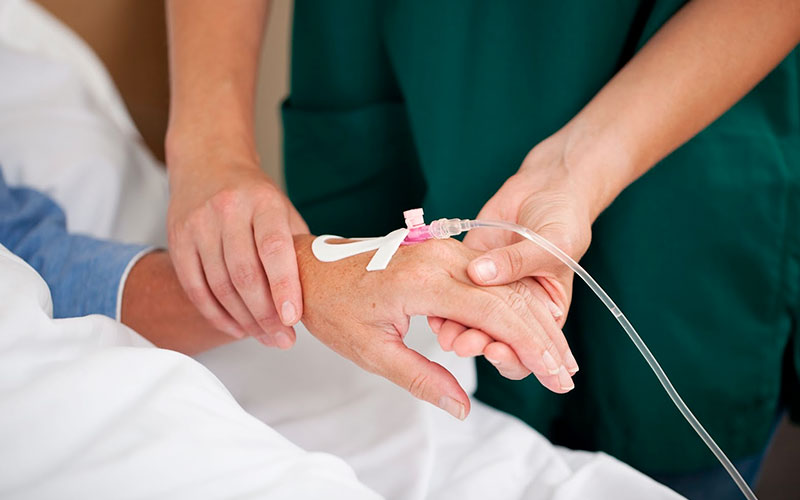
Механизм действия. Так же, как эверолимус, блокирует белок mTOR. Этот препарат часто применяют у пациентов с запущенным прогрессирующим раком почки, у которых плохой прогноз ввиду тех или иных факторов. Темсиролимус назначают в виде внутривенных инъекций, вводят один раз в неделю.
Побочные эффекты во многом напоминают таковые у эверолимуса:
- Язвы во рту.
- Повышенная утомляемость, слабость.
- Сыпь на коже.
- Отеки на лице и на ногах.
- Снижение аппетита.
- Тошнота.
- Повышение уровня холестерина и сахара в крови.
Механизм действия. Препарат блокирует рост новых кровеносных сосудов в опухоли и белки-тирозинкиназы. Принимают в таблетках, один раз в сутки.
- Жидкий стул.
- Тошнота.
- Повышенное артериальное давление.
- Головные боли.
- Нарушение работы печени.
- Уменьшение количества лейкоцитов в крови и снижение иммунитета.
- Повышенная кровоточивость, ухудшение заживления ран.
- Аритмии сердца.
Во время лечения пазопанибом нужно контролировать ЭКГ и функции печени (биохимический анализ крови).
Механизм действия. Препарат блокирует рост новых кровеносных сосудов. Эффективность повышается в сочетании с интерфероном-альфа (иммунопрепарат). Вводят бевацизумаб внутривенно.
- Повышенное артериальное давление.
- Головные боли.
- Слабость, повышенная утомляемость.
- Редко возникают нарушения работы сердца, повышенная кровоточивость, повреждение стенки кишечника.
Механизм действия. Блокирует ферменты-тирозинкиназы и рост новых кровеносных сосудов. Обычно его применяют как препарат второй линии, если до этого не помогли другие лекарства. Принимается в виде таблеток два раза в день.
- Тошнота и рвота.
- Слабость, повышенная утомляемость.
- Повышение артериального давления.
- Ухудшение свертываемости крови.
- Иногда нарушается функция печени.
- Ухудшение функции щитовидной железы (необходим контроль во время лечения).
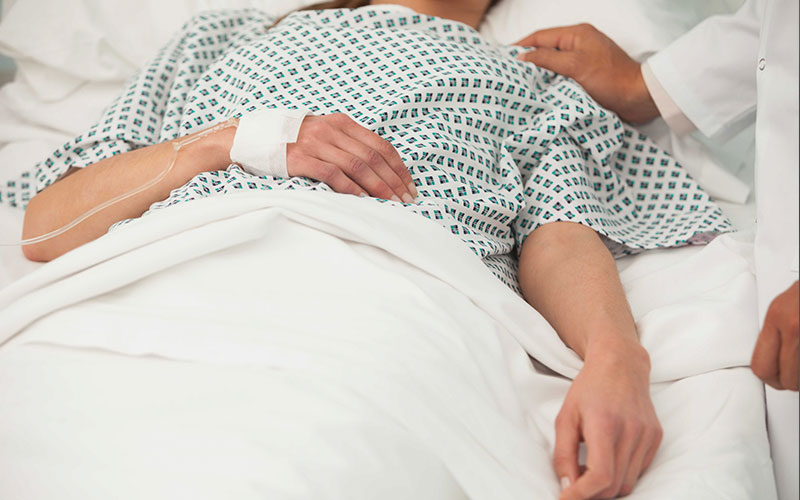
Механизм действия. Блокирует тирозинкиназы, рост сосудов, некоторые белки, которые активируют рост злокачественных опухолей. Обычно применяется в сочетании с эверолимусом в качестве препарата второй линии, если другие лекарства не помогли. Ленватиниб принимают в капсулах один раз в сутки.
- Боль в мышцах и суставах.
- Повышенная утомляемость.
- Жидкий стул (в редких случаях возникает тяжелая диарея).
- Тошнота и рвота.
- Снижение аппетита.
- Повышенное артериальное давление.
- Потеря веса.
- Редко встречаются тяжелые осложнения: нарушение работы сердца, печени, почек, сильное повышение артериального давления, кровотечения, образование тромбов, повреждение стенки кишки.
Кабозантиниб
Механизм действия. Блокирует ферменты-тирозинкиназы, в том числе те, которые нужны для формирования в опухолевой ткани новых сосудов. Препарат второй линии, применяется, когда не помогло другое лечение. Кабозантиниб принимают в таблетках один раз в день.
Преимущества таргетной терапии при раке почки
Главный недостаток классической химиотерапии в том, что химиопрепараты атакуют не только раковые, но и здоровые клетки, если они активно размножаются. В первую очередь страдают: красный костный мозг, кожа и волосяные фолликулы, слизистые оболочки. Таргетные препараты действуют прицельно, поэтому у них меньше побочных эффектов, они менее выражены. Тяжелые осложнения встречаются редко.
При этом таргетные препараты зачастую эффективны там, где классические химиопрепараты не справляются. Благодаря им лечение рака почки и других органов на поздних стадиях стало более эффективным. Пусть таких пациентов до сих пор чаще всего невозможно вылечить, но таргетная терапия помогает продлевать жизнь. Если удалось подарить онкобольному хотя бы еще один день — это уже победа. На практике зачастую речь идет о более существенных сроках.
Стоимость таргетной терапии в Европейской онкологической клинике
Стоимость курса таргетной терапии — от 150 тыс. р.
Для подробного расчета получите консультацию врача.
Врачи Европейской онкологической клиники добились больших успехов в лечении рака на поздних стадиях. Наши пациенты получают наиболее современные химиопрепараты и таргетные препараты, качественное обезболивание и другие виды симптоматического лечения. Свяжитесь с нами, чтобы узнать больше.
Сегодня, 4 февраля, мы отмечаем Всемирный день борьбы против рака. Онкологическое заболевание – одна из самых тяжелых проблем, с которой может столкнуться каждый человек. Но, к счастью, в наше время рак перестал быть фатальным диагнозом.

Применение современных методов лечения и совершенствование системы онкологической помощи дают хорошие результаты.
За последние годы московским пациентам стали доступны такие современные технологии, как ПЭТ/КТ-томография, операции с использованием робота Да Винчи, гамма-нож, 3D и 4D-лучевая терапия.
Город постоянно расширяет скрининговые программы, например, для раннего выявления рака молочной железы.
Начата массовая вакцинация подростков против вируса папилломы человека.
Сегодня мы сделаем еще один важнейший шаг в борьбе с раком.
После консультаций с министром здравоохранения Вероникой Игоревной Скворцовой и профессиональным сообществом врачей-онкологов принял решение.
С 2019 года московские больницы перейдут на использование новых федеральных клинических рекомендаций по профилю онкология по лечению 6 локализаций рака.
Это рак молочной железы, предстательной железы, меланома, рак почки, прямой кишки и рак легкого. На эти заболевания приходится порядка 80% всех онкологических диагнозов в Москве.
Что это значит?
В рамках новых стандартов лечения все нуждающиеся больные смогут бесплатно получить наиболее эффективную таргетную и иммунную терапию.
Таргетная терапия подразумевает использование препаратов, блокирующих развитие опухолевых клеток. В отличие от традиционной химиотерапии, таргетные препараты практически не повреждают здоровые клетки. Поэтому их применение позволяет добиться контроля над опухолью на годы без серьезных побочных явлений.
В международной онкологической практике используется 36 препаратов таргетной направленности, из которых 32 наименования одобрены для применения в Российской Федерации и уже используются в Москве.
При иммунотерапии назначаются препараты, которые активизирует собственный иммунитет для борьбы с опухолью. Иммунотерапия совершила настоящую революцию в онкологии. Ее использование дает шанс на излечение в случае ряда заболеваний, которые ранее считались абсолютно фатальными.

Основным сдерживающим фактором применения таргетных и иммунных препаратов во всем мире является их высокая стоимость.
Мы подсчитали, сколько будет стоить обеспечение этими препаратами нуждающихся москвичей. Необходимая сумма дополнительных средств будет предусмотрена в бюджете. Фактически мы увеличиваем в 2 раза расходы на лекарственную терапию онкологических больных.
Переход на новые стандарты лечения онкологии в Москве начнется уже во II квартале 2019 года.

Надеюсь, что в течение нескольких месяцев мы обеспечим полную доступность новых лекарств, для всех, кто нуждается в таком лечении, и продлим жизнь тысячам москвичей.
- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
Что такое квота?
Благодаря этой статье, жители России могут прийти в поликлинику и получить бесплатное лечение по полису обязательного медицинского страхования (ОМС). Однако, это относится только к недорогим видам медпомощи, таким как прием у терапевта или узкого специалиста государственного медучреждения, лечение больного зуба, диспансеризация и другое.
На дорогостоящее лечение государство выделяет отдельный бюджет и, согласно ему, распределяет квоты (количество оплаченных из госсредств медицинских услуг) между медучреждениями. Всего есть четыре вида медицинских квот:
- квота на операцию;
- квота на лечение (при необходимости принимать дорогостоящие лекарства);
- квота на высокотехнологичную медицинскую помощь (ВМП);
- квота на экстракорпоральное оплодотворение (ЭКО).
Перечень видов ВМП и диагнозов, попадающих под госфинансирование, прописаны в приказе Минздрава и постановлении Правительства России.

Кому положена квота?
Квоту на лечение онкологии может получить любой гражданин России, который нуждается в дорогостоящем лечении, но только в том случае, если эту необходимость подтвердит лечащий врач. Направление на операцию или ВМП может выдать участковый терапевт вашей поликлиники, но после еще нужно будет получить одобрение трех комиссий: в своем медучреждении, Минздраве и клинике, где пройдет операция.
Какие документы нужно собрать, чтобы получить квоту?
После того, как терапевт поставил вам диагноз и дал направление на лечение, для комиссии медицинского учреждения нужно собрать следующие документы:
- заключение терапевта, медицинская карта, результаты обследований и другие документы, подтверждающие диагноз;
- письменное заявление пациента на получение ВМП;
- копию паспорта;
- копию полиса ОМС и пенсионного страхования (СНИЛС)
- если ВМП необходимо ребенку — свидетельство о рождении и копию паспорта одного из родителей.
Важно запросить в учреждении не только диагноз и метод лечения, но и код ВМП. Это необходимо, чтобы в госоргане могли посчитать, сколько будет стоить лечение и принять решение о выделении квоты.

Куда нести документы?
Если врачебная комиссия решает, что у вас есть все показания для получения ВМП, вы получаете направление с подписью главврача и выписку из медкарты. Добавив их к ранее перечисленному перечню документов, вы можете подавать заявку на квоту в региональный орган управления здравоохранением (местный департамент, министерство здравоохранения или комитет). Подать можно через направляющее учреждение или самостоятельно через госуслуги, МФЦ или приемную Минздрава.
После того, как в региональном Минздраве или Депздраве одобрили заявление на получение квоты на ВМП, комиссия решает, в каком учреждении вас будут лечить и направляют туда документы. Узнать, когда и в какую клинику вас планируют госпитализировать можно по номеру квоты в информационной системе Минздрава.
Уже в медцентре соберут еще одну, последнюю врачебную комиссию, которая решит, есть ли у вас противопоказаний для ВМП. Если их нет, об этом сообщают в Минздрав, а далее вам.
Как долго комиссии рассматривают документы?
По закону решение в местном Минздраве должны вынести не позднее, чем через 10 дней с момента подачи документов. Еще столько же времени отводится на выбор клиники. Однако, к сожалению, даже после этого не всегда пациент сразу попадает на операцию: если в медучреждении уже есть очередь на данный вид ВМП, человека ставят в лист ожидания на госпитализацию.
В экстренных случаях, когда срок лечения нельзя откладывать, комиссия делает соответствующую пометку в направлении и заявку рассматривают быстрее.

Что если я уже обследуюсь в центре, где лечат по квотам?
Возможен и другой сценарий процесса получения квоты. Если вы проходили обследования в клинике, где делают операции по квотам, она может стать и направляющим и принимающим учреждением. Таким образом, вы сначала проходите две комиссии (о необходимости лечения и об отсутствии противопоказаний) в одном месте и уже после все эти документе несете в Минздрав.
Что если говорят, что квот нет?
Такое действительно может случиться: количество квот, которое государство распределяет в начале каждого года между клиниками, ограничено. О наличии квот по тому или иному виду лечения можно узнать в региональном отделении Минздрава.
Если сейчас квот нет, все же есть смысл подать заявку, так как в любой момент пациент может отказаться от квоты и ее могут отдать вам. Также, есть смысл проверить, есть ли необходимые вам квоты в других регионах.
Где можно получить лечение по квотам?

Таргетная терапия - одна из новейших разработок в лечении рака. Она препятствует его развитию на молекулярном уровне. Таргетные препараты нарушают кровоснабжение злокачественных клеток и противодействуют их воспроизводству. Они блокируют команды, сигнализирующие патологическим клеткам о росте.
В отличие от стандартной химиотерапии, которая влияет на все клетки организма, таргетная воздействует только на злокачественные. Ее задача – препятствовать специфическим молекулам, вовлеченным в рост опухоли, чтобы сдерживать развитие и распространение болезни. Поэтому данный вид лечения вызывает меньшее количество побочных эффектов.
Почки изобилуют числом кровеносных сосудов, что способствует росту опухолевых клеток. По этой причине при раке почек таргетная терапия эффективна, предлагая ангиогенные препараты. Они воздействуют на сосуды, которые ведут к злокачественному новообразованию.
Лечение рака почки в Израиле является персонализированным и включает наиболее передовые методы лечения с наименьшим количеством возможных побочных эффектов – лапароскопическую и роботизированную хирургию, криодеструкцию и радиочастотную абляцию, таргетную терапию.
Таргетные препараты рекомендуются:
- при неоперабельной первичной опухоли;
- при метастатическом раке почки;
- в рамках клинических испытаний, чтобы предотвратить рецидив заболевания после хирургического вмешательства.
Лечение предполагает применение одного или нескольких лекарственных средств, для каждого пациента подбирается индивидуальный план лечения. С целью определения наиболее эффективного варианта используется система стратификации риска, применяется генетическое тестирование. Состояние здоровья, особенности конкретного случая болезни влияют на выбор. Во время консультации с врачом в Израиле у пациента есть возможность задать интересующие вопросы (примерный список):
- Принесет ли результаты в конкретном случае таргетная терапия, окажет ли помощь?
- Какие препараты доступны?
- Почему мне была предложена таргетная терапия?
- Что является целью лечения?
- Есть ли другой выбор?
- Каковы краткосрочные и долгосрочные побочные эффекты?
- Какие меры можно предпринять, чтобы снизить действие нежелательных побочных явлений или предотвратить их?
- Как долго будет длиться лечение?
Препараты таргетной терапии рака почки первой линии
В основном данные виды лекарств используются, чтобы уменьшить или контролировать течение болезни при распространенном опухолевом процессе. По результатам исследований и отзывам таргетная терапия рака почек останавливает или замедляет развитие болезни на нескольких месяцев, а иногда - лет.
Обычно лекарственные средства принимают, пока они способны контролировать заболевание. Пациент встречается с врачом каждые 4-6 недель, также сдает анализы крови. Раз в три месяца выполняется сканирование, что выяснить, результативно ли лечение.
Рассмотрим схемы таргетной терапии рака почки. Сунитиниб (Сутент) в основном рекомендуют первым при наличии вторичных очагов. Другой распространенный препарат - Пазопаниб (Pazopanib). Эти лекарства блокируют сигналы о росте в злокачественных клетках и называются ингибиторами тирозинкиназы. Также в ряде случаев назначают сорафениб (Nexavar).
Сунитиниб (Sunitinib)
Сунитиниб имеет другие название - сутент. Его используют на 3 или 4 стадии заболевания. Принимается в капсулах, ежедневно на протяжении 4-х недель с последующим перерывом в 2 недели.
Этот препарат относится к группе ингибиторов тирозинкиназы. Он блокирует внутриклеточные белки под названием тирозинкиназы в опухолевых клетках, которые дают сигналы к росту и делению, связывают клетки с ядром и клеточными структурами. Помимо этого, сутент препятствует кровоснабжению, лишая патологические клетки поступления питательных веществ и кислорода.
Возможные нежелательные последствия приема включают усталость, повышенный риск инфекции в связи с низким уровнем лейкоцитов, анемию, изменения вкусовых ощущений, диарею, кожную сыпь и зуд, ладонно-подошвенную кератодермию, артериальную гипертензию. Сунитиниб может ухудшить работу щитовидной железы, по этой причине больной регулярно сдает анализы крови, чтобы проверить это.
Пазопаниб (Pazopanib)
Пазопаниб – ингибитор роста рака, врач может порекомендовать препарат в качестве первичного лечения при распространенном опухолевом процессе и как вторичное после применения интерферона или интерлейкина-2. Выпускается в таблетках, его принимают каждый день. К потенциальным отрицательным последствиям приема относят: диарею, ладонно-подошвенную кератодермию, сыпь и зуд кожи, повышенную утомляемость, тошноту.
Препараты таргетной терапии рака почки второй линии
Если лечение перестает работать и рак начинает снова расти, врач назначает вторую линию терапии. Назначен может быть один из упомянутых выше препаратов. Либо врач предложит бевацизумаб (Авастин) внутривенно с интерфероном. Другие лекарства - Темсиролимус (Torisel) или эверолимус (Afinitor). Они блокируют сигналы о росте, и называются MTOR блокаторами (MTOR – белок, управляющий ростом, делением и метаболизмом клетки).
Авастин в таргетной терапии рака почки и интерферон
Бевацизумаб (Авастин) – моноклональное антитело, препятствует развитию кровеносных сосудов в опухолевом новообразовании. Препарат назначают внутривенно каждые две недели, интерферон - три раза в неделю в виде инъекций.
Чаще всего при приеме интерферона наблюдаются гриппоподобные симптомы на протяжении недели – двух. Прием парацетомола за полчаса до инъекции может помочь – предотвратит их или уменьшит. Среди других нежелательных явлений отмечают кровотечения из носа, запор – диарею, депрессию, тошноту, гипертонию.
Темсиролимус (Torisel)
Темсиролимус дают внутривенно один раз в неделю. Он блокирует сигналы о росте в злокачественных клетках, относится к препаратам MTOR ингибиторам. Рекомендуется при распространенном опухолевом процессе в качестве вторичной таргетной терапии рака почки. К нежелательным явлениям терапии относят: сыпь, зуд и красноту кожи, тошноту, потерю аппетита, диарею, воспаление в полости рта; низкие уровни клеток крови.
Эверолимус (Afinitor)
Эверолимус выпускается в таблетках, его принимают раз в день. Как и темсиролимус, Afinitor – это ингибитор MTOR, блокирующий сигналы о росте для злокачественных клеток. Врачи применяют его в качестве второй линии таргетной терапии рака почки при метастазах, когда нет реакции на сутент и сорафениб.
К возможным нежелательным явлениям терапии относят низкую устойчивость к инфекции, усталость и одышку из-за недостаточного уровня эритроцитов, повышенное содержание холестерина и сахара в крови, воспалительный процесс в полости рта; высыпания, зуд и сухость кожи; тошноту.
Сорафениб (Nexavar)
Принимается ежедневно, перорально. Он работает в двух направлениях таргетной терапии рака почки: блокирует сигналы о росте и процесс агиогенеза в злокачественном новообразовании. Используется при наличии вторичных очагов рака почки, когда неэффективны препараты биологической терапии, у пациента наблюдается непереносимость к сутенту.
Среди потенциальных нежелательных явлений отмечают: диарею, чрезмерную утомляемость, ладонно-подошвенную эритродизестезию, тошноту, истончение волос.
На сегодняшний день нет методов лечения, уменьшающих вероятность рецидива рака почки после хирургии. Но проводится большое количество исследований в мире, в рамках которых изучаются таргетные препараты. Также разрабатываются новые лекарства данного вида лечения.
У каждого препарата - свои побочные действия. Большинство людей, принимая их, испытывают усталость. В зависимости от назначенного лекарства побочные эффекты включают: диарею, кожные высыпания, боль в руках и ногах. Врач подробно обсуждает с пациентом этот вопрос и консультирует, как лучше справляться с ними.
Читайте также:





