Современные методы лечения опухолей головного мозга
Несмотря на значительное развитие современной медицины, лечение такого заболевания, как опухоль головного мозга, далеко не всегда приносит свои плоды, являясь при этом довольно дорогостоящим мероприятием. К самым распространенным методам лечения относятся хирургическое вмешательство, лучевая терапия и химиотерапия. Однако все чаще в мире говорят об использовании новейших технологий, которые позволяют значительно повысить эффективность методов лечения опухолей мозга, сделав их более точными и успешными. Одним из таких достижений является так называемая стереотаксическая радиотерапия. В рамках данного метода используются трехмерные изображения, полученные с помощью магнитно-резонансной томографии, которые позволяют гораздо точнее составить карту области расположения и распространения новообразования.
К другим современным новшествам, применяемым для лечения опухолей головного мозга, можно отнести использование лазера и ультразвука при операционном вмешательстве. Это позволяет произвести значительно более точное удаление опухоли, уменьшая риск того, что какие-то раковые клетки будут пропущены и оставлены (это может привести к рецидиву опухоли). Кроме того, использование лазерной и ультразвуковой техники для проведения хирургических операций значительно уменьшает риск повреждения здоровых тканей человеческого мозга.
Некоторые из наиболее отличительных новых методов лечения опухолей головного мозга основаны на применении радиации. Лечение, в рамках которого точно нацеленный радиационный луч направляется непосредственно в опухоль в мозгу, называется стереотаксической радиохирургией. Отличие от обычного хирургического вмешательства заключается в отсутствии необходимости использования скальпеля. Метод стереотаксической радиохирургии позволяет доставить радиационный луч прямо в точку назначения, то есть, в нужную область новообразования в головном мозгу.
Кроме вышеперечисленных способов лечения, активно изучаются новые методы доставки медицинских препаратов, направленных на борьбу с раковыми клетками, непосредственно в область опухоли в мозгу. При некоторых видах новообразований достаточно успешно проявил себя новый метод терапии, в рамках которого непосредственно в область опухоли в мозгу хирургическим путем вживляется специальная пластинка, содержащая определенный химиопрепарат. По сути, речь идет о частном случае химиотерапии, при котором постепенно разлагающаяся в опухоли пластинка высвобождает борющиеся с распространением рака медицинские препараты.
Дополнительно можно упомянуть и о новом экспериментальном методе лечения, который подразумевает использование генной терапии. В рамках данного метода пациенту назначается прием медицинских препаратов, которые отрезают опухоль от кровоснабжения; другие медикаменты могут приостановить рост аномальных клеток, а также распознавать и уничтожать раковые клетки. Большинство из этих методов не скоро станут применяться повсеместно, так как сейчас лишь проходят стадию лабораторных испытаний и тестирований. Однако нельзя не подчеркнуть важнейшую роль, которую играют в данных исследованиях сами пациенты, участвуя в испытаниях многих клинических методов и препаратов, и даруя тем самым шанс на выздоровление всем людям, страдающим от различных видов опухолей головного мозга.
(495) 506 61 01
Лечение опухоли мозга должно быть индивидуальным. Методы лечения зависят от таких факторов, как возраст, общее состояние здоровья и наличие сопутствующих заболеваний, а также от размера, локализации и типа опухоли.
Обзор методов лечения опухолей мозга
Лечение опухоли мозга обычно сложное. Прежде всего, оно требует участия нескольких специалистов.
- Специалисты, которые требуются для консультации - нейрохирург, онколог, радиолог, а также невролог. Кроме того, в лечении принимают участие физиотерапевт и реабилитолог.
- Протоколы лечения опухолей мозга зависят от размера опухоли, ее локализации, возраста пациента, а также общего состояния пациента.
- Среди методов лечения опухолей мозга обычно применяются оперативное вмешательство, лучевая терапия и химиотерапия. В большинстве случаев применяются сочетания этих методов.
Хирургическое лечение опухолей мозга
В большинстве случаев опухолей мозга проводится хирургическое лечение.
Целью хирургического лечения является идентификация опухоли и ее оперативное удаление. Если опухоль находится в таком месте мозга, что удалить ее невозможно, хирург проводит биопсию, чтобы определить тип опухоли.

В некоторых случаях, в большинстве своем - при доброкачественных опухолях, хирургическое удаление опухоли может полностью устранить симптоматику болезни. По возможности, нейрохирург старается удалить всю опухоль.
Отличием от оперативных вмешательств при обычных полостных операциях по поводу злокачественных опухолей является то, что в тех случаях хирург может иссечь не только опухоль, но и захватывая здоровые ткани по краям, максимально снижая риск рецидива опухоли. В случае с головным мозгом такое невозможно, так как каждый миллиметр мозга отвечает за определенные функции организма.
Сегодня хирургические методы лечения опухолей мозга все чаще заменяются безоперационными радиохирургическими методами - т.н. стереотаксическая хирургия. К ним относятся гамма-нож и кибер-нож, а также протонная хирургия. Эти методы имеют свои огромные преимущества перед скальпелем хирурга, но они не всегда применимы. Среди преимуществ радиохирургии перед традиционными хирургическими вмешательствами при опухолях головного мозга является то, что она характеризуется меньшим периодом восстановления и обладает меньшим риском осложнений.
Перед операцией обычно пациенту проводятся некоторое консервативное:
- Назначаются стероидные противовоспалительные средства, такие как дексаметазон, чтобы уменьшить отек тканей в области опухоли.
- Назначаются противосудорожные препараты для профилактики эпилептического припадка или снижения его риска.
- При наличии внутричерепной гипертензии проводится шунтирующая операция, целью которой является отведение излишней скапливающейся цереброспинальной жидкости через тонкий пластиковый катетер (трубочку). Обычно из всех таких операций чаще всего прибегают к вентрикуло-перитонеальному шунтированию - созданию соединения бокового желудочка мозга с брюшной полостью. Это наиболее распространенный вид шунтирующих операций.
Лучевая терапия при опухолях мозга
Лучевая терапия давно применяется в лечении опухолевых заболеваний, в том числе и опухолей головного мозга. Касательно опухолей мозга лучевая терапия применяется обычно тогда, когда хирургическое лечение невозможно по тем или иным причинам, например, при наличии сопутствующих заболеваний у пациента. В некоторых случаях лучевая терапия может применяться после хирургического вмешательства, чтобы уменьшить риск рецидива опухоли и уничтожить возможно оставшиеся опухолевые клетки в мозгу. Лучевая терапия проводится местно, то есть облучается определенный отдел мозга, а не весь мозг. Доза облучения подбирается врачом индивидуально, в зависимости от размера опухоли, ее состава и глубины залегания. В зависимости от типов опухолей формируются различные схемы лучевой терапии. Лучевая терапия при опухолях мозга проводится двумя путями:
- Наружная лучевая терапия, когда применяется пучок радиации высокой интенсивности. Такое лечение обычно проводится в течение пяти дней в неделю. Курс длится несколько недель, а сам сеанс облучения занимает обычно несколько минут.
- Брахитерапия. Этот метод заключается в том, что в толщу опухоли вводится радиоактивное зерно, и таким образом происходит разрушение опухоли радиацией изнутри. Доза такой радиации рассчитывается так, чтоб она воздействовала только на ткань опухоли. В данном случае пациенту бывает необходимо пребывание в стационаре в течение нескольких дней.
Химиотерапия при опухолях мозга
Химиотерапия относится к системным методам лечения, так как химиопрепараты оказывают влияние на весь организм, то есть, как на опухолевые клетки, так и на здоровые. В настоящее время существуют разные группы этих препаратов. Для проведения химиотерапии применяют препараты алкилирующей группы, антиметаболиты, препараты природного происхождения, антибластические антибиотики, синтетические и полусинтетические препараты. Химиотерапия чаще всего заключается в применении либо одного препарата, либо, что чаще, нескольких, по определенной схеме. Химиопрепараты могут вводиться как перорально, так и внутривенно. В некоторых случаях они могут вводиться через ликворный шунт.
Эффективность химиотерапии повышается при ее сочетании с лучевой терапией, при этом курс должен состоять из нескольких препаратов. Химиотерапия обычно назначается в виде циклов, между которыми химиотерапия не проводится. Каждый такой цикл химиотерапии опухоли мозга длится несколько недель. В большинстве своем проводится 2-4 цикла химиотерапии. Далее проводится перерыв в лечении, чтобы определить эффективность лечения. Химиотерапия характеризуется значимыми побочными эффектами. Они связаны с токсическим влиянием химиопрепаратов на эпителий ЖКТ и на клетки костного мозга, который играет ключевую роль в кроветворении и иммунитете.
Стереотаксическая радиохирургия

Среди преимуществ радиохирургии можно отметить то, что она позволяет врачу обойтись без скальпеля, то есть отсутствуют какие-либо хирургические осложнения, а также, что самое важное, такой метод позволяет подобраться к труднодоступным опухолям мозга, которые ранее считались неоперабельными.
В некоторых случаях стереотаксическая радиохирургия может быть единственным возможным методом лечения.
Эндоскопические вмешательства при опухолях головного мозга
Сегодня в лечении опухолей мозга, а также других патологических образований, таких как кисты, гематомы после черепно-мозговых травм и т.д. применяются эндоскопические хирургические вмешательства. Традиционное хирургическое вмешательство, которое включает в себя вскрытие черепной коробки - трепанацию черепа - приводит к дополнительному травмированию пациента. Эндоскопическое вмешательство представляет собой вмешательство без широких разрезов, с использованием особой эндоскопической техники. Такое вмешательство позволяет избежать травмирования мелких кровеносных сосудов и нервов, которые могут быть повреждены при традиционном нейрохирургическом вмешательстве. Кроме того, эндоскопически можно эвакуировать жидкость из желудочков головного мозга у детей с гидроцефалией (вентрикулоскопия). Среди эндоскопических операций при опухолях мозга можно отметить, к примеру, трансназальное удаление аденомы гипофиза, когда эндоскоп вводится через носовой ход.
(495) 506-61-01 - где лучше оперировать головной мозг
Кибер-нож - современная инновационная технология применения лучевой терапии, позволяющая воздействовать на опухоль мозга и служит альтернативной оперативным методам лечения. Кибер-нож относится к методам так называемой радиохирургии, как и гамма-нож. Подробнее

На базе нейрохирургической клиники Аахенского Университета с 1998 года применяется специальная методика гамма-кобальтового облучения для лечения опухолей и сосудистых новообразований головного мозга. Подробнее
Национальный Онкоцентр Им. Сураски является интегральной частью крупнейшей муниципальной мед. клиники Сураски и предоставляет передовое лечение опухолей мозга всех видов.Подробнее
Неудачи операций в первую очередь связаны с отсутствием границ опухоли головного мозга, а лучевой и химиотерапии —с переменными генетическими аберрациями в клетках опухоли, их неоднородностью, невозможностью адекватной поставки лекарств из-за гематоэнцефалического барьера (ГЭБ) и устойчивостью тканей к диффузии, усиливающейся липофильной основой структуры мозга.
а) Нацеливание и доставка. Концепция нацеливания включает широкий спектр лечебных принципов, основанных на специфических свойствах клеток опухолей головного мозга, отличающих их от окружающих тканей, а также на том, что лекарства могут быть введены непосредственно в опухоль, пострезекционную полость и головной мозг.
Такая терапия включает в себя методы генной терапии и генной инженерии; терапии на основе иммунологических свойств и иммунной системы в целом, лекарственные препараты, распознающие специфические и уникальные рецепторы мембраны опухоли, в том числе использование естественных, а также искусственных лигандов и лигандов, связанных с препаратами; пути внутриклеточного вмешательства, влияние на ангиогенез опухоли, а также воздействие на свойства опухолевых клеток к миграции, которые необходимы для их выживания и распрос гранения.
Разработки в области доставки включают в себя методы, предназначенные для преодоления проблем классических перорального, внутривенного или внутриартериального путей введения лекарственных препаратов. Методы, которые развивались и были разработаны в клинике, основываются на местной доставке путем прямой интрапаренхимальной инъекции вируса во время операции, вектор-продуцирующих клеток или медленного высвобождающихся полимеров с химиотерапевтическими веществами.
Кроме того, были использованы полимерные пластины с устойчивым медленным высвобождением BCNU для внутриполостного размещения. Внутриполостная доставка через катетер, соединенный с подапоневротическим резервуаром, является еще одним вариантом радиоиммунотерапии. Ниже представлены новые методы лечения на основе специфического нацеливания, передовых методов доставки и сочетания обеих технологий.
Также применяются ретровирусы и аденовирусы. Во многих странах мира были выполнены многоцентровые исследования (фазы II и III) ретровирусной системы, однако результаты пока неудовлетворительные. Неэффективная доставка генов приводит к недостаточной скорости трансдукции. Аденовирусное направление трансфекции оказалось более эффективным, но и более рискованным.
Другой метод генной терапии направлен на восстановление одного или нескольких генов, которые удаляются в процессе онкогенеза. Наиболее сложный из них ген ТР53, участвующий в нескольких аспектах управления клеточного цикла, удаляется в значительной группе мультиформных глиобластом. С использованием аденовирусного вектора переноса генов ТР53 была достигнута успешная гибель опухолевых клеток в лабораторных условиях, а также клинических, например, при колоректальном раке. Начаты клинические исследования в отношении глиобластом, и вскоре можно будет оценить результаты.
Третья сфера, в которой генные технологии играют важную роль, охватывает повышение иммунного ответа на опухолевые клетки. Это может быть достигнуто, например, путем устранения иммуносупрессоров. Методы основываются на блокировании генов, отвечающих за формирование инсулиноподобного фактора роста I (IGF I), трансформирующего фактора роста бета (TGFbeta) и другие.
Аналогочно иммунологическим факторам, путем вмешательства в соответствующие гены могут осуществляться и манипуляции с генами, влияющими на ангиогенез опухоли. Глиомы высокой степени злокачественности имеют высокую активность ангиогенеза, необходимую для роста и выживания. Данная методика находится на стадии клинического применения (фаза I).
Вирусы также могут быть использованы для прямого влияния на клетки, вызывая их гибель. При рекомбинантных методах они могут быть безопасны и эффективны. В частности, нейротрофические вирусы, как например, вирус простого герпеса и его аналоги представляются перспективными при мутации в формы, имеющие прямое цитопатическое воздействие на опухолевые клетки, а не на нормальные ткани мозга. Были начаты или уже привели к интересным результатам различные клинические испытания. Кроме того, представляется перспективным применение аденовируса, а также другого типа вируса — реовируса.
Различные другие методы существуют и работают в лабораторных условиях, а некоторые уже достигли клинической стадии. Среди них трансдукции ИЛ-2 и ИЛ-7 в опухолевых клетках с целью повышения Т-клеточной реакции; активация естественных дендритных клеток (пассивная и активная иммунизация с риском аутоиммунных реакций в неопухолевой ЦНС) и различные формы иммунизации аутологичных опухолевых клеток. Последний метод был опробован в клиническом многоцентровом исследовании, при этом опухолевые клетки использовать для повторной вакцинации.
3. Нацеливание с помощью мембранных рецепторов:
• Как многие другие опухоли, полноценные опухоли головного мозга, такие как мультиформная глиобластома, имеют специфические рецепторы на клеточной мембране. Среди наиболее распространенных рецепторов на поверхности глиом являются EGF-R, PDGF-R, FGF-R, VEGF-R, трансферрин, рецепторы цитокинов, таких KaKTGF-бета, ИЛ-13 или ИЛ-4. При взаимодействии специфических антител с этими рецепторами образуются так называемые иммунотоксины. Некоторые из препаратов и токсинов, способные вызывать такие реакции, были подвергнуты клиническим испытаниям. Наиболее важные из них:
• Трансферрин с дифтерийным токсином (Trans-MID).
• TGF (лиганд для EGF-R) с псевдомонадным экзотоксином (ТР-38).
• ИЛ-4 лиганд с псевдомонадным экзотоксином (NBI-3001).
• ИЛ-13 с псевдомонадным экзотоксином (PRE-CISE)).
Стоит отметить, что опухолевые клетки обладают гиперэкспрессией всех этих рецепторов, а также их лигандов, что приводит к аутокринной петле, стимулирующей и поддерживающей клеточную пролиферацию. К особой группе лигандов и рецепторов следует отнести TNF-связанные апоптоз-индуцирующие лиганды (TRAIL) и TRAIL рецепторы. Многие опухоли, в том числе глиобластомы, обладают экспрессией TRAIL и TRAIL рецепторов. Таким образом, эта составляющая тоже может стать конкретной ориентацией для лекарственного апоптоза.
4. Внутриклеточные пути нацеливания, связанные с мембранными рецепторами. Большинство упомянутых лигандов и рецепторов связаны с их внутриклеточным доменом тирозинкиназы (Т3). Ее активация приводит к каскаду внутриклеточных процессов, многие из которых ведут к дальнейшему распространению клеток и/ или миграции. Прямое вмешательство в эти процессы может прервать подобные явления и в дальнейшем привести к апоптозу клеток. Было разработано множество молекул, АТФ-миметиков подобного действия, которые в настоящее время испытываются при многих видах рака, включая мультиформные глиобластомы. Например, эрлотиниб, гефитиниб (пресса), иматиниб (гливек).
5. Терапия, направленная на ангиогенез и миграцию клеток. Злокачественные опухоли, особенно глиобластомы, вызывают неоангиогенез. Неоваскуляризация необходима для дальнейшего роста, а торможение ангиогенеза может ее предотвратить. Клетками-мишенями при антиангиогенной терапии могут быть опухолевые клетки, вырабатыающие ангиогенные факторы, такие как VEGF и VEGF-R, а также сами эндотелиальные клетки, являющиеся более доступными, так как находятся вне ГЭБ.
С ангиогенной активностью опухолевых клеток тесно связан и их миграционный потенциал. Для пролиферации клетки должны вовлекаться в окружающий матрикс и синтезировать матричные металлопротеиназы (ММП). Ингибирование ММП предотвращает миграцию раковых клеток и косвенно их пролиферацию, в результате чего рост опухоли останавливается. Тесная взаимосвязь между биохимическими ан-гиогенными факторами и ММП приводит к двойному действию антиангиогенных препаратов. Так как эти лекарственные препараты не убивают опухолевые клетки, а только предотвращают их дальнейший рост, их часто называют цитостатиками.
Примеры антиангиогенных препаратов, которые были уже испытаны в клинических исследованиях: талидомид, ангиостатин, эндостатин, ZK222584/PTK787 и ингибиторы ЦОГ-2, такие как целекоксиб и циленгитид. Наиболее перспективными представляются результаты исследований, в которых эти препараты используются в сочетании с лучевой терапией и/или цитотоксической химиотерапией.
б) Доставка. За последние годы были разработаны различные методы для преодоления основных препятствий адекватной доставки лечебных препаратов к клеткам головного мозга.
1. Местные инъекции. При разработке направления лечения с помощью ретровирусов возникла необходимость использования продуцирующих клеток. Эти клетки могут быть размещены только в пределах и вокруг остаточной опухоли или полости путем прямой инъекции в паренхиму. В ряде исследований было показано, что такой способ доставки не причиняет никакого вреда пациентам и в большинстве случаев вызывает только минимальные изменения видимые при МРТ. Однако эффективность доставки даже после 50 инъекций была низкой.
Инъекции клеток или препаратов с помощью резервуара Оммайя и постоянного катетера приводит к созданию пула материала вокруг кончика катетера. Лекарственные препараты могут растворяться в тканях путем диффузии, для этого необходимо, чтобы они были липофильными и имели низкий молекулярный вес.
2. Системы медленного высвобождения. Более перспективной представляется концепция систем медленного высвобождения, хотя и при этом диффузия является движущей силой доставки препаратов с вышеупомянутыми ограничениями, особенно, при отеке мозга и высоком интерстициальном давлении. Накопленный опыт в большинстве своем связан с применением биодеградирующих пластин, содержащих BCNU. Однако он оказал незначительный эффект на показатели выживаемости.
Другими системами медленного высвобождения, проверенными в лаборатории и избирательно на пациентах, являются системы на основе липосом, сфер альгината и полимерных наночастиц.
3. Конвекционный метод доставки. В отличие от диффузии, когда градиент концентрации является движущей силой молекулы/лекарства, конвекция основывается на градиенте давления. Это позволяет поставить даже крупные молекулы на более дальние расстояния. Данная технология особенно эффективна, когда дело касается иммунотоксинов, действительно больших молекул. Этот метод хорошо воспроизводиться у небольших животных, тогда как у людей изменение в устойчивости мозговой ткани и ткани опухоли, вероятно, препятствует прогнозируемому распределению растворителей и препаратов.
После большого опыта, накопленного за последние несколько лет, возможности конвекционных методов доставки доказаны в нескольких исследованиях (например, ТП 38, PRECISE). С помощью максимум четырех катетеров, помещенных в мозг, можно покрыть довольно большую часть одного полушария. Все исследования с препаратами с большой молекулярной массой в настоящее время проходят с помощью этого метода.
в) Перспективные разработки:
- В ближайшее время еще один способ нацеливания может достичь клинической стадии: нервные стволовые клетки и клетки-предшественники, похоже, имеют тропность к клеткам опухоли головного мозга. В лабораторных условиях после трансфекции этих клеток с определенными генами было показано, что они имеют возможность преследовать и убивать клетки опухоли головного мозга, даже находящиеся далеко от места инъекции.
- Хирургические усовершенствования могут привести к реальному и значительному сокращению опухолевой нагрузки: интраоперационная визуализация посредством интраоперационной МРТ или визуализации остаточных опухолевых клеток с помощью окрашивания (ALA) сможет решить эту задачу.
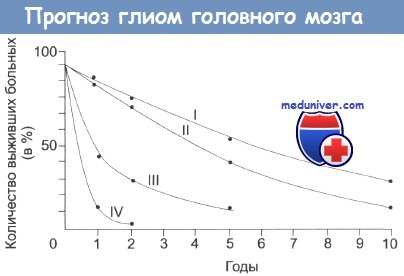
Продолжительность жизни больных со злокачественной глиомой различной степени.
Отметьте, что даже в случаях низкозлокачественной опухоли выживает немного больных.
Тактика лечения рака головного мозга во многом предопределяется стадией этого тяжелого заболевания, типом опухоли, которые зависят от клеточного состава новообразования, и общего состояния здоровья пациента. Именно поэтому, при подозрении на развитие этого тяжелого недуга, для определения тактики избавления от опухоли больному следует пройти все необходимые этапы диагностики, которые включают как лабораторные, так и инструментальные методы исследования.
В нашей статье вы сможете найти ответы на многие вопросы о причинах развития, разновидностях, стадиях, симптомах, прогнозах, методах диагностики и современных способах лечения рака головного мозга. Эта информация поможет вам вовремя заподозрить возможное развитие злокачественной опухоли, и вы сможете задать своему лечащему врачу вопросы о современных способах лечения злокачественной опухоли головного мозга.
Причины

Точные причины развития рака головного мозга до сих пор не определены. Ученые и врачи выдвигают множество версий о причинах развития этого онкологического заболевания.
В рамках нашей статьи выделим некоторые из них:
- травмы головного мозга в прошлом;
- воздействие радиации;
- никотиновая, наркотическая и алкогольная зависимости;
- заболевания иммунной системы;
- операции по трансплантации органов или тканей в прошлом;
- работа на химических предприятиях;
- наследственная предрасположенность.
Выраженность симптомов раковой опухоли во многом определяется местом ее локализации и клеточной структурой.
Классификация опухолей
Различные онкоцентры и клиники могут классифицировать опухоли головного мозга по различным параметрам. В этой статье мы рассмотрим лишь некоторые из них.
Злокачественные новообразования мозга могут быть:
- первичными: опухоли, которые сразу начинают развиваться из тканей головного мозга;
- вторичными: опухоли, которые появляются из-за метастазирования первичной опухоли или из других органов организма.
Среди злокачественных новообразований онкологи выделяют множество их разновидностей по тканевому и клеточному составу. Основными из них являются такие раковые патологии головного мозга:
- нейроэпителиальная опухоль: астроцитома (пилоцитарная, фибриллярная, анапластическая, глиобластомная), эпендиома;
- новообразование мозговых оболочек: менингиома;
- олигодендроглиома: опухоль, развивающаяся из таких клеток мозга, как олигодендроциты;
- смешанная глиома: опухоль содержит как олигодендроциты, так и астроциты;
- эпендиома: опухоли, развивающиеся из эпителиальных тканей мембраны, которые выстилают полость желудочков мозга;
- гемангиома: опухоли, развивающиеся из тканей сосудов мозга;
- нейрональная опухоль: новообразование развивается из ганглиозных клеток.
К самым редким и опасным опухолям головного мозга относят эмбриональные типы новообразований, которые развиваются у плода во время его внутриутробного развития. К ним относят такие новообразования:
- нейроэктодермальные: опухоли, которые развиваются из эмбриональных тканей;
- медуллобластома: новообразование, начинающее свой рост из тканей мозжечка.
Стадии рака головного мозга
При типичном течении рака головного мозга могут выделяться такие стадии этого заболевания:
- I – опухоль растет медленно и сопровождается слабовыраженными симптомами;
- II – рост новообразования еще остается небыстрым, но оно уже распространяется на близлежащие ткани;
- III – рост опухоли ускоряется, и у опухоли могут быть метастазы;
- IV – новообразование захватывает обширные участки мозга и дает метастазы в разные органы.
При использовании классификации TNM онкологи могут выделять такие три стадии рака мозга:
- Т – опухоль, характеризуется определенным размером;
- N – опухолевый процесс начинает распространяться на лимфоузлы;
- М – опухолевый процесс дает метастазы.
В клиниках России онкологи чаще ориентируются на методику классификации раковых опухолей мозга, которые описывают четыре стадии заболевания.
Симптомы
Степень выраженности симптомов при раке головного мозга во многом зависит от места локализации опухоли, стадии заболевания, общего состояния здоровья и возраста пациента. Учитывая тот факт, что клиническая картина злокачественных опухолей мозга может быть различной, в рамках этой статьи мы сможем рассмотреть основные признаки этого тяжелого заболевания. Их разделяют на:
- общемозговые;
- очаговые.
Эти признаки рака головного мозга вызываются смещением и сдавлением тканей мозга, повышением внутричерепного давления. Они во многом зависят от размера новообразования, но среди них можно выделить наиболее часто наблюдающиеся и характерные для этой патологии симптомы.
Этот симптом при злокачественных новообразованиях мозга всегда носит большую интенсивность и отличается от типичных головных болей постоянностью или регулярностью. Многие больные могут не придавать этому симптому должного внимания и, как принято среди многих из нас, принимают анальгетики для его устранения, но не обращаются к врачу. После обращения к доктору они жалуются на тот факт, что даже самые сильнодействующие обезболивающие средства не приносят облегчения, или интенсивность боли снижается только после приема препаратов, которые способны снижать внутричерепное давление.
Этот симптом рака мозга может вызываться как сдавливанием структур мозга (мозжечка), так и нарушениями нормального кровоснабжения мозга. При смещении мозжечка пациент может предъявлять жалобы на ощущение поворачивания или сдвигания тела в ту или иную сторону (при этом тело больного находится на месте). Кроме этого, у больного при осмотре может наблюдаться нистагм (подергивание глазных яблок).
Этот симптом ракового новообразования головного мозга связан с повышением уровня внутричерепного давления, которое происходит с различной периодичностью. После акта рвоты пациенты отмечают облегчение общего состояния.
Кроме этого симптома у больного часто (практически постоянно) наблюдается тошнота. А после интенсивных приступов рвоты он не может принимать пищу и проглатывать жидкость.
Опухоль сдавливает сосуды, и у больного наблюдается нарушение мозгового кровообращения. Некоторые участки мозга могут испытывать гипоксию, и этот симптом сказывается на общем самочувствии.
Выраженность и характер очаговых симптомов злокачественных новообразований головного мозга зависят от места локализации опухолевого процесса и показателей общего состояния здоровья. Например, при поражении речевого центра у больного наблюдаются признаки нарушения речи, а при поражении мозжечка – расстройства координации, атаксия и неспособность выполнять повторяющиеся действия (сгибать и разгибать пальцы рук и др.).
У больного могут наблюдаться такие симптомы и жалобы:
- нарушения памяти;
- изменения чувствительности (в ощущениях температур, положения тех или иных частей тела);
- проблемы с чтением;
- нарушения в письме;
- различные параличи и парезы;
- неконтролируемое или затрудненное мочеиспускание и акт дефекации;
- нехарактерное изменение черт личности и характера;
- гормональные нарушения и др.
Диагностика
Процесс диагностики раковых опухолей головного мозга затруднен из-за анатомического строения черепа, т. к. новообразование располагается внутри черепной коробки. Затрудняют ранее выявление и нехарактерные симптомы этого заболевания, т. к. они могут наблюдаться и при других патологиях организма.
План обследования больного с подозрением на злокачественное новообразование головного мозга должен включать в себя такие этапы:
- осмотр у невролога, нейрохирурга или невролога-онколога;
- анализы на онкомаркеры;
- МРТ с введением контрастного вещества;
- пункционная биопсия (при возможности проведения этой инвазивной манипуляции) и гистологическое исследование тканей биоптата.
Лечение
Тактика лечения определяется индивидуально для каждого пациента и зависит от стадии заболевания, типа раковых клеток и общего состояния здоровья больного. После изучения всех диагностических данных больному необходима консультация:
- невролога;
- нейрохирурга;
- оноколога;
- радиолога;
- химиотерапевта;
- врачей других специальностей (при необходимости).
Для избавления от злокачественной опухоли могут применяться хирургические способы (в т. ч. и эндоскопические), методики стереотаксической хирургии, радиолучевой и химиотерапии. Наряду с этими способами лечения больному назначается симптоматическая терапия.
Среди инновационных методов лечения рака мозга применяются такие методики:
- генная терапия;
- гипертермия;
- иммунотерапия;
- физиологическое картирование;
- фотодинамическая терапия.
При проведении операции по удалению ракового новообразования врач может не только удалить опухоль, но и провести гистологический анализ, который позволяет установить тип раковых клеток. В дальнейшем такая тактика выполнения оперативного вмешательства позволяет составить наиболее эффективный план лечения больного при назначении радиолучевой или химиотерапии.
Для выполнения хирургических операций могут проводиться как радикальные операции, так и эндоскопические, которые являются менее инвазивными и выполняются при помощи специального оборудования.
Для выполнения таких неивазивных операций применяются такие методики:
- кибер-нож;
- гамма-нож;
- протонная хирургия.
Главными преимуществами таких вмешательств является их высокая точность, минимальный риск развития осложнений и более короткий срок реабилитации больных после проведения операции.
Применение лучевой терапии для лечения опухолей головного мозга может осуществляться при неоперабельных случаях и в качестве дополнения к основному курсу терапии после проведения хирургического удаления новообразования. Доза лучевой нагрузки определяется индивидуально для каждого пациента и зависит от глубины расположения новообразования и клеточного состава опухоли.
При раке головного мозга может проводиться:
Химиотерапия при раке головного мозга может проводиться по различным схемам, выбор которых зависит от клинических показаний. Она может выполняться путем назначения одного препарата или нескольких химиотерапевтических средств. Путь их введения также определяется индивидуально для каждого больного и может проводиться перорально, внутривенно или через специально установленный ликворный шунт.
Для проведения курса химиотерапии могут использоваться такие группы препаратов:
- антиметаболиты;
- алкилирующая группа;
- антибластические антибиотики;
- полусинтетические и синтетические препараты;
- средства природного происхождения.
В некоторых случаях для повышения эффективности химиотерапии целесообразно параллельное назначение лучевой терапии.
Цикл химиотерапии длится несколько недель, а для достижения необходимого результата, как правило, проводится около 2-4 курсов. После этого больному рекомендуется перерыв, во время которого врач сможет установить эффективность проведенного курса терапии.
Во время химиотерапевтического лечения больному назначаются препараты и диета, которые необходимы для поддержания функционирования различных органов и систем, т. к. цитостатики обладают широким спектром побочных действий.
После завершения курса лечения больному показано диспансерное наблюдение, проходить которое он может в поликлинике по месту жительства или в других лечебных учреждениях.
Реабилитация больных после лечения и прогноз
После проведения лечения рака головного мозга больному необходима длительная реабилитация, которая направлена на возможное восстановление утраченных функций. Курс такой восстановительной терапии проводится в специализированных центрах или близкими больного, которых обучает врач.
Прогноз выживаемости после лечения рака мозга зависит от стадии и типа опухолевого процесса. К сожалению, большинство летальных исходов от этого тяжелого онкозаболевания наступает вследствие позднего выявления злокачественного новообразования. Помните об этом и будьте здоровы!
К какому врачу обратиться
При появлении признаков, указывающих на проблемы с головным мозгом, следует обратиться к неврологу. После обследования пациента врач направляет его к нейрохирургу и онкологу.
Читайте также:

