Современные методы лечения лимфом
2020. Gilead заплатила $4.9 млрд за перспективный иммуно-онкологический препарат
Компания Gilead Sciences купила за $4.9 млрд стартап Forty Seven, чьим основным активом является препарат Magrolimab - антитело против раковых клеток. Оно нацелено на рецептор CD47, который позволяет раковым клеткам избежать нападения иммунной системы. В данный момент Magrolimab проходит клинические испытания сразу по нескольким типам рака: неходжкинская лимфома, В-клеточная лимфома, колоректальный рак, рак яичек и мочевого пузыря. Говорят, препарат действительно показывает многообещающие результаты и такая огромная сумма, заплаченная за него - это серьезное подтверждение.
2019. Новая иммунотерапия дает надежду на излечение лимфомы

Исследователи из Центра Маунт-Синай (в Нью-Йорке) под руководством доктора Джошуа Броди (на фото) разработали новый метод иммунотерапии, помогающий остановить развитие особо агрессивного и трудноизлечимого рака крови - неходжкинской лимфомы. Они создали вакцину, которая заставляет иммунные клетки организма (а именно, дендритные клетки) мигрировать к опухолям и помечать их маркерами для других иммунных клеток-убийц (Т-лимфоцитов). Броди говорит, что они вводят вакцину в одну опухоль, а остальные исчезают сами собой. Разработчики испытали вакцину на 11 пациентов с тяжелой формой лимфомы, и у 3 из них произошла значительная ремиссия.
2017. CAR-T иммунотерапия показала высокую эффективность для лечения неходжкинской лимфомы
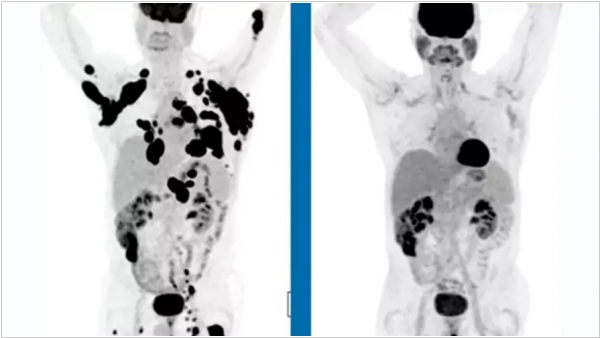
Фармацевтическая компания Kite Pharma обнародовала первые результаты клинических испытаний новой CAR-T иммунотерапии YESCARTA для лечения неходжкинской лимфомы. Новая технология позволяет перепрограммировать собственные иммунные клетки больного лимфомой человека за пределами его организма. Ученые модифицировают клетки, так, чтобы на своей поверхности они несли так называемые химерные антигенные рецепторы. Получившиеся модифицированные клетки начинают сами охотиться на раковые клетки и эффективно разрушать опухоли. В исследовании принимал участие 101 пациент с тремя различными формами лимфомы, причем в тяжелой, терминальной стадии заболевания, когда никакие способы лечения уже не действовали. В отчете говорится, что у трети таких пациентов спустя шесть месяцев наблюдалась полная ремиссия. На фоне успеха клинических испытаний акции компании выросли сразу на 25%. Конкуренты Kite Pharma - Juno Therapeutics и Novartis тоже проводят клинические испытания подобных препаратов.
2015. Ученые разработали гель для лечения лимфомы кожи

Первая фаза клинических исследований продемонстрировала безопасность и эффективность применения геля с резиквимодом (resiquimod) в терапии ранней стадии Т-клеточной лимфомы кожи. Результаты КИ были опубликованы в журнале Blood. В испытаниях экспериментального геля приняли участие 12 пациентов с Т-клеточной лимфомой кожи стадии IA-IIA. В течение 16 недель пациенты использовали гель с резиквимодом (0,03% и 0,06%) для обработки пораженных участков кожи. Согласно полученным результатам, состояние кожного покрова улучшилось у 75% пациентов, а у 30% полностью прошли поражения кожи. Ученые констатировали, что новый гель обладает позитивным профилем безопасности. Резиквимод (R-848) относится к группе имидозолинов и является модулятором иммунного ответа. Препарат обладает противоопухолевой и противовирусной активностью.
2015. В Китае разработали лекарство от лимфомы

Спустя 14 лет с начала разработок в китайская компания ChipScreen Biosciences начала продажи препарата Epidaza, предназначенного для лечения лимфомы – злокачественного новообразования лимфатических узлов. Epidaza стала первым в Китае и четвертым во всем мире препаратом класса селективных ингибиторов для пациентов с Т-клеточной лимфомой. На его исследование и разработку было потрачено $70 млн. ChipScreen Biosciences объявила, что месячный курс лечения Epidaza в Китае будет стоить 26 500 юаней ($4 275), что гораздо меньше стоимости ряда новых онкопрепаратов в США.
2012. Adcetris - первый в мире сертифицированный препарат для лечения лимфомы
Компания Seattle Genetics получила сертификацию FDA на свой препарат Adcetris, предназначенный для лечения злокачественных опухолей – лимфомы Ходжкина и анапластической крупноклеточной лимфомы. Препарат показан к применению взрослым пациентам с рецидивирующей формой этих заболеваний, а также пациентам, которым не помогают традиционные виды лечения. Adcetris направлен на уничтожение раковых клеток, однако, в отличие от стандартной химиотерапии, лекарство не уничтожает здоровые клетки и ткани организма. Adcetris – первый фармакологический препарат для лечения лимфогранулематоза, одобренный FDA с 1977, и вообще первый препарат, непосредственно рекомендованный для лечения анапластической крупноклеточной лимфомы.
| Радиоперехваты круглых столов [8] |
| Радиомагазин-73 [505] |
Войти через uID
Эпидемиология. В связи с выраженной гетерогенностью рассматриваемой группы заболеваний сложно получить достоверные эпидемиологические данные по каждой из нозологических форм.
В целом на долю НЛ приходится около 10—15% от всех онкогематологических заболеваний, заболеваемость — 10,5 случаев на миллион жителей.
НЛ составляют 1/3 среди всех злокачественных заболеваний у детей.
У взрослых НЛ встречаются в любом возрасте.
Этиология
Среди этиологических факторов выделяют:
1) ионизирующее облучение;
2) воздействие различных канцерогенов;
3) вирусные инфекции (вирус Эпштейна—Барра, человеческие Т-лимфотропные вирусы, герпесвирусы 6, 8 и т.д.);
4) физиологическая нестабильность генома;
5) наличие хронической иммунной стимуляции, что может быть связано с развитием иммунодефицита (у больных с инфекцией H.pylory часто развиваются MALT-лимфомы, также имеется повышенный риск развития лимфом у больных хроническим гепатитом С, саркоидозом, аутоиммунными заболеваниями; у ВИЧ-инфицированных наиболее часто развитие лимфом связано с действием вируса Эпшейна-Барра).
Патогенез.
Под действием этиологических факторов клетки иммунной системы могут подвергаться злокачественной трансформации. Лнмфоидные клетки способны озлокачествляться на любом этапе дифференцировки.
При этом они пролиферируют и создают клон клеток с блоком дифференцировки на определенной стадии созревания.
Хромосомные транслокации характерны для гистологических подтипов, вовлекают в патологический процесс различные протоонкогены.
Сущностью транслокаций является реципрокная рекомбинация между двумя специфическими участками хромосом. При этом протоонкоген располагается рядом с гете- рологичными регуляторными последовательностями (чаще всего это регуляторные гены-энхансеры иммуноглобулиновых локусов — V,D,J и С-участков или локусов ТКР). Чаще всего протоонкогены, заинтересованные в транслокациях (C-MYC,PAX-5,PIM-1,BCL2), регулируют клеточный цикл, рост и дифференцировку клеток, апоптоз. Инактивация генов-супрессоров опухолевой прогрессии также имеет место в патогенезе лимфом, при этом чаще всего обнаруживается биаллельная инактивация таких генов, как р53, р16, ATM. Транслокации при лимфомах вовлекают в патогенез множество различных генов.
Хромосомные транслокации, выявляющиеся в случаях лимфом, могут приводить к возникновению опухоли, по меньшей мере, реализовываясь в одном из 4 механизмов:
1) регуляция апоптоза;
2) участие в регуляции клеточного цикла;
3) активация NF-kB;
4) сигнальная трансдукция от В-клеточных рецепторов.
Утрата контроля над пролиферацией, вызванная нарушением регуляции экспрессии с—muc или другими аналогичными последствиями транслокаций хромосомного материала, открывает путь к неоплазии, но сама по себе недостаточна для злокачественной трансформации.
Поражение костного мозга при лимфоме (лейкемизация) приводит к развитию недостаточности костномозгового кроветворения с развитием цитопении периферической крови.
Рост опухолевых узлов может нарушать функцию близлежащих органов и вызывать их дисфункцию. Накопление опухолевой массы приводит к общему истощению организма — кахексии.
Классификация НЛ.
Существует множество различных классификаций НЛ.
Рабочая классификация выделяет лимфомы в соответствии со степенью дифференцировки клеток:
1) низкой степени злокачественности, характеризующиеся высоко дифференцированными лимфоцитами;
2) промежуточной степени злокачественности;
3) высокой степени злокачественности, характеризующиеся недифференцированными лимфоидными клетками.
Классификация ВОЗ подразделяет НЛ на В- и Т- клеточные.
В-клеточные лимфомы:
1) В-клеточные лимфомы/лейкемии из клеток-предшественников;
2) зрелоклеточные (периферические) В-НЛ (лимфомы маргинальной зоны) — MALT-лимфома, возникающая из лимфоидных клеток слизистой ЖКТ; нодаль- ные лимфомы маргинальной зоны; селезеночные маргинальные лимфомы;
3) фолликулярные лимфомы;
4) лимфомы мантийной зоны;
5) диффузные крупноклеточные В-лимфомы;
6) лимфома Беркита.
Т-клеточные лимфомы:
1) Т-клеточные лимфомы из клеток-предшествеников;
2) зрелоклеточные (периферические) Т-клеточные НЛ — Т-пролимфоцитарная лимфома; Т-лимфоцитарная лимфома; агрессивная лимфома из NK-клеток (натуральных киллеров);
3) лимфомы кожи (грибовидный микоз, болезнь Сезари) и другие.
Клиническая картина лимфом полиморфна.
В отличие от острых лейкозов злокачественная пролиферация начинается не в костном мозге, а в экстрамедуллярной лимфоидной ткани.
Наиболее часто — в лимфоузлах, однако необходимо помнить о возможности первичного поражения любого органа, где имеет место лимфоидная ткань (кожа, слизистая желудка и кишечника, головной мозг, молочная железа и т.д.).
Лимфому следует заподозрить, когда где-либо появляется плотная опухоль, не приносящая больному беспокойства.
Иногда лимфоме сопутствуют признаки интоксикации, аутоиммунной гемолитической анемии, аутоиммунной тромбоцитопении, васкулита с поражением кожи.
Клинические проявления зависят от локализации опухолевой массы: при НЛ с поражением медиастинальных лимфоузлов может развиваться синдром сдавления верхней полой вены, при поражении желудка — тошнота, рвота, боли в эпигастрии и т. д.
Достаточно патогномонична, но не обязательна для лимфопролиферативной опухоли триада признаков: проливные поты, особенно в ночные часы, потеря веса, кожный зуд.
Довольно часто имеет место повышение температуры тела без признаков инфекции.
Иммунологическая недостаточность у больных с лимфомами провоцирует присоединение бактериальных и вирусных инфекций.
Бактериальные агенты чаще всего вызывают развитие острой пневмонии или инфекции мочевыводящих путей.
Среди вирусных инфекций на первом месте стоят герпетические инфекции.
В зависимости от распространения опухолевой массы выделяют 4 стадии в соответствии со шкалой Энн-Арбор:
1 стадия — увеличение одной группы лимфатических узлов;
2 стадия — увеличение двух и более групп лимфатических узлов по одну сторону от диафрагмы;
3 стадия — увеличение двух и более групп лимфатических узлов по обе стороны от диафрагмы;
4 стадия — поражение паренхиматозных органов, в том числе костного мозга.
Диагностика НЛ основывается на гистологическом исследовании субстрата опухоли (лимфоузла, слизистой и т. д.) с использованием иммуногисто-фенотипирования.
Для диагностики необходимо использовать именно гистологический материал, данные цитологической (аспирационной) биопсии непригодны для диагностики.
Для определения стадии НЛ используют пальпаторное исследование периферических лимфоузлов, КТ органов грудной, брюшной полости, малого таза, биопсию костного мозга.
Для выявления факторов риска — b2-микроглобулин.
Таким образом, современная диагностика лимфом представляет собой комплексный процесс, сочетающий сразу несколько методов исследования. Только такой подход может обеспечить точную верификацию диагноза, являющегося основой выбора максимально эффективного лечения для больного.
Периферическая кровь не изменена, если нет поражения костного мозга.
Лейкемизация характеризуется лейкоцитозом за счет опухолевых лимфоидных клеток, в случае лимфоцитарных лимфом — за счет зрелых лимфоцитов, при лимфобластных лимфомах — за счет лимфобластов.
Дифференциальная диагностика:
1.С реактивными лимфоаденопатиями на фоне регионального банального лимфаденита, инфекционного мононуклеоза, краснухи, аденовирусных инфекций, болезни кошачьих царапин, туберкулеза, бруцеллеза, туляремии и т. д. (в неясных случаях назначают антибиотикотерапию с контрольным посешением через 2—4 нед.
В случае исчезновения увеличенных лимфоузлов ставят диагноз реактивной лимфоаденопатии.
При сохранении увеличения лимфоузла — показана биопсия).
2. С болезнью Ходжкина (лимфогранулематозом) — на основании гистологии.
3. С метастазами соллидной опухоли — на основании гистологии.
Для лимфом низкой степени злокачественности используются: выжидательная тактика при отсутствии признаков прогрессии; локальная лучевая терапия при 1 стадии; хлорбутин с преднизолоном; монотерапия флюдарабином; флюдарабин с циклофосфаном; флюдарабин с циклофосфаном и мабтерой; зевалин (ибритумомаб); полихимиотерапия по схемам CHOP (циклофосфан, рубомицин, винкристин, преднизолон), CVP (циклофосфан, винкристин, преднизолон) и др.
Получены первые обнадеживающие результаты терапии рефрактерных или рецидивирующих лимфом низкой степени злокачественности велькейдом с мабтерой, новыми пуриновыми аналогами (FLAMP, 2 CDA).
Для лимфом промежуточной и высокой степени злокачественности — полихимиотерапия по схемам CHOP с/без мабтеры, в зависимости от экспрессии CD20 на злокачественных клетках, и другие схемы ПХТ.
Аутотрансплантация ГСК и аллогенная ТГСК показаны в качестве консолидации ремиссии при лимфомах высокой степени злокачественности 3—4 стадии, особенно при рецидивирующих лимфомах, а также при лимфоме мантийной зоны.
Исходы лечения.
Полная ремиссия: отсутствие признаков лимфомы (100% регресс опухолевой массы), подтвержденное КТ спустя 6 недель после окончания XT.
Частичная ремиссия: уменьшение размеров опухоли более чем на 50% по контрольным очагам (при измерении двух диаметров) при отсутствии появления новых очагов.
Стабилизация заболевания: изменение размеров опухолевых образований (+ или - 25%).
Прогрессирование заболевания: увеличение размеров опухолевых образований более чем на 25%, или появление новых опухолевых очагов несмотря на проводимую терапию.
Рецидив: появление опухолевых образований более 1,5 см после достижения полной ремиссии.
Современное лечение лимфом, базирующееся на точном морфологическом диагнозе, позволяющее продлевать и сохранять жизнь больным, требует слаженной работы многих специалистов, привлечения наукоемких и ресурсоемких технологий и, безусловно, зависит от экономической политики государства в области здравоохранения.
Прогноз.
Индивидуальный прогноз зависит or подварианта лимфомы и возможности проведения адекватного лечения.
10-летняя выживаемость пациентов с лимфомой маргинальной зоны составляет 70%; фолликулярной зоны 60%; анапластической крупноклеточной лимфомой — 60%; диффузной крупноклеточной В-лимфомой, Т-лимфомой кожи, лимфомой Беркита и лимфоцитарной лимфомой — 40-50%; лимфомой мантийной зоны — 10-15%.

Основные варианты лимфом - лимфома Ходжкина и неходжкинские лимфомы. Раньше считалось, что лимфомы и лейкозы являются полностью отдельными заболеваниями. Однако, последние достижения в понимании клеточных маркеров показали, что границы между этими заболеваниями часто размыты.
Представление о том, что опухолевое поражение при лимфоме ограничено лимфатической системой, а при лейкозах - костным мозгом, также не всегда правильно. Соответственно, диагностика и лечение лимфом у лучших Израильских врачей с самого первого этапа является важным, жизне-сохраняющим моментом. Современные методы лечения лимфомы в Израиле методами химиотерапии спасают множество жизней.
Симптомы лимфомы схожи со многими заболеваниями и пациенту сложно заподозрить опасность для его жизни на первых этапах болезни. Больные, как правило, обращаются с жалобами на безболезненное увеличение лимфоузлов или со случайно выявленной при рентгенографии медиастинальной лимфаденопатией. При биопсии лимфоузла выявляются патогномоничные двухъядерные клетки Рид–Штернберга - характерные только для лимофмы Ходжкина.
При применении поли-химиотерапии, иногда в комбинации с лучевой и иммуно-терапией, удается добиться излечения у 70–80% больных.
Симптомами заболевания могут быть лимфаденопатия, лихорадка, ночные поты, потеря веса, кожный зуд, спленомегалия и гепатомегалия. Диагноз ставится на основании данных биопсии лимфатических узлов.
Соотношение пациентов /мужчины:женщины/ составляет 1,4:1. Заболевание редко встречается у детей до 10 лет, чаще всего выявляется в возрасте от 15 до 40 лет; второй пик заболеваемости отмечается у людей старше 50–60 лет.
Причина развития этого заболевания неизвестна, однако определенное значение имеют генетическая предрасположенность и влияние окружающей среды (профессия, в т. ч. работа в деревообрабатывающей промышленности; история воздействия фенитоина, лучевой терапии или химиотерапии; инфицирование вирусом Эпштейна–Барр, Mycobacterium tuberculosis, герпесвирусом 6 типа, ВИЧ).
Риск также повышен у больных с иммуносупрессией (например, пациенты после трансплантации, получающие иммунодепрессанты), у больных с врожденной недостаточностью иммунитета (атаксия-телеангиэктазия, синдром Клайнфельтера, синдром Чедиака–Хигаси, болезнь Вискотта–Олдрича) и с аутоиммунными заболеваниями (ревматоидный артрит, целиакия, синдром Шенгрена, СКВ).
У большинства больных выявляется безболезненное увеличение шейных лимфоузлов. В ряде случаев может возникать болезненность пораженных лимфатических узлов сразу после приема алкогольных напитков, что позволяет установить диагноз на ранних этапах; механизм этого феномена остается неизвестным.
- Рентгеноскопическое исследование органов грудной клетки
- КТ органов грудной клетки, брюшной полости и малого таза
- Общий анализ крови, биохимический анализ крови: щелочная фосфатаза, ЛДГ, показатели функции печени, альбумин, кальций, креатинин
- Биопсия лимфоузла
- ПЭТ для стадирования, МРТ при наличии неврологических симптомов
- Биопсия костного мозга – в отдельных случаях
При классической лимфоме Ходжкина отсутствие признаков заболевания в течение 5 лет после завершения лечения считается излечением от болезни. Рецидив после 5 лет происходит очень редко. При применении химиотерапии с или без лучевой терапии излечение достигается у 70–80% больных.
К факторам высокого риска рецидива относятся мужской пол, возраст > 45 лет, множественные экстранодальные поражения, наличие симптомов интоксикации при диагностике. Больные, не достигшие полной ремиссии или рецидивировавшие в течение первых 12 месяцев после завершения лечения, имеют неблагоприятный прогноз.
Лечение
- Химиотерапия
- Лучевая терапия
- Хирургическое вмешательство
- В отдельных случаях – трансплантация гемопоэтических стволовых клеток
Выбор варианта лечения сложен и в первую очередь зависит от точного определения стадии заболевания. До начала лечения лимфомы в Израиле мужчинам детородного возраста предлагают консервацию спермы, а женщинам – гормональную защиту яичников.
Больные IА, IIА, IВ или IIВ стадиями болезни, как правило, получают режим полихимиотерапии AБВД, включающий доксорубицин (адриамицин), блеомицин, винбластин и дакарбазин в сочетании с лучевой терапией или режимом длительного курса химиотерапии без лучевой терапии. Применение этого варианта лечения приводит к излечиванию до 80% больных. У больных с массивным опухолевым поражением средостения необходимо применение большего числа циклов лечения или более агрессивного режима полихимиотерапии, при этом, как правило, применяется лучевая терапия.
Аутологичная трансплантация гемопоэтических стволовых клеток должна рассматриваться как вариант лечения у всех соматически сохранных больных рецидивами или рефрактерными формами лимфомы Ходжкина, ответившими на терапию 2 линии.
Все лимфомы подразделяют на две большие группы — лимфома Ходжкина и неходжкинская лимфома.
Лимфома Ходжкина (лимфогранулематоз)
Злокачественная опухоль, поражающая лимфатическую систему. При этой лимфоме формируются характерные гранулемы.
Главное отличие лимфомы Ходжкина от неходжкинской лимфомы — наличие специфических патологических крупных (до 20 микрон) клеток в лимфатической ткани, которые называются клетками Рид-Штернберга. Наличие этих клеток предполагает лечение лимфомы Ходжкина принципиально отличающееся от лечения других видов лимфомы.

Методы лечения лимфомы
Лимфома Ходжкина встречается реже, чем другие злокачественные лимфомы. Происхождение клеток Рид-Штернберга пока непонятно, но развиваются они из В-лимфоцитов. Этим заболеванием страдают в основном мужчины в возрасте от 25 до 30 лет и от 50 до 55 лет. Установлено, что к лимфоме Ходжкина имеется генетическая предрасположенность.
Основной симптом заболевания — увеличение как периферических, так и внутригрудных лимфатических узлов; обычно они образуют разные по размеру конгломераты. Чаще всего увеличиваются шейные, надключичные, подмышечные, паховые узлы, а также узлы средостения, внутригрудные узлы, бедренные узлы.
При лимфоме Ходжкина организм испытывает сильную интоксикацию: обильная ночное потоотделение, снижение веса; повышенная температура до 38 градусов держится месяцами. Увеличенные лимфатические узлы могут оказывать давление на сосуды и органы, что может привести к одутловатости лица и шеи; вызвать кашель и одышку; сдавливать легкие, трахеи, спинной мозг (может развиться паралич). Часто злокачественным процессом поражаются внутренние органы (печень), костная система (позвоночник, тазовые кости, грудина, ребра).
Лимфома неходжкинская (лимфосаркома)
Выделяют несколько видов неходжкинских лимфом.
Лимфома Беркитта — лимфома очень высокой степени злокачественности. Опухолевые клетки имеют происхождение из В-лимфоцитов. Лимфома этого вида распространяется за пределы лимфатической системы во внутренние органы, в кровь, в костный мозг. Развитие болезни связывают с активностью вируса Эпштейн-Барр в организме, плохой экологией.
Начало заболевания по симптомам напоминает простуду — регионарная лимфаденопатия, ночная потливость и повышенная температура (следствие интоксикации). Если патологический очаг локализуется в зоне желудочно-кишечного тракта, то клиническая картина может дополниться непроходимостью кишечника; при локализации лимфомы в зоне мочеполовой системы появляются симптомы почечной недостаточности, нарушается электролитный баланс. По мере развития заболевания пациенты ежемесячно могут терять до 10 килограммов.
Диффузная крупноклеточная лимфома — лимфома с высокой степенью агрессивности. Чаще болеют люди среднего и старшего возраста. Опухолевые клетки имеют происхождение из В-лимфоцитов. Первичный очаг может иметь локализацию как в лимфатических узлах, так и вне лимфатических узлов (как правило в этом варианте опухоль располагается на уровне желудочно-кишечного тракта и мочеполовой системы).
Отдельным случаем выделяют первичную В-крупноклеточную лимфому средостения; считается, что первоначально опухоль развилась из вилочковой железы (тимуса), а затем проросла в средостение. Характерной особенностью этого вида лимфомы является тот факт, что, несмотря на способность быстро прорастать в соседние органы, она никогда не метастазирует. Чаще этому виду лимфомы подвержены молодые женщины.
Лимфобластные лимфомы (Т и В) — могут развиваться как из Т-лимфоцитов, так и из В-лимфоцитов. Клиническая картина очень похожа на лейкоз. Образуются массивные опухоли с локализацией, как правило, в средостении. Этот вид лимфомы характеризуется поражением центральной нервной системы; происходит трансформация костного мозга как при остром лейкозе. При дальнейшем развитии болезни поражаются печень, почки, селезенка. На долю Т-клеточных лимфом приходится 80% , на долю В-клеточных лимфом — 20%.
Маргинальная лимфома — отличается высокой степенью злокачественности, развивается из пограничной (маргинальной) зоны клеток в селезенке. Относится к вялотекущим опухолям.
Анапластическая лимфома — происхождение берет из Т-клеток. При этом виде злокачественного процесса клетки утрачивают свои характеристики (аплазия).
- Первая стадия — характеризуется поражением одного или нескольких лимфатических узлов, находящихся в одной зоне. Если лимфома локализована в одном органе без поражения окружающих лимфатических узлов — это тоже опухоль первой стадии.
- Вторая стадия — опухоль поражает два или больше лимфатических узлов, находящихся по одну сторону от диафрагмы. Если опухоль поразила один лимфатический узел и расположенный рядом орган – этот вариант тоже относят ко второй стадии.
- Третья стадия — в патологический процесс вовлечены два и более лимфатических узлов, расположенных по одну сторону от диафрагмы; также к третьей стадии относят опухоли, поразившие одновременно селезенку и несколько лимфоузлов, находящихся с противоположных сторон по отношению к диафрагме. К третьей стадии относят ситуации, когда в злокачественный процесс вовлечены лимфоузлы из разных зон и один орган, расположенный рядом с лимфоузлом.
- Четвертая стадия — диссеминированная (массово распространенная) опухоль; злокачественным процессом поражен не один, а несколько органов, которые находятся в отдалении от первичной локализации лимфомы.
Проводится комплексное тщательное обследование больного: развернутый анализ крови (обычно выявляются высокие показатели СОЭ и лейкоцитов, пониженные показатели гемоглобина и лимфоцитов), рентгенография грудной клетки, КТ, УЗИ, ПЭТ, трепабиопсия, фиброларингоскопия и биопсия измененных структур; проводят пункцию и цитологические исследования.
Современные методы лечения позволяют достичь хороших результатов в лечении лимфом.
Полного излечения от лимфомы можно достигнуть при применении комбинированной терапии( химиотерапия и лучевая терапию). Интересно, что излечению лучше всего поддаются лимфома Ходжкина и агрессивные лимфомы.
Смотрите также другие научные статьи:
Лимфома являет собой злокачественное образование, поражающее лимфатическую систему. При заболевании лимфома лечение должно быть начато своевременно и в полном объеме, чтобы обязательно достичь результатов.
Пациенту необходимо знать, что лимфома – это не приговор, и она успешно лечится, в частности, в Израиле.
Когда нужно обследоваться
Если замечены припухлости или другие изменения со стороны лимфатической системы, то нужно без промедления обратиться к врачу. Раннее обнаружение болезни существенно улучшает ее прогноз.
В самом начале обследования врач проводит первичный осмотр. Осматривается состояние лимфатических узлов, в частности, под мышками, в паху, на шее. Другие же исследования обязательно должны включать в себя такие мероприятия:
- Анализы крови. Имеется в виду общий анализ крови, а также биохимия. Чем тщательнее будет проведен анализ крови, тем более точным будет диагноз. Кроме того, анализ крови в Москве стоимость имеет несколько более высокую, но он поможет определить, как далеко зашел опухолевый процесс в организме.
- Ренгтенография.
![]()
- Магнитно-резонансная томография.
- Лимфангиография. При этом лимфатическая система исследуется при помощи особого контрастного раствора.
- Биопсия. Это исследование показывает характер опухолевого образования.
Применение лекарств
В результате химиотерапии уничтожаются опухолевые клетки. Для того, чтобы методика была как можно более результативной, применяют не один, а несколько лекарственных препаратов. Если они принимаются в комплексе, то новообразование быстрее будет уничтожено.
Любая химическая процедура является системным видом лечения. Препараты распространяются по всему организму, влияют на состояние всех клеток, в том числе и желудка. Соглашаясь на такую терапию, важно помнить о том, что препарат уничтожает и нормальные, и раковые клетки.
С одной стороны, это дает возможность убить раковые клетки еще в зародыше. А с другой стороны, химпрепараты нарушают функционирование нормальных клеток.
Для того, чтобы препараты принесли как можно меньше вреда, при химиотерапии надо:
- уделять внимание режиму дня,
- полностью исключить вредные привычки,
- улучшить питание.
Применение методов лучевой терапии
Высокоактивные лучи воздействуют на онкоклетки, разрушая их. А вот здоровым организмам вред причиняется минимальный. Положительное влияние этого метода в том, что лучи действуют только на больные органы, не затрагивая всего организма. Так что лучевое воздействие существенно улучшает ответ на вопрос: излечима или нет лимфома.
Такое лечение обычно назначается вместе с химиотерапией – так оно может дать более заметные результаты. Если же лучевая терапия назначается как самостоятельное лечение, то это может быть только на первой стадии заболевания, когда опухоль еще не достигла значительных размеров. Все процедуры проходят в условиях стационара.
Пересаживание костного мозга
Этот вид лечения также способен давать неплохие результаты. По крайней мере, отзывы лечившихся в Москве говорят о том, что пересадка такого мозга – высокорезультативный метод терапии.
Операция назначается после прохождения курса химиотерапии, так как после нее клетки костного мозга являются практически разрушенными. После операции этот орган способен опять вырабатывать красные кровяные тельца.
Материал для пересадки получают из костного мозга самого пациента. Он извлекается до начала химиотерапии, когда мозг еще не поврежден полностью. Также можно пользоваться материалом, полученным от донора.
Биотерапия
При этом используются химические вещества, которые производятся в клетках самого пациента. Так можно задействовать защитные инструменты для борьбы с раком.
К сожалению, многие виды такой биологической терапии носят еще экспериментальный характер, да и цены на нее остаются все еще высокими. Но постоянное их усовершенствование дает врачам надежду, что болезнь вскоре будет побеждена.
В ходе терапии применяются такие методики:
- иммунотерапия;
- вещества, угнетающие ангиогенез, то есть процесс образования кровеносных сосудов в самой опухоли, способствуя тем самым ее уменьшению;
- генная терапия.
Что может сделать пациент для успешного выздоровления
Сегодняшние технологии лечения рака постоянно усовершенствуются. То, что раньше было недоступным, теперь становится все более и более эффективным.
Для того, чтобы лечение было как можно лучшим, пациент должен:
1 Дать врачу наиболее полную информацию о своей болезни, помочь собрать подробный анамнез.
2 Врач должен знать обо всех побочных эффектах лечения.
3 Необходимо правильно питаться, исключив из меню жареные, копченые блюда, а также алкоголь.
4 Неукоснительно выполнять все рекомендации лечащего врача.
Особенности протекания патологии у детей
Если у ребенка обнаружено это заболевание, его надо госпитализировать в детскую онкологическую клинику. Чаще всего применяется химиотерапия.
При этом ребенку назначаются препараты, которые не допускают патологического деления клеток. Тем самым можно достичь уничтожения опухоли. Для того, чтобы лечение
химиотерапией было как можно более эффективным, назначается комбинированный состав препаратов.
После химиотерапии у детей дополнительно назначается лучевая терапия для того, чтобы максимально закрепить результат.
Если химиотерапия (особенно в сочетании с лучевой) не показала результата, то назначают прием лекарственных препаратов с высокой дозировкой. При этом наблюдается отрицательное влияние этого лечения на костный мозг. Поэтому после проведенной химиотерапии ребенок дополнительно нуждается в пересадке костного мозга.
Лечение опухоли даже на первой стадии очень ответственное. Для достижения положительного результата пациенты должны всегда помнить об этом.
Читайте также:


