Сопроводительная терапия острых лейкозов
Всем больным назначается аллопуринол (300 мг/м2) в первые часы диагностики острого лейкоза. Объем вводимой жидкости при ОПЛ (физиологический раствор, раствор глюкозы, СЗП, криопреципитат, водорастворимый витамин K, альбумин при необходимости, тромбоциты, эритроциты) в течение суток может составлять более 3 л, поэтому необходим очень жесткий контроль водного баланса и стимуляция диуреза. Также следует помнить, что гиперволемия при ОПЛ может провоцировать более высокий риск легочных осложнений, сердечной недостаточности, имитировать синдром дифференцировки опухолевых клеток.
С учетом необходимости введения больших объемов растворов и трансфузионных средств больным после коррекции коагуляционных нарушений (переливание 10 - 16 доз тромбоцитов, криопреципитата, СЗП).
Регламентированное для ОМЛ использование гидроксимочевины при гиперлейкоцитозах для больных ОПЛ противопоказано вследствие развития фатальных геморрагических осложнений. При ОПЛ также не рекомендуется выполнять лейкаферезы - это усугубляет развитие ДВС-синдрома.
Важным для купирования осложнений на фоне начала химиотерапии при гиперлейкоцитозе, особенно на фоне большой волемической нагрузки и коагуляционных нарушений, является выполнение плазмаобменов.
Назначение антибактериальных, противогрибковых, противовирусных средств регламентируется при ОПЛ теми же правилами, которые используются в лечении острых миелоидных лейкозов. Применение колониестимулирующих факторов при ОПЛ не показано.
В лечении коагулопатии больных ОПЛ Рабочая группа рекомендует:
- Рекомендуется лечение ATRA (третиноин**) начать немедленно при малейшем подозрении на ОПЛ. [1 - 6]
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 1).
- Рекомендуется выполнять трансфузии СЗП, криопреципитата и тромбоцитов для поддержания уровня фибриногена выше 1,5 г/л и тромбоцитов более [1 - 6]
Уровень убедительности рекомендации - B (уровень достоверности доказательств - 1).
- Не рекомендуется использовать в рутинной практике гепарин**, транексамовую кислоту**, других антикоагулянтов или антифибринолитиков, так как их преимущество остается спорным. [1 - 6].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
В лечении гиперлейкоцитоза больных ОПЛ Рабочая группа рекомендует:
- Рекомендуется начать химиотерапию без промедления, без молекулярного подтверждения диагноза. [1 - 6]
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4).
- Рекомендуется назначение глюкокортикостероидных гормонов (дексаметазон**) с целью профилактики развития дифференцировочного синдрома. [1 - 6].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- Не рекомендуется лейкаферез из-за риска развития фатальных геморрагических осложнений. [1 - 6]
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4).
Сопроводительная терапия занимает существенное место в комплексном лечении онкологических больных. Качество и продолжительность жизни больных зависят от адекватно проведенной сопроводительной терапии. К задачам, стоящим перед сопроводительной терапией относятся:.
- обеспечение нормальной фармакокинетики химиопрепаратов,
- защита органов и тканей от токсического воздействия противоопухолевых препаратов и их метаболитов.
- поддержание гомеостаза и основного обмена,
- обеспечение функционирования всех жизненно важных систем организма,
- профилактика инфекций,
- лечение осложнений основного заболевания и вызванных химиотерапией.
Сопроводительная терапия должна быть максимально интенсивной, чтобы обеспечить возможность проведения химиотерапии в полном объеме и в нужные сроки.
Критичиеские состояния и их лечение
Синдром острого лизиса (распада) опухоли (СОЛО).
Этот синдром возникает чаще при опухолях с быстрой пролиферацией клеток: Т- и В-лимфомах, лейкозах и реже при солидных опухолях. Клинические проявления: острая почечная недостаточность, острая сердечная недостаточность, отек легких, коагулопатии (нарушение свертываемости крови).
При распаде опухолевых клеток в кровяное русло попадает большое количество внутриклеточных электролитов (фосфор, кальций, калий), продуктов деградации пуринов (ксантины, гипоксантины, мочевая кислота и др.), протеазы. При повышении концентрации в моче ксантинов, гипоксантинов и мочевой кислоты может возникнуть их кристаллизация и осаждение нерастворимых кристаллов в почечных канальцах и собирательных трубочках.
Фосфор и кальций образуют нерастворимые соединения, которые осаждаются в канальцах, а также в капиллярах тканей. В результате этого возникает гипокальцемия, олиго- и анурия и тканей некроз. Гипокальцемия часто приводит к гипомагнеземии, нарушению нервно-мышечной проводимости и сократимости гладкой и скелетной мускулатуры (спазмофилия, судороги, нарушение сердечной деятельности вплоть до остановки сердца).
Ксантины и мочевая кислота преципитируют в кислой среде (рН мочи 7,0). Гиперкалиемия - наиболее частое и наиболее опасное осложнение острого лизиса опухоли. Концентрация калия в крови более 7,0 ммоль/л вызывает остановку сердца.
Выход в кровяное русло в большом количестве протеаз и прокоагулянтов, находящихся в азурофильных гранулах промиелоцитов, повышение фибринолитической активности плазмы приводит к развитию тяжелой коагулопатии.
Возможность тяжелого кровотечения у больных миелоидным и лимфобластным лейкозом связывают с коагулопатией.
Внутрисосудистые лейкостазы характерны для острого миелоидного лейкоза с большим количеством бластных клеток на периферии (150-200 тысяч). Лейкостазы в крупных сосудах головного мозга и легких после распада клеток могут вызвать как тяжелых кровотечения, так и тромбоэмболии с клинической картиной мозгового инсульта и острой дыхательной недостаточности.
Переливание эритроцитарной массы до индукционной терапии является инициирующим фактором для развития лейкостазов. Быстрая коррекция анемии увеличивает вязкость крови. Выход субстанций из лейкозных клеток, лизированных химиотерапией, является потенциальным фактором либо повреждения легочного эпителия, либо сосудистой и легочной секвестрации клеток.
Острый пульмональный (легочный) тромбоз. Причины тромбообразования не вполне ясны. Предположительно тромбоз возникает из опухолевых эмболов после лизиса клеток. Не исключены механизмы нарушения внутрисосудистой микрокоагуляции. Можно предположить, что большое количество лейкоцитов серьезно влияет на циркуляцию крови в легочных сосудах.
Диагноз ставится на основании клинических данных острой дыхательной недостаточности (ОДН), возникающей сразу же после циторедуктивной терапии. Ангиография, пульмональная сцинтиграфия с Тс-альбумином помогают подтвердить диагноз.
Легочные осложнения, возникающие в начале заболевания или в течение первых дней от начала противоопухолевого лечения, связаны с различными факторами, включающими инфекцию, специфическую инфильтрацию легких лейкозными клетками, легочные сосудистые лейкостазы, внутрилегочные кровоизлияния, отек легких, токсичность химиотерапии.
СОЛО протекает тяжелее при поражении почек опухолевым процессом. Особенно опасна обструкция (непроходимость) мочеточников при лимфомах брюшной полости. Этот синдром может возникнуть и при небольшой опухоли, но в случае высокой чувствительности опухолевых клеток к химиотерапии.
Таким образом, при угрозе возникновения СОЛО циторедуктивная химиотерапия начинается с профазы, то есть с малых, постепенно увеличивающихся доз химиопрепаратов. СОЛО легче предотвратить, чем лечить.
ПРОФИЛАКТИКА СОЛО.
Повышенные уровни мочевой кислоты, калия, фосфора, креатинина должны быть приведены к норме до начала циторедуктивной терапии. Вместе с тем противоопухолевую терапию нельзя откладывать белее чем на 24 часа.
Меры профилактики СОЛО:
- Назначение аллопуринола.
- При лейкоцитозе более 100 тысяч в 1 мкл лейкаферез является методом выбора до начала специальной терапии, если такая возможность имеется в клинике.
- Все больные с угрозой развития уратной нефропатии должны получать гидратацию для коррекции существующего дефицита жидкости и для обеспечения форсированного диуреза в дальнейшем. Гидратация начинается с момента поступления больного в клинику до начала специального лечения. Увеличение объема выделяемой мочи, достигаемое при гидратации, уменьшает концентрацию уратов в моче. Необходим строгий контроль введенной и выделенной жидкости.
- Из-за угрозы возникновения гиперкалиемии либо из-за уже существующей гиперкалиемии в начале гидратации калий в инфузии не включается. Далее инфузия калия должна быть строго корригирована по концентрации его в крови. Допустима умеренная гипокалиемия.
- Алкализация мочи с помощью бикарбоната натрия до достижения рН мочи 7,0, но не более 7,5. При этом необходимо контролировать уровень ионизированного кальция. Коррекция дозы бикарбоната зависит от рН мочи.
- Назначение фуросемида.
- Ацетазоламид (ингибитор карбангидразы) может быть использован для усиления эффекта алкализации.
- При риске развития олигурии с профилактической целью необходимо введение микродоз дофамина.
- Ограничение энтерального питания, назначение через рот гидроокси алюминия для связывания фосфатов.
- Контроль (каждые 12 часов) уровня калия, ионизированного кальция, фосфора, мочевой кислоты, креатинина, мочевины в крови. Тщательный учет почасового диуреза, перспирации. Определение рН мочи.
- Контроль массы тела дважды в сутки.
- Ежедневный контроль уровня магния, натрия, альбумина, ЭКГ, КЩС (кислотно-щелочное состояние), СРБ (С-реактивный белок), коагулограммы.
ЛЕЧЕНИЕ СОЛО.
Основой лечения являются те же мероприятия, которые проводятся с целью профилактики развития СОЛО.
Гиперурекемия - увеличение объема внутривенно вводимой жидкости до 5 л/кв.м в сутки. При нормальном уровне фосфора дополнительная алкализация рН мочи может быть доведена до 7,5.
Гиперкалиемия (концентрация калия более 6 ммол/л) - начать подготовку к гемодиализу: глюкоза с инсулином, глюконат калиция, бикарбонат натрия. При концентрации калия выше 7 ммоль/л - немедленный гемодиализ.
Гиперфосфатемия - увеличение объема жидкости до 5 л/кв.м, рН мочи не более 7,0. Прекратить энтеральное питание, назначение гидроокиси алюминия через рот. При концентрации фосфора более 5 ммоль/л - гемодиализ.
Гипокалиемия - дотация кальция только при нормальной или пониженной концентрации фосфора.. Обязательный контроль уровня магния. При гипомагнеземии -введение магния.
Олиго- и анурия (диурез менее 50 мл/кв.м в час), несмотря на введение фуросемида и жидкости. Терапия: гемодиализ при уровне калия выше 6 ммоль/л. Необходимо исключить обструкцию мочеточников, инфильтрацию обеих почек.
Показания к гемодиализу:
- Уровень калия более 6 ммоль/л, несмотря на жидкостную терапию и диуретики.
- Уровень калия выше 7 ммоль/л - немедленный гемодиализ.
- Уровень фосфора выше 5 ммоль/л.
- Диурез менее 50 мл/кв.м в час при жидкостной нагрузке 130-200 мл/кв.м в час.
- Обструкция обоих мочеточников.
Коагулопатии. Лечение ДВС-синдрома (синдром диссеминированного внутрисосудистого свертывания) включает восполнение дефицита факторов свертывания - переливание свежезамороженной плазмы. При стойкой гипофибриногенемии - переливание криопреципитата фактора VIII.
Часто синдром протеолиза развивается быстрее, чем рост прокоагулянтной активности и развитие ДВС- синдрома, особенно у больных с большим числом бластов на периферии.
Вопрос использования гепарина или антифибринолитической терапии зависит от превалирования ДВС либо протеолитического синдрома. При тромбоэмболии легочных сосудов показано назначение урокиназы.
При пневмопатии и острой дыхательной недостаточности 3 степени показана искусственная вентиляция легких.
СИНДРОМ СДАВЛЕНИЯ ВЕРХНЕЙ ПОЛОЙ ВЕНЫ (ССВПВ)
Развивается очень быстро при сдавлении верхней полой вены в верхнем средостении. Эта вена окружена лимфатическими узлами. Симптомы: одышка, отек лица и мягких тканей головы, кашель, отек верхних конечностей, боли за грудиной, дисфагия, набухание вен шеи и грудной клетки, цианоз.
Данный синдром чаще возникает при лимфомах, тимомах и герминогенных опухолях. Тромбоз и тромбофлебит верхней полой вены также могут вызвать полную или частичную обструкцию сосуда. Инфузия ряда противоопухолевых препаратов вызывает тромбофлебиты. Длительно стояние центральных катетеров способствует тромбообразованию и инфицированию.
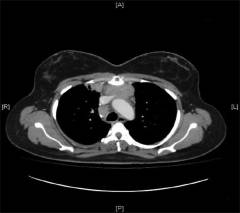
Диагноз устанавливается на основании клинических данных, рентгенографии грудной клетки (наличие опухоли, расширение средостения, плеврит), данных КТ и флебографии (в редких случаях).
Лечение ССВПВ, вызванного тромбозом вены. Стрептокиназа и урокиназа могут вызвать лизис тромба в ранней стадии тромбообразования. Гепарин и антикоагулянты непрямого действия уменьшают дальнейшее тромбообразование. Удаление центрального катетера проводят параллельно с антикоагулянтной терапией для предотвращения эмболии.
Для временного поддержания жизненных функций: возвышенное положение с приподнятой головой, увлажненный кислород. Мочегонные средства уменьшают отек, но эффект их паллиативный. Кроме того, риск тромбообразования при дегидратации увеличивается. В отдельных случаях применяются стероидные гормоны. Они снимают воспаление и отек тканей.
ССВПП, вызванный опухолью. Единственно эффективным является лечение основного заболевания (химиотерапия, гормонотерапия, лучевая терапия - 2-3 сеанса)
Компрессия (сдавление) спинного мозга. Может быть вызвана опухолью или метастазами. Симптомы сдавления спинного мозга могут быть единственным клиническим проявлением заболевания, например, неходжкинской лимфомы (лимфосаркомы) или нейрбластомы.
У 90% больных присутствует болевой синдром. Боли в спине усиливаются при движении, кашле. При отсутствии лечения появляется слабость в сочетании с потерей чувствительности. Нарушение функции тазовых органов появляется позже. После появления нарушения функции тазовых органов наступает быстрое прогрессирование симптомов сдавления и возникает параплегия.
Лечение: немедленное назначение дексаметазона и химиотерапии, в отдельных случаях дополнительно назначается облучение. При нейробластоме желательно удаление опухоли или ее части. Чем раньше начато лечение, тем больше вероятность полного восстановления неврологических функций.
Лактат-ацидоз. Лактат - это метаболит пирувата. Его образование катализирует фермент лактатдегидрогеназа (ЛДГ), уровень которого часто повышен у больных неходжкинской лимфомой и нейробластомой. Тип А возникает при нарушении тканевого дыхания и транспорта кислорода на периферии. Чаще всего этот вид регистрируется при шоке и септицемии. Тип В возможен при диабете, почечной недостаточности, печеночной недостаточности, при остром лимфобластном лейкозе и лимфомах, особенно в сочетании со специфическим поражением почек.
Острый лимфолейкоз
Острый лимфолейкоз – одна из разновидностей опухолей крови, злокачественное заболевание, при котором нормальная ткань красного костного мозга замещается опухолевой, происходит активное разрастание незрелых предшественников лимфоцитов – лимфобластов.
Острые лимфолейкозы в цифрах и фактах:
Клетки-лимфоциты: строение, функции, виды, где и как образуются.
Лимфоциты – клетки иммунной системы, которые отвечают за защиту организма от чужеродных веществ, вирусов, бактерий. Лимфоциты являются разновидностью белых кровяных телец – лейкоцитов.
Виды лимфоцитов:
| Название | Функции |
B-лимфоциты | Синтезируют антитела – молекулы, которые связываются с антигенами (чужеродными частицами) и запускают иммунный ответ. За активацию B-лимфоцитов отвечают T-лимфоциты. Изменения, происходящие с B-лимфоцитами после активации: |
Каждый лимфоцит, который выходит в кровь, является окончательной стадией деления ряда клеток, находящихся в органах кроветворения. Зрелые лимфоциты больше не могут размножаться и трансформироваться в другие клетки – их развитие завершено.
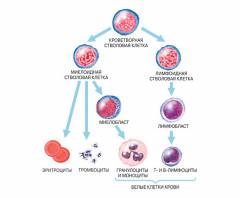
Стадии образования лимфоцитов:
| Центральные лимфоидные органы | |
| Орган | Описание |
| Красный костный мозг | 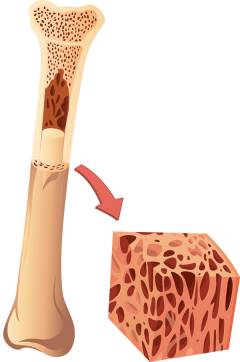 В красном костном мозге осуществляются начальные этапы созревания лимфоцитов. У детей этот кроветворный орган заполняет все кости. У взрослого часть красного костного мозга превращается в жировую ткань, он сосредоточен главным образом в позвонках, ребрах, костях таза, черепа, концах длинных костей рук и ног. Молодые лимфоциты находятся в периферической части красного костного мозга и постепенно, по мере созревания, передвигаются к центру. Затем лимфоциты выходят из красного костного мозга в кровоток и мигрируют в периферические лимфоидные органы, в которых происходит их дозревание. |
| Тимус (вилочковая железа) |  В вилочковой железе осуществляются начальные этапы созревания Т-лимфоцитов. Наиболее активен тимус в раннем детском возрасте. В нем выделяют две части: центральную и окружающую её кору. В коре находятся Т-лимфоциты. По мере созревания они смещаются всё глубже и в конце концов выходят в кровоток, мигрируют в периферические лимфоидные органы. В подростковом возрасте начинается атрофия тимуса. |
| Периферические лимфоидные органы | |
| Орган | Описание |
| Селезенка | 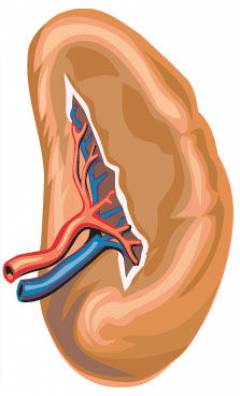 В селезенке выделяют красную и белую пульпу. В белой пульпе происходит дозревание T- и B-лимфоцитов, которые мигрируют сюда из тимуса и красного костного мозга. При поражении красного костного мозга селезенка может брать на себя его функции. |
| Лимфатические узлы | Лимфатические узлы распределены по всему организму, но работают вместе, как единый орган. В них происходит дозревание T- и B-лимфоцитов. В возрасте 4-8 лет активность лимфатических узлов максимальна. В 13-15 лет их формирование завершается. А в 20-30 лет начинается постепенная атрофия. |
| Скопления лимфатической ткани в кишечнике | Выполняют примерно те же функции, что лимфатические узлы. |
Причины возникновения острых лимфолейкозов

Первоначальной причиной развития заболевания является мутация, в результате которой в красном костном мозге возникает злокачественная лимфобластная клетка. Считается, что она присутствует в организме ребенка еще до рождения. Но для развития лимфолейкоза этого обычно недостаточно.
На организм должны подействовать другие негативные факторы:
- Хромосомные заболевания. Представляют собой нарушения количества и структуры хромосом. Например, дети, страдающие болезнью Дауна, имеют в 40 раз более высокий риск развития лимфолейкоза в возрасте до 4 лет.
- Действие радиации. Ученые обнаружили более высокую распространенность лимфобластных лейкозов среди следующих групп людей:
- работники, обслуживающие оборудование, излучающее радиацию;
- жители Японии, ставшие в свое время жертвами бомбардировок Хиросимы и Нагасаки;
- жители Украины, ставшие жертвами аварии на Чернобыльской АЭС и те, кто на данный момент проживают на территориях с повышенным радиационным фоном;
- больные со злокачественными опухолями, прошедшие курс лучевой терапии;
- дети, матери которых во время беременности проходили рентгеновское исследование (риск увеличивается незначительно, но повышается с каждой новой процедурой).
- Канцерогены. Существует большое количество токсичных веществ, попадание которых в организм повышает риск развития любых опухолей.
- Инфекции. На данный момент неизвестно, какие вирусы или бактерии могут провоцировать развитие лимфобластных лейкозов. Некоторые ученые считают, что играет роль не сама инфекция, а неправильный ответ на неё со стороны иммунной системы.
Проявления острого лимфолейкоза
Патологические изменения в организме при остром лимфобластном лейкозе, с которыми связаны все симптомы:
- Наличие опухолевой ткани. Фактически в красном костном мозге растет злокачественная опухоль.
- Нарушение кроветворения. В лимфоидных органах разрастается клон опухолевых клеток, и они вытесняют нормальную ткань. В итоге резко падает производство других видов лейкоцитов, эритроцитов, тромбоцитов.
Симптомы острого лейкоза всегда однотипны, вне зависимости от его разновидности. Не существует специфических признаков, по которым можно было бы однозначно установить диагноз. Врач может диагностировать острый лимфобластный лейкоз только после обследования.

Симптомы острого лимфолейкоза:
- Слабость, повышенная утомляемость, недомогание.
- Снижение аппетита.
- Повышение температуры тела без видимой причины.
- Бледность. Все вышеперечисленные симптомы возникают из-за анемии (уменьшение количества красных кровяных телец, — эритроцитов), интоксикации.
- Боли в руках, ногах, позвоночнике. Возникают из-за разрастания опухолевой ткани в красном костном мозге.
- Увеличение лимфатических узлов. Их можно прощупать под кожей, а иногда они хорошо заметны во время осмотра.
- Повышенная кровоточивость. Возникают кровоизлияния под кожей, во внутренних органах. После порезов кровь останавливается медленнее. Это происходит из-за снижения в крови количества тромбоцитов, которые отвечают за свертывание крови.
- Признаки поражения головного мозга: головные боли, тошнота и рвота, повышенная раздражительность. При остром лимфобластном лейкозе возникают очаги кроветворения вне красного костного мозга – они могут располагаться в нервной системе.
Диагностика острого лимфобластного лейкоза

Как правило, впервые подозрение на острый лимфолейкоз возникает у терапевта, когда обнаруживаются соответствующие патологические изменения в общем анализе крови. После этого пациента обычно направляют в гематологическую клинику для дальнейшего обследования и установления точного диагноза.
Исследования, которые назначаются при подозрении на острый лимфолейкоз:
| Название исследования | Описание | Как проводится? |
| Общий анализ крови | Общий анализ крови – самый быстрый и доступный способ, который позволяет заподозрить заболевание и направить больного на дальнейшее обследование. |
У 10% больных с острым лимфолейкозом картина крови нормальна – у них часто не удается заподозрить заболевание сразу.
У 90% больных выявляются патологические изменения:
- Резкое повышение количества лейкоцитов.
- Изменение соотношения разных видов лейкоцитов: число лимфоцитов резко возрастает, а других видов – уменьшается. Обнаруживаются молодые, незрелые лимфоциты, которых в норме не должно быть.
- Снижение числа эритроцитов и гемоглобина – анемия.
- Снижение числа тромбоцитов.
- Повышение скорости оседания эритроцитов.

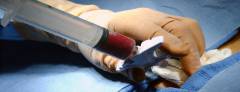
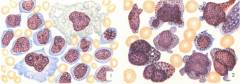
Исследования красного костного мозга:
- Миелограмма: подсчет количества разных типов клеток под микроскопом. Помогает обнаружить злокачественные бластные клетки.
- Цитохимические реакции. Специальные химические реакции, которые помогают различить бластные клетки, характерные для лимфобластного или нелимфобластного лейкоза.
- Иммунофенотипирование. Специальные иммунологические реакции, которые помогают установить тип бластных клеток в опухоли.
- Цитогенетическое исследование. Помогает обнаружить поломки в хромосомах, которые могли стать причиной развития заболевания.
- Полимеразная цепная реакция (ПЦР). Помогает точно установить мутации, которые могли привести к возникновению лейкоза.
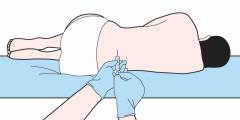
- Крыло подвздошной кости – их края находятся прямо под кожей справа и слева в области таза.
- Грудина – находится под кожей в центре грудной клетки.
- Остистые отростки позвонков – в виде небольших бугорков выступают посередине спины над каждым позвонком. Этот способ используется редко.
- Кости ноги: бедренная, большеберцовая, пяточная.

Лечение острого лимфолейкоза
Химиопрепараты представляют собой лекарственные средства, которые тормозят рост опухоли и уничтожают опухолевые клетки. Препараты и их дозировки подбирают строго индивидуально, в зависимости от некоторых факторов:
- Вид лимфолейкоза, особенности опухолевых клеток.
- Общее состояние организма больного. Оценивается по специальным формулам:
- Индекс Карновского. Может быть равен от 1 до 100%:
- 100%-80% — физическая активность нормальная, больному не нужен специальный уход;
- 70%-50% — активность ограничена, но больной может обслуживать себя сам;
- 40%-10% — больной нуждается в постоянном уходе или должен быть госпитализирован в стационар.
- Шкала ECOG:
- 0 баллов – активность больного не снижена, соответствует здоровому человеку;
- 1 балл – больной может выполнять сидячую и легкую работу, но не способен на тяжелый труд;
- 2 балла – больной не способен выполнять даже легкую работу, но может самостоятельно себя обслуживать;
- 3 балла – больной проводит половину времени бодрствования в кровати или в кресле, может себя обслуживать лишь частично;
- 4 балла – инвалид, который прикован к креслу или к кровати.
- Индекс Карновского. Может быть равен от 1 до 100%:
- Индекс коморбидности – специальный показатель, который разработан для оценки прогноза у больных, учитывает возраст пациента и наличие сопутствующих заболеваний.
- Личное согласие больного на терапию теми или иными препаратами.
Виды химиотерапии при остром лимфобластном лейкозе:
- Радикальная – направлена на достижение стойкого улучшения до полного выздоровления.
- Паллиативная – проводится обычно у пожилых пациентов для облегчения состояния и продления жизни.
Основные химиопрепараты, которые используются для лечения острого лимфолейкоза (строго по назначению врача):
- Цитарабин;
- Даунорабицин (Идарубицин, Доксарубицин);
- Митоксантрон;
- Этопозид;
- Амсакрин;
- 5-азацитидин;
- Флюдарабин;
- Винкристин;
- Циклофосфан;
- Метотрексат;
- L-аспарагиназа.
Химиопрепараты вводят внутривенно и в спинномозговую жидкость (это нужно для профилактики или лечения поражений головного мозга).
После того как отмечается стойкая положительная динамика, химиопрепараты продолжают вводить для закрепления эффекта и предотвращения рецидива.
Сопроводительное лечение дополняет химиотерапию, помогает бороться с симптомами, улучшить состояние больного, восстановить жизненно важные функции.
*Вся информация о препаратах и дозировках представлена исключительно в ознакомительных целях. Самолечение недопустимо.
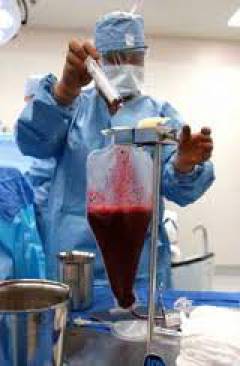
Трансплантация костного мозга может быть назначена больным с неблагоприятным прогнозом и тем, у кого произошел рецидив.
Во время подготовки к трансплантации проводят обследование больного, подбирают подходящего донора.
Красный костный мозг получают от донора под общим наркозом. Делают несколько пункций крыла подвздошной кости, во время которых при помощи шприца набирают костномозговую ткань.
Больному красный костный мозг вводят внутривенно. Перед этим проводят курс химиотерапии, во время которого стараются максимально уничтожить злокачественные клетки.
После введения трансплантата должно пройти некоторое время для того, чтобы клетки донора осели в красном костном мозге больного и прижились там. В это время у пациента сильно ослаблен иммунитет, имеется повышенный риск развития инфекции, кровотечения. Врач должен постоянно контролировать состояние больного.
Течение острого лимфолейкоза. Прогноз.
Острый лимфолейкоз обычно имеет более благоприятный прогноз по сравнению с другими видами острых лейкозов. В зависимости от вида и тяжести течения заболевания, 40%-80% больных выживают в течение 5 лет. Если во время обследования при этом не обнаруживаются патологические изменения, то можно говорить о выздоровлении.
У детей прогноз более благоприятный.
Стадии острого лимфолейкоза:
- Первая атака. Так условно называют стадию, во время которой пациент впервые обратился к врачу, были обнаружены изменения в анализах крови, проведено исследование и впервые установлен диагноз.
- Ремиссия. Улучшение состояния и положительная динамика анализов в ходе лечения. Если ремиссия продолжается более 5 лет – диагностируется выздоровление.
- Рецидив – повторное возникновение симптомов лейкоза и изменений в анализах после ремиссии.
- Резистентность. Состояние, когда проведено два курса химиотерапии, но положительных сдвигов нет.
- Ранняя смертность. Наиболее неблагоприятный вариант течения острого лимфобластного лейкоза, когда больной погибает во время первого или второго курса химиотерапии.
Факторы, которые влияют на прогноз:
- Количество лейкоцитов в крови. Чем оно выше, тем хуже прогноз. Если их более 100*10 9 /л, то прогноз крайне неблагоприятен.
- Возраст больного. Дети в возрасте 2-6 лет имеют самые высокие шансы на выздоровление. В возрасте 55-60 лет шансы самые низкие.
- Содержание лактатдегидрогеназы (ЛДГ) в крови. Чем оно выше, тем хуже прогноз. При показателях более 1000 ЕД/л прогноз крайне неблагоприятен.
Читайте также:
- Санаторно-курортное лечение при раке щитовидной железы
- Неоперабельная опухоль печени лечение
- Лечение лейкоза в астане
- Нейрохирург лечение кисты головного мозга
- Рак шейки матки лечение в белоруссии

