Препараты лечения онкологии костей

Метастазы в костях являются одним из самых частых клинических проявлений злокачественного опухолевого процесса и свидетельствует о четвертой стадии онкологического заболевания, что в целом ухудшает прогноз жизни.
Метастазы в кости могут определяться при многих онкологических заболеваниях, но наиболее часто они диагностируются при раке:
- молочной железы;
- предстательной железы ;
- легких;
- щитовидной железы;
- почек;
- миеломной болезни;
- при опухолях желудочно-кишечного тракта;
- при опухолях гепато-биллиарной системы (печени, желчевыводящих протоков).

При диагностике опухолевого поражения костей чаще всего выявляются вторичные изменения в позвоночнике, метастазы в тазовых костях, а также метастазы в ребрах, в трубчатых костях конечностей и метастазы в кости черепа.
Развитие и рост костных метастазов
Метастазы рака в кости характеризуются поражением костной ткани раковыми клетками, которые проникают в нее с током крови и лимфы из первичной опухоли. Кроме того, эти раковые клетки могут распространяться в другие органы и ткани, формируя в них метастазы. Поскольку кости выполняют важнейшую для организма опорно-двигательную функцию, их поражение негативно влияет на качество и прогноз жизни пациента.
Основными клетками костной ткани являются остеобласты, ответственные за образование новых клеток и рост кости, и остеокласты, отвечающие за разрушение и поглощение отработавших костных клеток.

При поражении костей метастазами нарушаются функции вышеуказанных клеток, в связи с чем, метастазы в кости в зависимости от типа поражения делятся на:
- остеолитические: при поражении остеокластов происходит истончение костной ткани, приводящее к патологическим переломами при нагрузках. При прогрессировании заболевания эти признаки могут появляться даже при малейшей нагрузке (например, при вставании с постели, при попытке сделать шаг и т.д.).
- остеобластические: при поражении остеобластов диагностируется патологическое увеличение костной ткани, образование наростов и выпячиваний на кости, ограничение подвижности суставов.
- смешанные: поражение остеобластов и остеокластов. Обнаруживаются наиболее часто у больных с метастазами в кости и проявляются истончением кости и появлением новых метастазов.
Симптоматика и характерные признаки
При небольшой площади поражения костной ткани у онкологических больных метастазы в кости клинически могут никак себя не проявлять. При отсутствии противоопухолевого лечения метастазы в кости растут, увеличиваясь в размерах и количестве. Это сопровождается появлением и, впоследствии, прогрессирующим усилением определенных признаков:
Все вышеуказанные симптомы у онкологических больных могут быть выражены по – разному, в зависимости от объема поражения костной ткани и эффективности проводимого лечения.

Диагностика метастазов в костях
Для диагностики метастазов в кости применяется ряд инструментальных методов обследования, которые можно при определенных показаниях комбинировать друг с другом, что повышает их диагностическую точность:
- Сцинтиграфия скелета основывается на накоплении раковыми клетками радиофармпрепарата (радиоактивный изотоп), который вводится внутривенно за некоторое время до исследования. Изотоп с током крови разносится по костной ткани и там, где есть метастазы в кости он поглощается опухолевыми клетками и накапливается. Сцинтиграфия скелета часто используется на первом этапе диагностики метастазов в кости.
- Рентгенография костей используется в основном как дополнительный метод дифференциальной диагностики метастазов в костях.
- Компьютерная томография является высокоинформативным методом обследования, в связи с чем широко применяется для подтверждения метастазов в кости.
- Магнитно-резонансная томография также является высокоинформативным и дорогостоящим методом обследования, помогающим в трудных клинических ситуациях оценить степень поражения костной ткани, распространение опухоли на окружающие мягкие ткани, сосуды, нервы.
- Биохимический анализ крови при метастазах в кости отражает повышенный уровень кальция в крови, повышение щелочной фосфатазы. Однако, выраженность этих нарушений в анализах крови определяется степенью костного поражения.
- Биопсия кости является самым точным методом диагностики, позволяющим определить морфологическое строение опухоли. Для верификации метастазов в кости может быть использовано как цитологическое, так и гистологическое исследование биоптата. В спорных случаях с целью верификации диагноза (когда неизвестна локализация первичной опухоли) биоматериал может быть направлен на иммуногистохимическое исследование для определения тканевой принадлежности.

Выбор метода определения метастазов в костях должен осуществляться по определенным диагностическим стандартам квалифицированным специалистом, обязательно в соответствии с клинической ситуацией и может варьировать у разных больных с одинаковым диагнозом.
Цели и методы терапии
Известно, что наличие метастатического поражения скелета повышает стадию онкопатологии, может ухудшить прогноз и качество жизни пациентов. Но, тем не менее, метастазы в кости поддаются лечению и при правильно подобранной и своевременной терапии можно достичь длительной выживаемости и улучшения качества жизни этой категории больных, что является главной целью онкологов. Для достижения этой цели необходимо:
- Уменьшить болевые ощущения за счет правильно подобранного обезболивания;
- Уменьшить размеры и количество метастазов в костях;
- Предотвратить осложнения, вызванные метастазами в кости, такие как, патологический перелом, компрессионный синдром;
- Уменьшить или предотвратить интоксикацию больного.
Лечение метастазов в кости проводится в комплексе с основным противоопухолевым лечением.
Методы лечения метастазов в кости:
- Лекарственный метод основан на применении бисфосфонатов, которые способствуют восстановлению костной ткани.
- Лучевая терапия направлена на разрушение опухолевых клеток, остановку их роста и деления. Она может осуществляться с помощью дистанционной лучевой терапии, стереотаксической лучевой терапии или сочетанием этих методов.
Кроме того, может быть назначено обезболивание, коррекция сопутствующей патологии, профилактика или лечение интоксикации пациента.

Часто больным с метастазами в кости назначается комплексное лечение, включающее все вышеуказанные методы.
Обязательно сочетать лечение метастазов в кости с основным лечением, это способствует увеличению продолжительности жизни.
Лечиться народными средствами не рекомендуется, поскольку это приведет к скорым осложнениям, ухудшению самочувствия и, самое главное, к прогрессированию болезни и потере бесценного времени жизни.
Прогноз и длительность жизни
Как уже говорилось выше, больные с метастазами рака в кости имеют IV стадию заболевания. Прогноз и продолжительность жизни этой категории пациентов варьирует в зависимости от многих факторов:
- основного диагноза (морфологического строения опухоли, степени злокачественности и т.д.)
- общего состояния больного и образа жизни;
- сопутствующей патологии и ее коррекции;
- степени распространения опухолевого процесса (размера, локализации и количества метастазов в кости, а также прорастания жизненно важных структур самой опухолью и ее метастазами);
- грамотности подобранного противоопухолевого лечения и его эффективности;
- соблюдения режима лечения и наблюдения и т.д.
Чем раньше диагностировано поражение скелета, тем эффективнее борьба с метастазами. В связи с этим, все пациенты с онкопатологией должны регулярно проходить контрольное обследование (в зависимости от своего диагноза) под наблюдением врача онколога и незамедлительно обращаться за помощью, если в промежутках между обследованиями появились какие-либо жалобы на изменение или ухудшение состояния здоровья.
Для профилактики рака
Говоря о профилактике рака, надо начинать с самого начала, а именно, ответить себе на вопросы:
- Где мы живем?
- Как мы живем?
- Что мы делаем для нашей жизни и здоровья?
В наш век доступной и открытой информации существует множество публикаций, интернет ресурсов о здоровом и правильном образе жизни, питании, отдыхе и т.д., где можно найти ответы на все интересующие нас вопросы. Нужно помнить, что наше здоровье только в наших руках, поэтому очень важно беречь его.

А что мы делаем для этого?
Как узнать, что пора обратиться к врачу, если ничего не беспокоит?
Необходимо проводить регулярные скрининговые обследования, медицинские осмотры.
Выявленный на ранней стадии рак имеет благоприятный прогноз и эффективно поддается лечению. Лечение рака направлено на уничтожение опухолевых клеток, предотвращение их роста и размножения, поэтому, чаще всего, для лечения онкопатологии используют комплекс мероприятий: хирургическое лечение, лекарственное лечение (химиотерапия, гормонотерапия, иммунотерапия), лучевую терапию. Такое комплексное лечение позволяет снизить риск возврата болезни (местного рецидива, прогрессирования), увеличивает продолжительность жизни и улучшает ее качество.
Цена, руб.
- О центре
- Специалисты
- Новости
- Партнеры
- Отзывы
- Запись на приём
- Стоимость лечения
- Консультация
- Диагностика
- FAQ
- Статьи
- Аппарат Кибернож
- Уникальность системы
- Показания к лечению
- Противопоказания
- Как происходит лечение
- Сравнение методов
- Дистанционная
- Комбинированное лечение
- Лечение
- Опухоли головного мозга
- Рак легкого
- Рак печени
- Рак почки
- Рак предстательной железы
- Рак носоглотки
- Опухоль спинного мозга
- Опухоль ЦНС у детей
- Рак поджелудочной железы
- Опухолевое поражение костей
- Метастазы
- Невралгия тройничного нерва
- Пяточная шпора
Выбор тактики лечения и прогноз определяются типом рака кости, который диагностирован у пациента, и некоторыми другими факторами.
Разновидности рака костей
Остеосаркома — наиболее распространенная разновидность первичного рака костей. Чаще всего встречается в возрасте 10–30 лет, как правило, возникает в костях рук и ног, таза. Мужчины болеют чаще по сравнению с женщинами. Менее 10% случаев остеосаркомы приходится на людей старше 60 лет.
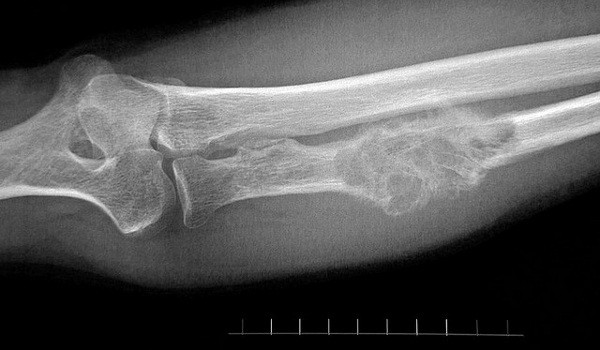
Хондросаркомы происходят из хрящевой ткани, это второй по распространенности тип первичного рака костей. Молодые люди до 20 лет болеют очень редко. С 20 до 75 лет риск возникновения хондросаркомы постепенно нарастает, мужчины и женщины болеют примерно одинаково часто. Хондросаркомы могут возникать в костях рук и ног, таза, черепа, в лопатке. Они могут начать расти и во внутренних органах, в которых присутствует хрящевая ткань, например, в гортани, трахее.
Саркома Юинга — третий по распространенности тип рака костей. Поражает детей, подростков, молодых людей. После 30 лет заболевание встречается крайне редко. Чаще всего опухоль локализуется в костях таза, нижних и верхних конечностях, лопатках, ребрах.
Злокачественная фиброзная гистиоцитома обычно локализуется в мягких тканях, в редких случаях — в костях. Заболевание преимущественно встречается в среднем и пожилом возрасте. При костной локализации чаще всего поражаются кости ног в области колена. Злокачественная фиброзная гистиоцитома склонна к локальному росту, но иногда может давать метастазы, например, в легких.
Фибросаркома также чаще встречается в мягких тканях. У людей среднего и пожилого возраста может поражать кости рук, ног.
Хордома — опухоль, которая чаще всего находится в основании черепа или позвоночном столбе. Обычно диагностируется после 30 лет, у мужчин примерно вдвое чаще, чем у женщин. Хондромы склонны к медленному локальному росту, в редких случаях дают метастазы в лимфатические узлы, печень.
Лечение рака костей
Лечением пациента со злокачественной опухолью костной ткани занимается команда врачей, в которую могут входить: онколог, хирург, специализирующийся в сфере ортопедии, химиотерапевт, врач лучевой терапии, ортопед, реабилитолог, психоонколог.
Хирургическое лечение рака костной ткани
Хирургия — основной радикальный метод лечения рака костей. В прошлом у большинства пациентов прибегали к ампутации — удалению всей конечности или ее части, пораженной опухолью. В настоящее время хирурги стараются отдавать предпочтение органосохраняющим вмешательствам. Удаленную часть кости заменяют костным трансплантатом или эндопротезом из металла, других материалов. Если приходится удалять фрагмент бедренной или плечевой кости, нижележащую часть конечности можно сохранить. При этом рука или нога станет короче, но сможет ограниченно выполнять свои функции.
Иногда в качестве альтернативы хирургическому вмешательству применяют криодеструкцию (разрушение опухолевой ткани низкой температурой), кюретаж (выскабливание специальным инструментом), введение в отверстие в кости цемента из полиметилметакрилата (при затвердевании он нагревается и разрушает опухолевые клетки).
Лучевая терапия при раке костей
Для того чтобы уничтожить опухолевые клетки в кости, требуются высокие дозы излучения, которые приводят к серьезным побочным эффектам. Поэтому лучевая терапия при раке костей находит ограниченное применение:
- Если опухоль невозможно полностью удалить хирургически.
- При положительном крае резекции по данным биопсии после операции.
- В качестве паллиативного метода лечения при рецидиве, чтобы уменьшить боль и отек.
Наиболее широкое применение лучевая терапия находит при саркомах Юинга.

Химиотерапия при раке костей
Химиотерапию чаще всего применяют для лечения остеосарком и сарком Юинга. Другие виды рака костей реагируют на нее плохо. Применяют различные химиопрепараты: цисплатин, доксорубицин, ифосфамид, этопозид, метотрексат, циклофосфамид, винкристин.
Иногда применяют таргетные препараты — лекарственные вещества, которые блокируют молекулы, необходимые для роста и выживания злокачественных опухолей.
Лечение при метастазах рака в костях
При лечении метастазов в костной ткани используют химиопрепараты, которые эффективны против первичной опухоли. Применяют лучевую терапию. Если метастатические очаги приводят к значительному разрушению костной ткани, назначают бисфосфонаты. Эти препараты вводят внутривенно каждые 3–4 недели, они помогают предотвратить патологические переломы, уменьшить боль, снизить уровень кальция в крови.

Хирургическое лечение носит паллиативный характер. При патологических переломах кости укрепляют с помощью винтов, стержней и других металлических конструкций. Иногда прибегают к радиочастотной аблации: в опухоль вводят иглу и подают на нее ток высокой частоты, который разрушает опухолевые клетки.
Реабилитация после лечения рака костей
После ампутации конечности показано протезирование. При правильно спланированных реабилитационных мероприятиях пациенты, перенесшие ампутацию нижней конечности, обычно могут снова ходить спустя 3–6 месяцев.
После органосохраняющих операций реабилитационный период продолжается дольше. Способность ходить восстанавливается примерно через год. Если не проводить реабилитационное лечение, возникает стойкая утрата функции конечности. При инфицировании, смещении или разрушении эндопротеза требуется повторное хирургическое вмешательство. Некоторым пациентам в последующем приходится выполнять ампутацию.
После наступления ремиссии и завершения лечения пациент должен находиться под наблюдением врача. При возникновении любых симптомов нужно посетить клинику и пройти обследование. Это помогает вовремя диагностировать рецидив рака в кости, метастазов в других органах.
Прогноз выживаемости
На прогноз влияют такие факторы, как тип и стадия рака кости, локализация и размер опухоли, возраст пациента. В среднем пятилетняя выживаемость (процент пациентов, которые остаются живы в течение 5 лет с момента диагностики заболевания) при всех типах злокачественных опухолей костей составляет 70%.
Стадии рака костей
Выделяют 4 стадии развития опухолей кости:
- 1 стадия: опухоль ограничена костью, не прорастает в соседние ткани, не распространяется в лимфатические узлы, отдаленные метастазы отсутствуют. Опухоль является высокодифференцированной и отличается низкой степенью агрессивности.
- 2 стадия: опухоль также ограничена костью, не прорастает в соседние ткани, но является низкодифференцированной (опухолевая ткань практически утратила черты нормальной ткани) и более агрессивной.
- 3 стадия: в кости имеется 2–3 очага, они могут быть высоко- или низкодифференцированными.
- 4 стадия: опухоль, которая распространилась за пределы кости в другие органы и ткани.

Причины и факторы риска рака костей
Точные причины возникновения злокачественных опухолей костей неизвестны. Некоторые факторы риска повышают вероятность развития заболевания:
- Остеосаркомы чаще диагностируют у людей, которые перенесли курс лучевой терапии и/или химиотерапии по поводу других типов рака.
- Риски остеосаркомы повышает применение металлических фиксирующих устройств (скоб, спиц, пластин, винтов) при переломах костей.
- Играют роль некоторые наследственные заболевания: наследственная ретинобластома (редкая злокачественная опухоль глаза), синдром Ли-Фраумени.
- У пожилых людей возникновению рака костей может предшествовать Болезнь Педжета — заболевание, при котором нарушается процесс естественного обновления костной ткани, и кости становятся хрупкими.
Симптомы злокачественных опухолей костей
Зачастую первым проявлением рака костей становится боль. Поначалу она возникает лишь во время сна и физических нагрузок, затем становится постоянной, мучительной. Если пораженный участок кости не прикрыт массивными мышцами и находится близко к коже, опухоль можно увидеть при визуальном осмотре, прощупать. Возникает отек.
Рак разрушает нормальную костную ткань, ослабляет кости, в итоге происходят патологические переломы от небольшого усилия. Во время перелома в кости возникает сильная острая боль. Если опухоль сдавливает нерв, в пораженной части тела появляется онемение, покалывание, слабость мышц (парезы, вплоть до паралича).
Похожие симптомы могут возникать и при других заболеваниях, например, при артритах, остеомиелите, после перенесенных травм. Рак костей встречается редко, но при возникновении болей в костях без видимой причины лучше сразу посетить врача и провериться.
Методы диагностики
Компьютерная томография помогает уточнить размеры, расположение, количество опухолевых очагов, степень прорастания в окружающие ткани, обнаружить метастазы в лимфатических узлах и внутренних органах. По показаниям назначают МРТ: она помогает лучше визуализировать опухоль, оценить состояние мягких тканей, головного и спинного мозга.
В поиске мелких метастазов помогает позитронно-эмиссионная томография. Во время исследования в организм вводят молекулы сахара с радиоактивной меткой. Опухолевые клетки поглощают радиофармпрепарат и становятся видимыми на снимках, выполненных специальным аппаратом.
Наиболее точный метод диагностики онкологических заболеваний — биопсия. Во время исследования получают фрагмент предположительно опухолевой ткани и отправляют в лабораторию для изучения внешнего вида клеток, строения ткани, молекулярно-генетических характеристик. Биопсию можно провести разными способами:
- При тонкоигольной биопсии используют шприц с иглой. Если кость находится глубоко, скрыта мышцами, процедуру проводят под контролем компьютерной томографии.
- При трепан-биопсии используют толстую иглу диаметром примерно полтора миллиметра. Считается, что этот метод лучше, чем тонкоигольная биопсия, он позволяет установить более точный диагноз.
- Иногда для исследования нужен большой фрагмент кости. В таких случаях проводят эксцизионную или инцизионную биопсию: выполняют хирургическое вмешательство, удаляют всю опухоль или ее часть.
Процесс лечения онкологических заболеваний очень долгий и сложный. Единого лекарства против рака пока не существует, но комбинация различных препаратов при онкологии позволяет добиться торможения роста опухоли, снятия болевого синдрома и общего улучшения состояния пациента.
Роль лекарственных препаратов в терапии онкозаболеваний
Современные препараты при лечении рака решают несколько задач, потому и назначаются они чаще всего комплексно. Одни лекарства от рака разрушают пораженные клетки, другие останавливают их рост и предотвращают возникновение новых раковых клеток. На поздних стадиях активно применяются обезболивающие препараты, а также средства, которые сами по себе никак не влияют на рост опухоли, но улучшают общее состояние человека, снимая неприятную симптоматику.
Химиотерапия — высокотехнологичный и эффективный способ лечения онкологических заболеваний, пусть и не лишенный недостатков. Препараты для химиотерапии подавляют рост раковых клеток или уничтожают их, однако многие их них воздействуют также и на здоровые клетки. Из-за этого химиотерапия переносится тяжело, а пациенты после каждого курса нуждаются в реабилитации. Побочными эффектами препаратов для химиотерапии являются рвота и тошнота, выпадение волос, снижение массы тела, ухудшение иммунитета, постоянное чувство усталости, нарушение свертываемости крови.
Специалисты различают цитостатическую и цитотоксическую химиотерапию. Они различаются по механизму воздействия на клетки. Цитостатические препараты замедляют размножение клеток опухоли. Цитотоксические убивают пораженные клетки, вследствие чего начинается некроз опухоли.
К препаратам для химиотерапии относятся следующие группы средств:
- Алкилирующие агенты . Эти лекарства против рака разрушают белки, ответственные за формирование ДНК раковых клеток. Самые распространенные препараты этой группы — средства на основе действующего вещества циклофосфамид.
- Препараты платины. Этот благородный металл токсичен. Препараты платины обладают тем же действием, что и алкилирующие агенты, а именно — разрушают ДНК раковых клеток. Цитостатические средства алкилирующего типа действия широко используются для лечения рака.
- Антиметаболиты. Они воздействуют на генетический аппарат клетки, убивая ее при делении. Наиболее известными антиметаболитами являются препараты на основе гемцитабина.
- Антрациклины. Эти препараты образуют свободные радикалы, повреждающие ДНК больных клеток. Самые известные представители группы антрациклинов — средства с действующим веществом даунорубицин.
- Таксаны нарушают процесс деления раковых клеток. Препараты на основе паклитаксела — самые распространенные в этой группе.
- Винкалкалоиды разрушают цитоскелет раковых клеток, что приводит к их гибели. Относятся к мягким средствам химиотерапии, так как раковые клетки гораздо более чувствительны к воздействию этого препарата, чем здоровые. В этой группе выделяют средства с действующими веществами винбластин и винкристин.
При лечении многих видов опухолей хорошие результаты дает применение гормональных препаратов. Они наиболее эффективны при лечении гормонозависимых опухолей — рака молочной железы, матки, простаты, а также при опухолях поджелудочной железы, почек, при меланомах.
Эстрогенсодержащие препараты назначаются для подавления андрогенов (например, при раке простаты), а андрогенсодержащие, наоборот, подавляют выделение эстрогенов. Препараты последней группы назначают при таких видах онкологии, как рак молочной железы и т.д.
Несмотря на эффективность, у гормональных препаратов много минусов — они способны ослаблять действие химиотерапевтических препаратов, при долгом лечении у многих больных вырабатывается резистентность к подобным средствам.
Некоторые виды рака развиваются вследствие деятельности вирусов (например, вируса папилломы человека). Кроме того, организм, ослабленный агрессивной химиотерапией, подчас не может самостоятельно защитить себя от вирусных инфекций. Именно поэтому в комплексной терапии рака используются и противовирусные лекарства, в частности — препараты на основе тилорона и их аналоги.
К ферментам относятся активные белковые соединения, которые способны разрушать аминокислоты, необходимые для роста клеток опухоли. Для лечения опухолей применяют аргиназу, аспаргиназу и некоторые другие ферменты. Эффективность такой терапии под вопросом, так как резистентность вырабатывается очень быстро: человеческая иммунная система начинает вырабатывать антитела к ним. Однако исследования показывают, что ферментотерапия значительно смягчает последствия химиотерапии.
При лечении рака большое внимание уделяется не только воздействию на саму опухоль, но и улучшению качества жизни пациента, в частности — борьбе с болью. Чаще всего боль вызывается ростом опухоли, но иногда болевой синдром — побочный эффект некоторых лекарств от рака.
Выбор обезболивающих препаратов зависит от стадии болезни. ВОЗ разработала трехступенчатую схему, которая предполагает переход ненаркотических анальгетиков к слабым опиатам, а затем — к сильным опиатам. Эта схема позволяет добиться заметного улучшения состояния у 9 из 10 пациентов.
- Адъювантные средства . Эти лекарства не являются обезболивающими в строгом смысле слова, однако они уменьшают побочные эффекты сильных опиоидов и усиливают их болеутоляющее действие (к примеру, клонидин). Определенный эффект дают и антидепрессанты.
- Ненарктотические анальгетики . Это первый шаг в снятии болевого синдрома при онкологических заболеваниях. Для этих целей применяются препараты на основе парацетамола, а также нестероидные противовоспалительные препараты (ибупрофен).
- Слабые опиаты . К этим средствам относятся кодеин, трамадол и некоторые другие. Это сильнодействующие препараты, которые тем не менее отличаются хорошей переносимостью. Они дают особенно заметный эффект в сочетании с ненаркотическими анальгетиками.
- Сильные опиаты . В случаях, когда боль становится слишком сильной и иные средства не помогают, врач назначает сильные опиаты на основе морфина, фентанила и т.д. Они воздействуют напрямую на ЦНС, подавляя нервные импульсы.
Онкологические заболевания распространены очень широко, количество больных раком увеличивается с каждым годом, причем врачи отмечают, что рак молодеет — все чаще этот диагноз ставится людям, не достигшим и 40 лет. Все это делает исследования в области разработки новых препаратов от рака приоритетом для международного фармацевтического сообщества. Исследования проводятся постоянно, и уже есть определенные результаты.
Возможно, уже через несколько лет подобные вакцины станут доступными, а таргетная терапия разовьется достаточно, чтобы полностью заменить химиотерапию. Однако пока эти направления являются экспериментальными.

Существует много разновидностей первичных злокачественных опухолей кости: остеосаркома, хондросаркома, саркома Юинга, злокачественная фиброзная гистиоцитома, фибросаркома, гигантоклеточная опухоль, хордома. Но у взрослых такие опухоли диагностируют редко. Намного чаще в костях встречаются метастатические очаги при злокачественных новообразованиях в других органах.

Сергеев Пётр Сергеевич
к.м.н ведущий хирург-онколог, химиотерапевт, зав.отделения онкологии
Методы лечения различаются в зависимости от типа злокачественной опухоли. Здесь мы поговорим об общих принципах и расскажем о том, где можно получить современную помощь в России.
Хирургическое лечение злокачественных опухолей костей
Хирургия – основной метод лечения злокачественных опухолей костей. Врач выбирает объем операции, опираясь на результаты МРТ и биопсии.
Ранее стандартным методом хирургического лечения при раке костей конечностей была ампутация. В настоящее время часто практикуются органосохраняющие операции. К ампутации прибегают, лишь когда не удается сохранить конечность, если в любом случае пришлось бы удалять важные сосуды, нервы и мышцы, что сделало бы пораженную конечность бесполезной.
После любого типа хирургического вмешательства требуется реабилитация. Это даже более сложный этап лечения, чем сама операция. Утраченную конечность замещают протезом, удаленный участок кости – эндопротезом. Обычно восстановительное лечение после органосохраняющих операций занимает больше времени, чем после ампутации. Например, после ампутации ноги многие пациенты могут ходить самостоятельно спустя 3–6 месяцев, а после органосохраняющего вмешательства – в среднем через год.
При раке тазовых костей и нижней челюсти опухоль удаляют, захватывая участок окружающей здоровой ткани, утраченная часть кости может быть замещена трансплантатом.
Злокачественную опухоль позвоночника и костей черепа зачастую сложно удалить, потому что рядом находятся жизненно важные структуры. В таких случаях прибегают к специальным хирургическим методам:
- Выскабливание пораженного участка кости.
- Криохирургия – уничтожение опухолевых клеток низкой температурой с помощью жидкого азота.
- Костный цемент на основе полиметилметакрилата помогает закрыть отверстие, которое осталось после выскабливания и криохирургии, кроме того, при застывании он выделяет тепло, которое уничтожает опухолевые клетки.
Лучевая терапия
Злокачественные опухоли костей непросто уничтожить с помощью облучения. Для этого приходится применять высокие дозы, которые могут повредить соседние органы, сосуды и нервы, поэтому лучевую терапию применяют редко, в основном при саркомах Юинга, которые, как правило, встречаются у людей младше 30 лет.
Лучевая терапия при опухолях костей может преследовать одну из трех целей:
- Борьба с новообразованиями, которые не могут быть удалены хирургически.
- В качестве адъювантного лечения, если по результатам биопсии после хирургического вмешательства получен позитивный край резекции.
- При рецидиве, для того чтобы уменьшить боль и отек.
Как правило, при злокачественных опухолях костей применяют интенсивно-модулированную лучевую терапию. Эта методика позволяет добиться максимального соответствия формы излучения форме злокачественной опухоли и избежать повреждения окружающих здоровых тканей. Иногда применяют протонную терапию, но она доступна только в специализированных центрах, так как требует сложного, дорогостоящего и очень массивного оборудования.
Химиотерапия
Химиопрепараты применяют при остеосаркомах, саркомах Юинга и определенных типах хондросаркомы. Другие злокачественные опухоли костей не очень чувствительны к химиотерапии. Этот вид лечения главным образом применяют в случаях, когда имеются отдаленные метастазы.
Обычно врачи назначают комбинацию 2–3 химиопрепаратов, таких как: цисплатин, доксорубицин, ифосфамид, этопозид, метотрексат, циклофосфамид, винкристин.
Таргетная терапия
В настоящее время при злокачественных опухолях костей в мировой практике есть опыт применения двух таргетных препаратов:
- Иматиниб применяют для лечения запущенных и рецидивировавших хордом. Препарат блокирует сигнальные молекулы, которые активируют размножение опухолевых клеток, на фоне его применения опухоль перестает расти или даже сокращается в размерах. Иматиниб принимают в виде таблеток один раз в сутки.
- Деносумаб используют для лечения неоперабельных и рецидивировавших гигантоклеточных опухолей. Препарат представляет собоймоноклональное антитело, которое ингибируетRANK-лиганд – белок, активирующий разрушение кости остеокластами. Деносумаб вводят подкожно. В течение нескольких месяцев он помогает уменьшить размеры опухоли.
Иммунотерапия
Иногда при гигантоклеточных опухолях применяют интерферон. Препарат можно вводить подкожно, внутримышечно или внутривенно.
Прогноз выживаемости
Средняя пятилетняя выживаемость для всех типов злокачественных опухолей костей у детей и взрослых составляет 70%. Это достаточно неплохой показатель. Можно сказать, что зачастую опухоли костей успешно лечатся. Конечно, большую роль играют такие факторы, как тип опухоли, стадия, степень злокачественности.
Центр Комплексной Медицины сотрудничает с лучшими онкологическими клиниками Москвы, мы знаем, где можно получить наилучшее лечение:
Читайте также:

