Осложнения хирургического лечения опухолей

Все это обосновывает проведение анализа возникающих осложнений при резекции опухолей спинного мозга и побудительной основой для разработки более щадящих методов их удаления и, возможно, изменения тактики лечения и, в конечном счете, для уменьшения частоты их развития [1, 5, 6, 9].
Цель работы. Изучить характер, структуру и частоту осложнений, возникающих после удаления опухолей спинного мозга.
Материалы и методы исследования
Всего за последние 13 лет (2000-2012 г.г.) в клинике нейрохирургии Новосибирского НИИТО получили хирургическое лечение 467 больных с опухолями спинного мозга, из них 356 человек имели экстрамедуллярные опухоли и 111 – интрамедуллярные новообразования. Использованы клинические, неврологические электрофизиологические (интраоперационный контроль ССВП), радиологические (МСКТ, МР-визуализация, в том числе, с контрастными методиками и сосудистыми программами, рентгенологические), лабораторные методы диагностики.
Результаты исследования и их обсуждение
Все возникшие осложнения после удаления опухолей спинного мозга классифицированы нами следующим образом:
1. По времени возникновения:
А. Интраоперационные осложнения.
Б. Ранние – до 1 месяца с момента проведения операции.
В. Поздние – спустя 1 месяц после оперативного вмешательства.
2. Осложнения со стороны спинного мозга:
А. Неврологические нарушения.
Б. Отек спинного мозга.
3. Осложнения неинфекционного характера области хирургического вмешательства:
А. Послеоперационная ликворея.
В. Гематомы позвоночного канала в зоне оперативного вмешательства.
С. Формирование ликворных кист в эпидуральном и межмышечном пространстве (псевдомиелорадикулоцелле).
4. Осложнения области хирургического вмешательства инфекционного характера:
А. Поверхностная инфекция разреза.
Б. Глубокая инфекция разреза.
5. Гнойные инфекционные осложнения со стороны центральной нервной системы
А. Гнойные менингиты.
Б. Гнойные миелиты.
В. Гнойные менинго-энцефалиты.
6. Экстрамедуллярные осложнения:
А. Воздушная венозная эмболия.
Б. Тромбэмболия легочной артерии.
В. Назокоминальная пневмония.
Г. Трофические нарушения (пролежни).
Е. Инфекция мочевыделительной системы.
И. Парез кишечника
7. Осложнения со стороны позвоночника (ортопедические осложнения):
В. Функциональная нестабильность.
Основное количество осложнений после резекции первичных опухолей спинного мозга развилось в раннем послеоперационном периоде, частота их встречаемости составила 34,3 % (160 случаев). Из них основное количество (n = 154) носило легкий характер и лишь 6 (1,3 %) явились причиной летального исхода.
В позднем послеоперационном периоде встречались два вида осложнений – формирования ликворных кист в эпидуральном и межмышечном пространстве (пссевдомиелорадикулоцелле) и различные деформации позвоночника. Они диагностированы у 48 (10,3 %) оперированных.
Осложнения со стороны спинного мозга. Проведен анализ неврологических нарушений, возникающих после удаления первичных новообразований спинного мозга у 234 человек (6 детей – 2,6 %, 228 взрослых – 97,4 %). 89 (38 %) имели интрамедуллярные, 145 (97,4 %) – экстрамедуллярные опухоли. Для оценки возникающих после операции нарушений функции спинного мозга исследовался в динамике неврологический статус пациента и его функциональное состояние по Евзикову Г.Ю. (2002) и по шкале Mc-Cormick P.C. (1990).
Как при экстра, так и интрамедуллярных новообразованиях развитие неврологических осложнений в послеоперационном периоде зависели в первую очередь от исходного функционального состояния больного, локализации, гистологической структуры опухоли и степени поражения спинного мозга. Наиболее часто эти осложнения развивались у больных с опухолью злокачественного характера в шейном отделе спинного мозга с исходно выраженным неврологическим дефицитом. Наибольшее и статистически достоверное количество неудовлетворительных функциональных результатов получено у пациентов в фазе частичного и полного поперечного поражения спинного мозга, по сравнению с ирритативной фазой заболевания. Частота неудовлетворительных функциональных исходов операций у пациентов старше 60 лет была также статистически достоверно выше. У больных после удаления экстрамедуллярных опухолей грубые неврологические нарушения в раннем послеоперационном периоде составили 5,9 %. Большая часть возникающей вновь и углубляющейся после операции неврологической симптоматики носит обратимый характер.
У пациентов с интрамедуллярными опухолями уже через 6 месяцев после проведенной операции у достоверно меньшего количества больных определяются чувствительные расстройства (F = 1,75), а через 1 и 3 года достоверность этих различий возрастает еще больше (F = 2,45; F = 2,01) – рис. 2, А. У этой группы оперированных через 6 месяцев и 1 год после хирургического лечения, по сравнению с дооперационным уровнем и перед выпиской, отмечался статистически достоверный регресс двигательных расстройств у большего числа пациентов (F = 1,67; F = 2,53) – рис. 1.
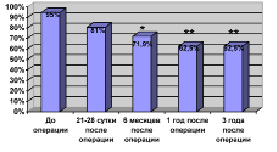
Рис. 1. Динамика двигательных нарушений у больных с ИМО. Примечание: * – различия достоверны
У них же через 1 год после хирургического лечения пациенты 2 и 3 функциональных классов по шкале Mc-Cormick P.C. (1990 г.) встречались достоверно чаще – 41,8 % – F = 2,47 и 28,6 % случаев – F = 1,98. Риск развития серьезных необратимых неврологических осложнений после радикального удаления интрамедуллярных опухолей в нашей серии составил 9 %. Большая часть возникающей в послеоперационном периоде неврологической симптоматики является обратимой.
Имеющийся отек спинного мозга после удаления опухолей на верхне-шейном уровне нередко прогрессирует, что значительно усугубляет клиническую картину заболевания и осложняет течение послеоперационного периода. Клиническое его прогрессирование проявляется появлением на 2-5 сутки бульбарных симптомов в виде нарушения глотания, а затем расстройствами сознания больного вплоть до комы. Восходящий отек спинного мозга у наших больных с опухолями шейного отдела диагностирован у 3 человек (0,6 %).
Неинфекционные осложнения области хирургического вмешательства. Осложнения неинфекционного характера наблюдались в раннем и позднем после операционном периоде у 31 больного, что составило 6,6 %. Из них наиболее часто встречалась послеоперационная ликворея. Она диагностирована в 6 % случаев (у 28 из 467 больных) от общего числа всех больных с опухолями спинного мозга. Это потребовало установки больным наружного люмбального дренажа на 7-11 суток и наложения на кожу в зоне ликвореи дополнительных герметизирующих швов. Такая тактика позволила без дополнительного оперативного вмешательства купировать возникшие осложнения. Ранее проведенная лучевая терапия на область частично удаленной опухоли значительно повышает риск развития послеоперационной ликвореи. Так, например, из 6 больных, оперированных нами повторно в связи с продолженным ростом экстра-интрамедуллярных опухолей и ранее проведенной лучевой терапией, у 2 (33 %) она развилась в раннем послеоперационном периоде
У 1 (0,2 %) человека в зоне оперативного вмешательства диагностирована клинически и по данным МРТ спинного мозга эпидуральная гематома, вызывающая компрессию спинного мозга. Проведенная операция, направленная на удаление гематомы привела к регрессу вновь возникшей неврологической симптоматики.
Формирование ликворных кист в эпидуральном и межмышечном пространстве (пссевдомиелорадикулоцелле) в большинстве случаев происходило у больных с послеоперационной упорной ликвореей. Данный вид осложнений отмечен в позднем послеоперационном периоде у больных в результате не герметичности твердой мозговой оболочки в зоне оперативного вмешательства у 11 больных (2,3 %).
Размер псевдомиелорадикулоцелле колебался от небольших до значительных размеров (от 25 до 150 мл). Ни у одного больного они не вызывали сдавление спинного мозга и не усугубляли неврологическую симптоматику. Но у 3 из 11 явились причиной развития поздней ликвореи, которая купирована нами хирургическим путем. Всем им проведена пластика ликворного свища путем герметизации ТМО гомотрасплантатом с использованием медицинского клея, тахокомба и послойного ушивания мягких тканей с установкой наружнего эндолюмбального катетера на срок 10-12 дней (рис. 2).
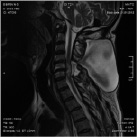
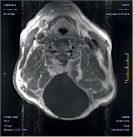
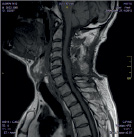
Рис. 2. МРТ спинного мозга больной с псевдомиелорадикулдоцелле: А, Б – до операции. В – послеоперационный МРТ контроль
Инфекционные осложнения области хирургического вмешательства. Осложнения подобного характера встретились у 9 оперированных – в 1,9 % случаев. Инфекционные осложнения области хирургического вмешательства в виде поверхностного либо глубокого нагноения послеоперационной раны возникли у 7 больных, что составило 1,5 % от всех оперируемых больных. Поверхностные нагноения купированы путем предварительной местной санации ран, а затем наложением вторичных швов на кожу. Глубокое нагноение операционной раны возникло у 1 человека (0,2 %). Оно потребовало раскрытие и санацию раны до твердой мозговой оболочки с эвакуацией нагноившейся гематомы и наложением вторичных швов.
Инфекционные осложнения со стороны центральной нервной системы в виде гнойного менингита отмечено у 1 (0,2 %) больного с экстрамедуллярной опухолью. Оно купировано местным и парентеральным введение антибиотиков.
Экстрамедуллярные осложнения. Данные осложнения в нашей серии наблюдений суммарно диагностированы 115 раз. Это связано с тем, что у 20 пациентов их развивалось по 2, а у 15 оперированных – по 3 в виде негрубых нарушений со стороны дыхательной, желудочно-кишечной и мочеиспускательной систем. В итоге 115 осложнений возникло у 65 (13,9 %) человек.
Экстрамедуллярные осложнения были представлены в большинстве своем дисфункцией желудочно-кишечного тракта. Интестинальная недостаточность проявлялась в виде динамической кишечной непроходимости. Она наблюдаются у 9 % пациентов (у 42 из 467). Для устранения динамической кишечной непроходимости использовали метоклопрамид, слабительные средства, гипертонические клизмы с одновременной стимуляцией кишечника прозерином или убретидом. В атонической стадии противопоказано введение газоотводной трубки. По мере восстановления перистальтики стимуляцию с помощью клизм заменяют применением свечей.
На втором месте по частоте встречаемости были назокоминальные инфекции. У больных с опухолями спинного мозга в первую очередь с интрамедуллярными на шейном уровне нередко наблюдаются выраженные нарушения функции дыхания, которые могут усугубляться после операции. Это приводит к ухудшению, а нередко и к выключению грудного дыхания с резким уменьшением легочной вентиляции, ателектазам и на фоне нарушения дренажной функции бронхов к развитию пневмонии. Послеоперационные бронхо-легочные осложнения при хирургическом лечении опухолей спинного мозга относятся к одним из наиболее частых. Частота послеоперационных пневмоний, по данным спинальной клиники Института нейрохирургии им. акад. А.П. Ромоданова, в различные годы колебалась от 7 % до 12 %. По нашим данным частота развития пневмонии составила 4 % (у 18 из 467 больных) и развивалась она только у больных с опухолями шейного отдела спинного мозга с исходным грубым неврологическим дефицитом. Но ни в одном случае данное осложнение не явилось причиной летального исхода.
Наиболее часто трофические нарушения в виде пролежней у наших больных развивались на фоне грубой неврологической симптоматики при поражении интрамедуллярной опухолью шейного отдела спинного мозга. Такие осложнения возникли у 7 больных, что составило 1,5 % от общего числа пациентов. Согласно классификации Когана 4 человека имели поверхностные пролежни в виде мацерации кожных покровов в стадии первичной реакции в области крестца, у 3-х имелись глубокие пролежни в некротической стадии.
Наличие у больных нескольких очагов инфекции в виде пневмонии, пролежней нередко приводит к развитию сепсиса. Из всех оперированных сепсис диагностирован у 3 (0,6 %) человек со злокачественными интрамедуллярными опухолями на шейном уровне на фоне двусторонней пневмонии и пролежней.
Венозная воздушная эмболия (ВВЭ). Частота встречаемости ВВЭ в нашей серии, состоящей из 135 больных с опухолями на уровне шейного и верхне-грудного отделов позвоночника, оперированных сидя, составила 7,4 % (у 10 их 135 больных). Она не носила массивный характер, летальных исходов от развившейся ВВЭ ни в одном случае не было.
Тромбоэмболия легочных артерий (ТЭЛА). В нашей серии больных, несмотря на использование нами отработанной в Институте им. Н.Н. Бурденко комплексной профилактики, ТЭЛА развилась в 1,4 % случаев (7 из 467 человек). При этом причиной летального исхода ТЭЛА явилась у 3 из 467 пациентов, что составило 0,6 %.
Инфекция мочевыводящих путей. У 64,4 % у наших больных, особенно с интрамедуллярными опухолями, уже до операции имелась дисфункция тазовых органов в виде нарушения мочеиспускания (рис. 3). Им проводилась периодическая катетеризация мочевого пузыря. Всем им и больным, у которых не наступало быстрое восстановление самостоятельного мочеиспускания, проводили продолжительную катетеризацию мочевого пузыря катетером Фолея. При восстановлении позывов на мочеиспускания предпочтение отдавали периодической катетеризации. В этой ситуации на фоне сохраняющейся дисфункции мочевого пузыря, несмотря на профилактику циститов, последние в нашей серии больных диагностированы у 25 человек – 5,4 % от общего числа больных.
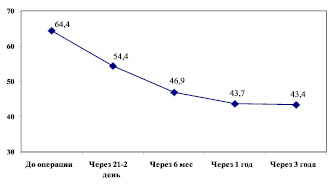
Рис. 3. Нарушения функции тазовых органов у больных с интрамедуллярными опухолями в динамике
Операции по поводу опухолей спинного мозга при сочетании ряда неблагоприятных факторов могут заканчиваться летальным исходом. Всего в представленной нами хирургической серии в раннем послеоперационном периоде умерло 6 из 467 больных, что составило 1,3 %. Причиной летального исхода явились осложнения в виде ТЭЛА (50 %) и восходящий отек спинного мозга (50 %). 3 человека имеющие интрамедуллярные опухоли на верхне-шейном уровне и погибли от восходящего отека на бульбарные отделы ствола головного мозга. У остальных 3-х опухоли локализовались в шейном (1) и у 2-х в грудном отделах позвоночника.
Осложнения со стороны позвоночника (ортопедические осложнения). Деформации позвоночника, как, например, сколиоз или, чаще, кифоз различной степени тяжести наблюдались в нашей хирургической серии больных у 37 из 467 пациентов (8 %). У детей после удаления интрамедуллярной опухоли осложнения в отдаленном послеоперационном периоде в виде сколиотической деформации возникли в 33 % случаев. Все они связаны с проведением расширенной ламинэктомии на шейно-грудном и грудопоясничном уровне, потребовавшейся для удаления распространенных интрамедуллярных опухолей на 5-7 позвонках.
Наши данные совпадают с литературными в том, что гемиламинэктомия, применяющаяся, при небольших, в основном экстрамедуллярных опухолях спинного мозга не подходят для интрамедуллярных опухолей, т.к. необходимо обнажение средней линии спинного мозга. Когда требуется обширная ламинэктомия или ламинотомия, рекомендуется сохранять одну заднюю дужку между каждым пятым или шестым позвонками. Для снижения травматичности операционных доступов к опухолям спинного мозга являются необходимо избегать повреждения межпозвонковых суставов, выполнять остеопластическую ламинотомию у детей с последующей иммобилизацией позвоночника как минимум на 4 месяца. Наряду с этим проводится ортопедический и радиологический контроль до окончания периода роста ребенка и отказ от назначения радиотерапии пациентам с доброкачественными интрамедуллярными опухолями. Ламинотомия проводится нами с использованием ультразвукового аппарата фирмы Misonix.
Для снижения травматичности операционных доступов к опухолям спинного мозга, по нашему мнению, также необходимо использовать микрохирургическую технику в сочетании с разработанными нами технологическими приемами лазерной хирургии на основе применения неодимового лазера. Сочетание данных технологий позволяет уменьшить травматичность операционных доступов и резецировать экстрамедуллярные опухоли только из геми- и интерламинарных доступов с сохранением суставных и остистых отростков позвонков. Наряду с этим, проведение ламинотомии и ламинопластики у взрослых позволяет в отдаленном периоде также уменьшать вероятность развития подобных деформаций.
Хирургическое лечение деформаций позвоночника осуществлялось путем: краниоцервикальной фиксации, проведения межтелового спондилодеза на нескольких уровнях, транспедикулярной и ламинарной фиксации позвоночного столба (рис. 4).
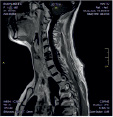
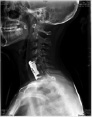
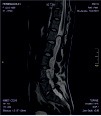
Заключение
Наибольшее количество осложнений после удаления опухолей спинного мозга развивается в раннем послеоперационном периоде (1 месяц с момента проведения операции).
Наиболее грозными осложнениями, часто приводящим в послеоперационном периоде больных к летальным исходам, является восходящий отек спинного мозга, развивающийся в 0,6 % и тромбэмболия легочных артерий, диагностированная в 1,4 % случаев.
Риск развития серьезных необратимых неврологических осложнений после радикального удаления интрамедуллярных опухолей составил 9 %. Грубые неврологические нарушения в раннем послеоперационном периоде после резекции экстрамедуллярных опухолей развиваются в 5,9 %. При этом большая часть возникающей вновь и углубляющейся после операции неврологической симптоматики носит обратимый характер.
Хирургическое лечение опухолей спинного мозга имеет минимальные риски развития общехирургических осложнений и не влияет на клинические результаты лечения больных и летальность.

Можно выделить три основных показания, при которых применяется хирургическое лечение:
При выполнении минимально инвазивных вмешательств хирург создает несколько небольших разрезов (отверстий) вместо одного большого разреза. Это делается для введения в исследуемую полость, например в живот, необходимого оборудования для манипуляций и лапароскопа (тонкая трубка с камерой на конце). Изображение с камеры на лапароскопе передается на специальный монитор при помощи которого хирург может визуально контролировать ход операции и выполнять необходимые манипуляции.
Выполнение таких операций, как правило, менее травматично для организма, следствием чего является более легкий послеоперационный период. Тем не менее, это не всегда возможно, например, по следующим причинам:
Перед тем, как выполнить Вам хирургическое лечение, Ваш лечащий врач должен убедиться, что Ваш организм в состоянии выдержать такое вмешательство, а в случае выявления нарушений – скорректировать их до операции или подготовиться к их развитию в ходе вмешательства или в послеоперационном периоде.
- Общий анализ крови – в ходе него производится подсчет количества форменных элементов (клеток) крови, включая эритроциты и концентрацию гемоглобина, тромбоциты, лейкоциты, кроме того отдельно определяются разновидности лейкоцитов;
- Биохимический анализ крови – определяются основные показатели обмена веществ, например концентрация общего белка и альбумина, глюкозы, показатели, отражающие функцию почек (креатинин, мочевина) и печени (АЛТ, АСТ);
- Коагулограмма – анализ, в ходе которого оценивается функциональное состояние свертывающей системы крови, это важно для того, чтобы выделить пациентов с высоким рисков развития сильного интраоперационного кровотечения;
- Ультразвуковое исследование вен нижних конечностей – для исключения наличия в них бессимптомного тромбоза, который может стать причиной тяжелых осложнений в ходе операции или в послеоперационном периоде;
- Функциональные пробы, включая электрокардиографию (ЭКГ), позволяющую оценить основные параметры сердечной мышцы, спирометрию (функции внешнего дыхания), рентгенография органов грудной клетки или флюорография;
Ваш лечащий врач проинструктирует Вас относительно ограничений в питании и питье перед операцией. Для обеспечения Вашей безопасности в ходе проведения анестезии, Вы не должны ничего есть и пить в день операции и, в некоторых случаях, вечером накануне. Это обусловлено риском развития рвоты во время наркоза, попадание желудочного содержимого в дыхательные пути представляет собой серьезную опасность для жизни. Если вы принимаете какие-либо препараты, разжижающие кровь (дабигатран, ривароксабан, апиксабан, эдоксабан, варфарин), или подавляющие функциональную активность тромбоцитов (аспирин, ацетилсаллициловая кислота и так далее), обезболивающие и противовоспалительные препараты - обязательно сообщите об этом своему лечащему врачу!
Кроме того, Вас могут попросить приобрести некоторые материалы для послеоперационного периода, например такие, как эластические бинты или чулки для нижних конечностей, которые Вы будут носить с целью профилактики развития тромбоза, а также перевязочные материалы, бандаж и так далее.
Непосредственно перед операцией Вас попросят сбрить волосы с места предстоящей операции, это может быть бритье живота и паха, груди или головы и шеи - в зависимости от органа который будет подвергнут операции. Накануне операции с Вами побеседует врач-анестезиолог – специалист по предоперационному обезболиванию и наркозу. В некоторых центрах пациентам вечером перед операцией назначают легкие седативные препараты, чтобы снизить уровень стресса больного. В зависимости от вида выполняемого вмешательства, в первую очередь Вам выполнят необходимое обезболивание в том объеме, который определен анестезиологом. Хирургическое вмешательство вызывает значительные болевые ощущения со стороны организма, поэтому перед его проведением всегда применяются те или иные виды обезболивания (анестезии):
- местная анестезия, при которой блокируются болевые ощущения на небольшом участке, примером является выполнение анестезии при стоматологических операциях. Раствор обезболивающего (анестетика) при этом вводится вблизи зоны планируемой операции;
- регионарная анестезия, при которой подавляется передача болевых импульсов от какой-либо части тела, например, руки или ноги.
- общая анестезия (наркоз).
После удаления опухоли и необходимого объема тканей выполняется послойное зашивание операционной раны (отдельно ушиваются мышцы, подкожно жировая клетчатка и так далее) и начинается послеоперационный период, в ходе которого Вы будете восстанавливаться после проведенного вмешательства. Ваш лечащий врач подробным образом проинструктирует Вас о будущих возможных ограничениях, о том, как правильно ухаживать за послеоперационной раной, возможных признаках инфекции, когда будут сняты швы и так далее.
После выполнения операции выполнятся срочное гистологическое исследование, чтобы убедиться, что удалена вся ткань опухоли – патоморфолог (специалист по патологической анатомии) под микроскопом изучает образцы ткани из края резекции (край удаленной ткани) на предмет отсутствия опухолевых клеток. После этого образцы опухолевой ткани будут специальным образом обработаны и подвергнутся глубокому изучению. Это позволяет более точно определить разновидность удаленной опухоли (это поможет при выработке дальнейшего плана лечения) и распространенность опухолевого процесса. При наличии показаний также проводится иммуногистохимическое исследование в ходе которого, например, можно определить чувствительность опухоли к некоторым лекарственным препаратам.
Если вы планируете обращение за консультацией в другое лечебное учреждение - обязательно возьмите с собой эти блоки и стекла с послеоперационным материалом.
После выполнения оперативного лечения и получения результатов гистологического исследования Вам может быть предложено проведение наблюдения или продолжение лечения, с использованием лекарственной терапии, лучевой терапии, или их сочетания. Подробнее про эти методы Вы можете прочитать в соответствующих разделах нашего сайта:
Рак - это название группы однородных заболеваний, при которых клетки начинают безостановочное деление, изменяя вид и функции органов (или тканей). Часто при раке атипичные клетки растут, образуя твердую (солидную) опухоль, в других случаях (при лейкозах, миеломной болезни) - патологические клетки распространяются по организму без формирования такой структуры. Если имеется солидная опухоль, то хирургическое вмешательство - основной способ лечения.
Виды хирургических операций в лечении рака
Основной способ - это удаление измененных тканей режущим хирургическим инструментом - скальпелем. Им можно рассекать кожу, мышцы, фасции и удалять измененные ткани. Все операции проводят с анестезией.
Иногда используются другие хирургические методы, которые не предполагают разрезов инструментом:
- Криохирургия (иногда говорят "криотерапия") - это замораживание жидким азотом или аргоном. Метод применяют при предраковых новообразованиях шейки матки, при ретинобластоме ранней стадии.
- Лазерная хирургия, когда для рассечения тканей используют мощные световые лучи. Лазерный луч фокусируют на небольшом участке ткани, что особенно важно при операциях, требующих большой точности. Лазерное удаление проводят при наличии хорошего доступа к опухоли, если она расположена на поверхности тела или внутри некоторых полых органов - например, при раке пищевода.
- Гипертермия - относительно новый метод, при котором на опухоль воздействуют очень высокой температурой. Такое нагревание повреждает раковые клетки, которые при этом или погибают, или становятся более чувствительными к воздействию других методов лечения, например, химиотерапии или лучевой терапии. К этому способу относят радиочастотную абляцию, которая позволяет достичь высоких температур. Из-за новизны метод не слишком широко доступен, его возможности еще продолжают изучать в клинических исследованиях: при проведении экспериментальных операций по удалению рака прямой кишки, мозга, легких, органов шеи, желчного пузыря, печени.
- Фотодинамическая терапия (ФДТ) проводится с применением специальных препаратов - фотосенсибилизаторов. После введения этого фотосенсибилизирующего вещества, например, порфимера натрия, опухоль облучают светом с определенной длиной волны, что вызывает активное выделение кислорода и гибель атипичных клеток. Кроме прямого повреждающего действия, ФДТ уничтожает кровеносные сосуды, питающие опухоль и стимулирует иммунную систему. Такой способ применяют при хирургическом лечении немелкоклеточного рака легкого.
Варианты хирургического вмешательства в зависимости от объема удаляемой опухолевой ткани:
- Радикальные операции. В этом случае есть техническая возможность удалить всю измененную раком ткань, тем самым добиться полного излечения. Показания к хирургическому лечению рака определяют индивидуально, обычно операция успешна при небольших размерах опухоли и отсутствии ее прорастания в соседние органы. Иногда даже в этом случае после хирургического лечения проводят дополнительное лечение. Так, хирургическое лечение рака поджелудочной железы дополняется 6-месячным курсом химиотерапии для того, чтобы снизить риск рецидива.
- Паллиативные операции. Они не излечивают пациента от рака, но проводятся для улучшения состояния. Например, если опухоль проросла в соседние органы, удаление всех раковых клеток может привести к повреждению этого органов. В этом случае опухоль удаляется частично, для уменьшения боли или для уменьшения других симптомов.
- Диагностические операции. Выполняются они, если другие методы не позволяют полностью диагностировать состояние инструментальными и лабораторными методами. Эти операции относятся к малоинвазивной хирургии, обычно проводится лапароскопия, т.е. введение специальных миниатюрных инструментов через небольшие разрезы.
Во время хирургических операций по удалению рака врачи придерживаются методов, которые не позволяют опухолевым клеткам распределяться по зоне вмешательства.
Абластика
Метод работы в операционной ране, который не позволяет опухолевым клеткам распространяться по сосудам и соседним тканям. Для этого используется лазерное излучение, операционное поле отграничивается от здоровых тканей специальным операционным материалом, после удаления опухоли оперирующие хирурги проводят смену перчаток.
Антибластика
Этот метод подразумевает максимальное удаление злокачественных клеток в операционной ране. Для этого рану обрабатывают противоопухолевыми препаратами, жидкостями со свойствами коагулировать белок, проводят лучевую обработку места операции.
Противопоказания к хирургическому лечению рака
В каждом конкретном случае вопрос о необходимости и возможности хирургического вмешательства решают несколько специалистов, включая хирургов-онкологов, анестезиологов, терапевта и специалиста по химиотерапии. Обычно операцию не проводят, если вреда от ее проведения будет больше, чем пользы или если есть более эффективные консервативные методы лечения.
Выживаемость после онкологических операций
Прогноз зависит от:
- объема операции
- стадии заболевания
- наличия отдаленных метастазов
- возраста
- общего состояния здоровья (наличия сопутствующих заболеваний)
Ошибки и осложнения при хирургических операциях по поводу рака
Онкохирурги - высококвалифицированные специалисты, которые делают все возможное, чтобы предотвратить проблемы во время и после операции. Так как операции при онкологических заболеваниях очень часто требуют длительного наркоза, подразумевают удаление большого участка органа или ткани, то высок риск развития осложнений, как во время хирургического вмешательства,так и после.
- Инфекционные осложнения. Из-за неправильного или бесконтрольного применения антибиотиков в течение жизни у пациента может быть резистентность (нечувствительность) к лечению определенными препаратами. В настоящее время это актуальная проблема, поэтому важно четко следовать указаниям врача относительно длительности приема и дозировки антибиотиков.
- Кровопотеря во время онкологических операций и так достаточно велика (из-за большого объема вмешательства), но может быть кровотечение из поврежденного кровеносного сосуда при удалении проросшей в его стенку опухоли.
- Повреждение близлежащих тканей. Иногда во время операции оказывается, что объем поражения гораздо больше предполагаемого. Хирург стремится удалить как можно больше измененной ткани для проведения радикальной операции и при этом затрагивает соседние органы.
- Послеоперационные боли в той или иной степени испытывают все пациенты. Порог чувствительности к ней разный, поэтому для снятия (или значительного уменьшения) болевого синдрома применяют разные методы.
Во время проведения операции часто выполняют экстренное (внутриоперационное) исследование удаленных тканей и на основании полученных результатов решают вопрос об объеме операции (например, об удалении регионарных лимфоузлов при раке молочной железы). Конечно, тщательное исследование затем проводят и после операции, и в некоторых случаях получают дополнительные данные, меняющие дальнейшую тактику ведения больного и даже прогноз.
Распространенные онкологические операции
Отражают общую статистику по заболеваемости раком. 5 самых распространенных злокачественных новообразований
- рак молочной железы
- рак толстой и прямой кишки
- рак легких
- рак шейки матки
- рак желудка
- рак легких
- рак предстательной железы
- колоректальный рак
- рак желудка
- рак печени
Соответственно, чаще всего проводят хирургическое лечение рака молочной железы (удаление участка железы или модифицированная радикальная мастэктомия, т.е. полное удаление железы с последующей реконструкцией) и оперативное лечение рака легких и предстательной железы.
Выбор метода операции зависит от стадии заболевания, операция в более тяжелых стадиях дополняется проведением химиотерапии, лучевой терапии или других методов. Также во время операции проводят удаление измененных близлежащих тканей и удаление регионарных лимфоузлов для предотвращения метастазирования опухоли.
Хирургическое лечение колоректального рака
Проводят хирургическую резекцию участка, пораженного раком и удаление регионарных лимфатических узлов.
При операциях по удалению рака ободочной кишки применяют лапароскопический способ, т.е. без широкого доступа в брюшную полость.
Операция по удалению рака прямой кишки
При раке прямой кишки возможны несколько типов хирургической помощи:
- Если опухоль небольшая и не проникает в стенку кишки, проводят иссечение измененных тканей.
- Резекция. При прорастании в стенку кишки удаляется участок кишки, врач может иссекать ткань между кишкой и передней брюшной стенкой.
- Радиочастотная абляция, когда в кишку вводят зонд с электродами и проводят деструкцию рака.
- Криохирургическое лечение.
- Вывод стомы. При обширном разрастании опухоли удаляют не только кишку, но и пораженные органы малого таза. При невозможности анастомоза, т.е. соединения участков органа, здоровый участок кишки выводят на переднюю брюшную стенку. Затем, после восстановления пациента, возможна реконструктивная операция с удалением стомы.
Читайте также:

