Младенческие гемангиомы схема лечения пропранололом

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Инфантильная гемангиома (ИГ) - это распространенная доброкачественная сосудистая опухоль, возникающая в основном у недоношенных и младенцев женского пола, с локализацией преимущественно на голове и шее. Заболеваемость среди доношенных новорожденных составляет, по данным разных авторов, от 1,1-2,6% до 10-12%. Инфантильная гемангиома определяется при рождении либо вскоре после него. Особенностью инфантильной гемангиомы является возможность бурного роста в течение первых недель и месяцев жизни с формированием грубого косметического дефекта и нарушением жизненно важных функций.
Гемангиомы входят в большую группу сосудистых аномалий. За время изучения этой патологии было разработано множество различных классификаций. Настоящая работа основана на принятой в мировой практике классификации, предложенной Международным обществом исследования сосудистых аномалий (ISSVA), согласно которой все сосудистые аномалии следует подразделять на сосудистые опухоли и сосудистые мальформации (пороки развития).
Инфантильная гемангиома является самой распространенной сосудистой опухолью. Врожденные гемангиомы (ВГ) подобны инфантильной гемангиоме. Их особенность - максимальный внутриутробный рост опухоли, которая часто достигает больших размеров при рождении и может иметь очаги некроза как проявление уже начавшегося спонтанного регресса.
Сосудистые мальформации обычно при рождении либо не видны, либо маскируются под гемангиомы. Для них не характерен ни спонтанный регресс, ни бурный рост. Увеличение объема поражения возможно в периоды физиологического вытягивания.
В своем развитии инфантильная гемангиома проходит четыре фазы. Первая фаза (быстрой пролиферации) характеризуется быстрым ростом, затем рост опухоли замедляется и наступает фаза медленной пролиферации. В фазу стабилизации опухоль не растет, а в фазу инволюции подвергается обратному развитию.
У большинства пациентов фаза быстрой пролиферации длится от 1 до 4 мес., фаза медленной пролиферации - до 6 мес., до года - фаза стабилизации и после года - фаза инволюции.
В патогенезе инфантильной гемангиомы ключевую роль играет патологический рост клеток эндотелия. В процессе эмбриогенеза кровеносные сосуды и клетки крови образуются из мезодермы. Под влиянием специфических активаторов ангиогенеза мезодерма дифференцируется в гемангиобласты и, неравномерно уплотняясь, формирует ангиогенные группы: клетки эндотелия формируются из внешних клеток ангиогенной группы, а клетки крови - из внутренних.
Инфантильная гемангиома происходит из гемангиобластов. Клетки гемангиом экспрессируют маркеры из гемопоэтических, и эндотелиальных клеток. В дальнейшем дифференцированная ангиогенная группа превращается в первичную сосудистую трубку (васкулогенез), а далее происходит рост уже сформированных сосудистых трубок, их объединение в замкнутую сосудистую сеть (ангиогенез). Нормальный ангиогенез полностью заканчивается к рождению и возобновляется только в периоды бурного роста, при некоторых заболеваниях и состояниях (ишемия, травма) в качестве компенсаторной реакции, а также при различных патологических состояниях (например, при опухолях).
Регулирование ангиогенеза - это сложный многофакторный процесс, однако в качестве главных регуляторов можно выделить два фактора: VEGF - эндотелиальный фактор роста сосудов, зависящий от фазы, и FRF - фактор роста фибробластов, который повышается в фазу быстрой пролиферации и снижается, а затем полностью исчезает в фазы стабилизации и инволюции.
В 85-90% случаев инфантильной гемангиомы подвергаются спонтанной регрессии до наступления школьного возраста, при этом в фазе инволюции в клетках опухоли определяются маркеры апоптоза. Механизм начала редукции инфантильной гемангиомы не ясен. Известно, что их редукция связана с увеличением числа тучных клеток и пятикратным увеличением числа апоптотических клеток, треть из которых эндотелиальные.
В 10-15% случаев инфантильной гемангиомы требуют вмешательства в пролиферативную фазу вследствие жизнеугрожающей локализации (дыхательные пути), местных осложнений (изъязвление и кровотечение), грубого косметического дефекта и психологической травматизации.
До настоящего времени терапия инфантильной гемангиомы была достаточно стандартизирована - довольно длительно и в высоких дозах использовались глюкокортикоиды (преднизолон или метилпреднизолон). При неэффективности гормональной терапии назначался препарат второго ряда - интерферон, а при его неэффективности - винкристин.
Глюкокортикоиды особенно эффективны в фазу ранней пролиферации при высоком уровне VEGF, являющемся главной мишенью для стероидов. Они тормозят рост опухоли и уменьшают ее размеры. Частота стабилизации и неполной ремиссии достигает 30-60 % с первыми признаками улучшения только на 2-3-й нед. Преднизолон per os обычно назначается в дозе 5 мг/кг в течение 6-9 нед, затем в дозе 2-3 мг/кг еще 4 нед, альтернирующий прием - следующие 6 нед. Стероиды при таком режиме дозирования должны отменяться постепенно во избежание адреналового криза и возобновления роста гемангиомы.
Интерферон альфа-2а или 2b (1х10 6 - Зх10 6 ед/м2) индуцирует раннюю инволюцию больших гемангиом, блокируя миграцию эндотелиальных и гладкомышечных клеток, а также фибробластов за счет снижения продукции коллагена и основного фактора роста фибробластов с первыми признаками регрессии после 2-12 нед. лечения.
Эффективность винкристина близка к 100% при режиме дозирования 0,05-1 мг/м 2 инфузионно 1 раз в неделю с начальными признаками инволюции после 3 нед лечения.
Однако при использовании стандартных препаратов нередко возникают серьезные побочные эффекты. При лечении преднизолоном - катаракта, обструктивная гипертрофическая кардиомиопатия, диабет, стеатоз печени; интерфероном - лихорадка, миалгия, лейкопения, гемолитическая анемия, пульмонит, интерстициальный нефрит; винкристином - запор, боли в нижней челюсти, периферическая нейропатия, миелотоксичность.
Альтернативными методами лечения детских гемангиом являются лазерная хирургия, склерозанты и эмболизирующие вещества, криодеструкция, хирургия или их различные сочетания. Однако и в этих случаях не всегда удается достичь желаемого результата.
Поэтому большой интерес вызывали новые сведения о перспективном средстве для фармакотерапии сосудистых гиперплазии - пропранололе, который давно известен в качестве антигипертензивного препарата.
Пропранолол - неселективный бета-блокатор, обладающий антиангинальным, гипотензивным и антиаритмическим эффектом. Неселективно блокируя бета-адренорецепторы, он оказывает отрицательное хроно-, дромо-, батмо- и инотропное действие (урежает частоту сердечных сокращений, угнетает проводимость и возбудимость, снижает сократимость миокарда).
На протяжении многих лет пропранолол использовали не только у взрослых для лечения гипертензии, но и у детей при кардиологической патологии для коррекции врожденных пороков сердца и аритмий. В процессе лечения кардиологической патологии у детей сотрудники госпиталя г. Бордо (Франция) во главе с доктором С. Leaute-Labreze обнаружили, что пропранолол может тормозить рост и вызывать регрессию гемангиом. У ребенка с сочетанной патологией - обструктивной гипертрофической миокардиопатией и с персистирующей носовой гемангиомой на следующий день после начала лечения пропанолом было отмечено, что опухоль стала мягче и темнее.
Доза кортикостероидов, которые применяли для лечения гемангиомы с небольшим успехом, была снижена, но опухоль продолжала уменьшаться. После прекращения лечения кортикостероидами рост гемангиомы не возобновлялся, а поверхность ее стала абсолютно плоской к 14-му мес. жизни ребенка.
Второе наблюдение в этом же госпитале было сделано у ребенка с поверхностной детской капиллярной гемангиомой, локализованной в правой части головы, которая не давала открывать правый глаз. Несмотря на лечение кортикостероидами, опухоль продолжала увеличиваться. Помимо этого МРТ выявило наличие внутришеечных образований, вызывающих сжатие трахеи и пищевода. Сделанное пациенту УЗИ показало увеличение сердечного выброса, в связи с чем было начато лечение пропранололом в дозе 2 мг/кг/сут. Семь дней спустя ребенок был в состоянии открыть правый глаз, а образование возле околоушной железы значительно уменьшилось в размерах. Лечение преднизолоном было прекращено к 4-му мес. жизни ребенка, рецидивов роста не возникло. К 9-му мес. удовлетворительно открывался правый глаз и не было отмечено серьезных нарушений зрения.
После того как от родителей было получено письменное информированное согласие, пропранолол начали давать еще девятерым детям с тяжелыми или уродующими детскими капиллярными гемангиомами. У всех пациентов через 24 часа после начала лечения наблюдались изменение цвета гемангиом с интенсивно красного на фиолетовый и ощутимое размягчение поражения. После этого гемангиомы продолжали регрессировать, пока не становились почти плоскими, с остаточной телеангиоэктазией кожи. О системных побочных эффектах не сообщалось.
Сотрудники Детского клинического госпиталя г. Цюрих (Швейцария) провели ретроспективный анализ данных с декабря 2008 г. по декабрь 2009 г. об эффективности пропранолола в качестве препарата первой линии для лечения сосудистых гиперплазии, а также о его влиянии на гемодинамику. Оценка проводилась в однородной группе детей с пролиферирующими проблемными гемангиомами на фоне лечения пропранололом (2 мг/кг/сут). Проблемные гемангиомы были определены как гемангиомы, неизбежно влекущие функциональные или косметические дефекты при отсутствии лечения. В исследование были включены пациенты не старше 9 мес., прошедшие полное 2-дневное внутрибольничное обследование, при условии отсутствия предшествующей кортикостероидной терапии. Родители пациентов должны были дать согласие на использование лекарственного средства по непрямому назначению. Помимо лечения пропранололом, альтернативной или адъювантной терапии не осуществлялось (двум младенцам ранее безуспешно проводилась лазерная терапия - их опухоли продолжали увеличиваться в размере).
Результат оценивался по фотографиям с помощью визуальной аналоговой шкалы (VAS), по данным УЗИ и, при необходимости, офтальмологического осмотра. Восприимчивость к терапии и гемодинамические показатели регистрировали с момента начала терапии в течение длительного периода в фиксированные моменты времени. В исследование были включены двадцать пять детей (средний возраст 3,6 (1,5-9,1) мес). Среднее время наблюдения составило 14 (9-20) мес. и 14 пациентов завершили курс лечения в среднем возрасте 14,3 (11,4-22,1) мес. при средней продолжительности лечения 10,5 (7,5-16) мес. У всех пациентов после 7 мес. наблюдалось значительное снижение интенсивности окраски гемангиомы (до - 9 по VAS) и значительное уменьшение гиперплазии в размере (до - 10 по VAS). Толщина поражений, выявляемых УЗИ, в начале лечения и через 1 мес составила в среднем 14 (7-28) мм и 10 (5-23) мм соответственно. У детей с поражениями периокулярных участков астигматизм и амблиопия устранились в течение 8 нед. Общая переносимость препарата была хорошей, не было отмечено гемодинамических изменений. В целом неблагоприятные явления во время лечения пропранололом очень незначительны по сравнению с серьезными побочными эффектами кортикостероидов и интерферона-а (развитие спастической диплегии с вероятностью до 25%). Не было выявлено существенных различий в восприимчивости между глубокими и поверхностными гемангиомами, но создалось некоторое впечатление, что поверхностные гемангиомы оставляют после себя телеангиэктазические изменения кожи, в то время как глубокие гемангиомы с большей вероятностью исчезают полностью.
У двух из 14 пациентов, прошедших курс лечения, через 8 нед после прекращения терапии были зафиксированы небольшой повторный рост и потемнение гиперплазии. Этим пациентам было повторно назначено лечение пропранололом 11 и 8,5 мес. соответственно с успешным результатом. Рецидивы, по-видимому, происходили примерно в 20-40% случаев. Примечательно, что повторный рост гемангиом после остановки терапии наблюдался также у детей старше 12-14 мес., т. е. в то время, когда фаза пролиферации гиперплазии, как полагают, уже завершена. Этот неожиданный феномен может указывать на то, что пропранолол задерживает естественный рост гемангиом. Признаки, свидетельствующие о возможности возобновления роста после прекращения лечения, пока не известны. Однако рецидивы гемангиом обычно протекают легко, и пациенты хорошо реагируют на повторную терапию.
Строгими критериями отбора отличались исследования швейцарских врачей, в которых описаны группы пациентов разного возраста, имевших различные стадии и течения гемангиом и получавших альтернативную терапию наряду с пропранололом. Были подтверждены отличный эффект и хорошая переносимость пропранолола и предложено использовать его в качестве препарата первой линии для лечения детских гемангиом.
J. Goswamy и соавт. сообщили о применении пропранолола (2 мг/кг/день, разделенные на 3 дозы) у 12 детей (9 девочек) со средним возрастом 4,5 мес в течение 1-9 нед. (в среднем - 4 нед.), которых предварительно лечили кортикостероидами в качестве терапии первой линии. Побочных эффектов при лечении пропранололом не было, за исключением транзиторной брадикардии у одного пациента, которая исчезала самостоятельно. Авторы считают, что пропранолол может быть предпочтительным вариантом для лечения инфантильной гемангиомы в качестве препарата первой линии.
Аналогичные результаты были получены Y. B.Jin и соавт. в проспективном исследовании применения пропранолола в качестве препарата первой линий для лечения инфантильной гемангиомы у 78 детей со средним возрастом 3,7 мес (1,1-9,2 мес.). Терапия длилась в среднем 7,6 мес (2,1-18,3 мес.). Через неделю лечения регрессия гемангиомы наблюдалась в 88,5% случаев, а через 1 мес. - в 98,7%. До лечения изъязвление гемангиом встречалось у 14 пациентов, оно проходило после 2 мес. лечения пропранололом. Слабые побочные эффекты пропранола были в 15,4% случаев, повторный рост гемангиом после прекращения лечения - в 35,9 %.
A. Zvulunov и соавт. сообщили о результатах лечения пропронололом (2,1 мг/кг/день, диапазон от 1,5 до 3 мг/кг/день, в течение 1-8 мес., в среднем 3,6 мес.) 42 больных детей (возраст от 7 до 12 мес.) с гемангиомами, находящимися в постпролиферативной фазе. Показатель визуальной шкалы гемангиом в результате лечения снизился с 6,8 до 2,6 (р
- Можно ли ребенку с младенческой гемангиомой делать массаж?
Ребенку с младенческой гемангиомой не рекомендуется проводить массаж, если гемангиомы множественные. Если младенческая гемангиома локализуется в области головы или шеи не рекомендуется проводить массаж шеи и воротниковой зоны
- Можно ли делать ребенку физиотерапию?
Ребенку с младенческой гемангиомой не рекомендуется проводить физиотерапию на области близлежащие к гемангиоме
- Когда нужно увеличивать дозировку препарата?
Увеличение дозы пропранолола происходит с ведома лечащего врача при увеличении веса ребенка на 1 кг. Пересчет дозировки делает либо кардиолог по месту жительства, либо лечащий врач.
- Можно ли делать прививки? Какие прививки можно делать?
По данному вопросу рекомендуется консультироваться с иммунологом. Со своей стороны, мы не видим противопоказаний к проведению прививок. Проведение прививок мы рекомендуется проводить с применением антигистаминных средств, а также использовать современные адаптированные вакцины (аАКДС и т.п.)
- Бывает ли аллергия на препарат?
Аллергия описана в осложнениях при применении пропранолола. Но мы в своей клинической практике с аллергией на пропранолол не сталкивались.
- При каком увеличении веса необходимо менять дозировку пропранолола?
Мы считаем целесообразно увеличивать дозу препарата при увеличении веса ребенка на 1 кг.
- Как отменяется препарат?
Препарат отменяется в течении месяца постепенно под контролем врача.
- Какие таблетки лучше принимать: анаприлин, обзидан , пропранолол?
Хотя все перечисленные препараты являются одним и тем же препаратом, но мы рекомендуем использовать Обзидан.
- Что делать, если по каким то причинам вы пропустили прием препарата?
Если вы пропустили прием препарата по какой либо причине, начните с ближайшего времени по графику приема.
- Влияет ли пропранолол на физическое, умственное и общее развитие ребенка?
Пропранолол не влияет на общее физическое и умственное развитие ребенка.
- Нужно ли придерживаться времени приема препарата?
График приема препарата придерживаться необходимо, это обусловлено фармакологическими свойствами препарата. Через 6-8 часов наступает период полного расщепления препарата в организме и он перестает действовать.
- До или после еды принимать пропранолол?
Прием препарата у маленьких детей не связан с приемом пищи. Нельзя подмешивать препарат к молоку, смесям, жировым эмульсиям ( витамин Д) и т.д.
- Какова вероятность развития гемангиомы у второго ребенка?
По данным нашего статистического исследования вероятность рождения второго ребенка с младенческой гемангиомой- 30%
- Какие препараты не сочетаются с приемом пропранолола?
Сочетание пропранолола с другими препаратами определяется лечащим врачом или специалистом, назначающим ребенку медикаментозную терапию. По всем вопросам рекомендуем проконсультироваться с лечащим врачом.
- Что делать, если ребенок заболел ОРВИ?
Прием пропранолола не прекращается. Причиной отмены препарата является только рвота и отказ ребенка от еды.
- Можно ли ребенку делать местную анестезию?
Применять лидокаин и пропранолол необходимо с крайней осторожностью!
- Как узнать, что гемангиома прошла?
- Возможно ли возобновление роста гемангиомы после отмены пропранолола?
Нет, возобновления роста гемангиомы посла отмены пропранолола не бывает.
- Можно ли ребенка мыть в бане?
Не рекомендуется, усиление кровотока, возникающего в результате нагревания тела способствует развитию гемангиомы.
- Все ли можно есть ребенку?
Ограничений в питании ребенка нет.
- Надо ли дома ребенку измерять пульс после каждого приема?
Рекомендуется контролировать частоту сердечных сокращений после приема пропранолола.
- Сколько времени дети бывают вялыми?
На фоне применения пропранолола некоторые дети первые недели становятся менее активными чем обычно, но этот эффект временный.
- Возможно ли последствия после курса проведения пропранолола?
Последствий от приема пропранолола нет.
- Сколько по времени занимает курс пропранолола?
Гемангиома (иначе – младенческая гемангиома) – это доброкачественная опухоль из эндотелиальных клеток.
Эндотелиальные клетки – это клетки, которые выстилают сосуды организма изнутри, что напрямую связывает появление гемангиомы с нарушениями закладки или развития системы кровообращения, хотя истинная причина гемангиомы до сих пор остается невыясненной.
Современный взгляд на гемангиому
Существует мнение, согласно которому гемангиома является в равной мере как опухолевым заболеванием, так и локальным проявлением сосудистой гиперплазии. Несмотря на то, что в данный момент нет научного подтверждения или опровержения такой теории, клиническая практика показывает, что принципиальной разницы между лечением гемангиомы как опухоли и как гиперплазии сосудов – нет.
Фактически, гемангиома – это пластинка (в 80% случаев возникающая на коже, но возможно ее возникновение в любом органе или ткани) с неровными, четкими краями, приподнятая над поверхностью кожи и имеющая темно-красный цвет, состоящая из здоровых и измененных клеток эндотелия, тромбоцитов и соединительно-тканных элементов, вместе формирующих структуру, отдаленно напоминающую нормальный кровеносный сосуд.
В 80% случаев появляется только одно образование, чаще всего на коже лица, шеи и головы, но возможно и множественное возникновение гемангиом на разных участках тела.
Для гемангиомы характерны следующие особенности:
- чаше всего она возникает еще внутриутробно, и может быть замечена сразу после родов
- частота встречаемости у детей – 10%
- у девочек гемангиома возникает в 7 раз чаще, чем у мальчиков
- гемангиома способна к инволюции, то есть, по прошествии 5-7 лет она начинает развиваться в обратном направлении вплоть до полного исчезновения.
Опасность гемангиомы
Гемангиома – опухоль сосудистого происхождения, поэтому и опасна она в первую очередь кровотечениями, появляющимися вследствие нестабильности стенки опухолевого сосуда. Хоть для нее не характерно спонтанное появление кровотечения, любая травма может легко к нему привести.
Если гемангиома расположена на коже, то кровотечение можно легко заметить и остановить. Но при локализации гемангиомы в тканях внутренних органов, кровотечение долгое время может оставаться незамеченным, а объем истекшей крови – значительно большим, что может привести к смерти.
Также, ткань гемангиомы имеет свойство отфильтровывать из кровотока тромбоциты, что повышает вероятность возникновения кровотечений.
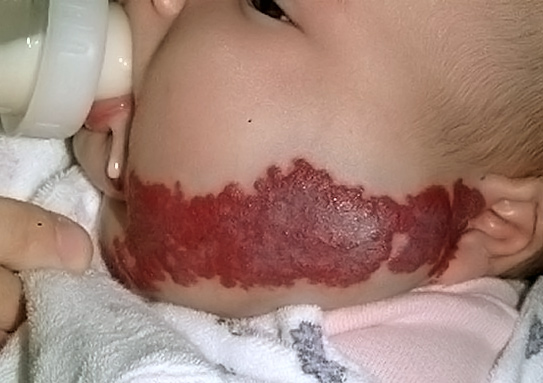
Фото: сайт кафедры дерматовенерологии Томского военно-медицинского института
Использование пропранолола для лечения гемангиомы
Согласно исследовательским протоколам, у пациента с гемангиомой кожи лица, которую лечили преднизолоном, развился серьезный побочный эффект – обструктивная гипертрофическая кардиомиопатия.
Для купирования побочного эффекта был назначен пропранолол, а на следующий день гемангиома сменила свой цвет с красного на фиолетовый и стала мягче. Год спустя после публикации этого наблюдения стали появляться статьи, в которых подтверждалось выраженное позитивное действие пропранолола при лечении гемангиомы.
На данный момент большинство исследований, посвященных антиангиогенному действию пропранолола еще не завершены, но уже можно с уверенностью говорить о следующих особенностях его применения для лечения гемангиомы:
Пропранолол категорически противопоказан детям со следующими заболеваниями:
- синусовая брадикардия,
- антриовентрикулярная блокада,
- сердечная недостаточность,
- бронхиальная астма,
- приступы бронхоспазма,
- периферическиме нарушения кровотока, например – болезнь Рейно.
Пропранолол имеет следующие лечебные эффекты:
1. Начальный эффект (первые 3 дня после начала применения), который характеризуется изменениями цвета и консистенции опухоли вследствие сужения сосудов под действием препарата.
2. Промежуточный – приостановка роста гемангиомы, вследствие угнетения сигнальной активности растущих клеток.
3. Долговременный – разрушение (апоптоз) клеток в капиллярах опухоли, с последующей регрессией гемангиомы в течение 2-3 месяцев.
Следует соблюдать следующие правила назначения и лечения пропранололом:
1. В первые 6 часов после перового применения препарата, каждые 30 минут производить измерение артериального давления и пульса. Если за этот промежуток времени побочных эффектов не обнаружено, ребенка можно выписывать домой.
2. Каждый месяц фотографировать и измерять опухоль для оценки динамики.
3. Регулярно проводить измерение веса, кривых пульса и артериального давления для коррекции дозы.
Таким образом, на основании предварительного изучения, эффективность пропранолола несомненно выше эффективности любого из ранее применяемых при лечении гемангиомы средств, при приблизительно одинаковой частоте встречаемости побочных эффектов.
Следует также сказать, что на территории РФ и некоторых других стран действуют, так называемые, протоколы лечения болезней, которые предписывают определенный алгоритм лечения.
На данный момент, в большинстве этих стран пропранолол не входит в список протокольных средств, применяемых для лечения гемангиомы (что связано с недостаточным количеством научных подтверждений его безопасности), а значит его применение не разрешено.
Важно! Все материалы носят справочный характер и ни в коей мере не являются альтернативой очной консультации специалиста.
Этот сайт использует cookie-файлы для идентификации посетителей сайта: Google analytics, Yandex metrika, Google Adsense. Если для вас это неприемлемо, пожалуйста, откройте эту страницу в анонимном режиме.

Согласно классификации Международного сообщества по изучению сосудистых аномалий 1996 г. (ISSVA), существует два основных вида образований из кровеносных сосудов, имеющих в своей основе разные клинические проявления и биологические механизмы: сосудистые опухоли (самой частой разновидностью которых является инфантильная гемангиома) и сосудистые мальформации [3].
Сосудистые опухоли (например, гемангиомы, капозиформные гемангиоэндотелиомы, тафт-ангиомы) – это настоящая неопластическая пролиферация эндотелиальных клеток. Сосудистые мальформации, с другой стороны, это структурные аномалии сосудов (артериальные, венозные, капиллярные, лимфатические, или смешанные), возникающие из-за ошибок в эмбриогенезе и имеющие нормальный эндотелиальный обмен. Несмотря на клинические отличия, различные патогенетические особенности, естественный ход развития и прогноз, сосудистые аномалии ошибочно диагностируются более чем в 70 % случаев, что ведет к неправильному лечению [8]. Частота распространения всех сосудистых аномалий в мире лежит примерно в диапазоне от 8 % до 10 % от всех новорожденных. Инфантильные гемангиомы встречаются с частотой около 10–12 % у детей европейской расы, 1,4 и 0,8 % у африканской и азиатской рас соответственно и с преимущественным поражением лиц женского пола (3:1). У недоношенных детей, родившихся с массой тела менее 1000 г, эти цифры достигают 22–30 %. Наиболее часто (68–74 %) образования из кровеносных сосудов располагаются в области головы и шеи, причем излюбленной локализацией являются концевой отдел носа, переносица, околоушно-жевательная область и область глазницы [10].
Обширные гемангиомы шеи и лица и сегментарные гемангиомы могут быть ассоциированы с множественными аномалиями, составляющими так называемый синдром " PHACES ", включающий мальформации головного мозга в задней черепной ямке, гемангиомы шейно-лицевой области, артериальные аномалии, коарктацию аорты, пороки сердца, аномалии глаз и грудинные и абдоминальные расщепления или эктопию хорды. Этот синдром значительно преобладает у лиц женского пола (9:1) и, скорее всего, представляет дефекты развития, которые происходят в период 8–10 недель гестации. Последние наблюдения показали, что дети с этими артериальными аномалиями имеют большой риск цереброваскулярной окклюзии и тенденцию к менее благоприятному клиническому прогнозу [7].
В ранее проведенном нами исследовании, включавшем 212 детей [1], было получено следующее распределение гемангиом в зависимости от локализации – представлено в диаграмме.
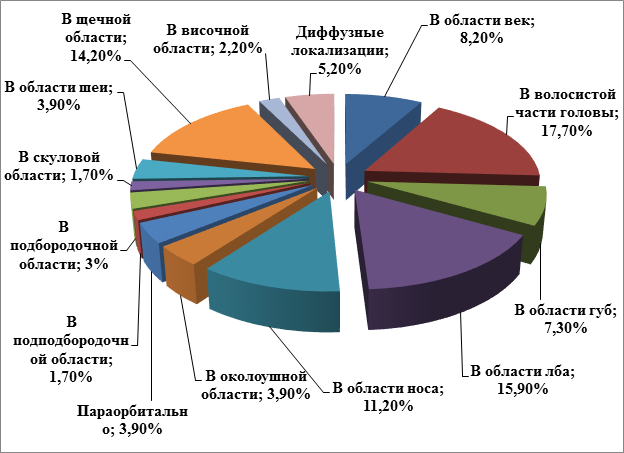
Распределение гемангиом в зависимости от локализации
Как можно видеть, большая часть гемангиом располагается в области головы и шеи. Сосудистые поражения данной локализации особенны, во-первых, тем, что приобретают большую социальную значимость из-за своей локализации. Во-вторых, они могут вызывать, помимо эстетических нарушений, и нарушение функций дыхания, жевания, глотания, зрения, слуха.
Проблема комплексной реабилитации больных с сосудистыми аномалиями до настоящего времени не теряет актуальности. Это связано, в том числе, с отсутствием однозначной тактики ведения данных пациентов, системного обобщения и решения проблемы комбинированного лечения больных. Несмотря на то, что многие из аномалий регрессируют спонтанно, вмешательство требуется, когда их рост может нанести вред жизненно-важным структурам. Даже сторонники выжидательной тактики (Свистунова Т.М., Абшилава Д.И.) говорят о необходимости лечения гемангиом с бурным ростом и при локализации в области головы, лица и шеи. В (10–20) % случаев кожных гемангиом появляются такие осложнения, как изъязвление и кровотечение, и вовлечение таких важных функций, как зрение, дыхание, слух или питание. Эти осложнения вместе с косметическими причинами являются абсолютными показаниями для лечения и должны немедленно подвергаться подходящему лечению [4, 6, 9].
К настоящему моменту проведены исследования в России (Рогинский В.В., Котлукова Н.П.), многоцентровые исследования в Европе, доказывающие эффективность и безопасность пропранолола для лечения гемангиом у детей и разрешающие его применение для этой цели (Jean-Pierre LEROY, 2011). В марте 2014 г. появилось сообщение о одобрении со стороны FDA (Управления по контролю за продуктами и лекарствами (США)) в отношении препарата Hemangiol , содержащего Пропранолола гидрохлорид в дозе 4,28 мг/мл для лечения пролиферирующих гемангиом, требующих системной терапии. В феврале того же года появилось сообщение о одобрении состава препарата, содержащего Пропранолола гидрохлорид со стороны Европейского комитета медицинских агенств по медицинским препаратам для использования у людей.
Задачами настоящего исследования явилось изучение влияния пропранолола на гемангиомы у детей, а также оценка безопасности данного метода лечения.
Материалы и методы
После установки диагноза гемангиомы новорожденных с использованием, в том числе УЗИ мягких тканей челюстно-лицевой области и по показаниям КТ-ангиографии черепа ребенок направлялся к детским кардиологам.
В условиях детского кардиологического стационара проводилось предварительное обследование ребенка для выявления отсутствия противопоказаний для проведения терапии Пропранололом (общие анализы крови и мочи, биохимический анализ крови с определением показателей трансаминаз, уровня глюкозы, мочевины и креатинина крови, ЭКГ, Допплер-ЭХОКГ, суточное мониторирование ЭКГ по Холтеру, измерение АД) и подбор дозы препарата, начиная с 0,25 мг/кг/сут. и постепенно выходя на лечебную дозу, которая, как правило, составляла 2 мг/кг/сут. Ежедневно контролировали показатели АД, ЧСС. Перед выпиской из дневного кардиологического стационара каждому ребенку проводили контрольное Допплер-ЭХОКГ-исследование с оценкой сократительной способности миокарда, а также биохимический анализ крови. Далее лечение проводилось в домашних условиях с ежемесячным посещением хирурга (для контроля динамики состояния сосудистого поражения) и кардиолога (для контроля показателей биохимического анализа крови (раз в 3 месяца), ЧСС, АД, ЭКГ, Допплер-ЭХОКГ, а также для увеличения дозы препарата по мере прибавки в массе тела). При повышении уровня трансаминаз выше возрастных норм назначалось наблюдение ребенка детским инфекционистом. Контроль эффективности терапии осуществляли путем фотодокументирования, УЗИ гемангиом с определением скорости кровотока в сосудистых поражениях, КТ-ангиографии при необходимости. По достижению регресса гемангиомы, что подтверждалось хирургом клинически и инструментально, ребенок направлялся для отмены препарата в кардиологический дневной стационар. Отмена терапии осуществлялась постепенно в течение 2–3 недель путем снижения разовой дозы препарата во избежание синдрома отмены. Вновь контролировали показатели гемограммы, биохимические параметры, ЭКГ, ЭКГ-мониторирование по Холтеру, Допплер-ЭХОКГ, АД. Длительность терапии в среднем составила 18 месяцев. Она определялась индивидуально и зависела от достигнутого клинического эффекта.
Результаты и их обсуждение
Во всех случаях пропранолол продемонстрировал быстрый и стойкий эффект на гемангиомы новорожденных. Регресс гемангиом был заметен уже на первой неделе начала терапии. Наиболее выраженная динамика отмечалась в течение первого месяца от назначения лечения, а также после очередных повышений дозы в связи с увеличением массы тела. Эффект от лечения был тем более выражен, чем в более раннем возрасте оно начиналось. Нежелательные явления были отмечены у 4 детей (4 %). В 1 случае наблюдался эпизод вагоинсулярного криза с клиникой гипогликемии, который купировался самостоятельно и не потребовал отмены лечения, у второго ребенка наблюдалось временное увеличение уровня креатинина, что потребовало перерыва в лечении на 2 месяца; еще у двух детей были зафиксированы брадикардия на ЭКГ и появление на Холтер-ЭКГ пауз в виде асистолии более 2 секунд, что потребовало отмены препарата.
Добиться полного регресса поражения кожи за счет только лечения Пропранололом удалось в 68 % случаев. В остальных случаях у ряда пациентов запустевание оставшейся части гемангиомы продолжается самопроизвольно, у некоторых приходится проводить лазерокоагуляцию оставшихся единичных сосудов
Особого внимания заслуживает эстетичность остающегося следа на месте бывшей гемангиомы. Учитывая, что в случае медикаментозного лечения не оказывается никакого химического или теплового воздействия на зону поражения кожи, не возникает никаких рубцов, соответственно нет изрытости поверхности, нарушений пигментации и т.д., что имеет место после таких других методов лечения, как криодеструкция, склеротерапия, иссечение. На месте бывшего поражения кожи во многих случаях практически не остается следа.
Дополнительным преимуществом является отсутствие необходимости общей анестезии при медикаментозном лечении, тогда как в большинстве остальных вариантов лечения проведение общей анестезии на каждом этапе лечения является обязательным, учитывая возраст пациентов.
Учитывая профиль возможных осложнений, представляется обоснованным и обязательным продолжение использования междисциплинарного подхода при лечении детей с гемангиомами, учитывающего необходимость совместного ведения данных пациентов с участием хирургов и кардиологов.
На фотографиях 1–4 показаны результаты лечения.
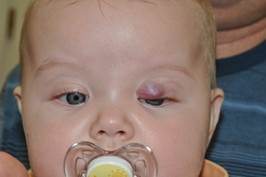

Фотография 1. Ребенок перед лечением
Фотография 2. Ребенок после терапии Пропранололом (продолжительность лечения 17 месяцев)
Читайте также:

