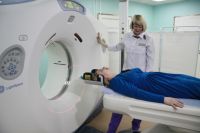
Лечение рака предстательной железы радиоактивным йодом
Имплантация радиоактивных зерен (брахитерапия или внутренняя лучевая терапия) – это форма лучевой терапии при раке предстательной железы. Существует два вида брахитерапии при раке предстательной железы. Один называется постоянной, и другой, более новый метод, называется временной брахитерапией.
Перманентная (низкодозированная) брахитерапия: LDR
Врач имплантирует радиоактивные зерна (йод-125 или палладий-103) в предстательную железу под контролем ультразвука. Количество зерен и место их расположения определяется планом лечения, созданным компьютером и разработанным для каждого пациента. Обычно имплантируют 40 – 100 зерен.
Имплантаты остаются на месте постоянно, и через несколько месяцев становятся биологически нейтральными (больше не активными). Этот метод позволяет поставлять в предстательную железу большую дозу радиации с ограничением вреда для окружающих тканей.
Временная (высокодозированная) брахитерапия: HDR
При этом методе полые иглы помещают в предстательную железу и наполняют их радиоактивным материалом (иридий-192) на 5-15 минут. После лечения иридий и иглы удаляют. Это повторяется 2 – 3 раза в течение следующих нескольких дней. Этот метод позволяет поставлять в предстательную железу большую дозу радиации с ограничением вреда для окружающих тканей. По сравнению с внешним облучением, которое требует 8 – 9 недель ежедневного лечения, удобство – основное преимущество этих видов лечения.
Кому подойдет эта процедура?
Имплантаты зерен – относительно низкоэнергетические источники, и, следовательно, имеют ограниченное проникновение в ткань. Поэтому наилучшими кандидатами для этой процедуры являются пациенты, у которых опухоль находится в пределах предстательной железы и не очень агрессивная. Обычные критерии для лечения включают уровень ПСА менее 10, балл по шкале Глисона (которая измеряет агрессивность опухоли) менее или равен шести, и минимальная патология или ее отсутствие при пальцевом ректальном исследовании.
Что происходит перед процедурой?
Чтобы радиолог узнал детали, специфические для вашего случая, выполняется трансректальное ультразвуковое исследование. Чтобы проконтролировать правильное размещение имплантатов, могут применяться более новые методы с использованием КТ или МРТ. Эта информация используется, чтобы разработать план лечения для вас. Другой вариант – проведение ультразвукового исследования и разработка плана лечения во время имплантации зерен.
Что происходит во время процедуры?
Вся процедура занимает приблизительно 90 минут. Большинство пациентов идут домой в тот же день. Процедуру выполняет онколог-радиолог или уролог. Оба специалиста активно вовлечены во все аспекты имплантации, от планирования до послеоперационного ухода. Во время процедуры уролог осуществляет контроль ультразвуком, а онколог-радиолог имплантирует радиоактивные зерна.
Процедура выполняется следующим образом:
После общей или спинальной анестезии ноги очень аккуратно подымают и подкладывают что-то мягкое.
Хотя это относительно новый вид лечения, результаты 10-летнего изучения отдаленных результатов показывают, что у пациентов с похожими видами рака предстательной железы брахитерапия так же эффективна, как радикальная простатэктомия и регулярное внешнее облучение.
Каковы побочные эффекты?
Наиболее часто встречаются симптомы со стороны мочеиспускательного тракта. К ним относятся частое мочеиспускание и необходимость посетить туалет быстро. Некоторые мужчины ощущают жжение во время мочеиспускания и, в некоторых случаях, неспособность опорожнить мочевой пузырь полностью. Обычно с этими симптомами можно справиться с помощь медицинских препаратов, и через некоторое время они исчезнут. Для опорожнения мочевого пузыря может понадобиться временная самокатетеризация.
Недержание мочи в целом встречается редко. Риск может быть несколько повышен у пациентов, которые предварительно перенесли хирургическую операцию по удалению части предстательной железы, которая называется TURP (трансуретральная резекция предстательной железы). Врач может свести риск к минимуму, тщательно выполнив ультразвуковое исследование предстательной железы перед процедурой, чтобы определить, сколько ткани предстательной железы осталось, чтобы имплантировать зерна.
Малоинвазиный метод лечения рака предстательной железы (РПЖ), равен по эффективности большой операции – радикальной простатэктомии
В нашей клинике применяют низкодозную (постоянную) брахитерапию. Радиоактивные гранулы размером с небольшое рисовое зерно импланитруют в предстательную железу. Нейтронное излучение разрушает ДНК раковых клеток, уничтожает их способность делиться и расти.
Здоровые ткани вокруг предстательной железы получают гораздо меньшую дозу радиации и легко восстанавливаются. Со временем активность имплантатов снижается, через 8-10 месяцев сводится на нет. Неактивные источники остаются в организме, они не влияют на состояние человека.
В отличие от традиционной лучевой терапии, брахитерапия уничтожает РПЖ без вреда окружающим тканям
- Не наносит вреда окружающим простату тканям
- Занимает два дня вместо семи недель наружной лучевой терапии.
- Вернуться к обычной деятельности можно через несколько дней после лечения.
- Не повреждаются кровеносные сосуды и нервы, которые контролируют эрекцию, поэтому низкая вероятность эректильной дисфункции .
- В случае рецидива, то есть повторного возникновения опухолевого процесса, возможно дальнейшее лечение. Как правило – методом гормональной терапии или криоабляции .
Брахитерапия рекомендована пациентам заинтересованным в сохранении половой функции
Выполняется мужчинам любого возраста с локализованным раком, низким и умеренным онкологическим риском (ПСА ≤ 20 нг/мл, шкала Глисона ≤ 7).
Существуют следующие условия для выбора брахитерапии :
- Объем простаты до 60 см. куб. При увеличенном размере может быть назначена гормональная терапия в течение трех месяцев для уменьшения органа.
- Опухоль не распространилась за пределами простаты (стадия Т1-Т2).
- Затрудненное мочеиспускание не достигло крайней формы (максимальная скорость мочеиспускания при урофлоуметрии не менее 10 мл/сек).
Если выполнялась трансуретральная резекция (ТУР) простаты, необходимо дождаться заживления раны. Как правило, заживление происходит через шесть месяцев.
Брахитерапия – ход процедуры
Имплантация, в среднем, занимает два-три часа. Капсулы с радиоактивным йодом-125 заводят специальными иглами в зону промежности между мошонкой и анальным отверстием под ультразвуковым контролем. Обычно требуется 50-60 радиоактивных капсул. Их оптимальное количество и расположение рассчитывают заранее компьютерной программой.
В начале операции в мочевой пузырь через мочеиспускательный канал устанавливают уретральный катетер, через него отводится мочи во время и после операции. Катетер также дает акустическую тень – врач хорошо видит мочеиспускательный канал, куда не нужно имплантировать источники.
Стоимость брахитерапии
Гражданам России выполняем бесплатно по каналам высокотехнологичной помощи. Наши врачи помогут оформить необходимые документы.
Для иностранных граждан стоимость брахитерапии по каналу платных медицинских услуг составляет 550 тыс. рублей. Это меньше, чем в других зарубежных или отечественных урологических центрах.
Брахитерапия считается реальной альтернативой радикальной простатэктомии и дистанционной лучевой терапии, и возможно полное излечение заболевания рака предстательной железы при правильном подборе больных и профессиональном выполнении операции.
Впервые брахитерапия была применена в 1910 году, когда Д. Пасто и П. Дегрэ ввели капсулы радия-226 в предстательную железу через уретру.
Далее в 1917 году в США Б. Барринджер ввел микроисточники в железу через иглы. Затем Р. Флокс вместе с соавторами в 1930 году применили в качестве имплантанта радиоактивное золото.

Возрождение брахитерапии рака предстательной железы началось в 1970 году с развитием технологии ретропубикальной открытой имплантации зерен I-125 в Мемориальном Госпитале Нью-Йорка. Однако, при открытой ретропубикальной технологии зерна йода располагались мануально, вследствие чего не достигалось оптимального распределения дозы в предстательной железе: наряду с зонами чрезмерной активности оставались холодные очаги.
В 1981 году Х. Холм и Дж. Гаммелгард применили технологию имплантации микроисточников йода-125 в ткань предстательной железы под контролем трансректального ультразвукового сканирования (ТРУЗИ). Это методика впервые была применена для получения биопсии, и стало очевидным, что она может использоваться для визуализации положения радиоактивных источников в простате. Это и послужило основой новой технологии брахитерапии.
В 1990 году П. Кутревелис использовал трехмерную стереотактическую приставку к компьютерному томографу (КТ) для лечения больных раком предстательной железы, которым невозможно провести лечение методом брахитерапии под контролем ТРУЗИ.
В 2000 году в НИИ урологии Минздрава России г. Москвы был внедрен новый метод лечения рака предстательной железы – брахитерапия. Этот институт стал первым медицинским учреждением в России, который освоил брахитерапию – уникальную технологию, известную и применяемую во всем мире.
С 2004 года метод профессора П. Кутревелиса (проведение брахитерапии под контролем КТ) используется в Центре брахитерапии в Медицинском Радиологическом Научном Центре РАМН г. Обнинска.
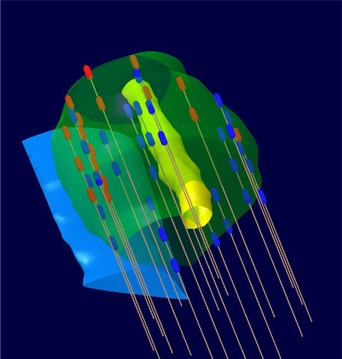
При выявлении рака предстательной железы на стадии T1 – Т2 (в некоторых случаях и на стадии Т3) наряду с радикальной простатэктомией и дистанционной гамма-терапией может быть применен менее травматичный и новый метод лечения данного заболевания – БРАХИТЕРАПИЯ.
Брахитерапия (от греч. слова “brachios” – короткий, быстрый) – это современный и высокотехнологичный метод лечения рака предстательной железы, когда микроисточники радиоактивного излучения на основе I-125 вводятся внутрь пораженного органа.
При этом максимальная доза излучения доставляется непосредственно в опухоль без поражения прилегающих органов и тканей. В простату под контролем ультразвукового аппарата (или под контролем КТ – компьютерного томографа) специальными иглами вводят небольшие, меньше рисового зернышка, металлические капсулы с радиоактивным йодом, которые постепенно губят раковые клетки.
Каждое зернышко облучает очень маленькое пространство, поэтому прилегающие здоровые ткани и органы не подвергаются повреждению. Считается, что брахитерапия – наиболее щадящий на сегодняшний день метод лечения.
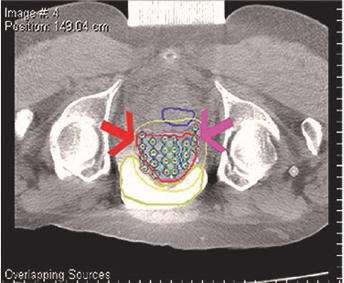
Первый этап подготовительный, в ходе которого проводится предимплантационное исследование пациента (обычно за 3-4 недели до операции) на мульти-спиральном компьютерном томографе, либо с помощью трансректального ультразвукового датчика. На основании полученных данных анализируется состояние и размеры предстательной железы, и семенных пузырьков. Возможно, после анализа полученных изображений, урологом будет принято решение о проведении биопсии семенных пузырьков с целью уточнения стадии заболевания и распространения злокачественных клеток. Полученные и проанализированные снимки передаются в компьютерную систему планирования лучевой терапии, где выполняется трехмерная объемная реконструкция анатомических структур: предстательной железы, семенных пузырьков, уретры, прямой кишки и мочевого пузыря.
Это необходимо, чтобы при предоперационной дозиметрии достоверно оценить лучевую нагрузку на все органы. Затем проводится предварительное планирование расположения источников и анализ дозного распределения. Главная цель – достижение равномерной дозы радиации в предстательной железе.
На полученных изображениях врач-уролог производит оконтуривание предстательной железы, уретры и прямой кишки.
Расчет доз осуществляется с помощью специальной компьютерной программы. Этот этап выполняет медицинский физик. Полученные изображения с контурами предстательной железы, уретры и прямой кишки импортируются в компьютерную планирующую систему. Зерна располагаются в узлах координатной сетки в соответствии с необходимой дозой излучения.
СОД очаговая доза рассчитывается на весь срок 596 суток активной персистенции импланта и составляет 160 Гр в предстательной железе. Нижний предел эффективной дозы составляет 144 Гр по контуру предстательной железы. При этом максимальная допустимая нагрузка на уретру составляет 140 Гр, прямая кишка и мочевой пузырь 30 Гр, причем не должна превышать 30% от объема, рассчитанного при планировании, обычно 1-1,5 см3 . Использование низких энергий гарантирует высокий градиент падения дозы. Нагрузка на прочие органы и структуры малого таза не превышает 0,1 Гр. Адекватность дозиметрического плана и доз оценивается лучевым терапевтом.
Существуют разные подходы к распределению зерен в разных центрах. Однако общим является расчет дозы, основанной на анатомии каждой индивидуальной предстательной железы, а не на принятом стандарте.
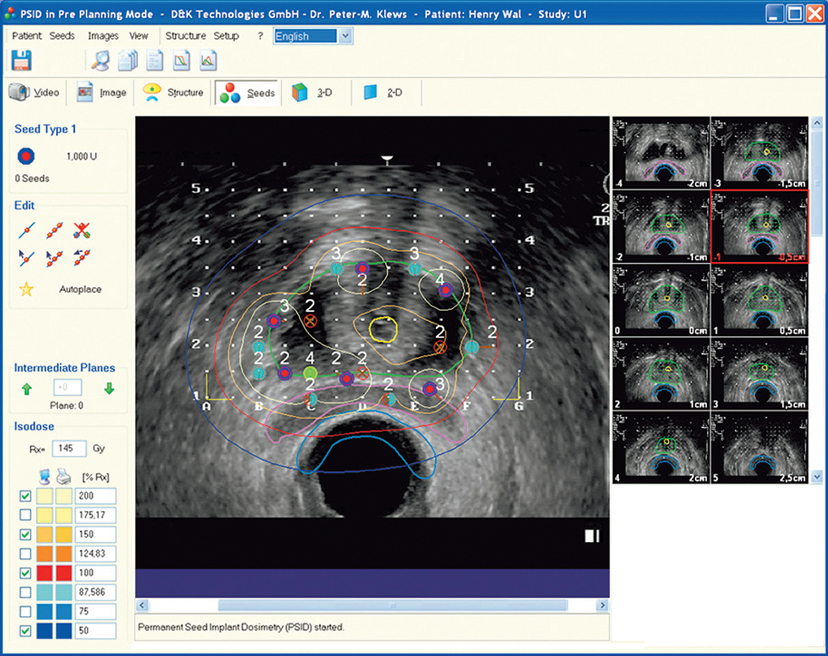
PSID 4.1.2 - программа планирования брахитерапии
Таким образом, подбирается наиболее оптимальная терапия с учетом индивидуальных особенностей каждого пациента. Благодаря тому, что микроисточники вводятся в предстательную железу, возможно увеличение дозы излучения в 2-3 раза по сравнению с дистанционной лучевой терапией, а с увеличением дозы излучения растут шансы излечения. Общепринятой дозой при имплантации изотопов радиоактивного йода (I-125) является величина в 140-160 Грей.

источник представляет собой цилиндрическую титановую микрокапсулу, внутри которой находятся изотопы радиоактивного I-125
В соответствии с ранее подобранным дозиметрическим планом, через специальный шаблон в предстательную железу вводятся иглы, которые доставят источники в ткань. Шаг шаблона – 2.5 мм. Столь маленький шаг позволяет добиться высокой точности расположения микрокапсул.
Рак предстательной железы — это проблема, с которой может столкнуться, пожалуй, каждый мужчина. К настоящему моменту не существует ни надежных методов профилактики этого заболевания, ни достоверных способов заранее узнать, каков риск столкнуться с бедой в каждом конкретном случае. Однако медики уже научились распознавать рак простаты на самых ранних стадиях, а также успешно лечить опухоли. Поэтому если онколог предполагает наличие рака простаты — не спешите впадать в отчаяние, ведь шансы на выздоровление высоки.
Стадии и особенности протекания рака предстательной железы
Предстательная железа — небольшой орган (размером с шарик для пинг-понга), расположенный у основания мочевого пузыря. Ее основная функция — синтез секрета, входящего в состав спермы, и участие в процессе семяизвержения.
Рак предстательной железы подразумевает появление и увеличение в размерах опухоли, способной к быстрому росту и метастазированию (переносу злокачественных клеток в другие органы и ткани). Это заболевание может возникнуть в любом возрасте, но в подавляющем большинстве случаев диагностируется у мужчин старше 60 лет.
Рак простаты — третье по распространенности онкологическое заболевание у представителей сильного пола в России после рака легких и рака желудка. Он обнаруживается у одного из пятнадцати мужчин старше 40 лет. Каждый год в мире злокачественные опухоли предстательной железы диагностируют у миллиона человек, и примерно каждый третий из них умирает вследствие данной патологии.
Почему развивается рак предстательной железы? Известно, что это сопряжено с изменениями гормонального фона, генетической предрасположенностью, неправильным питанием и воздействием некоторых других факторов, роль которых до сих пор окончательно не установлена.
От момента появления первой раковой клетки до развития симптомов, которые приводят мужчину на консультацию к врачу, обычно проходит несколько лет. По этой причине часто пациент оказывается на приеме у онколога с запущенной, разросшейся опухолью, которую сложно вылечить.
Всего принято выделять четыре стадии рака простаты:
- 1 стадия характеризуется маленькими размерами опухоли, отсутствием вовлечения в патологический процесс лимфатических узлов (туда раковые клетки могут попасть с током лимфы) и хорошим самочувствием больного. Как правило, на этой стадии рак простаты выявляется случайно — в ходе лечения другого заболевания железы. Прогноз для жизни пациента — благоприятный, терапия не занимает много времени.
- 2 стадия рака простаты означает, что новообразование увеличилось в размерах. Его можно прощупать — в ходе ректального осмотра (простата прилегает к передней стенке прямой кишки, поэтому врач способен дотянуться до нее пальцем). При этом симптомы заболевания зачастую по-прежнему не проявляются. Поэтому так важно регулярно проходить профилактическое обследование у уролога. Около 80% больных, у которых рак простаты был диагностирован на 2 стадии, выздоравливают.
- 3 стадия заболевания характеризуется разрастанием опухоли за пределы оболочки простаты. Раковые клетки обнаруживаются в лимфоузлах малого таза и в некоторых соседних органах. К этому моменту больной обычно ощущает дискомфорт: из-за деформации железы нарушается мочеиспускание, появляется боль в промежности. Чтобы победить опухоль, уже недостаточно сделать операцию, поэтому часто онкологи используют комбинированную тактику, сочетая различные подходы к уничтожению раковых клеток. Выживаемость на этой стадии рака простаты составляет менее 40%.
- 4 стадия подразумевает, что, помимо простаты, рак затронул отдаленные органы или лимфоузлы. Метастазы могут обнаруживаться в костях, легких, печени и т. д. Если пациент — пожилой человек с тяжелыми хроническими заболеваниями, врачи примут решение отказаться от операции в пользу щадящих методов терапии, которые продлят жизнь и облегчат страдания больного, хотя и не помогут победить рак.
Как будет проходить лечение рака простаты, зависит не только от стадии болезни. Важное значение имеет тип опухоли — его определяют при биопсии, взяв несколько образцов ткани и изучив их под микроскопом. Некоторые разновидности рака — например полиморфноклеточный рак предстательной железы — склонны к быстрому агрессивному росту, развитие других подвержено влиянию гормонов. Опытный онколог учитывает все эти обстоятельства, а также мнение самого больного, прежде чем принять решение о лечебной тактике.
Немаловажную роль играет и техническая оснащенность клиники. Не секрет, что многие современные технологии и лекарства попросту не доступны в отечественных онкологических центрах или находятся на стадии внедрения. И даже такие классические подходы, как хирургическое удаление простаты, могут значительно отличаться, что сказывается не только на успехе лечения, но и на качестве жизни пациента.
Предстательная железа — орган важный, но взрослый мужчина вполне способен прожить и без него. Поэтому, если рак не перекинулся на соседние органы и ткани, а состояние больного допускает проведение операции, онколог порекомендует мужчине радикальную простатэктомию — удаление простаты. На начальных стадиях болезни такой подход позволяет полностью вылечиться в короткий срок (пребывание в больнице занимает около 7 дней).
Между тем важно помнить, что речь идет о серьезном вмешательстве в работу организма, которое сопряжено с риском для жизни, а также приводит к некоторым неприятным последствиям. Так, больные нередко испытывают проблемы с мочеиспусканием на протяжении многих месяцев после операции, более половины мужчин — жалуются на исчезновение эрекции.
Щадящим вариантом хирургического лечения рака простаты является лапароскопическое вмешательство, при котором удаление простаты осуществляется через небольшие разрезы — всего несколько миллиметров длиной. В результате снижается риск послеоперационных осложнений, а сама процедура переносится пациентом гораздо легче.
Альтернативой традиционному хирургическому вмешательству может стать криохирургия опухоли простаты. Данный метод применим на ранних стадиях заболевания, когда рак еще не вышел за пределы органа. В ходе манипуляции пациенту в простату вводятся специальные иглы, через которые поступает жидкие аргон или азот. Низкие температуры разрушают ткани железы, а врач при помощи УЗИ контролирует, чтобы воздействие не повредило соседние органы. Как результат — железу не приходится удалять (хотя функции ее необратимо нарушаются). В последние годы криохирургию все чаще предлагают в качестве основного способа лечения рака простаты, который подходит больным всех возрастов.
Лучевая терапия назначается как отдельный метод лечения, так и в качестве дополнения к операции: до вмешательства или после него. Речь может идти как о внешней радиотерапии (когда пациент лежит под излучателем), так и о внутренней лучевой терапии, когда в тело больного вводят особые радиоактивные гранулы.
Внешняя лучевая терапия также имеет свои разновидности. Онкологи стремятся минимизировать губительное воздействие радиации на ткани тела, поэтому стараются как можно точнее направить пучок радиации на опухоль. В этом им помогают такие методы, как 3D-конформная лучевая терапия, лучевая терапия модулированной интенсивности (IMRT), стереотоксичечская лучевая терапия (SBRT) и протонная лучевая терапия. Каждый из этих подходов имеет достоинства и недостатки. Часто радиотерапия приводит к устойчивым расстройствам мочеиспускания и к эректильной дисфункции.
Внутренняя лучевая терапия (брахитерапия) значительно увеличивает эффект радиации за счет сокращения расстояния от ее источника до раковых клеток. Радиоактивные гранулы, используемые для процедуры, содержат радиоактивный йод, палладий и другие химические вещества, способные в течение длительного времени воздействовать на окружающие ткани. В зависимости от метода, эти гранулы могут находиться в организме многие месяцы (постоянная брахитерапия) или только во время лечебных сеансов (временная брахитерапия).
Химиотерапия применяется, как правило, в ситуациях, когда рак распространился по организму, поэтому воздействовать на болезнь нужно глобально. Препараты, используемые для лечения злокачественных опухолей простаты, назначают курсами, следя за результатами терапии и развитием побочных эффектов. Химиотерапевтические средства плохо влияют не только на рак, но и на здоровые ткани. Поэтому больные, проходящие такое лечение, часто страдают от расстройств пищеварения, слабости, потери волос и инфекционных заболеваний.
Данный вид лечения направлен на активацию иммунитета пациента. Раковые клетки чужеродны нашему телу, однако благодаря особым приспособительным механизмам они способны уклоняться от иммунного ответа.
Поскольку зачастую рост опухоли провоцируется действием мужских половых гормонов, на поздних стадиях рака простаты врачи могут назначать пациенту препараты, блокирующие синтез этих веществ. Обычно речь идет о пожизненном приеме фармацевтических средств. Такое лечение означает медикаментозную кастрацию: на его фоне затухает сексуальная функция. В сочетании с другими методами — например радиотерапией — прием гормонов способен привести к полному излечению пациентов, которым противопоказана радикальная простатэктомия. При этом медикаментозная кастрация обратима — после отмены лекарств.
Методы лечения рака простаты разнообразны, и каждый год появляется информация о новых эффективных подходах. Другими словами, безнадежных случаев, когда медицина оказывается бессильна помочь пациенту, уже почти не осталось. Важно найти врача, который подберет эффективную лечебную тактику. Не стоит отчаиваться — победа над раком во многом зависит от вас.
В России в прошлом году зарегистрирован новый препарат для проведения радионуклидной терапии – радий-223. Он показан пациентам на последних стадиях рака предстательной железы и призван продлить им активную жизнь.
Новое поколение онко-препаратов
Василию Андреевичу К. 69 лет, у него жена, сын, внучка. Третий год он борется с раком предстательной железы. Опухоль уже дала метастазы в кости, и Василия Андреевича начинают беспокоить боли.
За эти три года он уже прошёл курс радиотерапии, ему вводили препараты стронция (тоже радиоактивный изотоп). Но прогресса в лечении не случилось. Как только ему предложили стать первым пациентом в Челябинской области и в УрФО, лечить которого будут новейшим препаратом, он тут же согласился.
С раком предстательной железы на последних стадиях, когда опухоль метастазировала в кости, о полном излечении речь не идёт. Ранее радионуклидная терапия в таких случаях применялась только для снятия болевого синдрома. Радий-223 делает следующий шаг – он практически останавливает развитие матастазов, цементируя очаг.
«Представьте, - рисует картинку для наглядности представитель фармацевтической компании-производителя нового препарата, - раковые клетки из очага поражения через кровь или лимфу разлетаются по организму, поражая соседние органы и ткани. Чаще всего при такой локации рака метастазы образуются на копчике, крестце и в пояснично-крестцовом отделе позвоночника.
Секрет радия
Историей одного из своих первый пациентов, кому вводили радий-223, поделился заведующий отделением радионуклидной терапии медицинского радиологического научного центра города Обнинск, д.м.н. Валерий Крылов. Он приехал в Челябинск, чтобы познакомить врачей ЧОКОД и ЯМ с новым препаратом:
«Нашему первому пациенту с раком предстательной железы и метастазами мы ввели препарат в 2014 году. Его снимок буквально светился очагами поражения: весь позвоночник, кости таза. После 6 инъекций с интервалами в 4 недели мы не увидели этих очагов. Произошёл полный метаболический эффект. Сейчас пациент жив. У него всё хорошо.
Чем же так уникален радий? В чем его секрет?
«На сегодняшний день это единственный в мире зарегистрированный радиофармпрепарат на основе альфа-эмиттера (альфа-излучателя), - продолжает доктор. - С этим, как раз связана его высокая эффективность и безопасность. Потому что альфа-частицы имеют очень мощное поражающее действие: 1 альфа-частица может вызвать смерть 1 раковой клетки. В ранее используемых радиоактивных препаратах облучение производилось бета-частицами, их эффект значительно ниже: от 50-200 бета-частиц различной энергии вызовут тот же самый эффект.
Безопасная радиация?
Примечательно, что препарат нового поколения, по сути, не требует особых условий для хранения и использования.
Например, радиопрепараты йода являются сильно-летучими. Чтобы их использовать, нужны спецвентиляция и спецканализация в больнице, изолированные палаты для пациентов. Радий этого не требует.
Мало того, этот препарат в большинстве стран мира применяется амбулаторно и согласно российским нормам радиационной безопасности при введении не требует специального помещения. Излучение настолько мало, что не оказывает вредного воздействия на окружающих.
«Новый этап развития ядерной медицины – это альфа-излучатели, которые раньше не применялись, - считает главный врач Челябинского областного клинического онкологического диспансера Андрей Важенин.
Вся радиология, вся ядерная медицина начиналась именно с радия. Первые препараты радия супруги Кюри подарили институту Герцена в 1903-05 году.

Что такое брахитерапия рака предстательной железы
Брахитерапия рака простаты подразумевает уничтожение опухолевых клеток путем воздействия радиации. Для этого в железу внедряют заполненные специальным веществом иглы или зерна (капсулы) с радионуклидами. В качестве последних могут быть I-125 (микроисточник йода), Pd-103 (палладий), 198-Au (золото).

Капсула с изотопом
Цель брахитерапии – обеспечение предстательной железы такой дозой облучения, которая будет достаточна для уничтожения всех раковых клеток. Для этого важно правильно рассчитать дозировку, распределить зерна, чтобы диапазон воздействия охватывал контуры простаты, но облучение прилежащих тканей было бы минимальным.
Плюсы брахитерапии при РПЖ (раке предстательной железы):
- Минимальные кровопотери.
- Недолгий период реабилитации.
- Высокий шанс сохранения потенции.
- Возможно проведение у пожилых пациентов, состояние которых не совсем удовлетворительно.
- В большинстве случаев достаточно однократного проведения процедуры.
- Точечное воздействие на ткани.
- Незначительный период длительности побочных эффектов.
Основное условие успеха брахитерапии – тщательный отбор пациентов по показаниям.
Виды брахитерапии
По степени лучевой нагрузки и технике проведения выделяют низкодозную (постоянную, или LDR) и высокодозную (временную, или HDR) брахитерапию. Первая показана при раке простаты 1 и 2 степени. В качестве радиоактивного вещества используются йод или палладий. Эти вещества распадаются через несколько месяцев. Через год они станут биологически неактивными, но капсулы остаются в организме, не причиняя дискомфорта.
Высокодозная, или высокомощностная брахитерапия рака предстательной железы предполагает введение радиоактивного вещества (иридия-192) в заранее погруженные в ткани простаты полые иглы. Через 5-15 минут они извлекаются. Вещество подается в иглы через тонкие трубки, присоединенные к источнику – микроселетрону. Обычно процедура проводится трижды с интервалом в 2 дня. Временная брахитерапия показана пациентам с прогрессирующей карциномой, разрастающейся за пределы капсулы органа. При раке простаты 3 степени высокодозное излучение применяется в совокупности с внешним облучением.
По статистике 40% больных раком простаты получают чрезмерное лечение, поскольку их форма заболевания является клинически незначимой. В связи с этим остро стоит вопрос о развитии щадящих методов. Одним из таких является фокальная брахитерапия – зональное распределение источников излучения, при котором максимально высокая нагрузка направляется на только опухолевый очаг .

Примеры распределения лучевой нагрузки на простату методом фокальной брахитерапии: а – таргетная (ультрафокальная) схема; б – гемиаблативная (облучается одна доля простаты); в – фокусированная на видимый очаг; г – фокусированная на периферическую зону
Показания к проведению
Классическая низкодозная брахитерапия показана при локализованной опухоли (Т1-Т2), которая еще не проросла в простатическую капсулу. При принятии решения ориентируются на значение по шкале Глисона (градация найденных во время гистологии клеток опухоли по степени опасности). Оно должно быть меньше 7. Принимают во внимание и значение ПСА. Желательно, чтобы оно было в диапазоне от 10 до 20 нг/мл.
Основные критерии для назначения брахитерапии:
- Положительный прогноз на выживаемость пациента (более 5 лет), удовлетворительное самочувствие.
- Объем простаты по данным УЗИ не более 60 см 3 . Если железа слишком большая, то возможно ее уменьшение на 50% при помощи гормональной терапии – трехмесячного курса аналогов гонадотропин-рилизинг гормона.
- Отсутствие выраженных проблем с мочеиспусканием.
- В анамнезе пациента не должно быть трансуретральной резекции простаты. Брахитерапия допускается только в том случае, если последствия после ее проведения (рубцовые изменения) минимальны.
Если два последних условия игнорируются, то после брахитерапии очень высока вероятность развития недержания мочи.
Если по результатам гистологии раковые клетки обнаружены в различных областях простаты, то рекомендовано проведение брахитерапии в совокупности с гормональным лечением.

Показания к высокодозной брахитерапии
Лечит ли брахитерапия рак – эффективность метода
Согласно статистике, у пациентов со стадией опухоли простаты Т1 пятилетняя выживаемость составляет 100%, на Т2 – 75%, на Т3 – 60%. В среднем выживают 98% пациентов .
Успешного результата от постоянной брахитерапии изотопами I-125 либо Pd-103 (применяется в преимущественном большинстве клиник РФ) можно ожидать при соблюдении следующих условий:
- Локально ограниченная форма опухоли (стадия Т2а, статус N0M0);
- Значение по шкале Глисона меньше 6;
- Уровень ПСА не выше 10 нг/мл;
- Скорость потока мочи по итогам урофлоуметрии не меньше 15 мл/сек., объем остаточной мочи менее 50 мл;
- Объем простаты менее 50 мл.
От возраста пациента результат брахитерапии зависит не сильно. Гораздо большее значение имеет образ жизни: физическая и социальная активность. Говорить о победе над раком можно только через полтора года, в течение которых уровень ПСА будет стабильно низким, а по данным МРТ малого таза не обнаружится роста опухоли.

Подготовка к брахитерапии
Брахитерапии предшествует стандартный набор исследований:
- УЗИ, КТ малого таза.
- Коагулограмма.
- Анализ мочи и крови.
Полный список анализов и сроки их действия:

За сутки до брахитерапии следует соблюдать диету: минимум жиров, легкая пища, от ужина накануне лучше отказаться. Непосредственно в день процедуры рекомендуется сделать клизму для очищения прямой кишки. Пищу принимать нельзя.
Как проводится
Брахитерапия проводится в два этапа. На первом делают ТРУЗИ простаты. В мочевой пузырь предварительно вводится заполненный газом катетер, чтобы различить уретру. Затем на основании полученных УЗ-срезов формируют трехмерную модель, на которой определяют количество и места введения радиоактивных зерен. На втором этапе проводят собственно брахитерапию. Источник радиации герметичен, поэтому в дополнительных мерах предосторожности нет необходимости.

3D модель введения игл при высокодозной брахитерапии
Для проведения брахитерапии пациент укладывается в литотомическое положение (на урологическом кресле с разведенными ногами). Анестезия может быть как общей, так и местной. В прямую кишку помещают ТРУЗИ-датчик, изображение регулируют таким образом, чтобы оно максимально совпало с предварительно построенной моделью. Затем вводят иглы с зернами, которые могут быть размещены в них заранее, либо доставляются в ткани при помощи Мик-аппликатора. Последняя методика популярна за рубежом, а в России зерна выпускаются либо отдельно, либо нанизанными на рассасывающиеся нити (это исключает возможность их перемещения в тканях). Нити нарезают и заправляют в иглы-троакары. В качестве направляющего элемента для последних используется матрица, отверстия в которой совпадают с УЗИ-схемой.
Методикой последнего поколения является введение капсул при помощи игл Nucleotron. Зерна крепятся к кончику, а при доставке в нужную область отщелкиваются.
Под контролем КТ можно вводить капсулы в семенные пузырьки, область вокруг простаты. Такой метод контроля дает возможность проводить брахитерапию пациентам с железой более 50 см 3 в объеме, а также при наличии в ней конкрементов (камней).
Важным этапом является планирование дозы (составление дозиметрического плана). Эту задачу решает компьютерная программа (например, PSID 4.1.2) под контролем медицинского физика. Доза на всю железу составляет от 140 до 160 Гр. Мощность имплантата измеряется в греях (это мощность одной поглощенной дозы излучения).

Программный расчет дозировки 
Положение пациента во время брахитерапии 
Набор игл и матрица для облучения простаты 
Низкодозная брахитерапия при помощи матрицы
Сначала имплантируют капсулы в переднюю часть простаты, чтобы не затемнять область введения остальных. Всего имплантируется от 41 до 100 капсул. Процедура длится около 2 часов.
По завершении брахитерапии проводят цистоскопию (осмотр мочевого пузыря изнутри), чтобы не оставить случайно провалившихся или торчащих в просвет уретры зерен. КТ позволяет максимально четко идентифицировать каждое зерно и контуры железы, но сделать это можно и при помощи рентгенографии.

Рентгенография после брахитерапии 
Проведение высокодозной брахитерапии
Уровень ПСА после брахитерапии рака предстательной железы
После брахитерапии ПСА может сохраняться в крови еще длительное время. Первый раз анализ сдают через 3 месяца. Полностью маркер почти никогда не исчезает, поскольку какая-то часть деградировавшего эпителия все же сохраняется. Есть повод подозревать рецидив, если его уровень превысит 0,1-0,4 нг/мл. В течение первых трех лет может наблюдаться скачок ПСА до 0,2-0,3 нг/мл еще до достижения минимального порога.
Для контроля результатов также применяют биопсию (через год или позднее), УЗИ, КТ. Визуальные методы исследования в первый год проводят раз в 3 месяца, затем раз в полгода.
Последствия
Для брахитерапии в отличие от простатэктомии нехарактерно недержание мочи. Подобное может возникнуть только после ранее проведенной ТУР, поскольку лучевая энергия ослабляет наружный уретральный сфинктер. У пациентов после брахитерапии нередко развиваются другие осложнения со стороны мочеполовой системы: учащенное мочеиспускание, рези, чувство неполного опорожнения мочевого пузыря, но они проходят примерно за 3 месяца, в крайнем случае − через полгода. Для их лечения эффективнее всего альфа-адреноблокаторы.
Для брахитерапии характерна задержка мочи. Подобное случается у 5% пациентов. В таких случаях оптимальным методом лечения является периодическая катетеризация, при которой мочеиспускание нормализуется в течение нескольких недель.
У 10% пациентов в течение 5 лет после брахитерапии могут образоваться стриктуры (спайки) уретры. При необходимости они устраняются иссечением во время уретроскопии.

Стриктура уретры — это патологическое состояние, которое характеризуется сужением мочеиспускательного канала, и ведёт, в конечном итоге, к нарушению нормального оттока мочи при мочеиспускании
Что касается потенции, что в большинстве случаев она сохраняется. После брахитерапии качество эрекции и либидо сохраняется на 50-85%. Тут особую роль играет психологический фактор. Многие пациенты сами боятся вступать в половые отношения даже по истечении периода реабилитации. Им кажется, что уровень ПСА снижается слишком медленно, высока вероятность рецидива. От постоянного стресса падает потенция.
- Изъязвление или воспаление прямой кишки (1%).
- Некроз уретры (3%).
- Недержание мочи (6%).
- Цистит, уретрит (7%).
- Кровь в моче (1%).
Осложнения после брахитерапии минимальны по сравнению с радикальной простаэктомией или обычной лучевой терапией.
Реабилитация после брахитерапии простаты
После операции пациент около суток проводит в больнице. Катетер удаляют через 2-3 часа, после этого можно передвигаться, есть и пить. После высокодозной (временной) брахитерапии пациент может отправиться домой в тот же день, если нет противопоказаний.
На следующий день после введения зерен, а также через 4-6 недель обязательно осуществляют дозиметрический контроль для оценки лучевой нагрузки на органы. На расстоянии метра мощность излучения не должна превышать 10 мкЗв/час. Данные заносятся в выписку, которую пациент при необходимости может предъявить, например, в аэропорту. Этот же документ необходим при срабатывании металлоискателя (на зерна в простате).
В первые 2 недели нельзя подвергаться физическим нагрузкам, иначе капсулы начнут мигрировать в тканях простаты. Также не следует сидеть на одном месте дольше полутора часов, держать на коленях детей, ездить на велосипеде, ходить в баню. Кишечник и мочевой пузырь должны опорожняться своевременно, чтобы не давить на простату. Жирной, острой и жареной пищи, а также алкоголя нужно избегать. По истечении данного срока 80% пациентов без проблем возвращаются к своей нормальной жизни. К занятиям в спортзале можно приступать через 3 месяца.
В связи с тем, что после постоянной брахитерапии пациент на некоторое время становится носителем источника радиационного излучения, следует соблюдать особые меры безопасности. В первые 5 дней рекомендуется мочиться через марлю (чтобы капсула не попала в канализацию), а в течение 6 месяцев пользоваться презервативами во время полового акта. В первые 2 месяца после имплантации не следует долго находиться рядом с беременными женщинами.
Через полгода можно отменить данные меры предосторожности, поскольку носитель изотопа становится биологически нейтральным.
Стоимость брахитерапии простаты
Проведение брахитерапии за собственный счет стоит от 500000 руб. Например, цена в городском онкодиспансере СПб составит от 657400 руб. Что касается зарубежных клиник, то по сравнению с отечественными онкоцентрами стоимость брахитерапии в них возрастает в десятки раз при тех же результатах.
Отзывы пациентов
Заключение
Брахитерапия рака простаты является таким же радикальным методом лечения, как и хирургическое удаление, но негативных последствий в разы меньше. Многие пациенты из-за неосведомленности с опаской относятся к такого рода облучению, но бояться нечего: негативное воздействие на другие органы минимально, в случае рецидива можно провести или химиотерапию или повторную брахитерапию. Результат во многом зависит от квалификации врача. Отечественные онкологи в государственных специализированных центрах сейчас владеют техникой брахитерапии не хуже зарубежных.
Читайте также: