Лечение рака молочной железы вирусами
Иммунотерапия — метод лечения онкологических заболеваний, который использует ресурсы иммунной системы для уничтожения раковых клеток.
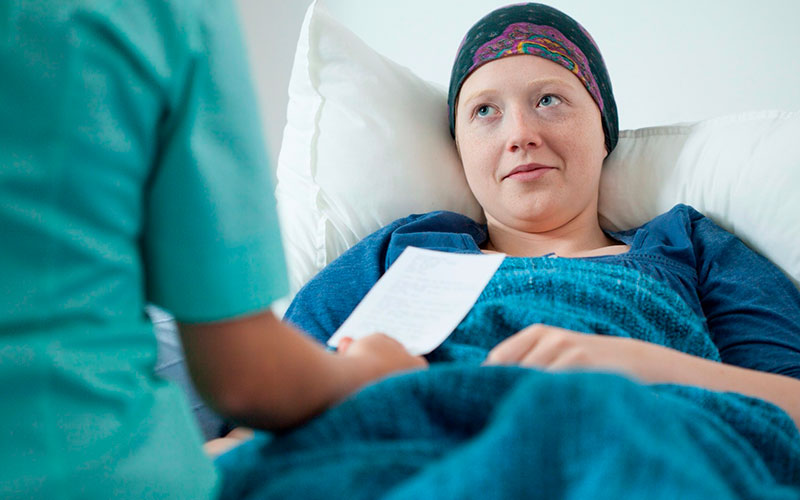
На данный момент иммунотерапия рака молочной железы — одно из наиболее активно развивающихся направлений в онкологии. Существует острая потребность в новых эффективных методах лечения, так как рак груди по-прежнему остается актуальной проблемой:
- Это один из наиболее часто диагностируемых у женщин типов рака. Он составляет 12% от всех онкологических заболеваний.
- Рак молочной железы находится на втором месте среди причин женской смертности от злокачественных опухолей.
- В 2012 году насчитывалось 1,7 миллиона новых диагнозов и полмиллиона смертей.
- Несмотря на то, что смертность от рака груди снижается, заболеваемость продолжает расти.
Виды иммунотерапии при раке груди
Выделяют две большие группы иммунотерапии при онкологических заболеваниях:
Существуют разные виды иммунотерапии при онкологических заболеваниях:
- противораковые вакцины;
- иммуномодуляторы;
- ингибиторы контрольных точек;
- онколитические вирусы;
- T-клеточная терапия;
- адъювантная иммунотерапия;
- моноклональные антитела;
- цитокины.
Но далеко не все это реально применяется в клинической практике при раке молочной железы. Многие методы пока проходят клинические испытания.
Виды препаратов
Злокачественные опухоли молочной железы могут обладать разными молекулярно-генетическими свойствами, и это определяет их восприимчивость к тем или иным методам лечения. На поверхности некоторых клеток увеличено количество белка-рецептора HER2. Его активация заставляет раковые клетки размножаться. Рак груди является HER2-позитивным примерно у каждой пятой пациентки.
В настоящее время американским Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрены для клинического применения три иммунопрепарата (их же относят к таргетным препаратам) из группы моноклональных антител: трастузумаб (герцептин), пертузумаб (перьета), трастузумаб эмтанзин (кадсила). Другие виды иммунотерапии пока проходят клинические испытания.

В каких случаях применяется иммунотерапия при раке молочной железы?
Моноклональные антитела применяют в случаях, когда рак является HER2-позитивным. Проверить это можно с помощью молекулярно-генетического анализа опухолевой ткани.
Иммунотерапия имеет некоторые преимущества перед химиотерапией:
- Она действует более прицельно, не повреждает здоровые клетки, и поэтому вызывает меньше побочных эффектов.
- Благодаря тому, что иммунопрепараты более безопасны, их можно вводить в течение длительного времени, применять в комбинациях с другими препаратами, не боясь усиления токсичности.
- Иммунная система может использовать в качестве мишеней разные антигены злокачественных опухолей, поэтому во время лечения у пациентов реже развивается резистентность.
Побочные эффекты
Моноклональные антитела при раке груди могут вызывать некоторые побочные эффекты. В большинстве случаев они мягкие, но иногда могут быть серьезными.
У некоторых женщин развивается застойная сердечная недостаточность. В большинстве случаев (но не всегда) она сохраняется в течение короткого времени и проходит после завершения лечения. Риски усиливаются, если ингибиторы контрольных точек применяют вместе с химиопрепаратами, особенно с доксорубицином и эпирубицином. Нарушения со стороны сердца проявляются в виде одышки, отеков на ногах, постоянной сильной усталости.
Пертузумаб может вызывать диарею.
Во время беременности моноклональные антитела опасны для плода, способны привести к его гибели. Поэтому, если есть вероятность, что пациентка беременна, врач не станет назначать данный вид иммунотерапии.
Иммунопрепараты, которые проходят клинические испытания для лечения рака молочной железы
- Блокаторы VEGF (вещества, которое выделяют раковые клетки, чтобы стимулировать рост новых сосудов): бевацизумаб (авастин), рамицирумаб (цирамза).
- Блокаторы Wnt (молекулярного сигнального пути, который способствует росту опухоли): вантиктумаб (OMP-18R5).
- Блокаторы HER3 (белка, который помогает опухолевым клеткам приобрести устойчивость к лечению): препарат LJM716.
- Блокаторы клеточных белков, которые помогают опухолям метастазировать: препараты CDX-011 и IMMU-132.

Онколитический вирус. Представляет собой генетически модифицированный вирус, который атакует и разрушает раковые клетки.
Адъюванты. Представляют собой химические вещества (чаще всего лиганды), которые связываются с рецепторами на поверхности клеток и усиливают или ослабляют иммунный ответ. Могут применяться отдельно или в сочетании с другими иммунопрепаратами.
Цитокины. Это небольшие информационные молекулы, которые могут стимулировать иммунную систему. В настоящее время при раке молочной железы проходят клинические испытания два препарата из этой группы: интерлейкин-2 и интерлейкин-7.
Стоимость иммунотерапии в Европейской клинике
Стоимость курса иммунотерапии — от 150 тыс. р.
Для подробного расчета получите консультацию врача.
В Европейской клинике доступны наиболее современные химиопрепараты, иммунопрепараты, таргетные препараты для лечения рака груди и других онкологических заболеваний, одобренные на территории России. Мы знаем, как помочь, если рак прогрессирует, если не помогает химиотерапия, которую вам назначили в другой клинике. Мы можем помочь пациентам, которые желают принять участие в клинических испытаниях новых препаратов. Свяжитесь с нами.

Среди добровольцев, которые испытывают эффективность нового метода, оказалась и Анастасия Заворотнюк.
Фото: GLOBAL LOOK PRESS
Пока коронавирус держит в страхе всю планету, российские ученые научились с помощью вирусов уничтожать злокачественные опухоли у онкологических больных. О перспективной технологии директор Института молекулярной биологии РАН Александр Макаров рассказал президенту Владимиру Путину время совещания по развитию генетических технологий. Этот способ лечения пока экспериментальный, он не прошел стадию клинических исследований. Среди добровольцев, которые испытывают эффективность этого метода, оказалась и Анастасия Заворотнюк.

Директор Института молекулярной биологии РАН Александр Макаров. Фото: Антон Новодережкин/ТАСС
По словам Александра Макарова у актрисы диагностирована глиобластома - злокачественная опухоль мозга. Родные Анастасии передали врачам образцы клеток ее опухоли и ученые подобрали вирусы, которые способны ее уничтожить. Однако в последний момент терапию отложили. О том, почему это произошло, и насколько эффективна новая методика, мы поговорили с член-корреспондентом РАН, профессором, главным научным сотрудником Института молекулярной биологии РАН Петром Михайловичем Чумаковым. Он заведующий лаборатории пролиферации клеток, которая разрабатывает новый метод лечения.
Не надо бояться вирусов
- Петр Михайлович, на чем основан механизм лечения онколитическими вирусами?
- Обычно люди на бытовом уровне боятся вирусов, но на самом деле большая часть вирусов не вызывает никаких болезней. А некоторые даже обладают противоопухолевым эффектом. Как это работает? Когда происходит злокачественная трансформация здоровой клетки в опухолевую, то такая клетка утрачивает природные механизмы противодействия вирусу. Это не надо путать с иммунитетом организма. Каждая клетка еще обладает собственным иммунитетом к вирусной инфекции.
- При появлении вирусной инфекции нормальная клетка начинает вырабатывать интерферон и вирусы вокруг этой клетки очень неуютно себя чувствуют и погибают. Опухолевая клетка лишена такой возможности, у нее этот защитный механизм подавлен. Поэтому вирусы очень хорошо размножаются в опухолевых клетках. Мы этим пользуемся. Если вирус не болезнетворный, то его можно с успехом использовать в терапевтических целях: когда мы доставим вирус в опухоль произойдет массированное размножение вируса и опухолевая клетка гибнет. А здоровые клетки при контакте с вирусом начинают вырабатывать интерферон и не заражаются. Кроме того, вирусы вызывают сильный ответ иммунной системы всего организма. Обычно иммунная система сама очищает организм от всего злокачественного, что там возникает. Но опухолевые клетки научились защищать себя от иммунной системы - они “выключают” белок, который “сигналит”, что клетка стала злокачественной. Возникает так называемая супрессия - подавление иммунного ответа в опухоли. А вирусы стимулируют выработку белков, которые эту супрессию снимают. В результате на опухолевые клетки наводится очень мощная реакция иммунной системы организма, которая завершает процесс онколиза - разрушения опухоли. Вот очень упрощенное описание того, что происходит.
Мы спасаем тех, от кого официальная медицина отказалась
- Какие виды рака можно лечить вирусами?
- Мы видим эффект для самых разных форм рака: это и глиобластома - опухоль мозга, и рак желудка, рак легкого, рак молочной железы, рак яичника… У нас нет официальных клинических испытаний, наши пациенты - это больные четвертой стадии, от которых официальная медицина отказалась. И эффект особенно заметен, когда нам больные поступают с прогнозом, что ему осталось жить неделю, максимум - месяц. А они живут уже по 2-3 года, у многих из них даже опухоли нет. Может быть, это ремиссия, может быть, это потом вернется. Но пока так.

Член-корреспондент РАН, профессор , главный научный сотрудник Института молекулярной биологии РАН Петр Чумаков. Фото: msu.ru
- Сколько пациентов через вас прошло - единицы, десятки, сотни?
- Несколько сотен. Мы ведь начали начали применять эту технологию всего три года назад, когда немного осмелели. Потому что до этого боялись: вдруг нас засудят. Сейчас мы страх потеряли, потому что видим, это безопасно - у метода практически нет побочных эффектов. Бывает только небольшое повышение температуры, что является положительным признаком: это говорит о том, что вирус попал в организм и он действует. Эта температура легко снимается обычными жаропонижающими препаратами, поэтому никакого вреда мы не наносим, а польза есть. И потом самая главная причина, почему мы не боимся - мы не берем за это деньги. Мы чисты в этом отношении.
- А как же пациенты о вас узнают?
- Это эффект сарафанного радио. Люди рассказывают друг другу. Мы боимся это широко заявлять, потому что у нас, естественно, ограниченные возможности, мы не можем много людей принять. А пациентов, от которых отказались врачи - огромное количество! Мы это видим даже по нашему ближнему окружению. Четвертая стадия рака - это когда никакая химия особо не действует. Обычно таких больных выписывают под наблюдение районного онколога. По сути это уже приговор.
Вакцина от рака
- Ваш директор рассказывал историю Анастасии Заворотнюк, ей тоже подбирали терапию, но в итоге не стали применять. Почему? Что не сложилось?
- Вы знаете, у них сейчас ремиссия наметилась. К нам приезжал ее муж, бывший спортсмен. Он оказался очень осторожным человеком и я его прекрасно понимаю. Он говорит: давайте подождем, ей сейчас лучше, если будет совсем плохо - тогда мы приступим. Но, по крайней мере, мы провели тестирование в культуре ее клеток и сейчас знаем, какой вирус на нее действует.

Актриса Анастасия Заворотнюк.
Фото: GLOBAL LOOK PRESS
- Вирусы подбираются индивидуально под пациента?
- Да, потому что опухоли очень индивидуальны, нет двух одинаковых опухолей. Если взять двух человек с глиобластомой, то если по морфологическим признакам это будет похоже, то по молекулярным признакам это очень разные опухоли. В настоящий момент мы ищем маркеры, по которым можно у больного провести быстрый тест и сказать, к какому вирусу опухоль чувствительна, а к какому - нет. Тогда, имея большой арсенал разных терапевтических вирусов, можно направленно под каждого пациента подбирать подходящий вирус. Так вот клетки из опухоли Анастасии Заворотнюк у нас в лаборатории хорошо пошли - они размножаются и мы можем их наработать сколько угодно. Это хорошо еще и потому, что на основе этих клеток можно сделать вакцину. Мы можем взять эти клетки, заразить их вирусом, а потом ввести ей в организм, и это будет стимулировать ее противоопухолевый иммунитет. Но это в том случае, если она снова обратится. Мы никогда не рекламируем и не уговариваем больных или родственников. Люди сами должны решать - рисковать или нет.
- А что людей настораживает, если противопоказаний нет?
- Все боятся вирусов, особенно во время нынешней пандемии. Когда они слышат словосочетание “лечение вирусами”, у них появляется страх в глазах. Но мы используем вирусы, которые никогда ничего не вызывали.
- Откуда вы их берете?
- Основная наша панель - это не патогенные энтеровирусы, выделенные из кишечника здоровых детей в возрасте до трех лет. Эти вирусы обеспечивают невосприимчивость детей к более серьезным инфекциям за счет того что у них вырабатывается интерферон. Кроме того, мы делаем инженерную селекцию и создаем генно-модифицированные вирусы, которые обладают усиленными противоопухолевыми свойствами. Но это пока в ограниченном масштабе.
Онколог рассказал о способе лечения рака, которым на совещании у Путина предложили спасти Анастасию Заворотнюк
На совещании по развитию генетических технологий в РФ директор Института молекулярной биологии РАН Александр Макаров рассказал о передовой технологии лечения рака на последних, терминальных стадиях. По его словам, исследователи подбирают вирусы, которые способны разрушать клетки опухоли больного. Макаров считает, что такой метод мог бы помочь, в том числе, актрисе Анастасии Заворотнюк. Она борется с глиобластомой, злокачественным образованием в головном мозге (подробности)
РАКА МОЛОЧНЫХ ЖЕЛЕЗ ВИРУСЫ (син.: вирус Биттнера, фактор молока) — группа вирусов сем. Retroviridae, возбудителей рака молочных желез мышей. Первый из них был открыт в 1936 г. амер. исследователем Дж. Биттнером, к-рый обнаружил, что рак молочных желез мышей может передаваться потомству через молоко матери, содержащее особый фактор.
Вирусы рака молочных желез мышей составляют группу антигенно родственных, морфологически идентичных вирусов, относящихся к онковирусам типа В и обладающих различной онкогенной активностью. Диаметр вириона 80—120 нм. Электронно-оптически плотный асимметрично расположенный нуклеоид вириона размером ок. 50 нм, окружен одинарной мембраной. Вирусы рака молочных желез мышей содержат 30% липидов, 2% РНК и 68% белка, инактивируются при нагревании до £° 65—66° в течение 30 мин., нечувствительны к воздействию больших доз рентгеновского излучения и могут длительное время (до нескольких лет) сохраняться при замораживании до —79°, лиофилизации и в 50% нейтральном глицерине.
Подобно другим ретровирусам (см.), вирусы рака молочных желез мышей содержат одноцепочечную РНК с мол. весом (массой) ок. 10 млн. дальтон и обратную транскриптазу (ревертазу). Помимо белка этого фермента, в составе вирионов различают 5 основных белков, два из к-рых являются гликопротеидами с мол. весом 52 000 и 34 000 дальтон, а три — негликозилированными белками (28 000, 18 000 и 12 000 дальтон).

Вирионы этих вирусов в большом количестве всегда присутствуют во всех раковых опухолях молочных желез (рис., а, б), в нормальной ткани молочной железы и в молоке мышей, в т. ч. и при первой беременности молодых самок тех линий, для к-рых характерна высокая частота развития опухолей молочных желез. Вирусы проявляют инф. свойства при введении новорожденным мышам; их можно титровать по способности вызывать опухоли молочных желез. Удовлетворительные методы титрования вирусов в культуре клеток не разработаны.
Вначале было показано, что исходный штамм вируса Биттнера содержит две разновидности — S и L. Причем штамм S вызывает опухоли у самок вскоре после родов и передается только через молоко матери и лишь у тех мышей, к-рые несут специфический аллель — MSe. Другой штамм вируса — L, напротив, не передается через молоко, однако одинаково хорошо распространяется со сперматозоидами и яйцеклетками. Этот вирус обладает менее выраженными бластомогенными свойствами, чем штамм S.
Впоследствии от нескольких линий мышей был выделен третий тип вируса — Р, к-рый аналогично штамму S был высокоонкогенен и передавался как с молоком, так и со сперматозоидами и яйцеклетками. Обработка мышей, считавшихся свободными от вирусов рака молочных желез, различными химическими и физическими онкогенами, а также гормонами приводит к продукции высокоонкогенного вируса, отношение к-рого к штаммам S, L и Р окончательно не установлено.
Общепризнанно, что практически нет ни одной линии мышей, не содержащей генетической информации ретровируса типа В. Передача эндогенного вируса ' у мышей различных линий осуществляется посредством неотделимого от генетического материала половых клеток ДНК-провируса, т. е. вирусных генов, находящихся в составе хромосомной клеточной ДНК. Выявлены доминантные клеточные гены, контролирующие чувствительность к онкогенному действию вируса. У мышей с высоким уровнем возникновения спонтанных опухолей молочных желез вирусы рака молочных желез передаются через молоко (экзогенная горизонтальная передача). Этот инф. вирус, вызывающий раннее развитие рака молочной железы у мышей первого поколения, отсутствует в молоке безвирусных мышей с низким уровнем возникновения спонтанных опухолей молочной железы. Вместе с тем в ДНК клеток нормальной молочной железы этих линий животных, а также в геноме клеток других паренхиматозных органов (придатки яичка, почки, вилочковая железа) содержатся ДНК-провирусные последовательности (провирус инфекционного вируса рака молочных желез мышей), к-рые передаются вертикально половыми клетками (эндогенная вертикальная передача). Эндогенные ДНК-провирусные последовательности ассоциированы с 3 независимыми парами хромосом мышей. Так, хромосома 4 содержит 2 копии ДНК вируса. Вероятно, 4 копии ДНК-провирусных последовательностей локализованы в хромосомах 15 и 17. В процессе индукции опухолей молочной железы онкогенами или гормонами постоянный уровень экспрессии (функционирования вирусных генов) эндогенного провируса резко увеличивается, и опухолевые клетки уже содержат в 30—50 раз большую концентрацию вирусных РНК.
Т. о., возможно, что онкогенное действие гормонов и хим. онкогенов опосредовано изменением экспрессии эндогенных вирусов рака молочных желез мышей, и, вероятно, вирусы, онкогены и гормоны являются коканцерогенными факторами (совместно ускоряющими) малигнизации клеток паренхимы молочной железы. Продукция инф. частиц вирусов происходит только в клетках молочной железы или опухолей этого органа. различия в чувствительности мышей к экзогенным вирусам не связаны с организацией и экспрессией генов эндогенных вирусов.
Различные линии мышей являются носителями специфичных для каждой из них типов вирусов рака молочных желез, к-рые отличаются по биол, характеристикам: по кругу хозяев, вирулентности, способу передачи, морфологии вызываемых ими опухолей и др. Вирусы рака молочных желез крыс, кошек и собак изучены мало. С раком молочных желез у крыс и кошек ассоциируют ретровирусы типа С, а у собак вирусные частицы обнаруживаются крайне редко. Большое внимание уделяют раку молочных желез обезьян в связи с выделением из спонтанно возникшей опухоли у макаки резуса ретровируса Мейсона—Пфайзера, отнесенного впоследствии к вирусам типа Б.
Предполагают наличие и у человека вируса, аналогичного или родственного вирусам рака молочных желез мышей. Эти предположения основаны на обнаружении в ультратонких срезах клеток раковой опухоли молочных желез человека, а также в клетках эпителия вирусных частиц, в нек-рых случаях морфологически неотличимых от вирусов рака молочных желез мышей. В клетках рака молочных желез человека обнаружены основные компоненты ретровирусов, а в нек-рых случаях и вирионы. С помощью иммунол. методов были получены данные, свидетельствующие о возможном наличии у человека белков, близко-родственных или даже идентичных основным белкам вирусов рака молочных желез мышей.
Механизм онкогенного действия вирусов рака молочных желез мышей чрезвычайно сложен и окончательно не выяснен. Генетические факторы влияют на гормональный баланс, репродукцию вируса, его передачу и восприимчивость клеток. Бластомогенная активность вирусов зависит от дополнительных факторов: диеты, численности популяции мышей, температуры среды и др. Для малигнизации клеток вирусами необходима постоянная стимуляция их пролиферации и дифференцировки маммотропными гормонами; в то же время длительная обработка этими гормонами приводит к малигнизации клеток паренхимы молочной железы, содержащих в ДНК гены эндогенных и экзогенных типов вируса рака молочных желез мышей.
Библиогр.: Городи лова В. В. Специфический антиген рака молочных желез и его значение в этиологии данной опухоли, М., 1961, библиогр.; Крюкова И. Н. О возможной ассоциации онковирусов, родственных онковирусам типа В мышей, с карциномами молочных желез человека, Эксперим. онкол., т. 2, № 4, с. 13, 1980; Gross L. Oncogenic viruses, Oxford а. о., 1970.
57-летняя актриса Келли Престон , жена Джона Траволты, умерла от рака груди после двух лет борьбы с заболеванием. О постигшей утрате рассказал Джон Траволта в социальных сетях.
Несмотря на всю опасность рака молочной железы, его можно победить. Например, это получилось у актрисы Джейн Фонды, писательницы Дарьи Донцовой, певицы Кайли Миноуг и других женщин. Киноактриса Анджелина Джоли и вовсе сделала предупреждающую операцию из-за генетической предрасположенности к раку груди (от этого онкозаболевания погибли мать и тетя звезды).
Рак молочной железы — это самое распространенное раковое заболевание у женщин во всем мире. На него приходится 16 процентов всех случаев заболевания раком среди женщин, по данным Всемирной организации здравоохранения.
В России этот показатель также высок. Как сообщает НМИЦ онкологии им. Н. Н. Блохина, ежегодно в стране выявляется около 50 тысяч случаев рака груди, что составляет примерно пятую часть от всех опухолей у женщин. Более 40 процентов случаев диагностируется на поздних стадиях. Каждый год от этого онкозаболевания умирают более 20 тысяч россиянок.
Важно помнить, что ранний скрининг дает шансы женщинам сохранить грудь и обойтись без хирургического вмешательства, уверены в ЦКБ №2 им. Н. А. Семашко. По данным онкологов, только 20 процентов женщин живут пять лет и более, если выявить рак молочной железы не на ранней стадии.
Что влияет на развитие онкологии
На развитие рака молочной железы у женщины (впрочем, от этого вида онкологии могут страдать и мужчины, но в меньшей степени) влияют такие факторы как: гормональный статус, различные хронические заболевания, ожирение, вирус папилломы человека, наследственность и т.д.
Например, если в одной семье по женской линии (бабушка, мама, тетя) была онкология, то последующие поколения девочек находятся в группе риска. Их шанс заболеть раком на 20 процентов больше, поэтому они должны находиться под активным наблюдением специалистов.
Наиболее яркий пример семейной онкологии груди связан с американской актрисой Анджелиной Джоли. Несколько лет назад она удалила молочные железы. Согласно ее анализам, вероятность развития рака груди, от которого умерли бабушка и мама актрисы, составляла 87 процентов. Джоли выбрала радикальное решение, также есть вариант с активным наблюдением и обследованием раз в полгода по персонально разработанному плану.
Отдельно как причину возникновения рака важно отметить вирус папилломы человека: он приводит к развитию различных опухолей в организме. Вирус выявляется у многих людей, примерно у 80 процентов, но его наличие опасно только в активном состоянии — когда иммунитет низкий. Когда иммунитет в порядке, то через два-три месяца после заражения вирус в крови может войти в латентное состояние.
Однако до конца от него избавиться нельзя, кроме этого ВПЧ легко передается. Против вируса существует вакцинация, она проводится до подросткового возраста у девочек. К сожалению, есть данные, что во взрослом возрасте прививка уже не работает. После вакцинации риск развития женской онкологии у девочек снижается до минимума.
Также возрастные изменения могут стать причиной опухоли. 50 лет — средний возраст женщины, когда чаще всего диагностируют рак груди. Но это не исключает более ранних случаев.
Симптомы рака молочной железы
Если опухоль не гормонально зависимая, то будет другой план лечения. Это влияет на диагностирование, которое может продолжаться до двух и более недель.
Хирургическое удаление груди
Потеря груди для женщины является сильным стрессовым фактором. В связи с этим разработано множество техник органосохраняющих операций – с помощью протезов, собственных тканей и т.д. Есть только одно но — у этих операций очень узкие показания.
Если перед онкологами стоит выбор сделать женщине органосохраняющую операцию с высоким риском развития рецидива или удалить железу с низким риском, то решение будет очевидным. Потому что от рецидива рака человек погибает. Органосохраняющую операцию можно сделать только на ранних стадиях развития опухоли, и чем она меньше, тем больше шанс сохранить грудь.
Также в лечении есть важный момент. Женщины с раком молочных желез очень редко подвергаются только хирургическому лечению. В основном это комплексный подход: химиотерапия, лучевая терапия и хирургия. Например, после операции женщина еще должна пройти курс облучения и делать это с протезом нельзя.
В случае с химиотерапией падает иммунитет, установка протеза также исключена, потому что может начаться воспалительный процесс.
Другой вопрос — зачем подвергать женщину лучевой и химиотерапии, если опухоль уже удалена. Затем, что врачи не могут точно знать, не осталось ли у нее микрометастазов. Рак молочной железы относится к высокоагрессивным видам онкологии, способный давать регионарные и отдаленные метастазы. Даже идеально проведенная операция и полное обследование не дает стопроцентной гарантии, что раковых клеток не осталось.
Современные способы лечения
Существует три вида лечения рака: лекарственное, лучевое и хирургическое, эти способы прошли огромный эволюционный путь. Так, операции сейчас проводятся малоинвазивным способом, который обеспечивает минимальное вмешательство в организм. Процедура, как правило, подразумевает использование эндоскопических инструментов. Например, через небольшой разрез можно удалить опухоль, если операция органосохраняющая.
Развитие лучевой терапии позволило больше облучать опухоль, чем окружающие ее ткани. Например, это могут делать такие аппараты как кибер-нож и гамма-нож. Луч установки испаряет только область опухоли, и поскольку границы удаления новообразования очень четкие, то аппарат называют ножом. Окружающие ткани повреждаются минимально.
У лекарственных препаратов тоже произошли существенные изменения. Если раньше химиопрепараты действовали на опухоль, ткани вокруг нее, да и на весь организм в целом, то сейчас разрабатываются целевые препараты. Они действуют на определенные факторы, например опухолевую прогрессию, и очень помогают в традиционной химиотерапии.
Методы и схемы лечения рака молочной железы на начальных и поздних стадиях отличаются количеством препаратов, а также их токсичностью и дозировкой. Поэтому важно не затягивать с терапией, так как в дальнейшем организму будет очень сложно выдержать медикаментозный объем и восстановиться. Существуют старые проверенные методы и новые разработки в плане лечения онкологии грудной железы. В сложных случаях врачи применяют все возможные варианты и схемы, чтобы сохранить и продлить жизнь пациентке.
Можно ли вылечить рак груди без хирургического вмешательства
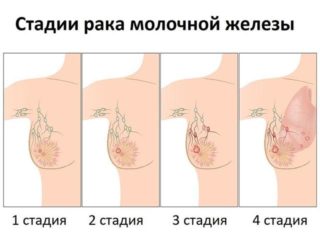
Чем раньше обнаружена опухоль, тем больше шансов, что ее можно вылечить консервативными методами. Основными показателями для медикаментозного лечения являются:
- Стадия онкологического процесса. На 1 – 2 этапе роста опухоли обычно не бывает метастазов и новообразование не выходит за рамки молочной железы, не прорастает окружающие ткани, поэтому удалить его и провести финальное уничтожение атипичных клеток химиолучевой терапией вполне возможно.
- Гистологические показатели рака. Хорошо поддаются лечению высокодифференцированные формы, когда клетки имеют рецепторы к эстрогену или другим факторам роста.
После того как опухоль частично уменьшается и ее контуры становятся более четкими, проводится хирургическое вмешательство, а далее химия и облучение, чтобы уничтожить оставшиеся атипичные клетки в тканях.
Прогнозы и особенности лечения на разных стадиях
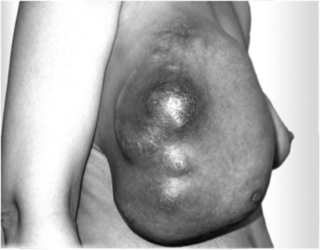
Опухоли молочной железы можно разделить на две большие группы- узловые и диффузные. Первая группа лучше поддается лечению и прогнозы более благоприятные, так как узел можно удалить целиком, а оставшиеся раковые клетки уничтожить химией или облучением.
Диффузный рак не имеет четких границ, хуже поддается лечению и сложнее диагностируется. Прогноз заболевания зависит от стадии процесса и степени вовлеченности окружающих тканей.
Легче вылечить гормонозависимые новообразования, чем низкодифференцированные опухоли, так как раковые клетки имеют рецепторы и не способны размножаться, если в организме нет соответствующих гормонов. При низкодифференцированных опухолях подобрать лечение сложнее – здесь все зависит от того, насколько запущен процесс.
По статистике на 1 стадии рака можно полностью вылечить до 95% пациенток. На второй – до 76%, на третьей до 50%. На четвертой только 10% женщин имеют шанс прожить 5 лет после лечения.
Известны случаи полного исцеления на поздних стадиях, такие женщины подключали все возможности, в том числе и внутренние психологические резервы.
Прогноз лечения зависит также от квалификации врача: насколько индивидуально была разработана схема терапии рака и учтены все показатели. Финансовые возможности пациентки играют важную роль, так как существуют новейшие разработки в области химиотерапии и хирургического вмешательства, способные более качественно воздействовать на опухоль. Стоимость такого лечения в разы выше, чем при обычном подходе. Эффективность, соответственно, также более высокая.
Методы лечения патологии
В разных ситуациях используются методы, наиболее подходящие для лечения именно этой женщины с ее типом рака – его скоростью распространения, зависимостью от половых гормонов, наличием или отсутствием метастазов.
Самым легким в плане лечения считается высокодифференцированный гормонозависимый рак. Для этой цели используются вещества, которые блокируют синтез эстрогена в организме, а также прекращают выработку ароматазы – фермента, с помощью которого осуществляется перевод андрогенов в эстроген. В некоторых случаях предлагается удаление яичников, чтобы полностью остановить производство эстрогена. Опухоль начинает разрушаться, так как прекращаются поставки питательных веществ – в данном случае эстрогена.
Лекарства имеют разный принцип действия:
- Блокируют рецепторы эстрогена в опухоли – Тамоксифен, Торемифен, Ралоксиифен, Летразол, Экземестан.
- Подавляют производство гормона – Аромазин, Аримидекс.
- Воздействуют на гипоталамус, который дает сигнал к производству эстрогена – Золадекс.
Если совмещать овариэктомию (удаление яичников) и гормональное лечение рака на ранней стадии, есть шанс полностью избавиться от опухоли и предотвратить рецидивы. Минус в том, что у молодых женщин в репродуктивном возрасте полностью утрачивается детородная функция и наступает ранний климакс.
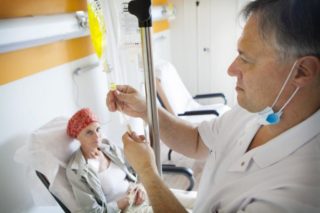
Химиотерапия проводится курсами от 4 до 16 сеансов, в перерывах между которыми женщина может восстанавливаться и отдыхать. Это высокотоксичный метод, рассчитанный на массовую гибель раковых клеток, так как под воздействием препаратов мутированные агенты уничтожаются быстрее, чем здоровые клетки организма. Существенный минус – среди здоровых клеток есть такие, которые быстро размножаются и быстро погибают – это клетки красного костного мозга.
Лечение рака молочной железы химиопрепаратами отличается количеством медикаментов, степенью их токсичности и объемом лекарственных средств в один курс. Различают красную, голубую, желтую и белую химию. Отличаются препараты каждой группы тем, насколько токсичны они для раковой опухоли и организма в целом.
Самые популярные лекарства – Метотрексат, Циклофосфамид, Фтораруцил, Доксорубицин, Эпирубицин.

Этот способ еще недостаточно изучен и востребован в практике лечения злокачественных опухолей, но отзывы об иммунотерапии при раке молочной железы позволяют говорить о нем, как об очень перспективном методе.
Существует три разновидности:
- Активная иммунотерапия, при которой в организм вводятся различные сыворотки и клеточные структуры, формирующие стойкий иммунитет.
- Пассивная – вводятся препараты, которые приготовлены из тканей организма, в котором опухоль регрессировала или находится в стадии ремиссии.
- Адаптивная, при которой вводятся лимфоциты в большом количестве для борьбы с раковыми клетками.
Исходя из принципа иммунотерапии, победить рак молочной железы можно, научив иммунную систему женщины эффективно бороться с ним на клеточном уровне.
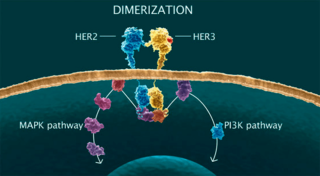
Суть таргетной терапии заключается в следующем:
- отключить механизмы, способствующие росту и делению клеток;
- спровоцировать естественную гибель атипичных клеток;
- доставить лекарства непосредственно в клетку, минуя здоровые ткани.
В результате исчезают метастазы, происходит ремиссия опухолевого процесса. Плюс методики в том, что она не имеет противопоказаний к народным методам лечения рака и не изматывает организм.
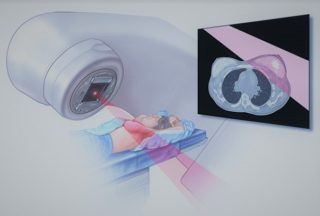
Облучение проводится несколькими видами – гамма излучение, бета излучение, рентгеновские лучи, нейтронные лучи. Проводится после операции для снижения риска рецидива.
Радиотерапия бывает дистанционной, при которой облучается вся грудная клетка или большая ее площадь. Брахиотерапия – луч настраивается целенаправленно и воздействует только на опухоль. В запущенных формах рака не применяется.
Назначается в следующих случаях:
- при множественной узловой форме;
- при начальной стадии метастазов в кровеносных сосудах и лимфоузлах;
- при поражении глубоких слоев тканей – большой грудной мышцы, подмышечных лимфоузлов;
- если опухоль проросла окружающие ткани.
Имеются побочные негативные эффекты – выпадение волос, нарушение кроветворной функции и изменение состава крови. Данные явления считаются временными, но в некоторых случаях, когда организм сильно ослаблен лечением, приходится лечить последствия лучевой терапии медикаментозно.

Аппарат Интрабим – это инновационная методика облучения, применяемая во время операции. Позволяет избежать послеоперационного лечения и дополнительной нагрузки, а также ускорить выздоровление, при этом меньше вреда нанести здоровым тканям. Луч направляется непосредственно на участок, в котором предположительно находятся раковые клетки.
Применяется в случае диффузного рака, который сложно оперировать. В место опухоли вводится газ, который снижает температуру в тканях до минус 170 градусов, после заморозки молочную железу размораживают, затем снова замораживают. Такую процедуру проводят несколько раз. Зависит от объема опухоли.
В результате криовоздействия происходит разрушение питающих опухоль сосудов, после чего она начинает регрессировать. Криотерапия считается малоинвазивным хирургическим вмешательством.
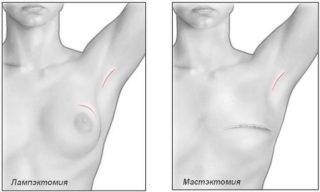
Рак груди лечится удалением опухоли, если консервативное лечение не помогает. Операции бывают малоинвазивными и радикальными – с удалением всех тканей молочной железы.
Виды хирургических операций:
- Если размер опухоли не превышает 2,5 см в поперечнике, проводится органосохраняющая операция – лампэктомия.
- Простая мастэктомия проводится, если в лимфоузлах не обнаружено раковых клеток. Удаляется вся молочная железа, но лимфатические узлы не затрагиваются.
- Радикальная модифицированная мастэктомия – удаление лимфоузлов и молочной железы.
- Радикальная мастэктомия – удаление железы, лимфоузлов и грудных мышц.
- Подкожная мастэктомия – удаляются все ткани, кроме кожи и соска, чтобы впоследствии можно было провести реконструкцию молочной железы.
После операции обычно проводится заключительный этап лечения – химиотерапия или облучение.
Альтернативные способы лечения рака
Альтернативные методики успешно применяются, но данных об их эффективности, безопасности или наоборот – нет. С одной стороны, фармацевтическая промышленность не заинтересована в дешевом избавлении от рака, поэтому исследования насчет эффективности альтернативных или народных методов лечения не проводятся. С другой стороны, люди предпочитают быть уверенными в излечении, поэтому следуют традиционным методам.
Среди альтернативных способов: прием соды, использование ядовитых растений, сокотерапия, чистый керосин и другие средства. На поздних стадиях лечение альтернативными методами может быть опасно, так как достоверно не известно, как именно они работают.
Читайте также:

