Лечение обширных комбинированных гемангиом и гемангиом сложной



- На заглавную
- О журнале
Поиск
Комбинированное лечение гемангиом у детей
Представлен обзор литературы и результаты собственных практических наработок по лечению гемангиом у детей. Отмечены хорошие результаты комбинированного применения склеротерапии и лазерного лечения гемангиом, удобство применения данной методики в амбулаторных условиях и однодневного стационара.
The review of literature and results of own practical operating time on treatment hemangioma at children is presented. Good results of the combined application of sclerotherapy and laser treatment hemangioma, convenience of application of this technique in out-patient conditions and an one-day hospital are noted.
Гемангиома новорожденных является наиболее частой опухолью этого периода. По сведениям части авторов, она встречается в 1,1-2,6% случаев [1], по другим данным — в 4-10% [2]. Отмечается преимущественно у девочек, недоношенных и маловесных детей. Гемангиомы относятся к сосудистым новообразованиям, имеют врожденный характер, как правило, не опасны для жизни, но причиняют немало страданий родителям и самому ребенку. Некоторые авторы указывают на способность гемангиом к самопроизвольному излечению и предлагают ограничить показания к лечению, ссылаясь на возможность гемангиом к спонтанной регрессии. Мы считаем, что необходимо начать лечение как можно раньше, так как предсказать возможность спонтанной регрессии очень трудно, а раннее начало лечения дает хороший шанс для выздоровления больного. Несмотря на свою доброкачественность, гемангиомы отличаются быстрым прогрессирующим ростом. Разрастаясь, они разрушают окружающие ткани и наносят ребенку значительный косметический ущерб [3]. В первую очередь это относится к гемангиомам лица и головы. При локализации гемангиом на веках, ушной раковине, носу, а также на слизистой ротовой полости, помимо косметических проблем, могут возникать чисто физиологические в виде нарушений функций некоторых важных органов (зрение, слух, дыхание). Поэтому можно сказать, что гемангиомам присущи некоторые черты клинически злокачественного течения.
Особенностью течения гемангиом является непредсказуемость их “поведения”: порой небольшая, точечная гемангиома щеки в течение 2-3 недель может превратиться в обширную и глубокую ангиому сложной анатомической локализации (например, гемангиома околоушной области, без тенденции к остановке роста). Расчет на спонтанную регрессию в этих случаях оказывается неоправданным, а потеря времени идет явно не на пользу больному.
Одной из очень серьезных проблем является лечение изъязвившихся гемангиом, сопровождающихся инфицированием и кровотечением. Иногда под воздействием незначительных травм, гемангиомы повреждаются, инфицируются и, изъязвившись, трудно поддаются традиционным методам лечения. Процесс лечения занимает всегда много времени, принося большие неприятности детям и, кроме того, требуя больших материальных затрат. Это тоже одна из актуальных проблем, требующая правильного решения.
Основными методами лечения являются: хирургический, склерозирующий, электрокоагуляционный, радиационный, гормональный, лазерный, криогенный. Наличие большого количества методов лечения свидетельствуют о том, что ни один из перечисленных не является универсальным, а их многообразие затрудняет выбор способа лечения конкретного больного [4].
Каждый из методов обладает определенными преимуществами, и вопрос стоит лишь в том, какой из них является наиболее рациональным, с точки зрения простоты, доступности, удобства для больного, эффективности по косметическому и функциональному результату. Рассмотрим основные методы лечения.
Лечение гемагиом оперативным путем.
Хирургический метод – один из первых методов, который использовался при лечении гемангиом и в настоящее время не потерял своего значения [5]. Удаление небольших по величине и глубине гемангиом обычно проводится радикально в пределах здоровых тканей. Это возможно на таких участках, где имеется хорошая подвижность кожи, и в косметическом плане менее значим послеоперационный рубец. Значительно сложнее иссечь обширную и глубоко расположенную сосудистую опухоль, так как трудности, возникающие при этом, обусловливаются возможным кровотечением, а значительный объем поражения не всегда возможно закрыть местными тканями. Кроме того, проведение оперативных вмешательств на лице часто связано с риском повреждения нервных стволов, а образование рубцов после удаления гемангиом в области суставов может привести к ограничению функций.
Техника требует бережного отношения к окружающим здоровым тканям. Большая часть пациентов — дети первых месяцев жизни, поэтому проведение радикальной операции требует проведения общего обезболивания, что является несомненным риском.
Электрокоагуляция и криотерапия.
Данные методики просты в проведении и не требуют наличия дорогостоящей аппаратуры, нет необходимости в проведении глубокого общего обезболивания. Вместе с тем попытки убрать крупные гемангиомы могут привести к развитию как первичных, так и вторичных кровотечений, повреждению крупных нервных стволов, например лицевого нерва. Массивный некроз тканей после данных процедур приводит к длительному заживлению, зачастую с инфицированием раневой поверхности. Даже при хорошем послеоперационном течении заживление заканчивается весьма посредственно в эстетическом плане [6].
Таким образом, метод прост и эффективен, но только при мелких гемангиомах (до 0,5 см 2 ). При более крупных гемангиомах этот метод не неэффективен, кроме того, на месте деструкции образуются грубые рубцы.
Существуют различные варианты медикаментозного лечения гемангиом, наиболее часто используется кортикостероидная терапия (преднизолон). Впервые кортикостероиды были применены Meeks, Jay, Heaton (1955) с целью повышения свертываемости крови у детей с тромбоцитопенией, сочетавшейся с обширными гемангиомами. Применение преднизолона обнаружило параллельный эффект – уменьшение гемангиом. Это послужило толчком для использования гормональных препаратов при лечении гемангиом.
Механизм действия при пероральном введении преднизолона сводится к изменениям межсосудистой соединительной ткани и стенок сосудов, где и происходит усиленное коллагенообразование. Новообразованная соединительная ткань сдавливает сосуды, которые подвергаются атрофии и запустевают, что ведет к исчезновению гемангиом.
А.В. Буторина, основываясь на опыте гормонального лечения самых обширных и самых сложных гемангиом у 630 детей, делает вывод, что в первом полугодии жизни гормональная терапия наиболее эффективна. Одним из важных результатов применения гормонов явилась задержка роста гемангиомы с постепенной их регрессией, но полного излечения данным методом удалось добиться только у 2% больных [2].
Таким образом, гормонотерапия рассматривается не как самостоятельный, а как вспомогательный метод лечения гемангиом. Этот метод лечения дает возможность замедлить, а иногда прекратить рост гемангиом для последующего активного лечения.
Короткофокусная рентгенотерапия, по мнению многих авторов, является высокоэффективным методом лечения гемангиом наружных покровов у детей. И.Е. Бринд в процессе своей работы пришел к выводу, что лучи рентгена в дозах не выше 600 рад вызывают в стенках сосудов функциональные изменения, и лишь при дозе свыше 600 рад в стенках периферических сосудов возникают морфологические изменения.
Общая доза облучения в 2000 рад является вполне достаточной для достижения желаемого лечебного эффекта. По данным Г.А. Федореева, при общей дозе в 2000 рад, хорошие косметические результаты были получены в 67,5 % случаев.
Однако лучи рентгена при энергичном или длительном применении оказывают неблагоприятное воздействие на организм, особенно растущий. Они оказывают вредное влияние на ростковую зону метаэпифизов трубчатых костей, тормозя их рост и вызывая трофические изменения в костной ткани. Кроме того, часто бывают неудовлетворительные косметические результаты – облысение на волосистой части головы, атрофия кожных покровов с лишением их естественной пигментации и развитие незаживающих трофических язв.
Лечение химическими веществами основывается на действии некоторых химических веществ на опухоль, вызывающих в ней асептическое воспаление или тромбирование. Это приводит к запустеванию гемангиомы и замещению соединительной тканью. Впервые этот метод применил Schwalbe в 1872 г., используя 50 о спирт. В настоящее время наиболее часто используется 70 о спирт или тромбовар, фибро-вейн, этоксисклерол. Вводятся химические вещества инъекционным методом или же посредством электрофореза.
Признаками успешного лечения гемангиом является прекращение ее роста и постепенное запустевание последней за счет разрастания соединительной ткани с хорошими косметическими результатами. При больших гемангиомах вводится большое количество склерозирующего вещества, приводящего к значительному разрушению опухоли с образованием изъязвления, а после длительного заживления образуются грубые рубцы. Недостатком склерозирующей терапии является болезненность и длительность лечения [7].
Таким образом, склерозирующий метод лечения гемангиом простой и радикальный, но болезненный, требует длительного лечения, оставляет после себя грубые гипертрофические рубцы и в некоторых случаях тяжелые функциональные осложнения.
Лазерное и фотолечение гемагиом.
Лазерное лечение сосудистых нарушений основано на тепловом воздействии. Эффект заключается в тепловом разрушении сосуда без изменения структуры прилегающих тканей [8]. Для обеспечения такой избирательности действия лазера необходимо:
1. Использовать лазерное либо мощное световое излучение, слабо поглощаемое эпидермисом и хорошо поглощаемое кровью — область 490-590 нм, где хромофором является преимущественно оксигемоглобин, область 490-700 нм с деоксигемоглобином в качестве хромофора-мишени, и длина волны 1064 нм, хорошо поглощаемая стенками сосудов.
2. Учитывать время релаксации сосуда (TR), поскольку от него зависит выбор параметров лазерного излучения. Время тепловой релаксации соответствует периоду, необходимому для перехода энергии за пределы сосуда и снижения температуры в центре сосуда до 50% от максимально достигнутого значения.
Выбор режима лазерного воздействия определяется длительностью импульса. В настоящее время различают два метода:
1. Селективный фототермолиз. Режим, при котором происходит очень быстрое нагревание сосуда до температуры выше 100°С при минимальном нагреве дермы. Применяются очень интенсивные лазерные импульсы (I=20 кВт/см²) длительностью меньше, чем период релаксации сосуда. Для этого используют лазер, излучающий импульсы порядка миллисекунд (0,5-5 мс). В крови энергия поглощенного излучения преобразуется в тепло, которое не успевает рассеиваться, вследствие чего накапливается в сосуде. Из-за этого внутри сосуда значительно повышаются температура и давление, что приводит к разрыву его стенки и к кровоизлиянию. Клинически это проявляется в виде пурпуры или микрогеморрагий.
2. Селективная коагуляция. Режим ограниченного теплового воздействия — температура порядка 75°С вызывает коагуляцию стенки сосуда. Излучение также поглощается кровью, но в этом случае задача заключается в избирательном повышении температуры стенки сосуда. Этого можно добиться только путем передачи тепла, что требует достаточно времени. Поэтому время импульса должно быть больше, чем время релаксации сосуда, но ограниченным, иначе могут произойти значительные изменения в обширной зоне окружающей дермы.
Обычно продолжительность импульса в 3-5 раз больше времени релаксации. Таким образом, для сосуда диаметром 150 мкм продолжительность импульса должна быть порядка 70 мс, что в 100 раз превышает значение, используемое при селективном фототермолизе. При приблизительно равном количестве потребляемой энергии в данном случае требуется более слабая интенсивность излучения (I=0,2 кВт/см²). Технически такие параметры получить гораздо проще, для этого подходит большое количество лазеров и даже импульсные лампы IPL с фильтрами.
Собственные клинические наблюдения.
Условно, пациенты были разделены на две группы. В первую группу вошли пациенты, у которых высота, либо глубина прорастания гемангиомы, не превышала5 мм(201 пациент). Во вторую группу вошли пациенты с высотой гемангиомы более5 мм(198 пациентов).
В первой группе пациентам проводилось только лазерное лечение. Попытки изолированного лазерного лечения гемангиом большей глубины, как правило, безуспешны и не приносят желаемого эффекта. Во второй группе первым этапом проводилась склеротерапия по Бернадскому, после уменьшения размеров гемангиомы – лазерное лечение. Склерозирование проводилось под премедикацией, в условиях стационара одного дня.
У 12 пациентов первой группы между сеансами лазерного лечения наблюдался рост гемангиомы, в связи с чем было проведено склерозирование гемангиомы по Бернадскому, а затем вновь несколько сеансов лазерного лечения.
Лазерное лечение гемангиом проводилось амбулаторно, в несколько сеансов с интервалом от 2-х до 4-х недель, в зависимости от скорости заживления раневой поверхности. Параметры лечения стандартные, рекомендованные произодителем аппаратуры. Интенсивность воздействия от 105 Дж\смІ, длительность 4,5 мс, потемнение гемангиомы является признаком успешно проведенного сеанса лечения, в случае отсутствия эффекта интенсивность воздействия поэтапно увеличивается на 5%. Количество импульсов за сеанс варьируется от 1 до 10 до появления цианоза, либо потемнения поверхности гемангиомы.
Результаты лечения оценивались по внешнему виду пролеченного участка кожи. Хорошим результатом считается отсутствие видимых следов на коже после излечения, удовлетворительным – наличие нормотрофического рубца, не нуждающегося в дополнительной хирургической коррекции. Неудовлетворительным результатом считается неполный регресс гемангиомы и (или) образование гипертрофического рубца. Результаты лечения в обеих группах были идентичны.
В 26% случаев были достигнуты хорошие результаты. В 67% случаев результаты оказались удовлетворительными, в 7% случаев — неудовлетворительными. В процессе лечения в обеих группах не было зарегистрировано таких осложнений, как воспаление и кровотечение.
Сочетание методик позволяет добиться хороших результатов как в плане остановки роста и регресса опухоли, так и в эстетическом плане.
Таким образом, своевременная диагностика, вовремя начатое лазерное лечение гемангиом, а также грамотное сочетание этой методики с классической склеротерапией, является эффективным, малоинвазивным и современным методом лечения, легко применимым в амбулаторных условиях и на базе однодневных стационаров.
Н.П. Паштаев, В.В. Трубин, Д.В. Рыжевский
Городская детская больница №3, г. Чебоксары
Рыжевский Дмитрий Владимирович — врач-офтальмолог
1. Кожевников Е.В., Маркина Н.В., Кожевников В.А. Диагностика и лечение обширных комбинированных гемангиом и гемангиом сложной анатомической локализации у детей // Детская хирургия. — 2009. — № 6. — С. 31-34.
2. Holcomb G.W. Ashkraft’s Pediatric Surgery. — Philadelphia: saunderselsevier. — 2010. — 1101 p.
3. Aresman Robert M. Pediatric surgery // Landesbioscience. — 2000. — Georgetown, Texas U.S.A. — 464 p.
4. Шафранов В.В., Тен Ю.В., Куров Н.В. Комбинированное лечение кавернозных гемангиом у детей // Детская хирургия. — 1987. — № 8. — С. 8-11.
5. Шафранов В.В, Буторина А.В. Лечение гемангиом у детей // Врач. — 1996. — № 9. — С. 17-18.
6. Шафранов В.В., Кожевников В.А. Комбинированное лечение гемангиом и доброкачественных образований кожи у детей: метод. рек. для врачей — дет. хирургов, дерматологов, онкологов, косметологов. — 1994. — 13 с.
7. Ашкрафт К.У. Детская хирургия. — СПб.: Раритет. — 1999. — 400 с.
8. Солдатский Ю.Л., Шехтер А.Б., Понкратенко А.Д. и др. Изучение криовоздействия и лазерной деструкции на экспериментальную модель сосудистой опухоли человека // Вестник отоларингологии. — 1995. — № 2. — С. 10.
Гемангиомы у детей — наиболее часто встречающиеся доброкачественные сосудистые опухоли, которые составляют более 50% всех опухолей детского возраста [1, 4, 5, 9, 10, 11, 16]. В отношении морфологической принадлежности этих новообразований
Гемангиомы у детей — наиболее часто встречающиеся доброкачественные сосудистые опухоли, которые составляют более 50% всех опухолей детского возраста [1, 4, 5, 9, 10, 11, 16].
В отношении морфологической принадлежности этих новообразований можно с уверенностью сделать вывод об опухолевой, а не диспластической природе гемангиом [6, 13, 15].
![]()
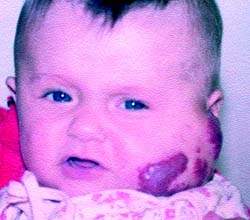
Рисунок 1. Ребенок с ангиомой до лечения Многими авторами установлена высокая митотическая активность в клетках опухоли, в то же время отмечена возможность спонтанной регрессии гемангиом, что полностью соответствует опухолевой природе заболевания [6, 10, 14, 17].
Несмотря на свою доброкачественность, гемангиомы отличаются быстрым прогрессирующим ростом. Разрастаясь, они разрушают окружающие ткани и наносят ребенку значительный косметический ущерб. В первую очередь это относится к гемангиомам лица и головы. При локализации гемангиом на веках, ушной раковине, носу, а также на слизистой ротовой полости, помимо косметических проблем, могут возникать чисто физиологические в виде нарушений функций некоторых важных органов (зрение, слух, дыхание). Поэтому можно сказать, что гемангиомам присущи некоторые черты клинически злокачественного течения.
Особенностью течения гемангиом является непредсказуемость их “поведения”; порой небольшая, точечная гемангиома щеки в течение 2-3 недель может превратиться в обширную и глубокую ангиому сложной анатомической локализации (например, гемангиома околоушной области, без тенденции к остановке роста). Расчет на спонтанную регрессию в этих случаях оказывается неоправданным, а потеря времени идет явно не на пользу больному.
Помимо этого, сосудистые опухоли могут изъязвляться, вызывать кровотечения и инфицироваться. Характерная особенность изъязвившихся и нагноившихся гемангиом — продолжительное течение заболевания и отсутствие тенденции к быстрому заживлению язвенных поверхностей.
Отдельного разговора заслуживает спонтанная регрессия гемангиом. По нашим данным, спонтанной регрессии подвергаются около 7-8% простых гемангиом, находящихся на “закрытых” участках тела и только у доношенных детей в возрасте старше одного года. Кавернозные и комбинированные гемангиомы практически не регрессируют.
Надеяться на спонтанную регрессию большой и глубокой ангиомы в области лица у маленького недоношенного ребенка в возрасте до шести месяцев было бы ошибкой!
Процесс течения гемангиом достаточно сложный и требует постоянного внимания, причем чем меньше ребенок, тем внимательнее надо следить за состоянием гемангиомы. Особенно быстрый рост ангиом наблюдается в первое полугодие жизни ребенка, после этого рост замедляется, кроме гемангиом сложной анатомической локализации.
Поскольку в ранний возрастной период прогноз довольно сложен, лечение гемангиом, по нашему мнению, следует начинать как можно раньше, и даже недоношенность ребенка не является противопоказанием к раннему лечению.
Вероятно, универсального метода лечения гемангиом у детей нет и быть не может. И хотя морфологические данные явно свидетельствуют в пользу опухолевой природы ангиом, использование простых и эффективных хирургических и парахирургических методов лечения приводит к положительному результату.
![]()
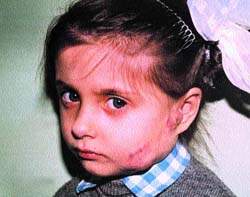
Рисунок 2. После СВЧ-криогенного лечения Клиника детской хирургии РГМУ за 20 лет накопила опыт лечения 300 тыс. детей с гемангиомами различной локализации и вида.
Но занимаясь проблемой лечения гемангиом, мы столкнулись с группой больных с обширными и глубокими гемангиомами сложной анатомической локализации: лицо, околоушная область и шея.
Эти гемангиомы отличаются определенным своеобразием: бурным ростом опухоли, клинической злокачественностью течения, характеризующейся разным уровнем деструкции окружающих тканей, изъязвлениями, артериальными кровотечениями. Лечение таких гемангиом представляет значительные трудности для хирурга, так как традиционные методы чаще всего оказываются неэффективными.
Поэтому мы решили выделить этих больных в отдельную группу (см. табл.).
Распределение детей с гемангиомами по виду и количеству последних Вид ангиом Количество больных % Простые 215500 71,8 Кавернозные 19 500 6,6 Комбинированные 53000 17,7 Смешанные 10500 3,5 Гемангиомы сложной анатомической локализации 1500 0,5 Всего 300000 100 При анализе полученных данных подход к лечению детей с гемангиомами становится вполне очевиден. Наименьшую проблему представляют простые гемангиомы, наибольшую — гемангиомы сложной анатомической локализации, хотя в количественном отношении первые явно преобладают над последними.
Из ныне существующих методов наиболее удачным для лечения простых гемангиом является локальная криодеструкция аппаратом, где в качестве хладоагента применяется жидкий азот (с температурой –1960 С) [3, 8].
Криогенное лечение гемангиом проводится амбулаторно. Специальной подготовки ребенка к лечению не требуется. Метод прост, экономичен, не требует анестезии, абсолютно бескровен. Во время процедуры и после нее нарушений общего состояния ребенка, повышения температуры и патологических реакций не наблюдается.
Оптимальное время криовоздействия — 20-30 с для гемангиом, располагающихся на коже, и 7-15 с для гемангиом, локализующихся на слизистых оболочках.
При множественных гемангиомах, особенно если они были малых и средних размеров, мы проводили криодеструкцию одновременно двух или трех ангиом, но так, чтобы общая площадь криоповреждения не превышала 10 см2.
При локализации гемангиом в местах, наиболее подверженных травмированию, особенно в области промежности и ягодиц, площадь однократного криовоздействия не должна превышать 5 см2.
При крупных и обширных гемангиомах лечение должно проводиться в несколько этапов с интервалами между ними 10-14-21 день. За это время местная реакция в области криовоздействия стихает, и лечение может быть повторено.
Для предупреждения распространения опухолевого процесса и с целью ограничения роста гемангиомы рекомендуется начинать лечение с периферии.
Наиболее выраженный перифокальный отек наблюдается после криовоздействия на гемангиомы лица, век, сгибательных поверхностей, а также слизистой оболочки губ и половых органов. Образование сухой корочки отмечается на третий-четвертый день, эпителизации идет под струпом в течение 2-4 недель.
Успеха при криогенном лечении удается достичь в 100% случаев. Очень важной стороной лечения является получение хороших косметических и эстетических результатов (99,7%) благодаря особенностям регенерации кожи после криогенных вмешательств (органотипическая регенерация). Осложнения при криогенном лечении гемангиом наблюдаются крайне редко, в 0,2% случаев.
Среди общепринятых методик лечения наибольшей популярностью пользуется хирургическое иссечение опухоли с пластикой кожи или без нее.
![]()
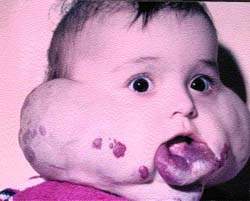
Рисунок 3. Ребенок с двухсторонней ангиомой до лечения В 95% случаев клиника отказалась от традиционных хирургических методов лечения гемангиом, отдавая предпочтение эффективным консервативным способам. Причем за 20 лет частота оперативных вмешательств снизилась в 50 раз.
Хирургический способ наиболее целесообразен при локализации гемангиом на “закрытых” участках тела, тогда как при расположении опухолей в области лица и шеи иссечение представляет определенную косметическую проблему.
Оперативный метод лечения целесообразно также использовать при зрелых формах гемангиом, которые закончили свою дифференцировку. Операция в качестве корригирующего метода может быть использована при наличии избытка кожи на месте большой туберозной гемангиомы в случае ее полного спонтанного исчезновения.
Для лечения небольших кавернозных гемангиом лица и кончика носа с успехом применяется склерозирующая терапия. Она основана на принципе асептического воспаления или тромбирования сосудов, возникающих в гемангиоме в результате введения склерозирующих веществ.
![]()
![]()
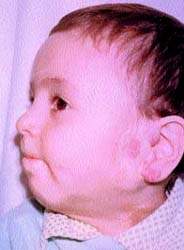
Рисунок 4. Тот же ребенок после лечения (локальная гипертермия) У всех больных для инъекций использовали 70%-ный спирт, отек на месте инъекции исчезал самостоятельно к 5 – 6 дню.
Недостатком инъекционного метода лечения является болезненность и длительность лечения, 76% больных потребовались дополнительные неоднократные инъекции спирта.
Диатермоэлектрокоагуляция применяется значительно реже, лишь при небольших точечных ангиомах, в тех случаях, когда опухоль располагается в областях, где нельзя воспользоваться другими методами лечения.
Эффективна, особенно в первом полугодии жизни ребенка, гормональная терапия гемангиом по альтернирующей схеме. Данный метод лечения был применен нами у 630 больных.
При подборе больных для кортикостероидной терапии мы руководствовались следующими критериями: сложность, т. е. критичность анатомической локализации; обширность поражения; быстрый рост гемангиом и поражение опухолью различных анатомических областей.
Мы считаем, что гормональной терапии подлежат самые обширные и самые сложные гемангиомы у детей.
Гормональное лечение проводилось преднизолоном по 4-6-8 мг на 1 кг веса ребенка. Суточная доза преднизолона в таблетках делилась на два приема: в 6 часов утра ребенок получал 2/3 дозы, в 9 часов утра 1/3 дозы. Препарат принимался через день без снижения дозировки. Продолжительность курса лечения составляла 28 дней.
Уже после второго или третьего приема преднизолона у большинства больных отмечались признаки регрессии ангиом, побледнение и некоторое уплощение опухоли. А к окончанию курса преднизолонотерапии все гемангиомы уменьшались в объеме, прекращался их рост и на поверхности опухоли появлялись белесоватые островки участков здоровой кожи, которые расчленяли ангиому на все меньшие и меньшие участки. После перерыва в 1-2 месяца, при необходимости, проводили повторные курсы гормонотерапии по той же методике.
Каких-либо осложнений во время лечения преднизолоном и после его отмены мы не наблюдали.
Гормонотерапия является довольно результативным методом лечения ангиом, однако при высокой его эффективности (98%) желаемого косметического результата достичь практически невозможно. Только у 2% детей ангиомы удалось полностью вылечить с помощью гормонотерапии, долечивание гемангиом другими методами позволяет решать лишь косметические проблемы.
Рентгенотерапия гемангиом относится к высокоэффективным методам. Она является весьма результативной, если лечение проводится у детей от 3 до 8 месяцев, так как в этом возрасте чувствительность ангиомной ткани к ионизирующему излучению очень высока, что обеспечивает излечение геманигиом с полным восстановлением нормальной кожи.
Близкофокусная рентгенотерапия применяется для лечения гемангиом таких областей, где другие методы невозможно использовать, например область орбиты, ретробульбарного пространства или простые гемангиомы большой площади.
Разовые очаговые дозы составляли от 0,8 до 1,6 Гр, в зависимости от возраста ребенка. Показанием к прекращению лучевой терапии при ангиомах являлось замедление роста и побледнение гемангиомы, т. е. лечение проводилось до появления симптомов регрессии, аналогичной естественной, после чего облучение прекращалось [7].
При лучевой терапии в дозах, не вызывающих местной реакции, изменения кожи и мягких тканей не развиваются. Надо учитывать, что этот метод лечения все же относительно сложен, и чтобы проявился эффект от лучевой терапии, требуется довольно длительное время.
При лечении кавернозных и комбинированных гемангиом с выраженной подкожной частью, чаще сложной анатомической локализации, следует проводить криоусиление за счет дестабилизации “связанной воды” путем предварительного СВЧ-воздействия на область замораживания. СВЧ-облучение проводится в физиотерапевтическом режиме в течение 3-5 минут, последующая криодеструкция выполняется в упомянутых выше режимах.
На наш взгляд, недоношенность не является противопоказанием к выполнению СВЧ-криодеструкции. В ряде случаев целесообразно проводить СВЧ-криогенное лечение по индивидуальным показаниям, например у новорожденных детей или в случае относительно большого объема опухоли.
Метод СВЧ-криодеструкции позволяет частично или полностью отказаться от хирургического лечения и добиться при этом хорошего результата (98%).
В клинике разработан подход к диагностике обширных и глубоких гемангиом сложной анатомической локализации, заключающийся в обязательной ангиографии. В результате были выявлены определенные закономерности, объясняющие, на наш взгляд, причину неэффективности лечения подобных опухолей. Оказалось, что через гемангиому проходит питающий ее мощный артериальный ствол, чаще аномального характера, который создает условия для активного роста сосудистой опухоли.
После обязательной ангиографии и эмболизации опухоли проводится лечение. Принимая во внимание преимущественную локализацию опухолей в проекции лицевого нерва, наиболее целесообразно было использовать СВЧ-криогенное вмешательство, так как этот способ гарантировал сохранность лицевого нерва, мимической мускулатуры и контуров лица ребенка.
Вмешательство не сопровождалось кровотечением и не было тяжелым для больного. В течение 5-6 месяцев гемангиома исчезала, оставляя после себя участки атрофированной кожи и атрофические рубцы.
К недостаткам этой методики мы отнесли развитие массивных отеков лица, которые держались до 5-7 дней, а затем исчезали самостоятельно, а также хоть и относительную, но все же хирургическую интервенцию.
На рис. 1, 2 представлен ребенок с ангиомой околоушной области до и после лечения (методом СВЧ-криодеструкции).
В последние годы исследуется и не без успеха применяется методика локальной СВЧ-гипертермии обширных и глубоких ангиом околоушной области. Данная методика была реализована у 180 больных. Метод заключается в повышении температуры в опухоли, регистрируемом введением под опухоль датчика в виде иглы. Температура доводится до 43-440С и поддерживается на этом уровне 5-6 минут.
Среди основных преимуществ методики основным является отказ от хирургического вмешательства, отсутствие отеков и возможность быстрой выписки ребенка домой. Косметические вмешательства, если ребенок в таковых будет нуждаться, можно выполнять в более старшем возрасте.
На рис. 3, 4 представлен ребенок с двухсторонней ангиомой сложной локализации до и после лечения (методом локальной гипертермии).
Таким образом, современное лечение гемангиом у детей и использование всего арсенала средств, имеющегося на вооружении в детской хирургии, позволяет добиться полного излечения опухоли с хорошим косметическим результатом. А следовательно, получить не только здорового, но и красивого ребенка!
Литература
1. Баиров Г. А. Хирургия пороков развития у детей. Л., 1968, с. 561-577.
2. Исаков Ю. Ф. Хирургические болезни у детей. М., 1993, с. 519-562.
3. Кандель Э. И. Криохирургия. М., 1974, с. 303.
4. Кондрашин Н. И. Клиника и лечение гемангиом у детей. М., 1963, с. 103.
5. Краковский Н. И., Таранович В. А. Гемангиомы. М., 1974, с. 168.
6. Лебкова Н. П., Кодрян А. А. О гистегенезе и механизме регрессии врожденных гемангиом кожи у детей // Архив патол., 1997, вып. 3. с. 44-50.
7. Свистунова Т. М. Низковольтная рентгенотерапия при гемангиомах у детей. Л., 1974, с. 142.
8. Ситковский Н. Б., Гераськин В. И., Шафранов В. В., Новак М. М. Лечение гемангиом у детей жидким азотом. Киев, 1968, с. 120.
9. Терновский С. Д. Хирургия детского возраста. М., 1959, с. 179-200.
10. Федореев Г. А. Гемангиомы. Л., 1974, с. 192.
11. Demuth R. J., Miller S. H., Keller F. Complications of embolization treatment for problem cavernous hemangiomas // Ann. Plast. Surg. 1984. V. 13. № 2. P. 135-144.
12. Edgerton M. T. Steroid therapy of haemangiomas // Symposium on Vascular Malformations and Melonotic Lesions. Ed. By Williams H. G. St. Louis, C. V. Mosby. 1983. P. 74-83.
13. Enjolras O., Herbretean F. Et al., Hemangiomes et Malformations vasculares superficielles: classification // J. Des Maladies Vasculaires. Paris. 1992. V. 17. № 1. P. 2-19.
14. Fingerhut A. Angiomas of the Smallintestine, Diagnostic and therapeutic problems // Gastroenterol. Clin. Biol. 1978. V. 2. № 12. P. 103-104.
15. Pasyk K. Classification and clinical and histopathological features of hemangiomas and other vascular malformations // Vascular Birthmarks. 1987. P. 1-54.
16. Peck J. E. The treatment of hemangiomas // British Med. J. 1974. V. 2. P. 198-200.
17. Traub E. F. Involution of Haemangiomas // Arch. Pediat. 1933. V. 50. P. 272-278.
Читайте также: