Как попасть на клинические испытания лечения меланомы

Российские онкологи предостерегают граждан от чрезмерного пребывания на солнце и в солярии, особенно в летний период. Ультрафиолетовое излучение является одним из главных факторов, вызывающих рак кожи, а за последние 10 лет прирост пациентов с этим диагнозом в мире составил 30%.
— Светлана Анатольевна, специальная сессия, посвящённая меланоме кожи, стала одним из центральных событий IV международного онкологического форума.
— Еще несколько лет назад считалось, что рак кожи — это смертельное заболевание. Что-то изменилось с тех пор?
— Много ли больных меланомой в России и в мире, если есть статистика?
— В мире на протяжении последних десятилетий отмечается неуклонный рост заболеваемости меланомой кожи, в год выявляется более 200 тысяч новых случаев.
В России ежегодно регистрируются около 10 000 новых случаев меланомы кожи. Причём большинство заболевших — это люди трудоспособного возраста. К сожалению, в нашей стране около четверти всех пациентов на момент постановки диагноза имеют местно-распространённую или метастатическую форму заболевания (III-IV стадию), при которой прогнозы обычно неблагоприятны.
Результаты лечения и показатели выживаемости напрямую зависят от того, на какой стадии заболевания был диагностирован опухолевый процесс. Если на раннем этапе 5-летняя выживаемость превышает 90%, при второй стадии составляет около 65%, то при локально-регионарной, третьей стадии снижается до 45%, а при метастатической (четвертой стадии) составляет не более 20%.
— Кто, прежде всего, находится в зоне риска?
— Один из главных факторов риска развития меланомы кожи, по мнению исследователей, связан с избыточным воздействием ультрафиолетовых лучей, как на открытом солнце, так и в солярии. Шансы развития меланомы увеличиваются у людей с первым и вторым фототипом кожи (белокожий/рыжий, светлокожий), при котором образуется меньше всего защитного пигмента. Поэтому хочу призвать всех читателей: при малейшем подозрении немедленно обращайтесь к врачу. Выявление меланомы на ранней стадии — как правило, залог полного излечения. И, конечно, по-прежнему актуальная рекомендация: не злоупотребляйте естественным или искусственным ультрафиолетом!

— Насколько эффективно сегодня борются с меланомой в России? У нас свои препараты, методики лечения и химиотерапии или в основном зарубежные?
— В России сейчас зарегистрированы и применяются в клинической практике все современные противоопухолевые препараты для лечения меланомы кожи (таргетные, иммуноонкологические). Они могут использоваться как при монотерапии, так и в комбинации. Эффективность комбинированной терапии выше, но и частота побочных эффектов значительно увеличивается. Поэтому применение противоопухолевой терапии должно осуществляться строго по показаниям и только в специализированных онкологических учреждениях. Благодаря использованию современных препаратов удалось добиться увеличения выживаемости пациентов, как общей, так и без прогрессирования заболевания.
Конечно, в основном сегодня мы пользуемся импортными противоопухолевыми препаратами, однако в настоящее время есть и отечественные разработки. Сейчас проводятся клинические исследования двух лекарственных образцов. Мы с нетерпением ждём результатов!
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Вчера потребовалось самому найти клинические испытания препаратов от меланомы. Вот решил набросать памятку. Чтобы все происходило быстро. Думаю что надо было сделать это гораздо раньше конечно, но лучше поздно, чем никогда. Процесс описан для больниц в РФ и только по меланоме, но думаю что подходит для любых видов рака и для любых стран.
Обсуждать саму процедуру с использованием плацебо я не буду. Исходим из того, что человеку предоставляется 50% шанс.
Не смотря на то, что на сегодняшний день уже существует несколько препаратов для лечения меланомы, КИ все равно пользуются популярностью. В первую очередь потому, что самостоятельно покупать препараты могут далеко не все, а получение их по полису ОМС может либо вообще не состояться, либо будет растянуто во времени, да так, что пациент может просто не дожить до счастливого момента принятие решения и окончания гос закупки.
Множество клинических исследований сейчас проходит в России, но если мест уже нет, то вы запросто можете обратиться взарубеж. Попав в КИ, вы будете платить только за обследования.
1. В первой строчке вбиваем название нашей болячки: melanoma . Если у вас не увеальная меланома (меланома глаза), то лучше именно так писать, а не выбирать какую-то конкретную стадию.
2. В следующей пишем название препарата (препаратов через запятую), если хотим конкретные КИ найти. Можно выбрать страну. Затем внизу страницы нажимаем Search.
3. Получаем список всех КИ. Обращаем внимание на мутацию гена. И смотрим то, что нам подходит и открываем в новом окошке.
4. Открывшуюся страницу нужно переводить, тут уж ничего не поделаешь. Но я хочу рассказать о том, как быстрее найти больницу, в которой эти КИ проводят. Опускаемся вниз и находим Show Study Location (рядом с плюсиком) и кликаем на надпись.
5. Ищем свою страну (найдете быстро, т.к. она будет подсвечена). Возле каждого города, в котором проводятся КИ, стоит ИНДЕКС больницы. И написано самое главное, принимают в КИ пациентов, или нет: Not yet recruiting / Recruiting
в поиск вашего браузера вбиваем индекс и получаем больницу с контактами. Дальше дело техники.
ОБРАЩАЮ ВАШЕ ВНИМЕНИЕ
23.09.2014
Вот сайт с информацией о клинических исследованиях препаратов в РФ
12.12.2014
1. Cкорее всего ни в одной больнице Вам сами не предложат участие в КИ, Вы должны им показать, что знаете что в этой больнице КИ идут и что есть набор.
2. Далее основное (мы это осознали в процессе лечения) — никогда не надо давить врачам на жалость, они это воспринимают как слабость. Т.е. всегда нужно приходить в хорошем расположении духа, красиво одетой, дать понять что не собираешься сдаваться, стараться улыбаться, уверенно говорить, что сможешь перенести все тяготы и сложности.
Никогда не придерживаться мнения, что чем ты хуже и беспомощней выглядишь, тебе захотят помочь (это всё наоборот, поверьте, врачи хотят помочь тем, кто сам борется и хорошо выглядит (улыбается, шутит, даже если ему очень плохо)
3. Ну и конечно вы должны настраивать себя на то, что вы очень нужны близким людям, и все препараты это только маленькая помощь вашему организму, который сильный и может со всем справиться.
Не начинайте лечение дакарбазином, если есть шанс попасть в КИ. Дакарбазин -во-первых ослабит организм, а во-вторых мы ещё не знаем ни одного больного кому бы он помог, и в третьих: частое условие попадания в КИ — это никакой химии и иммунки (возможно только хирургическое вмешательство)
04.03.2016
Поддельные сайты больниц, непонятные интернет-аптеки без адресов и т.д. мы уже проходили и ежедневно можем наблюдать, но такое на столь уважаемом сайте я вижу в первый раз. Будьте бдительны!
10.07.2016
Эпакадостат (epakadostat)
КИ проводятся в России. Вот список больниц
Уникальность в том, что пациенты в любом случае получают Кейтруду (пембролизумаб)
09.09.2016
BCD-100
Начались клинические исследования аналога Кейтруды и Ниволумаба — препарата производства компании Биокад, под названием BCD-100
12.10.2016
Ниволумаб + Ипилимумаб. Набор пациентов идет. Один человек из РФ уже попал в них, так что есть контакты врачей
КИ . Ервой + Опдиво. На сегодняшний день это самая действенная комбинация препаратов для лечения меланомы.
В связи с тем, что многие не могут сразу понять как пользоваться сайтом Росминнздрава, вот небольшая
Видим такую картинку:
Вопросы и ответы по бумажке под название ИНФОРМИРОВАНИЕ СОГЛАСИЕ
Диагноз: узловая меланома Т3аN1aM0, Бреслоу 1.8 мм, Кларк 4 ст, 14 митозов на кв/мм.
Результат биопсии сторожевых ЛУ в Израиле: в одном из 4х удаленных лимфоузлов обнаружен микрометастаз 3мм без распространения за пределы капсулы.
Чего пытались добиться дальше: клинические исследования, адъювантная терапия меланомы
Как мы знаем (а мы ведь знаем), на сегодняшний день окромя препарата Ервой (Ипилимумаб) никакой адъювантной терапии для пациентов с таким диагнозом не предусмотрено, т.к. интерферон альфа, после проведенных десятилетних исследований , был недавно фактически исключен из претендентов на дальнейшее использование, доказав свою бесполезность (заостряю внимание — именно в нашем случае! ).
Ну и, конечно, собранные тут: Адъювантная терапия меланомы III ст в РФ разнообразные Рефноты, Ригвиры и прочие вирусы-вредилусы, не проходившие никаких КИ, рассматривать в виде терапии мы тоже не будем (вы, уважаемые пользователи интернетов, конечно можете, т.к. у нас демократия, но я не буду).
По этому было принято решение попасть вот сюда //clinicaltrials.gov/ct2/show/study/NCT02362594 , в КИ по адъювантной иммунотерапии препаратом Кейтруда (Пембролизумаб).
Ну и вот, собственно:
Кейтруда (пембролизумаб) клинические исследования
22.06.2016 пока лайнер авиакомпании (не знаю какой) прогревал свои могучие турбины, дабы совершить перелет с Юга России в столицу (тоже России):
Диссекцию лимфоузлов было решено делать в Ростовском НИИ онкологии. Насчёт операции удалось договориться вне очереди и по квоте, что немаловажно. Быстро сдав все необходимые анализы, 13.04 я оформилась на госпитализацию и 14.04 была проведена левосторонняя подмышечно-подлопаточная лимфодиссекция. По результатам гистологии обнаружено /удалено 8 ЛУ , метастазов не обнаружено.
Правда обнаружились какие то нитки (или скобки), оставшиеся после БСЛУ. Наркоз и операцию перенесла хорошо, восстановление шло нормально, и на 6 день мне сняли лимфодренаж и отпустили домой. Но через пять дней пришлось откачивать жидкость, скопившуюся в месте операции (видимо, все-таки рановато убрали дренаж). Испугалась, конечно, до ужаса, очень не хотелось плюс ко всему заиметь ещё и лимфостаз, но, помня наставления Гутмана и моего хирурга, делала гимнастику и массаж, и где-то через месяц все пришло в норму.
Выписали меня с рекомендацией: интерферон альфа 3 млн через день в течение 12 мес; Радиолог предложил облучение (для профилактики). В высокодозной иммунотерапии (интерфероном прим. Дядя Вадик) отказано, так как у нас в Ростове её не делают вообще, мощностей не хватает.
Обращу ваше внимание, что телефоны, указанные там, это не телефоны больниц, а представительств фарм компаний, а они уже дали мне номера телефонов координаторов, в моем случае это были 62 больница и РОНЦ.
На звонки ответили и там, и там. Но в 62 предложили все прислать по почте, что и было незамедлительно сделано, а в РОНЦ предложили приехать и привезти все документы и блоки послезавтра! И уже 29.04 я полетела в Москву.
На консультации доктор посмотрел все мои документы, по первичным критериям я им подходила, хотя она сразу предупредила, что это ещё ничего не значит, так как надо пройти детальное обследование. Ну и ещё добавила, что я у неё первая пациентка с микрометастазом. Она ещё и звонила куда-то, уточняя, можно ли меня брать; оказалось — можно, так как по условиям микро метастаз должен быть не менее 1,5 мм.
Кстати сказать, про условия включения в КИ — разговор отдельный. Условия жесткие.
Включаются пациенты с 3ст, после удаления мтс в лимфоузлах, лимфодиссекция регионарных ЛУ, кол во удаленных ЛУ должно быть не менее 10, размер их, как я написала, не менее 1,5 мм, с момента последней операции и до начала терапии должно пройти не более 13 недель, никакой терапии по поводу меланомы, ну и последнее — полное физическое здоровье (никаких патологий, хронических заболеваний, никаких перенесённых гепатитов и т.п.). И, самое главное, это — наличие материала (блока ) с мтс , который они отправляют в лабораторию спонсора на определение PD-экспрессии!
Когда она мне сказала — давайте блоки с мтс , у меня сердце оборвалось . Мои-то блоки в Израиле, я их после БСЛУ не забрала, думала — не понадобятся… Договорились о том, что через две недели я должна быть на том же месте с израильскими блоками, иначе пролёт …
Вопрос с передачей блоков из Израиля решился за час (Вадиму отдельное спасибище. ). Альфа прислали блоки ,через Ассуту Москва через неделю. Правда стоит это 350$ (Такие у них правила, странные однако), но делать нечего, дело того стоит.
И еще (для тех кто читает не совсем вдумчиво): все эти финансовые штуки касаются только материала удаленного в Израиле, т.е. вашу привезенную/присланную на пересмотр гистологию отдадут конечно же бесплатно🙂
Следующие три дня я проходила обследования: кровь, моча, РКТ с контрастом, КГ, ОМТ, ОБП.
В рамках КИ обследования БЕСПЛАТНЫ!
Немного, конечно, пришлось усиленно попросить некоторых товарищей, так как запись везде на неделю вперёд, но это мелочи по сравнению с мировой революцией 🙂 . По поводу результатов сказали позвонят через дня 3-4.
Перезвонили, и сообщили , что КТ им не нравится и надо срочно приехать на дообследование. У меня земля ушла из под ног!
Все мысли опять в кучу, паника, истерика. Утром первым рейсом, я уже вылетела в Москву.
КТ показало увеличенные паховые лимфоузлов (1,6мм), образование на передней стенке живота (родинка выпуклая с рождения) и разрежение костной ткани 2х каких то ребер (остеопороз под вопросом).
Дообследование на исключение мтс : сцинти костей , УЗИ всего, пункция под контролем УЗИ пазовых ЛУ, удаление невуса с гистологией. Опять три дня хождения и сидения в очередях , но все не зря! Кости в порядке, невус папиломатозный, ЛУ нормальные.
Невус удаляли на 21 этаже, эл.ножом. Я была в шоке! По приезду домой я сходила к своему хирургу, выслушала проповедь на тему: носит вас где-то, а мне сопли собирай, но удалили все как надо — хирургически. От греха подальше .
Пока я там шастала, решила на всякий случай послушать мнения ещё одного спеца по меланома г-на Синельникова . Он был полностью солидарен с тем, что облучение и низкодозный интерферон не нужен, сказал пересдать на мутации, и конечно сказал, что было б неплохо попасть в эти КИ .
К тому времени нервы были на пределе…сказали опять позвонят. Позвонили, срочно привезти заключение фтизиатра и снимок легких , так как по всем КТ видят пост ТВс узлы до 0,3 мм. Привезла. Взяли ещё какую то кровь. Опять ждать. Но обрадовали, блок прошёл проверку на экспрессию PD, информативен. Ну хоть что то .
Еще неделя томительного ожидания и вот Алилуйя. Все хорошо, вас утвердили, но нужно приехать сдать кровь. Да, конечно, какие вопросы, что нам в Москву сгонять на анализы, всего то 1000км))) Приехала, сдала. Обещали через пару дней сказать когда первая капельница. Опять ждемс …
Все эти долгие недели ожидания, помимо моего мужа и семьи, меня очень поддерживали хорошие люди на форуме. Вера Григорьна, Екатерина, Михаил Александрович — Спасибо огромное вам за поддержку. Ну, а Вадима я вообще не знаю как благодарить… Все это время, мы в режиме онлайн держали связь, и он меня подбадривал как мог. Вадим, спасибище.
Вот такая вот положительная история….
Но это было 22.06, а следующий день начался вот с такого диалога:
— Пришли ответы вчерашних анализов, все хорошо, но выясняли, что прошёл срок КТ (28дней), завтра должны сказать надо переделывать или нет. У меня нет слов… хочется рыдать

Причиной смерти пациента-испытателя назвали неожиданную реакцию организма на экспериментальный препарат производства "Биокад". Ранее фармзавод удостоился похвалы Минздрава за "фантастические результаты" в лечении опухолей. Лекарство должно было появиться на рынке ещё год назад. Не остановит ли смерть добровольца исследования и когда ждать отечественное лекарство от рака — в расследовании Лайфа.
Одна из самых секретных разработок российской медицины попала в неприятную историю, которая могла бы так и остаться в стенах петербургской лаборатории. Рассказываем, как российские учёные изобретали молекулу для лечения меланомы и рака лёгких и с какими трудностями столкнулись.
1. Экспериментальный препарат стал главной темой онкологического конгресса
В ноябре 2018 года состоялся XXII Российский онкологический конгресс. Представители фармзавода "Биокад" и врачи рассказали об успешных испытаниях на людях новейшего отечественного лекарства от рака. Он заставляет иммунные клетки атаковать опухоль.
Речь о препарате под кодовым названием BCD-100. Это одна из самых засекреченных разработок отечественной фармацевтики — не разглашают даже имена учёных, разработавших молекулу (основное действующее вещество).
Препарат показал ошеломляющие результаты в лечении неоперабельной меланомы. Когда опухоль даёт метастазы, зловредные клетки проникают в окружающие органы и там формируют вторичные очаги болезни. Справиться с метастазирующей меланомой гораздо труднее. Однако BCD-100 сумел полностью убрать подобные опухоли у 7% пациентов. Ещё у 29% пациентов размер опухоли уменьшился не меньше чем на треть. В исследовании участвовало 126 онкобольных с неоперабельной меланомой. Испытания финансировал сам "Биокад".
Меланома (рак кожи)
Не самый частый, но один из самых агрессивных видов рака (≈74 тысяч больных в РФ). С 1950-х мировая заболеваемость выросла на 600%
Однако пациентов ждут серьёзные побочные эффекты, которые стали сюрпризом и для врачей — препарат-то новый.
"Внедрение [иммунотерапии], по-русски сказать, взорвало химиотерапевтам мозг. Мы столкнулись со спектром сложных и не понятных для нас [побочных] реакций. Может поражаться любой орган: начиная от щитовидной железы и заканчивая воспалением сосудов".
онколог центра им. Блохина Михаил Федянин
Но в декабре 2018 года НИИ онкологии им. Н.Н.Петрова (Санкт-Петербург) презентовал новые данные о результатах того же исследования.
У пациентов, принимавших BCD-100, чаще воспалялась щитовидная железа, чем у пациентов, принимающих аналогичные зарубежные препараты. Об этом заявил на конференции Федянин, то же впоследствии подтвердил и химиотерапевт из НИИ онкологии им. Н.Н. Петрова Алексей Новик. Его выступление находится в открытом доступе. Однако другие показатели побочных явлений не сильно отличались от уже выпущенных на рынок аналогов, так что Новик осторожно назвал BCD-100 "не менее безопасным", чем ему подобные.
2. Летальный исход, о котором умолчали
В ноябрьском выступлении доктор Федянин коротко обмолвился: были описаны смертельные случаи после приёма подобных препаратов. Одна из причин летальности — воспаление сердечной мышцы (миокардит).
Ни Федянин, ни Новик подолгу не останавливались на опасностях подобного рода препаратов. Врачи не упомянули и о смертельном случае с одним из пациентов-добровольцев. А самое главное, этого не сделала медицинский директор фармзавода "Биокад" Юлия Линькова.
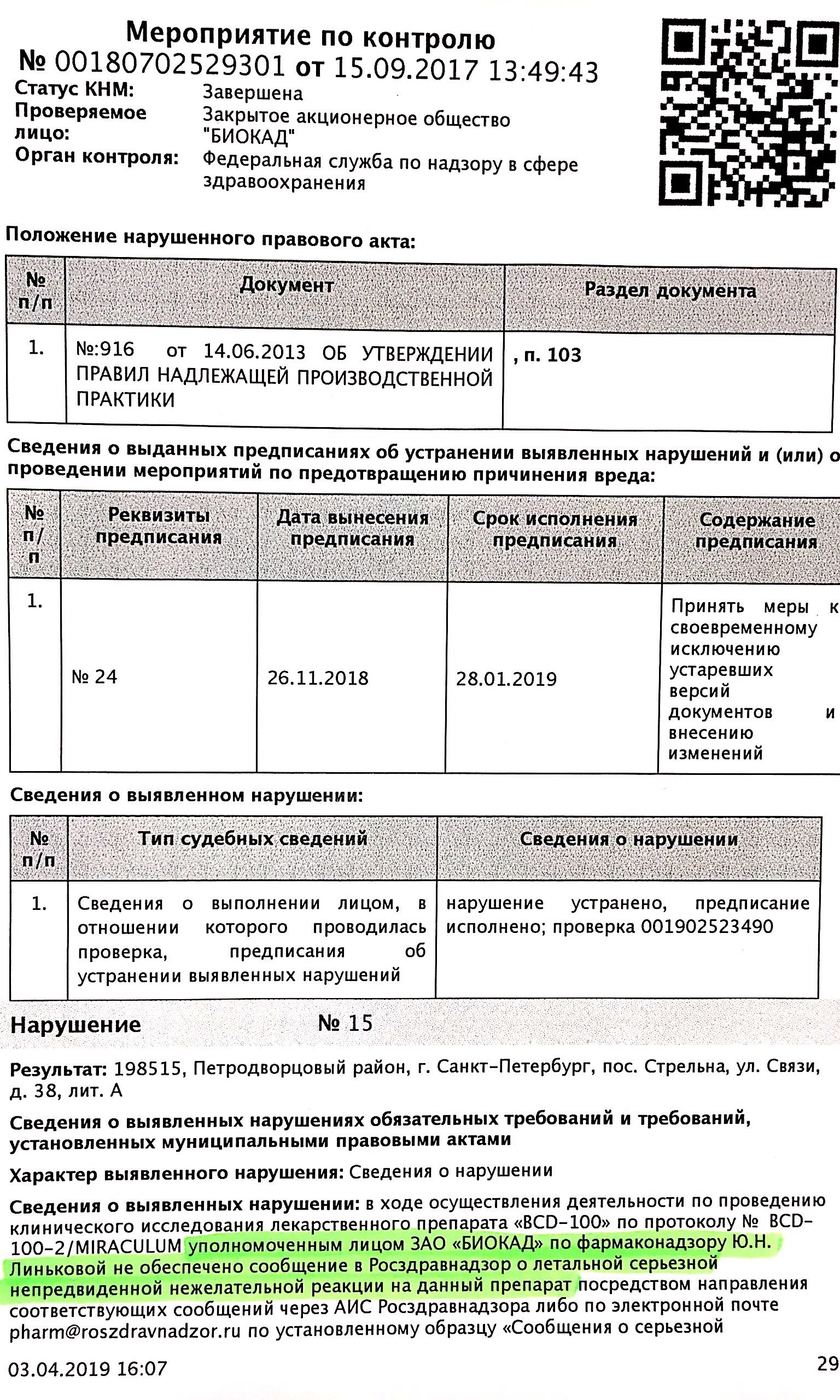
Представители завода "Биокад" вовремя не проинформировали государственные службы о смерти пациента из-за приёма BCD-100. Об этом говорится в материалах проверки Росздравнадзора, которые попали в Лайф из прокуратуры.
"В ходе клинического исследования препарата BCD-100 по протоколу Miraculum уполномоченное лицо ЗАО "Биокад" Юлия Линькова [не сообщила] в Росздравнадзор о летальной непредвиденной нежелательной реакции на данный препарат".
Материалы проверки Росздравнадзора от 26.11.18
Линькова обязана была уведомить о произошедшем либо через защищённую информационную систему Росздравнадзора, либо просто по электронной почте.
В том же предписании Росздравнадзор отмечает, что ни в 2017-м, ни в 2018-м в адрес ведомства вообще не поступало данных о безопасности трёх других препаратов, которые разрабатывает "Биокад".
Недавние исследования показали — больше половины российских медиков не сообщают в Росздравнадзор о побочных эффектах на препараты, с которыми столкнулись их пациенты. Ещё 8% вообще считают, что рассказывать о нежелательных реакциях нецелесообразно.
3. В надежде на "чудо"
Ещё в 2016 году министр здравоохранения Вероника Скворцова назвала результаты использования BCD-100 фантастическими. Протоколу, по которому исследовали лекарство, даже придумали соответствующее метафорическое название. С латыни "miraculum" переводится как " чудо". И действительно, с некоторыми пациентами BCD-100 сотворил чудо.
У 64-летней пациентки из Питера был опухолевый очаг в лёгком
Через несколько месяцев после приёма BCD-100 опухоль заметно уменьшилась в объемах. Это видно на снимках НМИЦ им. Н.Н.Петрова.
Но для других пациентов чудо обернулось проблемами или трагедией. Побочные эффекты от BCD-100 испытывали 80% пациентов, заявил на ноябрьской конференции доктор Федянин.
Чтобы разобраться, как работает BCD-100, важно понимать принцип работы иммунной системы человека.
Очень упрощённо иммунитет можно описать как систему "свой-чужой". Некоторые клетки крови умеют распознавать чужеродные бактерии и опасные тела и уничтожать их. Такой тип иммунных клеток называют Т-лимфоцитами. Получается эдакий "иммунный спецназ", который способен проникать через стенки сосудов в окружающие ткани и проводить там боевые действия против чужаков.
На поверхности Т-лимфоцита живёт белок PD-1, который отвечает за восприятие чужеродных клеток. Раковые же клетки "прячутся" от лимфоцитов, обманывая белок PD-1. Лимфоциты начинают думать, что раковая клетка — "своя", и не трогают смертельную опухоль.
Учёные по всему миру ломают головы над тем, как взломать маскировку и обучить лимфоциты распознавать в раковой клетке врага. Как уверяют создатели Miraculum, именно это им и удалось.

Создатели препарата рассчитывают, что его можно будет использовать не только для лечения меланомы и рака лёгких, но и других видов онкологии.
Поначалу на заводе "Биокад" рассчитывали выпустить лекарство на рынок в 2018 году. Сейчас сроки отодвинулись до 2022 года. Причин может быть множество: от недостаточного финансирования до неожиданно вскрывшихся проблем при использовании препарата.
В одном из интервью представители завода сравнивали цены на зарубежные аналогичные препараты. Выходило, что лечиться израильскими либо японскими средствами стоит примерно 9 миллионов рублей за курс. Отечественные разработчики обещали существенно меньшую цену за курс BCD-100. Возможно, в разы.
Хронология разработки препарата
4. Человечество писало кровью правила исследований препаратов
Лайф попросил эксперта, который много лет занимается клиническими исследованиями, рассказать о морально-этической стороне испытаний препаратов на людях. Вот что рассказала исполнительный директор Ассоциации организаций по клиническим исследованиям Светлана Завидова.
"Человечество двигалось к системе регулирования через лекарственные трагедии. Где-то, конечно, своим умом доходили, но в основном двигателем послужил негативный опыт, который и приводил к разработке тех или иных правил. Правила писали "на крови".
Светлана Завидова, Ассоциация по клиническим исследованиям
Один из первых мировых законодательных актов на тему регулирования исследований препаратов появился в США в 1938 году. Взяться за его разработку пришлось после того, как из-за неподтверждённого по критериям безопасности препарата сульфаниламида погибло 107 человек, большинство из которых — дети. Именно после этой трагедии фармпроизводителей обязали подтверждать безопасность лекарств. В том числе и на пациентах.
Исследования на людях идут в три фазы и длятся годами. В первую, как правило, включают только здоровых добровольцев. Вторая фаза — это испытания на пациентах, страдающих от конкретного заболевания. Обычно в них участвует несколько сотен человек. Третья фаза — самая масштабная: здесь в выборку могут включить несколько тысяч больных. Именно на третьей фазе появляется большинство данных о побочных реакциях и их частоте. Все добровольцы подписывают информированное согласие, соглашаясь на все риски (вплоть до летального исхода). Для многих пациентов участие в испытаниях — последний шанс.
Только при успешном завершении третьей стадии препарат регистрируют в госорганах и завозят в аптеки.
Второй случай изучают в медвузах как пример халатного отношения к безопасности препарата в угоду его продаваемости. Препарат талидомид в середине ХХ века был одним из самых продаваемых успокоительных и снотворных. Особенно его рекомендовали беременным и кормящим матерям, чтобы справляться с ночной бессонницей, утренней тошнотой и беспокойством. При этом никакие тесты влияния таблеток на плод не проводились. Препарат активно продавался в Европе. Через несколько лет стали чаще рождаться дети с патологиями: у новорожденных не было рук, ног либо ушей.
Ещё год потребовался властям нескольких стран, чтобы увязать страшную статистику с популярностью талидомида. Всё это время компания-производитель не признавала связи между этими событиями и продолжала рекламировать лекарство как безопасное.
5. Биокад: мы ничего не пытались скрыть!
Действия петербургской фармацевтической компании, которая не сообщила в Росздравнадзор о смерти пациента, на первый взгляд выглядят попыткой скрыть негатив во избежание репутационных и иных потерь. Однако в "Биокаде" заявляют, что специально ничего не утаивали.
"Первично полученные данные не соответствовали определению "Серьёзная непредвиденная нежелательная реакция". После получения дополнительных сведений информация была передана в Росздравнадзор".
Юридический департамент ЗАО "Биокад"
— Предположение о том, что ЗАО "Биокад" пыталось скрыть летальный случай, не соответствует действительности, поскольку данная информация сообщалась в ряд компетентных органов и учреждений, — добавили представители фармзавода. — Компания провела внутреннюю проверку, по результатам которой были детализированы внутренние процедуры.
Один из корпусов завода "Биокад" в Петербурге.
Компания "Биокад" создана в 2001 году. Это одна из крупнейших биотехнологических компаний России, где разрабатывают, изучают и производят новые типы лекарств. В штате трудятся более 1800 человек. Компания фокусируется на препаратах для терапии онкологических и аутоиммунных заболеваний, также ведёт разработки в области терапии других социально значимых заболеваний.
19 апреля 2019 года Национальный медицинский исследовательский центр радиологии Минздрава сообщил об увеличении числа онкобольных в стране. На первом месте в России рак лёгких. Каждый год онкологией заболевают около 600 тысяч человек. Всего в России на онкологическом учёте стоят 3,6 миллиона человек.
- Recent Entries
- Archive
- Friends
- Profile
- Memories
Об участии в клинических исследованиях.

Чтобы ответить на такие вопросы, нужно немного раскрыть суть того, что из себя представляет клиническое исследование (далее – КИ), зачем это все нужно, какова кухня, и как, собственно, в КИ попадать. Разумеется, что освещая тут эти вопросы, я рассматриваю только клинические исследования в онкологии. В каждой специальности есть своя специфика проведения исследований, и обсуждать сейчас особенности например испытания новых вакцин на здоровых добровольцах я не буду.
Итак, что такое КИ. Клиническое исследование – это испытание нового лекарственного препарата или нового метода лечения на добровольцах. Поскольку речь у нас идет об онкологии, то на добровольцах, больных онкологическим заболеванием.
Зачем. Дело в том, что многие онкологические заболевания в поздних стадиях развития плохо поддаются лечению Или вообще ему не поддаются. Например, 5-летняя выживаемость пациентов с метастатической меланомой при использовании всех современных методов лечения и лекарственных препаратов составляет 5 %. То есть, 95% пациентов умирает в течение пяти лет, несмотря на все проводимое лечение. А большая часть из них умирает в течение 6-8 месяцев после развития метастатического процесса. Существующий арсенал стандартных методов лечения – это пять-семь лекарственных препаратов и несколько возможных их комбинаций, в целом малоэффективных.
Разумеется, что такое положение вещей обуславливает постоянные поиски новых лекарственных препаратов и новых методов лечения.
Кто занимается этими поисками? В наше время – не врачи. Большая часть исследований в поисках новых лекарственных препаратов проводится фармкомпаниями. Иногда – лабораториями, принадлежащими каким-то организациям, например, НИИ в России, но за последние десятилетия ничего действительно стоящего отдельные лаборатории научно-исследовательских институтов, насколько я могу сходу вспомнить, не изобрели. Связано это с финансированием – крупные фармкомпания единовременно финансируют большое количество лабораторий, исследований, и получают на выходе этого финансирования большое количество молекул, которые могут быть активны в отношении опухолей.
После того, как молекулу получили в лаборатории, она проходит преклинические исследования – в пробирках, на животных. В ходе этих исследований предварительно изучаются ее противоопухолевые свойства и токсичность. После того, как завершились эти преклинические исследования, и в том случае, если показано, что противоопухолевые свойства имеются, а токсичность на животных контролируема, начинаются исследования на людях. Сразу оговорюсь, что этическая и юридическая сторона таких исследований очень хорошо проработана, но в объеме одного сообщения я не смогу эту часть раскрыть – слишком объемный вопрос.
Поначалу в исследования I-й фазы включается очень небольшое количество пациентов, поскольку токсичность у людей еще не изучена. Десяток, несколько десятков человек. и у этой группы изучается переносимость препарата. Иногда оказывается, что препарат, который легко переносили мышки, кошки и обезьянки, у человека вызывает такие побочные эффекты, что его применять нельзя, несмотря на все прочие прекрасные свойства. И приходится такой препарат сдавать на свалку истории.
Дальше, если показано, что препарат хорошо переносится человеком, начинают изучать различные дозовые режимы, его фармакокинетику (как препарат распределяется в организме, как быстро выводится, сколько времени длится его максимальная концентрация, и т.д.). Это вторая фаза исследований. В этой фазе подбирается оптимальная доза препарата и предварительно оцениваются его клинические эффекты. В этой фазе препарат исследуется на уже большей группе людей. Но окончательные выводы об эффективности препарата после окончания исследования II фазы сделать еще нельзя – выборка недостаточна.
После того, как особенности взаимодействия препарата и организма более-менее изучены, приступают к изучению эффективности препарата.
Для этого проводятся крупные клинические исследования. Согласно современным критериям, доказательным считается хорошо спланированное исследование, которое проводится во многих центрах одновременно, и в котором больные разделены на группы сравнения – в одной группе исследуется новый препарат, а в другой группе больные получают стандартное лечение или плацебо (в онкологии последнее редко). При этом больные распределяются случайно, без учета мнения исследователя – это называется рандомизацией. Суть рандомизации заключается в том, чтобы исследователь умышленно или нет не набирал в исследуемую группу, например, более легких пациентов, оставляя в группу контроля более тяжелых. Иногда, чтобы исключить психологический эффект приема нового препарата, пациент не знает, какой препарат – исследуемый или контрольный он принимает (слепой метод), а иногда об этом не знает не только пациент, но и врач (двойной слепой). Всё это сделано, чтобы уменьшить влияние врача и пациента на ход исследования.
В ходе этих крупных исследований III – IV фаз оценивается эффективность препарата при лечении какого-то заболевания. Дополнительно оцениваются побочные эффекты на большой группе больных. По окончании этих исследований, если препарат показал, что он эффективен в лечении болезни, он проходит регистрацию в неком государственном органе, в ведении которого лежит контроль за существующими лекарственными препаратами. В США это FDA (Food and Drug Administration), в Евросоюзе – EMA (European Medicines Agency), в России регистрацией препаратов занимается Минздрав.
После регистрации производитель может начинать продавать препарат.
Собственно, для производителя эта цель и является основной – окупить расходы на все лаборатории, которые изучали много молекул, лишь одна из которых вышла на рынок; на все преклинические исследования (и персонал, и кощки-мышки-обезянки стоят денег, и немалых); ну и на клинические исследования – это самая расходная статья в изучении препарата. Окупить предшествующие исследования и заработать.
Что кому дает клиническое исследование. Что дает производителю препарата – я уже написал. Окупаемость, прибыль, развитие.
Что дает науке и медицине в целом? Появление новых лекарственных препаратов, развитие экспериментальной и клинической науки, победы над болезнями.
Что дает непосредственно врачу-исследователю, участвующему в процессе? Во-первых деньги – эта контрактная оплачиваемая работа. Во-вторых, возможность поработать с современным препаратом и узнать много нового. Работа по исследованиям – это интересная работа, в ходе нее растешь как специалист.
Что дает пациенту? В идеале пациенту дает возможность вылечиться от неизлечимого заболевания. Да, такое бывает, и я таких пациентов знаю и наблюдаю. В других случаях, если препарат эффективен, дает возможность длительное время контролировать заболевание, не давать ему развиваться, и дать, таким образом, дополнительные месяцы, годы, а иногда десятилетия жизни. А иногда, когда препарат оказывается неэффективным, участие в исследовании ничего не дает пациенту. И пациент, когда ему предлагается участие в КИ, информируется о том, что польза от исследования может быть, а может не быть. В последнем случае есть польза только науке, в которой отрицательный результат тоже важен.
В любом случае, пациент, участвующий в исследовании, получает лечение и контроль за лечением по общемировым стандартам. В ходе исследования нет проблем сделать пациенту необходимые обследования в нужное время, назначить что-то дополнительно. При этом, все процедуры, обследования и лекарственные препараты по исследованию пациент получает бесплатно.
Это обуславливает то, что многие пациенты хотят принимать участие в КИ, поскольку КИ все-таки предоставляет шанс и обеспечивает высокое качество лечебного процесса.
И вот тут мы возвращаемся к вопросу, как туда попасть. И для этого опять придется вернутся к тому, кто исследования организует.
Организуют спонсоры, чаще всего спонсор - фармкомпания. Не имея возможности проводить клинические исследования самостоятельно, они заключают контракты с врачами-исследователями, которые проводят уже исследования на базе клиник. Но на деньги фармкомпаний. Какие врачи и клиники интересны фармкомпаниям для таких контрактов? Те, что во-первых, смогут набрать достаточное (заказанное фармкомпанией) количество испытуемых, во-вторых, качественно провести исследование (в соответствии с планом фармкомпании и правилами GCP) и обеспечить достоверность результатов.
Соответственно, в первую очередь спонсор исследования заинтересован в контрактах с крупными клиниками, имеющими большой поток пациентов с заболеванием, лечение которого исследуется. Бессмысленно заключать, например, контракт на исследование препарата в лечении рака почки с больницей какого-нибудь небольшого российского городка: там за год может быть таких пациентов один-два, а может и не быть вообще. А вот профильное отделение онкоурологии или химиотерапии в каком-то крупном онкологическом центре – самое то. То есть, чтобы найти исследование, нужно ехать в доступный крупный центр – там шансов больше.
Мало смысла искать исследование препарата, который уже исследован, прошел регистрацию, и продается. Конечно, такое желание понятно: препарат уже заведомо эффективный, а цена высокая (тот же Сутент, эффективный при раке почки, стоит порядка 200 тысяч рублей в месяц), получить его бесплатно в рамках КИ – очень заманчиво.
Но тот же Сутент уже прошел все фазы исследований. Сейчас фармкомпания заинтересована его не исследовать, а продавать, окупать свои расходы и зарабатывать, в том числе и на новые исследования. То есть, она может и поисследовать сутент, но уже на меньшей выборке, и исходя из каких-то своих целей – изучить новые показания к применению лекарства, например. То есть, искать исследование Сутента сейчас бессмысленно, искать нужно препарат, который еще не прошел регистрацию, а находится во II - III фазе клинических исследований. Препаратов, которые перечислены в письме в начале поста это тоже касается – они уже прошли регистрацию FDA, и наборов в исследование по ним сейчас гораздо меньше, чем год-два назад.
Итак, ищем еще не зарегистрированный препарат, на первом этапе обращаясь в какую-то крупную онкологическую клинику. Не факт, что получится. При том, что в крупных клиниках практически всегда проводятся клинические исследования, совершенно не обязательно, что они проводятся именно по этому заболеванию, и именно сейчас. Например, сейчас я участвую в трех исследованиях по раку почки, но обращаться к нам с этим заболеванием бессмысленно – набора в эти исследования мы уже не проводим. И это зависит совершенно не от нас, а от условий, которые выдвинул нам спонсор. Набор проводится ограниченное время, несколько месяцев, а потом мы годы изучаем препарат на уже набранных пациентах. Откроем еще один-два набора по раку почки в разные исследования осенью-зимой, но с таким заболеванием ждать этих наборов не имеет смысла, можно не дожить, и надо искать как-то еще.
Следует еще учесть, что если препарат уже раскручен, если уже были опубликованы какие-то статьи, касающиеся его эффективности, если среди профессионалов и пациентов уже ходят слухи о том, что это что-то стоящее, попасть в КИ с этим препаратом всегда сложнее. Желающих много, количество мест ограничено. И тут бессмысленно жаловаться на то, что мы набираем мало пациентов – у нас план набора с четко оговоренным количеством больных, которое мы можем включить. Мы лишь выполняем заказ спонсора. И сами порой от этого страдаем, если видим, что препарат хороший, а включить всех больных не можем.
Как искать, если нет подходящих КИ в доступных центрах?
Можно искать по тематическим сайтам. Например, я, при начале у нас какого-то исследования обычно оставляю информационное сообщение о нем на онкофоруме. Это не реклама онкофорума, это просто пример. Сейчас на нем не висит моих объявлений, но, например, в разделе онкоурологии висят объявления исследователя Ильи Тимофеева о наборе в исследования по раку почки:

А некоторое время назад висели наши – о наборе, в том числе и в исследования по вемурафенибу при меланоме. Есть и другие тематические сайты – ракпочки.нет, где можно периодически найти объявления о наборах по тому же раку почки, исследования по другой тематике можно иногда найти на сайтах клиник и онкологических диспансеров, других онкологических ресурсах.

В результатах поиска, которые представляют из себя данные о КИ, часто перечислены страны, в которых они проводятся, контакты, куда можно обратиться.

Найти так набор в клиническое исследование можно почти всегда по почти любому заболеванию. Просто отнюдь не всегда это будет в вашем городе и иногда даже в вашей стране. Существующее законодательство позволяет бесплатно участвовать в клиническом исследовании в других странах, и, собственно то, что исследование проводится, например, в США, не препятствие к участию в нем. Проблемы тут возникают в оплате дороги, жилья, визах, каких-то дополнительных медицинских услугах, не входящих в стоимость исследования. Таким образом, поиск клинического исследования – это процесс, который требует определенного труда и затрат, связанных с перемещением в другие города, и иногда страны.
Найдя где-то подходящее клиническое исследование на clinicartrials.gov, нужно позвонить, либо списаться с теми людьми, координационными центрами, которые представлены в контактной информации. Там можно узнать, продолжается ли набор в КИ, где есть ближайший центр и с кем нужно связаться, чтобы стать кандидатом на участие в КИ. Из американского офиса крупной фармкомпании вас, вероятнее, всего, направят в российское ее представительство, если вы в России, и если в России проводится набор. Либо дадут контакты ближайшего центра в другой стране. Конечно, в реальности все происходит иногда сложнее - до кого-то не удается дозвониться, кто-то в отпуске, нужного человека может не быть на месте и попросят перезвонить, но в целом, последовательность телефонных переговоров и писем может помочь добиться цели – выйти на врача, который непосредственно занимается набором больных в исследование.
Следующая сложность, которая может возникнуть, это несоответствие пациента критериям включения в исследование. Дело в том, что в каждое исследование есть свои критерии включения и исключения, суть которых сводится к тому, чтобы создать однородную выборку больных с заданными характеристиками. Например, в исследование могут не включаться пациенты с метастазами определенных локализаций, или требуемым условием может быть определенный гистологический тип опухоли или наличие в ней определенных мутаций. Основные критерии включения и исключения всегда приводятся в аннотации к исследованию, но они всегда неполные.

Например, частым условием является хороший статус по ECOG, что означает, что пациент должен быть в хорошем самочувствии, полностью сам себя обслуживать, сохранять в той или иной мере работоспособность. Если пациент не соответствует критериям включения или у него есть критерии исключения, то как бы не хотел сам пациент, и как бы не хотел врач его включить, в это исследование врач пациента включить не может.
В этом случае приходится начинать все сначала. В связи с этим, лучше вести поиск сразу в нескольких направлениях – списываться с разными центрами, пытаться стать кандидатом в разные КИ.
На этом я закончу написание этой простыни, которая является ответом на вопрос, заданный в начале. На самом деле, я тут не осветил и малой части вопросов, касающихся клинических исследований, которые мне бы хотелось осветить. Быть может, займусь этим еще как-нибудь. Ну а тем, кто ищет - удачи в поиске!
Читайте также:


