Герцептин при лечении рака желудка
Bang Y-J, Van Cutsem E, Feyereislova A, et al
ToGA [Trastuzumab for Gastric Canser] - это первое рандомизированное исследование III фазы по изучению Герцептина в комбинации с химиотерапией в лечении метастатического HER2-положительного рака желудка или пищеводно-желудочного перехода
Герцептин в комбинации с химиотерапией значимо увеличивает общую выживаемость больных HER2 + раком желудка или пищеводно-желудочного перехода
Дополнительный анализ в подгруппах показал, что наилучшие результаты были получены у больных с гиперэкспрессией HER2 (медиана общей выживаемости составила 16 месяцев)
Герцептин в комбинации с химиотерапией значительно увеличивает общую выживаемость по сравнению с применением только химиотерапии у больных HER 2 – положительным метастатическим раком желудка или пищеводно-желудочного перехода
- Пятилетняя выживаемость при распространенном или метастатическом раке желудка составляет 15-20% 1-3
- Необходимы новые методы Плечения с более высокой эффективностью и благоприятным профилем безопасности 4-7
- Доказано, что HER2 играет важную роль в развитии рака желудка 4-7
Исследование ToGA
- В исследовании приняли участие пациенты, страдающие HER2-положительным местнораспространенным и/или метастатическим раком желудка или пищеводно-желудочного перехода (Рисунок 1)
- В рамках исследования HER2 позитивность опухоли определялась как:
- гиперэкспрессия HER2, определенная методом иммуногистохимии (ИГХ 3+);
- амплификация HER2, определенная методом флуоресцентной гибридизации in situ (FISH)
 |
| Рисунок 1. Дизайн исследования ToGA |
Корреляция между уровнем экспрессии HER2 и общей выживаемостью
- В процессе скрининга в исследовании ToGA HER2 статус был определен у большого числа больных раком желудка
- Запланированный анализ предполагал корреляцию между гиперэкспрессией HER2 и общей выживаемостью (Рисунок 2)
- Корреляция между гиперэкспрессией HER2 и общей выживаемостью была подтверждена анализом в подгруппах
- IHC 2+/FISH+ или IHC 3+ /независимо от статуса FISH (n = 446)
- Герцептин в комбинации с химиотерапией увеличивает общую выживаемость до 16 месяцев по сравнению с 11.8 месяцев в группе пациентов, получавших только химиотерапию
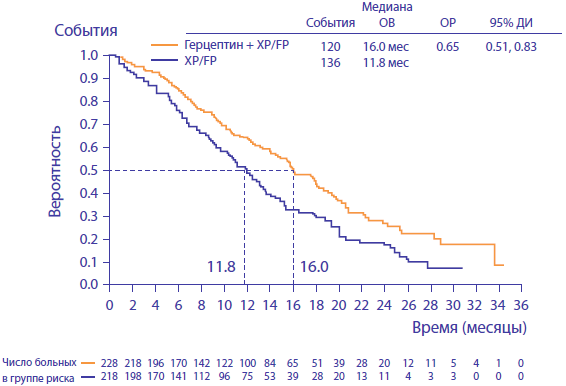 | ||
| ОВ - общая выживаемость | ОР - относительный риск | ДИ - доверительный интервал |
| Рисунок 2. Общая выживаемость больных с гиперэкспрессией HER2 Герцептин в комбинации с режимом XP обеспечивает хорошую переносимость лечения | ||
Безопасность
- Частота возникновения нежелательных явлений не различалась в группах пациентов, получавших только химиотерапию и Герцептин в комбинации с химиотерапией
- Наиболее часто отмечаемыми нежелательными явлениями были тошнота, нейтропения, рвота и анорексия (таблица 1)
- Частота развития нежелательных явлений со стороны сердечно-сосудистой системы не различалась в группах пациентов, получавших только химиотерапию и Герцептин в комбинации с химиотерапией
| Нежелательные явления , % | Герцептин + XP/FP n=294 | XP/FP n=290 | ||
| Все* | Степень + | Все* | Степень + | |
| Тошнота | 67 | 7 | 63 | 7 |
| Анорексия | 46 | 6 | 46 | 6 |
| Рвота | 50 | 6 | 46 | 8 |
| Запоры | 26 | |||
| *Возникали у >10% больных + Возникали у >5% больных | ||||
| Таблица 1. Частота нежелательных явлений (НЯ) | ||||
Герцептин в комбинации с режимами химиотерапии XP/FP 9,10
- Рекомендуемый режим введения Герцептина –в комбинации с Кселодой или внутривенным введением 5-фторурацила и препаратом платины
- XP режим – Кселода 2000 мг/м²/сутки в дни 1-14 каждые 3 недели × 6 циклов, Цисплатин 80 мг/м² в день 1 каждые 3 недели × 6 циклов
- FP режим – 5-фторурацил 800 мг/м²/день в виде непрерывной в/в инфузии в дни 1-5 каждые 3 недели × 6 циклов, Цисплатин 80 мг/м² в день 1 каждые 3 недели × 6 циклов
| Дозы Герцептина | Длительность лечения | |
| Нагрузочная доза | 8 мг/кг | |
| Поддерживающая доза | 6 мг/кг каждые 3 недели (через 3 недели после нагрузочной дозы) | До прогрессирования заболевания |
Выводы
- Герцептин в комбинации с химиотерапией устанавливает новый стандарт терапии HER 2 –положительного метастатического рака желудка или пищеводно-желудочного перехода
- Дополнительный анализ продемонстрировал, что наилучшие результаты получены у больных с гиперэкспрессией HER2 (ИГХ2+/FISH+ или ИГХ3+). Медиана обшей выживаемости составила 16 месяцев
- Частота развития нежелательных явлений не различалась в группах пациентов, получавших только химиотерапию и Герцептин в комбинации с химиотерапией
- КЛЮЧЕВЫЕ СЛОВА: таргетная терапия, химиотерапия, опухоли органов пищеварения, рак желудка, онкология
Рак желудка занимает второе место в структуре онкологической смертности в мире. Восточная Европа по заболеваемости находится на третьем месте после Японии и Китая. В России ежегодно регистрируются 40 000 новых случаев и 25 000 смертей от рака желудка. В развитии лекарственного лечения рака желудка наблюдаются тенденции, характерные для лечения чувствительных к химиотерапии опухолей. Метаанализ рандомизированных исследований при раке желудка показал, что комбинированная химиотерапия приводит к существенному повышению показателей общей выживаемости по сравнению с монохимиотерапией или наилучшей поддерживающей терапией [1].
Режим DCF (доцетаксел, цисплатин, 5-фторурацил (5-ФУ)) признан стандартом лечения на современном этапе в США. Однако этот режим обладает выраженной миелотоксичностью: по зарубежным данным, нейтропения 3–4-й степени развивается в 82,3% случаев. Была предложена следующая модификация режима DCF: доцетаксел (Таксотер) 75 мг/м2 во 2-й день, цисплатин 75 мг/м2 во 2-й день, 5-ФУ 500 мг/м2 – 3-часовая инфузия в 1, 2, 3-й дни каждые 21 день (TPF), что позволило сохранить эффективность терапии (ОЭ = 48,1%, МВДП = 5,5 мес.; МОВ = 11,5 мес.; 1-годичная выживаемость – 46,6%) и снизить частоту побочных эффектов: нейтропения 3–4-й степени – с 82,3% до 57,1%, фебрильная нейтропения 3–4-й степени – с 30% до 10,3% [2].
Наиболее эффективные режимы комбинированной химиотерапии, такие как DCF, EOX (эпирубицин, оксалиплатин, капецитабин), ХР (капецитабин, цисплатин), позволили увеличить медиану выживаемости больных с диссеминированным раком желудка до 9,2–11,2 мес. (рис. 1) [2, 3, 4]. Фундаментальные исследования подтвердили наличие амплификации и гиперэкспрессии гена HER2 не только при раке молочной железы, но и при ряде других солидных опухолей (табл. 1) [5]. Учитывая усиливающийся интерес к возможностям таргетной терапии и известные с 1994 г. данные о частоте гиперэкспрессии HER2 при раке желудка (по разным данным, у 12–55% больных), начато изучение Герцептина у больных с HER2-положительным раком желудка.
С этой целью было организовано международное рандомизированное исследование III фазы ToGA (Trastuzumab for Gastric Adenocarcinoma) [6]. В качестве схемы химиотерапии был выбран режим: 5-фторурацил или капецитабин с цисплатином ± трастузумаб (Герцептин). Данный режим был выбран как один из наиболее эффективных, хорошо переносимых, универсальных, используемых в качестве схемы сравнения во многих исследованиях. В качестве факторов стратификации рассматривались: распространенность процесса, локализация опухоли (желудок или пищеводно-желудочный переход – ПЖП), измеряемая или неизмеряемая опухоль, общее состояние больного по шкале ECOG (0–2), какой фторпиримидиновый препарат был использован – 5-фторурацил или капецитабин.
Критериям включения соответствовали мужчины и женщины старше 18 лет с гистологически подтвержденной неоперабельной местнораспространенной рецидивной или метастатической аденокарциномой желудка или гастроэзофагеального перехода; с общим статусом пациента 0–2 по критериям ECOG; с ненарушенной функцией печени, измеряемыми или неизмеряемыми очагами. HER2-статус опухолей определялся централизованно с помощью иммуногистохимии (HercepTest, Dako, Denmark) и флуоресцентной гибридизации in situ (FISH; HER2 FISH pharmDx, Dako). Вследствие биологических различий, характерных для опухолей молочных желез и желудка, особенно из-за гетерогенности опухолей, для рака желудка была разработана новая классификация иммуногистохимических критериев, специфичных для рака желудка. Эти критерии были скорректированы согласно исследованию Hofmann и соавт. [7].
Главной целью исследования ToGA являлось сравнение общей выживаемости больных. Был проведен скрининг 3807 больных, у 810 из них (22,1%) выявили HER2-положительный статус опухоли. В исследовании участвовали 584 пациента, удовлетворявшие всем критериям включения. Больные были рандомизированы на 2 группы: 290 больных получали 5-фторурацил или капецитабин с цисплатином, а 294 пациента – те же схемы + трастузумаб.

Герцептин - Первый таргетный биологический препарат, демонстрирующий существенное улучшение показателей выживаемости у больных раком желудка
Результаты международного исследования ToGA показали, что терапия Герцептином значительно продлевает жизнь больным раком желудка.
В исследовании ToGA медиана общей выживаемости пациентов с гиперэкспрессией HER2 составила 16 мес по сравнению с 11,8 мес у пациентов, которые получали только химиотерапию. «Герцептин является первым таргетным биологическим препаратом, увеличивающим выживаемость больных распространенным раком желудка.
В январе 2010 г. на основании убедительных результатов исследования III фазы ToGA регуляторными органами Европейского союза по ускоренной процедуре была рассмотрена заявка на расширение списка показаний к применению Герцептина, что позволило многим пациентам быстрее получить лечение, продлевающее жизнь. Данное одобрение вступило в силу сразу же после принятия решения во всех странах Евросоюза и в государствах Европейской ассоциации свободной торговли (Исландии, Лихтенштейн, Норвегии). Ожидается, что одобрения на расширение списка показаний к применению Герцептина будут вскоре получены и в других странах.
По мировым оценкам, в структуре онкологической смертности рак желудка занимает 2-е место. В структуре онкологической заболеваемости это заболевание занимает 4-е место: ежегодно регистрируется более 1 млн новых случаев заболевания. В России ежегодно регистрируется 40 тыс. новых случаев рака желудка. Распространенный рак желудка характеризуется неблагоприятным прогнозом, средняя продолжительность жизни после постановки диагноза на фоне проводимой современной терапии составляет около 10–11 мес. Приблизительно в 15–18% случаев определяется гиперэкспрессия HER2. Диагностика рака желудка на ранних стадиях затруднена, что связано с бессимптомным течением этого заболевания.
Клиническое исследование Герцептина
ToGA – первое рандомизированное исследование III фазы по изучению Герцептина в качестве терапии неоперабельного местно-распространенного, рецидивирующего и/или метастатического HER2-положительного рака желудка. Для этого исследования было исследовано около 3800 больных.
Таргетная противоопухолевая терапия представляет собой использование лекарственных препаратов и других субстанций для блокирования роста опухолевых клеток путем взаимодействия с особыми молекулами, участвующими в процессах роста и прогрессирования опухоли.
В исследовании ToGA все пациенты были рандомизированы на две группы, в каждой из которых в качестве первой линии терапии использовали один из следующих схем (протоколов) химиотерапии:
– фторпиримидин (Кселода или 5-фторурацил – 5-ФУ) в сочетании с цисплатином 1 раз в 3 нед (6 циклов). Большинство пациентов получали Кселоду и цисплатин в качестве химиотерапии;
– Герцептин в дозе 6 мг/кг 1 раз в 3 нед в комбинации с фторпиримидином и цисплатином (6 циклов) до прогрессирования заболевания.
Основная цель исследования – продемонстрировать преимущество комбинированного режима с включением Герцептина перед химиотерапией в показателях общей выживаемости. Дополнительными критериями эффективности были выживаемость без прогрессирования, частота объективного ответа, длительность ответа, безопасность и качество жизни.
В ходе исследования ToGA новых или ранее не зарегистрированных побочных эффектов не выявлено. При анализе данных общей выживаемости относительный риск составил 0,74 (CI 0,60, 0,91) при очень высоком уровне достоверности (p=0,0046).
В группе HER2-положительных пациентов (22% от всех больных, прошедших процедуру HER2-тестирования), получивших хотя бы одну дозу исследуемого препарата, Герцептин увеличивал медиану выживаемости до 13,8 мес, а показатель частоты объективного ответа – с 34,5 до 47,3%. В группе пациентов, у которых была выявлена гиперэкспрессия рецептора HER2 на поверхности опухолевых клеток (IHC3+ или IHC2+/FISH+), медиана общей выживаемости увеличилась до 16 мес (16% от всех больных, прошедших процедуру HER2-тестирования).
Герцептин (трастузумаб)
Герцептин – гуманизированное антитело, разработанное для связывания с белком HER2 и блокирования его функции. Синтез белка HER2 контролируется особым онкогеном. Уникальность механизма действия Герцептина заключается в его способности активировать иммунную систему организма и блокировать HER2-рецепторы, такое прицельное действие способствует разрушению опухоли.
Герцептин продемонстрировал свою беспрецедентную эффективность при лечении HER2-положительного рака молочной железы как на ранних стадиях, так и при распространенной (метастатической) форме заболевания. Показано, что монотерапия Герцептином и его комбинация со стандартной химиотерапией или последовательный режим применения стандартной химиотерапии и Герцептина увеличивают частоту объективного эффекта, выживаемость без признаков заболевания и общую выживаемость, поддерживая качество жизни больных HER2-положительным раком молочной железы.
Герцептин - противоопухолевый препарат, представляющий собой моноклональные МИБП-антитела, действующие против HER2-neu рецепторов.
Как работает Герцептин?
Установлено, что Герцептин вызывает иммунно-опосредованную цитоксичность, блокирует пролиферацию и апоптоз клеток-мишеней, обладает антиангиогенной активностью. Подробно рассматриваются принципы использования Герцептина при лечении рака молочной железы как в качестве монотерапии, так и в комбинации с цитостатическими препаратами. Лечение Герцептином может быть эффективно и при других видах опухоли. Герцептин, в отличие от традиционных химиотерапевтических препаратов воздействует только на раковые клетки с повышенным содержанием рецепторов HER2 и поэтому вызывает меньше побочных эффектов.
Показания к применению Герцептина:
Метастатический рак молочной железы с опухолевой гиперэкспрессией HER2:
— в качестве монотерапии, после одной или более схем химиотерапии;
— в комбинации с паклитакселом или доцетакселом, в случае отсутствия предшествующей химиотерапии (первая линия терапии);
— в комбинации с ингибиторами ароматазы при положительных гормональных рецепторах (эстрогеновых и/или прогестероновых) у женщин в постменопаузе.
Ранние стадии рака молочной железы с опухолевой гиперэкспрессией HER2:
— в виде адъювантной терапии после проведения хирургического вмешательства, завершения химиотерапии (неоадъювантной или адъювантной) и лучевой терапии;
— в комбинации с паклитакселом или доцетакселом после адъювантной химиотерапии доксорубицином и циклофосфамидом;
— в комбинации с адъювантной химиотерапией, состоящей из доцетаксела и карбоплатина;
— в комбинации с неоадъювантной химиотерапией и последующей адъювантной монотерапией препаратом Герцептин при местно-распространенном (включая воспалительную форму) заболевании или в случаях, когда размер опухоли превышает 2 см в диаметре.

Насколько он эффективен?
Удаление опухоли молочной железы (мастэктомия или лампэктомия) само по себе не гарантирует, что заболевание не вернется. Наряду с лучевой терапией и химиотерапией, Герцептин назначается после операции для предотвращения рецидива HER2 позитивного рака молочной железы.
Риск развития рецидива рака молочной железы у женщин, получавших Герцептин и химиотерапию в течение года после операции, на 40 - 50 процентов ниже, чем у получавших только химиотерапию.
Безопасен ли Герцептин?
Наиболее серьезным побочным действием курса приёма Герцептина является нарушение деятельности сердца - кардиомиопатия, которая наблюдается в 2 - 7 процентов случаев. Все пациенты, получающие Герцептин проходят исследования сердца: эхокардиография или, что предпочтительнее, MUGA тест каждые несколько месяцев. Риск развития кардиомиопатии особенно повышается при одновременном применении Герцептина и химиотерапевтического препарата Доксорубицин.
Примерно у 1 процента пациентов развиваются легочные осложнения.
Наиболее частым (40%) побочными эффектом лечения Герцептином являются гриппоподобные симптомы: повышение температуры, боли в мышцах, тошнота. Как правило, эти симптомы появляются в начале лечение, и в дальнейшем проходят.
В целом, лечение Герцептином переносится больными гораздо легче, чем традиционная химиотерапия.
Состав
Помимо активного вещества в состав Герцептина входят L-гистидин и L-гистидина гидрохлорид, 1-O-α-D-глюкопиранозил-α-D-глюкопиранозид (или α,α-трегалоза), неионогенный ПАВ полисорбат 20.
Форма выпуска
Препарат выпускается во флаконах прозрачного стекла в виде лиофилизированного порошка для приготовления инфузионного раствора. Каждый флакон комплектуется флаконом растворителя, который представляет собой содержащую в своем составе бензиловый спирт бактериостатическую воду.
Количество активного вещества в одном флаконе лиофилизата может составлять:
- 150 мг;
- 440 мг.
Герцептин (Herceptin): фармакологическое действие
Герцептин относится к группе медицинских иммунобиологических препаратов, которые применяются для лечения злокачественных образований.
Активное вещество препарата трастузумаб — это синтезируемое из клеток яичников китайского хомяка и обладающее противоопухолевым действием лекарственное вещество, которое применяется в таргетной терапии рака молочной железы.
Вещество представляет собой так называемые моноклональные (то есть вырабатываемые аналогичными иммунными клетками) антитела, которые обладают способностью обнаруживать и блокировать HER-2 рецепторы, локализирующиеся на поверхностях клеточных мембран опухолевых клеток. Это в свою очередь обеспечивает прекращение их дальнейшего роста и — в ряде случаев — уменьшение размеров раковой опухоли. При этом трастузумаб не оказывает влияния на здоровые ткани.
Герцептин, воздействуя на генетические механизмы злокачественного перерождения клеток, блокирует их и существенно снижает восприимчивость клеток к излишкам мембранного белка HER-2, повышенная экспрессия которого напрямую связана с вероятностью развития рака молочной железы. В результате этого процесса тормозятся процессы деления раковых клеток и устраняется так называемый эффект перепроизводства.
Фармакодинамика и фармакокинетика
Связываемый с ростом раковых клеток белок HER-2 является протоонкогеном или, иначе говоря, обычным геном, который при стечении определенных условий (мутации, повышения степени экспрессии, например) может спровоцировать рак. Его гиперэкспрессия отмечается примерно в каждом третьем или четвертом случае, когда у пациентки диагностируется первичный рак молочной железы. Также выявляется и значительная вариабельность HER-2 в отношении распространенного рака желудка.
Белок HER-2 находится на оболочке отдельных раковых клеток. Он создается специальным геном, который носит название HER-2/neu, и является рецептором для определенного фактора роста, который принято называть человеческим эпидермальным фактором роста. Прикрепляясь к рецепторам HER-2 на раковых клетках молочной железы, последний стимулирует их рост и активное деление. Отдельные раковые клетки характеризуются повышенным количеством рецепторов HER-2, что позволяет идентифицировать раковую опухоль как HER-2 позитивную. Новообразования подобного типа диагностируются у каждой пятой женщины с раком груди.
Входящий в состав Герцептина трастузумаб оказывает блокирующее действие на пролиферацию атипичных клеток у пациенток с повышенной экспрессией HER-2. Использование препарата в качестве монотерапевтического средства при лечении HER-2 позитивного метастатического рака молочной железы, проводимого в качестве терапии второй и третьей линии, позволяет добиться 15-типроцентной суммарной частоты ответа и увеличить медиану выживаемости пациенток до 13 месяцев.
Применение же Герцептина в сочетании с доцетакселом, анастрозолом или паклитакселом у женщин с метастатическим раком груди способствует увеличению:
- частоты суммарного ответа;
- медианы временного интервала до начала прогрессирования заболевания (в некоторых случаях практически вдвое);
- периода выживаемости;
- общей частоты эффекта;
- частоты клинического улучшения.
При назначении препарата после проведенного хирургического вмешательства или вспомогательной (адъювантной) терапии после хирургического лечения пациенткам, у которых диагностированы ранние стадии рака груди, в значительной степени повышается:
- продолжительность выживаемости без появления симптомов заболевания;
- выживаемость без развития рецидива заболевания;
- выживаемость без появления отдаленных метастазов.
Антитела к трастузумабу выявляются у одной из 903 женщин, однако, при этом аллергические реакции на препарат отсутствуют.
Фармакокинетические параметры Герцептина зависят от дозы: чем она выше, тем больше средний показатель периода полувыведения трастузумаба и тем меньше клиренс препарата.
Фармакокинетические параметры не изменяются при одновременном назначении с Герцептином анастрозола. Также на распределение трастузумаба в организме. Исследования фармакокинетики препарата у пациенток преклонного возраста, страдающих от почечной и/или печеночной недостаточности, на сегодняшний день не проводились.
Показания к применению
Препарат показан для лечения метастазирующего рака груди у пациенток, у которых установлена повышенная экспрессия HER-2. При этом эффективность Герцептина отмечается как при использовании его в качестве монотерапевтического средства после проведения процедуры химиотерапии, так и в сочетании с другими препаратами. Как правило, комплексная терапия при отсутствии предшествующей химиотерапии подразумевает одновременное назначение с Герцептином паклитаксела или доцетаксела. У пациенток с позитивными эстрогеновыми и/или прогестероновыми рецепторами также допускается назначение препарата в комбинации с препаратами-ингибиторами ароматазы.
На ранних стадиях развития заболевания, которые не характеризуются наличием у пациентки с HER-2 позитивным раком груди метастазов, препарат назначают в качестве средства адъювантной терапии:
- после проведеннойхирургической операции;
- по завершении курса химиотерапии (как адъювантной, так и неоадъювантной);
- по завершении курсалучевой терапии.
Противопоказания
Основным противопоказанием к назначению Герцептина является гиперчувствительность пациентки к активному веществу или какому-либо из вспомогательных компонентов препарата (включая бензиловый спирт).
С осторожностью препарат рекомендуется назначать:
- женщинам, страдающим от ишемической болезни сердца;
- пациенткам с устойчиво повышенным артериальным давлением и сердечной недостаточностью;
- пациенткам, прошедшим курс лечения кардиотоксичными препаратами (например, антрациклинами или циклофосфамидом);
- если раку грудисопутствуют заболевания легких;
- если опухоль дала метастазы в легкие;
- детям (поскольку эффективность и безопасность лечения Герцептином у этой группы пациентов не изучена).
Также с соблюдением мер осторожности препарат прописывают больным на ранних стадиях HER-2 позитивного рака груди, у которых отмечается:
- застойная сердечная недостаточность (в анамнезе);
- устойчивая к терапии аритмия;
- требующая медикаментозного лечения стенокардия;
- пороки сердца, характеризующиеся клинической значимостью;
- трансмуральный инфаркт миокарда по данным электрокардиограммы;
- устойчиво повышенное артериальное давление, резистентное к лечению.
Побочные действия
Как и большинство противоопухолевых средств (википедия подтверждает этот факт) препарат в определенной степени обладает токсичностью, может провоцировать нежелательные реакции, а в отдельных случаях и летальный исход. Наиболее вероятные побочные эффекты Герцептина, которые развиваются на фоне лечения им, это:
- различного рода инфузионные реакции (как правило, они возникают после первого введения препарата и выражаются в виде озноба, лихорадочного состояния, одышки, появления высыпаний, повышения слабости и т.д.);
- общие реакции (слабость, болезненность молочной железы, гриппоподобный синдром и т.д.);
- нарушения функции пищеварительной системы (тошнота, рвота, симптомы гастрита, расстройства стула и т.д.);
- нарушения функции опорно-двигательного аппарата (болезненность в конечностях, артралгия и т.д.);
- кожные реакции (высыпания, зуд, крапивница и т.д.);
- нарушения функции сердца и сосудистой системы (застойная сердечная недостаточность, вазодилатация, тахикардия и т.д.);
- нарушения со стороны системы кроветворения (лейкопения, тромбоцитопения и т.д.);
- нарушение функции нервной системы (головные боли, парестезии, повышение мышечного тонуса и т.д.);
- расстройства функции органов дыхания (одышка, кашель, кровотечения из носа, боли в горле и гортани и т.д.);
- нарушения со стороны мочеполовой системы (цистит, урогенитальные инфекции и т.д.);
- нарушение функций зрения и слуха;
- побочные эффекты, обусловленные повышенной чувствительностью к компонентам препарата (ангионевротический отек, анафилактический шок, аллергические реакции).
Инструкция на Герцептин: способ применения и дозирование препарата
Инструкция по применению Герцептина предупреждает, что препарат предназначен исключительно для внутривенного капельного введения. Струйное введение запрещено.
Продолжительность внутривенной капельной инфузии составляет 1,5 часа (или 90 минут) при нагрузочной (максимальной) дозе трастузумаба, равной 4 мг на 1 кг веса пациентки.
При возникновении во время введения препарата побочных реакций, которые могут выражаться в виде озноба или лихорадки, одышки появления хрипов в легких и т.д., инфузию приостанавливают и возобновляют лишь после полного исчезновения неприятных клинических симптомов.
При проведении поддерживающей терапии дозу трастузумаба сокращают вдвое (до 2 мг на 1 кг веса пациентки). При этом кратность процедур инфузии составляет 1 раз в неделю.
При хорошей переносимости предшествующей дозы Герцептин вводят капельным методом в течение получаса, до прогрессирования заболевания.
Передозировка
Клинические исследования препарата не выявили случаев передозировки Герцептином. Введение разовой дозы, которая превышала бы 10 мг трастузумаба на 1 кг массы тела, не проводилось.
Взаимодействие
Специальные исследования взаимодействия препарата с другими лекарственным средствам у человека не проводились. Клинически значимые взаимодействия Герцептина с другими препаратами, которые применялись у пациенток одновременно с ним, выявлены не были.
Нельзя допускать разведения или смешивания инфузионного раствора с другими лекарственными средствами. В частности, нельзя разводить его глюкозой, поскольку последняя провоцирует агрегацию белка.
Герцептин характеризуется хорошей совместимостью с инфузионными пакетами из поливинилхлорида, полиэтилена или полипропилена.
Условия продажи
Отпуск Герцептина осуществляется по рецепту.
Условия хранения
Препарат хранят при температуре от 2 до 8 °C. Готовый инфузионный раствор при таком температурном режиме сохраняет стабильность своих фармакологических свойств на протяжении 28 дней. Это обусловлено содержанием консерванта в бактериостатической воде, которая используется в качестве растворителя для лиофилизированного порошка и по этой причине допускается многократное использование концентрата раствора. По прошествии 28 дней раствор необходимо утилизировать.
При разведении лиофилизата водой, не содержащей консервантов, концентрат следует использовать немедленно.
Помещенный в инфузионный пакет раствор Герцептина подлежит хранению в течение 24 часов при условии, что соблюдается указанный выше температурный режим, а раствор был приготовлен в строго асептических условиях.
Срок годности
Препарат считается годным к употреблению на протяжении 4 лет.
Читайте также:

