Фотодинамическая терапия опухоли стеноза пищевода
Фотодинамическая терапия (ФДТ) была одобрена для использования в США с декабря 1998 года. Показания к ее применению вышли за пределы патологии пищеварительного тракта и включают рак легких и кожи. В дополнение к этому появились сообщения о новых показаниях для применения ФДТ в лечения заболеваний желудочно-кишечного тракта (ЖКТ) включая патологию пищевода (в основном пищевод Барретта) и заболевания желудка, ДПК, билиарного и панкреатического трактов 1 . Основой для столь широкого применения ФДТ является ее способность к оказанию лечебного воздействия на большие области слизистой без необходимости их полной визуализации. Терапевтическое воздействие может осуществляться через фиброволокно, которое проводит свет перпендикулярно оси эндоскопа, что делает эту технологию идеальной для ЖКТ. Также наблюдается прогресс в способах доставки светового излучения и лазерных технологиях, что сделало эту процедуру гораздо более легкой для применения, чем в прошлом.
Технология
ФДТ заболеваний ЖКТ может проводиться путем инъекции Фотофрина II. Он обычно вводится внутривенно в дозе 2 мг/кг за 48 часов до проведения эндоскопии с фотооблучением. Хотя формула препарата не претерпела изменений Администрация по пищевым продуктам и лекарствам США обновила данные по длительности кожной фоточувствительности связанной с приемом препарата, которая составляет 30-90 дней после введения. Эти цифры более соответствуют клиническому опыту. Однако пациент может снизить этот период фоточувствительности путем дозированного действия солнечного света на кожу, что приводит к разрушению препарата в ней в результате процесса называемого "photobleaching." [5] . Этот препарат недавно был продан его первым владельцем QLT (Ванкувер, Британская Колумбия) Канадской компании Axcan Pharma (Монреаль, Квебек). Это привело к изменению дистрибьютора препарата в США от Sanofi к Axcan.
5-аминолевулиновая кислота (5-ALA) так же применяется в США, но в настоящее время только в сфере дерматологии. Фотосенсибилизаторы второго поколения, дающие возможность более глубокого разрушающего эффекта на патологические ткани и с кожной фоточуствительностью только в течение 1-3 дней в настоящее время проходят клинические испытания.
Фотооблучение осуществляется светом лазера с помощью фиброволоконного рассеивателя проведенного через биопсийный канал стандартного эндоскопа. В прошлом, длинна рассеивателя была ограничена 1,0-2,5 см, что приводило к повышению длительности процедуры при необходимости облучать большие участки тканей т.к. приходилось перемещать фиброволокно через каждые 2,5 см патологического участка ЖКТ. Недавно разработанный рассеиватель длинной 5,0 см облегчил выполнение процедуры. Появления рассеивателей такой длинны делает необходимым использование измерителей мощности излучения для его адекватной установки. Т.к. работа лазера оценивается на основе мощности излучения на верхушке рассеивателя, все фиброволокно должно быть помещено в измеритель мощности для получения правильного результата. В дополнении к этому был разработан баллонный рассеиватель, предназначенный для лечения длинных сегментов пищевода Барретта, который позволяет поместить 9 см фиброволокно в специальный 7 см баллон [6] . Этот баллон устанавливается в необходимое положение по проводнику под контролем детского гастроскопа. В коммерческой продаже этот баллон в настоящее время отсутствует. Красный свет лазера, проходящий через фиброволокно рассеивателя и активирующий фотосенсибилизатор ранее генерировался путем использования аргонового или содового-титаново-фосфатного/ неодим: иптрий-алюминий-гранатового (KTR-YAG) лазеров с целью заставить цветные лазеры дать необходимую длину волны. Этот тип лазеров был относительно громоздким и иногда требовал использования специальных источников питания и охлаждения. Размер и сложность этих устройств был обусловлен необходимостью совместного использования двух разных типов лазеров. Значительно более маленькие, простые и меньше весящие устройства для фотооблучения были созданы с помощью диодной лазерной технологии (630 PDT Laser, Model T2USA, Diomed, Кембридж, Великобритания). Эти лазеры могут быть помещены в стандартную эндоскопическую стойку и используют нормальную силу тока. Этот прогресс в сфере технологии уменьшил сложность ФДТ и должен значительно уменьшить уровень ее осложнений.
Применение при патологии пищевода
ФДТ была изначально одобрена для паллиативного лечения рака пищевода, для которого другое лечение не возможно. Было показано, что оно эффективнее абляции высокоэнергитическим неодим: иптрий-алюминий-гранатовым лазером (Nd:YAG) [7] . Это лечение применяется как для аденокарциномы так и плоскоклеточного рака пищевода как с паллиативной целью так и для радикального лечения [8] . Лечебное воздействие осуществляется легко т.к. пищевод просто достижим при выполнении эндоскопии. Терапия наиболее эффективна при раке с обструкцией и резким сужением просвета пищевода, что делает термальное паллиативное воздействие, например Nd:YAG лазером более сложным. ФДТ также высоко эффективна в областях пищевода сложных для установки стента, что наиболее часто встречается в проксимальных его отделах. Sodium porfimer вводится пациенту в дозе примерно 2,0 мг/кг за примерно 48 часов до облучения. Затем выполняется эндоскопия с подведением к о опухоли цилиндрического фиброволоконного рассеивателья диаметром около 1 мм. Длинна фиброволокна выбирается в зависимости от протяженности опухоли, с тем расчетом, что бы некоторое количество нормальных тканей захватывалось в область облучения (для гарантии адекватного воздействия на опухоль). Сила светового воздействия обычно соответствует 400 милливаттам на сантиметр фиброволокна облучающего опухоль и общей дозе 300 джоулей на сантиметр фиброволокна. Т.к. некроз тканей не виден сразу после облучения, некоторые эндоскописты предпочитают осмотреть область лечения через 1-2 дня, что бы быть уверенными в адекватном его объеме. Если ответа на терапию не получено, то проводится повторное облучение в дозе 80 джоулей на сантиметр фиброволокна. Исследования показывают, что паллиативный эффект лечения рака пищевода через месяц после лечения имеет место в 32 % случаев при использовании ФДТ и 20 % в случае Nd:YAG лазера [7] .
ФДТ так же используется для радикального лечения поверхностных случаев рака пищевода у пациентов имеющих противопоказания к хирургическому лечению. Первые сообщения указывали, что ФДТ может быть эффективна в лечении поверхностных опухолей менее 2 см в диаметре у 74 % пациентов в сроках наблюдения 5 лет, хотя сроки наблюдения в этой группе были ограничены в связи с сопутствующей патологией [8] . Недавние исследования показали, что опухоли меньшего размера лучше отвечают на ФДТ и опухоль должна проникать вглубь не более чем на 2 мм для достижения успешной абляции при использовании в качестве фотосенсибилизатора ALA [9] . Использование эндоскопической резекции слизистой имеет основное преимущество в точной установки глубины пенетрации опухоли, что должно помочь эндоскопистам в выборе оптимальных кандидатов для ФДТ.
Одной из наиболее интересных сфер применения ФДТ является пищевод Барретта (ПБ) [1,10] . Надежды связаны с циркулярным повреждающим воздействием на патологические ткани, что возможно при ФДТ, при диффузном поражении слизистой, что имеет место при ПБ. Начальные исследования показали способность ФДТ устранять дисплазию высокой степени у почти 90 % пролеченных пациентов [1] . В дополнение к этому все сегменты ПБ были полностью устранены у 1/3 пациентов. Это было достигнуто при применении существующей в настоящее время технологии - введения sodium porfimer в дозе 2 мг/кг и дозы облучения около 200 джоулей на сантиметр фиброволокна рассеивателя. ФДТ проводилась с использованием такого же цилиндрического рассеивателя, как и при паллиативном лечении рака пищевода. Контрольная эндоскопия, проводившаяся через 48 часов после первой процедуры, являлась стандартной процедурой. При обнаружении "пропущенных" областей или оценке лечебного воздействия как "неполного" проводилась добавочная терапия в дозе 50 джоулей на сантиметр фиброволокна. Основной проблемой связанной с этим видом терапии являются осложнения, наиболее серьезное из которых - формирование стриктур и кожная фотосенсибилизация [11] . Стриктуры формируются у примерно 28 % - 35 % всех пролеченных пациентов. Требующими решения техническими задачами остается разработка лучших облучающих устройств как, например, баллонный рассеиватель и улучшенных фотосенсибилизаторов дающих кожную фоточувствительность только в течение 1- 14 дней. Некоторые, интенсивно изучаемые в Европе фотосенсибилизаторы, такие как ALA, могут назначаться перорально в день облучения [12] . Важным вопросом, ответ на который еще предстоит получить является отдаленный результат лечения т.к. преимущество абляции слизистой над наблюдением при ПБ с дисплазией высокой степени не доказано. Предварительные результаты продолжающегося проспективного рандомизированного исследования включающего 208 пациентов с дисплазией высокой степени и сравнивающие результаты применения ФДТ в сочетании с ингибиторами протонной помпы и только ингибиторов протонной помпы обнаружило, что ФДТ имеет значительное преимущество в сфере ингибиции развития рака. Однако это заключение базируется на предварительном анализе проведенном спустя 6 месяцев после включения последнего пациента в исследование. Хотя долговременная эффективность этой терапии не изучена, имеются указания, что для успеха может требоваться полная эрадикация слизистой ПБ [13] . Генетический дефект слизистой может сохраняться после ФДТ несмотря на гистологическое улучшение. Другой потенциальной проблемой абляции является наличие слизистой ПБ лежащей под нормальным плоским эпителием. Имеется сообщение о, по крайней мере, одном таком случае, что показывает, что карцинома может развиваться и при этом типе слизистой [14] . В настоящее время ФДТ по поводу ПБ, как и другие вмешательства основанные на абляции, должны применяться только у избранных пациентов. Необходимость наблюдения за пациентами сохраняется и после выполнения процедуры.
Применение при патологии желудка
ФДТ в основном применяется для радикального лечения у пациентов с поверхностными желудочными неоплазмами и противопоказанным хирургическим лечением. ФДТ с sodium porfimer в дозе 2 мг/кг и дозой облучения 30 - 50 джоулей на сантиметр квадратный, как было выявлено, ведет к излечению поверхностного рака желудка у 82 % пациентов [15] . Наилучший эффект достигается в случае приподнятых опухолей менее 20 мм в диаметре и незначительно углубленных опухолей менее 10 мм в диаметре [16] . Недавние исследования так же подтвердили эти результаты - примерно 80 % поверхностного рака "кишечного типа" были успешно пролечены ФДТ с использованием в качестве фотосенсибилизатора мезо-тетрагидрофенил-хлорина (mTHPC) [17] . Этот препарат в настоящее время не доступен в США, но известно, что он увеличивает глубину некроза и дает меньшую кожную фоточувствительность, чем sodium porfimer. Сообщается о минимальных побочных эффектах ФДТ в желудке с менее выраженными болевыми ощущениями и меньшим риском формирования стриктур, чем при применении ее в пищеводе [18] .
Неопластические заболевания поджелудочной железы
Клиническое использование ФДТ в лечении неопластических поражений поджелудочной железы все еще находится в состоянии развития. На основании исследований на животных с использованием mTHPC и феофорбида A выявлено, что эти фотосенсибилизаторы накапливаются в очагах рака поджелудочной железы 20 . Исследования с использованием одного из вариантов коммерчески доступного sodium porfimer под названием дериват гематопорфирина, показали, что этот фотосенсибилизатор так же может распределяться в поджелудочной железе [23] . Существуют неопубликованные сообщения о небольшой группе пациентов пролеченных по поводу злокачественных заболеваний поджелудочной железы с помощью mTHPC и использовании техники "кишечной имплантации". Трудностью лечения в случае поджелудочной железы является необходимости обеспечения адекватной дозиметрии светового воздействия на опухоль. Это обычно достижимо только путем использования светочувствительных зондов установленных непосредственно рядом с опухолью, что трудно осуществить клинически. В дополнение к этому mTHPC не доступен в США.
Неопластические заболевания билиарного тракта
Начальные преклинические работы показали, что холангиокарцинома должна быть чувствительна к ФДТ с использованием sodium porfimer [24] . Лечение хирургически некурабельных холангиокарцином (Bismuth III-IV) этим методом вызвало большой интерес т.к. первые сообщения показали, что у пролеченных с помощью ФДТ 9 человек наблюдалось значительное улучшение качества жизни и выживаемости по сравнению с контрольной группой [25] . Это лечение может проводиться путем введения sodium porfimer в дозе 2,0 мг/кг за 48 часов до облучения. Фотооблучение может быть сложно осуществить в билиарном тракте из-за ригидности коммерчески доступных цилиндрических фиброволоконных рассеивателей. Эта проблема может быть преодолена путем предварительного введения 1,0-2,5 см цилиндрического рассеивателя в билиарный катетер диаметром 8F [26] . Этот катетер имеет отверстие, размером 0,038-inch, на дистальном конце, которое может быть использовано для введения проводника диаметром 0.035-inch. Локализация холангиокарциномы выявляется при РХПГ, устанавливается ее проксимальный и дистальный края. Проводник диаметром 0.035-inch проводится через холангиокарциному. Катетер затем может быть аккуратно продвинут по проводнику к дистальной части области обструкции и затем аккуратно извлечен. Позиция цилиндрического рассеивателя проверяется путем использования флюроскопии. Затем осуществляется лечебное воздействие на холангиокарциному с мощностью 400 милливатт на сантиметр длинны фиброволокна и в общей дозе 180 джоулей на сантиметр квадратный. Наиболее сложным моментом фотооблучения является осторожная установка фиброволокна без нарушения его целостности. После фотооблучения производится установка билиарных катетеров размером 10F или 11.5F для обеспечения дренажа желчи непосредственно после лечения. Возможные осложнения этого лечения включают холангит и длительную кожную фоточувствительность. Хотя этот факт и не доказан, кажется разумным инструктировать пациентов получавших лечение по поводу билиарной обструкции соблюдать осторожность в отношении воздействия солнечного света более длительный период т.к. соединения порфирина экскретируются через билиарную систему.
Неопластические заболевания ДПК
Существует сообщение о небольших исследованиях включавших 10 пациентов как с карциномой ампулы БДС так и дуоденальным полипозом [27] . Эти исследователи также использовали производные гематопорфирина в дозе 4 мг/кг, которые должны быть эквивалентны коммерчески доступному sodium porfimer в дозе 2,0 мг/кг. Через 48 часов проводилось лечебное фотооблучение в дозе варьирующей от 50 до 70 джоулей на сантиметр фиброволокна. Об осложнениях (исключая кожную фоточувствительности у 3х пациентов) не сообщалось. Если зона поражение была ограничена ампулой, могла быть достигнута ее полная абляция, хотя через год часто возникал рецидив. Если опухоль выходила за пределы ампулы, наблюдалось только некоторое уменьшение ее размеров, а большие опухоли переходящие на ДПК на лечение вообще не отвечали. Полипы ДПК у 6 пациентов с семейным аденоматозным полипозом также были пролечены с использованием sodium porfimer [3] . Полный ответ наблюдался у одного пациента с поверхностным очагом рака в полипе. Другое исследование с использованием sodium porfimer у 3х пациентов с большими полипами ДПК обнаружило уменьшение их размеров на 50 % после лечения [28] . Эти исследования показывают, что ФДТ заболеваний ДПК должно выполняться в случае небольших поражений ампулы БДС или поверхностных полипов ДПК.
Неопластические заболевания толстой кишки
Интенсивные доклинические исследования на клеточных и животных моделях показали, что большой спектр фотосенсибилизирующих агентов могут быть эффективными в лечение рака толстой кишки [2,29-31] . В особенности важно то, что ФДТ оставляет коллагеновый слой стенки толстой кишки интактным, в отличие от термального воздействия, что должно уменьшит риск перфорации кишки после лечения [32] . Множество агентов исследовались in vitro, включая фталоцианины, аминолевулиновую, mTHPC, и алюминий сульфацированный фталоцианин. Однако доступно ограниченное количество клинической информации по использованию ФДТ в случае полипов и рака толстой кишки. Восемь пациентов с неполным удалением ворсинчатых опухолей с помощью Nd:YAG лазера получили лечение ФДТ с сочетанием sodium porfimer и производных гематопорфирина [2] . Световое воздействие осуществлялось в дозе 50 джоулей. Положительный ответ, заключающийся в полной элиминации полипа, наблюдался во всех, кроме 2 случаев. ФДТ с использованием mTHPC также применялась и при раке толстой кишки, но результаты его противоречивы [28] . Один из пациентов в этом исследовании был полностью излечен от поверхностного рака 8 мм в диаметре при использовании ФДТ основанной на sodium porphimer.
Заключение
Было установлено, что ФДТ превосходит термальное воздействие в палиативном лечении рака пищевода. Ее основная роль базируется на возможности воздействия на большие участки слизистой желудочно-кишечного тракта без необходимости их непосредственной визуализации. Большие поверхностные полипы или небольшие очаги рака в областях пищевода, желудка, ДПК и билиарного древа неудобных для хирургической резекции являются перспективными областями для проведения дальнейших исследований. ПБ с дисплазией высокой степени может стать показанием для данного вида терапии при положительном заключении проводящегося в настоящее время рандомизированного исследования.
Рак пищевода представляет собой заболевание, при развитии которого на стенках органа образуется злокачественная опухоль. Это состояние весьма распространено, оно находится на шестом месте в списке наиболее часто встречающихся раковых патологий. Самым первым симптомом обычно становится затрудненное глотание во время употребления грубой пищи. Это объясняется сужением пищевода.
Симптоматика
- На первоначальном этапе, когда образование еще имеет небольшой размер, у пациента обычно отсутствуют какие-либо признаки рака. Однако потом начинает казаться, будто проглоченная еда застревает в пищеводе и ее надо запить жидкостью.
- Следующим симптомом является боль в области грудины. Еще через некоторое время пациент страдает от пищеводной рвоты или срыгивания, которое возникает из-за закупорки. В результате вся пища возвращается назад. Из-за застоя остатков продуктов появляется неприятный запах из ротовой полости.
- Когда опухоль распространяется на другие органы, может появиться одышка, сильная боль в грудине, осиплость голоса, утомляемость, сонливость и апатия.
Чтобы надеяться на благоприятный прогноз лечения, не следует игнорировать появление первых симптомов.

Стадии
- На предраковой стадии клетки располагаются на поверхности органа, не попадая вглубь стенок.
- На 1-й стадии раковое новообразование прорастает вглубь слизистой оболочки, но при этом не поражает мышечные ткани. Метастазирование отсутствует, однако опухоль хорошо заметна.
- На 2-й стадии могут появиться трудности во время глотания. Опухоль прорастает в мышечные ткани. Могут образоваться метастазы в соседних лимфатических узлах.
- Для 3-й стадии характерно выраженное нарушение глотания, резкое похудение. Новообразование прорастает сквозь все слои пищевода. Появляются метастазы на близнаходящихся лимфатических узлах и других органах.
- На 4-й стадии метастазы затрагивают отдаленные лимфоузлы и органы. Терапия на данном этапе развития заболевания затруднена, а прогноз будет неблагоприятным.

Методы лечения
Выбор лечения при злокачественных опухолях пищевода определяется типом и стадией рака, общим состоянием здоровья пациента, наличием у него сопутствующих заболеваний. На ранних стадиях обычно прибегают к хирургическому лечению после курса неоадъювантной химиолучевой терапии. На более поздних стадиях, когда удаление опухоли невозможно, химиолучевая терапия становится основным методом лечения.
Хирургическое лечение
Обычно хирургическое лечение при раке пищевода проводят после предварительного курса неоадъювантной химиолучевой терапии. Чаще всего выполняют эзофагэктомию: удаляют пораженный опухолью участок с захватом здоровой ткани выше и ниже. Затем оставшуюся часть пищевода соединяют с желудком. Если остался слишком короткий участок, который не удается подтянуть к желудку, используют отрезок кишки. Если рак находится в месте соединения пищевода с желудком, удаляют также часть желудка. Эзофагэктомию можно выполнить двумя способами:
- Классический вариант — открытая операция через разрез.
- При миниинвазивном вмешательстве хирург делает несколько небольших проколов и вводит через них специальные эндоскопические инструменты. Миниинвазивные вмешательства менее травматичны, после них быстрее происходит восстановление, но они возможны не всегда и требуют от хирурга специальных навыков, а от операционной — соответствующего оснащения.
Если опухоль не получается удалить, возможно паллиативное хирургическое лечение (о нём речь пойдет ниже).

Химиотерапия
При раке пищевода обычно назначают следующие комбинации химиопрепаратов: карбоплатин + таксол, цисплатин + 5-фторурацил, эпирубицин + цисплатин + 5-фторурацил, доцетаксел + цисплатин + 5-фторурацил, цисплатин + капецитабин, оксалиплатин + 5-фторурацил/капецитабин. Химиотерапия, как правило, не может полностью уничтожить опухоль. Обычно её применяют с другими целями:
- Перед хирургическим вмешательством, чтобы сократить размеры опухоли и упростить её удаление (неоадъювантная химиотерапия).
- После хирургического лечения, чтобы уничтожить оставшиеся раковые клетки и снизить риск рецидива (адъювантная химиотерапия).
- В качестве основного лечения, в сочетании с лучевой терапией, если опухоль невозможно удалить, либо имеются иные противопоказания к хирургическому лечению.
- В качестве паллиативного лечения, чтобы избавить от боли и облегчить глотание.
Новое направление в лечении рака пищевода — таргетная терапия
- В некоторых раковых клетках присутствует слишком много копий гена HER2. В итоге на их поверхности увеличивается количество молекул одноименного белка, который способствует их размножению. Заблокировать белок HER2 помогает препарат трастузумаб.
- Некоторые опухоли выделяют много вещества под названием VEGF, которое стимулирует рост новых сосудов, снабжающих раковые клетки кислородом и питательными веществами. В данном случае применяют таргетный препарат рамуцирумаб.
Лучевая терапия
Как и химиотерапия, лучевая терапия при раке пищевода бывает неоадъювантной, адъювантной, может (в сочетании с химиотерапией) выступать в качестве основного метода лечения, в том числе паллиативного.
Чаще всего процедуры проводят по классической методике: на определенном расстоянии от пациента устанавливают аппарат и направляют излучение на проекцию места, в котором находится опухоль. Иногда прибегают к брахитерапии: миниатюрный источник излучения при помощи эндоскопа помещают внутрь пищевода. При этом излучение уничтожает раковые клетки, но мало затрагивает здоровые ткани.
Борьба с осложнениями рака пищевода
Одно из основных осложнений рака пищевода на поздних стадиях — непроходимость, когда больному становится трудно глотать даже жидкую пищу. При этом врач может назначить разные виды паллиативного лечения:
- Может быть выполнена гастростомия или еюностомия. Хирургическим путем в стенке брюшной полости создают отверстие и подшивают к нему желудок или тощую кишку. Через получившееся отверстие (стому) больной получает питание в обход пищевода. Это помогает нормализовать вес и общее состояние, чтобы пациент мог перенести курс лучевой терапии и химиотерапии.
- Дилятация — искусственное расширение пищевода. В его просвет вводят специальный баллон в спущенном состоянии и, достигнув места сужения, раздувают его. Процедуру можно повторять.
- Стентирование — эндоскопическое вмешательство, во время которого в пищевод устанавливают стент — полый металлический каркас с сетчатой стенкой. Он расширяет просвет органа и позволяет нормально проходить пище.
- Фотодинамическая терапия предусматривает обработку опухоли специальным веществом — фотосенсебилизатором — с последующим облучением светом определенной длины волны. Это приводит к разрушению раковых клеток.
- Электрокоагуляция и криодеструкция — процедуры, во время которых опухолевую ткань, соответственно, разрушают при помощи электрического тока или низкой температуры.
Паллиативное лечение на поздних стадиях также включает химиолучевую терапию, которая помогает уменьшить опухоль и продлить жизнь больного, борьбу с болью и другими симптомами.
Каковы прогнозы на разных стадиях?
Шансы на победу над раком наиболее высоки, если опухоль находится в пределах стенки пищевода и не распространяется на соседние структуры. При этом пятилетняя выживаемость составляет 40–41%, то есть почти половина больных остаются живы спустя 5 лет после постановки диагноза.
При прорастании опухолевой ткани в соседние органы и лимфоузлы выживаемость падает почти вдвое — до 21–23%. При появлении отдаленных метастазов прогноз в большинстве случаев неблагоприятный, пятилетняя выживаемость составляет не более 4–5%.
Рак пищевода представляет собой опухоль злокачественного характера, происходящую из эпителиальных клеток пищевода. Заболевание берет начало с внутреннего слоя, то есть слизистой оболочки, а затем распространяется наружу, преодолевая подслизистый и мышечный слои.
Существует два основных вида такого заболевания:
- Плоскоклеточный рак. Он возникает из клеток, составляющих слизистую оболочку пищевода. Чаще всего встречается в зоне шеи, а также двух верхних третей грудной клетки.
- Аденокарцинома, другими словами – железистый рак. Чаще всего диагностируется в нижней трети пищевода. Вначале происходит замещение железистого эпителия плоскоклеточным (при пищеводе Барретта).
Статистика
Чаще всего (до 80% случаев) новообразование находится в нижне- и среднегрудном отделах пищевода. С частотой 10-15% случаев диагностируется рак шейного отдела пищевода.
Факторы риска
Основные факторы риска возникновения и развития такой болезни:
- мужской пол, потому что мужчины чаще подвержены вредным привычкам – курению и употреблению спиртного в больших количествах;
- возраст – чем он больше, тем выше риск, лишь 15% пациентов были младше 55-ти лет;
- избыточная масса тела;
- курение и злоупотребление спиртным;
- употребление очень горячих напитков и еды;
- пищевод Барретта (когда в нижней части пищевода возникает клеточное перерождение, вызываемое кислотным повреждением хронической формы);
- рефлюкс;
- ахалазия (когда нарушена запирательная функция отверстия между желудком и пищеводом);
- рубцы в пищеводе, приведшие к его сужению;
- синдром Пламмера-Винсона (для такого синдрома характерна триада, то есть три вида нарушений одновременно: нарушенная глотательная функция, суженный пищевод, железодефицитная анемия);
- контакт с химикатами.
Примерно у 1/3 заболевших диагностирован ВПЧ (вирус папилломы человека).
Риск заболеть этим видом рака можно снизить, если разнообразно питаться, не пить крепкий алкоголь, а при наличии синдрома Барретта отслеживать изменения в слизистой оболочке.
Скрининг этого заболевания не проводится. Однако при повышенном риске появления рака пищевода рекомендуется проходить эндоскопическое исследование, при необходимости с биопсией подозрительной зоны.
Симптомы
Обычно рак пищевода обнаруживается на поздних стадиях, когда терапия уже осложнена, или случайно.
Наиболее частая симптоматика включает следующее:
Есть и более редкие симптомы:
- кашель;
- икота;
- хриплый голос;
- рвота;
- костные боли (при наличии метастазов);
- пищеводное кровотечение (после того как кровь проходит по ЖКТ, стул окрашивается в черный цвет);
- как следствие кровотечения – анемия (человек становится бледным, слабым, быстро утомляется, испытывает постоянную сонливость).
Важно! Наличие подобных симптомов еще не означает рак. Однако нужно обязательно обратиться к врачу и обследоваться.
Классификация рака пищевода
По области возникновения:
- внутригрудной отдел пищевода;
- шейный отдел (от нижней границы перстневидного хряща до входа в грудную полость);
- верхняя грудная зона (от входа в грудную полость до области бифуркации трахеи);
- средняя грудная область (проксимальная часть пищевода распространяется от зоны бифуркации трахеи до соединения пищевода с желудком);
- нижняя грудная область (дистальная часть пищевода примерно 10 см в длине, включая абдоминальную часть пищевода, распространяется от зоны бифуркации трахеи до соединения пищевода и желудка).
По характеру роста опухоли:
- в просвет пищевода (экзофитный);
- язвенный (эндофитный);
- круговая форма (инфильтративный склерозирующий).
По степени дифференцировки новообразования:
- степень не определена – Gx;
- высокодифференцированное образование – G1;
- умеренно дифференцированное – G2;
- малодифференцированное – G3;
- недифференцируемое – G4.

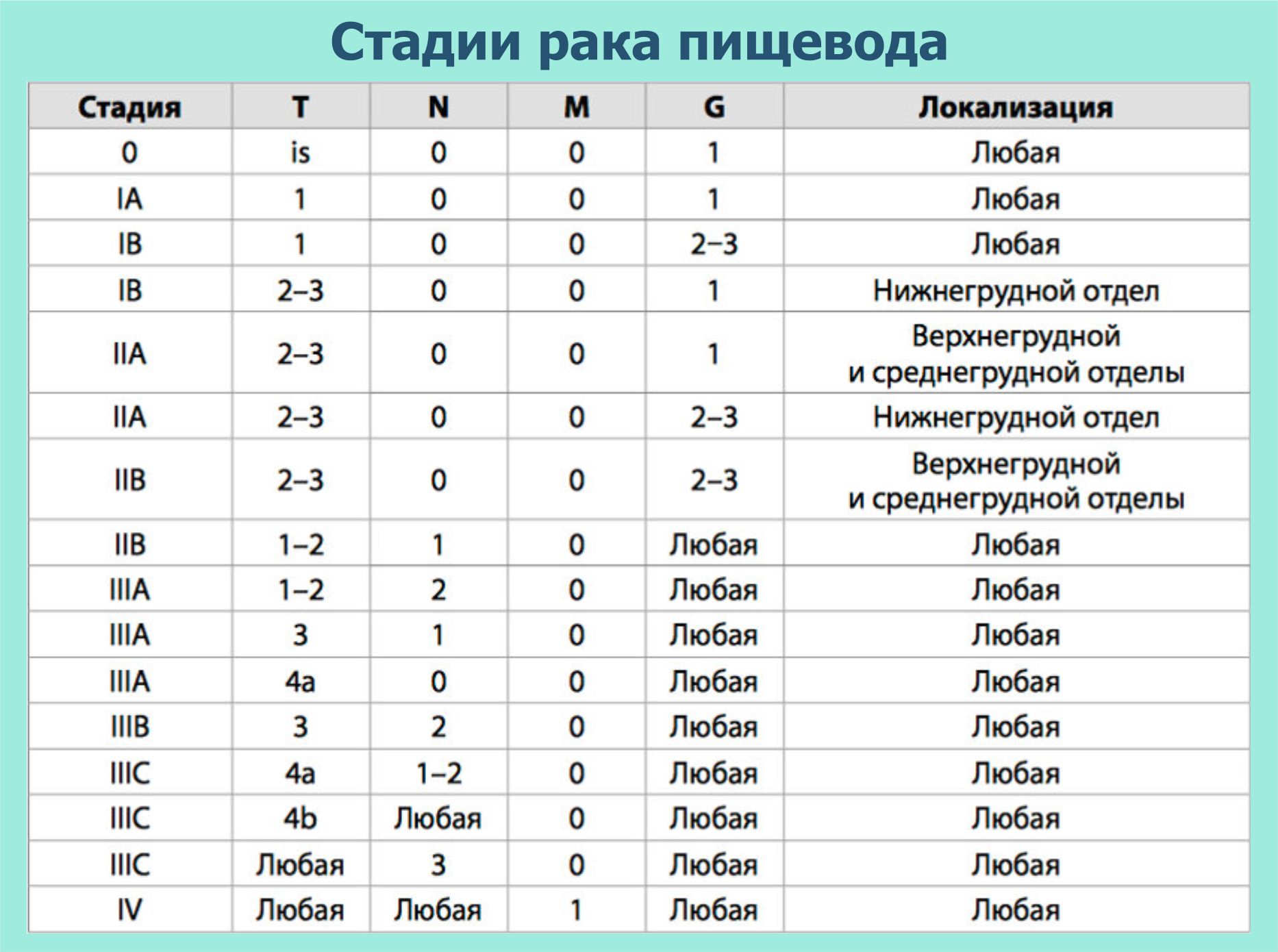
Стадии рака пищевода
Предлагаем ознакомиться с таблицей стадирования заболевания:
Диагностика
Диагностирование осуществляется инструментальными и лабораторными методами.
-
Рентгенография с бариевым контрастом. Пациент принимает внутрь сульфат бария, который обволакивает стенки пищевода. Это позволяет увидеть на снимке рельеф стенок и обнаружить сужение просвета. На ранней стадии рак может иметь вид небольших круглых выпуклостей, то есть бляшек. На поздней стадии развития новообразование принимает вид большой опухоли неправильной формы, которая может вызывать сильное сужение пищевода. Рентгенография также позволяет диагностировать трахеопищеводную фистулу, то есть когда из-за разрушения новообразованием стенки пищевода на всю толщину пищевод начинает сообщаться с трахеей.
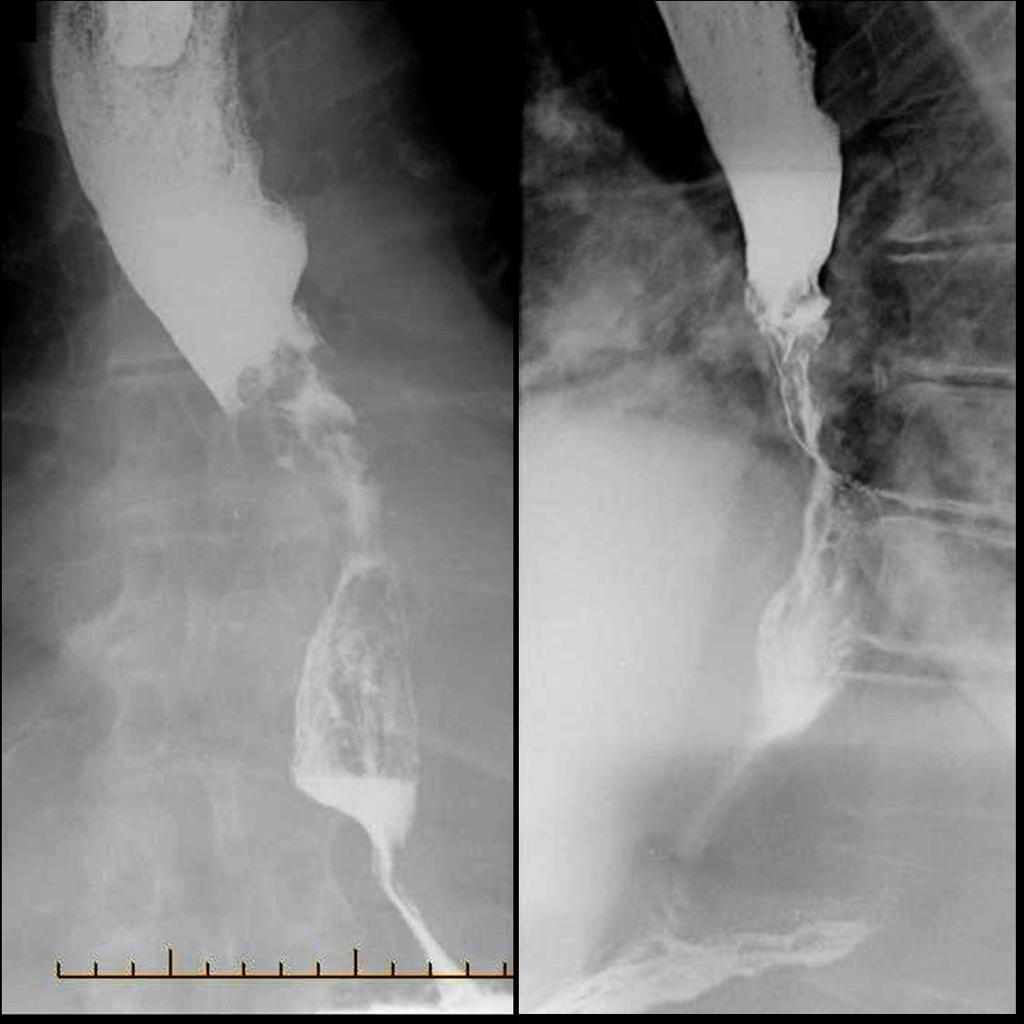
Рентгенодиагностика рака пищевода
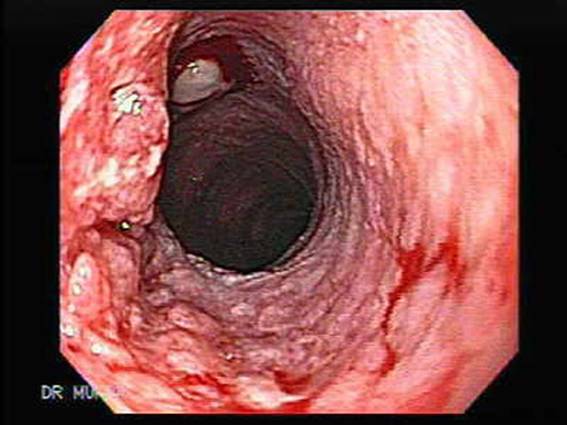
Эндоскопическая картина аденокарциномы
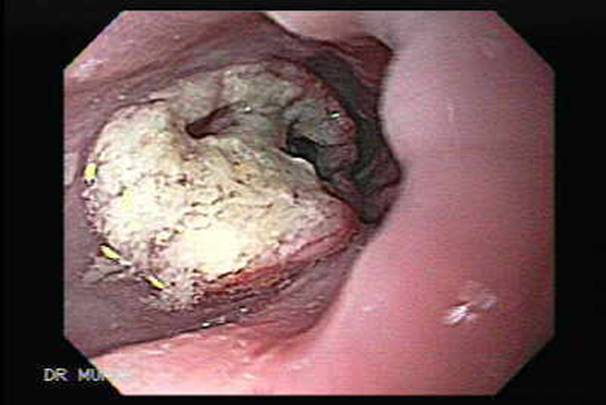
Эндоскопическая картина плоскоклеточного рака
- Клинический анализ крови. Позволяет выявить анемию, которая возникает из-за кровотечения или скудного рациона.
- Биохимический анализ крови. Он показывает состояние внутренних органов, а именно почек, печени и др.
- Анализ на онкомаркеры СА 19-9, РЭА.
- Исследование биоматериала, взятого во время биопсии. В нем определяют рецепторы белка HER2. При их наличии против новообразования можно использовать таргетную терапию.
Лечение
Основной метод лечения – хирургическая операция, однако комплексный подход позволяет улучшить результаты. Поэтому различные методики комбинируются.
В ходе операции удаляют пищевод целиком или его часть, все зависит от распространенности и локализации патологического процесса.
Когда опухоль находится в шейном отделе, удаляют большую часть пищевода. После этого желудок поднимают и подшивают к оставшейся части пищевода. Кроме того, вместо удаленной части методом пластической операции может быть использована часть толстой или тонкой кишки. При возможности выполнения резекции шейного отдела пищевода может быть выполнена пластика кишкой с микрососудистым анастомозом сосудов на шее.
При локализации опухоли в шейном отделе пищевода с большим распространением приходится выполнять операцию в объеме: удаления фаринголарингоэктомии с одномоментной пластикой пищевода желудочным трансплантатом, с пришиванием его к корню языка.
Хирургическое вмешательство по удалению части пищевода с последующим замещением трансплантатом может быть проведено открытым способом или методом торакоскопии и лапароскопии.
При любом типе вмешательства удаляют регионарные лимфоузлы, которые потом исследуют в лаборатории методом гистологии. Если в них обнаруживаются раковые клетки, то после операции пациенту прописывают лучевое лечение или химиотерапию в комбинации с ЛТ.
Также существуют паллиативные операции. Их проводят для того, чтобы пациент мог питаться, если из-за опухоли он не может глотать. Этот тип вмешательства называется гастростома, то есть введение через переднюю брюшную стенку в желудок специальной трубки для питания.
Применяется ионизирующее излучение с целью уничтожения клеток новообразования. Такая терапия может проводиться:
Разновидности лучевого лечения:
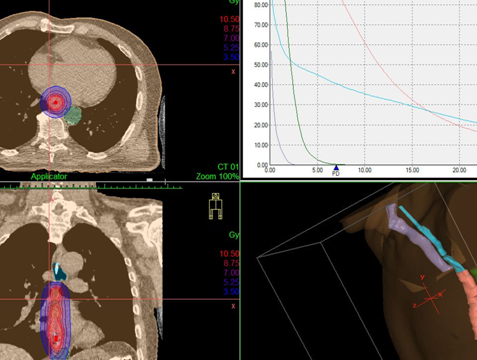
Дозное распределение, получаемое при дистанционной конформной лучевой терапии и внутрипросветной брахитерапии
Данная методика представляет собой введение в организм препаратов, затормаживающих жизнедеятельность опухолевых клеток или уничтожающих их. Лекарственные средства принимаются внутрь или вводятся в вену, после чего попадают в кровоток и достигают почти всех областей организма.
Химиотерапия осуществляется циклами. Это связано с тем, что действие препарата направлено на те клетки, которые постоянно делятся. Введение повторяется через определенное число дней, что связано с клеточным циклом. Циклы химиотерапии, как правило, имеют продолжительность 2-4 недели, больным обычно показано несколько циклов.
Как и облучение, химиотерапия показана в адъювантном и неоадъвантном режимах. Также она применяется, чтобы облегчить симптоматику тем больным, у которых рак распространен и не поддается хирургическому лечению.
Направлена на блокировку роста новообразования путем воздействия на определенные мишени, то есть на те молекулы, которыми определяются деление и рост опухоли. Если в биоматериале, взятом методом биопсии, находят такие белковые молекулы, то может быть эффективна именно таргетная терапия.
При проведении паллиативной терапии применяют следующие методики:
- Бужирование, то есть расширение пищевода.
- Установку стентов эндоскопическим методом. Стенты – это полые цилиндры, которые устанавливаются в просвет пищевода, чтобы обеспечить проходимость пищи.
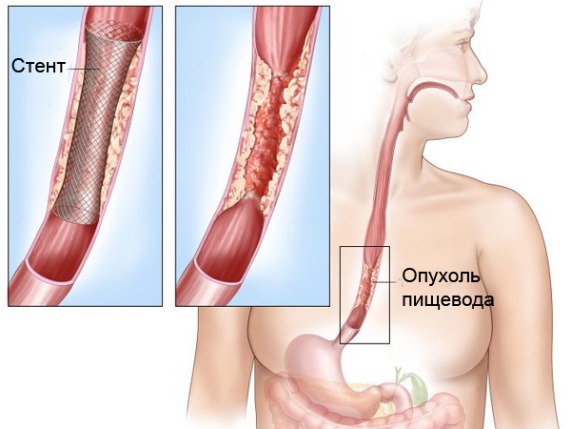
Стентирование рака пищевода
Лечение рака пищевода изменяется в зависимости от стадии
Обычно применяются эндоскопические методики лечения:
- PDT, или фотодинамическая терапия;
- RFA, то есть радиочастотная абляция;
- EMR, эндоскопическое удаление опухоли слизистой оболочки (после этого обеспечивается длительное наблюдение с применением эндоскопии, чтобы вовремя заметить рецидив, если он возникнет).
Новообразование затрагивает мышечную или собственную пластинку слизистой, но не поражает другие органы и лимфоузлы.
- Рак T1. Заболевание на ранней стадии, когда оно находится только в небольшой зоне слизистой и не достигло подслизистой основы (новообразования Т1а), может быть удалено путем эндоскопической резекции в рамках слизистой или подслизистого слоя. Иногда медики рекомендуют хирургически удалить часть пищевода, а затем провести облучение и химиотерапию.
- Рак Т2. Опухоль затрагивает мышечную пластинку слизистой. Таким пациентам перед операцией проводятся химиотерапия и облучение. Исключительно хирургическое удаление рекомендовано, только когда новообразование менее 2 см в размере.
Когда рак локализуется в зоне шеи, вместо операции в качестве основного метода лечения могут быть рекомендованы облучение и химиотерапия.
На второй стадии опухоль распространяется на главный мышечный слой пищевода либо его наружную оболочку. Также новообразование поражает 1 или 2 расположенных рядом лимфоузла.
При третьей стадии новообразование прорастает на наружную оболочку пищевода, может распространяться на соседние органы, им поражены регионарные лимфоузлы. Рекомендовано комбинированное лечение, которое включает операцию и предваряющие ее химиотерапию либо химиотерапию в сочетании с облучением. Если по состоянию здоровья для пациента есть риск не пережить операцию, то химиотерапия в сочетании с облучением становится основным методом лечения.
Рак затрагивает отдаленные лимфоузлы, есть метастазы в отдаленных органах (легких, печени). На такой стадии основная цель лечения – как можно более долгий контроль над распространением и размером новообразования. Пациентам проводится симптоматическое лечение для облегчения боли, восстановления возможности питаться и др. Применяется лучевая терапия и химиотерапия.
Профилактика
Чтобы предупредить такое заболевание, нужно исключить алкоголь и курение, контролировать массу тела. Если у человека присутствует повышенный риск развития этого типа рака (это такие патологии, как пищевод Барретта, ахалазия кардии, стриктуры пищевода, хронические эзофагит), то он должен регулярно обследоваться с обязательным применением эндоскопии.
Важно! Если рано диагностировать рак пищевода, то его можно вылечить с вероятностью от 85% до 100%.
Когда лечение рака завершено, нужно регулярно проходить контрольные обследования:
- После радикального лечения, сочетающего хирургию, химиотерапию и лучевую терапию: в первые 2 года – каждые 3-6 месяцев, в следующие 3-5 лет – каждые 6-12 месяцев, затем – каждый год.
- Тем, у кого был обнаружен ранний рак и кто подвергся эндоскопическому удалению слизистой: в первый год – каждые 3 месяца эндоскопическое обследование, во 2-й и 3-й годы – каждые полгода, затем – каждый год.


Авторская публикация:
Бекяшева Зоя Салаватовна
Ординатор хирургического отделения опухолей головы и шеи
НМИЦ онкологии им Н.Н. Петрова

Под научной редакцией:
Раджабова Замира Ахмедовна
Заведующий отделением опухолей головы и шеи, врач-онколог, научный сотрудник, доцент, кандидат наук
НМИЦ онкологии им. Н.Н. Петрова
Читайте также:

