Что такое комбинированное и комплексное лечение в онкологии
Методы лечения в онкологии:
г) комбинированный – хирургическое + лучевое / лекарственное лечение
д) комплексный – лучевое + лекарственное
е) сочетанный – два варианта одного метода (например, внутритканевая + наружная лучевая терапия)
2.5. Виды оперативных вмешательств в онкологии.
а) радикальные – см. вопрос 2.7
б) паллиативные – см. вопрос 2.6
в) косвенно действующие – см. вопрос 2.6.
г) циторедуктивные – направлены на уменьшение объема опухоли для улучшения условий последующего консервативного лечения. Бессмысленны, если в дальнейшем не планируется адъювантная терапия.
2.6. Паллиативные хирургические операции при раке. Косвенно действующие операции, их значение.
Паллиативные операции – выполняются для улучшения качества жизни по жизненным показаниям, у ослабленных больных с нерезектабельной опухолью, при осложненных формах рака (пример: гастростомия или гастроэнтероанастомоз).
Косвенно действующие операции – выполняются на эндокринных органах для увеличения эффективности последующей консервативной терапии (пример: сальпингоовариэктомия или орхиэпидидимэктомия).
2.7. Принципы радикальных хирургических операций в онкологии, их отличие от операций при неонкологической патологии.
Радикальные операции предполагают полное удаление всех очагов опухолевого роста.
Принципы радикальных операций в онкологии:
- соблюдение абластики (хирургической профилактики рецидивов и метастазирования злокачественной опухоли) и антибластики (совокупности хирургических мероприятий по очищению раны от раковых клеток)
- опухоль удаляется в пределах здоровой ткани вместе с органом или его частью в едином блоке с регионарными л.у.
- орган вместе с опухолью удаляется в пределах закрытого тканевого футляра; футляр выделяется послойно; все сосуды и нервы обрабатываются экстрафутлярно.
Для всех онкологических операций в отличие от неонкологических характерны радикализм и соблюдение принципов абластики и антибластики.
2.8. Принципы комбинированного лечения. Комплексное лечение при опухолях.
Комбинированное лечение предполагает использование обязательно оперативного лечения вместе с лучевой терапией или химиотерапией. Комплексное лечение – применение химиотерапии и лучевого лечения.
Лучевая терапия и химиотерапия в составе комбинированного лечения могут быть:
а) неоадъювантными (предоперационными) – при местно-распространенном процессе дает возможность значительно уменьшить размеры первичной опухоли и регионарных метастазов, достич операбельности; рано воздействовать на возможные отдаленные метастазы; выявить опухоли, не чувствительные к данному режиму химиотерапии и таким образом определить более рациональное послеоперационное лечение
б) адъювантными (послеоперационными) – комплекс дополнительных лечебных мероприятий, направленных на уничтожение скрытых микрометастазов после хирургического удаления первичной опухоли; ее цель – улучшение безрецидивной и общей выживаемости.
Комбинированное – использование двух принципиально разных методов лечения (например, оперативного и лучевого; оперативного и химиотерапии; лучевой терапии и химиотерапии).
Комплексное лечение – представляет использование всех трех методов лечения (лучевое, хирургическое, химиотерапия).
Методы лучевой терапии:
· Самостоятельный метод лучевой терапии предусматривает полное разрушение опухоли.
· Предоперационная лучевая терапия направлена на полное повреждение наиболее злокачественных пролиферирующих опухолевых клеток.
· Послеоперационная лучевая терапия рассматривается как средство “стерилизации” операционного поля и влияния на зоны возможного субклинического распространения опухоли, недосягаемые для хирургического вмешательства.
· Паллиативная лучевая терапия применяется с целью улучшения клинической ситуации в больного.
Химиотерапиязлокачественных опухолей предусматривает применение лечебных средств естественного или синтетического происхождения с целью необратимого повреждения пролиферации
При лечении одним химиопрепаратом, речь идет о монохимиотерапии. Однако, экспериментальные данные указывают на то, что разные химиопрепараты действуют на раковую клетку в разные фазы митотического цикла. На этом основана методика полихимиотерапии - одновременного применения нескольких препаратов за такими принципами:
Комбинированный метод лечения
Хирургическое удаление опухоли не всегда выключает возможность оставления опухолевых клеток, как в участке операционного поля, так и в ближайших и отдаленных местах организма, который и есть причиной рецидива заболевание. Оперативное удаление первичного очага возможно в основном на начальных стадиях заболевания. При значительном распространенные опухоли с втягиванием в процесс жизненно важных сопредельных органов провести операцию с соблюдением основных принципов абластики и антибластики практически невозможно. Лучевая терапия хотя и имеет самое широкое применение при лечении злокачественных опухолей, но лишь при незначительном количестве локализаций (рак кожи, губы, шейки матки) разрешает ликвидировать первичный опухолевый костер и в преобладающем количестве случаев дает лишь паллиативный эффект. Химиотерапию как самостоятельный метод лечения также применяют в ограниченных случаях. Именно поэтому в клинической практике онкологии комбинированное лечение злокачественных опухолей на современном этапе усиленно развивается и совершенствуется.
Симптоматичное лечение
Паллиативное, или симптоматичное лечение применяется в больных с запущенными формами рака (IV клиническая группа), которые не подлежат специальному лечению.
БИЛЕТ №26
9.Отдельные виды кровоизлияний и кровотечений. Спонтанная остановка кровотечений.
10.Виды обезболивания для проведения операции и подготовка к нему.
11.Синдром длительного раздавливания тканей (СДРТ). Первая помощь, клиника, лечение.
12.Хирургический метод в лечении опухолей. Принципы хирургического лечения, виды операций.
1)КРОВОИЗЛИЯНИЕ — попадание в полости и ткани тела жидкой либо свернувшейся крови вследствие нарушения герметичности сосудов (или вследствие увеличения проницаемости стенки сосуда).
Виды кровоизлияний:
·Гематома — жидкая, либо свернувшаяся кровь, находящаяся в тканях организма с образованием некоторой полости
·Петихии — проникшие сквозь утонченную стенку капилляра эритроциты, образующие небольшие (1-2мм) геморрагические пятна или точечные кровоизлияния в слизистые оболочки. Отличительная особенность данного вида кровоизлияний — не имеют выпуклости и не выделяются на ощупь.
·Экхимозы — проникшие сквозь утонченную стенку капилляра эритроциты, образующие крупные (крупнее 3мм) геморрагические пятна на кожном покрове. Более привычное название — синяк. Отличительная особенность этого вида кровоизлияний — не имеют выпуклости и не пальпируются.
·Кровотече́ние —выход кровиза пределы сосудистого русла или сердца в окружающую среду (наружное кровотечение), в полость тела или просвет полого органа (внутреннее кровотечение).
Классификация кровотечений
По направлению тока крови
Наружное
Кровотечение называют наружным, если кровь изливается во внешнюю среду непосредственно из раны или через естественные отверстия тела. Наружное кровотечение, в свою очередь, подразделяется на скрытое и явное.
Внутреннее
При внутреннем кровотечении кровь скапливается в полостях тела, не сообщающихся с окружающей средой.
Скрытое кровотечение — кровотечение в полости организма, сообщающиеся с внешней средой — желудочное кровотечение, кровотечение из стенки кишечника, лёгочное кровотечение, кровотечение в полость мочевого пузыря и т. д.
Явное кровотечение - кровотечение, которое легко определяется при осмотре.
По повреждённому сосуду
Кровотечение поверхностное, кровь по цвету близка к артериальной, выглядит как насыщенно-красная жидкость. Кровь вытекает в небольшом объёме, медленно.
Венозное кровотечение характеризуется тем, что из раны струится тёмная по цвету венозная кровь.
Артериальное кровотечение легко распознается по пульсирующей струе ярко-красной крови, которая вытекает очень быстро.
Наблюдается при ранениях паренхиматозных органов (печень, поджелудочная железа, лёгкие, почки, селезенка), губчатого вещества костей и пещеристой ткани. При этом кровоточит вся раневая поверхность. В паренхиматозных органах и пещеристой ткани перерезанные сосуды не сокращаются, не уходят в глубину ткани и не сдавливаются самой тканью. Кровотечение бывает очень обильным и нередко опасным для жизни. Остановить такое кровотечение очень трудно.
Возникает при одновременном ранении артерий и вен, чаще всего при повреждении паренхиматозных органов (печень, селезёнка, почки, лёгкие), имеющих развитую сеть артериальных и венозных сосудов. А также при глубоких проникающих ранениях грудной и/или брюшной полости.
По происхождению
Травматическое кровотечение возникает в результате травмирующего воздействия на органы и ткани, превышающего их прочностные характеристики.
Патологическое кровотечение является следствием патофизиологических процессов, протекающих в организме больного. Причиной его может являться нарушение работы любого из компонентов сердечно сосудистой и свертывающей системы крови.
По степени тяжести
10—15 % (ОЦК), до 500 мл,
15—20 % ОЦК, от 500 до 1000 мл,
20—30 % ОЦК, от 1000 до 1500 мл,
>30 % ОЦК, более 1500 мл
>50—60 % ОЦК, более 2500—3000 мл
>60 % ОЦК, более 3000—3500 мл
По времени
·Первичное — кровотечение возникает непосредственно после повреждения сосудов (капилляров) .
·Вторичное раннее — возникает вскоре после окончательной остановки кровотечения, чаще в результате отсутствия контроля за гемостазом во время операции.
·Вторичное позднее — возникает в результате деструкции кровеносной стенки. Кровотечение плохо поддается остановке более 5 суто
Спонтанный гемостазв ряде случаев позволяет организму справиться с кровотечением самостоятельно.
Гемостаз - сложный биохимический и биофизический процесс, в котором участвуют кровеносный сосуд и окружающие его ткани, тромбоциты и плазменные факторы свёртывающей и противосвёртывающей системы крови.
Сокращение гладкомышечных клеток сосуда приводит к вазоконстрикции, в зоне повреждения сосудов нарушенный эндотелий создаёт поверхность, место для образования тромба. Изменение гемодинамики, замедление кровотока делают возможным процесс тромбообразования, а тромбопластин повреждённого сосуда и окружающих тканей (тканевой тромбопластин) принимает участие в процессе свёртывания крови. Изменение электрического потенциала повреждённого сосуда, обнажение коллагена, накопление активных биохимических веществ (гликопротеидов, фактора фон Виллебранда, ионов кальция, тромбоспандина и др.) обеспечивают адгезию (прилипание) тромбоцитов к об- нажённому коллагену стенки сосуда. Прилипшие тромбоциты создают условия для агрегации тромбоцитов - сложного биохимического процесса с участием эпинефрина, АДФ, тромбина с образованием арахидоновой кислоты, простагландинов, тромбоксана и других веществ. Агрегированные тромбоциты вместе с тромбином и фибрином образуют тромбоцитарный сгусток - поверхность для последующего тромбообразования с участием свёртывающей системы крови.
В 1-ю фазу свёртывание происходит с участием плазменных факторов (VIII, IX, XI, XII фактора Хагемана) и тромбоцитов крови - образуется кровяной тромбопластин. Последний вместе с тканевым тромбопластином в присутствии ионов Са2+ переводит протромбин в тромбин (2-я фаза свёртывания), а тромбин в присутствии XIII фактора переводит фибриноген в фибрин-полимер (3-я фаза). Процесс образования сгустка заканчивается ретракцией последнего с формированием тромба. Тем самым обеспечивается гемостаз, и кровотечение из мелких сосудов надёжно останавливается. Весь процесс тромбообразования происходит очень быстро - в течение 3-5 мин, а такие процессы, как адгезия тромбоцитов, переход протромбина в тромбин, образование фибрина, занимают несколько секунд.
Продолжающееся кровотечение в случае, если организм не справился с ним самостоятельно, служит показанием для временной остановки кровотечения.
2)регионарная (меСТНая)
2.Местная инфильтрационная(блокада рецепторов и мелких нервов)
5.Проводниковая (блокада нервов U нервных сплетении)
-Эпидуральная (блокада на уровне корешков спинного мозга)
г)анестезия челюстной области
Общая
1. Внутривенный наркоз
2. Масочный наркоз (ингаляционная анестезия).
3. Эндотрахеальный наркоз (тотальная внутривенная анестезия с ИВЛ и миорелаксацией)
Анестезиолог осматривают больного перед операцией, при этом не только обращает внимание на основное заболевание, по поводу которого предстоит операция, но и подробно выясняет наличие сопутствующих заболеваний.
·Если больной оперируется в плановом порядке, то при необходимости проводят лечение сопутствующих заболеваний, санацию полости рта.
·Врач выясняет аллергологическийанамнез (все ли препараты и вещества переносятся больным).
·Уточняет, переносил ли больной в прошлом операции и наркозы.
·Обращает внимание на форму лица, грудной клетки, строение шеи, выраженность подкожной жировой клетчатки.
Все это необходимо, чтобы правильно выбрать метод обезболивания и наркотический препарат.
·Важным правилом подготовки больного к наркозу является очищение желудочно-кишечного тракта (промывание желудка,очистительные клизмы).
·Перед операцией больному проводят специальную медикаментозную подготовку — премедикацию:
- На ночь дают снотворное, больным с лабильной нервной системой за сутки до операции назначают транквилизаторы (седуксен, реланиум).
- За 40 мин до операции внутримышечновводят наркотические анальгетики и 0.5 мл 0,1% раствора атропина.
- Непосредственно перед операцией осматривают полость рта, удаляют съемные зубы и протезы.
3)Синдром длительного сдавления
Синдром длительного сдавления, или краш-синдром (англ., crash ^ авария, крушение), — своеобразное патологическое состояние, обус. ловлснное длительным (более 2—4 ч) и различным по интенсивности
сдавлением, преимущественно мягких тканей.
Особенность указанного синдрома заключается в том, что его проявления наступают сразу же после ликвидации воздействия механического фактора, т.е. после извлечения пострадавшего из-под обломков разрушенных зданий, из завалов и т.д. При этом развивается травматический токсикоз как следствие ишемии, венозного застоя, попадания в общий кровоток большого количества продуктов распада разрушенных тканей и освобождённых токсических метаболитов, болевого раздражения при сдавлении и травматизации нервных стволов. а также плазмопотери, возникающей в результате массивного отёка повреждённых мышечно-костных сегментов.
Патогенез синдрома складывается из:
- нервноболевого фактора (следствие длительного болевого раздражения);
- токсимии (следствие всасывания токсических продуктов из раздавленных, разможженых тканей);
- плазмопотери ( следствие массивного отека, поврежденных тканей, чаще конечностей)
Периоды по М.И.Кузину:
- Ранний (начальный, отека и сосудистой недостаточности);
- Промежуточный (острой почечной недостаточности);
Ранний
Признаки появляются в ближайшие часы после освобождения пораженного от завала.
В поврежденной части отмечается расстройства:
- исчезает пульсация периферических сосудов,
- наблюдается сгущение крови,
- появляется жажда, рвота.
Образуются пузыри с прозрачным или геморрагическим содержимым.
- Реакция мочи кислая, в ней появляется белок,
- Гиалиновые и пигментные цилиндры,
Промежуточный
Через 2-3 дня появляется:
- повышение температуры тела,
- снижение резервной щелочности крови,
- развивается картина острой азотемической уремии,
Поздний
Если функция почек постепенно восстанавливается,то с конца второй недели начинается поздний период.
-восстановлением движением суставов,
- появлением очагов некроза, в коже, мышцах.
- омертвление пальцев, сегментов конечностей,
- появляются посттравматические невриты, мышечные атрофии, контрактуры суставов.- обратным всасыванием жидкости из места отека поврежденной конечности,
Лечение
- Начальный
- тугое бинтование от периферии к центру до развития отека,
- наложение жгута у основания конечности при тяжелом раздавливании,
- комплексная противошоковая терапия,
- футлярные новокаиновые блокады, проксимальнее поражения,
- двухсторонняя паранефральная блокада,
- 5% р-р глюкозы с инсулином до 4-5 литров,
- 0,1% р-р новокаина (300-500 мл.)
- гемотрансфузии по показаниям.
Промежуточный
С нормализацией гемодинамики для уменьшения токсических явлений прибегают:
- к широкому и глубокому рассечению пораженных тканей,
- вскрытию фасциальных влагалищ,
- рыхлой тампонаде марлевыми салфетками с гипертоническим растворам NaCl, K Mg О4, Н2О2.
Инфузионные мероприятия проводимые в начальный период.
В позднем периоде применяют физиотерапевтические, общехирургические методы лечение ран, профилактику и лечение анкилозов, мышечной атрофии, невритов и прочих осложнений.
4)1. Лечение доброкачественных опухолей
Основным и, в подавляющем большинстве случаев, единственным способом лечения доброкачественных новообразований является хирургический. Лишь в лечении опухолей гормонозависимых органов вместо или вместе с хирургическим методом применяют гормональную терапию.
Показания к операции
Доброкачественные опухоли, не несущие угрозы для жизни пациента, не всегда должны быть обязательно удалены. Если у пациента длительное время существует доброкачественная опухоль, не причиняющая ему никакого вреда, и в то же время есть противопоказания к хирургическому лечению (тяжелые сопутствующие заболевания), то оперировать больного вряд ли целесообразно.
Показания:
1) Постоянная травматизация опухоли.
2) Нарушение функции органа.
3) До операции нет абсолютной уверенности в том, что опухоль не является злокачественной. В этих случаях операция кроме лечебной функции выполняет еще и роль эксцизионной биопсии.
4) Косметические дефекты. (опухоли на лице и шее).
Последнее изменение этой страницы: 2019-04-27; Нарушение авторского права страницы
Под комплексным лечением понимают вид терапии, в который входят два или несколько разнородных воздействий на опухолевый процесс, но при этом обязателен хотя бы один метод лечения, направленный на уничтожение опухолевых клеток, циркулирующих в кровяном русле или осевших в тканях за пределами местно-регионарной зоны поражения. Метод предусматривает комбинацию хирургического и/или лучевого лечения с химио-, гормоно- и иммунотерапией. Речь идет, таким образом, о проведении в той или иной последовательности различных мероприятий, характеризующихся неодинаковым влиянием на опухоль и организм и направленных как на местно-регионарный процесс, так и на весь организм в целом.
Сюда относятся, например:
- предоперационное лучевое лечение + хирургическое лечение + химиотерапия;
- предоперационное химиолучевое лечение + хирургическое лечение + химиотерапия;
- хирургическое лечение + лучевая терапия + гормонотерапия;
- химиотерапия + хирургическое лечение;
- хирургическое лечение + химиотерапия или гормонотерапия;
- лучевое лечение + химиотерапия + гормонотерапия.
Таким образом, лекарственный, т.е. химиотерапевтический, элемент занимает в комплексном методе лечения одно из ведущих мест, причем, по мнению большинства исследователей, без него лечение не может быть названо комплексным. Химиотерапевтический, гормонотерапевтический и иммунотерапевтический компоненты используются как для воздействия на первичную опухоль, так и с целью подавления возможных субклинических рецидивов и метастазов.
Химиотерапия, проводимая в рамках комплексного лечения, в частности после операции, с целью подавления возможных субклинических очагов опухолевого роста, опухолевых клеток и их комплексов в зоне операционного вмешательства, а также в кровеносном русле, называется адъювантной, профилактической, вспомогательной. По определению ее следует отличать от химиотерапии, применяемой с лечебной целью в качестве самостоятельного или дополнительного воздействия на первичную, рецидивную опухоль и выявленные метастазы; такое лечение чаще всего носит паллиативный характер.
Адъювантная химиотерапия находится в стадии интенсивного изучения, но остается пока еще на уровне клинического эксперимента. Для некоторых нозологических форм опухолей (например, остеогенная саркома, саркома Юинга, злокачественные опухоли яичка, нефробластома, некоторые формы меланомы и др.) целесообразность проведения адъювантной химиотерапии уже не вызывает сомнений. Известные перспективы открываются по мере изучения и внедрения в клиническую практику методов химиоиммунотерапии.
В последнее десятилетие все большее внимание в рамках комплексного лечения придается предоперационной, или неоадъювантной, индукционной химиотерапии.
Основной целью лечебной стратегии при использовании этого метода обобщенно являются:
- уменьшение размеров опухоли;
- снижение агрессивности опухоли на определенный период.
Далее предпринимаются хирургическая операция и последующие противоопухолевые мероприятия. В результате расширяются показания к выполнению хирургических вмешательств. Неоадъювантная химиотерапия — новый вариант лечения, требующий еще всестороннего углубленного изучения при различных нозологических формах злокачественных новообразований. Он может оказаться весьма перспективным при лечении рака молочной железы, сарком мягких тканей, сарком костей, забрюшинных злокачественных опухолей и др.
С этих позиций большой научный и практический интерес приобретает многокомпонентное лечение как направление, включающее, наряду с традиционными, классическими, видами терапии злокачественных опухолей, новые методы, целесообразность которых обоснована и уже подтверждена клинической практикой. Использование этого термина на современном этапе развития онкологии представляется весьма рациональным прежде всего с позиций общей ориентировки врача среди многочисленных методик лечения и упорядочения терминологической путаницы, отражающейся на качестве оценки результатов.
С развитием науки клинические онкологи все больше узнают о процессах формирования злокачественных новообразований. Понимание клеточных, молекулярных и генных механизмов дает возможность разрабатывать новые средства борьбы с опухолями. Несмотря на то, что сражение идет с переменным успехом, врачам удается отвоевать больше жизней, чем раньше.
Классическая триада лечения онкологии (хирургия, лучевая и химиотерапия) пополняются новыми, направленными на опухоль и более щадящими для организма, методами. К традиционным способам терапии формируются обновленные подходы.
Лечение онкологии в зависимости от стадии заболевания

Для классификации опухолевого процесса используют различные показатели, такие как структурные и анатомические особенности, размеры и скорость роста, локализацию и риск метастазирования.
Всего выделяют пять стадий развития онкозаболеваний. В зависимости от того, на какой стадии выявлено заболевание и начато лечение, составляется план лечебных мероприятий, а также определяется прогноз.
Чем в более ранней стадии начато лечение онкологии, тем выше шансы на полное выздоровление и тем менее агрессивной и масштабной будет терапия.
0 стадия — опухоли любой локализации. Границы очага не выходят за границу эпителиального слоя клеток, из которых произошла опухоль. Такой рак при своевременном адекватном лечении можно полностью вылечить.
I стадия — рак распространяется в границах органа. Если такую опухоль вовремя выявить и удалить, то прогноз в целом благоприятный.
II стадия — практически все опухоли на этой стадии в границах органа, но с большим проникновением вглубь или больших размеров. Здесь уже прогноз зависит от вида опухоли и ее расположения.
III стадия — опухоль и дальше прогрессирует, дает метастазы в регионарные лимфоузлы, но отдаленных метастазов, как правило, еще нет. Это может дать надежду на продление жизни. Но общий прогноз зависит от целого ряда факторов: типа опухоли, ее анатомических особенностей, нарушений функции соседних органов, сопутствующих заболеваний и общего состояния пациента.
IV стадия — распространенная. Первичные очаги большого размера, часто прорастающие в соседние органы, нарушение кровоснабжения, поражение регионарных и отдаленных лимфоузлов, общая интоксикация. Для облегчения состояния проводится паллиативное и симптоматическое лечение.
Лечение рака с помощью оперативного вмешательства: от радикальных операций к органосохраняющим
Хирургические вмешательства по-прежнему остаются стандартом лечения рака с вполне удовлетворительными результатами. В этой области онкологи достигли большого мастерства.
Операции при лечении опухолевых заболеваний могут быть:
- Радикальными. Предусматривается полное удаление первичного новообразования и его метастазов. После такого вмешательства в организме не остается очагов опухоли, которые можно определить каким-либо диагностическим методом.
- Паллиативными. После такого хирургического лечения в организме могут оставаться опухолевые очаги. Основная задача — предотвратить тяжелые осложнения, связанные с ростом опухоли (кровотечения, сдавливания соседних органов и сосудов, резкое сужение просвета или уменьшение полости органа).
Последние достижения хирургической (в т.ч. роботизированной) техники позволяют расширить количество органосохраняющих операций, число вмешательств, которые выполняются в один этап, уменьшить послеоперационные осложнения и сократить реабилитационный период.
Кроме того, в настоящее время до 54,3% увеличилось число случаев лечения рака, когда хирургический способ использовался как самостоятельный. Особенно эффективен он при раке почки, меланоме кожи, раке щитовидной железы.
В комбинации с другими методами в РФ оперативное лечение опухолей проводится в 85% случаев. Это говорит о том, что хирургия лидирует в лечении злокачественных новообразований. Намного чаще стали использоваться эндоскопические, в том числе лапароскопические методы, которые меньше травмируют ткани, окружающие опухоль, и дают возможность сохранить орган. Конечно, специалисты, в первую очередь, оценивают индивидуальную клиническую ситуацию, стадию, распространенность и тип рака, состояние пациента. И только потом коллегиально (на онкоконсилиуме) принимают решение в пользу открытой операции или эндоскопического вмешательства.
Также доказано, что результат лечения при меланоме кожи мало зависит от того, насколько широко иссекли ткани в районе опухоли, то есть достаточно отступить всего на 1–2 см (а не до 15 см, как было принято ранее).
Изменилось отношение и к лечению рака молочной железы — от радикальной мастэктомии (полного удаления вместе с группой лимфоузлов) до органосохраняющей операции и одномоментной пластики.
Используются инструменты (например, электронож), которые помогают более строго следовать таким принципам хирургического лечения, как
- Абластика — резекция (иссечение) пораженного органа в пределах здоровых тканей для уменьшения риска распространений опухолевых клеток по кровеносным сосудам.
- Антибластика — уничтожение раковых клеток, которые остались в зоне оперативного вмешательства с помощью промывания специальными растворами или облучения.
Хотите мы вам перезвоним?
Лучевая терапия в лечении онкологии
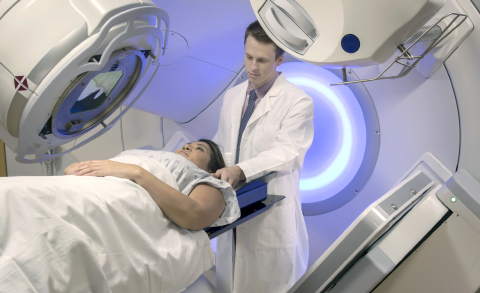
Лучевая терапия в составе комплексной или комбинированной применяется сейчас в 60–70% случаев онкозаболеваний и приводит к выздоровлению у половины пациентов. Методы постоянно совершенствуются, чтобы при минимальном воздействии на здоровые ткани достичь наибольшего результата по удалению опухоли.
Для лучевой терапии используют ионизирующее излучение. Оно может отличаться по механизму биологического действия, проникающей способности и распределению энергии. В клинической практике чаще других применяют фотонное излучение, к которому относится:
- Гамма-излучение — излучение от радионуклидов, проникающее на глубину до 1 м и больше.
- Рентгеновское (с помощью рентген-аппаратов) — излучение вследствие перехода электронов в ядре с орбиты на орбиту.
- Тормозное излучение — получают с помощью протонных ускорителей.
Также используется корпускулярное излучение (от ядерных частиц). Виды: бета-излучение, позитронное излучение, альфа-частицы.
Основные источники ионизирующего излучения — это естественные и искусственные радионуклиды (радиоактивные вещества) и специальные аппараты — ускорители, генераторы нейтронов, рентгеновские аппараты.
Возможно дистанционное, контактное и внутреннее облучение, при котором радионуклиды вводятся внутривенно или через рот.
При дистанционной лучевой терапии источник излучения (в основном фотонного) удален от опухоли на 80–100 см. При контактном облучении, которое называется брахитерапия, источник находится на близком расстоянии, до 30 см, от опухолевого очага или в непосредственном контакте. Это более щадящий вид терапии. Основные виды контактного облучения: внутриполостное, внутритканевое, аппликационное (на поверхности тела).
Под действием ионизирующего излучения образуются свободные радикалы, которые повреждают клетки, также нарушается воспроизведение ДНК и деление клеток, что приводит к уничтожению опухоли. При этом есть мгновенное действие и отсроченное.
В сочетании с хирургическими методами лечения рака применяется:
- предоперационная — для понижения жизнеспособности клеток опухоли перед операцией;
- интраоперационная — облучение зоны опухоли во время операции для предупреждения развития рецидивов и метастазов;
- послеоперационная лучевая терапия — для предупреждения метастазов после нерадикального удаления опухоли.
Для того чтобы общая реакция организма на лучевую терапию была менее выраженной, современные методики дополняются способами визуализации опухоли, в том числе 3D, а также фиксирующими приспособлениями. Это помогает наиболее точно воздействовать на опухоль.
Лучевая терапия хорошо сочетается и с лекарственными методами лечения онкологии.
Химиотерапия
Химиотерапевтические методы лечения рака (и монотерапия, и комбинированное применение средств) связаны с действием лекарственных препаратов на опухолевые клетки в определенных фазах их развития.
В зависимости от места химиотерапии в лечении опухолевого заболевания выделяют:
- Адъювантную химиотерапию — дополнение к основному (хирургическому или лучевому) методу лечения. Назначают при высоком риске развития метастазов или рецидива — повторной опухоли, когда первичный очаг уже удален.
- Неадъювантную химиотерапию, которая проводится перед удалением опухоли хирургическим или другим путем. Цель — уменьшить объем образования, чтобы выполнить менее травматичную операцию, возможно, органосохраняющую.
- Первичную химиотерапию при неоперабельном раке или развитии множественных метастазов. Задача — продлить жизнь пациента с сохранением ее качества. Используются наименее токсичные препараты, удобные для введения.
При полихимиотерапии подбираются препараты с различным механизмом действия.
Возможна цитостатическая терапия, когда препарат замедляет развитие опухоли и цитотоксическая, если раковые клетки уничтожаются.
В зависимости от того, на каком этапе и каким образом химиопрепарат действует на клетку, его относят к той или иной группе:
- Алкилирующие агенты: хлорэтиламины, эфиры дисульфоновых кислот, производные нитрозметилмочевины, соединения платины, триазины. Действуют на клетки, которые активно делятся, независимо от фазы клеточного цикла. Механизм действия: повреждение ДНК атипичной клетки, мутация и гибель. Имеют широкий спектр активности, поэтому возможно их назначение для лечения любой чувствительной опухоли (рак молочной железы, бронхов, желудочно-кишечного тракта, головы, шеи и головного мозга). Их недостаток в высокой токсичности и для здоровых клеток. Особенно важно угнетение кроветворения, с которым очень тяжело справиться. Кроме того, эти препараты могут вызвать почечную недостаточность и другие нарушения в мочевыводящей системе.
- Антиметаболиты: антагонисты фолиевой кислоты, аналоги пиримидина, пурина, аденозина. По структуре схожи с веществами, которые участвуют в продукции ДНК и РНК, встраиваются в них и нарушают синтез нуклеотидов, в результате чего клетка гибнет. Особенно хорошо действуют на клетки, которые интенсивно делятся. Применяются для лечения злокачественных опухолей желудка и кишечника, молочной железы, костей и мягких тканей. Также угнетают кроветворение, приводят к поражению кишечника.
- Противоопухолевые антибиотики: доксиорубицин (с самым широким спектром), блеомицин, митомицин и другие. Активно действуют на клетки медленно растущих опухолей. Проявляют разнообразное действие — от нарушения воспроизведения ДНК до торможения активности определенных ферментов. Эффективны для лечения опухолей молочной железы, опорно-двигательного аппарата, лимфом. Токсичны в отношении кроветворения и сердечной мышцы.
- Антимитогенные: винкаалкалоиды, таксаны. Останавливают или нарушают митоз (деление) клеток, в результате чего наступает их гибель. Применяются для химиотерапии рака молочной железы и яичников, бронхолегочной системы. Из токсических реакций опасны нарушение кроветворения, неврологические расстройства, паралич кишечника, аллергические проявления.
- Ингибиторы ДНК-топоизомеразIиII: производные камптотецина, эпиподофиллотоксины. Механизм действия состоит в нарушении работы ферментов, которые участвуют в синтезе ДНК, что приводит к обрыву деления клеток и их разрушению. Эффективны для лечения рака толстого кишечника, рака легкого и яичников. Так же, как и другие цитостатики, угнетают кроветворение, могут вызвать сильную диарею.
Гормонотерапия при лечении онкологии
Одним из направлений химиотерапии является терапия гормонами, которую еще называют эндокринотерапия. Дело в том, что отдельные опухоли растут из-за гормональной стимуляции, поэтому удалив источник гормонов, можно остановить развитие злокачественного процесса. При этом такого воздействия можно добиться хирургическим путем (удаление органа, в котором синтезируются гормоны), с помощью лучевой терапии и введением лекарственных препаратов (гормонов и антигормонов).
Главная цель введения гормонов — это блокировка патологических сигналов.
- Антиэстрогены — блокируют эстрогеновые рецепторы. Используют в лечении гормонзависимого рака молочной железы.
- Ингибиторы ароматазы — снижают количество эстрогенов у пациенток в менопаузе.
- Кортикостероиды — разрушают клетки лимфоидных опухолей, а также назначаются для уменьшения токсического действия прочих цитостатиков на печень и другие органы (при тошноте и рвоте).
- Андрогены — подавляют деление раковых клеток при метастазах рака молочной железы.
- Антиандрогены — не дают андрогенам связываться с рецепторами тканей при раке предстательной железы.
- Агонисты LH-RH — угнетают синтез тестостерона и эстрогена.
- Прогестины — при раке эндометрия блокируют развитие опухолевых клеток.
Иммунотерапия
Один из самых прогрессивных методов лечения онкозаболеваний, который позволяет действовать на раковые клетки высокоспецифическими механизмами. Применяется в комбинации с другими способами терапии.
Иммунотерапия дает возможность организму сформировать иммунный ответ на опухоль, проявить цитотоксическое действие, а также повысить иммунную защиту.
Применяются следующие группы препаратов:
- Иммуномодуляторы (пассивная иммунотерапия): цитокины (интерфероны, интерлейкины), иммуноглобулины, вещества микробного происхождения — для коррекции иммунитета.
- Моноклональные антитела (активная иммунотерапия) — для воздействия на поверхностные антигены опухолевых клеток, которое приводит к гибели клеток.
Таргетная терапия
Это новый метод лечения онкологии и метастазов. Он призван действовать только на определенные мишени. Это могут быть рецепторы гормонов, гены, ферменты. Также происходит повреждение структур, которые питают опухоль, или выключение внутриклеточных обменных процессов за счет нарушений в цепочке биохимических реакций.
В настоящее время применяется для лечения устойчивых к терапии видов рака, может значительно повысить эффект от лечения в сочетании с химиотерапией. С препаратами для таргетной терапии возможно лечение даже запущенных стадий.
Доказана эффективность для лечения рака молочной железы, рака легкого, меланомы и других.
Под контролем онкологов проходит не только терапия опухоли, но и лечение сопутствующих заболеваний, профилактика и уменьшение побочных эффектов, а также полный курс реабилитационных мероприятий.
Читайте также:

