Что такое адъювантная терапия при раке молочной железы
Эстрогеновые рецепторы (ЭР) — это белки, обнаруженные как в злокачественных, так и доброкачественных гормонально-зависимых тканях. Количество рецепторов, представленных в препарате опухоли молочной железы, позволяет предсказать успех или неудачу гормональной терапии.
Определение эстрогеновых рецепторов (ЭР) в некоторых видах рака молочной железы (РМЖ) человека и последующее объяснение роли эстрогенов в росте опухоли прояснили это клиническое взаимоотношение. В 1896 г. Beatson вызвал регресс рака молочной железы (РМЖ) овариэктомией.
В 1952 г. Huggins и Bergenstal продемонстрировали, что некоторые злокачественные новообразования молочной железы и простаты не были автономными, а частично контролировались эндокринной системой. Регрессии рака молочной железы (РМЖ) неоднократно удавалось добиться путем удаления источника эндогенных гормонов в результате овариэктомии, адреналэктомии и гипофизэктомии.
Регрессия рака молочной железы (РМЖ) достигалась также назначением больших доз эстрогенов, андрогенов, прогестерона и кортикостероидов.
Выбор конкретной гормональной терапии был в значительной степени эмпирическим и определялся такими клиническими особенностями, как наступление менопаузы, длительность безрецидивного промежутка, локализация основного очага, ответ на предшествующую терапию.
Базовые исследования метаболизма стероидных гормонов, проведенные Jensen, Smith и DeSombre, привели к появлению серий анализов, которые могут определить с относительной точностью, что злокачественные опухоли молочной железы не автономные и реагируют на эндокринные воздействия.
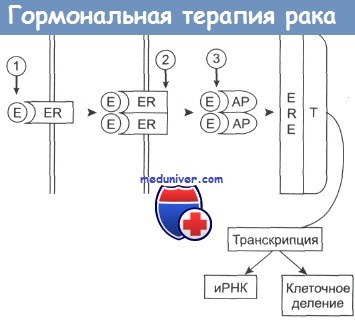
Эстроген (Е) связывается с рецептором (ER), который димеризуется.
Комплекс приобретает активность (АР) и присоединяется к эстроген-зависимым структурам (ERE) клеточного ядра.
Происходит активация таких белков, участвующих в транскрипции (Т), как РНК-полимераза II, что приводит к синтезу белка и делению клетки.
Гозерелин вызывает снижение уровня эстрогенов в плазме крови (1); фульвестран (2) предотвращает процесс димеризации рецептора и его активацию; тамоксифен (3) связывается с активным комплексом, подавляя его способность инициировать транскрипцию.
Такой метод предварительного прогнозирования реакции опухолей на изменения в эндокринной среде значительно увеличивает пользу гормональной терапии и позволяет рекомендовать такие виды лечения.
Сведения о содержании эстрогеновых рецепторов (ЭР) как в первичном, так и рецидивирующем раке молочной железы (РМЖ) должны рассматриваться с клинической точки зрения.
Необоснованным представляется возражение против этого на основании только того, что некоторые пациентки со значительным содержанием эстрогеновых рецепторов (ЭР) не отвечают на гормональную терапию (из-за возможного пренебрежения ролью гормональной регуляции или по причине неполного понимания роли других рецепторов стероидных или белковых гормонов).
Знание о содержании эстрогеновых рецепторов (ЭР) в первичной или метастатической опухоли не помогает врачу прогнозировать гормональную зависимость опухоли с достаточной точностью для рационального выбора паллиативного лечения. Однако это позволяет оценить возможные преимущества гормональной терапии для больных раком молочной железы (РМЖ).
Национальная всеобщая онкологическая сеть США (NCCN) в ноябре 2000 г. впервые опубликовала результаты сравнительного изучения адъювантной терапии рака молочной железы (РМЖ) на ранних стадиях. С тех пор проводились его уточнения.
Наиболее значительные изменения в руководствах 2005 г. в отношении адъювантной терапии рака молочной железы (РМЖ) касались включения HER-2 (рецептор эпидермального фактора роста, протоонкоген) как параметра для выбора лечебной тактики и рекомендации по применению трастузумаба для адъювантной терапии. Использование трастузумаба было предложено для больных с гиперэкспрессией HER-2 или с показателем флюоресцентной гибридизации in situ 2,1 и более при размере опухоли более 1 см.
II РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
АДЪЮВАНТНАЯ ТЕРАПИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ: ГИПОТЕЗЫ И ПРАКТИКА.
Тюляндин С.А.
Онкологический научный центр им.Н.Н.Блохина РАМН, Москва
Важнейшим этапом лечения раннего рака молочной железы является адъювантная терапия. Системная терапия с использованием цитостатиков или гормональных препаратов после хирургического удаления опухоли способна увеличивать как безрецидивную, так и общую выживаемость больных. Рандомизированные исследования, проведенные в Европе и США в конце 70-х годов, убедительно показали, что химиотерапия улучшает прогноз больных пременопаузального возраста с наличием метастазов в региональные лимфоузлы(1;2). Впоследствии назначение тамоксифена продемонстрировало улучшение отдаленных результатов лечения по сравнению с контролем в группе больных пожилого возраста(3;4). Эти результаты стимулировали поиск оптимальных режимов проведения системной терапии и определение показаний к ее проведению в зависимости от факторов прогноза(5). До недавнего времени адъювантная химиотерапия была зарезервирована для больных с метастазами в подмышечных лимфоузлах с сохранной менструальной функцией. Исследованиями последних лет значительно расширены показания к проведению химиотерапии.
Адъювантная химиотерапия у постменопаузальных больных с метастазами в подмышечные лимфоузлы.
Считалось, что для больных в постменопаузе с метастазами в подмышечные лимфоузлы и наличием рецепторов эстрогенов в опухоли препаратом выбора является тамоксифен. В исследовании Fisher et al. больным старше 50 лет с наличием положительных рецепторов назначали либо тамоксифен в течение 5 лет, либо 4 курса химиотерапии комбинацией доксорубицин и циклофосфан с последующим приемом тамоксифена в течение 5 лет(6). Сочетание химиотерапии и тамоксифена достоверно увеличило продолжительность безрецидивной и общей выживаемости. В исследовании Albain et al.(7) больным в постменопаузе с положительными рецепторами проводилось лечение тамоксифеном на продолжении оставшейся жизни или 4 курса химиотерапии СAF с последующим назначением тамоксифена или одновременный прием тамоксифена и проведение 4 курсов СAF. В настоящее время известны лишь предварительные данные, где группы химиотерапии и тамоксифена были объединены для сравнения с приемом одного тамоксифена. Показано, что больные, получавшие химиогормональное лечение, имели достоверно большую безрецидивную выживаемость, сведения о продолжительности жизни не были представлены.
Результаты мета-анализа показали, что проведение химиотерапии больным старше 50 лет с метастазами в подмышечные лимфоузлы достоверно увеличивает 5-летнюю безрецидивную выживаемость на 5,4% (с 38% в группе без химиотерапии до 43,4% в группе химиотерапии) и на 2,3% 5-ти летнюю общую выживаемость (с 46,3% до 48,6% соответственно)(8). Таким образом, накапливается все больше данных о целесообразности проведения адъювантной химиотерапии больным в постменопаузе с наличием метастазов в лимфоузлах. Это является терапией выбора у больных с отрицательными рецепторами к эстрогену и прогестерону в опухоли. Однако, и при положительных рецепторах проведение химиотерапии, в первую очередь с включением антрациклинов, с последующим назначением тамоксифена улучшает результаты лечения. Вероятно, назначение тамоксифена можно считать достаточным для проведения адъювантной терапии у больных с высоким содержанием рецепторов эстрогенов или прогестерона (>50 фмоль/мг белка). Проведение адъювантной терапии тамоксифеном показано также у больных старше 70 лет.
Адъювантная химиотерапия у больных с отсутствием метастазов в подмышечных лимфоузлах.
Ранее у больных с отсутствием метастазов в подмышечные лимфоузлы адъювантная химиотерапия не проводилась. В настоящее время в литературе опубликовано несколько важнейших рандомизированных исследований, результаты которых послужили основанием для рекомендаций по лечению больных с отсутствием метастазов в регионарных лимфоузлах. В исследовании NSABP B-209 , в которое включено около 3000 больных с отсутствием метастазов в регионарных лимфоузлах и положительными гормональными рецепторами, назначали тамоксифен в течение 5 лет, комбинированную химиотерапию в составе метотрексата и 5-фторурацила в течение 6 месяцев с последующим назначением тамоксифена в течение 5 лет или 6 курсов СMF с последующим приемом тамоксифена в течение 5 лет. Если объединить две химиотерапевтические группы, то проведение химиотерапии достоверно увеличило безрецидивную (p 2 в/в и циклофосфан 600 мг/м 2 в/в однократно каждые 3 недели 4 курса). В третьей группе больные сначала получали 4 курса АС, а затем спустя 6 месяцев 4 курса СMF с в/в введением циклофосфана. По данным 4-х летнего наблюдения отдаленные результаты лечения больных были одинаковыми во всех трех группах. Авторы сделали вывод о том, что реиндукция CMF не улучшает результаты лечения. Однако, несмотря на равнозначные результаты комбинаций AC и CMF, был сделан вывод о целесообразности использования АС. Во всех последующих исследованиях в качестве контрольной группы NSABP использовала назначение 4 курсов АС. Преимущество АС авторы видят в более короткой продолжительности терапии (АС заканчивается на 63 день от начала химиотерапии, а СМF - на 154 день). При проведении всего запланированного объема лечения АС (4 курса) само введение препаратов занимает 4 дня, в то время как при CMF (6 курсов) - 84 дня. Для купирования тошноты и рвоты при использовании АС противорвотные назначались в течение 12 дней, а при CMF в течение 84 дней. Добавьте сюда более редкую необходимость визитов к врачу при получении АС, и станет понятно, что как экономически, так и практически комбинация АС более оправдана, удобна и проста как для больных, так и для медперсонала. Более короткая продолжительность адъювантной терапии без потери эффективности приобретает особую актуальность в свете необходимости проведения лучевой терапии большинству больных в связи с выполнением органосохраняющей операции. В этом случае целесообразно начинать проведение лучевой терапии сразу после окончания адъювантной химиотерапии. Считается, что основное преимущество CMF перед комбинациями с включением антрациклинов - это отсутствие алопеции, которая крайне болезненно воспринимается большинством женщин. Исследование В-15 показало, что при назначении CMF у 71% пациенток наблюдалась алопеция, из них у 41% она носила выраженный характер (II и более степень по классификации ВОЗ).
По данным мета-анализа 11 рандомизированных исследований (около 7000 больных), сравнивавших эффективность CMF и антрациклин-содержащих комбинаций, последние уменьшают риск развития рецидива на 12 % и смерти на 11% по сравнению с CMF8 . Это приводит к улучшению 5-летней безрецидивной выживаемости на 3,2% (с 54,1% при CMF до 57,3% при использовании антрациклинов) и 5-летней общей выживаемости на 2,7% (с 68,8% до 71,5%). Большее число больных и длительный срок наблюдения позволят выявить, небольшую добавку за счет применения антрациклинов к безрецидивной и общей выживаемости больных раком молочной железы, а также четко определить риск возникновения сердечной недостаточности и острого миелоидного лейкоза, обусловленного антрациклинами.
Делаются попытки включения в режимы адъювантной химиотерапии и других активных при лечении рака молочной железы цитостатиков, таких как таксаны или винорельбин. В настоящее время известны предварительные данные большого рандомизированного исследования, в котором 3170 больным с наличием метастазов в подмышечные лимфоузлы (из них 62% в пременопаузе) получали химиотерапию с использованием комбинации АС. Контрольной группе проводили 4 курса АС каждые 3 недели, экспериментальной группе после этого назначали паклитаксел в дозе 175 мг/м 2 каждые 3 недели 4 курса. Анализ результатов после 18 месяцев наблюдения показал, что добавление паклитаксела достоверно уменьшает риск развития прогрессирования на 22% и смерти на 26% по сравнению с контрольной группой(15). Аналогичные исследования проводятся с использованием препарата доцетаксел.
Оптимальная стратегия проведения адъювантной терапии больным раком молочной железы постоянно совершенствуется. Многие нерешенные вопросы являются стимулом для планируемых многоцентровых рандомизированных исследований. Итогом недавно проведенных исследований стали более широкие показания к проведению адъювантной химиотерапии. Еще недавно химиотерапия была показана только больным в пременопаузе с метастазами в подмышечные лимфоузлы. В настоящее время только больным с низкой степенью риска при отсутствии метастазов в подмышечные лимфоузлы и больным старшей возрастной группы (старше 70 лет) с положительными рецепторами не показано проведение химиотерапии. Для всех остальных групп больных независимо от менструального и рецепторного статуса и состояния подмышечных лимфоузлов доказана целесообразность проведения химиотерапии.
С увеличением числа больных в рандомизированных исследованиях стало очевидно небольшое (не более 5% прибавки безрецидивной и общей выживаемости) преимущество антрациклин-содержащих комбинаций над CMF8;(10). Учитывая меньшую продолжительность терапии (4 однодневных курса каждые 4 недели), простоту введения и удобство для пациентов и медперсонала, становится понятным, почему комбинации с включением антрациклинов постепенно вытесняют CMF. При этом стало очевидным, что классический CMF с приемом циклофосфана per os обеспечивает лучшие результаты лечения, чем многочисленные его модификации с внутривенным введением(11). Подчеркивается важность проведения адъювантной химиотерапии с определенной интенсивностью. Уменьшение доз препаратов и/или интервалов между курсами ведет к неизбежной потере эффективности терапии.
Появились первые свидетельства целесообразности использования в качестве адъювантной химиотерапии новых противоопухолевых препаратов, зарекомендовавших себя при лечении больных с метастатическим процессом, например таксанов. Гормональная терапия тамоксифеном широко используется как самостоятельно, так и в комбинации с адъювантной химиотерапией. Оптимальной с точки зрения противоопухолевой эффективности и токсичности является ежедневная доза препарата 20-30 мг при продолжительности приема не менее 5 лет (14). Целесообразность более длительного приема препарата изучается в проводящихся в настоящее время исследованиях.
Остается открытым вопрос о роли выключения функции яичников у больных в пременопаузе с положительными рецепторами.
Можно надеяться, что в ближайшие годы онкологи получат в свои руки новые эффективные лекарственные препараты для лечения рака молочной железы, применение которых адъювантно предотвратит прогрессирование болезни и смерть у наибольшего числа больных.
Список литературы.
1. Bonadonna G, Brussamolino E, Valagussa P, et al. Combination chemotherapy as an adjuvant treatment in operable breast cancer. N.Engl.J.Med. 1976;294:405-410.
2. Fisher B, Carborne P, Economou SG, et al. L-phenylalanine mustard (L-PAM) in the management of primary breast cancer: a report of early findings. N.Engl.J.Med. 1975;292:117-122.
3. Carmichael J, Possinger K, Phillip P. Advanced Breast Cancer: A Phase II Trial With Gemcitabine. J.Clin.Oncol. 1995;13:2731-2736.
4. Nolvadex Adjuvant Trial Organization. Controlled trial of tamoxifen as a single adjuvant agent in the management of early breast cancer. Br.J.Cancer 1988;57:608-611.
5. Early Breast Cancer Trialists' Collaborative Group. Systemic treatment of early breast cancer by hormonal, cytotoxic or immune therapy: 133 randomized trials involving 31,000 re-currences and 24,000 deaths among 75,000 women. Lancet 1992;339:1-15-71-85.
6. Fisher B, Redmond C, Legault-Poisson S, et al. Postoperative chemotherapy and tamoxifen compared with tamoxifen alone in the treatment of positive-node breast cancer patients aged 50 years and older with tumor responsive to tamoxifen: results from the National Surgical Adjuvant Breast and Bowel Project B-16. J.Clin.Oncol. 1990;8:1005-1018.
7. Albain KS, Green S, Osborne K, et al. Tamoxifen versus cyclophosphamide, Adriamycin and 5-FU plus either concurrent or sequential tamoxifen in postmenopausal, receptor-positive, node-positive cancer: a Southwest Oncology Group phase III intergroup trial (SWOG-8814, INT-0100). Proc.ASCO 1997;16:128a.
8. Early Breast Cancer Trialists' Collaborative Group. Polychemotherapy for early breast cancer: an overview of the random trials. Lancet 1998;352:930-942.
9. Fisher B, Dignam J, DeCillis A, et al. The worth of chemotherapy and tamoxifen over tamoxifen alone in node negative patients with estrogen-receptor positive invasive cancer: first results from NSABP B-20. Proc.ASCO 1997;16:abstr.1a.
10. Hutchins L, Green S, Ravdin P, et al. CMF versus CAF with and without tamoxifen in high-risk node-negative breast cancer patients patients and a natural history follow-up study in low-risk node-negative patients: first results of Intergroup trial INT 0102. Proc.ASCO 1998;17:1a(Abstract).
11. Goldhirsch A, Coates AS, Colleoni M, et al. Adjuvant Chemoendocrine Therapy in Postmenopausal Breast Cancer: Cyclophosphamide, Methotrexate, and Fluorouracil. Dose and Schedule May Make a Difference. J.Clin.Oncol. 1998;16:1358-1362.
12. Misset J-L, di Palma M, Delgado M, et al. Adjuvant Treatment of Node-Positive Breast Cancer With Cyclophosphamide, Doxorubicin, Fluorouracil, and Vincristine Versus Cyclophosphamide, Methotrexate, and Fluorouracil: Final Report After a 16- Year Median follow-up Duration. J.Clin.Oncol. 1996;14:1136-1145.
13. Henderson IC, Berry D, Demetri G, et al. Improved disease-free and overall survival from the addition of sequential paclitaxel but not from escalation of doxorubicin dose level in the adjuvant chemotherapy of patients with node positive primary breast cancer. Proc.ASCO 1998;17:101a(Abstract).
14. Early Breast Cancer Trialists' Collaborative Group.Tamoxifen for early breast cancer: an overview of the randomized trials. Lancet 1989;351:1451-67.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Российский онкологический научный центр им. Н.Н. Блохина РАМН
Х имиотерапия и гормонотерапия играют существенную роль в комплексном лечении рака молочной железы практически при всех стадиях заболевания. Это объясняется особенностями данной опухоли – даже на ранних стадиях заболевания велик риск существования отдаленных микрометастазов, особенно при наличии факторов риска (поражении подмышечных лимфоузлов, отрицательных рецепторах эстрадиола и прогестерона, гиперэкспрессии Неr–2/neu и т.д.). Применение адъювантной химио– и гормонотерапии значительно улучшило результаты лечения операбельного рака молочной железы. При запущенном раке молочной железы химиотерапия и гормонотерапия являются основными методами лечения, позволяющими значительно продлить жизнь больного и улучшить ее качество. У 10–25% женщин с диссеминированным раком молочной железы возможно достижение полной регрессии опухоли с длительным безрецидивным периодом.
Адъювантная терапия
Адъювантная терапия рака молочной железы сегодня представляет собой систему стандартов, эффективность которых доказана в большом числе клинических исследований [1].
До настоящего времени остается четыре независимых прогностических фактора при резектабельном раке молочной железы: поражение регионарных лимфатических узлов, размер первичной опухоли, степень дифференцировки и содержание рецепторов к стероидным гормонам (к эстрогенам – РЭ и к прогестерону – РП).
Стандартами химиотерапии и эндокринной терапии являются: 4 цикла химиотерапии в режиме АЦ (адриамицин + циклофосфан) или АЦФ (адриамицин + циклофосфан + фторурацил) или 6 циклов химиотерапии по схеме ЦМФ (циклофосфан + метотрексат + фторурацил), а также тамоксифен 20 мг в день в течение 5 лет.
Первый фактор, положенный в основу назначения адъювантной терапии – поражение регионарных лимфатических узлов, разделяет всех больных на две группы.
Рак молочной железы без метастазов в регионарные лимфоузлы
Для назначения адъювантной терапии в этой группе необходимо определение групп повышенного риска. Граница для назначения адъювантной лекарственной терапии, что означает группу повышенного риска – снижение пятилетней выживаемости до 95% и менее (табл. 1).
Только в группе низкого риска пятилетняя выживаемость больных составляет более 95%. Во всех остальных группах проведение адъювантной лекарственной терапии улучшает результаты хирургического лечения.
Больным в пременопаузе с умеренным или высоким риском и положительным уровнем эстрогенных рецепторов показана химиотерапия с последующим назначением тамоксифена. При гормононезависимых опухолях показано назначение только химиотерапии.
Больным в постменопаузе с умеренным или высоким риском и положительным уровнем эстрогеновых рецепторов показан прием тамоксифена, а в группе высокого риска – комбинация химиотерапии с тамоксифеном. При отрицательном уровне рецепторов к эстрогенам показано применение только химиотерапии.
Всем пожилым больным (старше 70 лет) показан прием тамоксифена, а в группе высокого риска возможно дополнительное назначение химиотерапии. С уче– том возраста больных дополнительное назначение химиотерапии должно быть индивидуально обоснованным.
Рак молочной железы с метастазами в регионарные лимфоузлы
У всех больных раком молочной железы с метастазами в регионарные лимфатические узлы применение адъювантной лекарственной терапии улучшает результаты лечения.
При положительном уровне рецепторов к эстрогенам вне зависимости от менструальной функции показана комбинированная адъювантная терапия – химиотерапия и эндокринная терапия тамоксифеном.
При гормононезависимых опухолях показано применение только химиотерапии.
Всем пожилым больным (старше 70 лет) показан прием тамоксифена вне зависимости от уровня эстрогеновых рецепторов. Если уровень рецепторов к эстрогенам отрицательный, возможно дополнительное назначение химиотерапии. С учетом возраста больных дополнительное назначение химиотерапии должно быть индивидуальным.
При всей внешней простоте и схематичности назначения адъювантного лечения лишь методы, доказавшие свою эффективность в результате длительных клинических исследований, применяются для лечения больных. Оптимальная тактика адъювантной терапии постоянно совершенствуется. Совсем недавно химиотерапия рекомендовалась только больным в пременопаузе с метастазами в регионарные лимфатические узлы. В настоящее время только больным с низким риском и пожилым больным с положительными эстрогеновыми рецепторами не показано проведение химиотерапии.
При проведении адъювантной химиотерапии необходимо строго придерживаться оптимального режима (стандартных доз и интервалов между циклами). Неоправданные модификации режимов химиотерапии, несомненно, ухудшают результаты лечения.
Сегодня продолжаются исследования роли выключения функции яичников и рутинное применение данного метода адъювантного лечения нецелесообразно.
Появились данные об эффективности таксанов, как дополнительной химиотерапии к антрациклин–содержащим комбинациям у больных с неблагоприятным про– гнозом.
В связи с широкими исследованиями роли гиперэкспрессии рецептора Her2/neu наметились новые тенденции в оценке прогноза и лечения больных. Однако пока необходимо дополнительное число исследований для изменения практических рекомендаций.
Исследования по адъювантной терапии рака молочной железы интенсивно продолжаются, и можно надеяться, что в ближайшее время все больше и больше женщин будут излечиваться от рака молочной железы.
Неоадъювантная терапия
Неоадъювантная терапия – системное лечение, которое проводится до начала локального лечения (хирургического вмешательства или лучевой терапии).
Задачи неоадъювантной терапии:
- уменьшение размеров первичной опухоли и регионарных метастазов
- уменьшение объема оперативного вмешательства (радикальная резекция вместо радикальной мастэктомии)
- определение чувствительности опухоли к цитостатикам, выявление резистентных случаев с целью использования альтернативных режимов для адъювант– ной химиотерапии
- увеличение общей и безрецидивной выживаемости
- оценка новых режимов лечения по частоте полной клинической и морфологической ремиссии.
Стандартом неоадъювантной химиотерапии по результатам многоцентрового исследования NSABP B–18 признана схема АЦ, при применении которой объективный эффект составил 80%, полная морфологическая ремиссия отмечена у 15% больных.
Предполагалось, что раннее воздействие противоопухолевых лекарств на микрометастазы приведет к увеличению общей и безрецидивной выживаемости. Однако анализ 7 крупных рандомизированных исследований, в том числе NSABP B–18, включившего 1500 женщин с операбельным раком молочной железы, проведенный Wolff [2], не подтвердил эту гипотезу. Продолжительность жизни может быть увеличена только за счет рационального подхода к лечению – использования альтернативных режимов для адъювантной химиотерапии в случае низкой эффективности неоадъювантного лечения.
Продолжается поиск наиболее эффективного режима неоадъювантной химиотерапии. Особенно важным показателем является достижение полной морфологической регрессии опухоли, так как именно этот показатель статистически достоверно коррелирует с ростом общей выживаемости. С этой целью исследуются комбинации, включающие наиболее эффективные препараты, входящие в режимы неоадъювантной химиотерапии в последние годы – цисплатин, навельбин, таксаны. Некоторые авторы показали преимущество комбинаций антрациклинов и таксанов по сравнению со стандартным режимом АС. Разрабатываются новые режимы, включающие препараты, недавно вошедшие в практику химиотерапии, например, кселода и герцептин. Исследуются интенсивные режимы химиотерапии, однако пока не получено достоверных доказательств влияния интенсификации неоадъювантной химиотерапии на отдаленные результаты лечения.
Обсуждается количество курсов неоадъювантной химиотерапии. Признано, что эффект химиотерапии и частота полных регрессий опухоли зависят от количест– ва курсов лечения. Поэтому целесообразно проводить не менее 4 курсов, что безопасно для больных при условии регулярного контроля за динамикой заболевания.
У больных в менопаузе с положительными РЭ и/или РП применяется неоадъювантная гормонотерапия. Объективный эффект гормонотерапии достигает 50–70%. Для неоадъювантной гормонотерапии могут быть рекомендованы тамоксифен, анастразол, летрозол, экземестан.
Диссеминированный рак молочной железы
Для выбора метода лечения перед началом терапии необходимо оценить ряд прогностических факторов, определяющих возможный ответ заболевания на проводимое лечение. Длительный период, прошедший после лечения первичной опухоли до появления отдаленных метастазов, поражение только мягких тканей и костной системы или единичные отграниченные очаги в легких, медленный рост опухоли, удовлетворительное общее состояние больной, пожилой возраст и постменопауза, положительный уровень рецептов эстрадиола и/или прогестерона свидетельствуют о вероятно высокой чувствительности опухоли к гормонотерапии. В случае раннего появления отдаленных метастазов после лечения первичной опухоли, быстрого прогрессирования заболевания, молодого возраста больной, при множественных висцеральных метастазах, наличии лимфангоита кожи или легких лечение необходимо начинать с химиотерапии.
Эффективность гормонотерапии при положительном уровне РЭ и РП достигает 50–70%, снижается при положительных рецепторах одного вида (33%). При отрицательных РЭ и РП существует небольшой процент больных (5–10%), отвечающих на гормонотерапию. Традиционными препаратами, рекомендованными для первой линии гормонотерапии у больных в менопаузе, являются антиэстрогены – тамоксифен и торемифен. В настоящее время в I линии эндокринотерапии альтернативой тамоксифену являются антиароматазные препараты – анастрозол и летрозол. Во II линии эндокринотерапии больных раком молочной железы в менопаузе (при использовании тамоксифена в I линии) в настоящее время вместо прогестинов используются антиароматазные препараты (анастрозол, летрозол, экземестан). Применять прогестины во II линии гормонотерапии считается неэтичным.
У больных в пременопаузе гормонотерапию можно начинать с выключения функции яичников с помощью агониста гонадотропин–рилизинг гормона гипофиза – гозерелина (золадекса), а также хирургическим или лучевым методами.
Эффект гормонотерапии оценивается через 6–8 нед после начала лечения. Положительным ответом считается не только полная или частичная регрессия опухоли, но и длительная стабилизация заболевания (>=6 месяцев). Лечение продолжается до прогрессирования болезни. В случае быстрого прогрессирования болезни после гормонотерапии первой линии следует начать химиотерапию. При прогрессировании после длительного положительного эффекта на фоне первой линии гормонотерапии, а также кратковременной полной или частичной регрессии опухоли начинают гормонотерапию второй линии – ингибиторы (инактиваторы) ароматазы.
Третья линия гормонотерапии – прогестины – медроксипрогестерона ацетат (фарлутал, провера) и мегестрола ацетат (мегейс). Достаточно редко в наше время в III линии гормонотерапии используются андрогены и у женщин в постменопаузе – эстрогены.
Химиотерапия
Стандартами I линии химиотерапии рака молочной железы являются схемы: ЦМФ (циклофосфан 100 мг/м 2 внутрь ежедневно дни 1–14, метотрексат 40 мг/м 2 в/в дни 1,8, фторурацил 600 мг/м 2 в/в дни 1,8, интервал 4 нед), ЦАФ (циклофосфан 100 мг/м 2 внутрь ежедневно дни 1–14, доксорубицин 30 мг/м 2 в/в дни 1,8, фторурацил 500 мг/м 2 в/в дни 1, 8, интервал 4 недели), АЦФ (фторура– цил 500 мг/м 2 , доксорубицин 50 мг/м 2 , циклофосфан 500 мг/м 2 каждые 3 нед), ЕЦФ (фторурацил 500 мг/м 2 , эпирубицин 100 мг/м 2 , циклофосфан 500 мг/м 2 каждые 3 нед), АЦ (доксорубицин 60 мг/м 2 , циклофосфан 600 мг/м 2 каждые 3 нед).
Большинство исследователей отдают предпочтение антрациклиновым комбинациям, учитывая более высокий противоопухолевый эффект этих комбинаций по сравнению с ЦMФ. Комбинация ЦМФ чаще используется у пожилых больных, при противопоказаниях к применению антрациклинов.
Высокую эффективность показали комбинации антрациклинов и таксанов – АТ (доксорубицин 50–60 мг/м 2 , паклитаксел 175 мг/м 2 , интервал 3 нед), ЕД (эпирубицин 100 мг/м 2 , доцетаксел 75 мг/м 2 , интервал 3 нед).
Длительность химиотерапии обычно определяется ответом опухоли: после достижения максимального эффекта проводится дополнительно 2 курса ПХТ. Затем предпочтение может быть отдано наблюдению за больным до прогрессирования. При продолжении лечения до прогрессирования увеличивается время до прогресси– рования, однако общая выживаемость не меняется, при этом снижается качество жизни больных.
Ведется поиск эффективных комбинаций для первой линии лечения диссеминированного рака молочной железы, включающих новые препараты, в частности, капецитабин (кселода). Показано, что капецитабин имеет лечебную активность, сходную с ЦМФ.
У больных, имевших прогрессирование после химиотерапии антрациклинсодержащими комбинациями, стандартом дальнейшего лечения являются таксаны (паклитаксел 175 мг/м 2 в/в со стандартной премедикацией 1 раз в 3 нед, доцетаксел 100 мг/м 2 в/в со стандартной премедикацией 1 раз в 3 нед). В монотерапии у резистентных к антрациклинам больных объективный эффект составляет 41%. В последнее время все более популярным становится еженедельное введение таксанов, при этом увеличивается интенсивность лечения без увеличения токсичности. Эффективны комбинации таксанов с другими препаратами: навельбин 20 мг/м 2 в/в дни 1, 5-й + доцетаксел 75 мг/м 2 в/в со стандартной премедикацией день 1-й, интервал 3 нед; паклитаксел 175 мг/м 2 в/в со стандартной премедикацией день 1-й + фторурацил 1 г/м 2 /день в/в кап. 72–часовая инфузия дни 1, 2, 3-й, интервал 3 нед; кселода 1650 мг/м 2 дни 1–14 + паклитаксел 175 мг/м 2 (или доцетаксел 75 мг/м 2 )1 раз в 3 нед; гемцитабин 1 г/м 2 дни 1, 15-й + паклитаксел 135 мг/м 2 дни 1, 15-й, интервал 4 нед.
Для третьей и последующих линий лечения четких стандартов не разработано. Применяются комбинации препаратов, включающие навельбин, препараты платины (цисплатин, оксалиплатин), антиметаболиты (длительные инфузии фторурацила, гемцитабин, томудекс, кселода). Следует отметить высокую эффективность кселоды у больных во II (объективный ответ у 36% больных) и III (20%) линиях химиотерапии. Препарат может быть рекомендован, как альтернатива таксанам во II линии химиотерапии.
Некоторые режимы, эффективные во II–III линии лечения диссеминированного рака молочной железы: МММ – митомицин 8 мг/м 2 в/в день 1 + митоксантрон 8 мг/м 2 в/в день 1 + метотрексат 30 мг/м 2 в/в день 1; МЕП – митомицин 10 мг/м 2 в/в день 1 + цисплатин 40 мг/м 2 в/в дни 2, 7 + вепезид 100 мг/м 2 в/в дни 3 ,4, 5, интервал 4 нед; цисплатин 80 мг/м 2 в/в день 1 + кселода 2000 мг/м 2 внутрь ежедневно дни 1–14; навельбин 25 мг/м 2 в/в дни 1, 8 + митомицин 7 мг/м 2 в/в день 1, интервал 4 недели; навельбин 20 мг/м 2 в/в дни 1, 15 + цисплатин 80 мг/м 2 в/в день 1, интервал 4 нед; циклофосфан 600 мг/м 2 в/в день 1 + лейковорин 500 мг/м 2 в/в кап. в течение 2 часов + фторурацил 1,5 г/м 2 в/в постоянная 24–часовая инфузия, дни 1, 15, интервал 4 нед; навельбин 25 мг/м 2 в/в дни 1, 8 + томудекс 1 мг/м 2 в/в дни 1, 8, интервал 3 нед.
В 25–30% случаев в опухоли молочной железы отмечается гиперэкспрессия Неr–2/neu, коррелирующая с плохим прогнозом заболевания. У таких больных эф– фективен Герцептин – препарат принципиально нового механизма действия – рекомбинантные гуманизированные моноклональные антитела, связывающиеся с рецептором Неr–2/neu. Герцептин применяется еженедельно, первое введение – 4 мг/кг в/в, последующие – 2 мг/кг. Лечение продолжается до прогрессирования заболевания. Герцептин рекомендуется к применению у больных с гиперэкспрессией Неr–2/neu в комбинации с гормонотерапией и химиотерапией. Добавление герцептина к комбинации АС повысило частоту объективных эффектов с 42 до 60%. При резистентности к антрациклинам комбинация герцептина с таксолом была эффективна у 49% больных (при монотерапии таксолом эффект составил 17%). Изучаются комбинации герцептина с другими цитостатиками, например, с кселодой, навельбином [5].
1. Материалы шестой конференции по адъювантной терапии рака молочной железы, Сан–Галлен Швейцария, 1998 год.
2. A.C.Wolff, N.E. Davidson: Primary systemic therapy in operable breast cancer. J Clin Oncol 18:1558–1569, 2000.
3. C.А. Тюляндин: Химиотерапия диссеминированного рака молочной железы. Практическая онкология, 2, 2000.
Читайте также:

