1-я линия терапии рака почки

Таргетная терапия - одна из новейших разработок в лечении рака. Она препятствует его развитию на молекулярном уровне. Таргетные препараты нарушают кровоснабжение злокачественных клеток и противодействуют их воспроизводству. Они блокируют команды, сигнализирующие патологическим клеткам о росте.
В отличие от стандартной химиотерапии, которая влияет на все клетки организма, таргетная воздействует только на злокачественные. Ее задача – препятствовать специфическим молекулам, вовлеченным в рост опухоли, чтобы сдерживать развитие и распространение болезни. Поэтому данный вид лечения вызывает меньшее количество побочных эффектов.
Почки изобилуют числом кровеносных сосудов, что способствует росту опухолевых клеток. По этой причине при раке почек таргетная терапия эффективна, предлагая ангиогенные препараты. Они воздействуют на сосуды, которые ведут к злокачественному новообразованию.
Лечение рака почки в Израиле является персонализированным и включает наиболее передовые методы лечения с наименьшим количеством возможных побочных эффектов – лапароскопическую и роботизированную хирургию, криодеструкцию и радиочастотную абляцию, таргетную терапию.
Таргетные препараты рекомендуются:
- при неоперабельной первичной опухоли;
- при метастатическом раке почки;
- в рамках клинических испытаний, чтобы предотвратить рецидив заболевания после хирургического вмешательства.
Лечение предполагает применение одного или нескольких лекарственных средств, для каждого пациента подбирается индивидуальный план лечения. С целью определения наиболее эффективного варианта используется система стратификации риска, применяется генетическое тестирование. Состояние здоровья, особенности конкретного случая болезни влияют на выбор. Во время консультации с врачом в Израиле у пациента есть возможность задать интересующие вопросы (примерный список):
- Принесет ли результаты в конкретном случае таргетная терапия, окажет ли помощь?
- Какие препараты доступны?
- Почему мне была предложена таргетная терапия?
- Что является целью лечения?
- Есть ли другой выбор?
- Каковы краткосрочные и долгосрочные побочные эффекты?
- Какие меры можно предпринять, чтобы снизить действие нежелательных побочных явлений или предотвратить их?
- Как долго будет длиться лечение?
Препараты таргетной терапии рака почки первой линии
В основном данные виды лекарств используются, чтобы уменьшить или контролировать течение болезни при распространенном опухолевом процессе. По результатам исследований и отзывам таргетная терапия рака почек останавливает или замедляет развитие болезни на нескольких месяцев, а иногда - лет.
Обычно лекарственные средства принимают, пока они способны контролировать заболевание. Пациент встречается с врачом каждые 4-6 недель, также сдает анализы крови. Раз в три месяца выполняется сканирование, что выяснить, результативно ли лечение.
Рассмотрим схемы таргетной терапии рака почки. Сунитиниб (Сутент) в основном рекомендуют первым при наличии вторичных очагов. Другой распространенный препарат - Пазопаниб (Pazopanib). Эти лекарства блокируют сигналы о росте в злокачественных клетках и называются ингибиторами тирозинкиназы. Также в ряде случаев назначают сорафениб (Nexavar).
Сунитиниб (Sunitinib)
Сунитиниб имеет другие название - сутент. Его используют на 3 или 4 стадии заболевания. Принимается в капсулах, ежедневно на протяжении 4-х недель с последующим перерывом в 2 недели.
Этот препарат относится к группе ингибиторов тирозинкиназы. Он блокирует внутриклеточные белки под названием тирозинкиназы в опухолевых клетках, которые дают сигналы к росту и делению, связывают клетки с ядром и клеточными структурами. Помимо этого, сутент препятствует кровоснабжению, лишая патологические клетки поступления питательных веществ и кислорода.
Возможные нежелательные последствия приема включают усталость, повышенный риск инфекции в связи с низким уровнем лейкоцитов, анемию, изменения вкусовых ощущений, диарею, кожную сыпь и зуд, ладонно-подошвенную кератодермию, артериальную гипертензию. Сунитиниб может ухудшить работу щитовидной железы, по этой причине больной регулярно сдает анализы крови, чтобы проверить это.
Пазопаниб (Pazopanib)
Пазопаниб – ингибитор роста рака, врач может порекомендовать препарат в качестве первичного лечения при распространенном опухолевом процессе и как вторичное после применения интерферона или интерлейкина-2. Выпускается в таблетках, его принимают каждый день. К потенциальным отрицательным последствиям приема относят: диарею, ладонно-подошвенную кератодермию, сыпь и зуд кожи, повышенную утомляемость, тошноту.
Препараты таргетной терапии рака почки второй линии
Если лечение перестает работать и рак начинает снова расти, врач назначает вторую линию терапии. Назначен может быть один из упомянутых выше препаратов. Либо врач предложит бевацизумаб (Авастин) внутривенно с интерфероном. Другие лекарства - Темсиролимус (Torisel) или эверолимус (Afinitor). Они блокируют сигналы о росте, и называются MTOR блокаторами (MTOR – белок, управляющий ростом, делением и метаболизмом клетки).
Авастин в таргетной терапии рака почки и интерферон
Бевацизумаб (Авастин) – моноклональное антитело, препятствует развитию кровеносных сосудов в опухолевом новообразовании. Препарат назначают внутривенно каждые две недели, интерферон - три раза в неделю в виде инъекций.
Чаще всего при приеме интерферона наблюдаются гриппоподобные симптомы на протяжении недели – двух. Прием парацетомола за полчаса до инъекции может помочь – предотвратит их или уменьшит. Среди других нежелательных явлений отмечают кровотечения из носа, запор – диарею, депрессию, тошноту, гипертонию.
Темсиролимус (Torisel)
Темсиролимус дают внутривенно один раз в неделю. Он блокирует сигналы о росте в злокачественных клетках, относится к препаратам MTOR ингибиторам. Рекомендуется при распространенном опухолевом процессе в качестве вторичной таргетной терапии рака почки. К нежелательным явлениям терапии относят: сыпь, зуд и красноту кожи, тошноту, потерю аппетита, диарею, воспаление в полости рта; низкие уровни клеток крови.
Эверолимус (Afinitor)
Эверолимус выпускается в таблетках, его принимают раз в день. Как и темсиролимус, Afinitor – это ингибитор MTOR, блокирующий сигналы о росте для злокачественных клеток. Врачи применяют его в качестве второй линии таргетной терапии рака почки при метастазах, когда нет реакции на сутент и сорафениб.
К возможным нежелательным явлениям терапии относят низкую устойчивость к инфекции, усталость и одышку из-за недостаточного уровня эритроцитов, повышенное содержание холестерина и сахара в крови, воспалительный процесс в полости рта; высыпания, зуд и сухость кожи; тошноту.
Сорафениб (Nexavar)
Принимается ежедневно, перорально. Он работает в двух направлениях таргетной терапии рака почки: блокирует сигналы о росте и процесс агиогенеза в злокачественном новообразовании. Используется при наличии вторичных очагов рака почки, когда неэффективны препараты биологической терапии, у пациента наблюдается непереносимость к сутенту.
Среди потенциальных нежелательных явлений отмечают: диарею, чрезмерную утомляемость, ладонно-подошвенную эритродизестезию, тошноту, истончение волос.
На сегодняшний день нет методов лечения, уменьшающих вероятность рецидива рака почки после хирургии. Но проводится большое количество исследований в мире, в рамках которых изучаются таргетные препараты. Также разрабатываются новые лекарства данного вида лечения.
У каждого препарата - свои побочные действия. Большинство людей, принимая их, испытывают усталость. В зависимости от назначенного лекарства побочные эффекты включают: диарею, кожные высыпания, боль в руках и ногах. Врач подробно обсуждает с пациентом этот вопрос и консультирует, как лучше справляться с ними.
Бюро по изучению рака почки, Москва
1. Motzer RJ, Bander NH, Nanus DM. Renal-cell carcinoma. N Engl J Med 1996;335:865–75.
2. Faivre S, Delbaldo C, Vera K, et al. Safety, pharmacokinetic, and antitumor activity of SU11248, a novel oral multitarget tyrosine kinase inhibitor, in patients with cancer. J Clin Oncol 2006;24(1):25–35.
3. Chow LQ, Eckhardt SG. Sunitinib: from rational design to clinical efficacy. J Clin Oncol 2007;25(7):884–96.
4. Motzer RJ, Hutson TE, Tomczak P, et al. Sunitinib versus interferon alfa in metastatic renal-cell carcinoma. N Engl J Med 2007;356(2):115–24.
5. Motzer RJ, Hutson TE, Tomczak P, et al. Overall Survival and Updated Results for Sunitinib Compared With Interferon Alfa in Patients. J Clin Oncol 2009;27(22):3584–90.
6. Gore ME, Szczylik C, Porta C, et al. Safety and efficacy of sunitinib for metastatic renal-cell carcinoma: an expanded-access trial. Lancet Oncol 2009;10(8):757–63.
7. Tsimafeyeu IV. Salvage therapy with sunitinib malate in metastatic renal cell carcinoma patients. EMUC 2009;130:91.
8. Yang ОС, Haworth L, Sherry RM, et al. A Randomized Trial of Bevacizumab, an Anti– Vascular Endothelial Growth Factor Antibody, for Metastatic Renal Cancer. N Engl J Med 2003;349:427–34.
9. Escudier B, Pluzanska A, Koralewski P, et al. Bevacizumab plus interferon alfa-2a for treatment of metastatic renal cell carcinoma: a randomised, double-blind phase III trial. Lancet 2007;370(9605):2103–11.
10. Escudier BJ, Bellmunt J, Negrier S, et al. Final results of the phase III, randomized, double-blind AVOREN trial of first-line bevacizumab (BEV) + interferon-alpha 2a (IFN) in metastatic renal cell carcinoma (mRCC). J Clin Oncol 2009;27:15.
11. Rini BI, Halabi S, Rosenberg J, et al. Bevacizumab plus interferon-alpha versus interferon-alpha monotherapy in patients with metastatic renal cell carcinoma: Results of overall survival for CALGB 90206. J Clin Oncol 2009;27:18.
12. Awada A, Hendlisz A, Gil T, et al. Phase I safety and pharmacokinetics of BAY 43-9006 administered for 21 days on/7 days off in patients with advanced, refractory solid tumours. Br J Cancer 2005;92(10):1855–61.
13. Clark JW, Eder JP, Ryan D, et al. Safety and pharmacokinetics of the dual action Raf kinase and vascular endothelial growth factor receptor inhibitor, BAY 43-9006, in patients with advanced, refractory solid tumors. Clin Cancer Res 2005;11(15):5472–80.
14. Strumberg D, Richly H, Hilger RA, et al. Phase I clinical and pharmacokinetic study of the Novel Raf kinase and vascular endothelial growth factor receptor inhibitor BAY 43-9006 in patients with advanced refractory solid tumors. J Clin Oncol 2005;23(5):965–72.
15. Szczylik C, Demkow T, Staehler M, et al. Randomized phase II trial of first-line treatment with sorafenib versus interferon in patients with advanced renal cell carcinoma: Final results. J Clin Oncol 2007;25(18):25.
16. Hudes G, Carducci M, Tomczak P, et al. Temsirolimus, interferon alfa, or both for advanced renal-cell carcinoma. N Engl J Med 2007;356(22):2271–81.
17. Sternberg C, Szczylik C, Lee E, et al. A randomized, double-blind phase III study of pazopanib in treatment-nave and cytokine-pretreated patients with advanced renal cell carcinoma (RCC). J Clin Oncol 2009;27(15):5021.











Первая линия терапии метастатического рака почки
Представлены обнадеживающие результаты рандомизированных исследований эффективности 5 различных таргетных препаратов (сунитиниб, сорафениб, темзиролимус, пазопаниб и бевацизумаб), применяемых в первой линии терапии метастатического почечно-клеточного рака. При внедрении новых препаратов в повседневную практику врача особое внимание должно быть уделено стандартизации подходов к оказанию медицинской помощи, согласно критериям эффективности.
До недавних пор системное лечение метастатического почечноклеточного рака (ПКР) было ограничено применением цитокинов и клиническими испытаниями новых препаратов. Несмотря на то что применение цитокинов являлось стандартным лечением ПКР на протяжении 15 лет, в настоящее время в качестве первой и второй линий терапии используются таргетные препараты на основе ингибиторов тирозинкиназы и моноклональных антител.
Выбор препарата первой линии терапии зависит от нескольких параметров. Во-первых, важно учитывать, к какой группе риска относятся пациенты. Наиболее широко используется модель стратификации риска по критериям Онкологического центра MSKCC (Memorial Sloan Kettering Cancer Center) [1].
Факторы риска, или критерии короткой выживаемости, включают:
- высокий уровень лактатдегидрогеназы (ЛДГ), более, чем в 1,5 раза превышающий верхнюю границу нормы;
- высокий уровень кальция в крови (скорректированный уровень кальция более 10 мг/дл, или 2,5 ммоль/л);
- анемию;
- время от момента установления диагноза до начала системной терапии менее года;
- плохое общее состояние (индекс Карновского 0,20). Побочные эффекты всех степеней токсичности были достоверно выше в группе “бевацизумаб в высокой дозе” и включали артериальную гипертензию (36 %), бессимптомную протеинурию (64 %,) гематурию (13 %), а также носовое кровотечение (20 %).
Впоследствии было проведено кооперированное рандомизированное двойное слепое исследование III фазы (AVOREN) по сравнению эффективности комбинации бевацизумаба и ИФН с комбинацией плацебо и ИФН. Рандомизации было подвергнуто 649 больных (лечение получил 641 пациент) [9]. Добавление бевацизумаба к ИФН статистически значимо увеличило БВ (10,2 месяца по сравнению с 5,4; р = 0,0001) и частоту объективных ответов (31 против 13 %; р = 0,0001). Новые побочные эффекты, помимо ожидаемых, для каждого препарата по отдельности при их применении в комбинации не отмечены. Кроме того, наблюдалась тенденция к повышению ОВ. Согласно окончательным результатам исследования AVOREN, медиана ОВ пациентов, получавших бевацизумаб в комбинации с ИФН, составила 23,3 месяца по сравнению с 21,3 –у больных, получавших плацебо в комбинации с ИФН. Различия были статистически незначимыми (р = 0,1291) [10].
Сходное исследование (CALGB 90206) провела в США исследовательская группа B по изучению рака и лейкозов (CALGB —Cancer and Leukemia Group B). В этом исследовании 732 больных, ранее не получавших лечение, были рандомизированы в две группы: в первой применяли только ИФН, во второй —комбинацию бевацизумаба и ИФН. По сравнению с одним ИФН применение комбинации сопровождалось увеличением БВ (8,5 месяца по сравнению с 5,2; р
Информация об авторе:
Тимофеев Илья Валерьевич – директор Бюро по изучению рака почки, член научного совета международной Ассоциации по раку почки.
E-mail: office@kidneytumor.org
1. Motzer RJ, Bander NH, Nanus DM. Renal-cell carcinoma. N Engl J Med 1996;335:865–75.
2. Faivre S, Delbaldo C, Vera K, et al. Safety, pharmacokinetic, and antitumor activity of SU11248, a novel oral multitarget tyrosine kinase inhibitor, in patients with cancer. J Clin Oncol 2006;24(1):25–35.
3. Chow LQ, Eckhardt SG. Sunitinib: from rational design to clinical efficacy. J Clin Oncol 2007;25(7):884–96.
4. Motzer RJ, Hutson TE, Tomczak P, et al. Sunitinib versus interferon alfa in metastatic renal-cell carcinoma. N Engl J Med 2007;356(2):115–24.
5. Motzer RJ, Hutson TE, Tomczak P, et al. Overall Survival and Updated Results for Sunitinib Compared With Interferon Alfa in Patients. J Clin Oncol 2009;27(22):3584–90.
6. Gore ME, Szczylik C, Porta C, et al. Safety and efficacy of sunitinib for metastatic renal-cell carcinoma: an expanded-access trial. Lancet Oncol 2009;10(8):757–63.
7. Tsimafeyeu IV. Salvage therapy with sunitinib malate in metastatic renal cell carcinoma patients. EMUC 2009;130:91.
8. Yang ОС, Haworth L, Sherry RM, et al. A Randomized Trial of Bevacizumab, an Anti– Vascular Endothelial Growth Factor Antibody, for Metastatic Renal Cancer. N Engl J Med 2003;349:427–34.
9. Escudier B, Pluzanska A, Koralewski P, et al. Bevacizumab plus interferon alfa-2a for treatment of metastatic renal cell carcinoma: a randomised, double-blind phase III trial. Lancet 2007;370(9605):2103–11.
10. Escudier BJ, Bellmunt J, Negrier S, et al. Final results of the phase III, randomized, double-blind AVOREN trial of first-line bevacizumab (BEV) + interferon-alpha 2a (IFN) in metastatic renal cell carcinoma (mRCC). J Clin Oncol 2009;27:15.
11. Rini BI, Halabi S, Rosenberg J, et al. Bevacizumab plus interferon-alpha versus interferon-alpha monotherapy in patients with metastatic renal cell carcinoma: Results of overall survival for CALGB 90206. J Clin Oncol 2009;27:18.
12. Awada A, Hendlisz A, Gil T, et al. Phase I safety and pharmacokinetics of BAY 43-9006 administered for 21 days on/7 days off in patients with advanced, refractory solid tumours. Br J Cancer 2005;92(10):1855–61.
13. Clark JW, Eder JP, Ryan D, et al. Safety and pharmacokinetics of the dual action Raf kinase and vascular endothelial growth factor receptor inhibitor, BAY 43-9006, in patients with advanced, refractory solid tumors. Clin Cancer Res 2005;11(15):5472–80.
14. Strumberg D, Richly H, Hilger RA, et al. Phase I clinical and pharmacokinetic study of the Novel Raf kinase and vascular endothelial growth factor receptor inhibitor BAY 43-9006 in patients with advanced refractory solid tumors. J Clin Oncol 2005;23(5):965–72.
15. Szczylik C, Demkow T, Staehler M, et al. Randomized phase II trial of first-line treatment with sorafenib versus interferon in patients with advanced renal cell carcinoma: Final results. J Clin Oncol 2007;25(18):25.
16. Hudes G, Carducci M, Tomczak P, et al. Temsirolimus, interferon alfa, or both for advanced renal-cell carcinoma. N Engl J Med 2007;356(22):2271–81.
17. Sternberg C, Szczylik C, Lee E, et al. A randomized, double-blind phase III study of pazopanib in treatment-nave and cytokine-pretreated patients with advanced renal cell carcinoma (RCC). J Clin Oncol 2009;27(15):5021.

- Опухоли почки
- Метастазы рака почки
- Как часто и у кого встречается рак почки?
- Диагностика опухолей почек
- Лечение рака почки на разных стадиях
- Цены в Европейской онкологической клинике на лечение рака почки
Опухоли почки
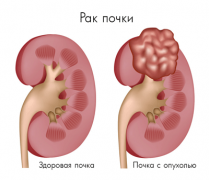
Второй характеристикой опухоли почки, как впрочем и большинства других опухолей, является потеря спецификации клетки – так как клетка быстро делится, она просто не успевает специализироваться. Таким образом, опухоль почки в первом приближении можно характеризовать, как массу клеток, бесконтрольно делящихся и потерявших способность к специализации. Чем меньше специализирована клетка опухоли для выполнения своей функции, чем быстрее она делится и чем больше его способность к распространению по кровеносным и лимфатическим сосудам, тем опухоль злокачественнее.
Почти 90 % опухолей почки злокачественны. Оставшиеся 10 процентов приходятся на ангиомиолипомы и другие, гораздо более редкие доброкачественные опухоли почки. Между тем, даже доброкачественные опухоли почки вполне могут быть опасны для здоровья. Например – ангиомиолипома может повредить сосуды почки, вызывая кровотечение. Что же касается злокачественных опухолей или рака почки, то тут мы сталкиваемся с повреждением функционирующей почечной ткани, ее сосудов и кровотечением, с метастазированием в кости, легкие, головной мозг и, соответственно, нестерпимыми болями.
Метастазы рака почки
Метастазирование — это распространение опухоли по кровеносным или лимфатическим сосудам. Опухоли, как и всему живому в организме, требуется питание, обеспечиваемое сосудами. Вот в эти сосуды и попадают 1-2 клетки из основной опухоли, которые распространяются на различные органы. Для рака почки характерно метастазирование в кости и легкие, а также в печень, надпочечники и головной мозг.
рака почки, как и основная опухоль, нарушает функцию органа, где развивается. Например, метастаз рака почки в легкие вызывает упорный кашель, метастаз в кости — страшные, изнуряющие боли, от которых помогают только сильнодействующие наркотические препараты. К сожалению, часть пациентов, обративших к врачу, уже имеют отдаленные метастазы в тех или иных органах. Это резко ухудшает прогноз течения заболевания, так как приходится бороться не с одной опухолью, а, по сути, с опухолями множеством опухолей в нескольких органах.
Как часто и у кого встречается рак почки?
Диагностика опухолей почек
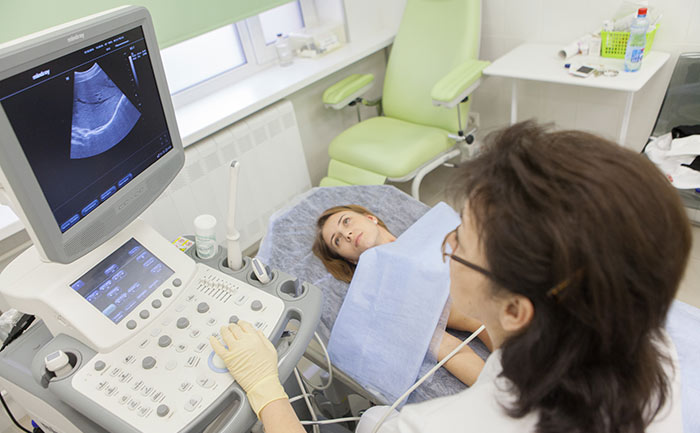
При подозрении на рак почки пациенту назначают общий анализ мочи, общий и биохимический анализы крови.
Один из наиболее информативных методов диагностики рака почки – компьютерная томография. Она помогает оценить размер, форму и локализацию злокачественного новообразования, обнаружить очаги в лимфатических узлах и других анатомических структурах за пределами почек. Исследование нередко дополняют внутривенным контрастированием. Введение контраста противопоказано при нарушении функции почек.
Магнитно-резонансную томографию применяют реже, чем КТ. Она показана, когда пациенту нельзя проводить компьютерную томографию с контрастом, если имеется подозрение на прорастание опухоли в нижнюю полую вену или другие крупные сосуды, для обнаружения метастатических очагов в головном и спинном мозге.

Ангиография – рентгенография с контрастирование сосудов, почки. Она помогает в диагностике заболевания и планировании хирургического лечения.
Позитронно-эмиссионная томография помогает обнаружить вторичные очаги рака в различных частях тела. Суть метода в том, что в организм пациента вводят вещество, которое обладает слабой радиоактивностью и накапливается в опухолевых клетках. Затем выполняют снимки с помощью специального аппарата, и на них опухолевые очаги хорошо видны.
В отличие от других онкологических заболеваний, биопсия при раке почки проводится редко. Обычно результатов других исследований хватает для того, чтобы принять решение о необходимости хирургического вмешательства. Уже после операции удаленную опухоль направляют в лабораторию, чтобы подтвердить диагноз. Биопсию проводят, если другие исследования не позволяют разобраться, показана ли операция. В случаях, когда хирургическое вмешательство противопоказано, исследование опухолевой ткани помогает определиться с тактикой лечения.
В медицине нет категоричных, стопроцентных ответов. Какова цель операции по удалению рака почки? Удалить опухоль? Удалить почку с подлежащими структурами? Удалить только первичный очаг опухоли, а потом бороться с метастазами теми или иными способами? Перенесет ли пациент операцию, каково его общее состояние? Какую именно операцию выбрать для конкретного больного? На эти вопросы должен ответить онкоуролог, перед тем, как предложить хирургическое, консервативное или комбинированное лечение. В основном, это зависит от стадии рака почки, расположения опухоли, наличия метастазов в лимфатические узлы и общего состояния здоровья пациента.

Это зависит главным образом от стадии, на которой была диагностирована опухоль, и начато лечение. Пятилетняя выживаемость (процент пациентов, оставшихся в живых спустя 5 лет) наиболее высока для I стадии и составляет 81%. На II и III стадиях она, соответственно, составляет 74 и 53%. При IV стадии — 8%.
Стадия рака почки зависит от размеров и расположения опухоли. Так, рак почки первой стадии — это опухоль меньше 7 см, не выходящая за пределы почки. Рак почки второй стадии — это опухоль меньше 10 см, также не выходящая за пределы почки. А вот рак почки третьей стадии — это уже опухоль любых размеров, ограниченная почкой, либо повреждающая надпочечник, почечную вену, но имеющую метастаз в ближайших лимфатических узлах. Рак почки четвертой стадии может быть любых размеров, однако при этой стадии опухоль либо выходит за пределы почечной фасции, либо имеются больше одного метастаза в ближайших лимфатических узлах, либо имеются метастазы в легкие, кости, печень или головной мозг.
Стадию рака почки определяют в соответствии с международной классификацией TNM. Рядом с каждой из трех букв аббревиатуры указывают индекс, описывающий характеристики первичной опухоли (T), поражение регионарных лимфатических узлов (N), наличие отдаленных метастазов (M):
T1 – опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр не более 4 см (T1a) или 4–7 см (T1b).
T2 - опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр 7–10 см (T2a) или более 10 см (T1b).
T3 – злокачественное новообразование распространяется на почечную вену и ее ветви, на надпочечник на одноименной стороне, паранефральную клетчатку, не прорастая фасцию Героты (T3a), на нижнюю полую вену ниже (T3b) или выше (T3c) диафрагмы или врастает в стенку вены.
T4 – опухоль распространяется за пределы фасции Героты.
N0 – опухолевые очаги в регионарных лимфоузлах отсутствуют.
N1 – обнаруживается опухолевый очаг в одном лимфоузле.
N2 – обнаруживаются опухолевые очаги в двух и более регионарных лимфоузлах.
M0 – отдаленных метастазов нет.
M1 – отдаленные метастазы присутствуют.
В зависимости от значений T, N и M, выделяют четыре стадии рака почки:
- Стадия I: опухоль в почке не более 7 см (T1), лимфоузлы не поражены, отдаленных метастазов нет.
- Стадия II: первичная опухоль более 7 см (T2), отсутствуют очаги поражения в лимфатических узлах и отдаленные метастазы.
- Стадия III: злокачественная опухоль распространяется на соседние структуры (T3) и/или поражен один регионарный лимфатический узел (N1).
Стадия IV: опухоль распространяется на соседние структуры (T4), либо поражено 2 и более регионарных лимфоузла (N2), либо обнаружены отдаленные метастазы (M1).
Опухоль почки размером 2 см может быть расположена вблизи почечных сосудов и ее удаление технически может быть невозможным. Однако данные литературы указывают, что если нет метастазов в лимфатические узлы и отдаленные органы, то опухоль почки до 7 см можно удалять с сохранением почки, что, безусловно, лучше полного удаления почки и инвалидизации пациента.
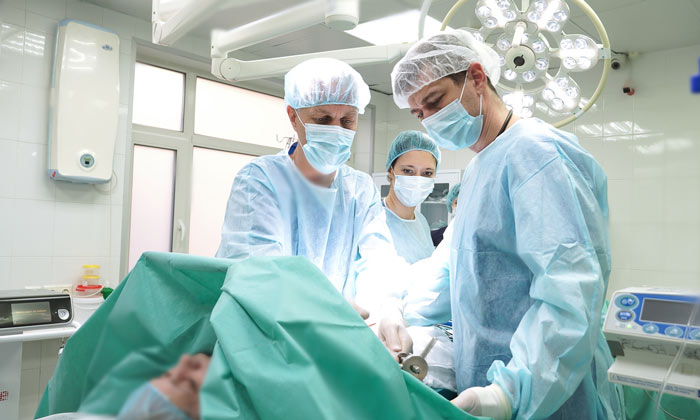
Лечение рака почки на разных стадиях
Выбор тактики лечения при раке почки в первую очередь определяется стадией опухоли и состоянием здоровья пациента.
При стадиях I и II возможно хирургическое лечение. Стандартным вариантом считается нефрэктомия. К органосохраняющим операциям прибегают реже, в частности, при опухолях в единственной почке. Кроме того, на выбор объема операции влияет размер опухоли. Также удаляют близлежащие лимфатические сосуды, особенно если они увеличены, окружающую жировую клетчатку.
При III стадии рака почки основным методом лечения также является нефрэктомия, при этом должны быть удалены все регионарные метастазы. Если опухоль прорастает в почечную или нижнюю полую вену или мигрирует в их просвете в виде опухолевого тромба, пораженные ткани также нужно удалить, при этом может потребоваться подключение пациента к аппарату искусственного кровообращения.
При высоком риске рецидива после операции применяют адъювантную терапию таргетным препаратом сунитинибом. Пациенты получают его в течение года.
Если хирургическое вмешательство противопоказано, прибегают к радиочастотной аблации, эмболизации.
На IV стадии подходы к лечению могут быть разными, в зависимости от степени распространения рака в организме. В некоторых случаях возможно хирургическое лечение, в том числе циторедуктивные операции, во время которых хирурги не могут убрать опухоль полностью, но стараются удалить как можно больший ее объем. В редких случаев возможно удаление основной опухоли в почке и единичных вторичных очагов в других органах. После операции назначают курс таргетной терапии, иммунотерапии.
При неоперабельном раке почки основными методами лечения становятся иммунотерапия и таргетная терапия.

В некоторых случаях рак почки удается выявить на ранних стадиях, когда опухолевые клетки не распространяются за пределы органа. Но зачастую заболевание диагностируют на более поздних стадиях. Во-первых, это связано с тем, что рак почки может очень долго протекать бессимптомно. Во-вторых, для этого типа рака на данный момент не существует рекомендованных скрининговых исследований.
Все симптомы можно разделить на ренальные (связанные с поражением почек) и экстраренальные.
Среди ренальных проявлений рака почки наиболее характерны три:
- Гематурия (примесь крови в моче) – самый распространенный и зачастую первый симптом. Он возникает более чем у половины пациентов с раком почки. Моча приобретает красный цвет, при этом боль не беспокоит либо носит острый характер и возникает после гематурии. Этим злокачественная опухоль отличается от неопухолевых заболеваний почки, например, мочекаменной болезни, при которой обычно сначала возникает боль, а потом появляется примесь крови в моче. Гематурия периодически исчезает, но через некоторое время снова появляется, причем, промежутки между кровотечениями сокращаются. Количество крови в моче не зависит от размеров опухоли.
- Боли беспокоят около половины пациентов. Острая боль после гематурии возникает из-за того, что сгустки крови перекрывают просвет мочеточника. Тупые сильные боли зачастую говорят о плохом прогнозе.
- Пальпируемая опухоль – симптом, который выявляет врач во время осмотра примерно у трети пациентов.
Все три симптома одновременно встречаются у одного из десяти пациентов с раком почкеи. Обычно при этом выявляют запущенные опухоли.
Среди экстраренальных симптомов в первую очередь стоит отметить повышение температуры тела. У 5% больных лихорадка – единственное проявление заболевания. У некоторых пациентов повышается артериальное давление, отмечается покраснение лица из-за увеличения количества эритроцитов в крови, у мужчин – расширение вен мошонки (варикоцеле). На поздних стадиях снижается аппетит, пациент теряет вес без видимой причины, постоянно ощущает утомление, недомогание.
Читайте также:

