Замещение метана с хлором
Химические свойства алканов
Алканы относятся к углеводородам, в которых отсутствуют кратные связи. Одно из названий углеводородов этого ряда – парафины, обозначает их химическую пассивность. Поэтому химические свойства алканов определяются таким образом:
1. Из-за предельности алканов реакции присоединения для них нехарактерны.
2. Из-за прочных связей С-С и С-Н (короткие и практически неполярные) следует малая реакционная способность (не реагируют с кислотами, щелочами, KMnO4 и т.п.)
3. Неполярность связей свидетельствует о том, что реакции могут проходить по свободнорадикальному механизму.
Основной тип реакций – радикальное замещение (radicalsubstitution) SR.
Разорвать связь можно при помощи нагревания или УФ-излучения. Обычно реакции алканов идут при повышенных температурах или на солнечном свету.
2. Реакция галогенирования
Взаимодействие алканов с галогенами ( элементы VII-A группы) носит общее название –реакция галогенирования. Скорость реакции зависит от активности галогенов, которая уменьшается с увеличением радиуса атома.
Фтор химически слишком активен, и реакции алканов с его участием сопровождаютсявзрывом и окислением до CF4.
Взаимодействие алканов с йодом практически не протекает.
Реакции хлорирования и бромирования проводят при 300–400 о C или при облучении УФ-лампой.
Механизм реакции замещения на примере хлорирования метана
При хлорировании атом Н в молекуле метана замещается на атом Cl. В избытке хлора происходит дальнейшее замещение:
СН4 + Сl2 
CH3Cl + HCl;
CH3Cl + Сl2 
CH2Cl2 + HCl;
CH2Cl2 + Сl2 
CHCl3 + HCl;
CHCl3 + Сl2 
CCl4 + HCl.
3. Механизм радикального замещения
Механизм реакции – последовательность стадий, через которые проходит химическая реакция.
Стадия 1 – зарождение цепи (инициация)
Когда молекулу хлора нагревают или облучают, слабая связь между атомами хлора рвется, при этом каждому из атомов при разрыве связи достается по одному электрону.
В результате образуются незаряженные частицы с неспаренным электроном – радикалы. Атомы в радикалах содержат на внешнем уровне нечетное число электронов. Поэтому радикалы – очень неустойчивые и реакционноспособные частицы.
Cl:Сl 
2 Сl · .
Стадия 2 – развитие (рост) цепи
Атом хлора при столкновении с молекулой алкана отрывает от нее атом Н, и образуется молекула HCl. Возникает новый свободный радикал · СН3. Он далее реагирует с другой молекулой хлора. Такие взаимодействия могут повторяться много раз, образуя длинную цепь.
Стадия 3 – обрыв цепи (рекомбинация)
Два радикала могут встретиться, и цепь прервется:
Обратите внимание: в последнем случае возникает вещество, в молекуле которого больше атомов углерода, чем в исходном алкане. Поэтому в смеси продуктов радикальных реакций алканов всегда присутствуют небольшие количества веществ с более длинной углеродной цепью.
В химии радикальным замещением называют реакции, в которых свободные радикалы атакуют молекулу вещества, замещая собой отдельные ее атомы. При реакции замещения образуются новые радикалы. Цепная реакция продолжается до момента, когда иссякнут все свободные радикалы.

Определение радикала
Радикал – это атом или молекула, имеющие на внешнем электронном слое один или более неспаренных электронов. То есть таких электронов, у которых нет пары. Радикал может образоваться, когда молекула приобретает один электрон или наоборот, теряет его. В своем большинстве свободные радикалы нестабильны, так как их внешний электронный слой не завершен. Поэтому радикалы легко вступают в реакции с некоторыми веществами, образуя при этом новые вещества и свободные радикалы.
Какими бывают радикалы?
Основные группы, по которым происходит классификация радикалов:
- стабильность: стабильные и нестабильные;
- заряженность: незаряженные, отрицательно заряженные и положительно заряженные;
- степень связанности: свободные и комплексные.
Стабильные радикалы
- углеводородные;
- гидразильные;
- нитроксильные;
- аминильные;
- ароксильные;
- вердазильные.

Механизм реакции радикального замещения
В механизме реакции выделяют три стадии:
- Инициирование. Посредством внешних факторов (нагревание, облучение, химические и электрические катализаторы) разрушается связь в молекуле вещества, образуя свободные радикалы.
- Развитие цепи или ее рост. Свободные элементы вступают во взаимодействие с молекулами, благодаря чему образуются новые вещества и радикалы.
- Обрыв цепи. На третьей стадии радикалы соединяются между собой. Происходит их рекомбинация (объединение неспаренных электронов, которые принадлежат разным частицам), благодаря чему появляются новые самостоятельные молекулы. Свободных радикалов не остается, и цепь реакции считается завершенной.
Типичные реакции замещения
Обычно реакцию радикального замещения показывают на примере галогенирования алканов. Самый простой алкан – метан – СН4, а самый распространенный галоген — хлор.
Алканы
Алканы – насыщенные углеводороды, содержащие только простые связи. Общая формула алканов – CnH2n+2. Насыщенными называются те углеводороды, которые содержат максимальное количество атомов водорода. Ранее алканы называли парафинами из-за того, что эти вещества не реагировали с кислотами, щелочами и т. д. На самом деле устойчивость к взаимодействию с сильными реагентами объясняется прочностью С-С и С-Н связей. Насыщенность алканов также говорит о том, что они не участвуют в реакциях присоединения. Для них характерны реакции разложения, замещения и прочие.

Галогены
Чтобы провести реакцию радикального замещения, нужно дать определение галогенам. Галогены – это элементы 17-й группы таблицы Менделеева. Галогенами являются Cl (хлор), I (йод), F (фтор), Br (бром) и At (астат). Все галогены являются неметаллами и сильными окислителями. Самую высокую окислительную активность имеет фтор, а самую низкую – астат. В процессе галогенирования алканов один или больше атомов водорода в веществе заменяется на галоген.
Механизм замещения на примере галогенирования метана
Простейшим алканом считается метан, поэтому реакции его галогенирования легко запомнить, и на этой основе проводить радикальное замещение других алканов. В качестве галогена обычно берется хлор. Он обладает средней силой реагирования. Реакция алканов с йодом не идет, так как он слабый галоген. Взаимодействие с фтором проходит со взрывом, потому что атомы фтора очень активны. Хотя при реакции замещения алканов с хлором тоже может произойти взрыв.
Зарождение цепи. Под воздействием солнечного, ультрафиолетового излучения или от нагревания молекула хлора Cl2 распадается на два свободных радикала. У каждого один неспаренный электрон на внешнем слое.
Развитие или рост цепи. Взаимодействуя с молекулами метана, свободные радикалы образуют новые и продолжают цепь превращений.
Далее реакция идет до тех пор, пока не исчезнут все свободные радикалы.
Обрыв цепи – заключительная стадия радикального замещения алканов. Радикалы соединяются друг с другом и образуют новые молекулы.
Хлорирование метана
Под действием солнечного света радикалы хлора замещают все атомы водорода в метане. Для полного замещения водорода доля хлора в смеси должна быть достаточной. Таким образом, из метана может получиться четыре его производных:
CHCl3 – трихлорметан (хлоформ).

Галогенирование других алканов
Начиная с пропана (С3Н8) у алканов появляются третичные и вторичные атомы углерода. Галогенирование разветвленных алканов может давать разные результаты. В результате реакции радикального замещения образуются изомеры алканов. Масса каждого получившегося вещества может сильно различаться в зависимости от температуры.
При термическом галогенировании состав получившегося продукта определяется исходя из соотношения количества С―Н–связей атомов углерода, которые в сложных алканах бывают первичными, вторичными и третичными. В результате фотохимического галогенирования состав получившихся продуктов будет зависеть от скорости, с которой атомы галогена сменяют атомы водорода. Галогенам легче всего встать на место третичного атома водорода. Сложнее заместить вторичный и первичный.
Хлорирование пропана
При хлорировании пропана с катализатором в виде повышения температуры до 450 ⁰С образуются 2-хлорпропан в количестве 25 % и 1-хлорпропан в количестве 75 %.
Если проводить реакцию радикального замещения алкана с помощью солнечного света, выходит 57 % 2-хлорпропана и 43 % 1-хлорпропана.
Разница в массе полученных веществ между первой и второй реакцией объясняется тем, что во втором случае скорость замещения на атом Н у вторичного атома выше в 4 раза, чем у первичного, хотя в молекуле пропана больше первичных С―Н -связей.

Реакции окисления
В реакциях окисления алканов опять же участвуют свободные радикалы. В этом случае радикал О2 присоединяется к молекуле алкана, и происходит реакция полного или неполного окисления. Полное окисление называется горением:
Реакция горения алканов по механизму радикального замещения широко используется в промышленности как топливо для ТЭЦ, для двигателей внутреннего сгорания. В такие машинные двигатели можно помещать только разветвленные алканы. Простые линейные алканы в ДВС взрываются. Из нелетучего осадка, образовавшегося в результате радикального замещения, производят смазки, асфальт, парафин и т. д.

Частичное окисление
В промышленности смеси, которые образуются при частичном окислении метана, используются для изготовления синтетических алканов. Из метана при неполном окислении воздухом можно получить метиловый спирт (СН3ОН), формальдегид (НСНО), муравьиную кислоту (НСООН). А при окислении бутана в промышленности вырабатывается уксусная кислота:
Для того чтобы алканы окислялись частично, используют катализаторы (Со 2+ , Mn 2+ и т. д.) при сравнительно невысоких температурах воздуха.
Алканы (предельные, насыщенные) – это нециклические углеводороды, в молекулах, которых атомы углерода связаны друг с другом только простыми (σ-связями). Алканы имеют общую формулу CnH2n+2 , не присоединяют водород и другие элементы.
Строение молекулы метана
Простейшим представителем предельных углеводородов является метан.
СН4 – молекулярная формула (качественный, количественный состав).
Молекула метана не имеет плоского строения. Молекула метана в действительности имеет формутетраэдра. Тетраэдр – это пирамида, в основании которой лежит равносторонний треугольник. Вцентре тетраэдра находится атом углерода, а атомы водорода – в вершинах тетраэдра.
Вывод: молекула метана в пространстве имеет тетраэдрическое строение.
1) Для метана характерны главным образом реакции замещения атомов водорода на атомы галогенов:
2)
СН4 + Cl2 →CH3Cl + HCl - хлорметан
СН3Cl + Cl2 →CH2Cl2 + HCl - дихлорметан
СН2Cl2 + Cl2 →CHCl3 + HCl – трихлорметан (хлороформ)
СНCl3 + Cl2 →CCl4 + HCl – тетрахлорметан (четыреххлористый углерод)
Метан с кислородом: реакция горения
Процесс горения метана — это взаимодействие метана с кислородом. В результате реакции образуется вода, двуокись углерода и много энергии. Уравнение реакции горения метана:
CH₄[газ] + 2O₂[газ] → CO₂[газ] + 2H₂O[пар] + 891кДж
ВОПРОС №7
Алкены ряда этена (этилена), их общая формула. Этилен, его химические свойства (горение, реакции присоединения и полимеризации)
Алкены – нециклические углеводороды с одной двойной связью и общей формулой С n Н2 n
Двойная связь – сочетание прочной σ–связи и непрочной π –связи.
Электронное строение молекулы этилена
Атомы углерода в составе молекулы алкена связаны между собой двойной связью. Эти атомы находятся в состоянии sp 2 -гибридизации. Двойная связь между ними образована из двух пар обобществленных электронов, т.е. это четырехэлектронная связь. Она сочетанием ковалентных σ-связи и π-связи. σ-Связь образована за счет осевого перекрывания sp 2 -гибридных орбиталей, а π-связь – за счет бокового перекрывания негибридизованных p-орбителей двух атомов углерода (рис. 1).
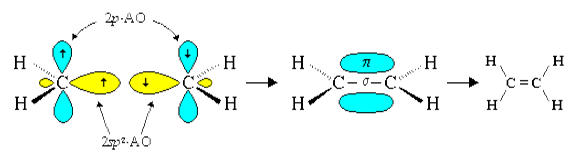
Рис. 1. Строение молекулы этилена.
Пять σ-связей двух sp 2 -гибридизованных атомов углерода лежат в одной плоскости под углом 120 o и составляют σ-скелет молекулы. Над и под этой плоскостью симметрично расположена электронная плотность π-связи, которую можно изобразить также в виде плоскости, перпендикулярной σ-скелету.
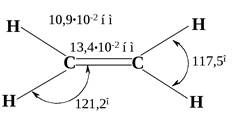
При образовании π-связи происходит сближение атомов углерода, потому что межъядерное пространство в двойной связи более насыщено электронами, чем в σ-связи. Это стягивает атомные ядра и поэтому длина двойной связи (0,133 нм) меньше одинарной (0,154 нм).
Рис. 4.3. Молекула этена:
а - боковое перекрывание 2р-орбиталей (p-перекрывание);
б - p-связь состоит из двух электронных облаков, одно из которых лежит над, а другое – под плоскостью молекулы
Таким образом, двойная углерод-углеродная связь построена из более прочной s-связи (347 кДж/моль) и менее прочной p-связи (260 кДж/моль). p-Связь делает невозможным вращение одного атома углерода относительно другого вдоль связи углерод-углерод. С этим связано явление геометрической изомерии.
Двойная углерод-углеродная связь в этене короче, чем простая связь в этане.
Реакции присоединения.
а) Взаимодействие с водородом (гидрирование)
б) Взаимодействие с галогенами (галогенирование)
обесцвечивание бурой окраски раствора брома в воде служит качественной реакцией на наличие двойной связи.
в) Взаимодействие с галогеноводородами
г) Взаимодействие с водой (гидратация)
Реакции полимеризации.
Полимеризация – соединение небольших молекул мономера в гигантские молекулы полимера:
Дата добавления: 2019-07-15 ; просмотров: 965 ;
Хлор, будучи смешан с метаном, на рассеянном свету постепенно атом за атомом замещает в метане водород, образуя хлорметан, затем дихлорметан, хлороформ и, наконец, четыреххлористый углерод:
CH4 + CI2 CH3CI + HCI
CH3CI + CI2 CH2CI2 + HCI
CH2CI2+ CI2 CH3CI + HCI
CHCI3 + CI2 CCI4 + HCI
В результате реакции образуется смесь продуктов.
Реакция идет длительное время, поэтому для демонстрации ее удобно воспользоваться двухчасовым занятием. Опыт ставят в начале первого урока и привлекают к нему внимание учащихся на втором уроке в связи с повторением и обобщением материала занятия. Можно опыт оставить до следующего дня занятий.
Опыт проводится в двух цилиндрах. Первый цилиндр с пришлифованными краями заполняют метаном по способу вытеснения воздуха. Второй такой же цилиндр заполняют хлором. Затем соединяют цилиндры отверстиями и перемешивают газы, переворачивая их вместе несколько раз. Цилиндры закрывают плотно пробками и один из них оставляют для наблюдения. В нем замечают ослабление окраски хлора вследствие реакции, а иногда и образование жидких веществ в виде маслянистых капель на стенках цилиндра. При открывании цилиндра появляется легкий туман, что подтверждает факт образования хлористого водорода в результате данной реакции.
Второй цилиндр со смесью метана и хлора опускают отверстием вниз в ванну с насыщенным раствором поваренной соли1. (Прибор не оставлять на прямом солнечном свету!) О течении реакции судят по уменьшению объема газовой смеси (уровень жидкости в цилиндре постепенно повышается), по ослаблению окраски хлора и по образованию маслянистых капелек на стенках цилиндра.
Чтобы маслянистые капли были отчетливо видны, цилиндр для смеси газов должен быть предварительно хорошо промыт и высушен.
Так как учащиеся иногда утверждают, что уровень жидкости повышается вследствие частичного растворения в воде метана и хлора, можно одновременно с цилиндром, содержащим смесь газов, погрузить в раствор поваренной соли цилиндр с метаном и цилиндр с хлором (рис. 6). Учащиеся в таком случае увидят, что уровень раствора в этих цилиндрах, в отличие от цилиндра со смесью газов, почти не повышается. Следовательно, метан и хлор в первом цилиндре тратятся на химическую реакцию между ними; образующийся при этой реакции газообразный продукт -- хлористый водород -- значительно лучше растворяется в воде, чем исходные газы.
Опыт можно также поставить, воспользовавшись вместо цилиндров демонстрационными пробирками.
Второй вариант демонстрационного эксперимента иллюстрирующего замещение атомов водорода на хлор в метане может быть осуществлен следующим образом.
Колбу емкостью около 1 л заполняют по способу вытеснения воды смесью метана и хлора (рис. 7). Для этого в нее пропускают вначале метан, затем примерно тройной объем хлора, пока вода полностью не будет вытеснена в стакан. После этого закрывают зажимы а и б и оставляют колбу стоять до тех пор, пока окраска хлора не исчезнет. Тогда открывают зажим б и наблюдают, как вода из стакана устремляется в колбу вследствие образовавшегося в ней разрежения. Если к этой воде предварительно добавить индикатор, то можно заметить изменение окраски под действием образовавшегося хлористого водорода.
Одной из характерных особенностей насыщенных углеводородов является их способность активно вступать в реакцию с таким химическим элементом как хлор. Молекулярный хлор обладает невысокой способностью вступать в реакцию с алканами, поэтому они хлорируются катионами или атомами хлора, обладающими большей активностью. Для осуществления процесса распада хлорной молекулы на атомы необходимо затратить энергию, составляющую 242,8 кДж/моль. Подобная диссоциация может быть легко проведена при обычных температурных условиях под воздействием ультрафиолетового света. В ходе процесса молекула хлора, поглощая ультрафиолет, получает энергию в 293,0 кДж/моль. Реализация термической диссоциации хлорной молекулы на атомы должна происходить в условиях достаточно высоких температур - около 300ºC. Затраты энергии на диссоциацию молекулы для получения ионов хлора составляют порядка 1130,2 кДж/моль. Анализируя энергетические показатели разнообразных вариантов хлорирования можно сделать вывод о том, что наиболее предпочтительным способом хлорирования насыщенных углеводородов является процесс, проводимый на свету.
Процесс хлорирования алканов по сравнению с фторированием представляет собой процесс менее экзотермический, сопровождаемый выделением теплоты в количестве 108,8 кДж/моль. Осуществление хлорирования алканов фотохимическим способом проходит с применением рассеянного света, по причине того, что воздействие прямого света при проведении реакции приводит к взрыву. В ходе реакции хлорирования происходит постепенное замещение в алканах атомами хлора атомов водорода. Для реакций данного вида характерно образование в их результате хлорпроизводных насыщенных углеводородов.
Таким образом, нагревая до 200ºC смесь метана и хлора или подвергая её воздействию ультрафиолетового света, обладающего длиной волны подходящей величины, запускается реакция, сопровождаемая достаточно сильным выделением теплоты:
Для расчёта теплового эффекта, получаемого в ходе хлорирования метана, находящегося в газовой фазе, на первой стадии до состояния CH3Cl и HCl применяется закон Гесса.
Величина суммарного теплового эффекта ∆Hº равна 25 ккал/моль. Рассматриваемые показатели позволяют сделать вывод о полной вероятности проведения процесса хлорирования метана, причём сопровождающий реакцию тепловой эффект никак не связан со скоростью её протекания, определяемой количеством свободной энергии активации.
Радикальный механизм хлорирования метана
Осуществление реакции хлорирования метана, сопровождаемой нагревом и облучением, а также участием в ней инициаторов, способствующих образованию радикалов, реализует механизм радикально-цепного типа SR (Семенов), состоящий из следующих трёх базовых стадий:
инициирования цепи, или её зарождения
рекомбинация или обрыв цепи
Под воздействием света (hv) или под воздействием температуры молекула хлора Cl2 обретает избыточную энергию и переходит в возбуждённое состояние, которое заканчивается её распадом на два атома, являющиеся по своей природе радикалами. Взаимодействие или столкновение атома-радикала хлора с другими молекулами метана CH4 приводит к отщеплению от них водородных атомов, при котором образуется метильный радикал ●CH3. В свою очередь он отщепляет от следующей молекулы атом хлора Cl2 и т.д. Образование одного радикала, таким образом, инициирует многократное повторение стадии, при которой растёт цепь. Для протекающей реакции длина кинетической цепи определяется в соответствии с количеством подобных повторений. Для процесса хлорирования число повторений может достигать 10 и более тысяч.
Энергетическая диаграмма взаимодействия метановой молекулы и атома хлора изображена на рисунке.
Закономерности радикального хлорирования метана
Согласно общетеоретическим положениям, взаимодействие атомов хлора и молекулы метана будет происходить исключительно в случае равенства их свободной энергии величине энергии активации (или энергетического барьера), составляющего 16,7 кДж/моль. Сама по себе свободная энергия, как правило, немного больше простой разницы между энергией разрыва существующей в молекуле связи C–H (+425 кДж/моль), и образования связи нового вида H-Cl (-431 кДж/моль), которая составляет -6 кДж/моль. По этой причине взаимодействие реагирующих частиц запускается не каждым столкновением между ними, а только обладающими достаточной энергией для преодоления барьера.
Возникновение дополнительной активационной энергии связано с нагревом либо облучением молекул. В возбуждённом состоянии молекулы движутся с достаточно высокой скоростью, что позволяет при столкновении превратить их кинетическую энергию в энергию потенциальную. В переходном состоянии ПС1, соответствующем первой вершине кривой энергетической диаграммы, практически одновременно происходят разрыв старых связей C-H и образование связей нового вида H-Cl в активированном комплексе, который сформировался. Метильный радикал, образуемый в ходе реакции, обладает достаточной потенциальной энергией и впоследствии взаимодействует с молекулой хлора Cl2 сравнительно легко. Энергия, необходимая для активации данной стадии относительно не высока и составляет всего 2 кДж/моль. Окончательное образование соединения CH3Cl осуществляется в находящемся в переходном состоянии ПС2 активированном комплексе, сформировавшемся повторно.
Процесс хлорирования алканов и метана в частности, протекающий при температурах такой величины, представляет собой процесс, плохо поддающийся управлению. Обычно он не прекращается на стадии формирования соединения хлористого метила CH3Cl и способен протекать далее с получением промежуточных соединений – хлористого метилена, хлороформа и тетрахлорометана.
Ионный механизм хлорирования метана
Реакция хлорирования, осуществляемая в кислой среде в присутствии способствующих её протеканию по ионному механизму катализаторов (ими обычно являются кислоты Льюиса SbF5, AlCl3), обладает электрофильным характером (Se). Сущность процесса реагирования молекулы хлора с электроноакцепторного хлорида алюминия, в химическом плане, состоит в значительной поляризации связи C-C, являющейся до этого неполярной, приводящей к образованию электрофильного агента после её диссоциации. При отсутствии катализаторов хлорирование, происходящее по ионному механизму, практически не может осуществляться, по причине того, что для гетеролитического расщепления на анион и катион молекулы хлора необходима значительная энергия – порядка 1130 кДж/моль.
Цепной ионный электрофильный механизм (Se), по которому осуществляется хлорирование в присутствии катализаторов насыщенных углеводородов, изображен на рисунке:
Под воздействием катализатора происходит гетеролитический распад молекулы хлора, сопровождаясь возникновением ионной комплексной пары [AlCl4] – Cl +, из-за того, что алюминий соединён с атомами хлора, имеющими отрицательный электрический заряд, и нуждается в электронах. По этой причине алюминием от атома хлора Cl2 отщепляется пара электронов, сопровождаясь одновременным образованием катиона хлора, взаимодействующего впоследствии с молекулой метана гетеролитично разрывая связь C-H. Результатом данного процесса является образование метильного карбкатиона, который затем реагирует с хлорной молекулой, образуя, в конце концов, хлористый метил и катион хлора, взаимодействующий впоследствии со следующей молекулой. Ионные реакции, у которых промежуточными частицами являются ионы с положительным зарядом, имеют название реакций электрофильных.
По причине того, что для диссоциации хлорных молекул на ионы необходима значительная энергия, хлорирование углеводородов в насыщенном состоянии в присутствии катализаторов должно сопровождаться нагревом реакционной смеси.
Насыщенные углеводороды активно вступают в реакцию с хлором. Хлорируют алканы атомами или катионами хлора, которые более реакционноспособны, чем молекулярный хлор. Диссоциация молекулы хлора на атомы требует затраты 242,8 кДж/моль энергии. Такая диссоциация хлора легко происходит при обычной температуре под действием УФ-света, поглощение которого молекулой придает ей 293,0 кДж/моль энергии. Для термической диссоциации молекулы хлора на атомы необходима температура около $300^\circ \ C$ . Диссоциация молекулы хлора на ионы требует затраты 1130,2 кДж / моль. Из приведенных энергетических данных видно, что насыщенные углеводороды легче хлорировать на свете.
Хлорирование алканов происходит с выделением 108,8 кДж / моль теплоты и является менее экзотермическим процессом, чем фторирование. Фотохимическое хлорирование алканов проводят при рассеянном свете, поскольку при прямом освещении реакция происходит со взрывом. При хлорировании атомы водорода алканов постепенно замещаются на хлор. В результате образуются хлоропохидни насыщенных углеводородов.
- Курсовая работа Хлорирование метана 410 руб.
- Реферат Хлорирование метана 250 руб.
- Контрольная работа Хлорирование метана 230 руб.
Итак, если смесь метана с хлором нагреть до $200^\circ \ C$ или воздействовать на неё УФ-светом подходящей длины волны, протекает сильно экзотермическая реакция:
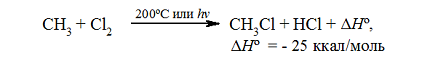
Рисунок 1. Хлорирование метана
Тепловой эффект первой стадии хлорирования метана в газовой фазе до $CH_3Cl$ и $HCl$ может быть рассчитан на основании закона Гесса.
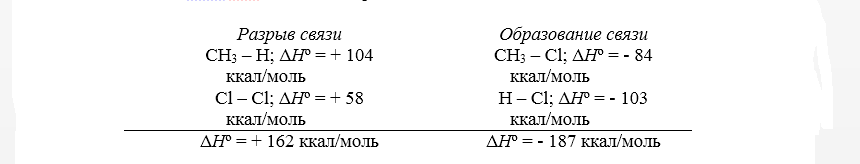
Рисунок 2. Хлорирование метана
Суммарный тепловой эффект $\Delta \underline
Задай вопрос специалистам и получи
ответ уже через 15 минут!
Радикальный механизм хлорирования метана
Хлорирование алканов при нагревании, облучении и в присутствии радикалообразующих инициаторов происходит радикально-цепным механизмом $SR$ (Семенов) и состоит из трех основных стадий:
зарождение цепи (инициирование)
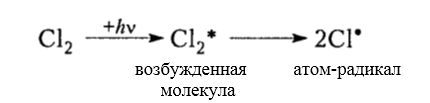
Рисунок 3. Хлорирование метана
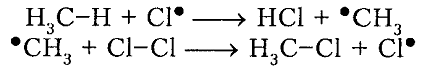
Рисунок 4. Хлорирование метана
обрыв цепи (рекомбинация)
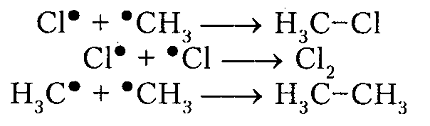
Рисунок 5. Хлорирование метана
Итак, молекула хлора $Cl_2$ под действием света ($h \nu $) или при нагревании получает избыток энергии, становится возбужденной и распадается на два атома, которые по своей природе являются радикалами. Атом-радикал хлора в процессе столкновений или взаимодействия с другими молекулами отщепляет атом водорода от молекулы метана $CH_4$ с образованием метильного радикала $^*CH_3$. Метательный радикал, в свою очередь, отщепляет атом хлора от следующей молекулы $Cl_2$ и т.д. Таким образом, один образованный радикал инициирует много повторений стадии роста цепи. Количество таких повторений определяет длину кинетического цепи всей реакции, для хлорирования может достигать $10 \ 000$ и более.
На рис. 6 показана энергетическая диаграмма хлорирования метана.
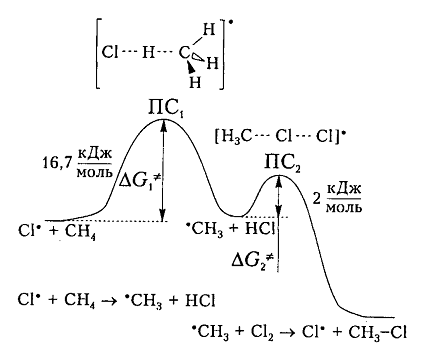
Рисунок 6. Диаграмма изменения свободной энтальпии для взаимодействия атома хлора и молекулы метана
Закономерности радикального хлорирования метана
Исходя из общетеоретических соображений атом хлора и молекула метана будут взаимодействовать между собой только тогда, когда их свободная энтальпия будет равна величине энергетического барьера (и энергии активации) 16,7 кДж / моль, которая всегда немного больше, чем просто разница (-6 кДж / моль) энергий разрыва старой связи $C-H$ (+425 кДж / моль) и образования новой связи - связи $H-Cl$ (-431 кДж / моль). Поэтому не каждое столкновение реагирующих частиц вызывает их взаимодействие, а только те, которые достаточны для преодоления этого барьера.
Дополнительная энергия активации возникает благодаря облучению или нагреву молекул. Возбужденые молекулы проявляют достаточно высокие скорости движения, кинетическая энергия которого и превращается в потенциальную энергию при столкновениях. На вершине кривой в переходном состоянии $ПС_1$ между реагирующими компонентами образуется активированный комплекс, в котором разрыв старого связи $C-H$ и формирования новой $<\rm H>-Cl$ происходят примерно одновременно. Образованный метательный радикал имеет достаточную потенциальную энергию и относительно легко взаимодействует с последующей молекулой $Cl_2$. Энергия активации этой стадии составляет всего 2 кДж / моль. Формирование конечного соединения $CH_3Cl$ проходит через стадию второго активированного комплекса с переходным состоянием $ПС_2.$
Хлорирование метана и других алканов при таких температурах - плохоуправляемый процесс, который обычно не останавливается на стадии образования хлористого метила $CH_3C1$ и может происходить дальше:
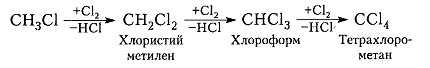
Рисунок 7. Хлорирование метана
Ионный механизм хлорирования метана
В присутствии катализаторов ( кислот Льюиса $A1C1_3$, $SbF_5$), способствующих ионному механизму реакции, процесс хлорирования в кислой среде имеет электрофильный характер ($Sе$). Химизм взаимодействия електроноакцепторного хлорида алюминия с молекулой хлора заключается в значительной поляризации неполярной связи $C-C$, что вызывает её диссоциацию с образованием электрофильного агента. Без таких катализаторов реакция хлорирования по ионному механизму почти не происходит, поскольку гетеролитических расщепления молекулы хлора на катион и анион требует значительной энергии (1130 кДж / моль).
Хлорирование насыщенных углеводородов при наличии катализаторов, происходит цепным ионным електрофильным механизмом ($Se$):
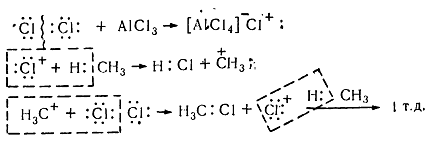
Рисунок 8. Хлорирование метана
Молекула хлора при воздействии катализатора распадается гетеролически с образованием комплексной ионной пары $[A1Cl_4]-Cl+$, поскольку алюминий соединен с электроотрицательными атомами хлора и имеет потребность в электронах. В связи с этим он отщепляет от молекулы $Cl_2$ атом хлора с парой электронов. При этом одновременно образуется катион хлора, который затем взаимодействует с молекулой метана и гетеролитично разрывает связь $C-H$. Такое взаимодействие приводит к образованию метильного карбкатиона. Последний дальше вступает в реакцию с молекулой хлора и образует хлористый метил и катион хлора, реагирует с другой молекулой метана. Такие ионные реакции, в которых промежуточными частицами являются положительно заряженные ионы, называют электрофильными.
Хлорирование насыщенных углеводородов при наличии катализаторов проводят при нагревании реакционной смеси, поскольку диссоциация молекулы хлора на ионы требует значительной затраты энергии.
Так и не нашли ответ
на свой вопрос?
Просто напиши с чем тебе
нужна помощь
Читайте также:

