Заключение о раке кишечника
Александр Владимирович Воробей, 64 года, окончил Минский мединститут, интернатуру по хирургии. Завкафедрой хирургии БелМАПО, член-корреспондент НАН, доктор медицинских наук, профессор, главный внештатный проктолог Минздрава РБ. Член Международной ассоциации университетских колоректальных хирургов; Всемирной ассоциации хирургов, гастроэнтерологов и онкологов; Европейской медицинской лазерной ассоциации; почетный член ассоциации хирургов-гепатологов России и стран СНГ ; член Правления Белорусской ассоциации хирургов. Председатель аттестационной комиссии МЗ РБ по хирургии и экспертного совета ВАК Беларуси по хирургии.
- Александр Владимирович, рак толстой кишки выходит в Беларуси на первое место, в мире ежегодно диагностируют 600 миллионов новых случаев. В чем причина?
- Влияет урбанизация, особенности питания: много мяса, особенно прожаренного, отсутствие клетчатки - банальные вещи. В Африке , где живут в основном на фруктах и овощах, этих заболеваний гораздо меньше. А цивилизованный мир любит мясо, гриль - гастроэнтерологи уже считают его вредным.
У нас заболеваемость этим видом рака выше, чем у ряда европейских стран. На 9,5 миллиона белорусов почти 5,5 тысяч новых случаев (за 2017 год. - Ред.) - это огромная цифра.
Плюс масса пациентов, которые продолжают лечение. Толстая кишка состоит из ободочной и прямой - в среднем это 1,5 метра. На I - III стадиях выявляется всего 52% случаев. Пятилетняя выживаемость на этих операбельных стадиях около 60%, а при запущенном раке пятилетняя выживаемость - 8%. Раньше этой патологии было меньше, мы выявляли ее поздно: если брать времена конца СССР , запущенных случаев было 60%.
- Поздно - потому что колоноскопии не было?
- В 80-е годы ее только учились делать. Я застал эту ситуацию, придя в нашу областную больницу. Был один колоноскоп, он был большего диаметра, чем теперешние, не очень удобный, картинка выводилась на экран не очень качественно.
Сегодня аппараты цифровые, есть технологии усиливающей колоноскопии - врачу проще увидеть проблему и более прицельно взять анализ для биопсии.
Залог улучшения 5-летней выживаемости - это раннее выявление опухоли. А усиливающая эндоскопия дает возможность увидеть образование на ранней стадии - еще плоское и не выступающее над поверхностью кишки.
У нас постепенно идет переоснащение с устаревших волоконно-оптических колоноскопов на цифровые. Есть эндоскопы высокого разрешения с зум-увеличением на экране монитора - как у современного фотоаппарата. Кроме того, есть возможность проведения виртуальной окраски слизистой с помощью различных технологий. Но, к сожалению, такие аппараты пока единичные в стране.
- Не проблема обезболить - проблема, скорее, в анестезиологах, в выделении дополнительных ставок для тех из них, которые будут обеспечивать обезболивание только на эндоскопиях. Это чисто материальный вопрос. 10-я и 2-я клиники Минска уже добились, что у них каждая колоноскопия идет с обезболиванием.
У нас в Минской областной больнице проблему решили отчасти - с обезболиванием идут процедуры в понедельник и пятницу. Человеку вводят седативный препарат, и он не так остро реагирует на процесс, состояние можно назвать легким сном. В это время возле пациента должны находиться анестезиолог и медсестра, поскольку любой наркоз может дать осложнение.

-Есть малые признаки опухоли толстой кишки: потливость, слабость, урчание в животе, потеря интереса к жизни. Это малые признаки любой опухоли. Человеку стало неинтересно жить - в организме уже может идти болезнь. Фото: Святослав ЗОРКИЙ
- Рак толстой кишки - один из медленно растущих раков. От первой клетки до видимой эндоскопом опухоли может пройти от двух до четырех лет.
- Как человеку понять, что у него проблема?
- Самое первое - любые нарушения нормального пищеварения: началось повышенное газообразование, урчание в животе, изменение стула, запоры, поносы. У пожилых людей и так есть склонность к запорам - так вот на фоне запоров появилось что-то новое: острые боли, еще тяжелее оправляться, появилась кровь. Кровь в кале важно не списывать на геморрой. После 40 лет он у многих, и это повод для ошибок - люди долго не подозревают, что это не геморрой, а запущенный рак. Должно тревожить появление в кале слизи - беловатого желе, как вареный крахмал. Это один из ярких симптомов либо большого полипа - предрака, либо опухоли левой половины толстой кишки.
- Слизь может быть признаком дисбактериоза кишечника?
- И это тоже повод для ошибок, лучше перестраховаться. Еще симптомом опухоли толстой кишки может быть анемия. Но у нас есть и примеры, когда у пациента тяжелейшая опухоль с метастазами, а анализ крови в норме. Хороший анализ крови при появившихся нарушениях пищеварения - повод не для спокойствия, а для колоноскопии. Есть малые признаки опухоли толстой кишки: потливость, слабость, урчание в животе, потеря интереса к жизни. Это малые признаки любой опухоли. Человеку стало неинтересно жить - в организме уже может идти болезнь.
Это медленно развивающийся рак, и умереть до развития непроходимости почти никому не удается. Человек с дикими болями, с огромным животом и крайне запущенным раком все равно придет в больницу. А оперировать уже поздно и помочь невозможно.
- Это те случаи, когда отрезанную кишку выводят в бок с калоприемником?
- Да, это та ситуация. При запущенной опухолевой непроходимости не идет речь об органосохраняющих операциях - задача попытаться спасти жизнь. И это уже удается плохо: при запущенной непроходимости до 80% пациентов умирают после операции. Но когда человек приходит своевременно, если нет метастазов, иногда достаточно одной операции: удаляем опухоль, восстанавливаем кишечную проходимость - и все. При необходимости, как и во всем мире, делаем пластические операции на толстой кишке.
- Тогда зачем калоприемник?
- Есть ситуации, когда необходимо удалить задний проход вместе с опухолью. Мы пытались, как и многие страны, воссоздавать из мышц бедра искусственный сфинктер, но эффективность таких операций невысокая. В хирургии толстой кишки позиция такая: если сохранен хотя бы задний проход длиной в несколько сантиметров и его сфинктеры - принципиально возможно восстановить кишечную проходимость и не иметь стому.
- Были в вашей практике случаи, когда люди сами себе сильно вредили?
- Был у меня пациент - умнейший человек, крупный строитель, я знаю всю его семью. Еще в 80-е мы выявили у него опухоль, еще не было кишечной непроходимости, но он решил, что его огромная сила воли в сочетании с таинственными упражнениями победят рак. Кончилось как у всех - метастазами, когда оперировать было поздно.
- Правда, что часто раком болеют целые семьи?
- Слышала, что иногда семьи болеют раком негенетическим.
- Да, есть так называемый семейный раковый синдром - по необъяснимым причинам в конкретной семье раки возникают чаще, причем разные. Был пациент из Борисова , в 30 лет у него диагностировали рак прямой кишки. В 28 лет такой же рак возник у его сына. И генетики тут нет - это подтвердила наша лаборатория. Но есть особенность семьи: может, питания, может, что-то есть такое в жилище - никто не знает.
- При боязни кононоскопии можно для начала сделать УЗИ органов брюшной полости. Совсем маленькую опухоль не увидят, но есть так называемый симптом полого органа - и это подозрение на рак толстой кишки.
- А онкомаркеры для рака толстой кишки информативны?
- Да, можно начать с этого. Это не 100% диагностика, но сигнал для пациента. Есть маркер РЭА (раково-эмбриональный антиген), если результат больше 5 - это повод для беспокойства. Есть и так называемая виртуальная колонография, ее делают в компьютерном томографе (без введения каких-либо аппаратов в толстую кишку), где есть специальная программа для обследования кишечника.
- Где лучше делать колоноскопию?
- В частных центрах нередко работают специалисты стационаров, по совместительству. Главное - выбирайте колоноскопию с усиливающей эндоскопией, не во всех аппаратах она есть.
- Есть страх, что во время колоноскопии удалят полип, и это даст толчок раку…
Считалось, что если размер полипа меньше сантиметра - он доброкачественный. Первыми забили тревогу японцы - даже в 5-миллиметровых полипах могут быть раковые клетки. Любой полип нужно немедленно удалять и сдавать на исследование - чтобы исключить ранний рак. В раннем отщипывании полипов не опасность, а профилактика рака.
Еще один повод для возникновения рака анального канала - длительно существующие анальные трещины или свищи. Это хронические воспаления, которые рано или поздно приведут к раку, в данном случае - к раку кожи. Если такой пациент долго не обращается к врачу, то почти безобидная болезнь превращается в рак перианальной области - они плохо протекают и имеют высокую смертность.

- Не проблема обезболить - проблема, скорее, в анестезиологах, в выделении дополнительных ставок для тех из них, которые будут обеспечивать обезболивание только на эндоскопиях. Фото: Святослав ЗОРКИЙ
- Сколько лет было самому молодому вашему пациенту?
- 18 лет, парнишка из Гомеля . На разных этапах ему долго ставили болезнь Крона (воспалительная болезнь кишечника), а у него была огромная опухоль прямой кишки.
- Почему не диагностировали вовремя?
- Потому что 18 лет - всем хотелось думать, что в таком возрасте рака толстой кишки не бывает. И ему долго не делали полнослойную биопсию (исследование подозрительных тканей прямой кишки).
- С возрастом обмен веществ замедляется. Посоветуйте - как поддержать работу кишечника?
- Нужно менять образ жизни, следить за питанием, есть побольше овощей, фруктов, клетчатки. Полезно делать себе массаж живота - поглаживая круговыми движениями по часовой стрелке. И не нужно слишком всего бояться, важно вовремя обследоваться. Страхов много, например, у молодых женщин с полипозами, после наших операций.
ЧИТАЙТЕ ТАКЖЕ
О таком докторе для своего ребенка мечтает каждая мама. Только вот встретиться с ним - недетский труд даже для журналиста [продолжение здесь]
Уролог Антон Главинский: На приеме у уролога жена узнает про мужа много интересного!
Узнали, как ЗОЖ мужа мешает наступлению беременности, всегда ли можно сказать, кто первый заболел, почему частенько мужчина с любовницей может, а с женой – нет и как укрепить брак [продолжение здесь]
В последние десятилетия заболеваемость колоректальным раком выросла в разы. Если сравнивать ситуацию с 60-ми гг. прошлого века, то рак прямой кишки тогда составлял 1,2 % от всех злокачественных опухолей, рак ободочной кишки – 1,8 %. В 2017 г. статистика выглядит уже так: 5,2 % и 7,3 %, соответственно.
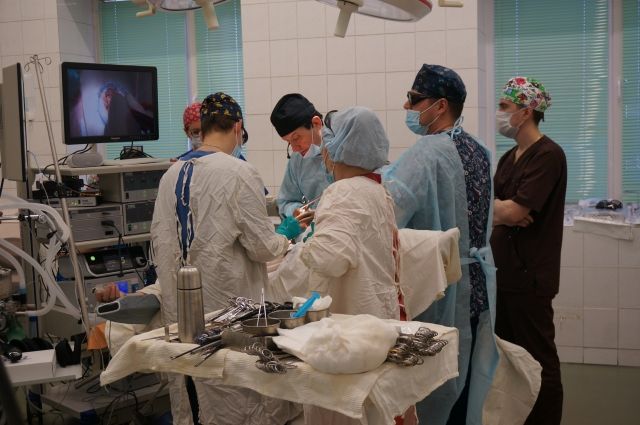
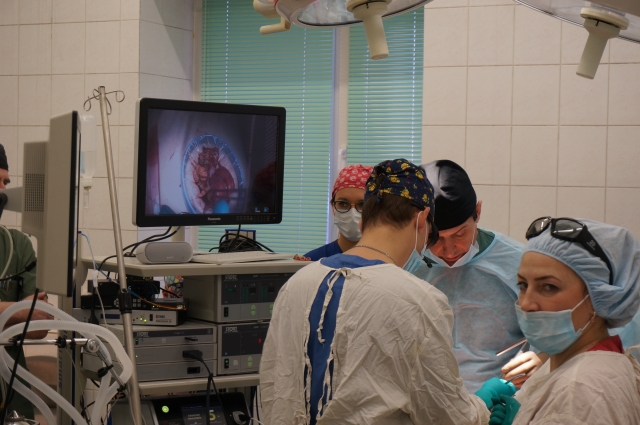
На днях в Пермском краевом онкологическом диспансере 74-летней пациентке сделали лапароскопическую операцию по удалению большой правосторонней опухоли кишечника. На хирургическое вмешательство, которое транслировали на экране в 3D-изображении, пригласили не только врачей-онкологов, но и журналистов.
Где чаще болеют?
Результат питания деликатесами – это частые запоры. И лечение недуга – одна из проблем современного здравоохранения. Это становится настолько актуальным, что в странах, где хорошо развит туризм, уже учитывают этот факт. В отелях гостям на завтрак обязательно предлагают распаренный чернослив, курагу, инжир.

Факторы риска
Запоры являются основным из факторов риска онкологических заболеваний. Если кишечник опорожняется ежедневно и своевременно, то канцерогенные газы и каловые массы не успевают активно воздействовать на его слизистую оболочку. А в случае запоров концентрация и время воздействия шлаков на слизистую толстой и прямой кишки увеличивается.
Ещё один фактор риска рака кишечника – хронические колиты, когда воспалительный процесс проявляется сменой запоров и поносов. Человек испытывает дискомфорт и болевые ощущения в животе, у него нередки вздутия и бурления. Есть случаи, когда повышается температура.
Ещё к группе риска относятся те, у кого есть наследственное заболевание – семейный полипоз. Ведь злокачественная опухоль может развиться и из полипа. Если у кого-то из родных заболевание было, нелишним будет обратиться к врачу и пройти плановое обследование.
Мужская или женская проблема?
Исходя из опыта, злокачественная опухоль кишечника чаще встречается у женщин, чем у мужчин. Несмотря на то что женщины внимательнее следят за здоровьем, обнаружить рак прямой и ободочной кишки на ранних стадиях удаётся нечасто. И это общая проблема выявления онкологических заболеваний: на ранних стадиях они протекают бессимптомно. Поэтому многие пациенты приходят к врачам в лучшем случае на второй, а иногда и на третьей стадии рака.
Немалый процент заболевших обращается лишь тогда, когда у них обнаруживают четвёртую стадию болезни. Человек идёт к медикам по другой проблеме. Его беспокоят сильные боли в печени или непрекращающийся кашель, а обследование обнаруживает у него метастазы в лёгких и печени.
Врачи начинают искать первопричину и нередко обнаруживают рак толстой и прямой кишки. Когда начинают подробно расспрашивать пациента о самочувствии, выясняют, что проблемы были давным-давно, но с обращением к доктору он тянул до последнего.
Выявить рак на ранних стадиях, говорят медики, нередко можно в ходе обычной диспансеризации в поликлинике, ведь в общий осмотр обязательно входит пальцевое обследование прямой кишки. Другое дело, что пациенты сами нередко отказываются от проведения такой диагностики.
Какие симптомы должны насторожить?
Признаков колоректального рака немного, но если они есть, то стоит своевременно записаться к врачу.
Что должно насторожить? Для рака правой половины ободочной кишки характерно необоснованное повышение температуры. Она может подняться и держаться несколько дней, потом становится нормальной, а через какое-то время ситуация снова повторяется.

Следующие симптомы – это ложные позывы, когда после опорожнения кишечника нет ощущения, что он пустой. Также пациента могут беспокоить точечные боли в правой половине живота. Это проявление развившегося воспаления на фоне злокачественной опухоли. Бывает, что опухоль справа иногда может прощупать и сам пациент, и врач.
При раке правой стороны кишечника не бывает непроходимости, пациента беспокоят ноющие боли, а при раке левой стороны, к сожалению, может развиться острая кишечная непроходимость. С резкой острой приступообразной болью люди попадают в экстренные хирургические отделения, и уже на операции у них обнаруживают опухоль.
Что делает врач?
Прежде всего узкий специалист-онколог проведёт пальцевое исследование прямой кишки. Это исключит геморрой и наличие полипов. Дальше он сам будет выстраивать методику обследования и лечения. Чаще, чтобы подтвердить диагноз, назначают обычное для таких заболеваний обследование – ректоскопию и колоноскопию.

Многих волнует вопрос: как быстро развивается рак прямой кишки? По мнению врачей-онкологов, все злокачественные опухоли развиваются от трёх до десяти лет до начала клинических проявлений. Поэтому любому заболеванию, когда его выявят, будет минимум три года. А вот за сколько времени процесс разовьётся от первой до четвёртой стадии, вам не скажет ни один врач. В этом вопросе всё индивидуально и зависит от уровня злокачественности опухоли, иммунитета человека и от множества других показателей.
Как проводят операцию?
Эндоскопические (через прокол) операции по удалению рака прямой кишки – более щадящие. Они позволяют пациенту быстрее покинуть хирургическое отделение и начать лечение, которое назначил врач. Однако эндоскопические операции делают в Пермском крае не так часто, как полостные.
В ряде случаев у прооперированных пациентов случаются рецидивы. Пусковым механизмом проявления метастазов могут стать стрессовые ситуации, которые происходят с человеком: тяжело заболел гриппом, потерял близкого человека, уволили с работы, ограбили. В такой период у человека снижается уровень иммунного ответа и иммунной защиты, и раковые клетки начинают быстрее размножаться и проявляться как отдалённые метастазы.
От 50 до 60 % прооперированных больных колоректальным раком первой-третьей стадии переживают пятилетний рубеж. Статистика такова: если рак прямой кишки удалили на первой стадии – то более 80 % пациентов живут дольше пяти лет, на второй – 70 %, на третьей – 50 % и ниже.
Если говорить о профилактике рака, то всем кажется: не ешь одного, не пей другого, и будет тебе счастье. Однако первичной профилактики в онкологии не существует. Тем более от рака нельзя поставить прививку, как, например, от гриппа или кори. Однако прислушаться к организму и своевременно обратиться к врачам при перечисленных выше симптомах вам обязательно стоит!
К.м.н. И.С. Базин, профессор А.М. Гарин, С.А. Жарков, к.м.н. М.Н. Нариманов
Российский онкологический научный центр им. Н.Н. Блохина РАМН
Статистические аспекты, вопросы канцерогенеза и факторы прогноза
Ежегодно в мире регистрируются 600 тыс. новых больных раком толстой кишки (РТК), половина из них умирает [1].
Отмечается рост заболеваемости в большинстве стран. Заболеваемость РТК в России с 1990 по 2000 год возросла у мужчин при раке ободочной кишки на 18,7%, прямой – 16,2%, а у женщин прирост составил 18,9 и 6,6% соответственно.
В России ежегодно регистрируется более 40 тыс. новых случаев рака толстой кишки (за 2000 год 47530 – первичных больных, умерло 34341 пациентов) [2].
До 6% пациентов от общего числа заболевших имеют наследственную природу болезни. Наследственный РТК включает в себя семейный неполипозный РТК (синдром Линча), а также рак, возникший из наследственных аденоматозных и гамартомных полипов.
Более чем у 90% больных возникает спорадический рак толстой кишки. К самым большим достижениям фундаментальной науки следует отнести идентификацию генетических изменений при спорадическом раке толстой кишки, которая дала возможность приступить к разработке генной терапии этого заболевания.
Впервые модель канцерогенеза РТК была представлена в литературе в 1988 году [3,4]. Ген АРС (аденоматозного полипоза кишки) ответственен за развитие аденом у больных семейным полипозом. Мутация этого гена (потеря аллели в 5–й хромосоме) ведет к гиперпролиферации нормального эпителия. При наследственном РТК потеря аллели в 5–й хромосоме не наблюдается никогда, при спорадическом ненаследственном РТК она отмечается у 30–50% больных.
Образование ранних аденом – второй этап в развитии РТК – связывают с мутированным колоректальным раковым геном ММС (ген, участвующий в передаче сигнальной трансдукции) и метилированием ДНК [5]. Метилирование ДНК необходимо для регуляции экспрессии генов и важно для метаболизма цитозин нуклеотидов.
Потеря аллели в 18 хромосоме отмечается у 70% больных РТК и 50% больных с поздними аденомами. Потерянная аллель обычно содержит ген DCC (D от слова deleted – потерянный, СС – рак ободочной кишки). DCC – это супрессорный ген, ответственный за процессы клеточной адгезии. Снижение экспрессии гена DCC ведет к метастазированию [9,10]. При развитии РТК важную роль выполняет и ген Р–53. Мутации этого супрессорного гена, тормозящего клеточную прогрессию и трансформацию, приводят к потере контроля над процессом пролиферации [11,12].
Замещение или подавление мутированных генов ras, MMC, P–53 восстановление гена DCC и т.д. – являются вполне достижимыми целями будущего лечения больных РТК.
Возраст – основной фактор риска развития РТК у здорового человека. Так, заболеваемость РТК у 40–летних составляет 8 заболевших, у 60–летних – 150 на 100 тыс. населения.
Доказано, что риск возникновения РТК у лиц, не имеющих предрасполагающих обстоятельств, составляет 1–3%; если у родственников 1–го порядка был РТК, риск повышается до 5%, среди больных язвенным колитом риск развития РТК равен 15–30%; среди пациентов с болезнью Крона – 15%, с неполипозным наследственным колоректальным раком – 15–20%; наследственным семейным полипозом 30–100% [13]. Данные группы риска должны подвергаться обязательным профилактическим осмотрам, что в ряде случаев способствует раннему выявлению РТК. Американское раковое общество рекомендует лицам старше 50 лет пройти тестирование на скрытую кровь и раз в год подвергаться сигмоскопии.
Поскольку РТК часто возникает метахронно, больные, леченные хирургически по поводу РТК, также должны рассматриваться, как группа риска – на предмет возникновения второй опухоли в кишечнике.
Наиболее известный маркер РТК – карциноэмбриональный антиген (СЕА) [15]. Диагностическое и прогностическое значение карциноэмбрионального антигена обсуждается с середины 80–х годов [16,17]. Карциноэмбриональный антиген отнюдь не обязательный маркер – у 40% больных РТК он не выявляется. Этот маркер нельзя назвать и специфическим, поскольку он обнаруживается и при других злокачественных опухолях (раке молочной железы, поджелудочной железы, легкого, яичников и даже саркомах), а также в эмбриональной ткани и незлокачественных заболеваниях (гепатотоксичность, гидронефроз, желчекаменная болезнь) [18].
Высокие цифры СЕА после операции являются признаком нерадикальности последней, возможного рецидива, короткой выживаемости. После радикальных хирургических операций систематическое определение СЕА позволяет выявить в 47% случаев рецидивы, в том числе и бессимптомные [19,20].
Американской гастроэнтерологической ассоциацией в 1989 году сформулирован консенсус по вопросам послеоперационного ведения больных РТК. Его порядок представлен в таблице 1 [21].
Информативным считается уровень СЕА в плазме более 10 ng/ml.
Маркер Са–19–9 имеет прогностическое значение при РТК. Если его уровень превышает 37 ед/мл, риск смерти в течение 3 лет после операции увеличивается в 4 раза по сравнению с теми, у кого этот показатель был отрицательным или более низким [22].
При РТК в 28% случаев экспрессируются цитокератинные антигены (СК 17 и 18). Больные, у которых обнаружена экспрессия этих антигенов, имеют наихудший прогноз выживаемости [23]. Вместе с тем цитокератинные антигены стали мишенью для моноклональных антител. В рандомизированном исследовании радикально оперированные пациенты получали раз в месяц адъювантно мышиные антитела против цитокератинного антигена 17 либо плацебо.
Муцинозные гликопротеины экспрессируют сиалозил –Тn антиген (Sialosyl–Tn). У 86% больных РТК определяется этот маркер. Те, у кого его нет, выжили 5 лет в 100% случаев, пятилетняя выживаемость больных с положительным сиалозил Тн маркером составила 73% [25].
Самой частой формой РТК является аденокарцинома тубулярной или ворсинчатой структуры – 95%. Другие варианты составляют всего 5% (это перстневидноклеточный рак, плоскоклеточный рак, аденоплоскоклеточный рак, мелкоклеточный рак и недифференцированный рак) [26].
Главным прогностическим фактором является стадия рака толстой кишки в момент первичной диагностики. К другим прогностическим факторам относят: возраст, пол, симптомность, наличие опухолевых осложнений, инвазию нервов и сосудов, число пораженных лимфоузлов, степень дифференцировки, высокие цифры ЛДГ и числа лейкоцитов в крови, плоидность ДНК, холецистэктомию в анамнезе, облучение таза в анамнезе. Остановимся на наиболее важных из них.
Чем моложе пациент, тем хуже прогноз [27]. У женщин прогноз лучше, чем у мужчин [28]. Наличие симптомов рака толстой кишки при постановке диагноза усугубляет прогноз. Бессимптомные больные (со случайной диагностикой) живут 5 лет в 71% случаев; больные, имевшие симптомы болезни до первичного диагноза, переживают пять лет в 49% случаев [29]. Наличие опухолевых осложнений (перфорации или непроходимости) ухудшает прогноз. Пятилетняя выживаемость в Дании среди имевших эти осложнения РТК (219 больных) составила 23%, а больных без этих осложнений (732 пациента) – 35% [30].
Опухоли толстой кишки получают потенциал метастазирования после прорастания подслизистого слоя кишечника, богатого лимфатическими сосудами [31]. Если опухоль не прорастает все слои кишечника, метастазы в лимфоузлы обнаруживаются лишь в 10%, если пенетрируется серозная оболочка – в 60% [32]. Если в лимфоузлах обнаруживается реактивная гиперплазия – это хороший прогностический признак [33].
При прорастании серозной оболочки, покрывающей частично прямую кишку и большую часть ободочной кишки, возможна диссеминация по брюшине [34].
Метастазы в печени обнаруживаются на секционном материале в 40% случаев, рак толстой кишки после метастазирования в печень может широко диссеминироваться по органам и тканям – легкие, кости и т.д.
Лечение рака толстой кишки
Главным методом лечения РТК остается хирургическая операция. Ее принципы не изменились за много лет и состоят: в удалении опухоли с проксимальным и дистальным запасом неизмененной кишки для элиминации подслизистого лимфатического распространения клеток; удалении региональных брыжеечных лимфоузлов; визуальном интраоперационном стадировании болезни; стремлении минимизировать постхирургические функциональные нарушения.
По современным данным, резектабильность рака ободочной кишки составляет 70–80%, послеоперационная летальность до 5%. Общая пятилетняя выживаемость варьирует от 50 до 70% в разных центрах.
Результаты хирургических операций при раке ободочной кишки в первую очередь зависят от вовлеченности в опухолевый процесс лимфоузлов и стадийности по Dukes.
При негативных лимфоузлах и Dukes A 5 лет выживают 90%, когда нет метастазов в лимфоузлах, но когда опухоль прорастает мышцу (Dukes B), выживают этот срок 80%, при Dukes C этот показатель снижается до 60%.
Если во время операции были удалены пораженные раковой опухолью лимфоузлы, пятилетняя выживаемость различается в зависимости от степени инвазии опухолью стенки кишки – 74% (Dukes A), 48% (Dukes B) – 30% (Dukes C) [36].
Результаты хирургического лечения рака прямой кишки также зависят от вовлеченности лимфоузлов и классификации по Dukes. Считается, что выживают 5 лет 50% больных. Локальные рецидивы возникают у 10% (обычно в первые 2 года).
Особое место занимает хирургия диссеминированных больных. На первом месте стоит хирургическое лечение метастазов в печень. После удаления одиночных метастазов в печень, 5–летняя выживаемость составляет 25%. Перспективной технологией является коагуляционная гипертермия метастазов (Radiofrequency, RF). Чрескожно или интраоперационно в центр метастаза вводится электрод, связанный с радиочастотным генератором.
В практику хирургии РТК вошли эндоскопические операции, сокращающие сроки пребывания пациентов в больнице, уменьшающие частоту некоторых осложнений. Вместе с тем метод ограниченно позволяет ориентироваться в брюшной полости (исключена возможность пальпации). Операции длительны даже в руках опытных хирургов, нередки случаи неадекватного удаления лимфоузлов [39].
Улучшить результаты хирургического лечения РТК возможно при использовании адъювантной терапии. На 141 больном В и С стадии колоректального рака проведено рандомизированое исследование, в котором сравнивалась пятилетняя выживаемость в контроле, в группе, где больные получали один фторурацил, и в группе, где применялся фторурацил + левамизол. 5 лет прожили в контроле 48% больных, в группе с фторурацилом – 56% и в группе с фторурацилом и левамизолом – 68% [40].
В исследовании, проведенном на 408 больных, было подтверждено, что комбинация левамизола и фторурацила уменьшает частоту рецидивов по сравнению с контролем. Выживаемость достоверно улучшилась лишь при стадии Dukes C [41].
Окончательное мнение среди онкологов по поводу ценности профилактического применения фторурацила и левамизола сложилось после публикации итогов межгруппового международного исследования (Moertel). В группе больных со стадией С летальность сократилась на 33%, а частота рецидивов на 41% по сравнению с контролем [42].
Итак, для адъювантной терапии рака ободочной кишки в стадии С (с вовлечением в опухолевый процесс регионарных лимфоузлов) следующий режим применения фторурацила и левамизола признается стандартным: левамизол 50 мг х 3 раза в день внутрь, 3 дня, каждые 4 недели; фторурацил 450 мг/м2 внутривенно 5 дней, затем с 28 дня один раз в неделю. Лечение проводится в течение года после операции [43].
Тем не менее эта комбинация уступает в популярности режиму фторурацил + кальция фолинат. В четырех крупных рандомизированных исследованиях (в Европе, США и Канаде) было доказано преимущество в выживаемости и безрецидивном течении применения фторурацила и кальций фолината. Разница с контролем по выживаемости составила от 5 до 14%, а по безрецидивному течению от 9 до 15%. Во всех исследованиях эта разница была достоверной [44,45,46,47].
Следующая комбинация признана стандартной для адъювантной терапии рака ободочной кишки в В и С стадиях:
– фторурацил 370–425 мг/м2 внутривенно 1–5 дни,
– кальций фолинат 300 мг/м2 внутривенно 1–5 дни.
Каждые 28 дней, 6 месяцев после операции.
В 1998 г. закончен анализ кооперированного международного сравнения эффективности адъювантной терапии РТК фторурацилом и кальция фолинатом и фторурацилом, кальция фолинатом и левамизолом. Последняя комбинация не улучшила выживаемость. От комбинации фторурацил + кальция фолинат выжило 66%, от комбинации фторурацил + кальция фолинат + левамизол – 67% [48].
В лечении рака прямой кишки, помимо химиотерапии, важная роль отводится лучевой терапии. Гастроинтестинальная исследовательская группа в США осуществила рандомизированное исследование на 277 послеоперационных больных раком прямой кишки в стадиях В и С. Больные были разделены на 4 группы: контроль, облучение таза (40 gy), фторурацил + семустин в течение 18 месяцев, облучение + фторурацил + семустин. После 10 лет наблюдений, статистически достоверной оказалась разница в результатах контроля и группы, где комбинировалось облучение и химиотерапия. Безрецидивное течение было соответственно в 45% и 65%, выживаемость 26% и 45% [49,50].
В исследованиях Северной онкологической группы США (NCCTG) были показаны преимущества комбинации послеоперационного облучения и химиотерапии по сравнению с одним облучением (45 gy). В исследование было включено 240 больных раком прямой кишки в стадиях В и С. Больные наблюдались 7 лет. Безрецидивное течение отмечалось в комбинированной группе в 63%, в чисто лучевой – в 42%, 5 лет прожили соответственно 58% и 47% [51].
Методические модификации применения фторурацила были осуществлены в Гастроинтестинальной исследовательской группе США.
Крупное Японское контролируемое исследование более чем на 300 больных показало, что 4–х летняя выживаемость на 13% выше в группе, где больные после операции в течение 2 лет получали UFT по 400 мг в сутки, по сравнению с группой пациентов, подвергнутых только операции [53].
Среди еще незаконченных исследований в области адъювантной химиотерапии – сравнение в рамках разных методов введения фторурацила (длительные инфузии или струйные), сравнение эффективности разных сроков адъювантной терапии (начало сразу после операции или отсроченное), продолжительность адъювантной терапии.
В настоящее время идет исследование по сравнению режима De Gramont и этой комбинации + современный противоопухолевый агент из группы кампотоцинов. Исследование не завершено.
Среди новых программ адъювантной терапии при РТК – сравнение раптитрексида и комбинации фторурацил + кальций фолинат после операций по поводу РТК Dukes C стадия.
В США планируется большое кооперированное сравнение эффективности UFT + кальций фолинат и фторурацил + кальций фолинат.
В рамках EORTC организовано сравнительное исследование адъювантной эффективности при опухолях со стадией Dukes C раптитрексида и фторурацила с кальций фолинатом. Современные режимы приема 5–фторурацила с кальций фолинатом представлены в таблице 2.
Лучевая терапия – метод, который чаще используется при ректальном раке, нежели при раке ободочной кишки. При раке прямой кишки метод применяется, как дооперационный, для уменьшения стадийности и улучшения местного контроля. Послеоперационное облучение призвано сократить локальные рецидивы, которые возникают у 25–50% оперированных больных, если первичная опухоль квалифицировалась, как Т3 или Т4 и как основной метод неоперабельного местнораспространенного ректального рака [55,56].
Идея послеоперационного облучения возникла в связи с довольно высокой констатацией локальных рецидивов до 30% при Т3N0 и 50% при Т3N1 [57]. Кооперированное исследование на большом числе больных выявило лишь уменьшение рецидивов от послеоперационного облучения (50 gy за 7 недель) в группе со стадией Dukes C; у больных со стадиями А и В рецидивы встречались одинаково в обеих группах, у 10% были постлучевые осложнения, на отдаленной выживаемости добавление лучевой терапии не сказалось. Лучше были лишь двухгодичные результаты: после облучения – 82%, в хирургической группе – 67% [58]. Подобные результаты получены и в других рандомизированных исследованиях [59].
Читайте также: