Впч рак какие номера
Основные факты
Общие сведения о ВПЧ
Вирусы папилломы человека (ВПЧ) — возбудители самой распространенной вирусной инфекции половых путей. Большинство ведущих половую жизнь женщин и мужчин рано или поздно приобретают эту инфекцию, а некоторые могут заражаться несколько раз в течение жизни.
Большинство женщин и мужчин заражаются ВПЧ вскоре после начала половой жизни. Инфекция ВПЧ относится к заболеваниям, передающимся половым путем, хотя заражение возможно и при половых контактах без проникновения. Известно, что передача вируса происходит и при простом соприкосновении половых органов.
Среди множества типов ВПЧ многие не представляют опасности для здоровья. ВПЧ-инфекции обычно исчезают за несколько месяцев без какого бы то ни было лечения, и примерно в 90% случаев элиминация инфекции из организма достигается в течение 2 лет. В небольшой доле случаев инфекции ВПЧ определенных типов могут принимать хронический характер и со временем приводить к развитию рака шейки матки.
Рак шейки матки вне всяких сомнений является самым распространенным из заболеваний, связанных с ВПЧ. Почти все случаи рака шейки матки вызваны ВПЧ-инфекцией.
Инфекциями ВПЧ некоторых типов также обусловлена определенная доля случаев рака заднего прохода, вульвы, влагалища, полового члена и ротоглотки, — заболеваний, которые можно предотвратить с помощью тех же методов первичной профилактики, что и рак шейки матки.
Некоторые не онкогенные вирусы папилломы человека, особенно ВПЧ 6-го и 11-го типов, могут приводить к образованию остроконечных кондилом и развитию респираторного папилломатоза (заболевания, при котором опухоли образуются в дыхательных путях, ведущих от носа и полости рта в легкие). Хотя эти патологические состояния очень редко приводят к смерти, распространенность заболевания может быть значительной. Остроконечные кондиломы очень широко распространены, отличаются высокой контагиозностью и отрицательно влияют на половую жизнь.
Каким образом инфекция ВПЧ приводит к развитию рака шейки матки
Несмотря на то, что большинство ВПЧ-инфекций исчезают сами по себе, а предраковые поражения в большинстве случаев самопроизвольно излечиваются, все женщины подвержены риску перехода инфекции в хроническую форму и прогрессирования предраковых поражений в инвазивный рак шейки матки.
У женщин с нормальным иммунитетом рак шейки матки может развиваться в течение 15-20 лет. Однако при нарушениях иммунной системы, например у женщин с нелеченой ВИЧ-инфекцией, этот процесс может занять всего 5–10 лет.
Факторы риска хронической ВПЧ-инфекции и рака шейки матки
- степень онкогенности ВПЧ (способности вируса вызывать рак);
- нарушения иммунитета: люди с ослабленным иммунитетом, в частности, лица, живущие с ВИЧ, подвержены более высокому риску хронической ВПЧ-инфекции и ускоренного развития предраковых поражений и рака;
- наличие сопутствующих инфекций, передающихся половым путем, таких как генитальный герпес, хламидиоз и гонорея;
- количество родов в анамнезе и роды в раннем возрасте;
- курение табака.
Бремя рака шейки матки в мире
Рак шейки матки — четвертый в мире по распространенности вид рака у женщин. Так, в 2018 г. было зарегистрировано около 570 000 новых случаев этого заболевания. Оно является причиной 7,5% всех случаев смерти от онкологических заболеваний среди женщин. Ежегодно от рака шейки матки умирает более 311 000 женщин, причем более 85% этих случаев приходится на развивающиеся страны.
В развитых странах реализуются программы по вакцинации девочек против ВПЧ и ведется регулярный скрининг женщин на ВПЧ-инфекцию. Скрининг позволяет выявлять предраковые поражения на стадиях, на которых они легко поддаются лечению. В этих странах раннее начало лечения позволяет предотвратить развитие рака шейки матки почти в 80% случаев.
В развивающихся странах из-за ограниченного доступа к профилактике рак шейки матки часто остается не выявленным до поздних стадий заболевания и появления клинических симптомов. Кроме того, в этих странах может быть крайне ограничен доступ к лечению поздних стадий рака (например, доступ к онкохирургии, лучевой и химиотерапии), в связи с чем смертность от рака шейки матки там намного выше.
Проведение эффективных лечебно-профилактических мероприятий могло бы позволить снизить высокий показатель смертности от этого заболевания в мире (стандартизированный по возрасту коэффициент смертности в 2018 г.: 6,9 на 100 000).
Комплексный подход к борьбе с раком шейки матки
ВОЗ рекомендует комплексный подход к профилактике и лечению рака шейки матки. В рекомендуемый набор действий входят мероприятия, относящиеся ко всем этапам жизненного цикла. В эту многопрофильную программу должны входить такие компоненты, как просветительская работа в сообществах, мобилизация социальных ресурсов, вакцинация, скрининг, лечение и паллиативная помощь.
Первичная профилактика
Вторичная профилактика
Третичная профилактика
Первичная профилактика начинается с вакцинации девочек в возрасте 9–14 лет до начала половой жизни.
В перечень других рекомендуемых профилактических мероприятий для девочек или мальчиков, в зависимости от ситуации, входят:
- информирование о практиках безопасного секса, в том числе о нежелательности раннего начала половой жизни;
- пропаганда использования презервативов и предоставление их тем, кто уже начал половую жизнь;
- предупреждение о вреде употребления табака, к которому многие приобщаются в подростковом возрасте и которое является серьезным фактором риска развития рака шейки матки и других онкологических заболеваний;
- мужское обрезание.
Начиная с 30 лет все женщины, ведущие активную половую жизнь, должны проходить скрининг на атипичные клетки шейки матки и наличие предраковых поражений.
Если для лечения предраковых поражений шейки матки необходимо иссечение участков с атипичными клетками или измененными тканями, рекомендуется применять метод криотерапии, основанный на разрушении патологических тканей путем их замораживания.
При обнаружении признаков рака шейки матки необходимо начинать лечение, вариантами которого могут быть хирургическое вмешательство, лучевая терапия и химиотерапия.
Вакцинация против ВПЧ
В настоящее время существуют три вакцины, которые защищают одновременно от ВПЧ 16-го и 18-го типов, вызывающих не менее 70% случаев рака шейки матки. Одна из этих вакцин обеспечивает дополнительную защиту от трех других онкогенных ВПЧ, ответственных еще за 20% случаев этого заболевания. С учетом того, что вакцины только от ВПЧ 16-го и 18-го типов, обеспечивают также определенный уровень перекрестной защиты от других менее распространенных онкогенных типов ВПЧ, ВОЗ считает, что эти три вакцины являются равноценными средствами профилактики рака шейки матки. Две из этих вакцин защищают также от ВПЧ 6-го и 11-го типов, вызывающих аногенитальные остроконечные кондиломы.
Клинические и пострегистрационные исследования показывают, что вакцины против ВПЧ отличаются высокой безопасностью и высокой эффективностью в предотвращении ВПЧ-инфекций.
Вакцины против ВПЧ дают максимальный эффект, если их вводят до контакта организма с этими вирусами. В связи с этим ВОЗ рекомендует вакцинировать девочек в возрасте от 9 до 14 лет, когда большинство из них еще не начали вести половую жизнь.
Вакцины не лечат ВПЧ-инфекцию и связанные с ВПЧ заболевания, в частности, рак.
В некоторых странах начали вакцинировать и мальчиков, так как вакцинация предотвращает развитие рака половых органов не только у женщин, но и у мужчин, а две из существующих вакцин способны также препятствовать развитию остроконечных кондилом у представителей обоих полов. Рекомендуемая ВОЗ вакцинация девочек в возрасте от 9 до 14 лет представляет собой наиболее эффективное с точки зрения затрат медицинское мероприятие по борьбе с раком шейки матки.
Вакцинация против ВПЧ не отменяет необходимости скрининга на рак шейки матки. В странах, где вакцинация против ВПЧ внедрена в медицинскую практику, может сохраняться необходимость в разработке или усилении программ по скринингу.
Выявление и лечение предраковых поражений
Скрининг на рак шейки матки предусматривает проверку на наличие предраковых и раковых образований у женщин, которые зачастую могут чувствовать себя совершенно здоровыми и у не иметь никаких симптомов заболевания. Если при скрининге обнаруживаются предраковые поражения, их лечение не представляет трудностей и позволяет избежать развития рака. Кроме того, скрининг позволяет обнаруживать рак на ранней стадии, когда высока вероятность полного излечения.
Поскольку предраковые поражения развиваются на протяжении многих лет, скрининг рекомендуется регулярно проходить всем женщинам, начиная с возраста 30 лет (периодичность скрининга зависит от используемого для этого метода). Регулярный скрининг у женщин с ВИЧ-инфекцией, ведущих активную половую жизнь, должен начинаться раньше — с момента, когда они узнают о своем ВИЧ-статусе.
При проведении скрининга необходимо обеспечить возможность последующего лечения и предусмотреть необходимые действия в случае получения положительных результатов теста. Без надлежащей организации таких мероприятий проведение скрининга неэтично.
Существуют три различных типа скрининговых тестов, рекомендуемых ВОЗ в настоящее время:
- тесты на ВПЧ, относящиеся к группе высокого риска;
- визуальная проверка с применением уксусной кислоты;
- традиционный ПАП-тест и метод жидкостной цитологии (ЖЦ).
Для лечения предраковых поражений ВОЗ рекомендует применять методы криотерапии и электрохирургической петлевой эксцизии. При обнаружении более глубоких поражений следует направлять пациенток на дополнительные обследования для принятия обоснованных решений о дальнейших действиях.
Лечение инвазивного рака шейки матки
При наличии у женщины симптомов, позволяющих заподозрить рак шейки матки, ее необходимо направить в специализированное лечебное учреждение для проведения дополнительных исследований, постановки диагноза и лечения.
На ранних стадиях рака шейки матки могут появляться следующие симптомы:
- нерегулярные мажущие кровянистые выделения или слабое кровотечение в период между месячными у женщин детородного возраста;
- мажущие выделения или кровотечение у женщин в постменопаузе;
- кровотечение после полового акта;
- более обильные выделения из влагалища, иногда с неприятным запахом.
По мере прогрессирования рака могут появляться более тяжелые симптомы, в том числе:
- постоянная боль в спине, ногах и (или) в области таза;
- потеря веса, утомляемость, снижение аппетита;
- неприятно пахнущие выделения и дискомфорт во влагалище;
- отек одной или обеих нижних конечностей.
При далеко зашедших формах рака могут развиться и другие тяжелые симптомы, в зависимости от того, на какие органы распространился рак.
Диагноз рака шейки матки должен быть подтвержден результатами гистологического исследования. Стадию заболевания устанавливают на основании размеров опухоли и распространения процесса на область таза и отдаленные органы. Выбор метода лечения зависит от стадии рака, при этом в перечень возможных вариантов входят хирургическая операция, лучевая терапия и химиотерапия. Кроме того, важную роль в ведении пациентов с онкологическими заболеваниями играет паллиативная помощь, позволяющая облегчать боль и страдания, причиняемые болезнью.
Действия ВОЗ
ВОЗ разработала руководство по профилактике рака шейки матки и борьбе с этим заболеванием путем вакцинации, скрининга и лечения инвазивной формы рака. Совместно со странами и партнерами ВОЗ занимается разработкой и осуществлением комплексных программ.
В мае 2018 г. Генеральный директор ВОЗ выступил с призывом к действиям, направленным на ликвидацию рака шейки матки, и предложил странам и партнерам объединить усилия для расширения доступа к мерам профилактики рака шейки матки и увеличения охвата населения. В качестве трех основных мер были названы вакцинация против ВПЧ, скрининг и лечение предраковых поражений, а также ведение пациенток с раком шейки матки.
Вирус папилломы человека (ВПЧ или Human papillomavirus, HPV) – это ДНК-содержащая разновидность парвовируса, вызывающая папилломавирусную инфекцию у человека.
ВПЧ передается преимущественно половым путем, реже отмечается передача вируса от матери плоду во время беременности и родов, а также заражение при проведении медицинских манипуляций. Специфической особенностью папилломавирусной инфекции является то, что даже презервативы не гарантируют 100% защиты от ВПЧ.
Поскольку ВПЧ инфекция может длительное время протекать бессимптомно, то основную роль в своевременном скрининге рака шейки матки играет раннее выявление предраковых состояний и заболеваний, связанных с инфицированием ВПЧ.
Всегда ли ВПЧ вызывает рак?
Нет. Вирус папилломы человека бывает онкогенным, потенциально онкогенным и неонкогенным. При этом, даже инфицирование наиболее онкогенными видами ВПЧ (ВПЧ 16 и ВПЧ 18) не всегда приводит к развитию онкологии. Однако, заражение этими типами вируса папилломы человека увеличивает риск развития рака шейки матки более чем в 30 раз.
Также необходимо учитывать, что на вероятность развития злокачественных новообразований при инфицировании ВПЧ влияет наличие факторов риска:
- курение, злоупотребление спиртным;
- отягощенная генетика (наличие рака шейки матки у близких родственников);
- наличие ВИЧ и инфекций, передающихся половым путем и т.д.
Почему важно обследоваться на ВПЧ?
Вирус папилломы человека с высоким онкогенным риском может приводить к развитию рака:
- шейки матки или рака полового члена (около 40% всех случаев рака шейки матки или полового члена связаны с ВПЧ 16 и ВПЧ 18 типов);
- заднего прохода (около 90% случаев связаны с ВПЧ);
- гортани и ротовой полости (с ВПЧ связаны 10-15% случаев рака).
От момента заражением ВПЧ до развития рака обычно проходит более 10 лет. При своевременной диагностике и лечении предраковых состояний, связанных с ВПЧ (папилломатозный цервицит, вагинит, эрозии) риск развития рака сводится к минимуму.
Обследование на ВПЧ проводится при
- плановых цервикальных скринингах (плановый профилактический осмотр + ПАП- мазок у женщин старше 30 лет);
- плановом скрининге на рак шейки матки у женщин старше 30 лет;
- выявлении других инфекций, передающихся половым путем;
- комплексных обследованиях на ИППП (инфекции, передающиеся половым путем);
- выявлении ВИЧ или иммунодефицитов, не связанных с ВИЧ (на фоне снижения иммунитета увеличивается риск перехода ВПЧ из латентной стадии в клиническую);
- выявлении предраковых состояний (эрозии, дисплазия, цервицит);
- наличии у пациента остроконечных кондилом, бородавок и других проявлений ВПЧ.
Также анализ на вирус папилломы человека показан при планировании беременности, при самопроизвольных абортах, а также после незащищенных половых контактов с непроверенным партнером.
Как проводится анализ на ВПЧ?
Лабораторная диагностика ВПЧ включает:
- методику выявления пролиферативных маркеров р16/ki 67;
- молекулярный анализ ПЦП (полимеразная цепная реакция позволяет провести качественную и количественную диагностику ВПЧ);
- определение генотипов ВПЧ.
Серологическая диагностика для выявления ВПЧ не используется.
Для диагностики папилломатоза половых органов также используется кольпоскопия (при помощи кольпоскопии можно обнаружить даже самые маленькие кондиломы на шейке матки или слизистой влагалища).
Материал для цитологической диагностики получают при помощи стандартного ПАП-мазка (мазок по Папаниколау). Цитологическая диагностика подразумевает изучение полученных при мазке эпителиальных клеток под микроскопом. Цитологическое исследование позволяет выявить видоизмененные вирусом клетки, а также атипичные клетки (в случае развития ракового или предракового процесса). Результат цитологического исследования обычно выдают через 5-7 дней после исследования. Результаты кодируются цифрами:
- 1 – пораженные клетки отсутствуют;
- 2 – обнаруженные измененные клетки, характерные для воспалительных процессов;
- 3 – сомнительный результат, требующий повторного цитологического исследования;
- 4-5 – обнаружены измененные клетки.
На основании одного результата ПАП-мазка диагноз не выставляют. При выявлении патологических процессов в шейке проводится повторный ПАП-мазок и назначается дополнительное обследование.
Для гистологического анализа проводится биопсия шейки матки, при которой получают небольшой фрагмент тканей из пораженного участка. Гистологическое исследование назначают после цитологического. Гистологическая диагностика позволяет оценить состояние пораженных клеток и отдиференцировать кондиломы от злокачественных или озлокачествляющихся новообразований. Результаты гистологической диагностики, как правило, приходят через 3-5 дней.
Для диагностики папилломатоза гортани и голосовых связок рекомендовано проведение фиброларингоскопии с взятием биопсии для гистологического и цитологического исследования.
К наиболее достоверным способам выявления ВПЧ относится анализ ПЦР. Полимеразная цепная реакция позволяет обнаружить ДНК вируса папилломы человека даже в случаях, когда концентрация вируса ее низкая и инфекция не проявляется клинически (нет симптомов ВПЧ).
Точность ПЦР диагностики ВПЧ практически 100%. Однако, на информативность анализа в значительной степени оказывает влияние правильность сбора биологического материала для исследования. Обычно при диагностике ВПЧ используют эпителиальные клетки, полученные с помощью соскоба или мазка-отпечатка из уретрального канала, шейки матки. Также для анализа могут использоваться: околоплодные воды, кровь, моча.
Результаты ПЦР диагностики обычно выдаются через 1-2 дня.
ПЦР диагностика может проводиться по двум методикам:
- качественная – определяется только наличие вируса в биологическом материале (отсутствует возможность определения количества вируса и риска развития предраковых состояний);
- количественная – оценивается степень вирусной нагрузки, риск развития и возможное наличие предраковых состояний (так как высокую вирусную нагрузку связывают с высоким онкогенным потенциалом ВПЧ).
В результатах качественного ПЦР указывается только + (наличие вируса) или – (вирус не выявлен). При проведении количественной оценки указывают степень вирусной нагрузки:
- вирус обнаружен в минимальной концентрации;
- обнаружено клинически значимое количество вируса;
- вирус обнаружен в высоких концентрациях.
Важно помнить, что выявление ВПЧ не означает диагноз: рак. Выявление ВПЧ свидетельствует о потенциально повышенном риске развития предраковых и раковых заболеваний. Для уточнения риска необходимо провести генотипирование ВПЧ и определить онкогенность вируса).
При выявлении ВПЧ в обязательном порядке проводят дополнительное обследование для исключения предраковых состояний и рака.
Отрицательный результат ПЦР на ВПЧ означает отсутствие вируса в исследуемом материале и низкий риск развития рака, связанного с ВПЧ.
Генотипирование проводится для определения типа папилломы человека и оценки степени его онкогенности.
Наиболее онкогенными считаются ВПЧ 16 и ВПЧ 18. При выявлении этих типов ВПЧ проводится расширенная диагностика для определения риска развития рака или предраковых состояний.
Также следует отметить, что более высокие риски развития рака наблюдаются у пациентов, инфицированных сразу несколькими типами ВПЧ.
Проведение генотипирования увеличивает точность других методов диагностик и позволяет составить более достоверный прогноз риска развития рака.
Для диагностики чаще всего используется мазок из уретры или шейки матки. Перед обследованием рекомендовано:
- за два дня до исследования избегать половых контактов;
- за 2-3 дня не рекомендовано проводить спринцевания и использовать антибактериальное мыло для личной гигиены.
Перед забором материала необходимо провести туалет половых органов чистой водой (без мыла, геля и т.д.).
Где можно пройти обследование на ВПЧ?
Сдать анализы на ВПЧ можно как в государственном медучреждении (урологическое, гинекологическое, венерологическое отделение), так и в частном центре.
Сколько стоит обследование на ВПЧ?
Стоимость кольпоскопии, в среднем, составляет от 800 до 1500 рублей. Проведение цитологического исследования (+стоимость взятия мазков) составляет от 1500 до 3000 рублей.
Стоимость гистологической диагностики (+стоимость взятия материала) от 2500 до 3500.
Цена на ПЦР колеблется от 800 до 2000 рублей.
Как размножается и передается вирус папилломы человека

Дмитрий Лубнин акушер-гинеколог, кандидат медицинских наук
Раком шейки матки женщин пугают и на приеме у гинеколога, и в СМИ. Но мало кто объясняет, какая связь между вирусом папилломы человека, собственно папилломами и кондиломами, появляющимися иногда на теле, и состоянием шейки матки, которое "не нравится" врачу при осмотре. Теперь обо всем этом можно подробно прочитать в книге, которая, без преувеличения, способна изменить плачевную ситуацию с раком шейки матки в нашей стране.

Что такое вирус и как он размножается
Для начала давайте разберемся, что такое вирус и чем он отличается от бактерии. Вирус — это небольшой кусочек ДНК или РНК, заключенный в оболочку из белков. Проще говоря, вирус — это флешка (карта памяти в пластиковой оболочке). Как на флешке, в вирусной ДНК записано небольшое количество информации, необходимой для того, чтобы сделать много новых флешек, точнее, новых вирусов.
Однако как флешка не может сама себя копировать — для этого ей нужен компьютер, так и вирусу нужна клетка, чтобы в ней осуществлять свое размножение. Для сравнения: бактерия — это уже не флешка, а планшет, то есть у нее есть не только карта памяти, но и все свойства полноценного компьютера.
Напомню, клетка нашего организма состоит из оболочки, ядра и вспомогательных структур, которые называются органеллами. Внутри она заполнена цитоплазмой. В ядре содержится ДНК, на которую записана вся генетическая информация, обеспечивающая работу клетки.
По сути, ДНК — это большая типографская установка, с гранок которой печатаются не газеты, конечно, а белки. Когда в клетку попадает вирус, он освобождается от своей белочной оболочки (капсида) и либо использует ДНК, просто находясь в клетке, либо встраивает свою ДНК в ДНК клетки.
Далее, используя "типографские возможности" ядра, вирус запускает процесс создания своих копий. Задача — сделать их множество, пока эта клетка не погибнет. При этом "печатается" не только ДНК вируса, но и белки для создания его новых оболочек.
В конечном итоге клетка, переполненная вирусами, лопается, и множество его копий выходят наружу, чтобы заразить соседние клетки или перебраться в другой организм. Так ведут себя, к примеру, риновирусы или вирус гриппа.
Как размножается ВПЧ
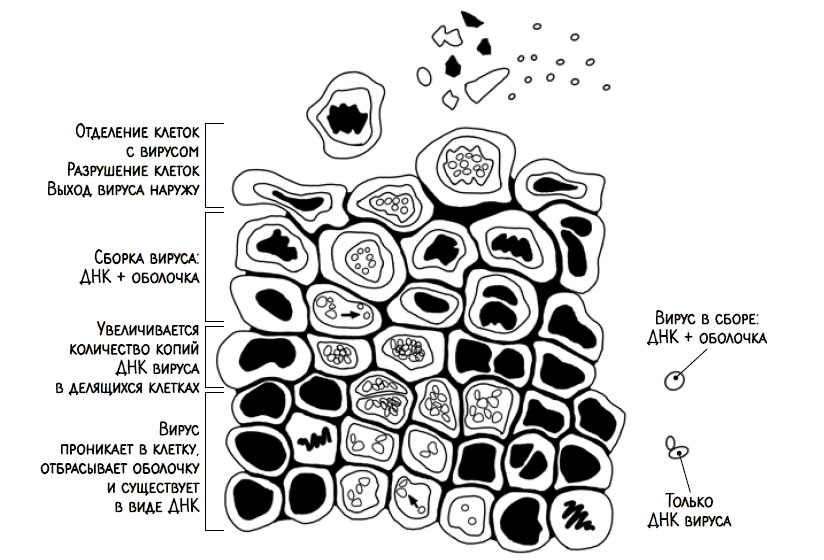
Однако не все вирусы ведут себя подобным образом. В частности, вирус папилломы человека (ВПЧ) выбрал для себя другую тактику. Он инфицирует только клетки эпителия (кожа и слизистые), проникая в базальный, самый нижний слой эпителия, где активно делятся клетки.
Многослойный плоский эпителий работает по принципу конвейера — клетки из нижних слоев постепенно продвигаются в верхние и после слущиваются. ВПЧ использует эту особенность для своих целей. Зачем ему переполнять клетку своими копиями, чтобы она лопнула? Ведь она лежит в глубине эпителия и, лопнув, сможет заразить только ближайшую, но не сможет распространиться за пределы организма — а это важно для выживания вида.
Основная задача ВПЧ — ускорить деление клеток. Чем их больше — тем больше копий вируса. Дальше инфицированные клетки выталкиваются в следующие слои. В промежуточных и поверхностных слоях начинается синтез белковой оболочки вируса, и как только инфицированные клетки достигают самого поверхностного слоя, они отторгаются, разрушаются, и на свободу выходят вирусы, готовые к новым заражениям. Вот так мудро использует ВПЧ "конвейер многослойного плоского эпителия".
При чем здесь эрозия шейки матки
Кстати, думаю, теперь будет понятно, почему наиболее уязвимым для ВПЧ является зона трансформации на шейке матки, которую мы привыкли называть "эрозией". В этом месте незрелый многослойный плоский эпителий, замещающий цилиндрический, содержит не четыре, а только два первых слоя, то есть добраться вирусу к клеткам базального слоя проще.
К примеру, на коже, где некоторые типы ВПЧ вызывают образование кондилом, инфицирование возможно только при наличии микротрещин, обеспечивающих возможность вирусу попасть в клетки базального слоя, так как инфицировать поверхностные слои эпителия он не может.
Немного забегая вперед, скажу, что вирус папилломы человека проявляется ростом кондилом, папиллом и бородавок на коже и слизистых, а также ответственен за развитие рака шейки матки, ануса, полового члена, влагалища и вульвы, а также ротовой полости и глотки. Получается, он может вызывать как совершенно неопасные состояния, проявляющиеся лишь косметическими дефектами, так и грозные онкологические заболевания.
Описано более 200 типов ВПЧ, и между ними есть существенная разница в том, какой процесс они могут вызвать в организме человека. Почему же одни типы вируса более опасны, чем другие?
Почему при заражении ВПЧ растут папилломы и кондиломы
Деление клетки — сложнейший процесс, который контролирует множество белков-наблюдателей. Их основная задача — не допустить ошибок в этом процессе, чтобы не образовалась неправильная клетка. Во время всего процесса деления белки-наблюдатели оценивают происходящее, и если что-то идет неправильно, тут же все останавливают и запускают процесс уничтожения клетки.
Вот так все категорично. Именно эти белки-наблюдатели становятся основной жертвой ВПЧ.
Попав в клетку, вирус вначале находится в цитоплазме и особо не привлекает внимание. Когда она начинает делиться, присутствие фрагмента чужеродной ДНК замечается белками-наблюдателями, и в норме они должны срочно дать команду на уничтожение клетки. Это нормальный защитный механизм. Однако вирус вступает во взаимодействие с этими белками и инактивирует их.
В результате клетка продолжает деление с присутствием вируса в цитоплазме, таким образом получается еще одна инфицированная клетка. Задача выполнена, вирус начал свое распространение.
При этом вирусная ДНК не проникает в ядро клетки и не меняет ее базовых свойств. Основная задача этого типа ВПЧ — ускорить деление клеток, не запускать в них программу самоубийства и за счет увеличения количества инфицированных клеток воспроизводить все больше своих копий.
Так как клеток становится все больше и больше, формируется вырост на слизистой оболочке или коже, который называется кондиломой или папилломой в зависимости от формы. Так действуют ВПЧ, входящие в группу низкого онкогенного риска. Они "паразитируют" в эпителиальных клетках, создавая свои колонии-домики (кондиломы, папилломы) с целью размножиться и двинуться дальше.

Как ведет себя в организме онкогенный ВПЧ
Немного иначе поступают ВПЧ с высоким онкогенным риском. Они способны проникнуть в ядро клетки и встроиться в ее ДНК. Их целью также являются белки-наблюдатели, вот только блокируются не уже синтезированные белки, а нарушается их производство. Клетка остается без этих белков и еще нескольких других, которые также контролируют клеточное деление.
В результате клетка с встроенным в ДНК вирусом папилломы человека начинает бесконтрольно делиться с большим количеством ошибок. При этом получающиеся клетки становятся бессмертными, так как механизм самоубийства у них редуцирован. Чем больше происходит делений, тем выше вероятность ошибок, а случающиеся ошибки накапливаются, делая все последующие клетки все более дефектными.
Вот этот процесс и лежит в основе формирования злокачественной опухоли. Как видите, он изначально отличается от того, что делают ВПЧ низкого онкогенного риска. Если те просто используют клетки для своего распространения, то онкогенные вирусы сразу же нацелены на завладение центром управления клетки, подчиняют своей цели всю клетку, делают из нее источник все более и более примитивных клеток, способных только бесконтрольно делиться и теряющих все остальные свойства.
Вирус папилломы человека как мафиозная структура
Если вы еще не окончательно запутались, предлагаю очень наглядный пример. Представьте себе город, в котором есть сеть предприятий по производству плитки. На них есть отдел контроля качества, сотрудники которого проверяют каждую плитку, и, если она дефектная, тут же ее утилизируют.
Небольшая, не сильно дерзкая преступная группировка решает заработать на этом бизнесе и путем угроз и подкупа запрещает контролерам уничтожать бракованные плитки. Соответственно количество продукции увеличивается. Для сбыта этой продукции вокруг завода организуются стихийные лавки, где эта продукция продается помимо поставок в официальные магазины. Это пример того, как работают вирусы низкого онкогенного риска.
Теперь представьте себе серьезную мафиозную структуру, которая приезжает сразу же к владельцу предприятия и под угрозами вводит своих людей в совет директоров. При этом основной задачей этой мафиозной структуры является не получение прибыли от производства плитки: ее они уже договорились реализовать по госконтрактам на благоустройство города, и там не важно, какого она будет качества.
Главное — отмывание денег через счета этого предприятия (да простят меня сейчас экономисты, если я несу полную чушь, но для примера необходимо). В результате с предприятия увольняют всех контролеров качества, устраняют другие, теперь не нужные службы, к примеру маркетинг, так как госконтракты гарантируют сбыт, и начинают гнать продукцию плохого качества в огромных масштабах.
Далее начинает разрастаться сеть филиалов, которые могут делать вид, что производят плитку, но главная их задача быть промежуточными структурами в финансовых манипуляциях. Так коррупция начинает поглощать весь город — и случается беда.
Куда смотрит полиция, или Почему иммунитет не защищает от ВПЧ?
Наверное, у вас возник вполне логичный вопрос — а куда же смотрит полиция? Все банально и вполне жизненно. Полицией в нашем организме является иммунная система. Прежде чем обозначить место полиции в нашей преступной схеме, стоит рассказать о том, какова роль иммунитета в борьбе с вирусной инфекций.
Клетка, пораженная вирусом, подает сигнал бедствия, выставляя на поверхности своей оболочки специальные маячки (рецепторы). Клетки иммунной системы, патрулируя межклеточные пространства, замечают эти маячки и, подключившись к ним, активируют систему клеточной гибели, то есть запускают каскад реакций, который приводит ее к разрушению.
Кроме этого, всю информацию о напавшем вирусе передают в другие более важные иммунные клетки, которые вначале распоряжаются сформировать специализированный отряд по борьбе с этим вирусом, который идет на поиски и уничтожает все инфицированные им клетки.
Когда они уничтожены, в организме формируется особый отряд клеток или особых белков, работающих на постоянной основе, которые уже обучены для борьбы с данным вирусом. Мы называем это иммунитетом.
Попав в клетку, ВПЧ, помимо блокирования белков-наблюдателей клеточного цикла, также препятствует появлению на поверхности клеток рецепторов-маячков. Таким образом, длительное время иммунная система не может распознать, что клетка инфицирована и в ней происходит неладное.
Однако если речь идет о вирусах низкой онкогенности, через некоторое время их активность становится заметной, хоть на это и требуется довольно много времени. Как только это происходит, иммунитет уничтожает инфицированные клетки и вирус покидает организм.
Высокоонкогенные вирусы за счет внедрения своей ДНК в ДНК клетки, как и в случае с белками-наблюдателями, блокируют на центральном уровне возможность появления сигнальных рецепторов.
Кроме этого, вирус нарушает работу системы разрушения клетки. То есть даже если иммунная клетка обнаружит инфицированную клетку, она не сможет запустить процесс ее разрушения, так как внутриклеточные сигнальные пути разрушены. Это как если бы вы пытались включить свет, нажимая на выключатель, провода которого оборваны.
Способность онкогенных типов ВПЧ избегать внимания иммунной системы и приводит к длительному нахождению вируса в организме, а это, в свою очередь, и является началом онкологического процесса.
Почему лечить ВПЧ надо на ранних стадиях
Возвращаемся к примеру с заводом плитки. Полиция в этом городе, конечно, есть. Когда первая, не сильно дерзкая преступная группировка напала на завод и стала гнать производство некачественной продукции и продавать ее возле завода, местный наряд полиции, возможно, и отреагировал. Но тут же получил взятку и на время прикрыл глаза на происходящее, пока масштаб производства не привлек внимание общественности и, соответственно, более серьезные полицейские структуры.
В результате полицейской операции преступная группа арестовывается, подкупленные контроллеры качества заменяются, а работа на предприятии восстанавливается. В цехах начинают дежурить сотрудники полиции, чтобы подобное не повторилось.
Неонкогенные вирусы действуют как одиночные преступники, и могут легко распознаваться иммунной системой. Онкогенные типы ВПЧ ведут себя как мафия, подкупившая полицию, а потому способны безнаказанно действовать длительное время.
Мафия же, как вы помните, действует через владельца предприятия, поэтому бездействие полицейских обеспечивается на самом высоком уровне. Когда рядовые полицейские патрули обнаруживают признаки преступной деятельности, все их попытки получить ордер на обыск оканчиваются неудачей. Запросы просто игнорируются начальством с формулировкой: "на предприятии все нормально, сами проверяли, а вы туда больше не лезьте".
Попытки назначить проверки также оказываются неэффективными. Направленные проверяющие органы возвращаются ни с чем, говорят, внутрь их не пускают, а вышедший директор предприятия сказал, что сам разберется со всеми проблемами и помощь ему в этом не потребуется.
Решается проблема, только когда силы внутренних войск с применением тяжелой военной техники полностью окружают проблемное предприятие и ликвидируют порочное производство, включая всех представителей мафиозной структуры и совета директоров. Однако, если время упущено и мафия сумела коррумпировать не только этот город, но и начала распространение на руководство региона, области и края, все заканчивается гибелью самого государства.
Надеюсь, на этом примере вам удалось понять, как работает вирус папилломы человека в клетках нашего организма и в чем разница между вирусами, вызывающими кондиломы, и теми, что могут привести к раку.
Читайте также:

