Vhl при раке почки
В.Н. Павлов 1 , И.Р. Гилязова 1,2 , А.А. Измайлов 1 , Е.А. Климентова 2 , И.Р. Султанов 1 , М.А. Бермишева 2 , З.Р. Ахмадеев 2 , А.Х. Нургалиева 3 , Г.В. Ишбулатова 3 , Э.К. Хуснутдинова 1,2,3
Введение
Рак почки (РП) – это гетерогенная группа злокачественных опухолей, подавляющее большинство которых представляют собой почечно-клеточные карциномы различных морфологических типов, но наиболее часто встречается светлоклеточный рак почки (СРП). Особое внимание в канцерогенезе СРП уделяется VHL-HIF1α пути. При нормоксии пролиновые остатки в HIFα гидрокислированы, что делает возможным работу VHL-комплекса и убиквитинилирование HIF1α. HIF участвует в регуляции многих биологических процессов - доставка кислорода и адаптация к его депривации, пролиферация клеток и ангиогенез (через фактор роста эндотелия сосудов (VEGF)), тромбоцитарный фактор роста β (PDGF-β) и трансформирующий рост фактор-α (TGF-α)), метастазирование через подавление E-кадгерина [1, 2]. Нарушения убиквитин-лигазного комплекса приводят к нарастанию концентрации HIF в клетках и приводит к гиперэкспрессии гипоксией-индуцируемых генов, которые участвуют в положительной регуляции клеточной пролиферации и ангиогенезе.
В настоящее время считается, что большую роль в возникновении злокачественных новообразований играют микроРНК – короткие некодирующие РНК длиной 18-25 нуклеотидов, которые взаимодействуют по комплементарному принципу с 3’-нетранслируемыми областями мРНК-мишеней. Согласно имеющимся данным, каждая микроРНК может регулировать сотни различных белок-кодирующих генов [2]. Было показано, что многочисленные гены, участвующие в патогенезе СРП, такие как VHL, PTEN, HIF1-α, mTOR, являются мишенями микроРНК [3]. Изменение характера взаимодействия микроРНК с сайтом связывания в результате однонуклеотидной замены может способствовать изменению экспрессии генов-мишеней, задействованных в возникновении и развитии опухолей.
Целью данного исследования был анализ роли отдельных полиморфных вариантов в сайтах связывания микроРНК (miRNA) генов VHL-HIF1α пути в развитии СРП.
Материалы и методы
Определение генотипов полиморфных локусов сайтов связывания микроРНК в генах VHL-HIFαзависимого пути (rs10982724 гена DEC1, rs406271 гена TFRC, rs10491534 гена TSC1, rs1642742 гена VHL, rs3025033 гена VEGFA) проводили методом аллельной дискриминации Taq-man на приборе CFX96 Touch™ Real-Time PCR Detection System. Результаты каждой аллельной дискриминации были проанализированы, используя программное обеспечение CFX96 Touch™ Real-Time PCR Detection System. При попарном сравнении частот генотипов и аллелей в группах больных и здоровых лиц использовался критерий χ2 (Р) для таблиц сопряженности 2х2 с поправкой Йетса на непрерывность.
Результаты
Проведён анализ полиморфных вариантов в генах VHL- HIFα-зависимого пути у пациентов со СРП и в группе здоровых индивидов. Анализ распределения частот аллелей и генотипов по полиморфным локусам rs10982724 гена DEC1, rs406271 гена TFRC, rs3025033 гена VEGFA между пациентами со СРП и здоровыми индивидами не показал каких-либо статистически значимых различий. При сравнительном анализе частот генотипов и аллелей полиморфного локуса rs1642742 гена VHL было показано, что генотип rs1642742*AA(p=0,0165; OR= 0,5978; 95% CI (0,3915- 0,9213)) встречался у пациентов со СРП в возрасте 55 лет и старше значительно реже, чем в контрольной группе той же возрастной категории, тогда как генотип rs1642742*GG чаще встречался у пациентов, являясь маркёром повышенного риска развития СРП (табл. 1).
Таблица 1. Распределение генотипов и аллелей полиморфного локуса rs1642742 гена VHL в группе пациентов со СРП
| Генотипы, аллели | Больные | Контроль | χ2 | OR (95%CI) | P-value | ||
| N | pi±Sp, CI% | N | pi±Sp, CI% | ||||
| Статус курения (положительный) Smoking status (positive) | |||||||
| AA | 55 | 29,73±3,36 (23,25-36,88) | 102 | 41,3±3,13 (35,09-47,71) | 5,81 | 0,59 (0,39-0,91) | 0,0165 |
| AG | 98 | 52,97±3,67 (45,51-60,34) | 102 | 41,3±3,13 (35,09-47,71) | 5,09 | 1,58 (1,05-2,36) | 0,0244 |
| GG | 32 | 17,3±2,78 (12,14-23,53) | 43 | 17,41±2,41 (12,89-22,72) | 0,0005 | 1,02 (0,60-1,73) | 1,0005 |
| A | 208 | 56,22±2,58 (50,99-61,34) | 306 | 61,94±2,18 (57,5-66,24) | 2,95 | 0,77 (0,58-1,03) | 0,0858 |
| G | 162 | 43,78±2,58 (38,66-49,01) | 188 | 38,06±2,18 (33,76-42,5) | 2,95 | 1,28 (0,96-1,70) | 0,0858 |
| Возраст (старше 55 лет) | |||||||
| Генотипы, аллели | Больные | Контроль | χ2 | OR (95%CI) | P-value | ||
| AA | 79 | 34,5±3,14 (28,36-41,04) | 82 | 46,86±3,77 (39,29-54,53) | 5,81 | 0,3915-0,9213 | 0,0165 |
| AG | 102 | 44,54±3,28 (37,99-51,23) | 71 | 40,57±3,71 (33,23-48,24) | 0,36 | 0,759-1,756 | 0,5748 |
| GG | 48 | 20,96±2,69 (15,88-26,81) | 22 | 12,57±2,51 (8,05±18,41) | 4,30 | 1,0324-3,3142 | 0,0381 |
| A | 260 | 56,77±2,31 (52,09-61,36) | 235 | 67,14±2,51 (61,95-72,04) | 8,56 | 0,4763-0,868 | 0,0043 |
| G | 198 | 43,23±2,31 (38,64-47,91) | 115 | 32,86±2,51 (27,96-38,05) | 8,56 | 1,1532-2,1019 | 0,0043 |
Кроме того, проведён анализ полиморфного локуса rs10491534 гена TSC1. TSC1 – ген, кодирующий белок туберозного склероза гамартин – ключевой интегратор сигналинга ростовых факторов. Белок TSC1 подавляет рост и пролиферацию клеток, ингибируя мишень комплекс рапамицина 1 в клетках млекопитающих.
При сравнении группы больных с учётом тяжести течения заболевания были выявлены статистически значимые различия в распределении частот аллелей и генотипов полиморфного локуса rs10491534 гена TSC1 (табл. 2).
Таблица 2. Распределение генотипов и аллелей полиморфного локуса rs10491534 гена TSC1 в группе пациентов со СРП тяжёлого течения и в контроле
| Генотипы, аллели | Больные | Контроль | χ2 | OR (95%CI) | P-value | ||
| N | pi±Sp, CI% | N | pi±Sp, CI% | ||||
| Статус курения (положительный) Smoking status (positive) | |||||||
| CC | 3 | 1,45±0,83 (0,3-4,18) | 2 | 0,41±0,29 (0,05-1,47) | 0,99 | 3.58 (0.48-3.79) | 0.319 |
| CT | 53 | 25,6±3,03 (19,81-32,12) | 87 | 17,76±1,73 (14,47-21,43) | 5,10 | 1,59 (1.06-2.39) | 0.024 |
| TT | 151 | 72,95±3,09 (66,35-78,87) | 401 | 81,84±1,74 (78,13-85,15) | 6,45 | 0,59 (0.40-0.89) | 0.011 |
| C | 59 | 14,25±1,72 (11,03-17,99) | 91 | 9,29±0,93 (7,54-11,28) | 6,96 | 1,62 (1.12-2.33) | 0.009 |
| T | 355 | 85,75±1,72 (82,01-88,97) | 889 | 90,71±0,93 (88,72-92,46) | 6,96 | 0,61 (0.42-0.88) | 0.009 |
Обсуждение
В результате проведённого анализа наиболее значимые ассоциации были выявлены для полиморфных локусов, расположенных в генах VHL и TSC1. Одним из важных генов-супрессоров опухолевого роста, инактивируемых при светлоклеточном раке почки (СРП) является ген фон Хиппеля-Линдау (VHL, von Hippel–Lindau), локализованный на коротком плече хромосомы 3 в области 3p25-3p26. Основной функцией белка VHL является регуляция индуцируемого гипоксией фактора α (HIF-1α) путём образования комплекса, обладающего E3 -убиквитин-лигазной активностью. Moore L.E. et al. показали, что полиморфный вариант rs1642742 гена VHL был связан с риском гиперметилирования VHL-промотора [4]. Случаи СРП с конкретными полиморфизмами зародышевой линии VHL с большей вероятностью имели инактивацию VHL посредством гиперметилирования промотора, чем путем изменения последовательности ДНК в опухолевой ткани. Таким образом, можно предположить, что присутствие этих SNP может представлять собой пример облегченной эпигенетической вариации (унаследованной склонности к эпигенетической вариации) в ткани почки. Мы показали значительно повышенный риск развития СРП у носителей аллеля rs1642742*G в возрасте 55 лет и старше. Такие же результаты были представлены в исследовании Wen-Chung Wang et al., где частота аллеля G в rs1642742 была намного выше при поздних стадиях карциномы почек у пациентов из Тайваня [5].
Гены туберозного склероза TSC1 и TSC2 действуют совместно для ингибирования сигнального пути mTOR. Этот универсальный для многих клеток организма путь отвечает за процессы клеточного роста, пролиферации, дифференциации, обладая онкогенной активностью. Известно, что нарушения пути mTOR путём гиперэкспрессии или структурных нарушений генов, входящих в сигнальный путь, может приводить к злокачественной трансформации клеток [6]. В исследовании Wei H et al. не было показано статистически значимых ассоциаций полиморфного варианта rs10491534 с риском развития СРП [2]. Также было показано, что полиморфный вариант rs10491534 гена TSC1 играет важную роль в модулировании риска развития вторичных опухолей / рецидивов [7].
Выводы
Полученные в результате настоящего исследования данные свидетельствуют об ассоциации полиморфных вариантов сайтов связывания микроРНК с риском развития рака почки, а также тяжестью течения заболевания. Вместе с другими известными эпидемиологическими, клиническими и генетическими факторами выявленные генетические маркёры могут способствовать выявлению лиц с высоким риском развития рака почки тяжёлого течения. Однако, необходимы дальнейшие исследования изученных генов на независимых выборках для установления их функциональной значимости и роли в патогенезе злокачественных новообразований почки.
Литература
- Zhang J, Zhang Q. VHL and Hypoxia Signaling: Beyond HIF in Cancer. Biomedicines. 2018;6(1),35. DOI: 10.3390/biomedicines6010035
- Wei H, Ke H-L, Lin J, Shete S, Wood CG, Hildebrandt MA. MiRNA target site polymorphisms in the VHL-HIF1α pathway predict renal cell carcinoma risk. Molecular carcinogenesis. 2014;53(1):1-7. DOI: 10.1002/mc.21917
- Chow TF, Youssef YM, Lianidou E, Romaschin AD, Honey RJ, Stewart R, Pace KT, Yousef GM. Diff erential expression profi ling of miRNAs and their potential involvement in renal cell carcinoma pathogenesis. Clinical Biochemistry. 2010;43(1- 2):150-158. DOI: 10.1016/j.clinbiochem.2009.07.020
- Moore LE, Nickerson ML, Brennan P, Toro JR, Jaeger E, Rinsky J, Han SS, Zaridze D, Matveev V, Janout V, Kollarova H, Bencko V, Navratilova M, Szeszenia-Dabrowska N, Mates D, Schmidt LS, Lenz P, Karami S, Linehan WM, Merino M, Chanock S, Boff eƩ a P, Chow WH, Waldman FM, Rothman N. Von Hippel-Lindau (VHL) Inactivation in Sporadic Clear Cell Renal Cancer: Associations with Germline VHL Polymorphisms and Etiologic Risk Factors. PLОS Genet. 2011;7(10):e1002312. DOI: 10.1371/journal.pgen.1002312
- Wang WC, Tsou MH, Chen HJ, Hsu WF, Lai YC. Two single nucleotide polymorphism sinthe von Hippel-Lindau tumor suppressor gene in Taiwanese with renal cell carcinoma. BMC Research Notes. 2014;7:638. DOI: 10.1186/1756-0500- 7-638
- Mehta MS, Vazquez A, Kulkarni DA, Kerrigan JE, Atwal G, Metsugi S, Toppmeyer DL, Levine AJ, Hirshfi eld KM. Polymorphic variants in TSC1 and TSC2 and their association with breast cancer phenotypes. Breast cancer research and treatment. 2011;125(3):861-868. DOI: 10.1007/s10549- 010-1062-1.
- Hildebrandt MAT, Lippman SM, Etzel CJ, Kim E, Lee JJ, Khuri FR, Spitz MR, Lotan R, Hong WK, Wu X. Genetic variants in the PI3K/PTEN/AKT/MTOR pathway predict head and neck cancer patient second primary tumor/recurrence risk and response to retinoid chemoprevention. Clinical Cancer Research. 2012;18(13):3705-3713. DOI: 10.1158/1078- 0432.CCR-11-3271
Статья опубликована в журнале "Вестник урологии" № 4 2018, стр. 36-41
Распространенная патология
На современном этапе рак почки считается одним из часто встречаемых онкологических заболеваний. И за последние годы можно отметить значимый прирост в выявлении опухолей этой локализации. Связано это с тем, что, конечно же, улучшилась инструментальная диагностика. Если раньше выявлялись преимущественно метастатические формы патологии, то сегодня довольно много больных с первичными локализованными и местно-распространенными формами заболевания. А это значит, что большему числу пациентов возможно провести операцию на ранней стадии, тем самым гарантируя в большинстве случаев полное выздоровление.
Однако при этом, к сожалению, остается довольно высокий процент больных с метастатическими формами заболевания — приблизительно каждый четвёртый пациент с впервые выявленным раком почки уже имеет метастазы в лимфоузлы или другие органы. Это усложняет лечение, так как необходимо проводить не только операцию, но и различные варианты системной терапии.
Также есть и такой нюанс — у каждого третьего пациента, которому на ранних стадиях заболевания выполнялось только одно хирургическое вмешательство, в течение последующих 5 лет (срок, признанный усредненным для оценки состояния человека с онкологическим заболеванием) появляются отдаленные метастазы. И им все равно в итоге приходится проводить системное лечение.

Факторы риска
Конечно же, многих интересуют факторы, которые могут поспособствовать развитию данной проблемы. Итак, если говорить про пол, то мужчины болеют раком почки в два раза чаще, чем женщины.
Если рассматриваем возраст, то и тут есть зависимость. Чем старше человек, тем выше риски. Частота встречаемости рака почки у тридцатилетних в разы меньше, чем у пятидесятилетних.
Из числа провоцирующих факторов на первом месте стоит наследственность и генетическая предрасположенность. Так, триггером запуска онкопроцесса в почке может служить ген VHL. Кроме того, негативным фактором является и окружающая среда. Спровоцировать рак почки могут радиация, химические производства, коррозийные производства.
Не стоит злоупотреблять и приемом нестероидных противовоспалительных средств, которые большинству известны как обезболивающие препараты. Они также могут влиять на частоту возникновения рака почки.
Определенным образом может влиять и питание. Да, этот фактор не самый значимый, но все же.
При этом довольно часто мы встречаем пациентов с раком почки, у которых он диагностируется независимо от связи с этими перечисленными факторами. Триггерами для развития рака почки могут служить такие сопутствующие патологии, как сахарный диабет, гипертония или какое-либо имеющееся у больного системное заболевание. Также спровоцировать проблему может доброкачественное образование почки, например аденома, или длительное воспаление органа — тот самый пиелонефрит. Киста почки озлокачествляется достаточно редко, поэтому при постановке такого диагноза впадать в панику не стоит, главное, просто вовремя проводить контрольные обследования.
Если мы говорим про поражение органа, чаще всего рак почки бывает односторонним. Очень редко бывает, чтобы в процесс вовлекались одновременно обе почки.
Что касается рецидивов, они напрямую зависят от стадии заболевания и степени дифференцирования опухоли. Чем более злокачественная опухоль, тем чаще она приводит к рецидиву заболевания.
Симптомы
Раньше, когда опухоль почки обнаруживалась на поздних стадиях, симптомами заболевания были боль в животе, кровь в моче и пальпируемая опухоль. Сейчас эти признаки встречаются крайне редко. Чаще всего рак почки характеризуется бессимптомным течением и случайно выявляется при диспансеризации, как правило, при ультразвуковом исследовании.
Если же говорить о симптомах, на которые надо обратить внимание, то я бы назвал одним из наиболее частых признаков рака почки гипертонию. Тем, у кого отмечаются скачки давления, стоит выполнять ультразвуковое исследование для проверки состояния почек. Почему гипертония? Потому что опухолевые клетки вырабатывают белки, токсины, которые выбрасывают в кровоток, приводя к сужению сосудов. На этом фоне и начинается повышение давления.
Хирургическое лечение
Одним из основных методов лечения является операция. Раньше при обнаружении такой патологии удаляли орган сразу. Сегодня же перед хирургами стоит другая задача — сохранение органа. Тем более что большинству пациентов можно выполнять органосохраняющую операцию — частичное удаление почки с опухолью.
Однако пациентам не стоит переживать, если понадобится удалить одну почку целиком. В общей популяции 10% людей рождаются с одной почки и даже не знают об этом, пока не пройдут обследование по поводу другого заболевания. Можно сказать, у нас одна почка запасная — так природа распорядилась. Причем даже если у человека остается после операции лишь половина почки, этого будет вполне достаточно, чтобы она смогла осуществлять свою секреторно-выделительную функцию в полном объёме.
Систематическая терапия
Ранее при раке почки использовались различные препараты, которые имели низкую эффективность (химиотерапия, гормонотерапия и др.). С 2005 года началась эпоха таргетной терапии, к настоящему времени уже зарегистрировано 8 препаратов. А в последние годы активное распространение получила иммунотерапия. Она показывает высокую эффективность, в 2-3 раза превышающую таргетные препараты. Согласно проведённым исследованиям, каждый третий пациент с отдаленными метастазами, получающий иммунотерапию, может быть полностью излечен от метастатического рака почки. Еще лет 5-7 назад мы о таком мечтать не могли.

Профилактические мероприятия
Обследование после
Частота обследований после обнаружения и лечения рака почки напрямую зависит от стадии заболевания. Обычно после операции рекомендуется выполнять обследования 1 раз в три месяца в первый год, 1 раз в полгода во второй год, 1 раз в год с третьего года после хирургического лечения. Если же имеются метастазы, контроль должен проводиться чаще — компьютерную томографию необходимо выполнять не реже чем 1 раз в 12 недель. Это необходимо, чтобы отслеживать прогрессию или метастазирование.
Людям после операции и эффективного лечения можно вести обычный образ жизни. Единственное, чего стоит избегать — курения, так как оно негативно влияет на сосуды.

- Опухоли почки
- Метастазы рака почки
- Как часто и у кого встречается рак почки?
- Диагностика опухолей почек
- Лечение рака почки на разных стадиях
- Цены в Европейской онкологической клинике на лечение рака почки
Опухоли почки
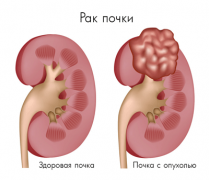
Второй характеристикой опухоли почки, как впрочем и большинства других опухолей, является потеря спецификации клетки – так как клетка быстро делится, она просто не успевает специализироваться. Таким образом, опухоль почки в первом приближении можно характеризовать, как массу клеток, бесконтрольно делящихся и потерявших способность к специализации. Чем меньше специализирована клетка опухоли для выполнения своей функции, чем быстрее она делится и чем больше его способность к распространению по кровеносным и лимфатическим сосудам, тем опухоль злокачественнее.
Почти 90 % опухолей почки злокачественны. Оставшиеся 10 процентов приходятся на ангиомиолипомы и другие, гораздо более редкие доброкачественные опухоли почки. Между тем, даже доброкачественные опухоли почки вполне могут быть опасны для здоровья. Например – ангиомиолипома может повредить сосуды почки, вызывая кровотечение. Что же касается злокачественных опухолей или рака почки, то тут мы сталкиваемся с повреждением функционирующей почечной ткани, ее сосудов и кровотечением, с метастазированием в кости, легкие, головной мозг и, соответственно, нестерпимыми болями.
Метастазы рака почки
Метастазирование — это распространение опухоли по кровеносным или лимфатическим сосудам. Опухоли, как и всему живому в организме, требуется питание, обеспечиваемое сосудами. Вот в эти сосуды и попадают 1-2 клетки из основной опухоли, которые распространяются на различные органы. Для рака почки характерно метастазирование в кости и легкие, а также в печень, надпочечники и головной мозг.
рака почки, как и основная опухоль, нарушает функцию органа, где развивается. Например, метастаз рака почки в легкие вызывает упорный кашель, метастаз в кости — страшные, изнуряющие боли, от которых помогают только сильнодействующие наркотические препараты. К сожалению, часть пациентов, обративших к врачу, уже имеют отдаленные метастазы в тех или иных органах. Это резко ухудшает прогноз течения заболевания, так как приходится бороться не с одной опухолью, а, по сути, с опухолями множеством опухолей в нескольких органах.
Как часто и у кого встречается рак почки?
Диагностика опухолей почек
При подозрении на рак почки пациенту назначают общий анализ мочи, общий и биохимический анализы крови.
Один из наиболее информативных методов диагностики рака почки – компьютерная томография. Она помогает оценить размер, форму и локализацию злокачественного новообразования, обнаружить очаги в лимфатических узлах и других анатомических структурах за пределами почек. Исследование нередко дополняют внутривенным контрастированием. Введение контраста противопоказано при нарушении функции почек.
Магнитно-резонансную томографию применяют реже, чем КТ. Она показана, когда пациенту нельзя проводить компьютерную томографию с контрастом, если имеется подозрение на прорастание опухоли в нижнюю полую вену или другие крупные сосуды, для обнаружения метастатических очагов в головном и спинном мозге.

Ангиография – рентгенография с контрастирование сосудов, почки. Она помогает в диагностике заболевания и планировании хирургического лечения.
Позитронно-эмиссионная томография помогает обнаружить вторичные очаги рака в различных частях тела. Суть метода в том, что в организм пациента вводят вещество, которое обладает слабой радиоактивностью и накапливается в опухолевых клетках. Затем выполняют снимки с помощью специального аппарата, и на них опухолевые очаги хорошо видны.
В отличие от других онкологических заболеваний, биопсия при раке почки проводится редко. Обычно результатов других исследований хватает для того, чтобы принять решение о необходимости хирургического вмешательства. Уже после операции удаленную опухоль направляют в лабораторию, чтобы подтвердить диагноз. Биопсию проводят, если другие исследования не позволяют разобраться, показана ли операция. В случаях, когда хирургическое вмешательство противопоказано, исследование опухолевой ткани помогает определиться с тактикой лечения.
В медицине нет категоричных, стопроцентных ответов. Какова цель операции по удалению рака почки? Удалить опухоль? Удалить почку с подлежащими структурами? Удалить только первичный очаг опухоли, а потом бороться с метастазами теми или иными способами? Перенесет ли пациент операцию, каково его общее состояние? Какую именно операцию выбрать для конкретного больного? На эти вопросы должен ответить онкоуролог, перед тем, как предложить хирургическое, консервативное или комбинированное лечение. В основном, это зависит от стадии рака почки, расположения опухоли, наличия метастазов в лимфатические узлы и общего состояния здоровья пациента.

Это зависит главным образом от стадии, на которой была диагностирована опухоль, и начато лечение. Пятилетняя выживаемость (процент пациентов, оставшихся в живых спустя 5 лет) наиболее высока для I стадии и составляет 81%. На II и III стадиях она, соответственно, составляет 74 и 53%. При IV стадии — 8%.
Стадия рака почки зависит от размеров и расположения опухоли. Так, рак почки первой стадии — это опухоль меньше 7 см, не выходящая за пределы почки. Рак почки второй стадии — это опухоль меньше 10 см, также не выходящая за пределы почки. А вот рак почки третьей стадии — это уже опухоль любых размеров, ограниченная почкой, либо повреждающая надпочечник, почечную вену, но имеющую метастаз в ближайших лимфатических узлах. Рак почки четвертой стадии может быть любых размеров, однако при этой стадии опухоль либо выходит за пределы почечной фасции, либо имеются больше одного метастаза в ближайших лимфатических узлах, либо имеются метастазы в легкие, кости, печень или головной мозг.
Стадию рака почки определяют в соответствии с международной классификацией TNM. Рядом с каждой из трех букв аббревиатуры указывают индекс, описывающий характеристики первичной опухоли (T), поражение регионарных лимфатических узлов (N), наличие отдаленных метастазов (M):
T1 – опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр не более 4 см (T1a) или 4–7 см (T1b).
T2 - опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр 7–10 см (T2a) или более 10 см (T1b).
T3 – злокачественное новообразование распространяется на почечную вену и ее ветви, на надпочечник на одноименной стороне, паранефральную клетчатку, не прорастая фасцию Героты (T3a), на нижнюю полую вену ниже (T3b) или выше (T3c) диафрагмы или врастает в стенку вены.
T4 – опухоль распространяется за пределы фасции Героты.
N0 – опухолевые очаги в регионарных лимфоузлах отсутствуют.
N1 – обнаруживается опухолевый очаг в одном лимфоузле.
N2 – обнаруживаются опухолевые очаги в двух и более регионарных лимфоузлах.
M0 – отдаленных метастазов нет.
M1 – отдаленные метастазы присутствуют.
В зависимости от значений T, N и M, выделяют четыре стадии рака почки:
- Стадия I: опухоль в почке не более 7 см (T1), лимфоузлы не поражены, отдаленных метастазов нет.
- Стадия II: первичная опухоль более 7 см (T2), отсутствуют очаги поражения в лимфатических узлах и отдаленные метастазы.
- Стадия III: злокачественная опухоль распространяется на соседние структуры (T3) и/или поражен один регионарный лимфатический узел (N1).
Стадия IV: опухоль распространяется на соседние структуры (T4), либо поражено 2 и более регионарных лимфоузла (N2), либо обнаружены отдаленные метастазы (M1).
Опухоль почки размером 2 см может быть расположена вблизи почечных сосудов и ее удаление технически может быть невозможным. Однако данные литературы указывают, что если нет метастазов в лимфатические узлы и отдаленные органы, то опухоль почки до 7 см можно удалять с сохранением почки, что, безусловно, лучше полного удаления почки и инвалидизации пациента.
Лечение рака почки на разных стадиях
Выбор тактики лечения при раке почки в первую очередь определяется стадией опухоли и состоянием здоровья пациента.
При стадиях I и II возможно хирургическое лечение. Стандартным вариантом считается нефрэктомия. К органосохраняющим операциям прибегают реже, в частности, при опухолях в единственной почке. Кроме того, на выбор объема операции влияет размер опухоли. Также удаляют близлежащие лимфатические сосуды, особенно если они увеличены, окружающую жировую клетчатку.
При III стадии рака почки основным методом лечения также является нефрэктомия, при этом должны быть удалены все регионарные метастазы. Если опухоль прорастает в почечную или нижнюю полую вену или мигрирует в их просвете в виде опухолевого тромба, пораженные ткани также нужно удалить, при этом может потребоваться подключение пациента к аппарату искусственного кровообращения.
При высоком риске рецидива после операции применяют адъювантную терапию таргетным препаратом сунитинибом. Пациенты получают его в течение года.
Если хирургическое вмешательство противопоказано, прибегают к радиочастотной аблации, эмболизации.
На IV стадии подходы к лечению могут быть разными, в зависимости от степени распространения рака в организме. В некоторых случаях возможно хирургическое лечение, в том числе циторедуктивные операции, во время которых хирурги не могут убрать опухоль полностью, но стараются удалить как можно больший ее объем. В редких случаев возможно удаление основной опухоли в почке и единичных вторичных очагов в других органах. После операции назначают курс таргетной терапии, иммунотерапии.
При неоперабельном раке почки основными методами лечения становятся иммунотерапия и таргетная терапия.

В некоторых случаях рак почки удается выявить на ранних стадиях, когда опухолевые клетки не распространяются за пределы органа. Но зачастую заболевание диагностируют на более поздних стадиях. Во-первых, это связано с тем, что рак почки может очень долго протекать бессимптомно. Во-вторых, для этого типа рака на данный момент не существует рекомендованных скрининговых исследований.
Все симптомы можно разделить на ренальные (связанные с поражением почек) и экстраренальные.
Среди ренальных проявлений рака почки наиболее характерны три:
- Гематурия (примесь крови в моче) – самый распространенный и зачастую первый симптом. Он возникает более чем у половины пациентов с раком почки. Моча приобретает красный цвет, при этом боль не беспокоит либо носит острый характер и возникает после гематурии. Этим злокачественная опухоль отличается от неопухолевых заболеваний почки, например, мочекаменной болезни, при которой обычно сначала возникает боль, а потом появляется примесь крови в моче. Гематурия периодически исчезает, но через некоторое время снова появляется, причем, промежутки между кровотечениями сокращаются. Количество крови в моче не зависит от размеров опухоли.
- Боли беспокоят около половины пациентов. Острая боль после гематурии возникает из-за того, что сгустки крови перекрывают просвет мочеточника. Тупые сильные боли зачастую говорят о плохом прогнозе.
- Пальпируемая опухоль – симптом, который выявляет врач во время осмотра примерно у трети пациентов.
Все три симптома одновременно встречаются у одного из десяти пациентов с раком почкеи. Обычно при этом выявляют запущенные опухоли.
Среди экстраренальных симптомов в первую очередь стоит отметить повышение температуры тела. У 5% больных лихорадка – единственное проявление заболевания. У некоторых пациентов повышается артериальное давление, отмечается покраснение лица из-за увеличения количества эритроцитов в крови, у мужчин – расширение вен мошонки (варикоцеле). На поздних стадиях снижается аппетит, пациент теряет вес без видимой причины, постоянно ощущает утомление, недомогание.
Читайте также:

