Вещество способствующее развитию злокачественных новообразований называют
Внешние факторы канцерогенеза многолики и обширны. Доказанные химические канцерогены – это около 400 соединений антропогенного и природного происхождения, вызывающие раковые опухоли. Негативное действие на клетки может быть прямым или опосредованным, медленным или быстрым, обратимым или необратимым, но исход один – злокачественное перерождение тканей разных органов и систем организма.

Химические вещества могут стать причиной опухолевого роста
Химические канцерогены
Любые соединения, провоцирующие прямо или опосредованно канцерогенные изменения в здоровых клеточных структурах живого организма, относятся к факторам, вызывающим злокачественные опухоли. Самым первым доказанным химическим канцерогеном стала обычная сажа в печных трубах (у лондонских трубочистов удалось резко снизить частоту рака мошонки после введения закона об обязательном и ежедневном принятии ванны по окончании работы). Сейчас имеется более 6 миллионов различных естественных и искусственно созданных химических соединений, из которых около 400 могут вызвать раковое перерождение. При этом следует понимать, что огромное количество веществ не исследованы с точки зрения возможного канцерогенеза.
Принцип воздействия на клеточные структуры
Химические канцерогены являются значимым фактором риска для 80% всех видов злокачественных опухолей. Выделяют следующие основные механизмы химического канцерогенеза:
- Генотоксический – прямое повреждение или мутация клеточного генетического кода;
- Опосредованный (негенотоксический) – вещество провоцирует внутриклеточные патологические изменения, способствующие возникновению рака.
В первом случае химические канцерогены сразу изменяют ДНК клеточных структур, запуская онкологический процесс, во втором – на начальном этапе в клетке происходят неонкогенные нарушения, но на их фоне возможна стимуляция злокачественного роста.
К важным закономерностям формирования раковой опухоли относятся:
- длительное и медленное влияние (с момента контакта с канцерогенным фактором до выявления опухоли может пройти большое количество времени – 5-20 лет);
- важная зависимость дозы вещества (чем сильнее каждое разовое воздействие, тем больше риск быстрого развития новообразования);
- отсутствие пороговой дозы (доказанные химические канцерогены в любых дозах и количествах вызывают рак);
- необратимость (даже после прекращения внешнего воздействия генотоксического фактора нет никаких гарантий, что через определенный промежуток времени не возникнет опухолевый рост).
Химические канцерогены убивают – отсрочено, медленно, но необратимо: понимая это, необходимо сделать все, чтобы предупредить контактирование с любым видом веществ, провоцирующих онкологию.
Классификация
В зависимости от опасности и значимости все химические вещества разделены на 4 группы:
- Доказанные химические канцерогены;
- Недоказанный фактор канцерогенеза для человека, но имеются факты возникновения рака у животных;
- Нет исследований на животных и людях, поэтому нельзя доказать отсутствие канцерогенности;
- Химическое вещество не вызывает рак.
Особо опасны соединения из 1 группы: именно с этими веществами недопустимо контактировать в быту и на рабочем месте.

Пыль бериллия способна быстро вызвать рак легких (через 3-4 года)
Химические канцерогены – какие виды рака вызывают
Важно знать и понимать, что могут сделать внешние факторы при длительном воздействии небольшими дозами, чтобы предотвратить риск для здоровья. Из наиболее опасных доказанных причин рака выделяют:
- ароматические углеводороды (бензпирен) – рак легких, кожи и мочевого пузыря;
- бензол – лейкоз (рак крови);
- нитрозосоединения (нитриты, нитраты) – рак желудка, пищевода, печени и головного мозга;
- тяжелые металлы (никель, ртуть, свинец, мышьяк, кадмий, бериллий, хром, кобальт) – рак кожи, легких, простаты и желудка;
- асбест – рак легких, органов желудочно-кишечного тракта;
- хлорвинил (газ, используемый для производства пластмасс) – стимулятор пластмассового канцерогенеза в легких, печени и крови;
- афлатоксин (продукт жизнедеятельности плесневого гриба) – рак печени;
- табак (в виде курения, жевания, вдыхания нюхательного порошка) – рак легких, пищевода, гортани, желудка, колоректальной области, почки, мочевого пузыря, цервикального канала.
Химические канцерогены, входящие в состав табачного дыма, вызывают 35% всех видов раковых опухолей. Человек сам создает условия для формирования опухолевого роста, продолжая использовать табак в повседневной жизни. Курение – это медленное и отсроченное самоубийство: когда придет время смертельной болезни, не надо спрашивать у врача, откуда взялась опухоль и кто виноват в возникновении заболевания.
Злокачественное новообразование состоит из клеток, которые утратили нормальные механизмы управления и поэтому размножаются избыточно и бесконтрольно.
Злокачественное образование, будь то опухоль или рассеянные злокачественные клетки в крови или лимфе, может развиваться из любой ткани любого органа. К злокачественным относятся как раковые образования, так и сходные с ними по механизму возникновения, например лимфомы и миеломы. По мере того как злокачественные клетки растут и размножаются, они могут вторгаться в смежные ткани и распространяться (метастазировать) по всему организму.
Как появляются злокачественные клетки
Злокачественные клетки развиваются из нормальных клеток в результате сложного процесса, называемого трансформацией. Первый шаг на этом пути — инициация, в процессе которой изменение в генетическом материале клетки делает ее злокачественной. Это изменение генетического материала вызывается канцерогенами, такими как некоторые химические вещества, вирусы, радиация и солнечное излучение. Однако не все клетки одинаково восприимчивы к канцерогенным веществам. Генетический дефект в клетке или другой агент, называемый промотером, и даже длительное физическое раздражение могут сделать ее более восприимчивой к канцерогенам. На этапе промоции клетка, которая уже была инициирована, становится злокачественной. Промоция не оказывает самостоятельного канцерогенного влияния на неинициированные клетки. Таким образом, для того чтобы вызвать развитие злокачественного образования, необходимо наличие нескольких факторов, в частности сочетания восприимчивости клетки и воздействия канцерогена.
В процессе превращения нормальной клетки в злокачественную происходит изменение ДНК (дезоксирибонуклеиновой кислоты, из которой состоят гены). Изменения в генетическом материале клетки часто трудно обнаружить, но иногда изменение длины или формы одной из хромосом указывает на наличие определенного типа онкологического заболевания. Например, патологическая хромосома, называемая филадельфийской, обнаруживается приблизительно у 80% больных хроническим миелолейкозом. Генетические изменения были выявлены также при злокачественных опухолях мозга, толстой кишки, молочных желез, легких и костей.
Для развития некоторых онкологических заболеваний необходим целый ряд хромосомных изменений. Изучение так называемого семейного полипоза толстой кишки (наследственного заболевания, при котором в толстой кишке развиваются полипы, впоследствии перерождающиеся в злокачественные) дало информацию о том, каким образом этот процесс может происходить при возникновении злокачественной опухоли толстой кишки: слизистая оболочка толстой кишки начинает расти более активно (избыточная пролиферация), поскольку в 5-й хромосоме клеток нет гена-супрессора, который в норме контролирует рост слизистой оболочки. Небольшое изменение в ДНК затем способствует изменениям, в результате которых формируется аденома (доброкачественная опухоль). Другой ген (RAS-онкоген) заставляет аденому расти более активно. Последующая потеря гена-супрессора в 18_й хромосоме стимулирует дальнейшее развитие аденомы, и наконец, потеря гена в 17_й хромосоме приводит к преобразованию доброкачественной аденомы в злокачественную опухоль. Дополнительные изменения могут способствовать появлению метастазов.
Даже когда клетка становится злокачественной, иммунная система часто может разрушить ее прежде, чем она начнет делиться и разовьется в злокачественное образование. Онкологическое заболевание возникает чаще, когда иммунная система организма ослаблена, как, например, у больных СПИДом, у пациентов, получающих иммуносупрессивную терапию (то есть препараты, которые подавляют иммунную систему организма) и страдающих некоторыми аутоиммунными болезнями. Однако даже в здоровом организме иммунная система не всегда может воспрепятствовать развитию злокачественного образования.
Факторы риска
Множество генетических факторов и факторов окружающей среды увеличивают опасность возникновения онкологических заболеваний. Наличие таких заболеваний у родственников, то есть генетическая предрасположенность к появлению злокачественных новообразований, — один из наиболее важных факторов этого рода. В одних семьях риск развития определенных злокачественных образований значительно выше, чем в других. Например, вероятность появления рака молочной железы у женщины возрастает в 1,5–3 раза, если такая злокачественная опухоль была обнаружена у ее матери или сестры. Некоторые типы рака молочной железы связаны со специфической мутацией гена, более распространенной в некоторых этнических группах и семьях. У женщин с этой мутацией вероятность развития рака молочной железы составляет 80–90%, а злокачественной опухоли яичников —40–50%. Исследователи обнаружили, что эту мутацию имеет 1% евреек-ашкенази (то есть выходцев из Европы). Многие другие онкологические заболевания, в том числе некоторые злокачественные опухоли кожи и толстой кишки, также имеют тенденцию к возникновению у членов одной семьи.
Повышенный риск возникновения онкологических заболеваний отмечен у людей с некоторыми хромосомными заболеваниями. Например, у больных с синдромом Дауна, имеющих три 21_х хромосомы вместо обычных двух, в 12–20 раз выше вероятность развития острого лейкоза.
Многие факторы окружающей среды также повышают риск возникновения злокачественных новообразований.
Один из самых важных среди них — курение, которое существенно увеличивает опасность появления опухолей в легких, полости рта, гортани и мочевом пузыре. Длительное воздействие ультрафиолетового излучения, прежде всего солнечного света, иногда вызывает рак кожи.
Особенно канцерогенная ионизирующая радиация используется в рентгенологических исследованиях, образуется при работе атомных электростанций и при взрыве атомных бомб, а также попадает на Землю из космоса. Например, у людей, оставшихся в живых после атомных бомбардировок Хиросимы и Нагасаки во время Второй мировой войны, повышена вероятность развития лейкоза. С воздействием урана на шахтеров было связано возникновение у них злокачественных опухолей легкого спустя 15–20 лет; опасность особенно увеличивается, если шахтер еще и курит. Длительное воздействие ионизирующей радиации предрасполагает к развитию онкологических заболеваний крови, в том числе острого лейкоза.
Особенности питания — другой важный фактор риска возникновения злокачественных новообразований, особенно опухолей пищеварительной системы. Пища с высоким содержанием волокон уменьшает вероятность развития опухолей толстой кишки. Рацион с обилием копченых и соленых продуктов увеличивает опасность появления рака желудка. Имеющиеся в настоящее время данные свидетельствуют о том, что рацион, в котором жир составляет меньше 30% от общей суммы калорий, уменьшает риск развития рака толстой кишки, молочной железы, а возможно, и предстательной железы. У людей, употребляющих большое количество алкоголя, выше вероятность возникновения рака желудка.
Известно немало химических веществ, вызывающих онкологические заболевания; кроме того, многие другие рассматриваются в качестве возможных канцерогенов. Некоторые химические вещества могут заметно увеличивать вероятность развития злокачественных образований, причем часто многие годы спустя. Например, воздействие асбеста часто вызывает рак легкого и мезотелиому (злокачественную опухоль плевры). У курильщиков, подвергавшихся воздействию асбеста, злокачественные опухоли еще более распространены. Вероятность появления злокачественных новообразований определенного типа также зависит от региона проживания. Так, встречаемость рака толстой кишки и молочной железы в Японии низкая (в частности, она ниже, чем в России), а у жителей Японии, переехавших в США, она увеличивается и постепенно сравнивается с таковой у остальной части американского населения. Среди японцев чрезвычайно высока распространенность злокачественных опухолей желудка. Однако у японцев, родившихся в США, они встречаются реже. В основе географической изменчивости риска возникновения онкологических заболеваний, вероятно, лежит много причин: здесь играет роль сочетание генетических факторов, рациона и факторов окружающей среды. Известны некоторые вирусы, вызывающие онкологические заболевания у людей. Папилломавирус, который приводит к образованию бородавок на половых органах, вероятно, является одной из причин рака шейки матки. Вирус цитомегалии вызывает саркому Капоши. Вирус гепатита B способствует появлению злокачественной опухоли печени, хотя является ли он сам канцерогеном или промотером, или только создает условия для возникновения опухоли, неизвестно. В Африке вирус Эпштейна–Барр является причиной лимфомы Беркитта; в Китае он вызывает злокачественные опухоли носа и глотки; однако, чтобы этот вирус мог вызвать онкологическое заболевание, необходимы еще какие-то дополнительные факторы — либо относящиеся к окружающей среде, либо генетические. Некоторые человеческие ретровирусы, например вирус иммунодефицита человека (ВИЧ-инфекции), вызывают лимфомы и другие злокачественные заболевания системы крови.
Заражение паразитом шистосомой (Bilharziа) может вызывать злокачественную опухоль мочевого пузыря за счет его хронического раздражения. В то же время подобное раздражение мочевого пузыря, вызванное другими причинами, не сопровождается развитием рака. Заражение гельминтом Clonorchis, выявляемое главным образом на Востоке, может привести к злокачественным опухолям поджелудочной железы и желчных протоков.
Содержание
- 1 Канцерогенез
- 1.1 Характеристика злокачественной опухоли
- 1.2 Причины
- 2 Интересно
- 3 Читайте также
- 4 Источники
Канцерогенез [ править | править код ]
Опухоль - это неопластические разрастания (новообразования) клеток. Рак относится к злокачественным, распространяющимся опухолям.
Доброкачественные опухоли лишены способности распространяться (метастазировать) из места своего начального возникновения.
Злокачественные опухоли, называемые также раковыми, метастазируют в результате клональной экспансии одиночной клетки, которая размножается, превращаясь в опухолевую массу, инвазирующую окружающие нормальные ткани и распространяющуюся по организму по лимфатической системе или через кровь (гематогенно). Рост злокачественной опухоли, называемый канцерогенезом или туморогенезом, представляет собой многоэтапный процесс.
К основным характеристикам раковых образований относится:
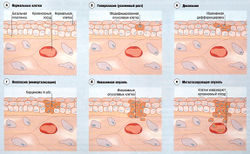
Рак может возникнуть под влиянием внешних воздействий (например, химический канцерогенез) или в результате генетической предрасположенности. В большинстве случаев существует очевидная связь между этими двумя факторами. Однако природа и степень ассоциации у разных индивидов могут варьировать. Так, исследования, проведенные на близнецах, показали, что генетические факторы обусловливают 42% относительного риска рака простаты, 35% — колоректального рака и 25% рака молочной железы. Вклад в развитие других типов рака менее значителен.
К внешним факторам, способствующим канцерогенезу, относятся бактерии, например Helicobacter pylori, вирусы, например вирус Эпштейна-Барр, вирусы папилломы человека или гепатита В и С, грибы, продуцирующие афлатоксины, и химические вещества, например бензол.
Онкогены представляют собой ДНК-последовательности, кодирующие ключевые белки, которые участвуют в канцерогенезе. Впервые их выделили из вирусов, вызывающих злокачественные опухоли у лабораторных животных. Онкогены также сверхэкспрессированы злокачественными клетками и способны кодировать факторы роста и митогенные факторы, поэтому злокачественные клетки могут стимулировать собственный рост. (рис. 7.2)
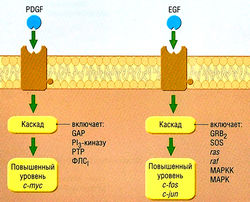
Рис. 7.2 Две схемы, показывающие, как внеклеточные факторы роста стимулируют пролиферацию злокачественных клеток. Сверхэкспрессия любого из этих клеточных гомологов онкогенов или мутация, вызывающая конститутивную активацию, способствуют усилению роста, c-fos, c-jun, с-тус — индукторы синтеза ДНК; ECF — эпидермальный фактор роста; САР — белок, активирующий ГТФазу; GRB2 — белок В2, родственный G-белку; МАРК — активированная митогеном протеинкиназа; МАРКК — активированная митогеном киназа протеинкиназы; PDGF — тромбоцитарный фактор роста; Р13-киназа — фос-фадилинозитол-3-киназа; ФЛС — фосфолипаза С; РТР — фосфоти-розинфосфатаза; ras, raf— клеточные передатчики сигнала.
Функциональные рецепторы факторов роста могут быть экспрессированы конститутивно на поверхности злокачественных клеток, тогда как другие появляются в результате индукции (часто химическими веществами, которые высвобождают сами злокачественные клетки).

Механизмы пролиферации нормальных клеток связаны с антипролиферативными механизмами, что дает возможность контролировать пролиферацию по типу обратной связи. Продукты некоторых онкогенов способны подавлять пролиферацию. Мутации или повышенная экспрессия онкогенов могут изменить баланс между стимуляцией и супрессией пролиферации. При канцерогенезе баланс сдвинут в сторону пролиферации.
Пролиферация нормальных клеток также контролируется серией генов-супрессоров опухолей, действующих на клеточный цикл. Мутации или утрата таких генов-супрессоров, например р53 при синдроме Аи-Фраумени, или rb при ретинобластоме, обусловливают повышенный риск онкогенеза у индивидов и семей.
Пролиферация нормальных клеток уравновешивается клеточной гибелью. Рост популяции злокачественных клеток представляет собой результат баланса между пролиферацией и гибелью клеток. Нормальные клетки подвергаются апоптозу — процессу запрограммированной клеточной гибели старых или поврежденных клеток. Апоптоз происходит либо в результате прямого связывания с рецептором (рецептор Fas и его лиганд лимфоцитов), либо высвобождения цитохрома С в цитоплазму после разрыва мембраны митохондрий вследствие летальных внутриклеточных процессов. Существуют проапоптотические белки, такие как Bad и каспазы, действие которых уравновешивается антиапоптотическими белками, например bcl-2. Повышенная экспрессия bcl-2 может быть обусловлена экспрессией онкогенов и ассоциирована с трансформацией нормальных клеток в опухолевые.
Нарушение нормальной репликации геномной ДНК является важнейшим фактором возникновения рака
Злокачественные клетки могут размножаться лишь в том случае, когда организм утрачивает способность распознавать и репарировать мутации в геноме. Индивиды и семьи с мутациями ДНК генов репарации предрасположены к возникновению опухолей, например:
- в ДНК генов, репарирующих не соответствующие друг другу пары оснований, обнаружены мутации при наследственном неполипозном раке толстой кишки;
- репарация ДНК под контролем хеликаз отсутствует или дефектна в случае пигментной ксеродермы — генетического заболевания, характеризующегося дефектом репарации повреждений, вызванных ультрафиолетовым облучением. Гену-супрессору опухолей р53 принадлежит существенная роль в клеточном ответе на повреждение или мутацию ДНК. В норме р53 останавливает клеточный цикл до репликации ДНК, давая возможность репарировать повреждения; этот ген также инициирует апоптоз. Утрата нормальной функции р53 позволяет реплицироваться поврежденной ДНК и таким образом способствует выживанию аномальных клеток.
Злокачественные клетки представляют собой иммортализованные клетки
Каждая нормальная клетка организма, за исключением зародышевых клеток гонад, запрограммирована на конечное число клеточных делении до своего старения. Эта клеточная программа заключена в теломере. Теломеры расположены на концах хромосом и должны соединиться друг с другом в митозе. Они образуются и сохраняются в зародышевых и эмбриональных клетках под контролем фермента теломеразы. Этот фермент утрачивает свою функцию в течение нормального развития. В связи с этим часть теломеры теряется при каждом клеточном делении, а утрата каждой теломеры служит для клетки сигналом, возвещающим гибель. Злокачественные клетки реэкспрессируют теломеразу, что дает им возможность пролиферировать неопределенно долго. Утрата контроля нормального клеточного цикла, осуществляемого генами rb и р53, способствует возобновлению экспрессии теломеразы. До 95% злокачественных клеток экспрессирует теломеразу, делая ее потенциальной мишенью для лекарственных веществ.
Достигнув определенной стадии развития, злокачественная опухоль проникает через базальную мембрану и инвазирует соседнюю соединительную ткань
Злокачественные клетки экспрессируют коллагеназы, гепараниазы и активаторы плазминогена и продвигаются через поддерживающие ткани по пути наименьшего сопротивления.
Ангиогенез играет существенную роль в доставке питательных веществ распространяющейся опухоли, его стимулируют фактор роста фибробластов и фактор роста сосудистого эндотелия. Синтез коллагена, витронектина и фибронектина злокачественными клетками создает основу для развития клеток опухоли и способствует ее приживлению в участках метастазирования. Многие из необходимых для этого сложного процесса компонентов предоставляют сами нормальные ткани, невольно способствуя собственной гибели. Процессы инвазии и метастазирования менее важны при лейкозах и лимфомах, т.к. эти опухоли представляют собой диффузный рак крови.
Инвазия и метастазирование часто достигают значительной степени развития до появления клинических симптомов и выявления опухоли. Лекарственную терапию необходимо начать сразу же, как только макро- или микроскопически опухоль распространится за пределы места возникновения.
Квалифицированный гистологический диагноз — важный компонент терапии рака
Гистологический диагноз некоторых опухолей играет существенную роль в определении цели лечебного вмешательства — паллиативный эффект или полное излечение, например:
Определение стадии развития злокачественной опухоли основано на степени ее местной инвазии и присутствии лимфатических и гематогенных метастазов
Для каждого гистологического типа рака существует система классификации опухоли по стадиям, основанная на клинических и анатомических характеристиках. Использование биохимических, цитологических и молекулярно-биологических показателей повышает точность такой классификации, которая служит двум целям:
- создание возможности сравнения пациентов и групп пациентов, позволяющего более точно оценить эффективность терапии;
- деление на стадии может служить руководством для выбора соответствующего метода лечения конкретного пациента.
Для пациентов с опухолью, выявленной на ранней стадии, и благоприятным прогнозом может потребоваться менее интенсивная терапия (например, менее обширное хирургическое вмешательство и/или отказ от проведения химиотерапии). Это снижает краткосрочные патологические реакции и отдаленные побочные эффекты, которые проявляются по мере повышения эффективности терапии; все это приводит к увеличению выживаемости пациентов, особенно детей. Отдаленными последствиями применения противоопухолевых препаратов могут быть бесплодие, задержка роста и возникновение вторичных опухолей.
3) борьба за существование 4) наследственная изменчивость
4. Как называется первый закон Грегора Менделя:
а) закон единообразия гибридов первого поколения:
б) закон расщепления признаков в фенотипе гибридов второго поколения:
в) неполное доминирование при промежуточном наследовании признаков.
5. В метафазе митоза происходит
1) расположение хромосом в плоскости экватора
2) диспирализация ДНК
3) репликация ДНК
4) растворение ядерной оболочки и ядрышка
6. В результате дробления зиготы образуется зародыш, состоящий из
1) зачатков нервной пластинки
2) трех слоёв с зачатками хорды и нервной пластинки
3) одного слоя клеток и полости (бластоцеля)
4) двух слоев с первичной кишечной полостью
7. Что Ламарк считал главной движущей силой эволюции?
1) естественный отбор,
2) внутреннее стремление к прогрессу
3) божественную силу
*8. О принадлежности человека к классу млекопитающих свидетельствует:
1) четырехкамерное сердце
2) наличие густого волосяного покрытия
3) лицевой отдел преобладает над мозговым отделом
4) слабо развитая кора головного мозга
9.Опыты Л. Пастера доказали возможность:
1) самозарождения жизни
2) появление живого только из живого
4) биохимической эволюции
10. Какому критерию вида соответствует следующее описание: у ушастого ежа ушные раковины большие, отогнутые вперёд; волосяной покров брюшка мягкий?
11. Приспособительный характер эволюции заключается в том, что организмы
1) изменяются вслед за изменениями условий среды
2) побеждают в борьбе за существование
3) подвергаются естественному отбору
4) приспосабливаются под влиянием внешних условий
12. Биогенетический закон Геккеля – Мюллера относят к доказательствам эволюции:
2) сравнительно- анатомическим
13. Какая пищевая цепь начинается от растений и останков животных и переходит к микроорганизмам?
1) цепь выедания
2) цепь разложения
3) пастбищная цепь
14. Наилучшим способом участия отдельного человека в сохранении биосферы является:
1) отказ от езды на автомобиле
2) участие в разработке законов по охране природы
3) сокращение потребления мясной пищи
4) отказ от браконьерства
15.Определите правильно составленную пищевую цепь:
1) клевер →ястреб→шмель→мышь
16.Какими способами можно сократить уровень экологической нагрузки на окружающую среду в рамках концепции устойчивого развития?
1) увеличение численности населения
2) увеличение уровня потребления материальных благ
3) проведение фундаментальных изменений в технологии
4) все перечисленные способы
17.Появление озоновых дыр приводит к:
1) усилению парникового эффекта
2) повышению температуры воздуха
3) уменьшению прозрачности атмосферы
4) повышению ультрафиолетового облучения
18. Постоянное вмешательство со стороны человека требуется для существования:
1) экосистем пресных водоемов;
2) природных экосистем суши;
3) экосистем Мирового океана
19.В условиях урбанизации (крупного города) происходят следующие изменения абиотических факторов:
1) снижение температуры, увеличение скорости ветра и кислотности;
2) повышение температуры и скорости ветра, снижение кислотности;
3) снижение температуры и скорости ветра, снижение кислотности;
4) повышение температуры, снижение скорости ветра, повышение кислотности
20.Как называется экологическая наука, изучающая закономерности общества с окружающей средой?
21. Вещество, способствующее развитию злокачественных новообразований, называют:
22. Число энергетических слоев и число электронов во внешнем энергетическом слое атомы мышьяка равны соответственно:
1) 4,6; 2) 2,5; 3) 3,7; 4) 4,5
23. Между атомами, каких элементов возникает ионная связь:
а) между атомами металлов;
б) между атомами металлов и неметаллов;
в) между атомами неметаллов.
24. В каком ряду химические элементы расположены в порядке увеличения металлических свойств?
а) Na, Mg, Al; б) Al, Mg, Na; в) Ca, Mg, Be; г) Mg, Be, Ca
Содержание
- 1 Канцерогенез
- 1.1 Характеристика злокачественной опухоли
- 1.2 Причины
- 2 Интересно
- 3 Читайте также
- 4 Источники
Канцерогенез [ править | править код ]

Опухоль - это неопластические разрастания (новообразования) клеток. Рак относится к злокачественным, распространяющимся опухолям.
Доброкачественные опухоли лишены способности распространяться (метастазировать) из места своего начального возникновения.
Злокачественные опухоли, называемые также раковыми, метастазируют в результате клональной экспансии одиночной клетки, которая размножается, превращаясь в опухолевую массу, инвазирующую окружающие нормальные ткани и распространяющуюся по организму по лимфатической системе или через кровь (гематогенно). Рост злокачественной опухоли, называемый канцерогенезом или туморогенезом, представляет собой многоэтапный процесс.
К основным характеристикам раковых образований относится:

Рак может возникнуть под влиянием внешних воздействий (например, химический канцерогенез) или в результате генетической предрасположенности. В большинстве случаев существует очевидная связь между этими двумя факторами. Однако природа и степень ассоциации у разных индивидов могут варьировать. Так, исследования, проведенные на близнецах, показали, что генетические факторы обусловливают 42% относительного риска рака простаты, 35% — колоректального рака и 25% рака молочной железы. Вклад в развитие других типов рака менее значителен.
К внешним факторам, способствующим канцерогенезу, относятся бактерии, например Helicobacter pylori, вирусы, например вирус Эпштейна-Барр, вирусы папилломы человека или гепатита В и С, грибы, продуцирующие афлатоксины, и химические вещества, например бензол.
Онкогены представляют собой ДНК-последовательности, кодирующие ключевые белки, которые участвуют в канцерогенезе. Впервые их выделили из вирусов, вызывающих злокачественные опухоли у лабораторных животных. Онкогены также сверхэкспрессированы злокачественными клетками и способны кодировать факторы роста и митогенные факторы, поэтому злокачественные клетки могут стимулировать собственный рост. (рис. 7.2)

Рис. 7.2 Две схемы, показывающие, как внеклеточные факторы роста стимулируют пролиферацию злокачественных клеток. Сверхэкспрессия любого из этих клеточных гомологов онкогенов или мутация, вызывающая конститутивную активацию, способствуют усилению роста, c-fos, c-jun, с-тус — индукторы синтеза ДНК; ECF — эпидермальный фактор роста; САР — белок, активирующий ГТФазу; GRB2 — белок В2, родственный G-белку; МАРК — активированная митогеном протеинкиназа; МАРКК — активированная митогеном киназа протеинкиназы; PDGF — тромбоцитарный фактор роста; Р13-киназа — фос-фадилинозитол-3-киназа; ФЛС — фосфолипаза С; РТР — фосфоти-розинфосфатаза; ras, raf— клеточные передатчики сигнала.
Функциональные рецепторы факторов роста могут быть экспрессированы конститутивно на поверхности злокачественных клеток, тогда как другие появляются в результате индукции (часто химическими веществами, которые высвобождают сами злокачественные клетки).

Механизмы пролиферации нормальных клеток связаны с антипролиферативными механизмами, что дает возможность контролировать пролиферацию по типу обратной связи. Продукты некоторых онкогенов способны подавлять пролиферацию. Мутации или повышенная экспрессия онкогенов могут изменить баланс между стимуляцией и супрессией пролиферации. При канцерогенезе баланс сдвинут в сторону пролиферации.
Пролиферация нормальных клеток также контролируется серией генов-супрессоров опухолей, действующих на клеточный цикл. Мутации или утрата таких генов-супрессоров, например р53 при синдроме Аи-Фраумени, или rb при ретинобластоме, обусловливают повышенный риск онкогенеза у индивидов и семей.
Пролиферация нормальных клеток уравновешивается клеточной гибелью. Рост популяции злокачественных клеток представляет собой результат баланса между пролиферацией и гибелью клеток. Нормальные клетки подвергаются апоптозу — процессу запрограммированной клеточной гибели старых или поврежденных клеток. Апоптоз происходит либо в результате прямого связывания с рецептором (рецептор Fas и его лиганд лимфоцитов), либо высвобождения цитохрома С в цитоплазму после разрыва мембраны митохондрий вследствие летальных внутриклеточных процессов. Существуют проапоптотические белки, такие как Bad и каспазы, действие которых уравновешивается антиапоптотическими белками, например bcl-2. Повышенная экспрессия bcl-2 может быть обусловлена экспрессией онкогенов и ассоциирована с трансформацией нормальных клеток в опухолевые.
Нарушение нормальной репликации геномной ДНК является важнейшим фактором возникновения рака
Злокачественные клетки могут размножаться лишь в том случае, когда организм утрачивает способность распознавать и репарировать мутации в геноме. Индивиды и семьи с мутациями ДНК генов репарации предрасположены к возникновению опухолей, например:
- в ДНК генов, репарирующих не соответствующие друг другу пары оснований, обнаружены мутации при наследственном неполипозном раке толстой кишки;
- репарация ДНК под контролем хеликаз отсутствует или дефектна в случае пигментной ксеродермы — генетического заболевания, характеризующегося дефектом репарации повреждений, вызванных ультрафиолетовым облучением. Гену-супрессору опухолей р53 принадлежит существенная роль в клеточном ответе на повреждение или мутацию ДНК. В норме р53 останавливает клеточный цикл до репликации ДНК, давая возможность репарировать повреждения; этот ген также инициирует апоптоз. Утрата нормальной функции р53 позволяет реплицироваться поврежденной ДНК и таким образом способствует выживанию аномальных клеток.
Злокачественные клетки представляют собой иммортализованные клетки
Каждая нормальная клетка организма, за исключением зародышевых клеток гонад, запрограммирована на конечное число клеточных делении до своего старения. Эта клеточная программа заключена в теломере. Теломеры расположены на концах хромосом и должны соединиться друг с другом в митозе. Они образуются и сохраняются в зародышевых и эмбриональных клетках под контролем фермента теломеразы. Этот фермент утрачивает свою функцию в течение нормального развития. В связи с этим часть теломеры теряется при каждом клеточном делении, а утрата каждой теломеры служит для клетки сигналом, возвещающим гибель. Злокачественные клетки реэкспрессируют теломеразу, что дает им возможность пролиферировать неопределенно долго. Утрата контроля нормального клеточного цикла, осуществляемого генами rb и р53, способствует возобновлению экспрессии теломеразы. До 95% злокачественных клеток экспрессирует теломеразу, делая ее потенциальной мишенью для лекарственных веществ.
Достигнув определенной стадии развития, злокачественная опухоль проникает через базальную мембрану и инвазирует соседнюю соединительную ткань
Злокачественные клетки экспрессируют коллагеназы, гепараниазы и активаторы плазминогена и продвигаются через поддерживающие ткани по пути наименьшего сопротивления.
Ангиогенез играет существенную роль в доставке питательных веществ распространяющейся опухоли, его стимулируют фактор роста фибробластов и фактор роста сосудистого эндотелия. Синтез коллагена, витронектина и фибронектина злокачественными клетками создает основу для развития клеток опухоли и способствует ее приживлению в участках метастазирования. Многие из необходимых для этого сложного процесса компонентов предоставляют сами нормальные ткани, невольно способствуя собственной гибели. Процессы инвазии и метастазирования менее важны при лейкозах и лимфомах, т.к. эти опухоли представляют собой диффузный рак крови.
Инвазия и метастазирование часто достигают значительной степени развития до появления клинических симптомов и выявления опухоли. Лекарственную терапию необходимо начать сразу же, как только макро- или микроскопически опухоль распространится за пределы места возникновения.
Квалифицированный гистологический диагноз — важный компонент терапии рака
Гистологический диагноз некоторых опухолей играет существенную роль в определении цели лечебного вмешательства — паллиативный эффект или полное излечение, например:
Определение стадии развития злокачественной опухоли основано на степени ее местной инвазии и присутствии лимфатических и гематогенных метастазов
Для каждого гистологического типа рака существует система классификации опухоли по стадиям, основанная на клинических и анатомических характеристиках. Использование биохимических, цитологических и молекулярно-биологических показателей повышает точность такой классификации, которая служит двум целям:
- создание возможности сравнения пациентов и групп пациентов, позволяющего более точно оценить эффективность терапии;
- деление на стадии может служить руководством для выбора соответствующего метода лечения конкретного пациента.
Для пациентов с опухолью, выявленной на ранней стадии, и благоприятным прогнозом может потребоваться менее интенсивная терапия (например, менее обширное хирургическое вмешательство и/или отказ от проведения химиотерапии). Это снижает краткосрочные патологические реакции и отдаленные побочные эффекты, которые проявляются по мере повышения эффективности терапии; все это приводит к увеличению выживаемости пациентов, особенно детей. Отдаленными последствиями применения противоопухолевых препаратов могут быть бесплодие, задержка роста и возникновение вторичных опухолей.
Читайте также:

