Узи опухоли при химиотерапии
В экспериментальных исследованиях установлено, что некоторая доза цитотоксического препарата вызывает гибель определенной части клеточной популяции, а не определенного количества клеток. Рисунок схематически иллюстрирует эту гипотезу гибели фракции клеток. Например, введение однократной дозы препарата может привести к гибели 99% клеточной популяции, причем эта же доля клеток погибнет независимо от общего их количества: оно может быть, например, 10 12 (тогда останется 10 10 клеток) или 10 4 (останется 10 клеток).
Если это положение справедливо для солидных опухолей человека, то приходим к выводу о том, что для небольших опухолей более эффективной оказывается схема с применением меньшего количества циклов лечения, чем для более крупных опухолей. Поскольку в этом случае препарат назначается ограниченное количество раз, вероятность развития к нему лекарственной устойчивости снижается. Прием препарата может быть спланирован таким образом, чтобы обеспечить максимальный цитотоксический эффект.
Последний зависит от скорости репопуляции клеток опухоли и восстановления тканей здоровых органов, наиболее сильно поврежденных цитотоксическим препаратом. У человека обычно к этим органам относятся кишечник и костный мозг. По сравнению с большинством опухолей, они быстро регенерируют. По этой причине химиотерапевтические препараты назначают в ритмическом режиме через определенные интервалы, необходимые для протекания восстановительных процессов.
Такой подход имеет некоторые теоретические и практические ограничения.
Справедливость гипотезы гибели фракции клеток оценивалась на экспериментальной модели гомогенных быстрорастущих опухолей, и экстраполяция ее положений на медленнорастущие опухоли человека выявляет очевидные недостатки.
Предполагается, что для экспериментальных опухолей, растущих в виде асцита или развивающихся в жидкой среде организма (например, лейкозы), противоопухолевые препараты распределяются равномерно. Очевидно, что этого не происходит в случаях плохо васкуляризованных солидных опухолей, и кинетика гибели клеток при этом описывается гораздо более сложной функцией, чем уравнение первого порядка, справедливое для экспериментальных систем.
При повторных курсах химиотерапии скорость репопуляции опухоли может изменяться. Хотя для экспериментальных асцитных моделей этого не наблюдается, в случае солидных опухолей ситуация меняется.
Степень восстановления здоровых тканей, например, если судить по данным анализа крови, может оказаться полной после первых нескольких циклов лечения. Однако, по мере продолжения лечения, восстановление замедляется, что накладывает ограничения на дозы препарата, назначаемые в последующих циклах.
Существует крайне ограниченный клинический материал о характере зависимости доза-эффект для конкретных цитотоксических агентов и определенного типа опухолей. Клиническая фармакология химиотерапевтических препаратов крайне сложна и отличается от препарата к препарату. Существуют клинические данные, согласно которым противоопухолевый эффект препарата проявляется только при его назначении в максимальной дозе, и на практике различие между неэффективной и максимально-переносимой дозой может быть незначительным.
Тем не менее, несмотря на высказанные соображения, в химиотерапии широко используется ритмический режим назначения препаратов через определенные интервалы времени. Этот режим был разработан на основании экспериментальных исследований и клинических испытаний.
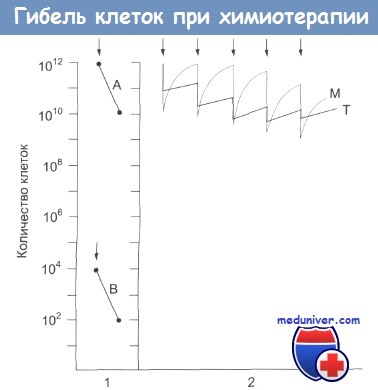
Фракционированная гибель клеток.
В первой части рисунка обозначена определенная доза препарата, вызывающая гибель 99% клеток как в случае А, так и в случае В.
В случае А количество клеток в опухоли снижается с 10 12 до 10 10 , а в случаев с 10 4 до 10 2 . Во второй части рисунка кривая Т иллюстрирует эффект повторных введений препарата (показаны стрелкой) на рост опухоли.
С введением каждой повторной дозы препарата гибель клеток снижается, что указывает на развитие у них устойчивости к препарату.
Кривая М иллюстрирует действие препарата на клетки-предшественницы в костном мозге. Эти клетки быстро восстанавливаются, однако по мере введения повторных доз препарата темпы восстановления снижаются и появляются клинические признаки подавления миелопоэза.
Даже в случаях таких чувствительных опухолей, как болезнь Ходжкина, назначение одного препарата редко приводит к излечению. Поэтому логично попытаться увеличить эффективность лекарственных средств и продолжительность их действия, одновременно назначая несколько препаратов. Цель применения рецептур заключается в попытке преодолеть возможно больше механизмов, ответственных за устойчивость опухоли к цитотоксическим агентам. Очень скоро такой подход оказался эффективным в лечении детских лейкозов и лимфом у взрослых, а также стал применяться для лечения больных с другими опухолями.
При разработке режима комбинированной химиотерапии необходимо соблюдать следующие общие принципы.
• Следует назначать только те препараты, которые оказываются эффективными при изолированном применении.
• По возможности необходимо назначать препараты, токсичность которых не перекрывается.
• Следует применять ритмический режим назначения препаратов с тем, чтобы обеспечить протекание восстановительных процессов в кишечнике и костном мозге.
• В идеале, каждое лекарственное средство должно назначаться в оптимальной дозе и по оптимальной схеме.
• По возможности, следует назначать препараты, характеризующиеся синергическим действием (правда, на практике такие агенты неизвестны).
• Если возможно, необходимо применять препараты, влияющие на различные фазы клеточного цикла.
• Большинство схем лечения разработаны эмпирически с учетом опыта врача.
Повышение эффективности, которое достигается при использовании рецептур, объясняется несколькими причинами.
• Опухоль подвергается воздействию нескольких препаратов, и вероятность развития лекарственной устойчивости снижается.
• Максимальный цитотоксический эффект достигается без увеличения токсичности.
• Существует меньшая возможность раннего появления популяции клеток, устойчивых к препаратам.
Онкология — одна из самых сложных сфер медицины. В настоящее время многие злокачественные опухоли хорошо изучены, о них имеется много данных. Но зачастую эти данные сложны для понимания. Человеку без медицинского образования очень непросто увязать их в общую стройную картину.
Все это бывает очень сложно объяснить пациентам. А там, где человек не до конца понимает ситуацию, возникает масса сомнений и вопросов. Действительно ли медицина может помочь? Врач понимает, что со мной происходит, и как меня лечить? Работает ли курс химиотерапии, который мне назначили?
В этой статье мы постараемся ответить — максимально подробно и понятно.
- В первую очередь нужно понимать цель лечения
- На основании чего врач приходит к выводу о том, что именно данная комбинация препаратов поможет конкретному пациенту?
- Что такое ремиссия?
- Как контролируют эффективность химиотерапии в процессе лечения?
- Что делать, если вы сомневаетесь в эффективности лечения?
В первую очередь нужно понимать цель лечения
В большинстве случаев единственный радикальный метод лечения, который помогает избавиться от рака — хирургическое вмешательство. Противоопухолевые препараты применяют как дополнение к операции, чтобы уничтожить оставшиеся раковые клетки и снизить риск рецидива.
Если основным методом лечения является химиотерапия, а не хирургия, это, как правило, говорит о том, что опухоль успела сильно распространиться в организме. Она неоперабельна, имеются отдаленные метастазы. Прогноз в плане полного излечения от рака в данном случае неблагоприятен. Скорее всего, врачи не смогут полностью ликвидировать опухолевый процесс.
Но это еще не приговор. Таким пациентам можно помочь. Химиотерапия может преследовать другие цели:
- Затормозить или полностью остановить рост опухоли.
- Уменьшить размеры опухоли.
- Продлить жизнь больного.
- Избавить от мучительных симптомов.
- Улучшить общее состояние.
Для пациента с самого начала важно понимать: для чего врач назначил химиопрепараты, какого результата он ожидает? Обязательно побеседуйте с доктором на эту тему. Не бойтесь задавать вопросы. Это поможет избежать недопонимания и ненужных сомнений в будущем. Если у вас нет медицинского образования, в некоторых моментах вам будет сложно разобраться сразу. Не стесняйтесь, попросите доктора еще раз объяснить более понятным языком.
На основании чего врач приходит к выводу о том, что именно данная комбинация препаратов поможет конкретному пациенту?
В настоящее время существует огромное количество разновидностей химиопрепаратов и других противоопухолевых средств: таргетных препаратов, иммунопрепаратов, гормональных препаратов. Как понять, какие именно и в каких комбинациях помогут в вашем случае? Ни один онколог не сможет на 100% правильно ответить на этот вопрос, руководствуясь лишь собственным опытом. Но этого и не требуется.
Каждый лицензированный химиопрепарат хорошо изучен. Проведены многочисленные клинические исследования с участием тысяч пациентов. Это очень серьезный, сложный и дорогостоящий процесс.

Например, для того чтобы создать и протестировать новый препарат, современным фармкомпаниям в среднем нужно потратить 12 лет и миллиард евро.
Если какой-либо препарат помог или не помог одному пациенту, это еще ни о чем не говорит. Не существует двух людей с полностью одинаковыми организмами, как и двух совершенно одинаковых по своим свойствам злокачественных опухолей. Но когда лекарство проверено на тысячах людей, ученые получают результаты, которым можно доверять, и на которые можно ориентироваться.
На основании проведенных исследований составлены протоколы химиотерапии. Ориентируясь на них, онколог может назначить лечение, которое с очень высокой вероятностью поможет. Конечно же, предварительно нужно провести тщательное обследование, разобраться во всех характеристиках конкретной злокачественной опухоли.
Что такое ремиссия?
Для того чтобы вовремя выявить возможный рецидив, после наступления ремиссии пациент должен периодически проходить обследования.

В зависимости от того, как пациент отвечает на химиотерапию, онкологи описывают результат лечения разными терминами:
- Полный ответ (полная ремиссия): опухоль исчезла и больше не обнаруживается.
- Частичный ответ (частичная ремиссия): опухоль осталась, но уменьшилась на определенный процент.
- Стабильное состояние: опухоль не уменьшается, но и не растет, не увеличивается количество очагов, не вовлекаются новые органы.
- Прогрессирование: опухоль растет, несмотря на лечение.
Опухолевые клетки коварны. Со временем в них происходят новые мутации. Начинается самый настоящий естественный отбор, как в теории эволюции: слабейшие быстро погибают под действием химиопрепарата, но сильнейшие выживают и обзаводятся новыми механизмами защиты. Поэтому все противоопухолевые средства помогают лишь в течение некоторого времени. Потом развивается резистентность (устойчивость), и вновь начинается прогрессирование. В таком случае врач назначит новые комбинации препаратов.
Как контролируют эффективность химиотерапии в процессе лечения?
- Инструментальные исследования: КТ, УЗИ, МРТ и др.
- Анализы крови на онкомаркеры.
- Исследование функции пораженных органов.
- Осмотр врача, беседа. Доктор оценивает состояние пациента, спрашивает о симптомах, общем самочувствии.
Если рак отвечает на химиотерапию, лечение продолжают в прежнем режиме. Если начинается прогрессирование, нужно менять тактику.
Одновременно контролируют побочные эффекты. При их возникновении назначают поддерживающую терапию, меняют состав и дозировки химиопрепаратов. В Европейской клинике этому моменту уделяется особое внимание. Мы считаем, что пациенты должны переносить курсы химиотерапии максимально комфортно и без лишних рисков.
Что делать, если вы сомневаетесь в эффективности лечения?
В первую очередь стоит поговорить с лечащим врачом, спросить, как он оценивает эффективность лечения, нельзя ли сделать что-то еще.
Но в онкологии нередко встречаются сложные ситуации, когда сам врач не до конца уверен в диагнозе, правильности назначений. По объективным причинам встречаются ошибки. Поэтому во всем цивилизованном мире давно стала нормой практика получения второго врачебного мнения. Не стесняйтесь проконсультироваться с другим специалистом.
Врачи в Европейской клинике всегда воспринимают позитивно возможность услышать мнение опытных коллег. У нас даже существует специальная система контроля качества. Ведь в конечном счете это идет на пользу пациенту, жизнь и здоровье которого — главные ценности для нас.

- Главная
- Клиника
- Услуги
- Статьи
- Контакты
- Анализы
- Беременность и роды
- Беременность обзор
- Бесплодие и репродуктивный статус
- Бессонница и расстройства сна
- Болезни желудочно-кишечного тракта
- Болезни легких и органов дыхания
- Болезни органов кровообращения
- Болезни щитовидной железы
- Боль в спине
- Восстановительная медицина
- Генитальный герпес
- Гинекология
- Головная боль
- Грипп
- Депрессия
- Детская онкология
- Детские болезни
- Детское развитие
- Заболевания молочных желез
- Здоровое питание. Диеты
- Здоровье и душевное равновесие
- Из истории болезни
- Иммунология
- Импотенция (эректильная дисфункция)
- Инфекции передаваемые половым путем
- Кардиология
- Кровеносная и лимфатическая система
- Лейкемии
- Лечение рака
- Лимфогранулематоз
- Маммология
- Медицина в спорте
- Менопауза
- Микробиология, вирусология
- Педиатрия (детские болезни)
- Проблемная кожа
- Путь к себе
- Рак желудка
- Рак молочной железы (рак груди)
- Рак ободочной, прямой кишки и анального канала
- Рак предстательной железы (рак простаты)
- Рак тела матки
- Рак шейки матки
- Рак яичников
- Сахарный диабет
- Сексология и психотерапия
- Сексуальная жизнь
- Современная контрацепция
- Урология
- Уход за кожей
- Факты о здоровом старении
- Химиoтерапия
- Школа здоровья
- Эндокринология
Речь может идти лишь о шансах, вероятности положительного результата химиотерапии. Потому что, даже при эффективности схемы 90%, «невезучий человек может попасть в 10% больных, леченных без эффекта. И, наоборот, при эффективности всего в 15-20% Вы можете оказаться счастливчиком.
В экспериментальных исследованиях, когда этот ген присутствует в опухолевых клетках в большом количестве, эти клетки оказываются устойчивыми к воздействию большого количества противоопухолевых препаратов. Ученые уже давно пытаются предсказать эффективность химиотерапии до начала лечения.
Попытки воздействовать противоопухолевыми препаратами на кусочек удаленной опухоли, помещаемый в пробирку, не принесли ожидаемых результатов. Оказалось, что чувствительность опухоли в пробирке и в человеческом организме существенно отличается. Грубо говоря, на опухоль в пробирке Вы можете подействовать серной кислотой и она (опухоль) исчезнет, а для человека такие эксперименты приводят к экстренному вызову скорой помощи.
Несоответствие экспериментальных данных клиническим наблюдениям давно стало истиной, набившей оскомину. С другой стороны, не вызывает сомнения польза исследования кусочка опухоли молочной железы на чувствительность к гормонам. В ряде случаев это избавляет больных от необходимости длительное время применять гормональные препараты или, наоборот, указывает на настоятельную необходимость их приема.
Альянс клиницистов и экспериментаторов, их непрекращающийся диалог, взаимный вызов, обогатят химиотерапию, сделают её более эффективной. Для оценки лечебного действия химиотерапии используются два термина: объективный эффект и субъективный эффект.
Не напрягая утомленного читателя лингвистическими изысками и научными формулировками, определим объективный эффект — как улучшение, возникшее под влиянием химиотерапии, которое можно точно измерить.
Это, прежде всего, уменьшение размеров как первичной опухоли, так и новообразований, вызванных опухолью, но располагающихся в других органах (легких, печени, лимфатических узлах и др.).
Сюда относится также уменьшение жидкости в плевральной полости, положительная динамика показателей различных биохимических и иммунологических опухолевых маркеров в крови, нормализация картины крови и костного мозга при опухолях, исходящих из кроветворных клеток.
Объективный эффект является главным и определяющим для оценки действия химиотерапии. Отсутствие объективного улучшения указывает на необходимость поменять схему лечения или вообще отменить химиотерапию.
Степень объективного улучшения различна — от незначительного уменьшения вплоть до полного исчезновения опухолевого процесса. Последнее — это первый шаг к излечению. Объективный эффект проявляется через 2-10 дней от начала лечения, но при некоторых заболеваниях возникает только после 2х - 3х курсов химиотерапии.
Субъективный эффект отражает изменение общего состояния больного, улучшение аппетита, настроения, активности, прибавление веса, уменьшение болей, одышки, улучшение проходимости пищи. Большинство методов лечения нетрадиционной медицины направлены на получение субъективного улучшения. Мы не располагаем достоверными подтвержденными сведениями ни об одном случае объективного эффекта, полученного в результате лечения по газетным рекламам или настенным объявлениям.
Не отрицая важность субъективного улучшения, необходимо сказать, что оно может достигаться большим количеством лекарственных средств, которые назначаются одновременно с химиотерапией или в промежутках между курсами. Субъективный эффект, вызванный химиотерапией, появляется, обычно, через 1-2 недели после окончания курса, когда стихают токсические действия препаратов. Однако, нередко улучшение наблюдается уже на другой день после введения препаратов.
Существуют опухоли высокочувствительные к химиотерапии, умеренно чувствительные и малочувствительные. При высокочувствительных опухолях выраженное объективное улучшение наступает уже после первого курса химиотерапии. При малочувствительных опухолях Эффект достигается с большим трудом, иногда после нескольких курсов лечения; нередко приходится использовать новые препараты или подключать лучевую терапию.
В отличие от космоса или глупости, химиотерапия имеет пределы, которые ограничены ее способностью повреждать определенную долю (процент) опухолевых клеток. Поэтому эффективность химиотерапии обычно обратно пропорциональна массе опухоли (числу составляющих ее опухолевых клеток).
Например, в опухоли 5000000 клеток и какая-то комбинация противоопухолевых препаратов способна повредить 20%. Естественно, что на выраженное улучшение после первого курса химиотерапии рассчитывать не приходится, впрочем, так же, как и после второго курса. Если же клеток всего 300000, и химиотерапия может разрушить 60%, то хоть и не сразу, но появляется шанс на полный эффект.
Указанные подсчеты являются чисто механистическими и умозрительными, потому что подсчитать количество клеток у больного и число клеток, которые может повредить химиотерапия в каждом конкретном случае, мало реально. Поэтому и приходится оперировать такими общими понятиями, как меньше или больше: чем меньше объем опухоли, тем больше вероятность на получение хорошего результата (при одинаковом строении опухоли).
На эффективность лекарственного лечения опухолевых заболеваний влияют также общее состояние больног возраст, состояние иммунитета. Заметно изменить (понизить или, реже, повысить) чувствительность опухоли химиотерапии могут предшествующие курсы химиотерапии или лучевой терапии.
Основной целью химиотерапии является получение объективного и субъективного эффекта, которые могут существенно улучшить качество жизни больных. Самое приятное дело для больных и для врачей — это оценивать эффективность лечения. Наблюдать, как уменьшается опухоль, улучшается самочувствие, настроение, повышается активность, аппетит.
Ради одного этого уже стоило бы лечиться. Но главная задача химиотерапии — увеличение продолжительности жизни больного. В настоящее время у большей части больных удается достигнуть объективного улучшения.
К сожалению, существенно увеличить продолжительность жизни удается не всегда. Тем не менее, нередко встречаются больные, которые получали химиотерапию 10-1 5 лет назад по поводу самых неблагоприятных — распространенных стадий заболевания Но даже, если имеется шанс лишь на небольшое увеличение продолжительности жизни, есть смысл проводи химиотерапию.
Дело в том, что химиотерапевтическая наука стремительно развивается. Появляются и постоянно изучаются новые активные лекарства и комбинации препаратов. Поэтому при опухолях, которые еще вчера считались устойчивыми к лекарственному воздействию, сегодня удается получить выраженный объективный эффект, завтра, возможно, можно будет достигнуть полного излечения.
Как же узнать, успешно ли действует химиотерапия? Для этого существуют многочисленные специальные методы исследования: рентгенография, ультразвуковое и радиоизотопное исследование, а также различные анализы крови.
Исследования при помощи сложной аппаратуры осуществляются до и через какое-то время после химиотерапии, а анализы крови проверяются обычно значительно чаще. Вы будете проходить регулярные осмотры у Вашего врача, у которого Вы можете узнать результаты указанных исследований и который оценит, насколько хорошо действует предписанное Вам лечение.
В России, Израиле, Германии рак яичников начинают лечить с операции. Удаляется матка с придатками, большой сальник, а также видимые проявления опухоли. Если выполнение операции маловероятно, т о начинают с химиотерапии. Это связано с тем, что рак яичников плохо отвечает на химию. Особенно низкую эффективность химиотерапии наблюдают при муцинозном и светлоклеточном раке яичников.

Операция при раке яичников
Хирургическое вмешательство – всегда всплеск опухолевого роста и метастазирования. Опухолевые клетки механически (скальпелем) разносятся по брюшине, попадают в кровоток. От избытка кислорода раковые клетки активизируются. Это чревато рецидивом и метастазами.
Если злокачественную опухоль до операции задавить химиотерапией, то это снизит активность клеток к росту и метастазированию, увеличит радикальность операции.
Простое введение химиопрепаратов малоэффективно. Поэтому в клинике “К-тест” химиотерапию усиливают, вводя препараты под нагревом методом общей электромагнитной гипертермии. В конечном счете предоперационная терапия по данной схеме улучшает результаты и выживаемость.
Общая гипертермия – перспективный метод лечения онкологии, который исследуется более полувека. Ученые разных стран пробуют возможные способы нагрева (в воде, в специальных камерах и т.д.). Разработками советских ученых в 80-х годах был предложен нагрев в электромагнитных полях. Нижегородские медики и физики объединились и была разработана и апробирована общая электромагнитная гипертермия. Ведущим онкологом этих исследований был профессор Карев. Сейчас он возглавляет клинику “К-тест”. Установки общей электромагнитной гипертермии в постперестроечный период не получили распространения в стране. Причина – высокая стоимость и сложность процедуры. В Нижнем Новгороде как начали лечить, так и лечат более 25 лет. Более простая и дешевая локальная гипертермия используется в ведущих онкоцентрах страны.
Если после 2-3 курсов проводимой химиотерапии в рамках стандартного лечения по ОМС нет заметной положительной динамики, улучшения самочувствия, уменьшения размеров опухоли и метастазов, то следует задуматься о необходимости усиления химиотерапии нагревом. Дальнейшее продолжение стандартной химиотерапии при отсутствии динамики, даже со сменой химиопрепаратов, приведет только к устойчивости рака яичников к лекарствам.
Лечение рака яичников после операции
После операции рекомендована курсовая общая электромагнитная гипертермия с химиотерапией. Для окончательного подавления опухоли и клеток, которые разнеслись по организму в ходе операции.
Введение химиопрепаратов на фоне разогрева тела до температуры гибели опухолевых клеток (42,5 °С и выше) решает проблему устойчивости опухоли к препаратам платины. Также до минимума снижает риск рецидивов.
Число курсов и выбор химиопрепаратов зависит от гистологической классификации опухоли и степени рака. С целью улучшения результата лечения может назначаться таргетная терапия (бевацизумаб).
Рецидив рака яичников можно остановить
Когда к нам обращались пациентки с прогрессированием опухоли яичников после химиотерапии первой линии (платинорефрактерный рак), введение этих же препаратов в условиях общей гипертермии давало ощутимый эффект: опухоль и метастазы уменьшалась уже после первого курса.
Такая картина наблюдалась даже у больных, которые до поступления к нам уже получали множество курсов химиотерапии второй и третьей линий (до 30 курсов) и их переводили на симптоматическую терапию.
Клинический пример:
Больная П., 44 года. Диагноз: Рак яичников T3cNoMo
В 2014 году больная в Екатеринбурге получала комбинированное лечение (экстирпация матки с придатками + адъювантная химиотерапия). Гистология и иммуногистохимия – аденокарцинома, метастазы в большой сальник. В январе 2019 года выявлен асцит. На ПЭТ КТ от 17.01.19 – рецидив опухоли в малом тазу. Проведена химиотерапия – 4 курса. На ПЭТ/КТ от 5.07.2019 выявлена отрицательная динамика – появились уплотнения и инфильтрация (канцероматоз) брюшины (SUV max 7.26), жидкость в малом тазу и брюшной полости. В надключичной области лимфоузлы 9х6 мм (SUV max 1,83). Субплеврально – очаг (SUV max 1,90).
Рак яичников 4 стадии
Применяемая схема позволяет добиться пятилетней выживаемости у 15-20 % пациенток с запущенным и рецидивирующим раком.
При платинорефрактерном раке яичников или рецидиве заболевания переход на химиотерапию в условиях нагрева предпочтительнее, чем химиотерапия второй или третьей линии, которая зачастую не увеличивает продолжительность жизни и ухудшает ее качество в связи с возникновением побочных эффектов.
Хорошие результаты при лечении внутрибрюшинных и отдаленных метастазов рака яичника в легкие и печень.
Под действием критической температуры происходит их резорбция. Становится возможно выполнение метастазэктомии (удаление крупных метастазов).
Лечебное действие электромагнитной гипертермии наряду с противоопухолевым эффектом снимает боли, стимулирует иммунитет, улучшает качество жизни больных.
Клинические примеры:
Сравнение схем лечения по стандарту ОМС и в клинике “К-тест”:
Средняя продолжительность жизни при карциноматозе брюшины без лечения – от 1,5 до 6 месяцев. Лечить же таких больных еще совсем недавно было нечем. Ни хирургия, ни химиотерапия не справлялись. Пациентов признавали инкурабельными (неизлечимыми). Показатель 5-летней выживаемости в начале 90-х был практически равен 0.
Но последние 20 лет активно развивается методика лечения перитонеального канцероматоза с применением HIPEC (англ. hyperthermic intraperitoneal chemotherapy) – гипертермической интраперитонеальной (внутрибрюшинной) химиотерапии. Методика дает отличные результаты: увеличивает 5-летнюю выживаемость до 40-50%, а иногда дает полное излечение.
Самое плохое – даже многие врачи не знают, что при канцероматозе существует способ продлить жизнь. Поэтому сегодня мы расскажем про HIPEC подробно: кому это поможет, какие дает результаты и сколько стоит.
Цель – уничтожить максимум опухолевых клеток, которые неизбежно останутся даже после самого тщательного хирургического удаления очагов и спровоцируют рецидив.
Свойства, которые делают HIPEC действительно уникальной методикой, мы разъясним чуть ниже, а сначала определимся, при каких диагнозах она может помочь и почему она иногда оказывается единственным способом продлить жизнь человеку на последних стадиях рака.
При каких опухолях образуется канцероматоз брюшины, и почему он так опасен
В брюшную полость распространяются многие из часто встречающихся видов рака.
- рак яичников – в 60-70% случаев приводит к канцероматозу;
- рак желудка – канцероматоз в 40-50% случаев;
- рак поджелудочной железы – в 30-40% случаев;
- рак толстой и прямой кишки (колоректальный рак) – в 10-15% случаев;
- рак печени;
- рак шейки матки;
- рак червеобразного отростка (аппендикса);
- редкие первичные опухоли брюшины (мезотелиома и псевдомиксома).
Все эти злокачественные новообразования распространяют раковые клетки либо когда первичная опухоль физически прорастает в брюшную полость, либо вместе с током крови и лимфы – иногда это происходит во время хирургических операций по поводу первичных опухолей.
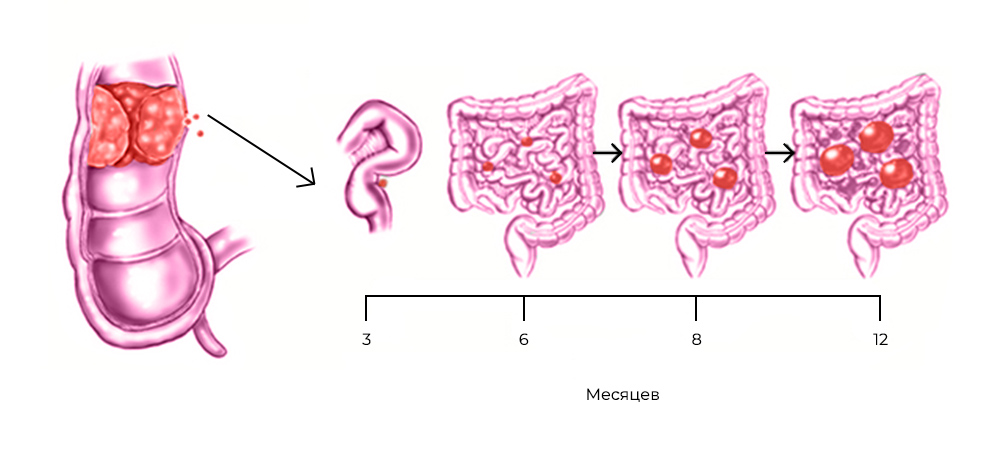
Развитие канцероматоза при колоректальном раке: из прямой кишки в брюшную полость
Стоит раковым клеткам попасть в полость, ограниченную брюшиной – они, скорее всего, дадут начало вторичным опухолям, метастазам. Перитонеальная ткань – богатый источник факторов роста и комфортная среда для их развития. Микроскопические метастазы распространяются по поверхности брюшины, поражают внутренние органы.
Метастазы нарушают кровоток и лимфоток, лишают внутренние органы питания и пространства, зачастую становятся причиной непроходимостей (например, кишечной, или сдавливают мочеточники). Кроме того, это провоцирует асцит – выпот и скопление жидкости в брюшной полости – наиболее распространенный симптом при канцероматозе.
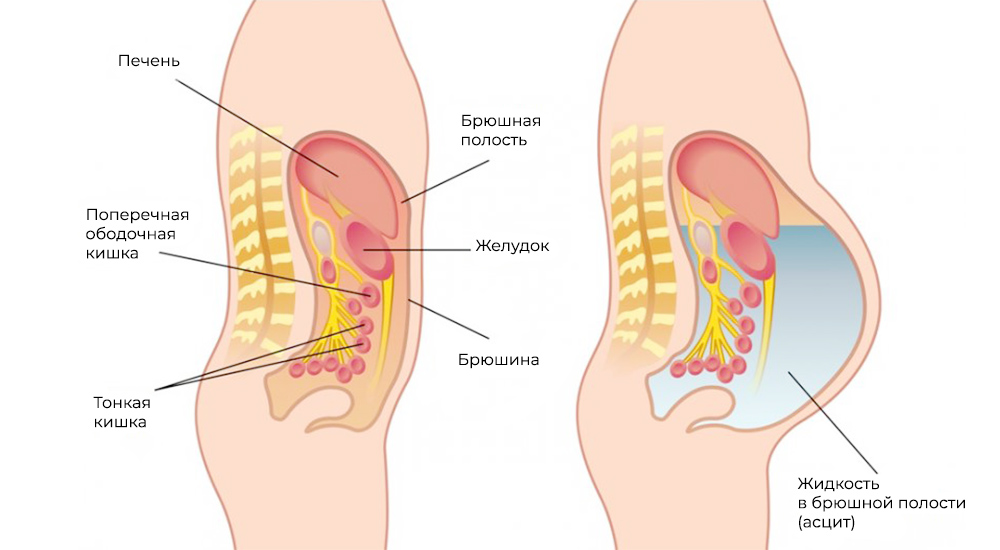
Асцит – скопление жидкости в брюшной полости
Застой крови и лимфы, интоксикация, сдавление внутренних органов метастазами и/или скопившейся жидкостью при асците – это причины, почему пациенты с канцероматозом без лечения не проживают и года.
На протяжении почти всей истории онкологии считалось, что перитонеальный карциноматоз и опухоли брюшины не поддаются никакому из существующих видов лечения.
Лучевая терапия в лечении канцероматоза не применяется, поскольку высокие дозы облучения такой обширной области живота опасны для пациента еще более серьезными осложнениями.
Хирургическое лечение малоэффективно, т.к. метастазы на поверхности брюшины могут быть микроскопического размера, либо расположены в недоступных местах, и врач не видит их во время операции. А для быстрого рецидива канцероматоза достаточно и единичных раковых клеток, оставшихся в полости брюшины.
Системная химиотерапия почти не дает чувствительного воздействия на опухоли брюшины –опухолевые очаги размером до 3 мм (таких при канцероматозе большинство) практически не развивают систему собственных кровеносных сосудов – и поэтому слабо доступны для системной внутривенной химиотерапии.
Вводить химиотерапию в более высоких дозах, чтобы повысить концентрацию препаратов в перитонеальной области – невозможно, т.к. это может необратимо навредить остальным органам и тканям, до которых доберется перенасыщенный химиопрепаратом кровоток.
Во второй половине 20 века появились первые работы, рассказывающие о возможностях применения внутрибрюшинной химиотерапии. Последние 20 лет это направление активно развивается, а создал его еще в 80-х годах XX века американский хирург-онколог Пол Шугабейкер – он первым придумал совместить циторедуктивную операцию с горячей химиотерапией, вводимой непосредственно в брюшную полость. И это дало результат
Гипертермия – это повышение температуры.
- Высокая температура сама по себе способна вызывать повреждение и гибель опухолевых клеток. К тому же, делает их более уязвимыми для действия химиопрепаратов: усиливает проницаемость клеточных мембран.
- Причем чувствительность увеличивается избирательно – опухолевые клетки начинают гибнуть при температуре 40 °C, а здоровые – сохраняются до 44°C. В условиях гипертермии особенности опухолевых тканей (иное кровоснабжение, степень оксигенации, особенности репарации ДНК) становятся для них не преимуществом, а слабым местом.
- Кроме того, повышение температуры обычно вызывает иммунную реакцию: растет количество лимфоцитов – клеток иммунитета, способных уничтожать опухолевые клетки. В плазме крове увеличивается уровень интерлейкинов, интерферонов, факторов некроза опухоли и т.д. Все они имеют собственную противоопухолевую активность, и дополнительно способны усиливать эффект некоторых химиопрепаратов.
- Еще один важный плюс гипертермии – она способствует более активному проникновению препарата в ткани – на глубину до 3 мм – этого хватит, чтобы охватить большинство микро-метастазов, которые останутся после хирургической операции.
Внутри брюшины – химиотерапия работает лучше. Для HIPEC используются стандартные химиопрепараты, но их локальное применение при перитонеальном карциноматозе – куда эффективнее.
Процедура HIPEC – это, строго говоря, вторая половина целого комплекса мероприятий. Без циторедуктивной хирургической операции HIPEC может проводиться в считанном количестве случаев по особым показаниям. Обычно процедура – продолжение хирургической операции, которое дает серьезное улучшение прогноза выживаемости.
Вместе с удалением опухолевых очагов, все вмешательство занимает от 6 до 18 часов. Процесс можно разделить на 4 этапа.
1) Ревизия брюшной полости. Проводится она для того, чтобы понять, показано ли лечение с помощью HIPEC для этого пациента, принесет ли оно увеличение продолжительности жизни и улучшение ее качества. Во время ревизии хирург внимательно осматривает брюшную полость и определяет перитонеальный индекс рака (peritoneal cancer index – PCI).
Чтобы его рассчитать, брюшную полость и тонкую кишку условно делят на 13 областей-квадрантов, в каждом из них оценивают самый крупный опухолевый очаг по шкале от 0 до 3:
- очагов не обнаружено — 0 баллов;
- очаги размером менее 0,5 см — 1 балл;
- очаги размером менее 0,5–5 см — 2 балла;
- очаг более 5 см или несколько узлов меньшего размера— 3 балла.
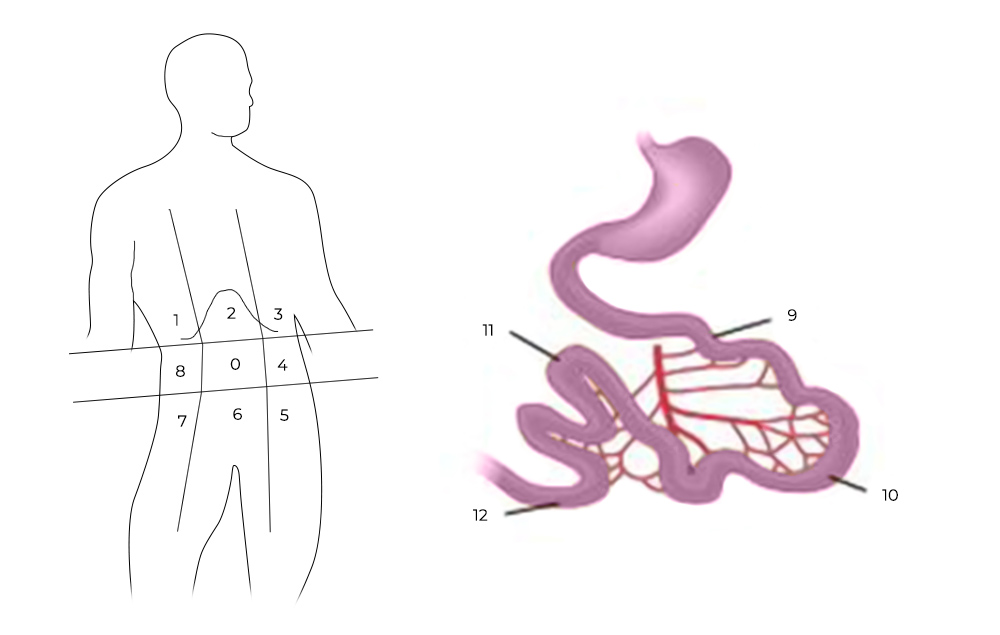
Разделение брюшной полости на участки для определения PCI
Баллы суммируются по всем квадрантам – это и есть значение PCI. Чем больше баллов – тем хуже прогноз. Если PCI выше критического (принимая во внимание тип опухоли и состояние пациента) – то и операцию, и процедуру HIPEC могут признать нецелесообразными.
Проводят ревизию интраоперационно – т.е. непосредственно перед проведением основной операции. В некоторых случаях ее можно провести в виде отдельной диагностической лапароскопической операции – малотравматичной, через небольшие проколы в стенке живота.
2) Циторедуктивная операция. Если по результатам ревизии PCI оценен как удовлетворительный, то хирург приступает к удалению всех видимых и пальпируемых (те, что чувствуются наощупь) опухолевых узлов.
Удаляют отдельные участки брюшины, орган, в котором находится первичная опухоль, соседние внутренние органы или их части, если они тоже поражены метастазами. Часто это участки кишечника, селезенка, желчный пузырь.
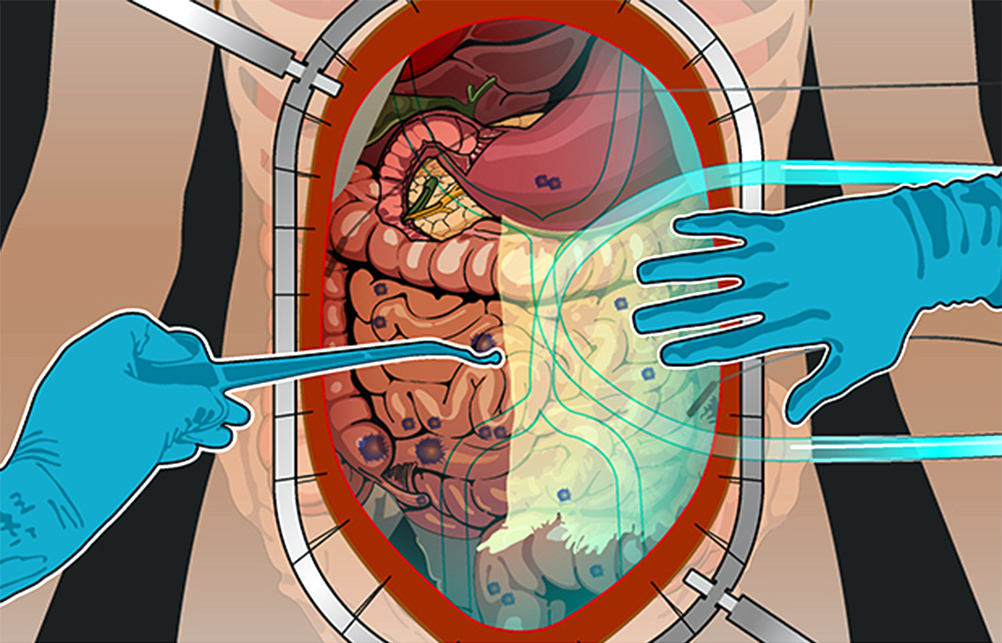
3) Гипертермическая интраперитонеальная химиотерапия. Собственно, HIPEC. В брюшную полость вводят катетеры и температурные датчики, соединенные со специальным аппаратом и емкостью с раствором химиопрепарата. Эта перфузионная система (под контролем врачей, конечно) поддерживает заданную температуру и давление циркулирующей жидкости. Раствор химиопрепарата в течение 60–90 минут циркулирует в брюшной полости пациента.
После процедуры препарат удаляют из брюшной полости, промывают ее физраствором, удаляют датчики и катетеры.
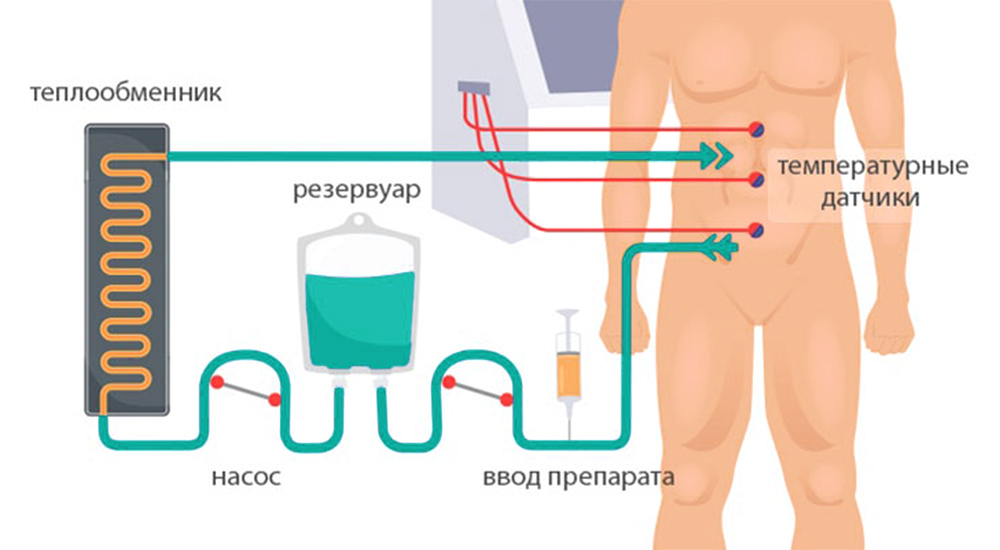
Схема проведения HIPEC
4) Реконструктивная операция. Если удалены части кишечника, хирург восстанавливает непрерывность кишки – формирует анастомоз, выводит верхний конец толстой/тонкой/слепой кишки на поверхность живота для отхождения каловых масс.
В среднем, в клинике пациент проводит 2-4 недели. Через 2-3 недели после операции проводится контрольное обследование. Его необходимо повторять через 3 месяца, и постепенно частоту проверок снижают до 1 раза в год.
В этом видео наши коллеги проводят процедуру HIPEC пациентке с раком яичников.
Как любое лечение, HIPEC имеет риски и противопоказания
Послеоперационный период стоит отдельным этапом, но он не менее важен. Мы всегда понимаем, насколько сложным для наших пациентов (а многие попадают к нам в крайне тяжелом состоянии) может быть период восстановления после такого длительного и достаточно агрессивного вмешательства, как циторедуктивная операция + HIPEC. Поэтому сразу после операции мы переводим пациента в отделение интенсивной терапии, под круглосуточное наблюдение.
Осложнения могут быть те же, что и после любого хирургического вмешательства на брюшной полости, поэтому за пациентом внимательно следят на случай появления признаков кровотечения или воспаления послеоперационной раны – и готовы в любую минуту оказать помощь.
Побочные действия от химиотерапевтического препарата при внутрибрюшной гипертермической химиотерапии даже менее выражены, чем при внутривенном введении – при том, что дозировки, а значит, и противоопухолевое действие, при HIPEC в десятки раз выше.
К сожалению, при всем нашем желании и мастерстве наших хирургов, есть пациенты, для которых полезный эффект вмешательства не оправдает сложностей послеоперационного восстановления.
Чтобы циторедуктивная операция с последующей процедурой HIPEC была эффективной, нужно соблюдение нескольких условий:
- Пациент должен быть в состоянии перенести и хирургическую операцию, и химиотерапию одновременно. Возраст или показатели здоровья не должны этому препятствовать – например, не должно быть почечной или печеночной недостаточности. Перед процедурой мы обязательно всесторонне обследуем пациента.
- Процесс распространения метастазов должен быть ограничен только брюшной полостью. Если есть метастазы в других органах, которые нельзя удалить – они будут распространяться дальше, и сведут эффект HIPEC на нет.
- Метастазы размером более 2,5 мм не должны покрывать всю поверхность брюшины – удалить их все будет невозможно.
Мы провели ей циторедуктивную операцию и процедуру HIPEC, и после этого она уже 10 месяцев живет без прогрессирования заболевания.
В некоторых случаях HIPEC приводит к устойчивому излечению. Например, коллеги из США сообщали о женщине с мезотелиомой брюшины. С помощью HIPEC она преодолела болезнь, уже 3 года живет без признаков рака и смогла родить ребенка.

Jessica Blackford-Cleeton, которой HIPEC позволила выжить и стать мамой.
К сожалению, HIPEC пока применяется в считанном количестве клиник. Причин этому несколько, и они характерны для всех новых технологичных способов лечения.
- Методика все еще считается инновационной, не все врачи имеют нужный опыт работы. К тому же, для проведения процедуры нужен не 1 и не 2, а целая бригада медиков самой высокой квалификации – это длительная, сложная и напряженная операция.
- Оборудование дорогое, не все страны и не все клиники могут потратиться на перфузионную систему и расходные материалы.
- Врачи бывают довольно консервативны. Кто-то считает, что процедура требует более подробного изучения. А кто-то из них не любит участвовать в проведении гипертермической химиотерапией, потому что опасается за собственное здоровье – испарения химиопрепаратов во время HIPEC могут быть вредными для медиков, которые при этом присутствуют. Хотя, в целом, испарения из закрытого контура минимальны, негативные последствия, даже если есть – не являются необратимыми, врачу нужно лишь более внимательно следить за состоянием почек и печени.
Однако более 70 ведущих хирургов-онкологов из 55 онкоцентров в 14 странах мира, включая США (где и родилась эта процедура), Канаду, Францию и Великобританию, пришли к выводу о том, что HIPEC может существенно повысить ожидаемую продолжительность жизни у пациентов, страдающих канцероматозом, особенно при колоректальном раке.
Клинические исследования из разных стран показывали результаты, когда пациенты после лечения канцероматоза брюшины с применением HIPEC жили 7 лет при опухолях аппендикса, более 5 лет при мезотелиоме брюшины, 5 лет при колоректальном раке, 2 года при раке яичников – тогда как при стандартном лечении их выживаемость колебалась от 2 до 14 месяцев.
Мы в свою очередь убедились в эффективности HIPEC на собственном обширном клиническом опыте. Мы надеемся, что через несколько лет HIPEC будет внедряться в стандарты лечения по ОМС и станет доступна по всей стране. А пока – мы даем пациентам возможность не искать подобную помощь за рубежом, а получить ее в Москве.
Читайте также:



